2. 辽宁省石化行业高效节能分离技术工程实验室,辽宁 大连 116024
2. Engineering Laboratory for Petrochemical Energy-Efficient Separation Technology of Liaoning Province, Liaoning Dalian 116024, China
医药化工废水组成相对复杂,有机溶剂含量高,无机盐浓度相对较高[1]。如果将含有大量有毒药物的废水直接排放,不仅会对环境造成严重的污染,也可能会通过动植物转移到人体[2]。同时,医药化工废水中含有大量高附加值的医药分子,对其进行截留回收,也具有较大的经济价值[3, 4]。
我国医药废水的环境生态污染问题也日益凸显,目前我国抗生素原料年产量超过20万t,抗生素废水年排放量超过350万t[5]。常用的化学氧化[6, 7]、生物处理[8]等方法处理医药废水中的抗生素类药物,虽然成本低廉但药物直接分解后会造成极大的资源浪费。物理方法[9, 10]如过滤、沉降、混凝和吸附技术不会降解废水中的抗生素,但分离效率较低。膜分离技术[11, 12]具有分离能力强、能耗低、易耦合的优点,在水处理领域已经受到研究人员的广泛关注。
膜的性质(材料类型、孔径、带电特性和亲水性等)和抗生素的理化性质(分子大小、粒径和pKa等)在膜分离过程中起着重要作用[13]。一般认为,Donnan效应和尺寸筛分效应是纳滤膜脱盐的主要机理,离子与荷电膜之间的静电排斥作用对膜的截留富集能力起到了重要作用。研究者通过改性膜表面基团,调控荷电性,增强纳滤膜对头孢氨苄、四环素、对乙酰氨基酚和布洛芬等药物的截留能力[14-16]。Zhang等[17]发现,纳滤过程中离子的截留率会同时受到平均孔径与膜表面电荷密度的影响,通过优化膜表面电荷与孔径,能够同时增强纳滤膜的截留率与渗透性。Weng等[18]使用两性离子单体AEPPS和TMC制成的两性离子聚酰胺复合纳滤膜(ZTFCMs)具有出色的透水性,对红霉素的截留率高达96.5%。抗生素类药物的活性成分多为两性离子,在不同pH值下处于不同电离状态,合成对pH值敏感的纳滤膜,增强对抗生素的分离,减少膜表面污染[19]。Zhao等[20]开发了一种具有定制孔径和表面电荷特性的复合纳滤膜,系统地研究了分离效率、溶液酸碱度与膜表面电荷特性之间的关系,在不同pH值下,带电膜与磺胺甲基嘧啶解离产物之间的静电作用决定了截留能力。Wu等[21]提出了一种多级纳滤分离回收头孢氨苄结晶残液的方法,利用纳滤膜界面荷负电的特性增强膜与医药大分子溶质之间的排斥。Zhen等[22]通过界面聚合法制备了CM-β-CD改性纳滤膜,利用CM-β-CD上的羧酸基团,增强了对头孢氨苄的排斥作用。
电场辅助膜分离技术[23, 24]能够进一步提高其渗透选择性、抗结垢与抗膜污染的能力。一般来说,电场辅助膜分离技术的强化机理[25]主要为3种,电增强吸附/脱附、电增强Donnan效应与膜表面的电化学氧化还原反应。电辅助方法不仅能增强对一二价离子与污染物的去除,通过电辅助反冲洗污染后的膜,损失的膜通量也几乎完全恢复[26]。
由于运用实验手段并不能获得不同电场强度对粒子在膜材料表面分子水平、皮秒尺度的微观运动行为,而这些微观尺度上的运动可能是决定膜分离性能与分离机理的关键。随着计算机模拟技术和运算能力的提升,智能化技术辅助化工研究已经成为重要趋势。
近年来,分子模拟技术在聚合物膜分离领域取得了卓越成果[27, 28]。很多关于聚合物膜分离过程的分子动力学模拟都基于溶解扩散机理来解释,即分子在膜内的溶解过程与扩散过程。Liu等[29]利用分子模拟方法,探究3种聚合物膜在甲醇、乙醇、丁腈和丙酮溶剂中的溶胀程度与溶剂渗透过程,提供了聚合物膜溶胀和有机溶剂渗透的微观见解。Wei等[30]构建了一种用于海水淡化的混合基质膜模型,对氯化钠的截留率接近100%,表明该材料在海水淡化方面具有一定潜力。这些研究结果为通过分子动力学模拟方法探究在外部电场作用下膜界面与膜内粒子的运动行为提供了有益的支撑。
因此,本论文基于Materials Studio软件,利用分子动力学模拟技术(MD)从分子层面上探究电场强度(0~0.15 V ·Å-1)对磺化聚砜膜表面的带电离子(主要研究了Na+, Cl-和头孢呋辛离子)空间分布的对应关系,电场强度(0~0.10 V ·Å-1)与膜内含水量(λ=0.5、2.0)对粒子动力学传递过程的影响。建立牛顿力学方程进行求解,获得荷电膜内各粒子微观状态的变化规律,进一步揭示电增强荷电膜分离医药废水的微观机制,进而得到电场辅助膜分离废水的宏观性质。探明了电场辅助磺化聚砜膜分离头孢呋辛钠医药废水的机理,为未来理性设计和选择荷电膜材料与膜表面的基团改性提供了有益的理论参考。
1 分子模拟步骤与分析方法本研究使用分子模拟软件Materials Studio 2017探究外加电场作用下粒子在膜表面运动的影响和电场与膜内含水量对粒子传递性能的影响,所使用的分子模拟力场均为COMPASS Ⅱ[31]。
1.1 电场强度对粒子在膜表面传递模型的构建与优化首先构建溶液层模型,先使用DMol3模块优化所使用的5种粒子:H2O、Na+、Cl-、SO42-和头孢呋辛离子(Cefuroxime-)。利用Amorphous Cell模块构建溶液的分子模型,系统包括500个水分子,按比例加入一定数量的离子。体系优化后,先使用NPT系综进行1 ns动力学弛豫,弛豫完成后使用NVT系综进行1 ns动力学模拟,得到溶液模型。
构建含有10个重复单元的SPSf与SPSf-Na聚合物分子链的结构模型。随后利用Amorphous Cell模块构建膜组件模拟晶胞,每个单元包含10条分子链,为了防止链段的过度堆叠与苯环发生刺穿或耦合现象,通常在远低于材料实验密度值的条件下建立模型,本部分初始模型的密度选择为0.2 g ·cm-3。优化后,对膜组件晶胞进行2 ns退火与1 ns的NPT动力学模拟,得到相对稳定的结构。使用Build Layer模块构建SPSf膜组件-溶液层双层结构模型,为了消除周期性边界对模拟的影响,在溶液层上方增加1个厚度为100 Å的真空层。
为了减少运算时间,增加运算效率,对模型施加的电压远大于实际电压。使用Perl脚本,对优化后的模型施加电场强度为0、0.10和0.15 V ·Å-1的外电场。模拟粒子在膜表面运动的动力学模拟过程中,固定膜组件下部,采用NVT系综,温度控制器选择Andersen方法[32],模拟总时长2.5 ns。
1.2 电场强度、含水量对膜内粒子传递模型的构建与优化为了探究含水量对粒子在膜内传递的影响,设计了2种含水量λ=0.5、2.0(基团数量与水分子数量之比)体系进行模拟。利用Amorphous Cell模块构建周期性结构,聚合物膜-小分子混合体系按照一定比例将上文构建的SPSf高分子链模型,与H2O、Na+、Cl-和Cefuroxime-进行混合,具体参数如表 1所示。
| SPSf chains | H2O | Na+ | Cl- | Cefur- oxime- | Water Content λ | |
| SPSf | 10 | 100 | 40 | 20 | 20 | 0.5 |
| SPSf | 10 | 200 | 40 | 20 | 20 | 1.0 |
| SPSf | 10 | 400 | 40 | 20 | 20 | 2.0 |
| SPSf-Na | 10 | 100 | 140 | 20 | 20 | 0.5 |
| SPSf-Na | 10 | 200 | 140 | 20 | 20 | 1.0 |
| SPSf-Na | 10 | 400 | 140 | 20 | 20 | 2.0 |
本部分初始模型的密度选择为0.2 g ·cm-3。模型构建后使用Smart法进行结构优化,最大迭代步数为30 000,对于非键作用、静电力作用与范德华作用分别采用Ewald、Atom based方法。初始优化结束后,先利用Forcite模块Anneal退火操作2 ns,平衡晶胞,释放晶胞内应力使晶胞达到平衡密度。再进行1 ns的NPT动力学模拟,取最终平衡结构,选用NVT系综,进行1 ns动力学运算,每1 000步输出1帧进行分析。优化后的模型结构见图 1。
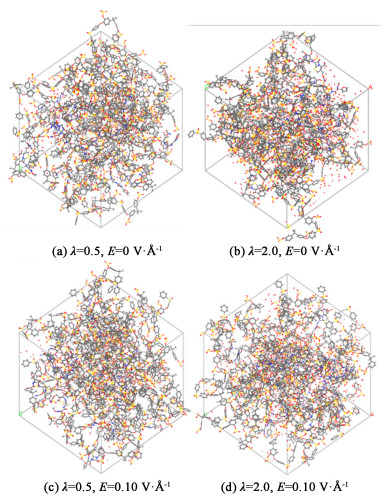
|
| 图 1 SPSf优化后的模型结构 Fig.1 Model structure of SPSf after optimization |
| |
为了了解膜内含水量与电场强度对H2O、Na+与Cefuroxime-在不同体系中的传递行为,先分析3种粒子在膜内的均方位移(MSD),利用MSD曲线计算粒子在膜内的扩散系数D[33],分析运动规律。在分子动力学模拟中,通常使用Esinstein方程来求解扩散系数。MSD的计算方法见式(1)。
| $ \begin{gathered} {\mathrm{MSD}}=\frac{1}{T-\Delta t} \int_0^{T-\Delta t}[r(t-\Delta t)-r(t)]^2 {\mathrm{~d}} t= \\ {[r(t-\Delta t)-r(t)]^2} \end{gathered} $ | (1) |
式(1)中,r(t-Δt)、r(t)分别表示粒子在t-Δt时刻及t时刻的位置。
Einstein方程中假设在高分子中物质时刻在做自由运动,MSD与D呈线性关系,则由式(1)可得扩散系数计算式:
| $ D=\frac{\mathrm{MSD}}{6 t}=\frac{a}{6} $ | (2) |
式(2) 中,a是MSD~t函数的斜率。
2 结果与讨论 2.1 模型平衡性验证通过体系温度与能量的波动来确定模拟体系是否已经达到平衡,如果体系的能量与温度波动低于10%,认为体系已经达到平衡。如图 2所示,粒子在SPSf膜表面传递模型的MD模拟过程中,体系的温度波动较小,能量随时间几乎没有变化,证明粒子在SPSf膜表面传递的模型已经达到平衡。为了获得准确的模拟结果,选择最后0.5 ns进行分析,每1 000步输出1帧原子坐标信息,用于数据的统计与计算。
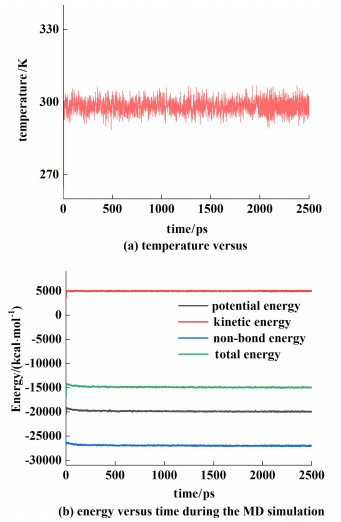
|
| 图 2 MD模拟过程中(a)温度与(b)能量随时间变化曲线 Fig.2 Changes of (a) temperature and (b) energy with time during the MD simulation |
| |
使用在 1.1小节构建的橡胶态聚合物膜模型,将模型逐步降温至玻璃化转变温度以下,每1个温度下进行300 ps的NPT动力学计算,取体系平衡时密度平均值进行分析。通过密度、比体积随温度变化曲线上的间断点,即可得到玻璃化转变温度,通过玻璃化转变温度验证模型合理性。图 3为SPSf模型的比体积-时间曲线,其间断点处即是模型的玻璃化温度(Tg),模拟所得Tg与实验值209 ℃非常接近,证明所选力场合适,构建的分离膜模型合理。
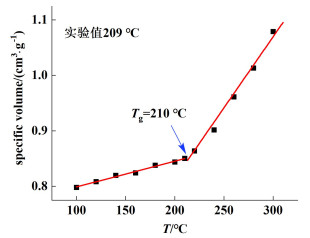
|
| 图 3 SPSf膜比体积-温度曲线 Fig.3 Specific volume of sulfonated polysulfone membrane as a function of temperature |
| |
为了更加准确地分析相关离子在SPSf膜表面的吸附-排斥行为和浓度分布,需要对溶液层中的离子和药物粒子的数量进行量化分析。将膜表面25 Å的溶液层沿Z轴正方向均分为20个区域,每2个区域记为1个水平液层(分别记为液层1~液层10),每个水平液层的高度为2.5 Å(如图 4所示),并统计出模拟过程中每个区域中离子/药物粒子的数量。将每个区域中粒子数量除以溶液层中粒子总数,所得到的数值为不同粒子在膜表面的分布强度值(Intensity),强度越高代表该区域内的粒子数量越多,所有区域内的同种粒子强度值和为100%。
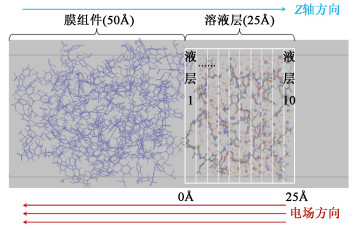
|
| 图 4 不同电场强度下膜-溶液层模拟示意图 Fig.4 Schematic diagram of the membrane-solution layer under different electric field strength |
| |
为了能够更清晰的判断电场强度对粒子分布的影响情况,先计算累加分布强度值(Intensity Sum,0~100%),计算方法如公式(3)所示。
| $ {\text { intensity }}\; {\rm{sum}}(r)=\mathop \sum \limits^{\substack{i=0 \\ i=25}}{ \text { intensity }}\left(r_i\right) $ | (3) |
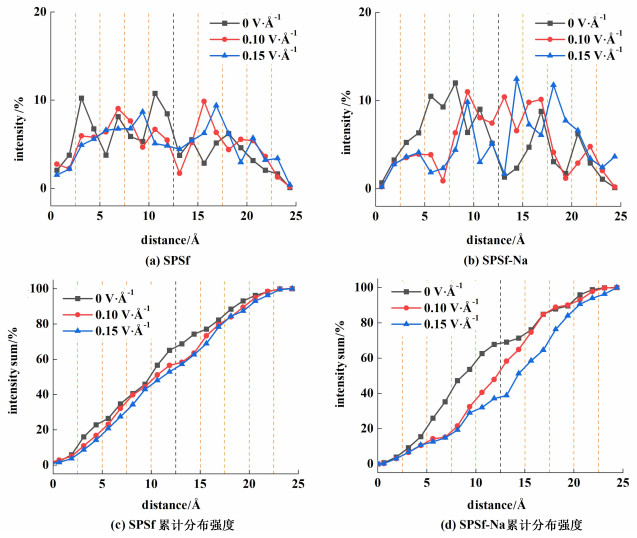
图 5和图 6是Cefuroxime-与Cl-在SPSf与SPSf-Na膜表面溶液层中的分布情况。电场强度为0 V ·Å-1时,SPSf膜表面Cefuroxime-聚集在液层2~液层5(距膜表面2.5~ 12.5 Å)区域内;随着电场强度增加至0.15 V ·Å-1,液层2中Cefuroxime-分布强度值从17.97%下降至10.47%,下降了约6%;而在远离膜表面区域的液层7内,分布强度值由0 V ·Å-1时的7.98%升高0.15 V ·Å-1时的15.62%,升高了约8%。0 V ·Å-1时,SPSf-Na膜表面Cefuroxime-聚集在液层3~液层5区域内;当电场强度增加至0.15 V ·Å-1时,Cefuroxime-受电场力作用移动在液层4~液层7区域内。由图 5(c)与图 5(d)对比发现,未加电场时,Cefuroxime-在SPSf膜表面与SPSf-Na膜表面的累计分布强度值数值相差不大,说明未加电场时Cefuroxime-在SPSf膜表面与SPSf-Na膜表面的浓度分布类似。但随着电场强度的增大,在液层1~6之间SPSf-Na膜表面累计分布强度值低于SPSf膜,SPSf-Na膜对Cefuroxime-的排斥作用更强。
|
| 图 5 Cefuroxime-分布强度(a) SPSf, (b) SPSf-Na与累计分布强度值(c) SPSf, (d) SPSf-Na Fig.5 Distribution intensity of Cefuroxime- in the solution layer (a) SPSf; (b) SPSf-Na and accumulated distribution intensity (c) SPSf; (d) SPSf-Na |
| |
|
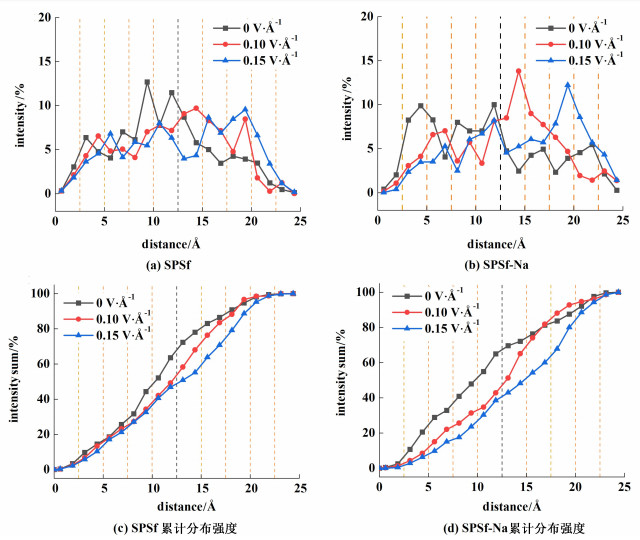
| 图 6 Cl-分布强度(a) SPSf, (b) SPSf-Na与累计分布强度值(c) SPSf, (d) SPSf-Na Fig.6 Distribution intensity of Cl- in the solution layer (a) SPSf; (b) SPSf-Na and accumulated distribution intensity (c) SPSf; (d) SPSf-Na |
| |
电场强度为0 V ·Å-1时,相比SPSf膜,Cl-在SPSf-Na膜表面(液层2)区域的分布强度值升高7%。这是由于SPSf-Na膜内使用Na+配平,Cl-被吸引至膜表面区域。随着电场强度的增加,Cl-分布强度的峰值出现在距膜表面更远处,累计分布强度下降。带负电的粒子会向远离膜表面的方向移动,外加电场能够增强SPSf膜截留Cefuroxime-与Cl-的能力。
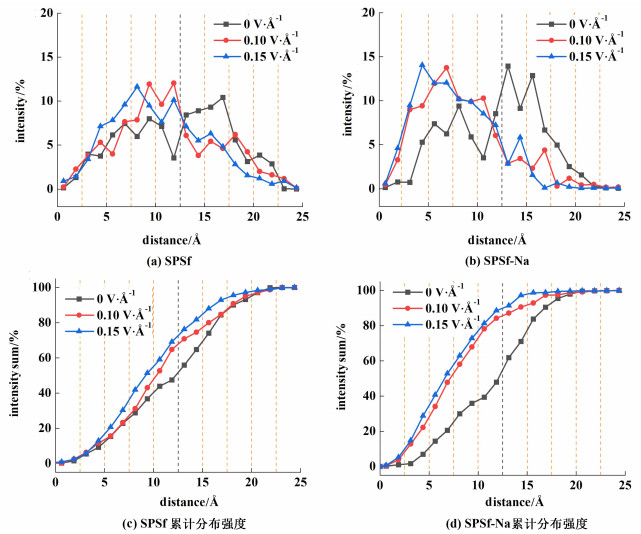
图 7是Na+在SPSf与SPSf-Na膜表面溶液层中的分布情况。当电场强度为0 V ·Å-1时,两体系中Na+主要聚集在液层6与液层7区域内。随着电场强度增加,在SPSf体系中,Na+在电泳作用下,逐渐移动至液层4与液层5;在SPSf-Na体系中,在电泳与膜表面负电基团的共同作用下,Na+被吸引至液层2与液层3,电场增强了SPSf膜对Na+的吸附作用。
|
| 图 7 Na+分布强度(a) SPSf, (b) SPSf-Na与累计分布强度值(c) SPSf, (d) SPSf-Na Fig.7 Distribution intensity of Na+ in the solution layer (a) SPSf; (b) SPSf-Na and accumulated distribution intensity (c) SPSf; (d) SPSf-Na |
| |
由图 7(c)与图 7(d)对比发现,电场强度为0 V ·Å-1时,SPSf-Na膜内Na+扩散至溶液层中,造成溶液层中Na+向远离膜表面方向扩散,液层1~4区域内SPSf-Na膜表面溶液层中Na+浓度低于SPSf体系。随着电场强度增大,SPSf-Na膜表面Na+累计分布强度增加的幅度>SPSf膜,SPSf-Na膜对Na+的吸附能力更强。
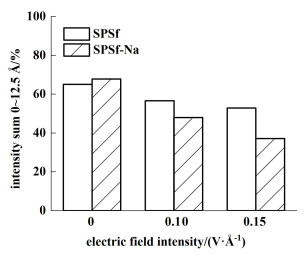
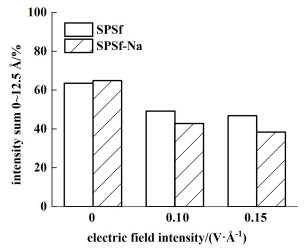
为了定量化对比不同电场强度下2种SPSf膜的作用能力,讨论电辅助荷电膜分离医药废水的理论机理,如图 8~图 10所示,我们计算了距离SPSf膜界面的前5个液层中(0~12.5 Å)不同粒子的分布强度累计。SPSf-Na是水解后的膜,膜自身带负电,为了电荷守恒,在膜内使用Na+配平。当电场强度为0 V ·Å-1时,距离SPSf膜界面0~12.5 Å区域内Cefuroxime-分布强度累计为65%,SPSf-Na体系Cefuroxime-分布强度累计为67.8%,增加了约2.8%;在SPSf体系中Cl-分布强度累计为63.6%,解离后SPSf-Na体系中Cl-分布强度累计为64.9%,增加了约1.3%。在距离膜界面前10个液层中的Cefuroxime-与Cl-分布强度累计大小为SPSf-Na体系>SPSf体系,这是因为SPSf-Na膜内含有大量的Na+,会吸引溶液层中带负电的离子,使得Cefuroxime-与Cl-富集在膜表面区域内。
|
| 图 8 距膜界面0~12.5 Å液层中Cefuroxime-分布强度累计 Fig.8 Accumulated distribution intensity of Cefuroxime- in the liquid layer from 0 to 12.5 Å from the membrane interface |
| |
|
| 图 9 距膜界面0~12.5 Å液层中Cl-分布强度累计 Fig.9 Accumulated distribution intensity of Cl-in the liquid layer from 0 to 12.5 Å from the membrane interface |
| |
|
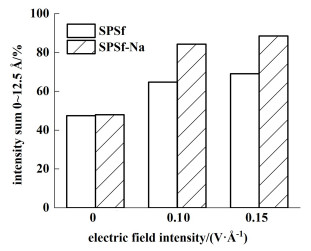
| 图 10 距膜界面0~12.5 Å液层中Na+分布强度累计 Fig.10 Na+ distribution intensity sum in the liquid layer from 0 to 12.5 Å from the membrane interface |
| |
SPSf为膜表面不带电的空白膜,溶液层中带电粒子受到电泳作用定向移动,Cefuroxime-分布强度累计从65%下降至52.8%,Cl-分布强度累计从63.6%下降至46.8%,对离子的排斥能力不强。但解离后的SPSf-Na体系中,随着电场强度从0增加至0.15 V ·Å-1,前5个液层内的Cefuroxime-分布强度累计从67.8%下降至37.1%,Cl-分布强度累计从64.9%下降至38.4%,Na+分布强度累计从47.9%增加至88.5%,对带负电粒子的排斥能力远强于SPSf体系,对Na+的吸附也更强。
荷电膜解离后,对Cefuroxime-与Cl-的排斥能力增强(相比SPSf,SPSf-Na膜表面Cefuroxime-强度下降15.7%),说明外加电场主要强化膜表面的Donnan效应,同时也增强对Na+的静电吸附作用(荷电膜解离后,膜表面Na+强度增加19.4%)。外加电场作用下,膜表面带电粒子的浓度差异应归因于电辅助增强Donnan效应与静电吸附或排斥作用,而不是电泳作用。
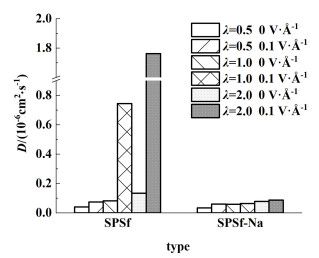
2.3 电场强度与膜内含水量λ对水分子及相关离子的扩散系数对比为了分析电场强度与含水量λ对SPSf膜内粒子的传输的影响,我们根据MSD曲线计算了体系中Na+与Cefuroxime-的扩散系数,如图 11和图 12所示。
|
| 图 11 不同λ与电场强度下SPSf膜内Na+扩散系数 Fig.11 Diffusion coefficient of Na+ in SPSf membranes with different water content and electric field strength |
| |
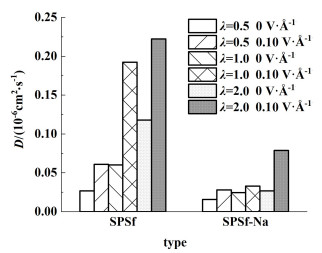
|
| 图 12 不同λ与电场强度下SPSf膜内Cefuroxime-扩散系数 Fig.12 Diffusion coefficient of Cefuroxime- in SPSf membranes with different water content and electric field strength |
| |
在2种SPSf膜体系中,随着λ的增大,水分子填充孔道,削弱了膜对离子的吸附,Na+与Cefuroxime-的扩散系数不断增大。由于Cefuroxime-与膜支链间容易形成氢键,Na+扩散系数的增加幅度明显高于Cefuroxime-。水解后SPSf-Na膜体系中含有大量带负电的—SO3基团,对Na+有较强吸附作用,Na+的扩散能力低于未水解的SPSf膜体系。随着电场强度增加,削弱了分子间氢键作用与膜对粒子的静电吸附能力,SPSf膜体系中离子扩散系数增大。
由表 2可以发现,在λ= 0.5时,随着电场强度的增加,SPSf膜中,Na+的扩散系数增大了1.87倍,Cefuroxime-的扩散系数增大了2.27倍。即随着电场强度的增加,SPSf膜的传导能力在增强,含水量对膜传输性能的影响很大,且Cefuroxime-的扩散系数要比Na+对电场的变化更为敏感。
| Na+ | Cefuroxime- | |
| SPSf | 1.87 | 2.27 |
| SPSf-Na | 1.74 | 1.79 |
为了探究电场强度与含水量λ对离子在膜内的选择性的影响,我们计算了Na+扩散系数与Cefuroxime-扩散系数的差值,如表 3所示。由于Na+的尺寸 < Cefuroxime-的尺寸,在相同λ与电场强度下,Na+的扩散系数>Cefuroxime-的扩散系数。随着电场强度与λ的增大,SPSf与SPSf-Na体系中2种离子扩散系数的差值增大。在λ=2.0、电场强度为0.1 V ·Å-1时,SPSf体系中2种离子扩散系数相差1.54×10-6 cm2 ·s-1,在这种条件下有非常显著的离子选择性。
| D/(10-6 cm2·s-1) | ||||
| λ=0.5 0 V·Å-1 | λ=0.5 0.10 V·Å-1 | λ=2.0 0 V·Å-1 | λ=2.0 0.10 V·Å-1 | |
| SPSf | 0.013 | 0.014 | 0.016 | 1.540 |
| SPSf-Na | 0.019 | 0.032 | 0.051 | 0.008 |
利用分子动力学模拟(MD)技术,通过统计分析磺化聚砜膜表面的带电离子(主要研究了Na+、Cl-和头孢呋辛离子)空间分布的变化趋势与膜内粒子的扩散系数,模拟分析了电场辅助下磺化聚砜膜分离头孢呋辛钠医药废水的作用机制,并得到以下结论。
外加电场增强荷电膜表面基团对同性离子的排斥能力,增加截留率。随着外部电场在一定程度上的增强(0~0.15 V ·Å-1),荷电膜解离后对带负电粒子具有更强的排斥能力(相比SPSf,SPSf-Na膜表面Cefuroxime-强度下降15.7%),对Na+吸附能力更强(荷电膜解离后,膜表面Na+强度增加19.4%),证明电增强Donnan效应与电增强吸附/脱附,是电辅助荷电纳滤膜分离医药废水的主要作用机理。在本文的模拟实验范围内,随着SPSf膜内含水量与电场强度增加,Na+扩散系数增大13.22倍,Cefuroxime-的扩散系数增大1.89倍,荷电膜内Cefuroxime-与Na+扩散能力增强。λ=2.0、电场强度为0.10 V ·Å-1时,SPSf体系这Na+扩散系数与Cefuroxime-扩散系数相差1.54×10-6 cm2 ·s-1,在这种条件下离子选择性最高,对于实现离子分离、医药分子综合回收有潜在的应用意义。
综上,本研究基于MD结果,为电场辅助下磺化聚砜膜分离头孢呋辛钠医药废水的机理研究提供了相关模拟数据,为未来理性设计和选择荷电膜材料与膜表面的基团改性提供了有益的理论基础。
| [1] |
LI Z, LI M, ZHANG Z, et al. Antibiotics in aquatic environments of China: A review and meta-analysis[J]. Ecotoxicology and Environmental Safety, 2020, 199: 110668. DOI:10.1016/j.ecoenv.2020.110668 |
| [2] |
SHAO Y, WANG Y, YUAN Y, et al. A systematic review on antibiotics misuse in livestock and aquaculture and regulation implications in China[J]. Science of the Total Environment, 2021, 798: 149205. DOI:10.1016/j.scitotenv.2021.149205 |
| [3] |
JIANG Y, RAN J, MAO K, et al. Recent progress in Fenton/Fenton-like reactions for the removal of antibiotics in aqueous environments[J]. Ecotoxicology and Environmental Safety, 2022, 236: 113464. DOI:10.1016/j.ecoenv.2022.113464 |
| [4] |
曹卫凯. 头孢呋辛钠的合成研究[J]. 精细石油化工进展, 2016, 17(4): 55-58. CAO Weikai. Research on synthesis of cefuroxime sodium[J]. Advances in Fine Petrochemicals, 2016, 17(4): 55-58. (in Chinese) |
| [5] |
ZHANG Q, YING G, PAN C, et al. Comprehensive evaluation of antibiotics emission and fate in the river basins of China: Source analysis, multimedia modeling, and linkage to bacterial resistance[J]. Environmental Science & Technology, 2015, 49(11): 6772-6782. |
| [6] |
SALAEH S, JURETIC PERISIC D, BIOSIC M, et al. Diclofenac removal by simulated solar assisted photocatalysis using TiO2-based zeolite catalyst; mechanisms, pathways and environmental aspects[J]. Chemical Engineering Journal, 2016, 304: 289-302. DOI:10.1016/j.cej.2016.06.083 |
| [7] |
顾俊璟, 王志, 樊智锋, 等. 化学氧化法处理抗生素制药废水[J]. 化学工业与工程, 2007, 24(4): 291-294, 313. GU Junjing, WANG Zhi, FAN Zhifeng, et al. Chemical oxidation technology in treatment of pharmaceutical wastewater containing antibiotic[J]. Chemical Industry and Engineering, 2007, 24(4): 291-294, 313. (in Chinese) |
| [8] |
ISIK O, ERBIL M C, ABDELRAHMAN A M, et al. Removal of micropollutants from municipal wastewater by membrane bioreactors: Conventional membrane versus dynamic membrane[J]. Journal of Environmental Management, 2022, 303: 114233. DOI:10.1016/j.jenvman.2021.114233 |
| [9] |
SHEARER L, PAP S, GIBB S W. Removal of pharmaceuticals from wastewater: A review of adsorptive approaches, modelling and mechanisms for metformin and macrolides[J]. Journal of Environmental Chemical Engineering, 2022, 10(4): 108106. DOI:10.1016/j.jece.2022.108106 |
| [10] |
ZHANG H, TU Y, DUAN Y, et al. Production of biochar from waste sludge/leaf for fast and efficient removal of diclofenac[J]. Journal of Molecular Liquids, 2020, 299: 112193. DOI:10.1016/j.molliq.2019.112193 |
| [11] |
薛冠, 胡小玲, 陈晓佩, 等. 膜分离技术在医药医疗中的研究和应用[J]. 化学工业与工程, 2009, 26(2): 183-188. XUE Guan, HU Xiaoling, CHEN Xiaopei, et al. Applications of membrane separation technology in the production of medicine and medical treatment[J]. Chemical Industry and Engineering, 2009, 26(2): 183-188. (in Chinese) |
| [12] |
汪瑶, 李天祥, 朱静. 膜蒸馏技术在工业废水处理中的研究进展[J]. 化学工业与工程, 2021, 38(4): 56-63. WANG Yao, LI Tianxiang, ZHU Jing. Research progress of membrane distillation technology in industrial wastewater treatment[J]. Chemical Industry and Engineering, 2021, 38(4): 56-63. (in Chinese) |
| [13] |
NASROLLAHI N, VATANPOUR V, KHATAEE A. Removal of antibiotics from wastewaters by membrane technology: Limitations, successes, and future improvements[J]. Science of the Total Environment, 2022, 838: 156010. DOI:10.1016/j.scitotenv.2022.156010 |
| [14] |
MEDHAT B F, PAKIZEH M. Preparation and characterization of a nanoclay/PVA/PSf nanocomposite membrane for removal of pharmaceuticals from water[J]. Applied Clay Science, 2018, 162: 326-338. DOI:10.1016/j.clay.2018.06.029 |
| [15] |
GUO S, CHEN X, WAN Y, et al. Custom-tailoring loose nanofiltration membrane for precise biomolecule fractionation: New insight into post-treatment mechanisms[J]. ACS Applied Materials & Interfaces, 2020, 12(11): 13327-13337. |
| [16] |
ALI ZAZOULI M, SUSANTO H, NASSERI S, et al. Influences of solution chemistry and polymeric natural organic matter on the removal of aquatic pharmaceutical residuals by nanofiltration[J]. Water Research, 2009, 43(13): 3270-3280. DOI:10.1016/j.watres.2009.04.038 |
| [17] |
ZHANG H, QUAN X, CHEN S, et al. Combined effects of surface charge and pore size on Co-enhanced permeability and ion selectivity through RGO-OCNT nanofiltration membranes[J]. Environmental Science & Technology, 2018, 52(8): 4827-4834. |
| [18] |
WENG X, JI Y, MA R, et al. Superhydrophilic and antibacterial zwitterionic polyamide nanofiltration membranes for antibiotics separation[J]. Journal of Membrane Science, 2016, 510: 122-130. DOI:10.1016/j.memsci.2016.02.070 |
| [19] |
HOMAYOONFAL M, MEHRNIA M R. Amoxicillin separation from pharmaceutical solution by pH sensitive nanofiltration membranes[J]. Separation and Purification Technology, 2014, 130: 74-83. DOI:10.1016/j.seppur.2014.04.009 |
| [20] |
ZHAO S, YAO Y, BA C, et al. Enhancing the performance of polyethylenimine modified nanofiltration membrane by coating a layer of sulfonated poly(ether ether ketone) for removing sulfamerazine[J]. Journal of Membrane Science, 2015, 492: 620-629. DOI:10.1016/j.memsci.2015.03.017 |
| [21] |
WU M, RUAN X, RICHMAN T K, et al. Cefalexin crystallization residual liquor separation via nanofiltration based multistage process[J]. Separation and Purification Technology, 2020, 251: 117356. DOI:10.1016/j.seppur.2020.117356 |
| [22] |
ZHEN H, WU M, YUAN Z, et al. Nanofiltration membrane with CM-β-CD tailored polyamide layer for high concentration cephalexin solution separation[J]. Journal of Membrane Science, 2023, 672: 121445. DOI:10.1016/j.memsci.2023.121445 |
| [23] |
王乾杰, 李红海, 耿道静. 电渗析法处理高盐度高COD废水矿化度的试验研究[J]. 化学工业与工程, 2019, 36(1): 72-77. WANG Qianjie, LI Honghai, GENG Daojing. Treatment of high COD waste water with high-salinity using electrodialysis[J]. Chemical Industry and Engineering, 2019, 36(1): 72-77. (in Chinese) |
| [24] |
LEE J H, YUN E, HAM S Y, et al. Electrically conductive carbon nanotube/graphene composite membrane for self-cleaning of biofouling via bubble generation[J]. Desalination, 2022, 535: 115841. DOI:10.1016/j.desal.2022.115841 |
| [25] |
FAN X, WEI G, QUAN X. Carbon nanomaterial-based membranes for water and wastewater treatment under electrochemical assistance[J]. Environmental Science: Nano, 2023, 10(1): 11-40. DOI:10.1039/D2EN00545J |
| [26] |
FAN X, ZHAO H, LIU Y, et al. Enhanced permeability, selectivity, and antifouling ability of CNTs/Al2O3 membrane under electrochemical assistance[J]. Environmental Science & Technology, 2015, 49(4): 2293-2300. |
| [27] |
LIU Q, WANG X, GUO Y, et al. Mechanism of ethanol/water reverse separation through a functional graphene membrane: A molecular simulation investigation[J]. Frontiers of Chemical Science and Engineering, 2023, 17(3): 347-357. DOI:10.1007/s11705-022-2246-z |
| [28] |
AHMAD A, LI S, ZHAO Z. Insight of organic molecule dissolution and diffusion in cross-linked polydimethylsiloxane using molecular simulation[J]. Journal of Membrane Science, 2021, 620: 118863. DOI:10.1016/j.memsci.2020.118863 |
| [29] |
LIU J, XU Q, JIANG J. A molecular simulation protocol for swelling and organic solvent nanofiltration of polymer membranes[J]. Journal of Membrane Science, 2019, 573: 639-646. DOI:10.1016/j.memsci.2018.12.035 |
| [30] |
WEI W, WANG M, JIANG J. Molecular simulation study on molecularly mixed porous organic cage/polymer composite membranes for water desalination and solvent recovery[J]. ACS Applied Nano Materials, 2021, 4(10): 10378-10388. DOI:10.1021/acsanm.1c01886 |
| [31] |
SUN H, JIN Z, YANG C, et al. COMPASS Ⅱ: Extended coverage for polymer and drug-like molecule databases[J]. Journal of Molecular Modeling, 2016, 22(2): 47. DOI:10.1007/s00894-016-2909-0 |
| [32] |
ANDERSEN H C. Molecular dynamics simulations at constant pressure and/or temperature[J]. The Journal of Chemical Physics, 1980, 72(4): 2384-2393. DOI:10.1063/1.439486 |
| [33] |
SINGH M B, DALVI V H, GAIKAR V G. Investigations of clustering of ions and diffusivity in concentrated aqueous solutions of lithium chloride by molecular dynamic simulations[J]. RSC Advances, 2015, 5(20): 15328-15337. DOI:10.1039/C4RA15124K |
 2024, Vol. 41
2024, Vol. 41





