2. 中国长江三峡集团有限公司科学技术研究院综合能源技术研究中心, 北京 100038
2. Comprehensive Energy Research Center, Institute of Science and Technology, China Three Gorges Corporation, Beijing 100038, China
在众多电化学能量储存与转化器件中,双电层电容器(EDLCs)具有快速充放电、长寿命等优点,广泛应用于新能源汽车动力电源以及航空航天等领域[1-7]。然而,较低的能量密度限制了EDLCs的发展,提高其能量密度成为研究的焦点。根据E=0.5CV2(C为多孔炭电极材料的比电容、V为EDLCs的电压窗口、E为EDLCs的能量密度)可知[8, 9],可以从两方面提高EDLCs的能量密度:(1)提高多孔炭电极材料的比容量;(2)拓宽电压窗口则可以平方倍地提高能量密度。因此扩宽电压窗口是提高EDLCs能量密度的关键。
提高多孔炭电极材料的耐电压特性是扩宽EDLCs电压窗口的好方法。而电导率、孔结构以及含氧官能团等均会影响多孔炭电极材料的耐电压特性[10-13]。其中含氧官能团(羟基、羧基、酸酐、内酯、醌基等)对多孔炭电极材料的耐电压特性影响很大。当电压升高(>3.0 V)时,正极多孔炭电极材料上的含氧官能团会与电解液(碳酸丙烯酯)发生电化学氧化反应,生成CO和CO2等气体[11]。此外,电极材料表面含氧官能团会与电解液反应生成一层固态电解质(SEI)膜[13]。SEI膜的存在会阻碍电解质离子进入多孔炭电极材料的孔道,导致EDLCs容量和能量密度的迅速衰减。因此,降低多孔炭电极材料表面含氧官能团的含量显得尤为重要。
脱除多孔炭电极材料表面含氧官能团的常用方法包括化学还原法和热还原法[14]。化学还原法是通过化学还原试剂(如水合肼、硼氢化钠、单宁酸、抗坏血酸等)脱除多孔炭材料表面的羟基、环氧基等含氧基团[15-17]。然而化学还原法所需的还原试剂对环境不友好。热还原法是通过热断键作用脱除炭材料表面热力学不稳定的官能团,如羧基、羟基和酯基等[18]。热还原法常用的气体氛围包括惰性气氛(N2、Ar)和还原性气氛(H2、NH3)。然而热还原法的温度一般小于1 000 ℃,使得多孔炭材料表面含氧官能团的摩尔分数降低至3%~5%[10, 18]。这是由于过高温度脱除多孔炭材料表面含氧官能团的同时,会破坏原有的炭骨架,造成多孔炭层次孔结构的坍塌。Chang等[10]经过800 ℃的热还原处理(N2气氛),使得框架填充型C/C多孔炭材料的表面含氧官能团摩尔分数从6.6%降低至5.6%,却破坏了框架填充型C/C多孔炭材料的层次孔结构,导致中孔孔容下降了32%。因此,有效降低多孔炭材料表面含氧官能团的含量而不破坏多孔炭材料的层次孔结构是一项富有挑战的工作。
氢溢流是指氢气分子吸附在固体催化剂表面后解离为高活性的氢原子,活化的氢原子迁移至其他位置的现象。氢溢流包括一级氢溢流和二级氢溢流[19-22]。催化剂表面解离的氢原子扩散到固体催化剂其他位置称为一级氢溢流。而催化剂表面解离的氢原子随着气相扩散到另一种材料表面被称为二级氢溢流。本论文选择镍基催化剂,利用催化剂表面的氢溢流现象来低温脱除多孔炭材料表面的含氧官能团。本论文对比了热还原(H2气氛)、一级氢溢流以及二级氢溢流脱氧前后多孔炭材料的形貌、碳微晶结构、层次孔结构和表面含氧官能团的变化,揭示了不同还原方法脱除含氧官能团的能力差异,分析了不同脱氧方法脱除多孔炭材料表面含氧官能团的作用机制。此外,进一步表征了所得多孔炭的电化学性能,揭示了多孔炭的结构与储能特性之间的构效关系,为耐电压多孔炭电极材料和高能量密度EDLCs的构建提供了理论指导。
1 实验与表征 1.1 实验部分热还原法(H2气氛)脱除多孔炭含氧基团:把多孔炭原料PC(型号:21-KSN)放入到管式炉中,在体积分数为7%的H2/Ar混合气中以5 ℃·min-1的升温速率加热至655 ℃,保温1 h后自然冷却即可得到热还原后(H2气氛)的样品PC-655。
一级氢溢流脱除多孔炭含氧基团:把0.02 g NiCl2·6H2O和0.1 g PC均匀分散在200 μL去离子水中,经过15 min超声浸渍、30 min真空浸渍和12 h浸渍后,烘干即可得到PC@NiCl2。将PC@NiCl2放入管式炉中,在体积分数为7% H2/Ar混合气的气氛中,以5 ℃·min-1的加热速率加热到655 ℃,保持1 h后降温即可得到PC@Ni-655。再经盐酸酸洗,即可得到一级脱氧后的多孔炭样品PC@Ni-655-HCl。
二级氢溢流脱除多孔炭含氧基团:将PC和PC@Ni-655分别放置在镍舟的不同位置,2种材料相邻但不接触,保证PC和PC@Ni-655的质量比为1∶1。在体积分数为7% H2/Ar混合气的气氛,以5 ℃·min-1的加热速率加热到655 ℃,保持1 h后降温即可得到二次氢溢流脱氧后的多孔炭样品PC-Ni-655。
1.2 材料表征催化剂和多孔炭的形貌通过扫描电子显微镜(SEM, S-4800)和透射电子显微镜(TEM, JEM-F200)进行表征。借助程序恒温还原确定发生氢溢流的温度区间。利用X射线粉末衍射(XRD, Rigaku D/max 2500, Cu_Kα, λ=0.15406 nm)、拉曼测试(LabRAM HR Evolution)、X射线光电子能谱(XPS, Perkin Elmer, PHI-1600)和物理吸附仪(北京贝士德,3H-2000PS2型)表征催化剂和多孔炭材料的结构。
1.3 电化学测试按照8∶1∶1的比例称取多孔炭、导电炭黑(Super P)和粘结剂PTFE,并均匀分散在乙醇溶液中。烘干多余的乙醇后将所得的混合物辊压成均匀的薄膜(厚度60~120 μm),随后把所得的薄膜和集流体(单面涂炭铝箔)压在一起即可得到极片。用所得的极片组装有机系EDLCs(电解液为1 mol·L-1的TEABF4/PC)。
采用电化学工作站(Ametek, Parstat 2273)对组装好的EDLCs进行循环伏安测试(CV)和交流阻抗测试(EIS)。CV测试电压区间为0~3.3 V,扫描速度的范围是0~100 mV·s-1。EIS测试的频率范围是0.01~105 Hz。
2 结果与讨论氢溢流包括一级氢溢流和二级氢溢流。两者脱除多孔炭含氧基团的过程不同。对于一级氢溢流脱除多孔炭含氧基团的过程,负载镍纳米颗粒的多孔炭(PC@Ni)同时作为催化剂和活性炭原料,氢气分子会吸附在镍纳米颗粒表面,随后被解离为高活性的氢原子。解离的氢原子扩散到负载镍纳米颗粒的多孔炭材料的其他位置,脱除多孔炭表面的含氧官能团。随后刻蚀掉镍纳米颗粒就能得到脱除含氧官能团的多孔炭(记为PC@Ni-655-HCl)。然而对于二级氢溢流脱除多孔炭含氧基团的过程,以负载镍纳米颗粒的多孔炭(PC@Ni)为催化剂,催化剂表面解离的高活氢原子能随气相扩散至另一多孔炭原料PC的表面,从而脱除PC表面的含氧基团得到的多孔炭PC-Ni-655。值得注意的是,二级氢溢流脱氧过程中,解离的高活性氢原子移动距离可达厘米级[19, 20, 23, 24],但其活性保持时间不长。
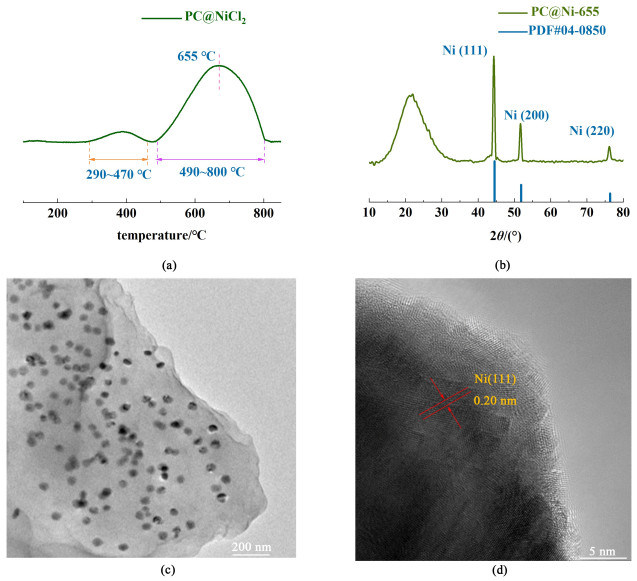
2.1 镍基催化剂的表征氢溢流的产生受催化剂的影响。以PC@NiCl2为前驱体,分析以PC@Ni催化剂时,发生氢溢流的温度范围。如图 1(a)所示,H2-TPR曲线中第1个峰(290~470 ℃)的产生有2方面原因:(1)部分镍离子还原成单质镍会消耗氢气,此时PC@NiCl2转变为PC@Ni;(2)在已还原的镍纳米颗粒的催化下,氢气解离为氢原子,解离的高活性氢原子扩散至PC@Ni的含氧基团上,并将含氧官能团还原。而第2个峰(490~800 ℃)的产生是由于随着温度的升高,更多的氢原子解离出来并获得足够大的能量来克服迁移过程中的能垒,从而迁移到远离金属镍的载体表面或者二级材料表面,并脱除材料表面的含氧基团。第2个峰的峰值温度为655 ℃,因此以PC@Ni为催化剂时,发生氢溢流的温度为655 ℃。
|
| 图 1 (a) C@NiCl2的H2-TPR分析图;PC@Ni-655催化剂的(b) XRD图像、(c) TEM图像和(d) HRTEM图像 Fig.1 (a) H2-TPR analyze of PC@NiCl2; (b) XRD pattern; (c) TEM image and (d) HRTEM image of PC@Ni-655 |
| |
多孔炭的脱氧效率与氢溢流过程中解离的高活氢原子的空间分布息息相关,而氢原子的空间分布则受催化剂镍颗粒的尺寸和空间分布的影响。对于PC@Ni-655催化剂[图 1(b)~图 1(d)],单质镍纳米颗粒(JCPDS: 04-0850)均匀分布在无定形的碳骨架当中。镍纳米颗粒上0.20 nm的晶格条纹对应于镍的(111)晶面。镍纳米颗粒(平均尺寸60~80 nm)有利于暴露出更多的活性位点,促进高活性氢原子的产生。
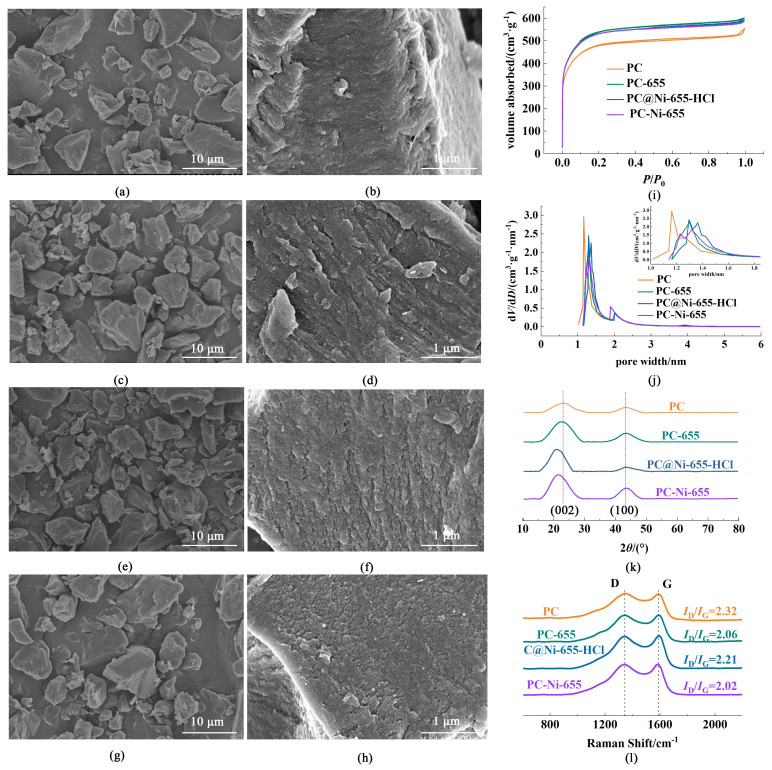
2.2 热还原(H2气氛)、一级氢溢流和二级氢溢流对多孔炭形貌、孔结构和石墨微结构的影响热还原(H2气氛)、一级氢溢流和二级氢溢流还原对多孔炭的形貌影响不大。多孔炭PC原料是5~10 μm的块状颗粒[图 2(a)~图 2(b)],经过热还原(H2气氛,655 ℃)脱氧后,所得的多孔炭PC-655的形貌没有明显变化[图 2(c)~图 2(d)]。而经过一级、二级氢溢流后得到的PC@Ni-655-HCl和PC-Ni-655的形貌与PC原料的形貌差别不大。因此,在655 ℃温度下氢气直接还原和氢溢流还原对多孔炭的形貌影响不大。
|
| 图 2 (a~(b) PC、(c)~(d) PC-655、(e)~(f) PC@Ni-655-HCl和(g)~(h) PC-Ni-655的SEM和HRSEM图像; 样品PC、PC-655、PC@Ni-655-HCl和PC-Ni-655的(i) N2吸脱附曲线、(j) 孔径分布曲线、(k) XRD图像以及(l) Raman图像 Fig.2 SEM images of (a)~(b) PC; (c)~(d) PC-655; (e)~(f) PC@Ni-655-HCl and (g)~(h) PC-Ni-655; (i) N2 adsorption/desorption isotherm curves; (j) pore distribution curves; (k) XRD patterns and (l) Raman spectra of PC, PC-655, PC@Ni-655-HCl and PC-Ni-655 |
| |
热还原(H2气氛)、一级氢溢流和二级氢溢流对多孔炭材料的比表面积和层次孔结构的影响相似。脱氧前后所得的4种多孔炭材料的N2吸脱附曲线均为典型的I型曲线,表明样品中存在大量微孔;而相对压力0.98~1.00处存在明显的翘尾,表明样品中存在一定数量的大孔。其中PC原料的比表面积(SBET)为1 511 m2·g-1,借助热还原(H2气氛)、一级氢溢流和二级氢溢流脱氧后,所得多孔炭PC-655,PC@Ni-655-HCl和PC-Ni-655的比表面积分别为1 684、1 658和1 661 m2·g-1。多孔炭比表面积的上升是由于PC原料中含氧官能团、缺陷位等以CO2、CO和H2O等脱除过程中,原有的小微孔变为尺寸较大的微孔。因此,脱氧后所得多孔炭的微孔孔径分布略微变大,微孔孔体积(Vmicro)也略有上升(表 1);而介孔孔径和介孔孔体积(Vmeso)几乎不变,表明热还原(H2气氛)、一级氢溢流和二级氢溢流脱除多孔炭表面含氧基团和缺陷位的同时不会破坏多孔炭的孔结构,造成孔道结构的收缩和坍塌。
| 样品 | SBETa/(m2·g-1) | Vtotalb/(cm3·g-1) | Vmesoc/(cm3·g-1) | Vmicrod/(cm3·g-1) |
| PC | 1 511 | 0.858 0 | 0.316 4 | 0.522 1 |
| PC-655 | 1 684 | 0.930 7 | 0.299 7 | 0.587 4 |
| PC@Ni-655-HCl | 1 658 | 0.919 0 | 0.299 2 | 0.583 9 |
| PC-Ni-655 | 1 661 | 0.906 8 | 0.307 3 | 0.565 2 |
| aSBET采用BET法计算,相对压力(P/P0)为0.05~0.35;bVtotal是根据P/P0为0.994时N2吸附量计算;cVmicro是孔径分布曲线(H-K模型)在0~2 nm之间的积分面积;dVmeso是孔径分布曲线(BJH模型)在2~50 nm之间的积分面积。 | ||||
经热还原(H2气氛)、一级氢溢流和二级氢溢流还原后,多孔炭材料的石墨微晶结构发生改变。和PC原料的(002)峰相比,经3种不同方法还原后的多孔炭的(002)峰变尖,表明还原后多孔炭中石墨微晶的结晶度升高。这是由于氢气还原和镍催化氢溢流还原会脱除部分缺陷并导致碳质颗粒的重排[25],从而生成有序度更高的石墨微晶结构。而和PC的(100)峰相比,经热还原(H2气氛)、一级氢溢流和二级氢溢流还原后,多孔炭(100)衍射峰峰位置向高角度方向偏移,表明多孔(100)面的微晶尺寸La100增大,进一步证明还原后多孔炭石墨微晶结构发生重排,平面芳香尺寸增大。此外,还原后多孔炭中碳原子的杂化形式也发生了变化。Raman图谱中(~1 360 cm-1)对应于sp3C(缺陷碳、边缘碳、平面裂隙和悬键等),G峰(~1 580 cm-1)对应于sp2C(石墨化碳)[9]。对于PC原料,其D峰与G峰的强度比(ID/IG,峰面积比值)为2.32[图 2(l)]。而还原后,PC-655、PC@Ni-655-HCl和PC-Ni-655的ID/IG值均变小,分别为2.06、2.21和2.02,表明sp3C含量逐渐减少,石墨微晶的有序度逐渐变大[图 2(l)],与XRD结果一致。然而,PC@Ni-655-HCl的ID/IG值减小并不明显,且D峰与G峰的位置没有偏移,这可能是由于Ni的d轨道与多孔炭的C的Π轨道杂化[26, 27]。综上分析,氢气还原(655 ℃)、一级氢溢流和二级氢溢流能够脱除热力学不稳定的缺陷碳,同时使碳质颗粒重排、石墨微晶结构更加有序。
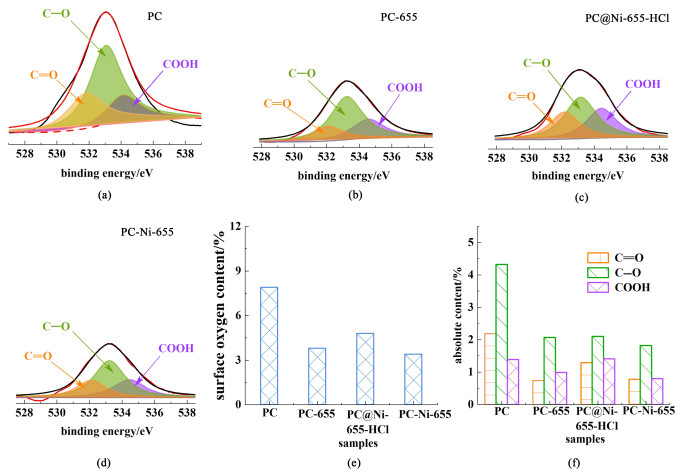
2.3 热还原(H2气氛)、一级氢溢流和二级氢溢流对多孔炭脱氧的作用多孔炭表面含氧基团的脱除效果与还原方式息息相关。相比于原料PC[表面含氧量摩尔分数为7.9%,图 3 (a)~图 3(d)和表 2],经过热还原、一级氢溢流和二级氢溢流还原后,所得的PC-655、PC@Ni-655-HCl和PC-Ni-655样品中表面含氧量摩尔分数分别降低为3.8%、4.8%和3.4%。而C/O比也从原料PC的11.7分别升高为25.3(PC-655),19.8(PC@Ni-655-HCl)和28.4(PC-Ni-655)。氧含量的降低说明氢气分子或解离的氢原子与多孔炭材料表面的含氧官能团发生反应,使含氧官能团转变为CO2、CO和H2O等气体产物而脱除。并且一级氢溢流脱氧效果较弱,而二级氢溢流的脱氧效果最优。
|
| 图 3 (a) PC、(b) PC-655、(c) PC@Ni-655-HCl和(d) PC-Ni-655的O 1s XPS图谱;PC、PC-655、PC@Ni-655-HCl和PC-Ni-655的(e) 表面含氧量对比图和(f) 各含氧官能团含量对比图 Fig.3 The O 1s XPS spectra of (a) PC; (b) PC-655; (c) PC@Ni-655-HCl and (d) PC-Ni-655. The contents of (e) total surface oxygen and (f) each oxygen-containing group of PC, PC-655, PC@Ni-655-HCl and PC-Ni-655 samples |
| |
| 样品 | XPS分析 | 绝对含量a/% | |||||
| C | O | C/O | C=O | C—O | COOH | ||
| PC | 92.1 | 7.9 | 11.7 | 2.19 | 4.32 | 1.39 | |
| PC-655 | 96.2 | 3.8 | 25.3 | 0.74 | 2.07 | 0.99 | |
| PC@Ni-655-HCl | 95.2 | 4.8 | 19.8 | 1.29 | 2.10 | 1.41 | |
| PC-Ni-655 | 96.6 | 3.4 | 28.4 | 0.78 | 1.82 | 0.80 | |
| aAbsolute content由样品表面氧元素原子含量乘以含氧基团峰面积比例计算得到,摩尔分数。 | |||||||
热还原、一级氢溢流和二级氢溢流对不同种类含氧官能团的脱除效果不同。3种还原方式对C—O基团的脱除效果最好[图 3(a)~图 3(d)和图 3(f)]。相比于原料PC中C—O组分(摩尔分数为4.32%),所得的PC-655、PC@Ni-655-HCl和PC-Ni-655样品中C—O组分摩尔分数分别下降为2.07%、2.10%和1.82%。PC-Ni-655样品中C—O组分含量最低表明相同温度(655 ℃)下氢原子对C—O还原效果最佳。3种还原方式对C=O的脱除效果次之,从摩尔分数2.19%(PC)降低到0.74%(PC-655),1.29%(PC@Ni-655-HCl)以及0.78%(PC-Ni-655),表明655 ℃下氢气分子、氢溢流产生的氢原子能够与C=O发生反应,使得C=O热解断裂生成CO气体或者加氢转化为C—OH等基团。而3种还原方式对COOH基团的脱除存在明显差异。经热还原(H2气氛)和二级氢溢流还原后,COOH的含量明显下降,其绝对摩尔分数均小于1%。这是由于COOH热稳定性较差,因此在还原过程中热解成CO2脱除。而一级氢溢流还原后COOH的绝对含量反而由原料PC的1.39%上升至1.41%。这一反常现象可能是由于后续酸洗去除镍颗粒时引入了新的含氧官能团。综上,3种还原方式中镍催化的二级氢溢流能够最大程度降低多孔炭表面的含氧官能团,且对C—O和C=O的脱除效果最好。而3种还原方式脱除含氧官能团的作用机理需要进一步的探讨。
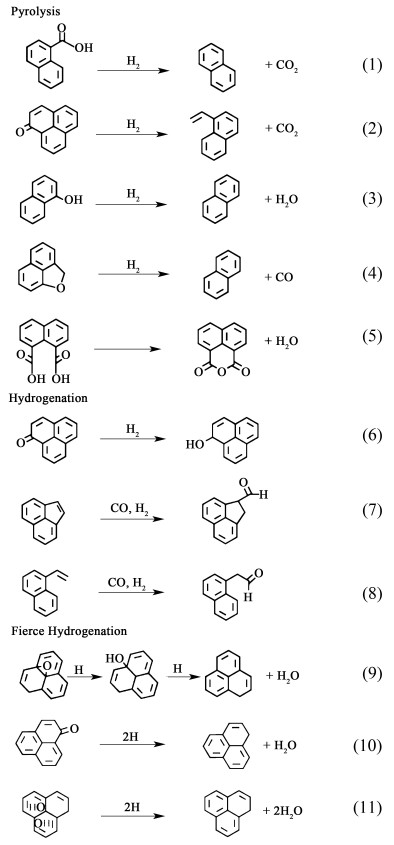
不同还原方式(热还原、一级氢溢流和二级氢溢流)脱除多孔炭表面含氧官能团的作用机制不同。热还原(H2气氛)主要是通过高温下的热解反应和加氢反应脱除多孔炭表面含氧官能团的[图 4,公式1)~公式(8)][16, 18, 28]。在655 ℃时,热稳定性差的COOH热解成CO2气体,而较为稳定的C=O则与氢气分子发生加氢反应,转变为CO气体脱除或加氢转化为C—OH[28]。而C—O基团则是通过氢气的高温还原作用以CO的形式从多孔炭表面脱除。
氢溢流脱氧过程与热还原脱氧过程不同。其脱氧过程主要包括解热反应、加氢反应以及氢溢流产生的高活性氢原子参与的剧烈加氢反应[图 4,公式(1)~公式(11)][16, 28, 29]。和热还原(H2)对比,二级氢溢流对C=O和COOH脱除的优势不太明显,证明了表面C=O和COOH的脱除受温度影响更大,而对还原介质(氢气分子或氢原子)不敏感。
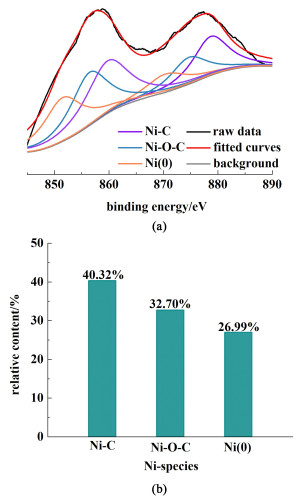
然而,二级氢溢流对C—O的脱除效果最佳,所得PC-Ni-655中C—O最低(摩尔分数82%),表明C—O的脱除受还原介质的影响较大。高活性的氢原子扩散到PC表面的C—O基团处,随后发生剧烈的加氢反应,即C—O基团和2个氢原子连续加氢从而得到H2O和无缺陷的碳平面。一级氢溢流脱氧过程同样包括解热反应、加氢反应以及氢溢流产生的高活性氢原子参与的剧烈加氢反应,但一级氢溢流对含氧基团的脱除效果不佳。这是因为单质镍能稳定碳结构,后续酸洗去除单质镍的同时会引入新的含氧官能团。酸洗前,PC@Ni-655样品中表面的镍主要以Ni—C、Ni—O—C和Ni(0)的形式存在,3者摩尔分数分别为40.32%、32.70%和26.99%[图 5 (a)~图 5(b)]。Ni—C和Ni—O—C表明镍纳米颗粒和多孔炭之间存在强化学相互作用,而单质镍具有稳定碳结构的作用[30],因此后续酸洗过程中部分含氧官能团难以脱除。此外酸洗过程会额外引入新的含氧官能团,所以一级氢溢流脱氧作用有限。
|
| 图 5 (a) PC@Ni-655样品的Ni 2p XPS图谱和(b) 含镍物种的相对含量 Fig.5 (a) XPS spectra (Ni 2p) of the PC@Ni-655 sample and (b) the relative contents of Ni-species |
| |
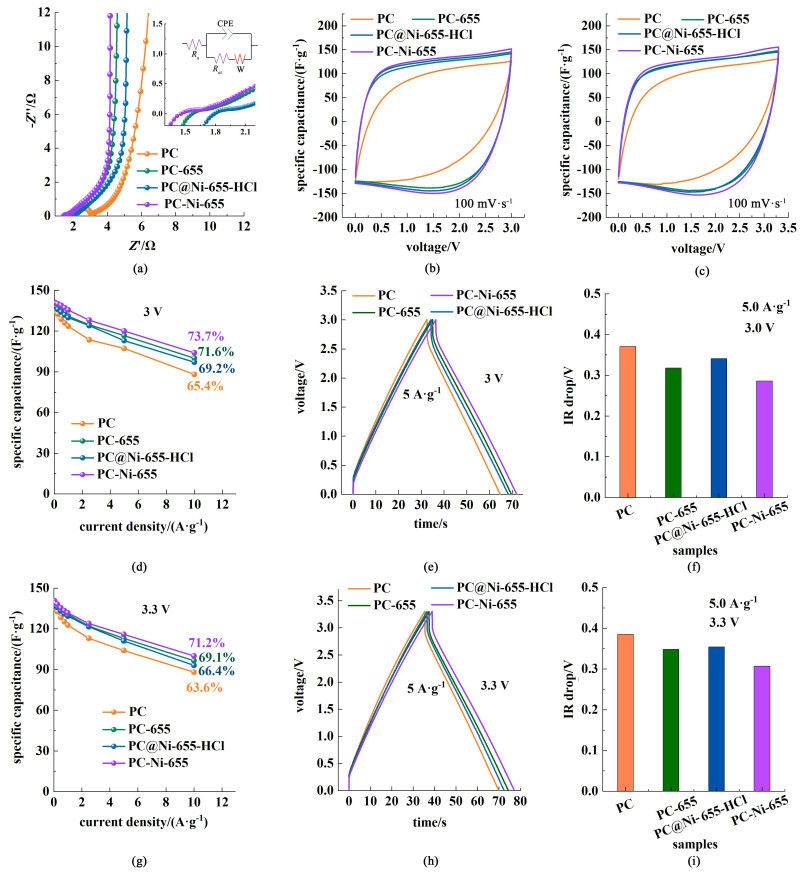
当PC、PC-655、PC@Ni-655-HCl和PC-Ni-655 4种样品分别作为电极材料组装成EDLCs时,表现出不同的电荷转移和离子扩散特性。热还原、一级氢溢流和二级氢溢流脱氧后得到的多孔炭表面含氧官能团含量降低,石墨微晶结构变得更加有序。因此,相比于PC样品较高的等效串联电阻Rs(2.26 Ω),PC-655(1.47 Ω)、PC@Ni-655-HCl(1.71 Ω)和PC-Ni-655(1.38 Ω)表现出更小的等效串联电阻Rs[图 6 (a)和表 3],此外,石墨微晶有序度提升和含氧官能团的脱除既有利于电子在多孔炭颗粒之间的转移。因此相较于PC样品较大的电荷转移电阻Rct(0.77 Ω),PC-655、PC@Ni-655-HCl和PC-Ni-655的电荷转移电阻Rct明显减小,分别为0.26、0.32和0.25 Ω。经热还原、一级氢溢流和二级氢溢流还原后,所得的多孔炭微孔孔径略微变大,因此电解质离子在还原后的3种样品(PC-655、PC@Ni-655-HCl和PC-Ni-655)的孔道中扩散特性有所提高,3种样品的瓦尔堡阻抗RW也均有所减小。二级氢溢流脱氧得到的PC-Ni-655表现出最小的电子转移和离子扩散电阻,更有利于双电层电容储能特性的提升。
|
| 图 6 (a) PC、PC-655、PC@Ni-655-HCl和PC-Ni-655在1 mol·L TEABF4/PC有机系电解液中的Nyquist曲线(插图是高频区数据);PC,PC-655,PC@Ni-655-HCl和PC-Ni-655在3.0 V区间下的(b) CV图、(d) 倍率曲线、(e) 恒流充放电曲线和(f) IR降;PC,PC-655,PC@Ni-655-HCl和PC-Ni-655在3.3 V区间下的(c) CV图、(g) 倍率曲线、(h) 恒流充放电曲线和(i) IR降 Fig.6 (a) Nyquist plots (Inset presents the data at high frequency) of PC, PC-655, PC@Ni-655 and PC-Ni-655 in 1 mol·L TEABF4/PC electrolyte. (b) CV curves, (d) rate performance, (e) galvanostatic charge-discharge curves and (f) IR drop curves of PC, PC-655, PC@Ni-655-HCl and PC-Ni-655 within 3.0 V. (c) CV curves, (g) rate performance, (h) galvanostatic charge-discharge curves and (i) IR drop curves of PC, PC-655, PC@Ni-655-HCl and PC-Ni-655 within 3.3 V |
| |
| 样品 | 等效串联电阻Rs/Ω | 电荷转移电阻Rct/Ω | 瓦尔堡阻抗RW/Ω |
| PC | 2.26 | 0.77 | 8.8 |
| PC-655 | 1.47 | 0.26 | 8.2 |
| PC@Ni-655-HCl | 1.71 | 0.32 | 8.2 |
| PC-Ni-655 | 1.38 | 0.25 | 8.0 |
多孔炭脱氧前后表现出不同的双电层储能特性。当电压窗口为0~3.0 V时,PC样品在100 mV· s-1扫速下的CV曲线严重偏离矩形且比容量低,而PC-655、PC@Ni-655-HCl和PC-Ni-655样品仍保持着良好的矩形形状[图 6 (b)]。这是由于脱氧处理增大了多孔炭的微孔孔径,扩宽了孔道结构的同时提高了碳层结构的有序度,因而电解质离子能够快速进入电极材料的内部孔道,多孔炭电极的活性比表面积得到有效利用。然而二级氢溢流还原后PC-Ni-655样品含氧基团含量最低,有效避免了含氧基团和电解液之间的副反应,因此表现出最低的IR降[0.286 V,图 6(e)~图 6(f)]和提升的倍率性能[10 A·g-1下电容保持率高达73.7%,图 6 (d)]。当电压窗口为3.0 V,电流密度分别为0.05、0.1、0.25、0.5、0.75、1.0、2.5、5.0、10.0 A·g-1时,原料PC的比电容分别为134.8、133.0、132.4、128.8、125.9、123.6、113.6、107.2、88.1 F·g-1。经过热还原后,PC-655在不同电流密度下的比电容为139.8、138.6、137.4、135.0、132.2、131.0、124.7、116.7、100.0 F·g-1。而经过一级氢溢流和二级氢溢流还原后,PC@Ni-655-HCl在不同电流密度下的比电容为140.2、137.9、136.0、134.0、131.8、130.0、124.1、113.2、97.0 F g-1,而PC-Ni-655在不同电流密度下的比电容为141.0、140.5、140.0、139.0、137.2、135.6、128.0、120.0、104.0 F·g-1。然而,当电压窗口提升为3.3 V时,原料PC在0.05、0.1、0.25、0.5、0.75、1.0、2.5、5.0、10.0 A·g-1不同电流密度下的比电容分别为137.7、135.1、132.6、128.4、125.2、122.7、113.0、104.0、88.0 F·g-1。经过热还原后,PC-655在不同电流密度下的比电容为139.7、137.2、136.4、134.3、132.4、130.7、122.0、113.0、96.4 F·g-1。而经过一级氢溢流和二级氢溢流还原后,PC@Ni-655-HCl在不同电流密度下的比电容为140.0、136.7、135.8、133.2、131.0、129.3、121.5、111.0、93.0 F·g-1,而PC-Ni-655在不同电流密度下的比电容为140.5、139.0、138.1、135.4、133.4、131.7、123.9、116.0、100.0 F·g-1。可以看出,在高电压窗口下PC-Ni-655样品仍表现出最小的IR降[0.307 V,图 6 (g)~图 6(i)]和良好的倍率性能[10 A·g-1下电容保持率高达71.2%,图 6(g)]。因此,二级氢溢流有效脱除多孔炭的含氧基团,提高了多孔炭石墨微晶的有序度,保留了多孔炭的层次孔结构,使得PC-Ni-655表现出更好的双电层储能特性。
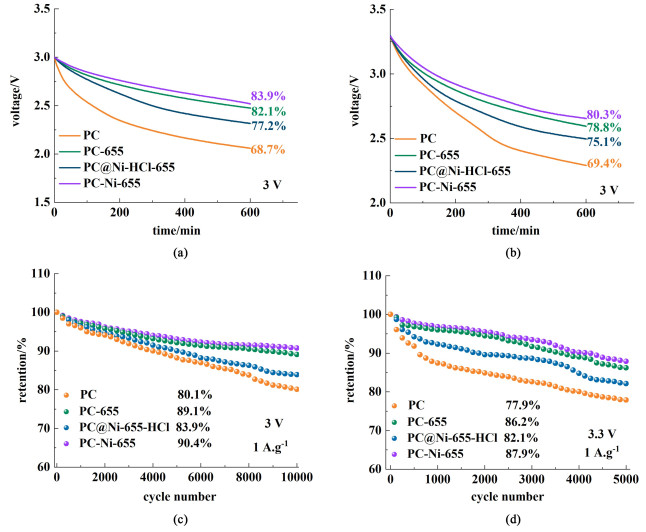
此外,二级氢溢流有效脱除了多孔炭的含氧官能团,能够影响EDLCs的自放电现象和长周期循环稳定性。经过10 h的自放电测试,PC、PC-655、PC@Ni-655-HCl和PC-Ni-655的电压保持率分别是68.7%、82.1%、77.2%和83.9%[图 7 (a)]。特别是当电压升高到3.3 V时,PC-Ni-655经过10 h的自放电测试后,其电压保持率仍高达80.3%[图 7 (b)]。高的电压保持率证明镍催化的二级氢溢流有效降低了PC-Ni-655含氧官能团的含量,减少了高压条件下含氧基团和电解液之间的副反应,从而减缓了自放电现象。此外,PC、PC-655、PC@Ni-655-HCl和PC-Ni-655的循环稳定性和自放电结果一致。PC-Ni-655表现出最好的循环稳定性,在3.0 V电压窗口下循环10 000圈后容量保持率高达90.4%,而在3.3 V电压窗口下循环5 000圈后容量保持率高达87.9%[图 7 (c)~图 7(d)]。长周期循环后高的容量保持率进一步证明了二级氢溢流有效脱除多孔炭表面C—O、C=O和COOH基团,从而兼顾了高比容量和长循环稳定性。
|
| 图 7 PC、PC-655、PC@Ni-655-HCl和PC-Ni-655在不同电压窗口下的(a)~(b)自放电曲线和(c)~(d) 循环性能 Fig.7 (a), (b) The self-discharge curve and (c), (d) cycling performance of sample PC, PC-655, PC@Ni-655-HCl and PC-Ni-655 |
| |
利用镍基催化剂表面的氢溢流现象,在655 ℃下脱除了多孔炭材料表面的含氧基团。对比传统热还原法(H2气氛)的脱氧过程,基于氢溢流现象的多孔炭脱氧过程除了热解反应和加氢反应,还包括高活性氢原子参与的剧烈的加氢反应。而基于一级氢溢流和二级氢溢流现象的脱氧过程不同。由于单质镍与多孔炭之间存在Ni—C和Ni—O—C等化学键合作用,因此一级氢溢流脱氧效果有限。而二级氢溢流避免了Ni—C和Ni—O—C等化学键的形成,厘米级别下可迁移的高活性氢原子可以更有效脱除多孔炭材料的含氧基团,所得的PC-Ni-655表面含氧量低至摩尔分数3.4%。此外,二级氢溢流脱氧后得到的多孔炭PC-Ni-655的石墨微晶有序度提高,微孔孔径略微变宽。因此,以PC-Ni-655作为电极材料组装EDLCs,能够有效减少含氧官能团和电解液之间的副反应,避免严重自放电现象的发生,在3.3 V电压下仍表现出良好的倍率性能和循环稳定性(循环5 000圈容量保持率高达87.9%)。
| [1] |
CHMIOLA J, YUSHIN G, GOGOTSI Y, et al. Anomalous increase in carbon capacitance at pore sizes less than 1 nanometer[J]. Science, 2006, 313(5794): 1760-1763. DOI:10.1126/science.1132195 |
| [2] |
SIMON P, GOGOTSI Y. Materials for electrochemical capacitors[J]. Nature Materials, 2008, 7(11): 845-854. DOI:10.1038/nmat2297 |
| [3] |
TRAN C, KALRA V. Fabrication of porous carbon nanofibers with adjustable pore sizes as electrodes for supercapacitors[J]. Journal of Power Sources, 2013, 235: 289-296. DOI:10.1016/j.jpowsour.2013.01.080 |
| [4] |
GANDLA D, WU X, ZHANG F, et al. High-performance and high-voltage supercapacitors based on N-doped mesoporous activated carbon derived from dragon fruit peels[J]. ACS Omega, 2021, 6(11): 7615-7625. DOI:10.1021/acsomega.0c06171 |
| [5] |
CHANG P, YANG F, CEN Y, et al. Hierarchical nanoporous C/C composite from humic fulvic acid and sulfonated pitch for high-energy-density EDLC electrodes[J]. ChemNanoMat, 2021, 7(10): 1131-1137. DOI:10.1002/cnma.202100217 |
| [6] |
李艳梅, 郝国栋, 崔平, 等. 超级电容器电极材料研究进展[J]. 化学工业与工程, 2020, 37(1): 17-33. LI Yanmei, HAO Guodong, CUI Ping, et al. Research progress of electrode material for supercapacitor[J]. Chemical Industry and Engineering, 2020, 37(1): 17-33. DOI:10.3969/j.issn.1006-7906.2020.01.004 (in Chinese) |
| [7] |
李超, 那伟, 张磊. 铁基二元金属氧化物超级电容器电极的研究[J]. 化学工业与工程, 2021, 38(2): 69-80. LI Chao, NA Wei, ZHANG Lei. Research progress on iron-based bimetal oxide as supercapacitor electrode[J]. Chemical Industry and Engineering, 2021, 38(2): 69-80. DOI:10.3969/j.issn.1006-7906.2021.02.015 (in Chinese) |
| [8] |
BÉGUIN F, PRESSER V, BALDUCCI A, et al. Carbons and electrolytes for advanced supercapacitors[J]. Advanced Materials (Deerfield Beach, Fla), 2014, 26(14): 2219-2251, 2283. DOI:10.1002/adma.201304137 |
| [9] |
LIU K, YANG T, ZHENG X, et al. Potassium-assisted carbonization of chlorobenzene in Ar/H2 to prepare porous carbon with low oxygen content for high withstanding voltage EDLCs[J]. Carbon, 2021, 172: 154-161. DOI:10.1016/j.carbon.2020.09.091 |
| [10] |
CHANG P, WANG C, KINUMOTO T, et al. Frame-filling C/C composite for high-performance EDLCs with high withstanding voltage[J]. Carbon, 2018, 131: 184-192. DOI:10.1016/j.carbon.2018.02.022 |
| [11] |
ISHIMOTO S, ASAKAWA Y, SHINYA M, et al. Degradation responses of activated-carbon-based EDLCs for higher voltage operation and their factors[J]. Journal of The Electrochemical Society, 2009, 156(7): A563-A567. DOI:10.1149/1.3126423 |
| [12] |
IZADI-NAJAFABADI A, YASUDA S, KOBASHI K, et al. Extracting the full potential of single-walled carbon nanotubes as durable supercapacitor electrodes operable at 4 V with high power and energy density[J]. Advanced Materials (Deerfield Beach, Fla), 2010, 22(35): E235-E241. DOI:10.1002/adma.200904349 |
| [13] |
NAOI K, ISHIMOTO S, MIYAMOTO J I, et al. Second generation 'nanohybrid supercapacitor': Evolution of capacitive energy storage devices[J]. Energy & Environmental Science, 2012, 5(11): 9363-9373. |
| [14] |
SHAFEEYAN M S, DAUD W M A W, HOUSHMAND A, et al. A review on surface modification of activated carbon for carbon dioxide adsorption[J]. Journal of Analytical and Applied Pyrolysis, 2010, 89(2): 143-151. DOI:10.1016/j.jaap.2010.07.006 |
| [15] |
PEI S, ZHAO J, DU J, et al. Direct reduction of graphene oxide films into highly conductive and flexible graphene films by hydrohalic acids[J]. Carbon, 2010, 48(15): 4466-4474. DOI:10.1016/j.carbon.2010.08.006 |
| [16] |
PHAM V H, PHAM H D, DANG T, et al. Chemical reduction of an aqueous suspension of graphene oxide by nascent hydrogen[J]. Journal of Materials Chemistry, 2012, 22(21): 10530-10536. DOI:10.1039/c2jm30562c |
| [17] |
LAVIN-LOPEZ M P, PATON-CARRERO A, SANCHEZ-SILVA L, et al. Influence of the reduction strategy in the synthesis of reduced graphene oxide[J]. Advanced Powder Technology, 2017, 28(12): 3195-3203. DOI:10.1016/j.apt.2017.09.032 |
| [18] |
QIN T, SHI Z, LI M, et al. Effect of reduction heat treatment in H2 atmosphere on structure and electrochemical properties of activated carbon[J]. Journal of Solid State Electrochemistry, 2015, 19(5): 1437-1446. DOI:10.1007/s10008-015-2767-1 |
| [19] |
BAUMGARTEN E, MASCHKE L. Hydrogen spillover through the gas phase[J]. Applied Catalysis A: General, 2000, 202(2): 171-177. DOI:10.1016/S0926-860X(00)00523-8 |
| [20] |
BADUN G A, JOHNSON B F G, SHCHEPINA N E. Long distance hydrogen spillover found by a radioactive assay for the Ru5Pt/MCM-41 catalytic system[J]. Mendeleev Communications, 2009, 19(4): 235-236. DOI:10.1016/j.mencom.2009.07.022 |
| [21] |
PSOFOGIANNAKIS G M, FROUDAKIS G E. DFT study of hydrogen storage by spillover on graphite with oxygen surface groups[J]. Journal of the American Chemical Society, 2009, 131(42): 15133-15135. DOI:10.1021/ja906159p |
| [22] |
PSOFOGIANNAKIS G M, FROUDAKIS G E. Fundamental studies and perceptions on the spillover mechanism for hydrogen storage[J]. Chemical Communications, 2011, 47(28): 7933-7943. DOI:10.1039/c1cc11389e |
| [23] |
RAZZHIVINA I A, BADUN G A, CHERNYSHEVA M G, et al. Hydrogen spillover through a gas phase[J]. Mendeleev Communications, 2016, 26(1): 59-60. DOI:10.1016/j.mencom.2016.01.023 |
| [24] |
NISHIHARA H, SIMURA T, KYOTANI T. Enhanced hydrogen spillover to fullerene at ambient temperature[J]. Chemical Communications, 2018, 54(27): 3327-3330. DOI:10.1039/C8CC00265G |
| [25] |
LIU K, JIAO M, CHANG P, et al. Pitch-based porous aerogel composed of carbon onion nanospheres for electric double layer capacitors[J]. Carbon, 2018, 137: 304-312. DOI:10.1016/j.carbon.2018.05.038 |
| [26] |
MARTA S, PATRICIA V, ANTONIO F. N-doped polypyrrole-based porous carbons for CO2 capture[J]. Advanced Functional Materials, 2011, 21: 2781-2787. DOI:10.1002/adfm.201100291 |
| [27] |
LOZANO-CASTELLÓ D, LILLO-RÓDENAS M A, CAZORLA-AMORÓS D, et al. Preparation of activated carbons from Spanish anthracite[J]. Carbon, 2001, 39(5): 741-749. DOI:10.1016/S0008-6223(00)00185-8 |
| [28] |
YUAN S, HUANG X, WANG H, et al. Structure evolution of oxygen removal from porous carbon for optimizing supercapacitor performance[J]. Journal of Energy Chemistry, 2020, 51: 396-404. DOI:10.1016/j.jechem.2020.04.004 |
| [29] |
PHAM V H, DANG T, SINGH K, et al. A catalytic and efficient route for reduction of graphene oxide by hydrogen spillover[J]. Journal of Materials Chemistry A, 2013, 1(4): 1070-1077. DOI:10.1039/C2TA00249C |
| [30] |
ZHOU C, SZPUNAR J A, CUI X. Synthesis of Ni/graphene nanocomposite for hydrogen storage[J]. ACS Applied Materials & Interfaces, 2016, 8(24): 15232-15241. |
 2022, Vol. 39
2022, Vol. 39