2. 湖南师范大学化学与化工学院, 长沙 410081
2. College of Chemistry and Chemical Engineering, Hunan Normal University, Changsha 410081, China
锂离子电池(LIBs)最初是为便携式电子产品进行商业开发的,使其应用于电动汽车、手机和电脑等设备产品,以满足人类对可持续能源和美好生活的需求[1-3]。目前在商业化LIBs市场中,石墨以其丰富的储量和优异的电化学性能占据主导地位[4, 5]。整个行业对LIBs的需求不断增加,估计到2030年将产生超过1 100万t的废旧LIBs,这将会导致大量电池陷入报废、回收再利用的问题[6, 7]。石墨材料占电池重量的12%~21%,并在各种储能应用中需要石墨作为电极,在全球范围内已消耗超过8亿t可回收石墨,为了环境保护和资源可持续性,迫切需要有效回收废旧石墨(SG)[8-10]。
目前,废旧LIBs的回收主要集中在Co、Ni、Li和Al等有价金属的回收,而对电池中石墨的回收研究有限[11-13]。因此需要对大量的废旧石墨(SG)进行回收及修复再生,才能让它像Li和Co一样成为“未来的关键材料”[14, 15]。石墨材料中Ni、Pb和Zn等有害金属含量低于0.01%,Fe、Al和Cu的含量约0.5%以及大约4%的Li[16]。因为在LIBs的使用过程中,石墨体积会发生变化,石墨表面和层间会残留部分黏合剂、导电剂和其他金属沉积物,这将导致石墨结构缺陷[17, 18]。SG作为LIBs负极的回收再利用,不仅可以降低原料成本,为新材料的合成带来更高的经济效益,而且可以实现废旧电池材料的回收利用,实现可持续发展的目标[19-21]。
目前,SG的回收利用主要有2种主要方法。第1个方法是将其转化为其他功能材料。例如,SG可以转化为吸附材料[22, 23]、电芬顿正极材料[24, 25]、石墨烯材料[26, 27]以及形成双离子电池(DIBs)独特的阴极材料[28, 29],这些回收方法对未来大规模回收废旧LIBs具有深远的意义。第2个回收方法是作为LIBs的再生石墨(RG)。例如,Yu等[30]系统地研究了N2、He和Ar气氛下高温石墨化处理(1 000~3 000 ℃)对石墨晶格重构的影响,最终在N2气氛下将石墨化程度优化到92.03%,RG在1 000次循环后容量保持率为97.3%。Gao等[31]提出了一种通过联合硫酸固化、浸出和1 500 ℃下连续煅烧再生SG的新方法,RG的初始充电容量和保留率分别为349 mAh ·g-1和98.8%。SG也可采用机械处理和湿法冶金等方法提纯回收,例如Yang等[16]和Guo等[32]研究了盐酸和柠檬酸对SG除杂效果的影响,获得的RG具有更好的晶体结构,在0.5 C下循环80次后具有330 mAh ·g-1的高放电容量。Da等[33]和Cheng等[34]提出了使用碱性试剂(KOH)蚀刻的新型深度纯化工艺修复石墨,通过在表面上形成孔来增加充电和放电倍率能力,从而增加锂离子嵌入和脱嵌的位点,RG优异的充放电倍率性能和循环性能为我们展示了一条回收SG的新思路。上述研究主要集中于通过不同手段对SG的电化学性能进行提升,而且大多是在高温和高浓度酸碱试剂以及复杂工艺下对SG进行处理。此外,针对SG中不同金属杂质的不同浸出工艺很少有详细报道,所以有必要探究一种SG中不同杂质金属的不同去除方法,并且回收过程需要低能耗和低酸碱试剂消耗,为SG的回收提供一种新方法。
目前的研究主要集中在不同金属杂质的浸出工艺和电化学性能的提升方面。首先通过水热法高效浸出Cu和Li,以及低浓度的盐酸浸出剩余的Co、Mn和Ni,在此过程中研究不同反应条件对不同金属元素的浸出率的影响,确保能够纯化SG。然后在不同条件下煅烧SG,以最大化去除黏结剂等有机成分。最后通过不同表征分析手段对石墨进行分析,制成纽扣电池测试电化学性能。预计这项研究可以阐明SG中不同金属的高效环保的浸出工艺,以实现其有效回收,并可能提供SG的电化学性能提升的新思路。
1 实验方法和材料 1.1 材料和试剂废旧石墨(SG)来源于深圳市沛城电子科技有限公司,具体金属杂质含量见表 1。商品石墨(Commercial Graphite, CG)来源于中国太原力之源科技有限公司,规格为电池级。本研究中使用的所有试剂均为分析纯,无需进一步处理即可直接使用。
| 金属元素 | 质量分数/% |
| Cu | 0.274 3 |
| Li | 0.056 5 |
| Co | 0.060 8 |
| Mn | 0.050 2 |
| Ni | 0.440 0 |
将SG、Na2S2O8和去离子水依次加入反应釜中,放在恒温干燥箱中加热,探究温度(80~160 ℃)、时间(10~50 min)、固液比(1:20~1:60 g·mL-1)、Na2S2O8和SG的质量比(0.2~0.6 g·g-1)对Cu的浸出率的影响。
1.2.2 剩余Li进行浸出将SG和去离子水依次加入反应釜中,放在恒温干燥箱中加热,探究温度(160~240 ℃)、时间(1~5 h)和固液比(1 : 10~1 : 50 g ·mL-1)对Li的浸出率的影响。
1.2.3 剩余Ni、Co和Mn的浸出将加入SG和HCl的磨口锥形瓶放入恒温加热磁力搅拌器中,探究温度(60~100 ℃)、时间(30~70 min)、固液比(1 : 10~1 : 50 g ·mL-1)和盐酸浓度(0~0.8 mol ·L-1)对Ni、Co和Mn的浸出率的影响。
1.2.4 煅烧过程对浸出后的石墨在不同温度和时间下进行煅烧以去除石墨表面的黏结剂和电解液,确定最适宜煅烧条件后的石墨为再生石墨(RG)。
1.3 分析方法石墨中的杂质金属浓度通过电感耦合等离子体发射光谱仪(ICP-OES,iCAP6300 Duo,England)进行定量分析。通过X射线衍射仪[XRD,Bruker D8 Advance,使用Cu_Kα λ=1.5406 Å,扫描速率2(°) ·min-1,2θ范围为10°~80°]对晶体结构进行分析。采用扫描电子显微镜(SEM,Tescan Mira Lms,Czech)分析石墨表面形貌。石墨中金属杂质浸出率(L)通过式(1)进行计算。
| $ L=\frac{c V}{m w} \times 100 \% $ | (1) |
式(1)中:c为被测元素在浸出液中的质量浓度,g ·L-1;V为浸出液的总体积,L;m为加入浸出液中的废旧石墨的质量,g;w为被测元素的质量分数,%。
1.4 电化学测试石墨电极由溶解在NMP中的石墨(80%)、乙炔黑(10%)和PVDF黏合剂(10%)制成。将获得的均匀浆料用刮刀涂布在铜箔上,然后在烘箱中在120 ℃下干燥12 h以去除残留的NMP,使用冲床压制、切割并称质量。在氩气气氛(H2O体积分数 < 1×10-8,O2体积分数 < 1×10-8)的手套箱中,使用CR2025型电池壳组装纽扣型电池,使用聚丙烯多孔膜作为隔膜,使用体积比为1 : 1 : 1,1.0 mol ·L-1的LIPF6-EC/DEC/EMC有机混合液作为电解液,将制备好的石墨材料电极片置于正极壳内。将高纯锂片(≥99.9%)置在负极壳中作为对电极。最后,组装电池应使用电池封口机进行密封,静置24 h后,以不同比例测试不同种类石墨的电化学性能。使用多通道电池测试仪(NEWARE CT-3008)在0.1 C下从0.005~2.000 V的电压范围内进行恒流充放电循环测试。在0.5 C下进行循环性能测试,在0.1~2.0 C(1 C=372 mAh ·g-1)的选定速率下进行倍率性能测试。
2 废旧石墨的除杂过程 2.1 Cu的浸出过程水热法是利用高温高压的水溶液使那些不溶或难溶的物质溶解,或反应生成该物质的溶解产物,使用亚临界水回收有价金属被认为是一种简单、廉价、安全和环保的技术[35, 36]。由于Na2S2O8对Cu有很好的氧化作用[37, 38],所以本研究使用Na2S2O8在水热条件下对废旧石墨(SG)中的Cu进行高效浸出,探究该方法在SG回收领域的应用,具体反应过程见方程式(2)。
| $ \mathrm{Na}_2 \mathrm{~S}_2 \mathrm{O}_8+\mathrm{Cu} \rightarrow \mathrm{Na}_2 \mathrm{SO}_4+\mathrm{CuSO}_4 $ | (2) |
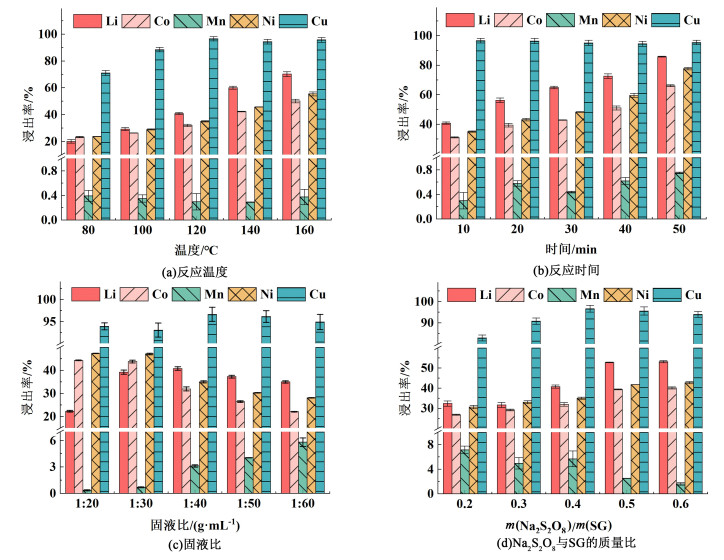
在80~160 ℃的温度范围内,研究了反应温度对Cu的浸出率的影响。在浸出过程中,时间保持10 min、固液比保持1 : 40 g ·mL-1以及Na2S2O8和SG的质量比保持0.4 g ·g-1。图 1(a)表明温度的变化对浸出过程有显著影响,随着温度从80 ℃升高到120 ℃,Cu的浸出率从71.02%增加到96.61%,说明温度可以极大地促进Cu的氧化,证实了该方法在石墨回收领域的可行性。随着反应温度升高至160 ℃,浸出率保持平稳,为95.75%。几乎所有的Cu都在120 ℃时浸出。对这种现象的合理解释是用于浸出Cu的Na2S2O8的电离反应是吸热反应,而且浸出反应也是吸热反应。因此温度的升高,可以加快反应速度。为降低Na2S2O8的消耗且保证Cu的高效浸出,选择120 ℃作为适宜的温度浸出Cu。
|
| 图 1 不同反应条件对Cu、Li、Co、Mn和Ni的浸出率的影响 Fig.1 Effect of different reaction conditions on the leaching efficiency of Cu, Li, Co, Mn and Ni |
| |
在10~50 min的时间范围内,研究了反应时间对Cu的浸出率的影响。在浸出过程中,温度保持120 ℃、固液比保持1 : 40 g ·mL-1以及Na2S2O8和SG的质量比保持0.4 g ·g-1。从图 1(b)可以看出时间的变化对浸出过程的影响很小,在10 min的时候,浸出率保持在96.61%,说明水热法对铜的浸出有很强的促进作用。当浸出时间增加到50 min时,浸出率的变化保持平稳,为95.42%。因此,选择10 min作为适宜的时间浸出Cu。
在1 : 20 g ·mL-1至1 : 60 g ·mL-1的固液比范围内,研究了固液比对Cu的浸出率的影响。在浸出过程中,温度保持120 ℃、时间保持10 min以及Na2S2O8和SG的质量比保持0.4 g ·g-1。从图 1(c)中可以看出固液比对浸出过程的影响很小,当固液比从1 : 20 g ·mL-1降低到1 : 40 g ·mL-1时,浸出率从93.90%增加到96.61%。当固液比降低至1 : 60 g ·mL-1时,浸出率基本不变,为94.87%。固液比的降低促进了溶液中离子的扩散以及降低了固液之间的黏度,从而提高了浸出率。而此后随着固液比的进一步降低,扩散速度和黏度的影响越来越弱,浸出效率没有明显变化。考虑到较低的去离子水消耗和较高的浸出率,选择1 : 40 g ·mL-1作为适宜的固液比浸出Cu。
在0.2~0.6 g ·g-1的质量比范围内,研究了Na2S2O8和SG的质量比对浸出率的影响。在浸出过程中,温度保持120 ℃、时间保持10 min以及固液比保持1 : 40 g ·mL-1。从图 1(d)中可以看出质量比对浸出率的影响较大,随着质量比从0.2增加到0.4 g ·g-1时,浸出率从82.88%增加到96.61%,说明较多的Na2S2O8能够更好地促进Cu的氧化,从而更好地纯化石墨。当质量比增加到0.6 g ·g-1时,浸出率略有下降,为93.95%。考虑到较低的化学品消耗和相对较高的效率,选择0.4 g ·g-1作为适宜的质量比浸出Cu。
综上所述,选择温度保持120 ℃、时间保持10 min、固液比保持1 : 40 g ·mL-1以及Na2S2O8和SG的质量比保持0.4 g ·g-1作为Cu的适宜的浸出条件,浸出率为96.61%。在此条件下,40.76%的Li、31.95%的Co、0.29%的Mn和35.02%的Ni也同时被浸出。
2.2 剩余Li的浸出过程SG的锂主要来源是存在于其表面并插入其孔中的SEI膜,其由Li2CO3、LiF、Li2O、ROCO2Li、ROLi和(ROCO2Li)2等组成[39, 40]。在电池的充电和放电循环期间,SEI膜中锂离子的扩散减慢,导致Li在石墨表面沉淀[41, 42]。此外,部分Li在电池的充电过程中,会扩散入石墨负极的晶格中。SG中Li与水发生水解和浸出反应,可以用如下反应式表示[32, 43]。
| $ \mathrm{Li}_2 \mathrm{O}+\mathrm{H}_2 \mathrm{O} \rightarrow 2 \mathrm{LiOH} $ | (3) |
| $ \mathrm{CH}_3 \mathrm{OLi}+\mathrm{H}_2 \mathrm{O} \rightarrow \mathrm{LiOH}+\mathrm{CH}_3 \mathrm{OH} $ | (4) |
| $ \mathrm{ROCO}_2 \mathrm{Li}+\mathrm{H}_2 \mathrm{O} \rightarrow \mathrm{LiOH}+\mathrm{ROCOOH} $ | (5) |
| $ 2 \mathrm{Li}+2 \mathrm{H}_2 \mathrm{O} \rightarrow 2 \mathrm{LiOH}+\mathrm{H}_2 $ | (6) |
| $ \mathrm{LiF}+\mathrm{H}_2 \mathrm{O} \rightarrow \mathrm{LiOH}+\mathrm{HF} $ | (7) |
| $ \mathrm{Li}_2 \mathrm{CO}_3+\mathrm{H}_2 \mathrm{O} \rightarrow 2 \mathrm{LiOH}+\mathrm{H}_2 \mathrm{CO}_3 $ | (8) |
| $ \mathrm{LiPF}_6+\mathrm{H}_2 \mathrm{O} \rightarrow \mathrm{LiF}+\mathrm{POF}_3+2 \mathrm{HF} $ | (9) |
对除铜后的SG进行Li的浸出,在160~240 ℃的温度范围内,研究了反应温度对Li的浸出率的影响,结果见图 2。
|
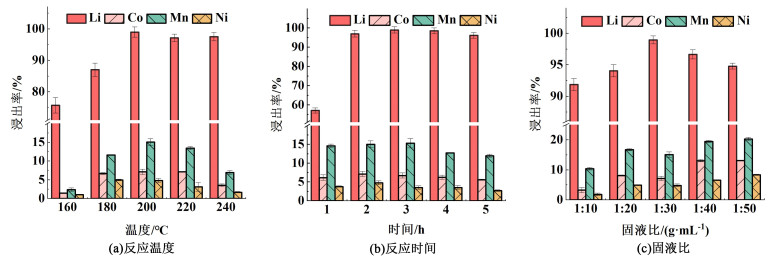
| 图 2 不同反应条件对剩余的Li、Co、Mn和Ni的浸出率 Fig.2 Effect of different reaction conditions on the leaching efficiency of residual Li, Co, Mn and Ni |
| |
在浸出过程中,时间保持3 h以及固液比保持1 : 30 g ·mL-1。图 2(a)显示了温度对浸出过程有显着影响,随着温度从160升高到200 ℃,Li的浸出率从75.69%增加到98.94%。石墨中几乎所有的Li都在200 ℃浸出。这说明在高温条件下,亚临界水可以破坏SEI膜、SG表面和层间结构,使Li被浸出。随着反应温度升高至240 ℃,浸出率保持平稳,为97.12%。综合以上情况,为减少能耗,选择200 ℃作为适宜的温度浸出Li。
在1~5 h的时间范围内,研究了反应时间对Li的浸出率的影响。在浸出过程中,温度保持200 ℃以及固液比保持1 : 30 g ·mL-1。图 2(b)显示了反应时间对浸出过程有显著影响,随着时间从1 h延长至3 h后,Li的浸出率从57.14%增加到98.94%,说明反应时间的延长对Li的浸出有很强的促进作用。因为浸锂过程主要分为SEI膜的溶解和石墨孔内Li的化合物的水解。随着反应时间的增加,石墨表面的含锂元素被溶解,SG的层状结构逐渐暴露出来,因此液体可以进入孔隙并与物质发生反应[44]。当浸出时间增加到5 h后,浸出率的变化保持平稳,为96.14%。因此,选择3 h作为适宜的时间浸出Li。
在1 : 10~1 : 50 g ·mL-1的固液比范围内,研究了固液比对Li的浸出率的影响。在浸出过程中,温度保持200 ℃以及时间保持3 h。从图 2(c)中可以看出固液比对反应过程影响较小,随着固液比从1 : 10降低到1 : 30 g ·mL-1时,浸出率从91.86%增加到98.94%。当固液比降低至1 : 50 g ·mL-1时,浸出率基本不变,为94.78%。固液比的降低使得SG中Li的化合物与去离子水充分反应,从而提高了浸出率。考虑到较低的去离子水消耗和较高的效率,选择1 : 30 g ·mL-1作为适宜的固液比浸出Li。
综上所述,选择温度保持200 ℃,时间保持3 h以及固液比保持1 : 30 g ·mL-1作为剩余的Li的适宜的浸出条件,浸出率为98.94%。在此条件下,有7.11%的Co、15.03%的Mn和4.78%的Ni也同时被浸出。
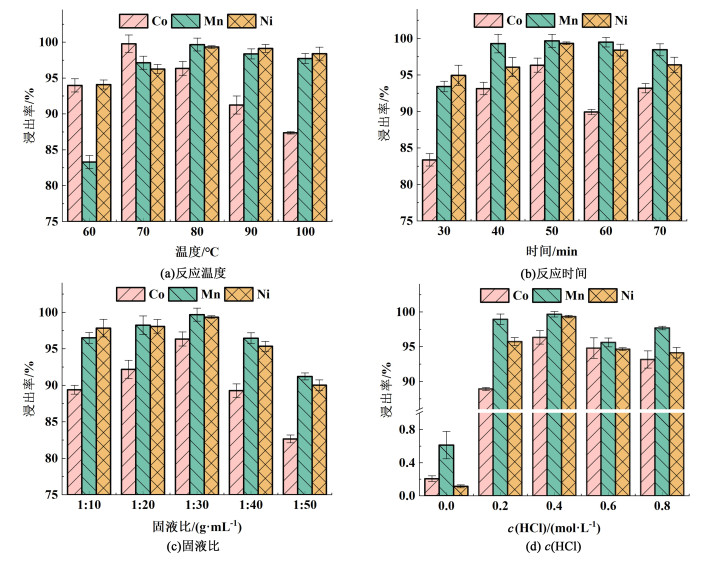
2.3 剩余Ni、Co和Mn的浸出过程在反应温度为60~100 ℃、反应时间为30~70 min、固液比为1 : 10~1 : 50 g ·mL-1和HCl浓度为0~0.8 mol ·L-1的实验条件下,对上述浸出Li后的SG中剩余的Co、Mn和Ni进行浸出。图 3(a)~图 3(d)显示了不同实验条件对剩余的Co、Mn和Ni的浸出率的影响,在考虑高的浸出率,降低能耗和减少试剂消耗的前提下,本研究选择反应温度为80 ℃,反应时间为50 min,固液比为1 : 30 g ·mL-1和HCl浓度为0.4 mol ·L-1为适宜的条件。在此条件下,Co的浸出率为96.34%、Mn的浸出率为99.67%和Ni的浸出率为99.34%。
|
| 图 3 不同反应条件对剩余的Co、Mn和Ni的浸出率的影响 Fig.3 Effect of different reaction conditions on the leaching efficiency of residual Co, Mn and Ni |
| |
将除杂后的石墨放在保持空气氛围的马弗炉里进行煅烧以去除石墨表面残余的黏结剂和电解液等有机杂质。由于石墨在600 ℃下会被氧化,因此本实验选择400~550 ℃的煅烧温度。
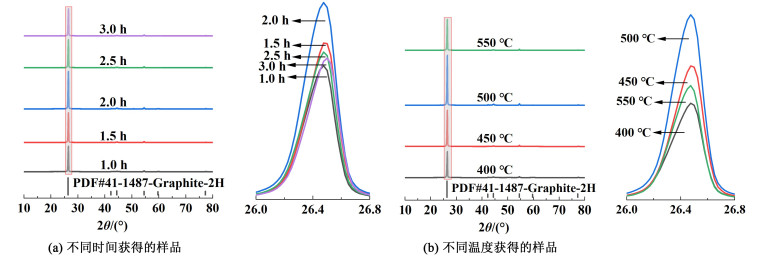
在500 ℃的煅烧温度下对煅烧时间进行探究,图 4(a)显示了煅烧时间为2 h时,石墨的XRD衍射特征峰最强且测试结果显示2θ均为26.474 6°,根据布拉格方程: 2dsinθ=λ,可以确定不同时间下的石墨层间距均为0.336 4 nm。因此综合考虑,煅烧时间选择2 h。在2 h的条件下对煅烧温度进行探究,图 4(b)显示了煅烧温度为500 ℃时,石墨的XRD衍射特征峰最强且计算结果显示不同温度下的石墨层间距均为0.336 4 nm,所以煅烧温度选择500 ℃。因此煅烧的最适宜条件为500 ℃和2 h,煅烧后的石墨称为再生石墨(RG)。
|
| 图 4 废旧石墨在不同时间和温度下的XRD图 Fig.4 XRD patterns of spent graphite at different times and temperatures |
| |
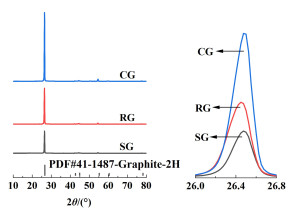
为了探究水热除杂和煅烧过程对石墨晶体结构的影响,本研究对SG、RG和CG 3种石墨进行了XRD表征分析。
图 5显示了不同石墨的XRD图像,它们均在约26°处具有d002的强衍射峰,这表明SG和RG仍保持完整的石墨结构。与SG相比,RG的衍射峰强度有所增加。2θ从SG和CG的26.474 6°移动到RG的26.449 4°,相应的层间距离分别为0.336 4和0.336 7 nm,由布拉格方程确定。这一结果归因于通过水热法和酸浸去除金属化合物以及煅烧去除残留的黏结剂和电解液,从而导致RG表面石墨相含量和层间距离增加。
|
| 图 5 不同石墨的XRD图 Fig.5 XRD images of different graphite |
| |
本研究对SG、RG和CG3种石墨进行了SEM表征测试。图 6显示了SG、RG和CG的SEM图像。

|
| 图 6 SEM图 Fig.6 SEM images |
| |
图 6(a)~图 6 (c)为SG的表面形貌,可以在石墨表面观察到很多的杂质,这些杂质可能来自SEI膜、黏结剂和电解液,所以SG表面不够光滑。图 6(d)~图 6(f)显示了RG的表面形貌,石墨表面的杂质被完全去除,表面变得更光滑,呈现出明显的层状结构,说明水热浸出和高温煅烧对SG的表面形貌有很大的改变。但在石墨表面出现细小的石墨碎片,说明在除杂和煅烧过程中部分石墨产生了破碎[图 6(d)~图 6(e)]。图 6(g)~图 6(h)显示了CG的表面形貌,由于其表面和层间结构中不含有任何杂质且结构未损坏,所以CG的表面十分光滑细腻,层状结构也十分清晰。对于光滑平坦的石墨表面,可以促进电解质和石墨颗粒之间的渗透,这可以提高电化学性能。
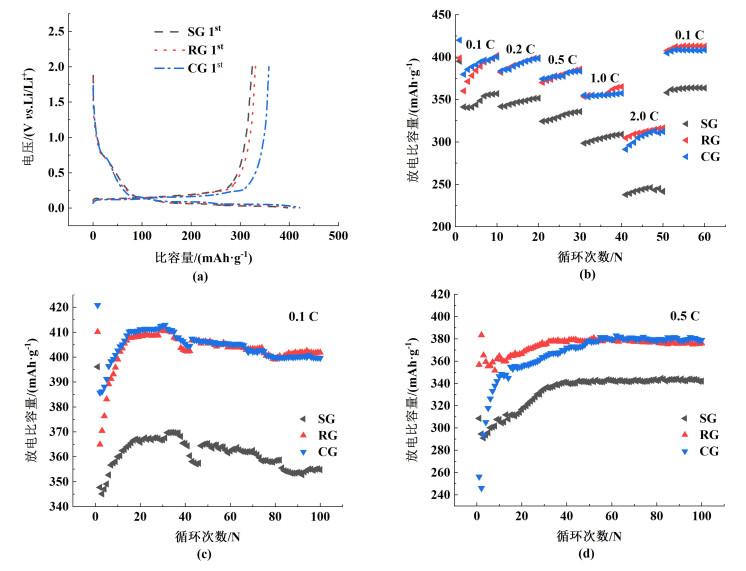
3.3 电化学性能分析不同石墨材料的首次恒电流充放电曲线如图 7(a)所示。SG、RG和CG在第1次循环中的首次放电比容量分别为396.13、410.11和420.86 mAh ·g-1,首次充电比容量分别为324.49、330.85和358.32 mAh ·g-1,初始库伦效率分别为81.91%、80.67%和85.14%。可以看出SG经化学浸出和高温煅烧后,充电和放电比容量都有所提升。但RG的第1次库仑效率低于SG,放电比容量高于SG,说明再生石墨在第1个循环的充放电过程中消耗更多的电解质和锂离子[16],这可能是RG受到石墨表面形貌、粒径大小分布等因素的影响。
|
| 图 7 不同石墨的电化学性能: (a)初始充放电;(b)倍率性能;循环性能: (c)0.1 C;(d)0.5 C Fig.7 Electrochemical properties of different graphite: (a) initial charge/discharge; (b) rate performances; cycling performance: (c) 0.1 C; (d) 0.5 C |
| |
图 7(b)显示了SG、RG和CG在0.1~2.0 C的不同电流速率下10个循环的倍率性能的比较。从图 7(b)中可以看出,随着电流密度的增加,不同样品之间的容量差异变得显著,SG在高速率下均表现出明显的容量衰减。这意味着多余杂质的加入,将严重降低速率能力。RG在不同电流密度下的首次放电比容量分别为398.82、382.01、370.00、353.323和304.66 mAh ·g-1。当电流密度恢复到0.1 C时,RG的放电比容量为407.48 mAh ·g-1,比初始值更高。此外,RG在2.0 C的高电流密度下可以达到高于CG的291.18 mAh ·g-1的放电比容量。这可能是因为锂离子不断嵌入石墨层内致膨胀和变形,随后的锂离子更容易嵌入石墨基体中,使其容量增强。这说明RG具有更加优异的循环稳定性,进一步证实了除杂和煅烧的重要性。
图 7(c)~7(d)显示了SG、RG和CG在0.1 C和0.5 C下的循环性能。在0.1 C下的初始放电比容量分别为396.13、410.11和420.86 mAh ·g-1。100次循环后的放电比容量分别为354.80、401.85和399.69 mAh ·g-1,容量保持率分别为89.57%、97.99%和94.97%。SG、RG和CG在0.5 C下的初始放电比容量分别为308.66、356.67和256.32 mAh ·g-1。100次循环后的放电比容量分别为342.06、376.06和378.97 mAh ·g-1,容量保持率均超过初始值。由于表面上的杂质颗粒,未经处理的SG样品无法形成稳定的SEI层,导致大量不可逆的Li+持续消耗,在不同电流密度下的长期循环过程中表现出相对较差的电化学性能。值得注意的是,RG和CG在0.1 C和0.5 C的电流密度下均表现出良好的循环性能并且RG的循环性能在0.5 C的初始循环下优于CG,循环100次后的放电比容量也十分接近。这说明水热除杂和煅烧过程提高了RG的电化学性能。
4 结论针对废旧石墨中Cu、Li、Co、Mn和Ni的不同高效去除方法以及黏结剂和电解液等有机物的去除,研究结果发现水热法对废旧石墨中Cu的去除率最高为96.61%,最适宜浸出条件为温度120 ℃、时间10 min、固液比为1 : 40 g ·mL-1以及Na2S2O8和SG的质量比保持0.4 g ·g-1。水热法对剩余Li的去除率最高为98.94%,最适宜浸出条件为温度保持200 ℃、时间保持3 h以及固液比保持1 : 30 g ·mL-1。剩余的Co、Mn和Ni的去除率最高分别为96.34%、99.67%和99.34%,最适宜浸出条件为反应温度保持80 ℃、反应时间为50 min、固液比为1 : 30 g ·mL-1以及0.4 mol ·L-1的HCl。最后,将去除金属杂质的石墨在空气气氛下的马弗炉中500 ℃下煅烧2 h,即可最大化去除黏结剂和电解液等有机物。此外,通过XRD和SEM形貌的表征分析发现RG的层间距离增大,整体结构呈现出明显的层状结构且出现细小的石墨碎片。在电化学性能方面,RG在0.1 C下的首次放电比容量为410.11 mAh ·g-1,充电比容量为330.85 mAh ·g-1,库伦效率达到了80.67%。100次循环后的放电比容量为401.85 mAh ·g-1,容量保持率为97.99%。在不同电流密度下进行循环充放电,当电流密度恢复到0.1 C时,RG的放电比容量为407.48 mAh ·g-1,高于初始值。以上结果可以说明水热除杂和煅烧过程对SG的电化学性能有很大的提升。
| [1] |
CHENG Q, MARCHETTI B, CHEN X, et al. Separation, purification, regeneration and utilization of graphite recovered from spent lithium-ion batteries-A review[J]. Journal of Environmental Chemical Engineering, 2022, 10(2): 107312. DOI:10.1016/j.jece.2022.107312 |
| [2] |
DU K, ANG E H, WU X, et al. Progresses in sustainable recycling technology of spent lithium-ion batteries[J]. Energy & Environmental Materials, 2022, 5(4): 1012-1036. |
| [3] |
GREY C P, HALL D S. Prospects for lithium-ion batteries and beyond—A 2030 vision[J]. Nature Communications, 2020, 11: 6279. DOI:10.1038/s41467-020-19991-4 |
| [4] |
LI N, SU D. In-situ structural characterizations of electrochemical intercalation of graphite compounds[J]. Carbon Energy, 2019, 1(2): 200-218. DOI:10.1002/cey2.21 |
| [5] |
YAN Z, JIN H, GUO J. Low-temperature synthesis of graphitic carbon-coated silicon anode materials[J]. Carbon Energy, 2019, 1(2): 246-252. DOI:10.1002/cey2.8 |
| [6] |
CHANDRAN V, GHOSH A, PATIL C K, et al. Comprehensive review on recycling of spent lithium-ion batteries[J]. Materials Today: Proceedings, 2021, 47: 167-180. DOI:10.1016/j.matpr.2021.03.744 |
| [7] |
ZHOU L, YANG D, DU T, et al. The current process for the recycling of spent lithium ion batteries[J]. Frontiers in Chemistry, 2020, 8: 578044. DOI:10.3389/fchem.2020.578044 |
| [8] |
ABDOLLAHIFAR M, DOOSE S, CAVERS H, et al. Graphite recycling from end-of-life lithium-ion batteries: Processes and applications[J]. Advanced Materials Technologies, 2022, 8(2): 2200368. |
| [9] |
NATARAJAN S, DIVYA M L, ARAVINDAN V. Should we recycle the graphite from spent lithium-ion batteries? The untold story of graphite with the importance of recycling[J]. Journal of Energy Chemistry, 2022, 71: 351-369. DOI:10.1016/j.jechem.2022.04.012 |
| [10] |
NIU B, XIAO J, XU Z. Advances and challenges in anode graphite recycling from spent lithium-ion batteries[J]. Journal of Hazardous Materials, 2022, 439: 129678. DOI:10.1016/j.jhazmat.2022.129678 |
| [11] |
ZHU X, XIAO J, MAO Q, et al. A promising regeneration of waste carbon residue from spent Lithium-ion batteries via low-temperature fluorination roasting and water leaching[J]. Chemical Engineering Journal, 2022, 430: 132703. DOI:10.1016/j.cej.2021.132703 |
| [12] |
ZHANG Y, ZHANG J, WU L, et al. Extraction of lithium and aluminium from bauxite mine tailings by mixed acid treatment without roasting[J]. Journal of Hazardous Materials, 2021, 404(Pt B): 124044. |
| [13] |
JIANG Y, CHEN X, YAN S, et al. Pursuing green and efficient process towards recycling of different metals from spent lithium-ion batteries through Ferro-chemistry[J]. Chemical Engineering Journal, 2021, 426: 131637. DOI:10.1016/j.cej.2021.131637 |
| [14] |
YI C, YANG Y, ZHANG T, et al. A green and facile approach for regeneration of graphite from spent lithium ion battery[J]. Journal of Cleaner Production, 2020, 277: 123585. DOI:10.1016/j.jclepro.2020.123585 |
| [15] |
NATARAJAN S, ARAVINDAN V. An urgent call to spent LIB recycling: Whys and wherefores for graphite recovery[J]. Advanced Energy Materials, 2020, 10(37): 2002238.1. |
| [16] |
YANG J, FAN E, LIN J, et al. Recovery and reuse of anode graphite from spent lithium-ion batteries via citric acid leaching[J]. ACS Applied Energy Materials, 2021, 4(6): 6261-6268. DOI:10.1021/acsaem.1c01029 |
| [17] |
WU J, ZHENG M, LIU T, et al. Direct recovery: A sustainable recycling technology for spent lithium-ion battery[J]. Energy Storage Materials, 2023, 54: 120-134. DOI:10.1016/j.ensm.2022.09.029 |
| [18] |
YAN C, YUAN H, PARK H S, et al. Perspective on the critical role of interface for advanced batteries[J]. Journal of Energy Chemistry, 2020, 47: 217-220. DOI:10.1016/j.jechem.2019.09.034 |
| [19] |
YU J, LIN M, TAN Q, et al. High-value utilization of graphite electrodes in spent lithium-ion batteries: From 3D waste graphite to 2D graphene oxide[J]. Journal of Hazardous Materials, 2021, 401: 123715. DOI:10.1016/j.jhazmat.2020.123715 |
| [20] |
XU Q, WANG Q, CHEN D, et al. Silicon/graphite composite anode with constrained swelling and a stable solid electrolyte interphase enabled by spent graphite[J]. Green Chemistry, 2021, 23(12): 4531-4539. DOI:10.1039/D1GC00630D |
| [21] |
VADIVEL S, TEJANGKURA W, SAWANGPHRUK M. Graphite/graphene composites from the recovered spent Zn/carbon primary cell for the high-performance anode of lithium-ion batteries[J]. ACS Omega, 2020, 5(25): 15240-15246. DOI:10.1021/acsomega.0c01270 |
| [22] |
ZAKI A H, MOTAGALY A T A, KHALED R, et al. Economic and facile approach for synthesis of graphene-titanate nanocomposite for water reclamation[J]. Journal of Contaminant Hydrology, 2022, 250: 104052. DOI:10.1016/j.jconhyd.2022.104052 |
| [23] |
CHEN S, LI Z, BELVER C, et al. Comparison of the behavior of ZVI/carbon composites from both commercial origin and from spent Li-ion batteries and mill scale for the removal of ibuprofen in water[J]. Journal of Environmental Management, 2020, 264: 110480. DOI:10.1016/j.jenvman.2020.110480 |
| [24] |
GAO Y, ZHU W, WANG C, et al. Enhancement of oxygen reduction on a newly fabricated cathode and its application in the electro-Fenton process[J]. Electrochimica Acta, 2020, 330: 135206. DOI:10.1016/j.electacta.2019.135206 |
| [25] |
CAO Z, ZHENG X, CAO H, et al. Efficient reuse of anode scrap from lithium-ion batteries as cathode for pollutant degradation in electro-Fenton process: Role of different recovery processes[J]. Chemical Engineering Journal, 2017, 337: 256-264. |
| [26] |
ZHANG J, LEI Y, LIN Z, et al. A novel approach to recovery of lithium element and production of holey graphene based on the lithiated graphite of spent lithium ion batteries[J]. Chemical Engineering Journal, 2022, 436: 135011. DOI:10.1016/j.cej.2022.135011 |
| [27] |
HE K, ZHANG Z, ZHANG F. Synthesis of graphene and recovery of lithium from lithiated graphite of spent Li-ion battery[J]. Waste Management, 2021, 124: 283-292. DOI:10.1016/j.wasman.2021.01.017 |
| [28] |
MENG Y, LIANG H, ZHAO C, et al. Concurrent recycling chemistry for cathode/anode in spent graphite/LiFePO4 batteries: Designing a unique cation/anion-co-workable dual-ion battery[J]. Journal of Energy Chemistry, 2022, 64: 166-171. DOI:10.1016/j.jechem.2021.04.047 |
| [29] |
YANG J, ZHAO X, LI W, et al. Advanced cathode for dual-ion batteries: Waste-to-wealth reuse of spent graphite from lithium-ion batteries[J]. eScience, 2022, 2(1): 95-101. DOI:10.1016/j.esci.2021.11.001 |
| [30] |
YU H, DAI H, ZHU Y, et al. Mechanistic insights into the lattice reconfiguration of the anode graphite recycled from spent high-power lithium-ion batteries[J]. Journal of Power Sources, 2021, 481: 229159. DOI:10.1016/j.jpowsour.2020.229159 |
| [31] |
GAO Y, WANG C, ZHANG J, et al. Graphite recycling from the spent lithium-ion batteries by sulfuric acid curing-leaching combined with high-temperature calcination[J]. ACS Sustainable Chemistry & Engineering, 2020, 8(25): 9447-9455. |
| [32] |
GUO Y, LI F, ZHU H, et al. Leaching lithium from the anode electrode materials of spent lithium-ion batteries by hydrochloric acid (HCl)[J]. Waste Management, 2016, 51: 227-233. DOI:10.1016/j.wasman.2015.11.036 |
| [33] |
DA H, GAN M, JIANG D, et al. Epitaxial regeneration of spent graphite anode material by an eco-friendly in-depth purification route[J]. ACS Sustainable Chemistry & Engineering, 2021, 9(48): 16192-16202. |
| [34] |
CHENG Q, YUGE R, NAKAHARA K, et al. KOH etched graphite for fast chargeable lithium-ion batteries[J]. Journal of Power Sources, 2015, 284: 258-263. DOI:10.1016/j.jpowsour.2015.03.036 |
| [35] |
NSHIZIRUNGU T, AGARWAL A, JO Y T, et al. Chlorinated polyvinyl chloride (CPVC) assisted leaching of lithium and cobalt from spent lithium-ion battery in subcritical water[J]. Journal of Hazardous Materials, 2020, 393: 122367. DOI:10.1016/j.jhazmat.2020.122367 |
| [36] |
NSHIZIRUNGU T, RANA M, JO Y T, et al. Rapid leaching and recovery of valuable metals from spent Lithium ion batteries (LIBs) via environmentally benign subcritical nickel-containing water over chlorinated polyvinyl chloride[J]. Journal of Hazardous Materials, 2020, 396(prepublish): 122667. |
| [37] |
LIU Z, YIN Z, XIONG S, et al. Leaching and kinetic modeling of calcareous bornite in ammonia ammonium sulfate solution with sodium persulfate[J]. Hydrometallurgy, 2014, 144: 86-90. |
| [38] |
POPESCU I A, VARGA T, EGEDY A, et al. Kinetic models based on analysis of the dissolution of copper, zinc and brass from WEEE in a sodium persulfate environment[J]. Computers & Chemical Engineering, 2015, 83: 214-220. DOI:10.3969/j.issn.1001-3695.2015.01.049 |
| [39] |
KULOVA TATIANA L, SKUNDIN ALEXANDER M. Electrode/electrolyte interphases of sodium-ion batteries[J]. Energies, 2022, 15(22): 8615. DOI:10.3390/en15228615 |
| [40] |
PARIMALAM B S, MACINTOSH A D, KADAM R, et al. Decomposition reactions of anode solid electrolyte interphase (SEI) components with LiPF6[J]. The Journal of Physical Chemistry C, 2017, 121(41): 22733-22738. DOI:10.1021/acs.jpcc.7b08433 |
| [41] |
KVHN S P, EDSTRÖM K, WINTER M, et al. Face to face at the cathode electrolyte interphase: From interface features to interphase formation and dynamics[J]. Advanced Materials Interfaces, 2022, 9(8): 2102078. DOI:10.1002/admi.202102078 |
| [42] |
LIU W, LIU P, MITLIN D. Review of emerging concepts in SEI analysis and artificial SEI membranes for lithium, sodium, and potassium metal battery anodes[J]. Advanced Energy Materials, 2020, 10(43): 2002297. DOI:10.1002/aenm.202002297 |
| [43] |
NATARAJAN S, BORICHA A B, BAJAJ H C. Recovery of value-added products from cathode and anode material of spent lithium-ion batteries[J]. Waste Management, 2018, 77: 455-465. DOI:10.1016/j.wasman.2018.04.032 |
| [44] |
LI J, HE Y, FU Y, et al. Hydrometallurgical enhanced liberation and recovery of anode material from spent lithium-ion batteries[J]. Waste Management, 2021, 126: 517-526. DOI:10.1016/j.wasman.2021.03.052 |
 2025, Vol. 42
2025, Vol. 42





