锂被誉为“21世纪能源金属”,自1817年由瑞典化学家Johann Arfvedson发现以来,目前已经被广泛的应用于航空航天[1]、陶瓷[2]和储能[3]等多领域中。现今全球已经探明的锂资源总储量约为8 000万t[4],其中59%的锂资源存在于盐湖卤水当中,未来随着锂矿石储量的不断减少和开采成本不断增加,卤水或者海水中的锂资源将成为重要的能源资源安全保障。传统的卤水提锂方法有沉淀法[5]、溶剂萃取法[6]、吸附法[7]和膜分离法[8]等。然而这些传统提锂技术存在环境污染大、适用性差、提锂效率低、循环寿命短等的问题。基于此,新型的电化学提锂技术因其绿色环保、能耗低、选择性高、吸附速率快和适应性广的特点迅速成为了锂资源开发领域的研究热点[9, 10]。
自1993年Kanoh等[11]首次提出了λ-MnO2//Pt体系的新型类锂电池提锂系统以来,研究者们开发出了诸多用于电化学提锂的电极材料,例如钒酸锂(LVO)电极[12]、富氧空位的CoP/Co3O4-石墨烯气凝胶电极[13]、H1.6Mn1.6O4电极[14]等。然而由于水系环境中的工作电压限制以及考虑到离子选择性能和提锂效率等因素,目前电化学提锂材料的研究主要集中于LiMn2O4(LMO)和LiFePO4(LFP)2种。其中尖晶石型LMO结构由于具有特殊的三维Li+扩散通道,所以LMO(10-13~10-14 cm2 ·s-1)的锂离子扩散系数远高于LFP(10-14~10-15 cm2 ·s-1)[15],此外LMO还具有更高的电导率和能量密度[16]。因此LMO成为电化学提锂研究领域最具应用潜力的电极材料之一。然而,尖晶石型LMO电极材料也存在着Mn的溶损和Jahn-Teller效应问题,导致其电化学循环稳定性不足。
基于LMO存在的问题,研究者们已经提出了许多应对的策略,主要包括表面包覆、离子掺杂和形貌控制等。Xu等[17]通过电沉积法制备了自支撑λ-MnO2电极,由于避免了黏接剂的使用以及薄膜电极较短的离子传输距离,该电极获得了较高的循环稳定性和提锂容量。Fang等[18]构筑了原位PPy衍生碳包覆的LMO电极,包覆层作为导电层有效增强了LMO电极的导电性能和循环性能。Zhou等[19]设计了一种截角八面体结构的LiMn2O4电极材料,其中高稳定的(111)晶面和Li+扩散速率更高的(100)晶面协同作用,表现出了优异的锂回收性能。离子掺杂作为一种常见的改性方法,常见的掺杂阳离子包括Ni2+[20]、Mg2+[21]、Co3+[22]、Al3+[23]和Cr3+[24]等。其中Al3+掺杂因其结构稳定和成本低廉成为了一种主要的改性策略。由于Al3+离子半径(0.053 nm)小于Mn3+(0.064 nm),所以Al3+替代部分的Mn3+后并不会明显改变晶体的结构和电荷性质。同时Gao等[25]通过对LiMn2O4及其LiAl0.125Mn1.875O4晶体的结构和电子性质进行计算发现,LiMn2O4在充放电过程中的Jahn-Teller畸变主要是由于Mn3+导致。而Al3+掺杂降低了Mn3+占比,理论上可以有效抑制Jahn-Teller效应,从而提升LMO电极提锂的循环稳定性能。
综上所述,为了提升尖晶石型LMO的电化学提锂性能,本研究通过简单的高温固相法制备了新型LiAlxMn2-xO4电化学提锂电极。通过XRD、SEM和XPS对样品的晶体结构、形貌特征以及表面的元素价态进行了表征。通过循环伏安法(CV)和恒流充放电法(GCD)研究了样品的电化学性能以及具体提锂机制。为了进一步研究不同含量掺杂、不同形貌的LMO对于电化学提锂性能构效关系,分别在模拟混合溶液和东台吉乃尔卤水中进行了电化学提锂,验证了该策略的有效性。
1 实验部分 1.1 材料二氧化锰(MnO2)、醋酸铝[Al(OH)(AC)2 ·2H2O]和碳酸锂(Li2CO3)购买于上海麦克林生化科技有限公司;无水氯化锂(LiCl)、氯化钠(NaCl)、氯化钾(KCl)、无水氯化镁(MgCl2)和无水氯化钙(CaCl2)购买于天津科密欧化学试剂有限公司;导电炭黑(Super-P)、聚偏二氟乙烯(PVDF)均购自中国上海阿拉丁化学试剂有限公司。所有的化学品都为分析纯,不用任何处理,直接使用。
1.2 LiAlxMn2-xO4粉体材料的制备本研究通过简单的固相燃烧法合成尖晶石型LiAlxMn2-xO4电极材料,按不同化学计量比称取二氧化锰、碳酸锂和醋酸铝,加入适量无水乙醇后放入球磨机内进行8 h研磨混匀,研磨结束后烘箱80 ℃烘干6 h,然后在马弗炉中高温煅烧,整个过程以5 ℃ ·min-1升温,首先温度升至500 ℃后保温3 h,再升温至800 ℃保温6 h,随炉冷却至室温,经研钵研磨既得到产物LiAlxMn2-xO4(x=0、0.05、0.10、0.15、0.20)粉体,分别命名为LAMO-x。
1.3 LiAlxMn2-xO4电极的制备以质量比为8 : 1 : 1称取LAMO-x粉末、PVDF、导电炭黑,加入适量NMP(N-甲基-2-吡咯烷酮)以220~250 r ·min-1速率搅拌10 h混合均匀,得到黑色的电极浆料。采用涂膜法将浆料均匀涂覆于10 mm× 10 mm的石墨集流体上(活性物质负载量约为1~2 mg ·cm-2),之后在烘箱中80 ℃干燥12 h,即得到LAMO-x电化学测试电极。考虑到真实提锂量的变化,在卤水提锂实验中采用有效负载面积为15 mm×20 mm的LAMO-x粉体电极(活性物质负载量约为12~16 mg ·cm-2)作为工作电极,提锂前需要以LAMO-x电极为工作电极,Ag电极为对电极,SCE为参比电极组成的三电极体系,在1 mol ·L-1的LiCl溶液中1.0 V恒电位下0.5 h进行预脱锂。
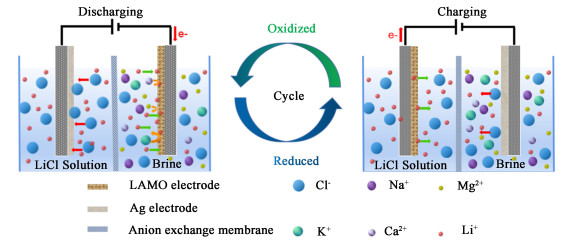
1.4 电化学锂回收如图 1所示为电化学提锂工艺示意图。
|
| 图 1 电化学提锂工艺示意图 Fig.1 Schematic diagram of electrochemical lithium extraction process |
| |
提锂电极采用15 mm×20 mm规格。整个提锂过程包含2个步骤:锂离子的捕获(放电)和释放(充电)。锂吸附过程中,LAMO-x电极位于卤水(见表 1)侧连接电源负极,Ag电极位于回收液(0.05 mol ·L-1的NaCl溶液)侧连接正极,施加电流密度为50 mA ·g-1,电压范围为0~1.0 V。脱锂过程为:使用去离子水清洗电极表面并交换电极位置和正负极,采用相同的电流密度,电压范围为0~1.0 V。最后通过电感耦合等离子体发射光谱仪(ICP-OES)分析各离子的浓度变化。
| Ions | concentration/(g·L-1) |
| Li+ | 0.126 |
| Na+ | 133.8 |
| K+ | 3.537 |
| Ca2+ | 0.56 |
| Mg2+ | 5.835 |
| Mg2+/Li+ | 46.31 |
通过测量回收溶液中Li+的初始浓度(ci)和最终浓度(cf)(体积Vr)以及电极活性物质的质量(m)来计算电极的Li+插层容量(Qr)。如式(1)所示。
| $ Q_{\mathrm{r}}=\frac{\left(c_{\mathrm{r}}-c_{\mathrm{i}}\right) V_{\mathrm{r}}}{m} $ | (1) |
能量消耗由充放电曲线所围面积积分得到,其中W为提锂的能耗(Wh ·mol-1),ΔE为电压(V),q为电荷(C),如式(2)所示。
| $ W=\frac{\int \Delta E \mathrm{~d} q}{V_{\mathrm{r}}\left(c_{\mathrm{r}}-c_{\mathrm{i}}\right)} $ | (2) |
电化学萃取锂的分离系数由式(3)计算得出。式(3)中:cLi为锂离子浓度,cM为杂离子浓度,下标r为回收溶液,f表示卤水溶液。α分离系数越大,分离效果越好,该电化学提锂系统的选择性越高。
| $ \alpha=\frac{c_{\mathrm{Li}, \mathrm{r}} / c_{\mathrm{M}, \mathrm{r}}}{c_{\mathrm{Li}, \mathrm{f}} / c_{\mathrm{M}, \mathrm{f}}} $ | (3) |
使用X射线衍射仪(XRD,UltimanIV,日本理学株式会社)对材料的晶型进行了结构分析,以Cu_Kα为辐射源(λ=0.1542 nm),扫描范围为10°~80°,扫描速率为8(°) ·min-1。使用场发射扫描电子显微镜(SEM,SU-020,日本日立公司)和透射电子显微镜(TEM,JEOL-TEM-2010F,日本JEOL公司)分析了材料的微观形貌。使用X射线光电子能谱(XPS,K Alpha+,赛默飞世尔科技公司)对样品进行了元素组成和价态分析。使用电化学工作站(CHI760E,上海辰华)对材料进行了电化学性能测试。
2 结果与讨论 2.1 LAMO-x的晶型表征图 2(a)中所有的LAMO-x样品的衍射峰都具有典型的立方尖晶石型LiMn2O4特征(JCPDS No. 35-0782),衍射峰形尖锐无杂峰出现,表明成功的合成了LAMO-x材料且纯度和结晶度较高。随着Al3+掺杂量的增加,观察到(400)晶面的衍射峰向更大角度发生了偏移,表明材料发生了晶格收缩。这是由于Al3+的掺入取代了LiMn2O4晶格16d位置部分的Mn3+,Al3+的离子半径(0.053 nm)小于Mn3+离子半径(0.064 nm),所以引起了晶格的收缩。同时Mn3+的占比降低后,Mn4+相对含量比例增加,而Mn4+半径小于Mn3+,使得MnO6八面体收缩,而导致LAMO-x的晶格常数减小[26]。使用Unitcell软件模拟计算LAMO-x的晶胞参数,随着Al3+的掺入晶胞参数呈下降趋势,晶胞体积由557.247 8 nm3降至553.297 2 nm3(大约收缩0.68%),这与Zhang等[27]的计算是一致的。当Al3+掺杂入LiMn2O4时,形成的Al—O键能(512 kJ ·mol-1)大于Mn—O键能(402 kJ ·mol-1),这意味着Al—O的键长较短,在LMO晶格中的LiO4四面体会被拉伸,这有利于锂离子的快速扩散。

|
| 图 2 尖晶石型LAMO-x的XRD图谱 Fig.2 XRD pattern of spinel-type LAMO-x |
| |
随着Al3+掺杂量的增加,LAMO-x的衍射峰强度I(111)/I(400)比值随之降低。衍射峰强度的相对比值反映了晶体的主要晶体取向的变化。有研究表明LiMn2O4的电化学稳定性能与晶粒表面的晶面取向有密切关系[28]。图 2中LAMO-0的衍射峰I(111)/I(400)的峰强比值最高,表明LAMO-0.10中的(111)晶面占比最大。而Al3+掺入后I(111)/I(400)的比值均低于未掺杂的LAMO-0,表明Al3+的掺入有可能抑制了LiMn2O4中(111)晶面的生长。而由于尖晶石型锰酸锂的(111)晶面具有较低的表面能和最密集的Mn原子排列,所以Li+在该晶面的扩散速率较低[29]。
2.2 LAMO-x的微观形貌图 3为LAMO-x(x=0、0.05、0.10、0.15、0.20)材料的微观形貌表征。其中图 3(a)中LAMO-0材料呈现规则的八面体结构,符合典型的尖晶石型LiMn2O4结构,表面均由(111)晶面构成,具有明显的棱角,表面光滑,直径大约为600 nm。当Al3+掺入后,图 3(b)~图 3(e)中LAMO晶粒半径明显变小,随着Al3+的掺杂量增加,大部分LAMO-x晶粒尺寸降低,呈现出不规则的多面体结构。可能是由于(111)晶面生长受到影响,导致LMO晶粒发育不完整。表明Al3+的掺入影响了LMO晶粒的生长。过大的晶粒尺寸导致Li+在LMO中的扩散路径增加,造成Li+的脱出和嵌入效率降低。而Al3+的掺入降低了LMO的平均粒径,这有利于Li+的快速嵌入和脱出。

|
| 图 3 (a)~(e)分别为尖晶石型LAMO-x的SEM图(x=0、0.05、0.10、0.15和0.20);(f)~(i) LAMO-0.10样品的元素映射图像 Fig.3 (a)—(e) SEM images of spinel-type LAMO-x (x=0, 0.05, 0.10, 0.15, 0.20) respectively; (f)—(i) element mapping image of LAMO-0.10 sample |
| |
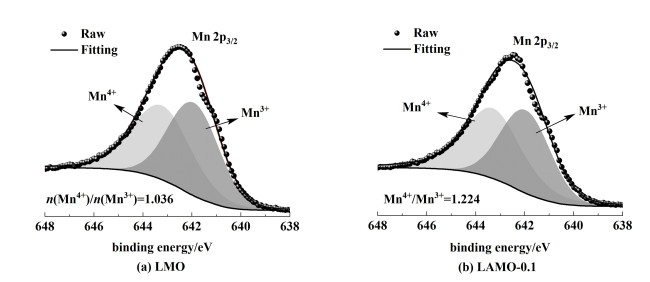
为了进一步研究Al3+掺杂对Mn价态的具体影响,分析了LMO和LAMO-0.10材料Mn 2p3/2的XPS光谱。如图 4(a)和图 4(b)所示,2个样品的Mn 2p3/2峰都具有明显的不对称特征,表明LAMO-x中Mn的价态不唯一[30]。根据拟合的XPS分峰的面积积分计算Mn3+和Mn4+的相对含量,其中Mn3+的相对含量从LAMO-0的48.9%下降到LAMO-0.10的44.7%,Mn4+的含量从LAMO-0的50.7%上升至LAMO-0.10的54.6%。有研究表明,当LiMn2O4中Mn4+与Mn3+的峰面积比值≥1.18时,Jahn-Teller效应可以被有效抑制[31]。经计算LAMO-0和LAMO-0.10的Mn4+与Mn3+的峰面积比值分别为1.036和1.224,因此Al3+的掺入对LiMn2O4中的Jahn-Teller畸变效应有抑制作用。
|
| 图 4 LAMO-x的Mn2p3/2峰XPS拟合曲线 Fig.4 XPS spectra of fitted curves of Mn 2p3/2 spectra |
| |
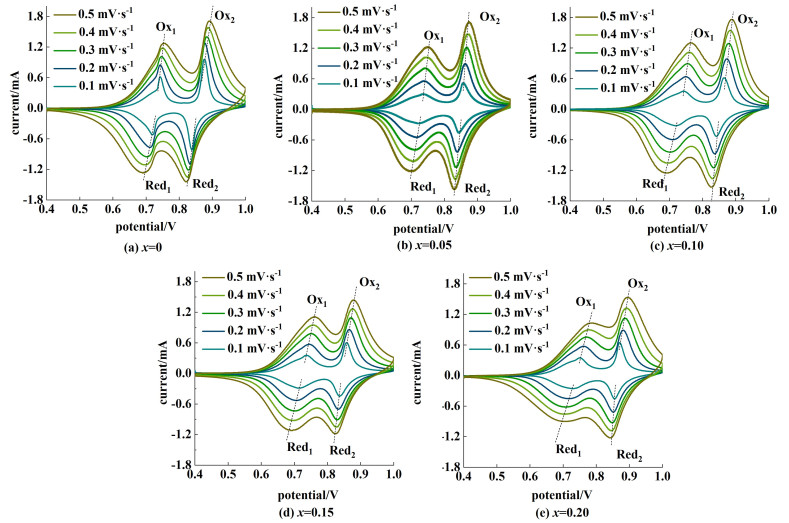
在电压为0~1 V,0.1~0.5 mV ·s-1扫描速率范围下,LAMO-x电极在1 mol ·L-1氯化锂中的CV曲线如图 5所示。可以很明显的观察到所有的CV曲线在0.7~0.9 V区间内存在着2对明显的氧化还原峰,分别对应着在充放电过程中锂离子分为2步从工作电极材料中脱出和嵌入,这也证明了LAMO-x拥有与LMO相似的晶型结构和Li+插层机理。当扫描速率由0.1升至0.5 mV ·s-1过程中,出现了峰值电流Ip绝对值增加,电极的氧化还原峰电位位移以及氧化峰与还原峰的分离度减小,这主要是由于电极材料的欧姆电阻和较低的锂离子扩散性能导致的电极极化造成的,每对氧化还原峰的峰值电流绝对值略有差异,表明了该电极材料具有准可逆性。图 5(c)LAMO-0.10的CV曲线相比于其他LAMO-x的积分面积和峰值电流更大,说明LAMO-0.10电化学活性更高,对于Li+的储锂容量更高,这是由于LAMO-0.10特殊的晶体结构导致,适量的(100)晶面为Li+的快速插层和脱出提供了更高的扩散速率。
|
| 图 5 LAMO-x不同扫描速率下的CV曲线 Fig.5 CV curves of LAMO-x at different scan rates |
| |
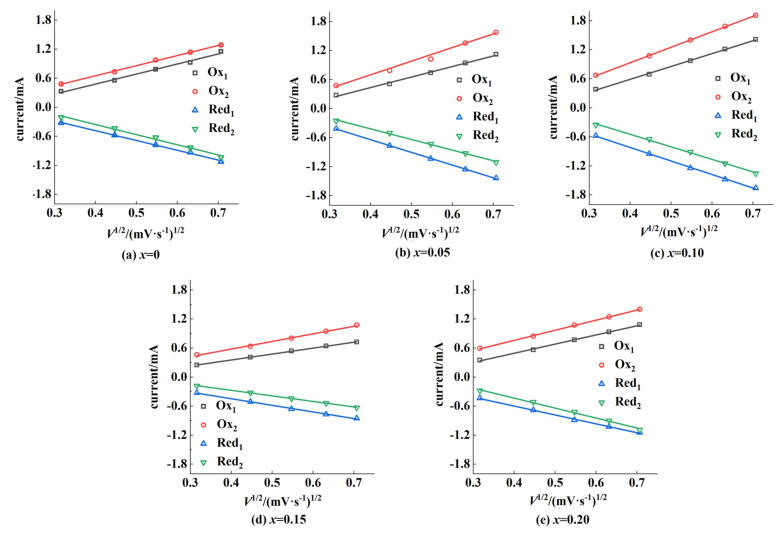
图 6为经由CV曲线中峰值电流(Ip)和扫描速率(V1/2)的拟合曲线。所有的峰值电流与扫速的平方根之间都存在着良好的正线性相关,这说明Li+在电极材料内部嵌入脱出的过程是受扩散反应控制。其扩散系数的计算方程如式(4)。
| $ I_{\mathrm{p}}=2.69 \times 10^5 n^{3 / 2} S D_0^{1 / 2} V^{1 / 2} c_0 $ | (4) |
|
| 图 6 LAMO-x的CV曲线拟合的Ip vs. V1/2曲线 Fig.6 Ip vs. V1/2 curves fitted to CV curves for LAMO-x respectively |
| |
式(4)中:Ip(A)为峰值电流,n为反应中转移的电子数,S(cm2)为活性材料的石墨板的表面积,D0(cm2 ·s-1)为电极材料的宏观扩散系数,V(V ·s-1)为扫描速率,c0(mol ·cm-3)为固相浓度(LiMn2O4为0.023 8 mol ·cm-3)。
表 2为不同Al3+掺杂LAMO-x电极在氧化还原过程中锂离子的扩散系数和平均扩散系数。LAMO-0.10的平均扩散系数为7.68×10-14 cm2 s-1,远高于LAMO-0的扩散系数(3.76×10-14 cm2 ·s-1),扩散系数更高表明了Li+在电极氧化还原过程中嵌入和脱出的电化学动力学更好。有研究表明,LiMn2O4的(111)晶面相对于(100)等其他晶面具有更高的表面能,当锂离子在LMO中进行插层脱嵌时,(100) 晶面的氧化还原电位为3.1 V,比(111)晶面的3.3 V更低,这表明锂离子更容易从(100)晶面发生插脱行为[32]。所以,适当的控制LMO中(111)晶面的占比,有利于提升锂离子的扩散速率和提锂容量。这与本研究中锂离子扩散系数的计算保持一致。
| Ox1 | Ox2 | Red1 | Red2 | Average | |
| LAMO-0 | 2.937 7 | 5.465 7 | 2.870 6 | 3.787 9 | 3.765 5 |
| LAMO-0.05 | 4.744 1 | 9.465 2 | 4.593 2 | 6.949 5 | 6.438 0 |
| LAMO-0.10 | 6.130 7 | 1.057 2 | 6.227 4 | 7.789 5 | 7.679 9 |
| LAMO-0.15 | 4.493 9 | 8.067 9 | 4.691 7 | 6.390 4 | 5.911 1 |
| LAMO-0.20 | 2.075 9 | 3.743 9 | 2.186 0 | 3.080 8 | 2.771 1×10-14 |
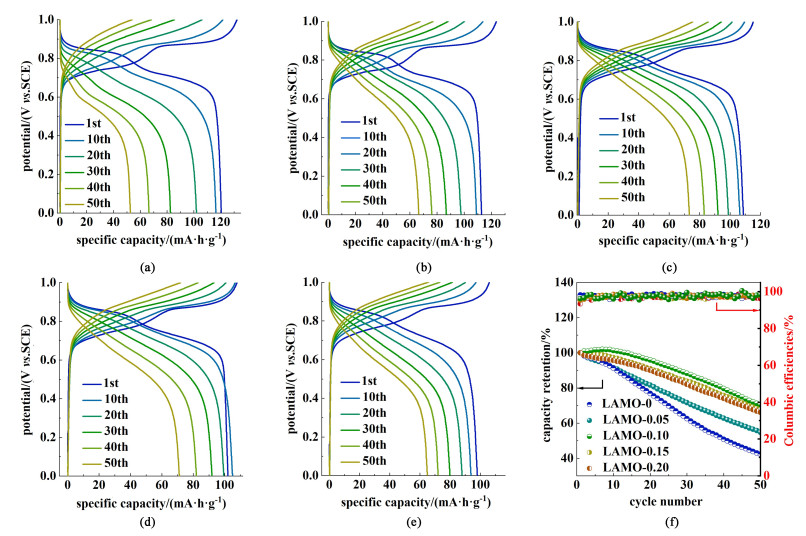
如图 7,在1 mol ·L-1氯化锂溶液中,电压为0~1 V,电流密度为50 mA ·g-1条件下,所有的充放电曲线都表现出了2个较长的的充放电平台,对应着CV曲线中的2对氧化还原峰,代表了Li+的插入和脱出都是分为2个阶段进行。图 7(a)LAMO-0展现出了最高的初始放电容量121.3 mAh ·g-1,在经历50次循环充放电后放电容量急剧降低至51.4 mA ·h ·g-1,容量保持率仅为42.38%。LAMO-0.10的初始放电容量为109.4 mA ·h ·g-1,50次循环充放电后容量保持率达到67%。当Al3+掺杂含量进一步升高时,容量保持率出现了下降,这可能是由于不规则晶粒中(111)晶面比例过低导致。图 7(f)为不同LAMO-x电极50次循环充放电的放电容量保持率曲线和库伦效率曲线。随着Al3+掺入量的增加,首次放电容量呈现下降趋势,而放电容量保持率则整体呈现出上升趋势,所有电极在循环充放电过程中的库伦效率均大于97%。LAMO-0.10电极在模拟提锂的循环充放电过程中表现出了较高的Li+插层容量同时还具有优异的循环稳定性能。
|
| 图 7 (a)~(e)分别为LAMO-x (x=0、0.05、0.10、0.15、0.20)在不同扫描速率下的CV曲线;(f)容量稳定性曲线和库伦效率图 Fig.7 Cyclic charge-discharge curves of (a)—(e)LAMO-x (x=0, 0.05, 0.10, 0.15, 0.20) at different scan rates; (f) Coulombic efficiency and cyclic stability |
| |
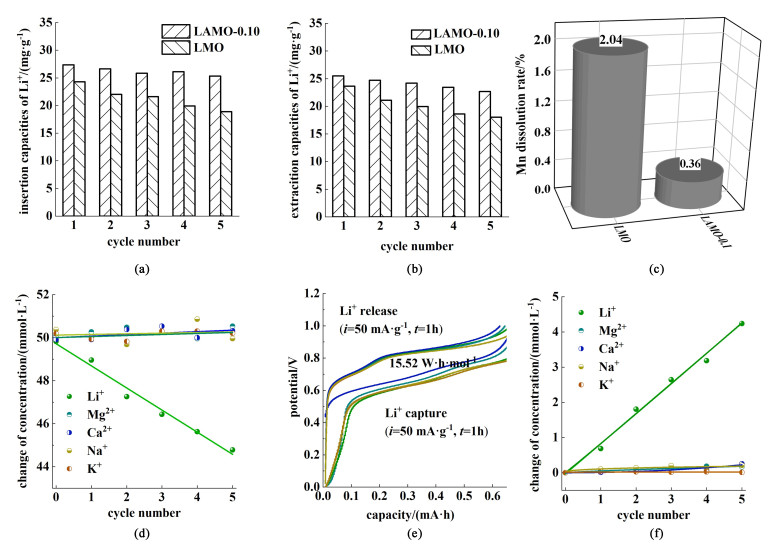
如图 8(a)和图 8(b)为LAMO-0.10和LMO电极在50 mmol ·L-1的LiCl溶液中,进行5次连续提锂的离子插层容量和脱出容量变化。相比于LMO的平均插层容量(21.36 mg ·g-1)和脱嵌容量(20.53 mg ·g-1),LAMO-0.10的平均插层容量(26.25 mg ·g-1) 和脱嵌容量(25.17 mg ·g-1)更高,并且Li+的回收率均超过了96%。图 8(c)中LMO电极Mn的溶损率达到2.04%,而LAMO-0.10电极Mn的溶损率仅为0.36%,并且在两侧溶液中均未检测到Al3+存在。得益于其较低的Mn溶损率,LAMO-0.10展现出了更高的Li+嵌入/脱出容量和循环稳定性能。
|
| 图 8 (a)(b)分别为LAMO-0.10和LMO电极提锂的嵌入和脱出容量对比;(c)为5次循环提锂Mn的溶损率;(d)为模拟卤水中的离子浓度的变化;(e)为5次的电化学提锂平均能耗计算;(f)为回收液中的离子浓度的变化 Fig.8 (a) and (b) Comparison of the lithium intercalation capacity and de-embedding capacity of LAMO-0.10 electrode and LMO electrode for 5 consecutive cycles, respectively; (c) dissolution loss rate of Mn after 5 cycles of lithium extraction; (d) and (f) variation curves of ion concentration in the adsorption solution and recovery solution with the number of cycles in electrochemical lithium recovery of LAMO-0.10 electrode; (e) average energy consumption was calculated |
| |
图 8(d)~图 8(f)为LAMO-0.10//Ag系统的电化学模拟溶液提锂实验。模拟溶液为浓度均为50 mmol ·L-1的混合溶液(K+、Na+、Li+、Mg2+和Ca2+),恒定电流密度50 mA ·g-1,连续进行电化学吸脱附5次并记录模拟溶液和回收液中的离子浓度变化。图 8(d)和图 8(f)显示,经过5个周期提锂的循环后,模拟溶液中的Li+浓度与循环次数呈线性变化,表明LAMO电极材料可以进行连续电化学提锂,平均Li+脱嵌容量为22.87 mg ·g-1。而其他竞争离子的浓度没有发生明显变化。结果表明LAMO-0.10//Ag系统对锂离子具有较高的选择性。图 8(e)通过式(2)对提锂过程中能耗W进行计算,5次提锂平均能耗仅为15.52 Wh ·mol-1。
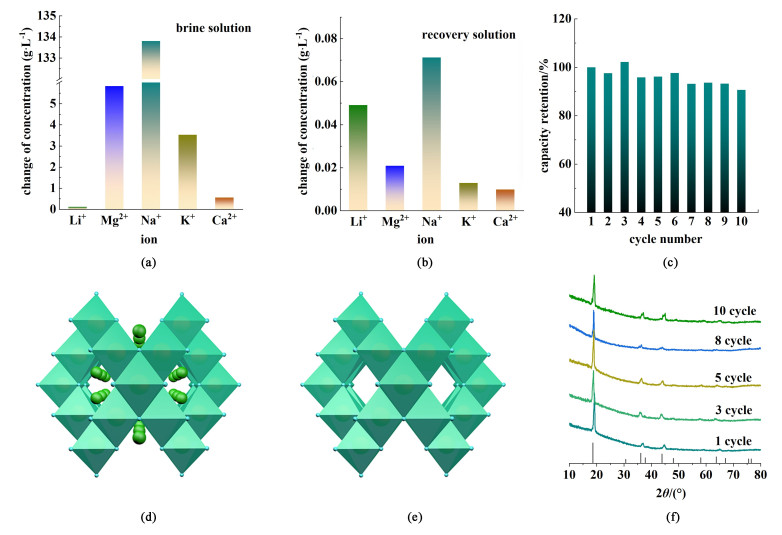
2.5.2 电化学盐湖卤水提锂为进一步研究LAMO-0.10电极在真实卤水中的提锂性能表现,以东台吉乃尔盐湖的卤水为原溶液进行电化学提锂。以10 g ·L-1的NaCl为回收液,LAMO-0.10为工作电极,对电极为Ag电极,采用恒定电流50 mA ·g-1,充放电压范围0~1 V。如图 9(a)和图 9(b)分别为连续10次提锂过程中原溶液和回收液中离子浓度。在经过LAMO-0.10电极10次连续提锂后,原溶液中Li+浓度由初始的0.126降低至0.069 g ·L-1,回收液中Li+浓度对应的增加到0.053 g ·L-1,锂离子回收率达到92.98%。而镁离子浓度则由5.83 g ·L-1降低至回收液中0.021 g ·L-1,n(Mg2+)/n(Li+)由46.31降低至0.39,锂镁分离系数αLi-Mg高达118.74,表明了LAMO-0.10电极在高Mg/Li的卤水环境中仍具较高的提锂容量和选择性能。经过10次连续循环提锂后容量保持率90.2%,平均Li+提取容量达到19.75 mg ·g-1,具体提锂性能参数见表 3。图 9(d)和图 9(e)为LiMn2O4和脱锂后的λ-MnO2的原子结构示意图,LMO特殊的三维传输通道允许锂离子从Mn-O结构中快速脱出嵌入。图 9(f)为连续提锂过程中的XRD图谱,提锂过程中的XRD衍射图并未有新衍射峰出现和消失,所有衍射峰的强度和位置并未发生较大改变,峰形尖锐且无杂峰出现,表明LAMO-0.10电极在电化学提锂过程中具有较高的循环可逆性能。随后使用王水将提锂后的LAMO-0.10电极材料溶解,通过ICP-OES分析测得n(Li) : n(Mn) : n(Al)=1.00 : 1.96 : 0.11,与LAMO-0.10电极基本保持一致,并且没有检测到其它竞争离子(K+、Na+、Ca2+和Mg2+)。
|
| 图 9 LAMO-0.01电极和LAMO-0电极卤水提锂(a)卤水溶液中离子浓度;(b)回收液液中离子浓度;(c)卤水提Li+吸附容量保持率;(d)和(e)为LiMn2O4和λ-MnO2的原子结构示意图;(f)为循环过程中的XRD图谱 Fig.9 LAMO-0.10 electrode and LAMO-0 electrode brine lithium extraction (a) ion concentration in brine solution; (b) ion concentration in recovery liquid solution; (c) brine extraction Li+ adsorption capacity retention; (d) and (e) schematic diagrams of the atomic structures of LiMn2O4 and λ-MnO2; (f) XRD patterns of the cycling process |
| |
| items | ρ(Li+)/ (g·L-1) | ρ(Na+)/ (g·L-1) | ρ(K+)/ (g·L-1) | ρ(Ca2+)/ (g·L-1) | ρ(Mg2+)/ (g·L-1) | V/ mL |
| Initial catholyte(brine) | 0.120 | 133.80 | 3.53 | 0.56 | 5.83 | 150 |
| Initial anolyte | 1.16 | 150 | ||||
| Final catholyte | 0.069 | 127.96 | 3.47 | 0.51 | 5.67 | 152 |
| Final anolyte | 0.049 | 1.24 | 0.014 | 0.01 | 0.021 | 147 |
| Separation coefficient | 347.62 | 155.91 | 24.73 | 118.74 |
综上表明,该LAMO-0.10电极在高Mg/Li的卤水中电化学提锂依然具有较高的提锂容量、循环稳定性能和Li+选择性能。
3 结论为改善LiMn2O4在电化学提锂过程中提锂容量衰减,提升电化学提锂效率,本研究通过简单的高温固相法合成了LAMO-x电极材料用于电化学提锂。Al3+的掺杂降低了LMO的晶格参数和晶粒尺寸,XRD分析表明掺杂后LMO(111)晶面占比明显降低,这有利于Li+在LMO晶格内部的快速扩散,提升提锂效率。同时Al3+的掺入有效提升LMO中Mn的平均价态,降低了Mn的溶损和Jahn-Teller效应,提升了LMO的电化学提锂稳定性。在电化学测试中,LAMO-0.10电极表现出了较高的放电容量(109.4 mA ·h ·g-1)和循环稳定性能(67%/50)。在50 mmol ·L-1的LiCl溶液中连续提锂,LMO电极平均Li+脱嵌容量为20.53 mg ·g-1,而LAMO-x电极脱锂容量达到25.17 mg ·g-1,循环提锂后LAMO中Mn的溶出率仅约为LMO的1/6。LAMO-0.10电极在模拟混合溶液中进行电化学提锂,平均Li+脱嵌容量达到22.87 mg ·g-1,而其他阳离子浓度未发生明显变化,5次连续提锂平均能耗为15.52 Wh ·mol-1(Li+)。即使在高Mg/Li的东台吉乃尔盐湖卤水中进行提锂,LAMO-0.10提锂电极依旧表现出了超高的离子选择性能(αLi-Mg=118.74),平均提锂容量达到19.75 mg ·g-1,10次循环提锂容量保持率为90.2%。综上所述,Al掺杂的LAMO-0.10电极在电化学提锂领域具有选择性高、吸附容量大和循环性能稳定的优势。这些优异的性能有望促进LiMn2O4在电化学提锂中的规模化应用。
| [1] |
RENEWABLE I, IRENA I. Electricity storage and renewables: Costs and markets to 2030[R]. Abu Dhabi: International Renewable Energy Agency, 2017
|
| [2] |
CHEN W, LEE C H, CHUNG Y F, et al. Recovery of rubidium and cesium resources from brine of desalination through t-BAMBP extraction[J]. Metals, 2020, 10(5): 607. DOI:10.3390/met10050607 |
| [3] |
ZHAO X, LI G, FENG M, et al. Semi-continuous electrochemical extraction of lithium from brine using CF-NMMO/AC asymmetric hybrid capacitors[J]. Electrochimica Acta, 2020, 331: 135285. DOI:10.1016/j.electacta.2019.135285 |
| [4] |
MIATTO A, RECK B K, WEST J, et al. The rise and fall of American lithium[J]. Resources, Conservation and Recycling, 2020, 162: 105034. DOI:10.1016/j.resconrec.2020.105034 |
| [5] |
ZHANG Y, HU Y, WANG L, et al. Systematic review of lithium extraction from salt-lake brines via precipitation approaches[J]. Minerals Engineering, 2019, 139: 105868. DOI:10.1016/j.mineng.2019.105868 |
| [6] |
ZHOU Z, QIN W, CHU Y, et al. Elucidation of the structures of tributyl phosphate/Li complexes in the presence of FeCl3 via UV-visible, Raman and IR spectroscopy and the method of continuous variation[J]. Chemical Engineering Science, 2013, 101: 577-585. DOI:10.1016/j.ces.2013.07.020 |
| [7] |
CHEN J, LIN S, YU J. High-selective cyclic adsorption and magnetic recovery performance of magnetic lithium-aluminum layered double hydroxides (MLDHs) in extracting Li+ from ultrahigh Mg/Li ratio brines[J]. Separation and Purification Technology, 2021, 255: 117710. DOI:10.1016/j.seppur.2020.117710 |
| [8] |
ZHANG C, MU Y, ZHAO S, et al. Lithium extraction from synthetic brine with high Mg2+/Li+ ratio using the polymer inclusion membrane[J]. Desalination, 2020, 496: 114710. DOI:10.1016/j.desal.2020.114710 |
| [9] |
YOON H, LEE J, KIM S, et al. Review of concepts and applications of electrochemical ion separation (EIONS) process[J]. Separation and Purification Technology, 2019, 215: 190-207. DOI:10.1016/j.seppur.2018.12.071 |
| [10] |
TRÓCOLI R, ERINMWINGBOVO C, LA MANTIA F. Optimized lithium recovery from brines by using an electrochemical ion-pumping process based on λ-MnO2 and nickel hexacyanoferrate[J]. ChemElectroChem, 2017, 4(1): 143-149. DOI:10.1002/celc.201600509 |
| [11] |
KANOH H, OOI K, MIYAI Y, et al. Electrochemical recovery of lithium ions in the aqueous phase[J]. Separation Science and Technology, 1993, 28(1/2/3): 643-651. |
| [12] |
SHANG X, LIU Z, JI W, et al. Synthesis of lithium vanadate/reduced graphene oxide with strong coupling for enhanced capacitive extraction of lithium ions[J]. Separation and Purification Technology, 2021, 262: 118294. DOI:10.1016/j.seppur.2020.118294 |
| [13] |
JIN W, HU M, SUN Z, et al. Simultaneous and precise recovery of lithium and boron from salt lake brine by capacitive deionization with oxygen vacancy-rich CoP/Co3O4-graphene aerogel[J]. Chemical Engineering Journal, 2021, 420: 127661. DOI:10.1016/j.cej.2020.127661 |
| [14] |
WANG Q, DU X, GAO F, et al. A novel H1.6Mn1.6O4/reduced graphene oxide composite film for selective electrochemical capturing lithium ions with low concentration[J]. Separation and Purification Technology, 2019, 226: 59-67. DOI:10.1016/j.seppur.2019.05.082 |
| [15] |
DAS S R, MAJUMDER S B, KATIYAR R S. Kinetic analysis of the Li+ ion intercalation behavior of solution derived nano-crystalline lithium manganate thin films[J]. Journal of Power Sources, 2005, 139(1/2): 261-268. |
| [16] |
ZHAO X, FENG M, JIAO Y, et al. Lithium extraction from brine in an ionic selective desalination battery[J]. Desalination, 2020, 481: 114360. DOI:10.1016/j.desal.2020.114360 |
| [17] |
XU X, ZHOU Y, FENG Z, et al. A self-supported λ-MnO2 film electrode used for electrochemical lithium recovery from brines[J]. ChemPlusChem, 2018, 83(6): 521-528. DOI:10.1002/cplu.201800185 |
| [18] |
FANG J, WANG J, JI Z, et al. Establishment of PPy-derived carbon encapsulated LiMn2O4 film electrode and its performance for efficient Li+ electrosorption[J]. Separation and Purification Technology, 2022, 280: 119726. DOI:10.1016/j.seppur.2021.119726 |
| [19] |
ZHOU G, CHEN L, LI X, et al. Construction of truncated-octahedral LiMn2O4 for battery-like electrochemical lithium recovery from brine[J]. Green Energy & Environment, 2022. |
| [20] |
SHANG X, HU B, NIE P, et al. LiNi0.5Mn1.5O4-based hybrid capacitive deionization for highly selective adsorption of lithium from brine[J]. Separation and Purification Technology, 2021, 258: 118009. DOI:10.1016/j.seppur.2020.118009 |
| [21] |
YU Y, XIANG M, GUO J, et al. Enhancing high-rate and elevated-temperature properties of Ni-Mg Co-doped LiMn2O4 cathodes for Li-ion batteries[J]. Journal of Colloid and Interface Science, 2019, 555: 64-71. DOI:10.1016/j.jcis.2019.07.078 |
| [22] |
LARHRIB B, NIKIFORIDIS G, ANOUTI M. Safe and efficient phosphonium ionic liquid based electrolyte for high-potential LiMn2O4 and LiNi0.8Co0.15Al0.05O2 cathodes for Li-ion batteries[J]. Electrochimica Acta, 2021, 371: 137841. DOI:10.1016/j.electacta.2021.137841 |
| [23] |
TAO Y, LU Y, GUO Y, et al. Facile synthesis and electrochemical properties of truncated octahedral Al, Ni dual doped LiMn2O4 cathode materials[J]. Journal of Alloys and Compounds, 2022, 904: 164027. DOI:10.1016/j.jallcom.2022.164027 |
| [24] |
LIANG Q, WANG Z, BAI W, et al. Stimulative formation of truncated octahedral LiMn2O4 by Cr and Al co-doping for use in durable cycling Li-ion batteries[J]. Dalton Transactions, 2021, 50(46): 17052-17061. DOI:10.1039/D1DT03221F |
| [25] |
GAO T, LIU H, ZHANG P, et al. Structural and electronic properties of Al-doped spinel LiMn2O4[J]. Acta Physica Sinica, 2012, 61(18): 187306. DOI:10.7498/aps.61.187306 |
| [26] |
WANG Q, ZHANG Y, ZHANG H, et al. Structure and electrochemical performance of cobalt oxide layer coated on LiNi0.03Mn1.97O4 cathode materials[J]. Journal of Alloys and Compounds, 2017, 693: 474-481. DOI:10.1016/j.jallcom.2016.09.130 |
| [27] |
ZHANG Z, CHEN Z, WANG G, et al. Dual-doping to suppress cracking in spinel LiMn2O4: A joint theoretical and experimental study[J]. Physical Chemistry Chemical Physics, 2016, 18(9): 6893-6900. DOI:10.1039/C5CP07182H |
| [28] |
WARBURTON R E, IDDIR H, CURTISS L A, et al. Thermodynamic stability of low- and high-index spinel LiMn2O4 surface terminations[J]. ACS Applied Materials & Interfaces, 2016, 8(17): 11108-11121. |
| [29] |
WANG Z. Structural analysis of self-assembling nanocrystal superlattices[J]. Advanced Materials, 1998, 10(1): 13-30. DOI:10.1002/(SICI)1521-4095(199801)10:1<13::AID-ADMA13>3.0.CO;2-W |
| [30] |
BIESINGER M C, PAYNE B P, GROSVENOR A P, et al. Resolving surface chemical states in XPS analysis of first row transition metals, oxides and hydroxides: Cr, Mn, Fe, Co and Ni[J]. Applied Surface Science, 2011, 257(7): 2717-2730. DOI:10.1016/j.apsusc.2010.10.051 |
| [31] |
DING X, ZHOU H, LIU G, et al. Electrochemical evaluation of LiAl0.05Ni0.05Mn1.9O4 cathode material synthesized via electrospinning method[J]. Journal of Alloys and Compounds, 2015, 632: 147-151. DOI:10.1016/j.jallcom.2015.01.163 |
| [32] |
NAKAYAMA M, TAKI H, NAKAMURA T, et al. Combined computational and experimental study of Li exchange reaction at the surface of spinel LiMn2O4 as a rechargeable Li-ion battery cathode[J]. The Journal of Physical Chemistry C, 2014, 118(47): 27245-27251. DOI:10.1021/jp509232m |
 2025, Vol. 42
2025, Vol. 42





