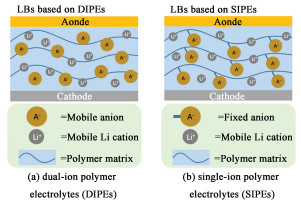
可持续能源市场的蓬勃发展对锂离子电池(LIBs)的充放电性能、能量密度提出了更高的要求。然而,以有机溶剂作为电解液的LIBs存在易燃易爆的安全性问题以及与高容量电极材料匹配差成为了其迈向更高能量密度发展的主要瓶颈[1, 2]。固态电解质可以规避有机溶剂易挥发问题显著降低热失控和爆炸的风险[3, 4],而且还可以匹配高容量电极材料比如金属锂以实现更高能量密度的电池[5],为储能行业的可持续发展、高效能源的利用铺平道路[6]。固态电解质按照组分不同可分为固态聚合物电解质(SPEs)、无机固态电解质(ISEs)和聚合物/无机复合电解质(PIEs)[7, 8]。与界面相容性差,加工难度大的ISEs相比,以高分子聚合物为基体的SPEs具有高度设计灵活性,因而其能开发出多功能的电池以满足可穿戴和柔性电子产品的市场需求[9-11]。如图 1所示,根据SPEs中载流子的不同,SPEs可以分为双离子传导型聚合物电解质(DIPEs)和单离子传导型聚合物电解质(SIPEs)[12]。其中DIPEs可以再分为:“salt-in-polymer”电解质(SIP SPEs)与“polymer-in-salt”电解质(PIS SPEs)[13]。前者具有低的玻璃化转变温度(Tg),它们通常具有结晶相和无定形相;后者具有较高的锂盐含量(>50%)。
由于在聚合物相结构中同时存在晶体区和无定形区,锂盐在其中还存在一定的解离,会形成各种离子对及多合离子等,配位环境复杂,所以对离子传导机制的研究一直是学术界讨论要点和研究设计高性能电解质所必须考虑的[14-16], 本论文主要从DIPEs、SIPEs 2大类入手,系统总结了不同体系的SPEs的离子传导机制、并分析了影响离子传导性质的主要因素;相应地,我们从调整聚合物的结晶度、解耦Li+传输与聚合物链段的弛豫和高分子结构设计3方面阐述了提高离子传输性能的策略,此外本文还循序渐进地介绍了研究人员为什么试图使用相应的策略方法来促进离子传输,这些原则和策略可以应用于其他电解质以提高其离子电导率和迁移数并实现高性能的电池。
1 双离子传导型聚合物电解质(DIPEs)1973年Fenton等[17]报道了聚环氧乙烷(PEO)和几种碱金属盐[如硫氰酸钾(KSCN)和硫氰酸钠(NaSCN)]的混合物在较高温度下(>60 ℃)可以作为离子传导材料。Armand等[18]认识到这些聚合物对开发固态电池技术的深远意义和潜在应用,自此DIPEs应用于固态电池的研究吸引了学术界和工业界的广泛关注。
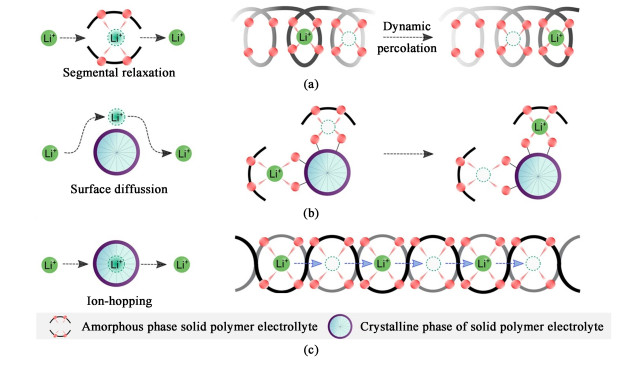
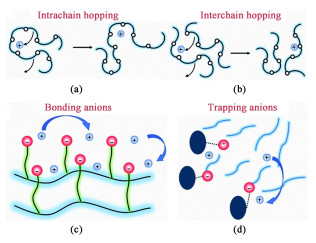
1.1 “Salt-in-polymer”电解质(SIP SPEs)目前已报道的聚合物电解质大部分为基于中性聚合物骨架和少量锂盐的双离子传导型体系,即经典的“salt-in-polymer”电解质(SIP SPEs),其中锂离子和阴离子均能自由迁移。图 2展示了基于PEO的SIP SPEs的离子传导机制。Song等[19]概述了SIP SPEs中离子迁移主要存在3种传导机制,(1)在PEO聚合物-盐络合物电解质的非晶相中[图 2(a)],锂盐中的Li+与聚合物链段上的强极性基团(—O—)存在强配位作用,锂离子的传导就是随着聚合物链段运动并在各个配位点之间发生配位键的断裂与形成进行跳跃迁移实现的[20-23],很多研究者称之为聚合物链段迁移机制(vehicular机制)[24];(2)在无定形和结晶的混合相中[图 2(b)],结晶表面可通过表面配位来帮助离子传输,一般为聚合物/无机复合电解质的传导机制;(3)对于由低相对分子质量PEO与碱金属盐的配合物形成的一些特定结晶相[25, 26],锂离子跳跃在相邻位点进行传输[图 2(c)],由于该过程不涉及PEO链的链段运动,被认为是解耦离子传输,称之为离子跳跃机制(结构传输机制)。需要指出的是,因为SIP SPEs的结晶区通常认为其聚合物链段是固定排列的[27],锂离子无法进行迁移,结晶区的存在能中断非晶相的传导途径导致离子电导率显著下降[28],所以上述离子跳跃机制仅限于特定的结晶SIP SPEs体系。此外,PEO的相对分子质量(Mn)对于锂离子的传导机制也有影响。PEO基聚合物电解质是由部分聚合物链段排列或缠结的链随机构成多个局部结晶区的材料,其链段之间是存在各种相互作用包括物理交叉、打结和成环。这种相互作用约束被认为限制了聚合物长链的松弛和离子运输[29]。Devaux等[30]研究表明,对于较低的Mn的PEO,与甲基(—CH3)等非极性端基相比,羟基(—OH)极性端基与阴离子和阳离子之间的强相互作用能引起短暂的交联,降低了链段运动的自由度,但是对离子传导机制无影响(离子运输主要为vehicular机制)。而对于高Mn的PEO,离子传输不受端基的影响,因为其离子传导遵循的是锂离子从一个配位位置到另一个配位位置的离子跳跃机制,其离子传输与链段动力学无关。除了某些特定情况外,目前关于SIP SPEs的离子传导机制达成的共识是,锂离子传导主要遵循vehicular机制,即与无定形区的聚合物链段的运动高度相关。[31-36]。
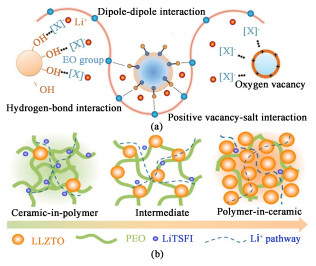
基于上述传导机理,为了SIP SPEs中更高效的离子运输,大量研究围绕促进锂盐的解离、降低玻璃化转变温度(Tg)展开了一系列的探索。最早用于SIP SPEs的盐主要含有无机阴离子如SCN-[17]、ClO4-[37]、BF4-[38]和有机阴离子如CF3SO3-[39],它们均存在与锂离子紧密结合的问题,研究人员试图通过减弱盐阴离子和锂离子之间的相互作用来提高离子电导率。比如用离域程度更高的双三氟甲磺酰亚胺TFSI-替换锂盐中的CF3SO3-,使得锂盐解离程度大大增加,离子电导率在100 ℃时>10-3 S ·cm-1[40]。在过去的10年中,锂盐阴离子的结构设计主要集中在扩大阴离子的离子半径(如六氟磷酸锂(LiPF6)[41]、二氟(草酸)硼酸盐锂(LiDFOB)[42]和(苯磺酰)(三氟甲磺酰)亚胺锂(LiBTFSI)[43],带有高离域负电荷的分子的设计取得了进一步的进展。但是以上方法并未对Li+的传导机制产生任何影响,此类体系中的锂离子传导仍然与聚合物链段的动力学紧密联系,这限制了Li+传输的改善效果。降低SIP SPEs玻璃化转变温度(Tg)以提高聚合物链段运动自由度是另一个可行的策略。研究人员开始将无机填料引入聚合物基体[44],试图综合ISEs与SPEs的各自优势得到PIEs。典型的惰性填料如Al2O3、SiO2、BaTiO3等和活性填料如Li7La3Zr2O12 (LLZO)、Li0.3La0.557TiO3(LLTO)和Li6.4La3Zr1.4Ta0.6O12 (LLZTO)等可以通过表面特性以及自身的结构特征改变PIEs中的相互作用模式。如图 3(a)所示,聚合物电解质与无机填料之间存在几种路易斯酸碱相互作用如氢键相互作用、偶极-偶极相互作用和正空位-盐相互作用等[45]。填料对电解质中的离子传导的影响可总结为2点:(1)填料和聚合物之间的相互作用可以增强聚合物链段的运动自由度,促进离子传导;(2)填料和锂盐之间的相互作用可以促进锂盐解离,提高体系中载流子的浓度。值得注意的是,相较于惰性填料,如图 3(b)中的活性填料LLZTO可以直接参与Li+传导,甚至形成连续的传导网络以构建Li+通过填料传导的离子迁移途径[46, 47]。由于填料在电解质体系中的相互作用对聚合物的聚集态结构、载流子的浓度、离子迁移行为均有影响,仍需更多实验和模型用于讨论其中的离子传输行为[48]。
在过去的几十年中,其他策略包括引入增塑剂如有机电解液[49]、离子液体等[50, 51]得到凝胶或准固态电解质、聚合物共混[52]以及交联/共聚柔性聚合物链[53]也被提出用于降低聚合物的结晶度。以上策略都是意图将具有优势互补的电解质材料结合起来得到离子传导更优的多组分聚合物电解质,相应地,其中的离子传导就会由不同组分提供的不同离子传导机制共同贡献,离子传导路径变得更多更复杂[54]。
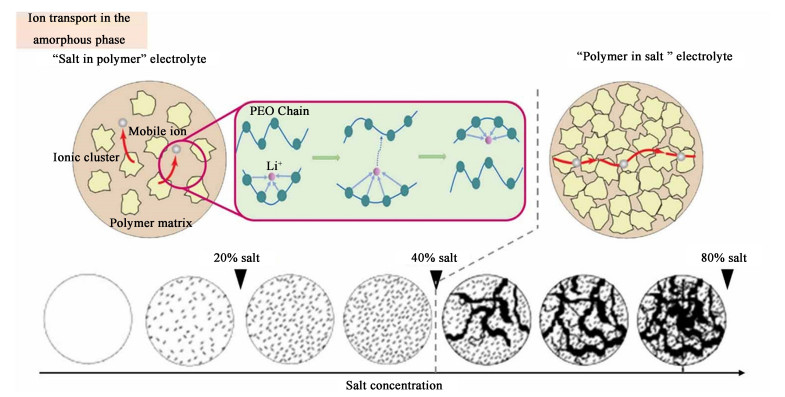
1.2 “Polymer-in-salt”电解质(PIS SPEs)鉴于聚合物的结晶度高的性质,锂离子的传导又与聚合物动力学(如段扩散、链弛豫等)紧密相关,仅靠提高聚合物链段运动自由度不足以促进锂离子的快速迁移。一些试图解耦锂离子与聚合物链段之间运动的策略被提出,比如通过引入松散弱配位的聚合物单元如聚碳酸酯、聚酯或聚四氢呋喃来改变聚合物骨架的化学性质[55-59]。然而以上体系均为SIP SPEs,其改进的离子传导性能有限。Angell等[60]提出了通过“polymer-in-salt”电解质(PIS SPEs)来实现锂离子与聚合物链段弛豫解耦的超离子体系。研究表明当SIP SPEs变成PIS SPEs电解质经历这样一个过程[13, 61, 62]:如图 4,在较低盐浓度的SIP SPEs中,锂盐解离度高,离子传导依赖于无定形区的聚合物链段运动,当SIP SPEs中盐浓度不断增加到一个临界值时,Tg最终会达到最大值,随着盐浓度的进一步增加(盐浓度大于50%)时,电解质中过量的盐会形成盐聚集体,这些聚集体之间的相互连接会变得更加紧密,形成了一个连续的阳离子/阴离子簇组成离子传导网络,从而促进锂离子通过第2条传导路径进行扩散[63, 64]。这表明PIS SPEs有能力使锂离子传导不再受限于缓慢的聚合物链段动力学,而是构建了1条以跳跃迁移为主导的快速离子传输通道(室温下离子电导率可以达到1.32×10-3 S ·cm-1)。这种离子传导机制的变化也可以体现在离子电导率的温度依赖性曲线上[65, 66],由温度依赖性曲线得到的离子迁移活化能Ea是探究聚合物电解质中的离子传导机制重要量化参数[67]。Goodenough等[68]探究了84% LiTFSI/16% PAN组合的PIS SPE的离子电导率的温度依赖性曲线,根据Arrhenius方程,计算出活化能为23.1 kJ ·mol-1,低于PEO基SIP SPE的活化能(约38 kJ ·mol-1),活化能的降低意味着离子迁移机制的转变。一般来说,在SIP SPEs遵循的vehicular机制中,除了锂离子络合-解络合需要能量外,聚合物链段作为一个大的载体基团,它的松弛或运动,也需要消耗能量才能完成离子的传导;而PIS SPEs中跳跃迁移机制中,Li+传导发在相邻的或者附近的配位点之间,不存在载体基团的运动,能够实现与聚合物链段弛豫解耦,所以其迁移活化能会更低[24, 69]。虽然PIS SPEs可以实现高离子电导率,但随着盐浓度的增加,机械强度恶化是不可避免的。因此,近年来关于PIS SPEs的研究集中在引入刚性结构来改善聚合物电解质的机械性能。交联结构设计[70]、引入刚性支撑膜[71]、聚合物共混[72]等策略都已被提出用于补偿高盐浓度下机械强度的损失。
除了SPEs中总离子电导率外,由锂离子贡献的占比(即锂离子迁移数)也是开发高性能电解质的另一个重要考量标准[73-75]。无论是SIP SPEs还是PIS SPEs电解质,其中Li+与聚合物链段上Lewis碱性位点之间存在高度耦合的强配位关系会阻碍锂离子运动,导致阴离子的移动速度比Li+快约4倍[76],表现为低的锂离子迁移数(~0.2)[77, 78]。在电池中,阴离子在外加电场的作用下沿着与Li+相反的方向移动并在电极附近聚集。然而,在电极界面上没有发生与阴离子相关的可逆电化学反应,所以阴离子积聚会造成电池内部的浓度梯度,从而导致在电极/电解质界面处存在浓差极化和副反应,这意味着电池难以获得出色的循环性能[79]。为了限制SPEs中阴离子的迁移,单离子传导型聚合物电解质(SIPEs)采用了共价键合等策略将阴离子固定于聚合物骨架[80],从而使Li+成为电解质中唯一载流子,有利于减小界面处的浓差极化。此外,根据Chazlviel模型所预测的,高锂离子迁移数将有助于延缓枝晶生长[81]。因此,SIPEs为具有高安全性、快速充放电能力和高能量密度的下一代电池带来了巨大希望。在SIPEs中,分子动力学模拟表明2种离子传输模式是可能的:(1)通过与聚合物链段运动相关的离子对重排进行迁移,如图 5(a)~5(b)所示(与vehicular机制类似);(2)通过离子聚集体网络直接跳跃迁移,如图 5(c)~图 5(d)所示(与离子跳跃机制类似)[82, 83]。
在这2种情况下,Li+不会被聚合物基体溶剂化,而是在运输过程中与阴离子基团配位,在各个配位点之间可以实现Li+的跳跃过程,阴离子的运动可以被极大地抑制,因此实现较高的锂离子迁移数(接近1)。高的锂离子迁移数意味着SIPEs的总电流主要由Li+转移贡献,但锂离子不易解离,导致其离子电导率很低(10-6 S ·cm-1,60 ℃)[80]。基于上述SIPEs离子传导机制,我们可以将促进其离子传导的策略归为2类:(1)加速聚合物链段动力学;(2)削弱聚合物链段上阴离子基团与锂离子的结合力。第1类方法与DIPEs中降低聚合物玻璃化转变温度(Tg)的本质相同,因而添加填料、增塑剂、聚合物共混和交联等策略也适用于SIPEs。
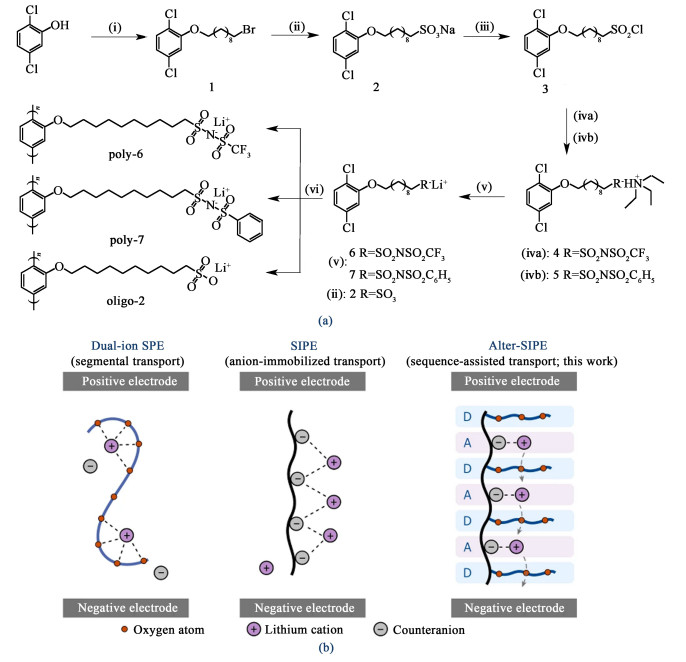
Wang等[84]以聚(乙二醇)二丙烯酸酯(PEGDA)、对苯乙烯磺酸锂(SSLi)和聚(乙二醇)甲基丙烯酸酯(PEGMEMA)共聚制备得到具有3D交联网络的SIPE,其中SIPE交联度越高,越有利于抑制聚合物结晶,聚合物链段运动越自由,离子电导率越高。He等[85]将低相对分子质量聚环氧乙烷(PEG250)作为增塑剂加入SIPE中,SIPE玻璃化转变温度(Tg)从8.3显著降低至-77.2 ℃,有效地促进了聚合物链段运动,降低了离子迁移活化能,从而表现为较高的离子电导率:30 ℃时为7.4×10-5 S ·cm-1。但是第1类策略侧重在改善聚合物主链段运动动力学,由此改进的离子传导性对于大多数在室温下工作的电池来说仍有其局限性。而第2类方法是一种更直观的策略,比如通过对侧链上的各种阴离子基团(如羧酸根、磺酸根、磺酰亚胺和硼酸根阴离子)修饰或改性从而将离子传输与主链段运动动力学分离。如图 6(a)所示,Liu等[86]合成了3种对聚苯基侧链聚合物电解质oligo-2、poly-6和poly-7,侧链上分别为3种对Li+具有不同的结合力的悬挂阴离子基团(—SO3-、—TFSI-和—PSI-)。通过介电弛豫分析和理论分析表明了poly-6和poly-7为侧链链段弛豫主导的锂离子迁移机制,与主链段运动动力学分离。与之前报道的聚(对苯乙烯磺酰)(三氟甲基磺酰)亚胺锂(LiPSTFSI)相比,相同TFSI-但侧链长度更长的poly-6电解质表现为至少高3个数量级的电导率(150 ℃时为6.7×10-6 S ·cm-1,改性前为1.2×10-10 S ·cm-1)。然而这种策略下的离子电导率仍低于DIPEs。最近Han等[87]设计了一种具有交替序列的固态氟化单离子聚合物电解质(alter-SIPE),来促进Li+传导。如图 6(b),alter-SIPE由周期性排列的阴离子和PEO侧链组成,这种特定的结构有利于电解质中Li+均匀分布、避免阴离子-锂离子团聚。密度函数理论(DFT)表明交替序列结构中Li+和聚合物之间结合能(-7.9 eV)比随机/嵌段(-8.5 eV)和均聚型SIPE(-8.9 eV)都低,证明了调节聚合物序列能有效促进Li+与聚合物链段上的阴离子基团解离。得益于交替序列结构的上述优势,alter-SIPE在30 ℃时离子电导率达到约4.0×10-5 S ·cm-1和锂离子迁移数为0.93。
|
| 图 6 (a) 含不同阴离子基团(—SO3-、—TFSI-和—PSI-)单体及其相应聚合物(分别为oligo-2、poly-6和poly-7)的合成路线[86]; (b)不同聚合物电解质体系中电池充电过程中Li+迁移模式[87] Fig.6 (a) Synthesis routes of monomers with different anionic groups(—SO3-、—TFSI-和—PSI-) and their corresponding polymers (oligo-2, poly-6 and poly-7, respectively)[86]; (b) Illustration of Li+ transport patterns during battery charging in different polymer electrolyte systems[87] |
| |
这种对锂离子传导的局部微环境的设计策略可以实现更快离子传输且不会牺牲电解质的机械性能。同样的思路和策略可以进一步扩展到含离子基团型聚合物包括聚阴离子型,聚阳离子型(聚离子液体),聚两性离子型等材料,关于这类聚合物电解质的报道仍然很少,未来含离子基团型聚合物有望代替典型的中性聚醚/聚酯类聚合物,以调节离子-离子相互作用,从而实现与聚合物链段运动解耦的超离子传导体系。
3 锂离子传输性能的提升策略和展望基于上述不同类型SPEs的发展思路,我们不难得到所有这些提高锂离子传输性能策略可归纳为以下3种:(1)增强聚合物链段运动动力学;(2)设计弱配位电解质;(3)高分子结构设计。本节重在介绍近几年关于促进离子传输性能提升的研究和思考。
3.1 增强聚合物链段运动动力学增强聚合物电解质链段运动动力学常用方法有添加有机增塑剂、离子液体、无机填料或低相对分子质量的聚合物形成多组分的电解质。过去的大多数研究表明:(1)在聚合物基体中添加有机增塑剂能有效降低离子迁移活化能,但是溶剂会导致电解质泄漏、易燃性、电化学稳定性差和机械性能下降;(2)加入高热稳定性离子液体也可以削弱聚合物链段的相互作用,促进聚合物链段的移动和锂盐的解离,但机械性能也会变差;(3)与以上情况相反,使用低相对分子质量的聚合物既可以提高热稳定性和机械强度,同时也可以通过降低聚合物基体的结晶度来提高离子电导率。比如Lu等[88]为了在不牺牲锂离子选择性的情况下提高SIPEs的链段的流动性,选择采用低相对分子质量的聚两性离子3-(1-甲基-3-咪唑基)丙磺酸盐(MIPS)和聚两性离子聚-3-(1-乙烯基-3-咪唑基)丙磺酸盐(VIPS)作为锂盐解离加速器和增塑剂来提高2种SIPEs的离子传导性,两性离子独特的偶极结构与SIPEs的聚合物框架中的阴离子基团具有的强相互作用可以软化聚合物链段,并且聚两性离子与PEO共混能够有效降低结晶度,在无任何有机溶剂的条件下,电解质在90 ℃表现出高达8.39×10-5 S ·cm-1离子电导率和接近1的高锂离子迁移数。在这种策略中,聚合物基质和聚合物添加剂之间的强相互作用会增强机械性能,但也有可能导致离子电导率下降。因此,在制备共混聚合物电解质时,应仔细考虑混合聚合物的相容性和聚合物之间的相互作用。此外添加无机填料也能降低聚合物的Tg,后来人们期望添加的填料不仅可以充当增塑剂,还可以在SPEs中传输锂离子,比如LLZO[47]、石榴石[89]、NASICON[90]等可用作功能性填料,然而大量研究结果证实,只有当这些填料能够形成连续的传输通道时才能有效地促进整体锂离子传导[91, 92]。在最近的研究中,研究人员试图开发一些低成本、功能性更多的填料来提高聚合物中的离子传导。Li等[93]将氟化石墨(CFx)n作为填料引入PEO-LiTFSI基体中,(CFx)n上大量的氟离子与Li+发生强烈的相互作用,一方面提高聚合物电解质中游离的锂离子的比例,另一方面大量的氟离子促使电解质获得更高的电化学稳定性,含10%氟化石墨的复合固态电解质(SPE-10CF)在45 ℃时离子电导率高达4.8×10-4 S ·cm-1。Yuan等[94]将兼具铁电性和离子传导性的多功能填料LiTaO3与聚偏氟乙烯基聚合物电解质复合,通过溶液浇铸法制备了复合固态电解质P-LTO15。与粒径相似的非铁电性填料SiO2相比(仅仅通过提升聚合物链的非晶相区域来提高离子传输性能),LiTaO3具有强的铁电响应,极化时可以产生均匀的电场,可以削弱聚合物/陶瓷之间的空间电荷层促进锂离子的跨界面传输;同时离子导体LiTaO3能提供更多的Li+传输通道。得益于以上优势,构建的P-LTO15复合固态电解质在室温下的离子电导率和锂离子迁移数分别达到4.90×10-4 S ·cm-1和0.45,有效提高了复合固态电解质的离子传输并调控界面处的锂沉积,实现了室温下固态锂金属电池的高性能运行。
如上所述,每种策略都有其自身的优点和缺点。未来的研究可能会通过2种或多种方法的组合将进一步提高离子电导率或其他性能,又或者引入的某种成分能够同时发挥多种功能,从而基于协同效应促进聚合物电解质在固态电池中的可行应用。
3.2 弱配位电解质的设计当增强聚合物链段运动动力学不能完全实现所需的Li+电导率和迁移数时,提高体系中自由的锂离子浓度、引入松散配位的重复单元和调节Li+与不同种类的离子偶极之间的相互作用形成竞争配位等策略用于设计弱配位电解质有望实现电解质中Li+传导与聚合物链段的弛豫解耦。Wen等[95]报道了一种高性能聚合物电解质,该电解质通过调节锂离子和聚合物链之间的相互作用实现快速离子传导。具体来说,丁二腈(SN)和锂离子(
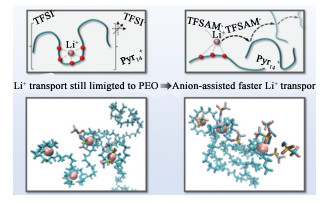
此外,近年来大量的研究工作引入阴离子作为添加剂形成弱配位电解质。Hoffknecht等[98]在体系中引入其他盐阴离子基团三氟甲磺酰-N-氰胺(TFSAM),如图 7所示,TFSAM与Li+相互作用能够与PEO形成竞争配位,这样可以为Li+提供额外的传导途径,在基于PEO的三元固态聚合物电解质TSPEs中,TFSAM极大地加速了Li+的传输(使锂离子迁移数增加了6倍,锂离子的电导率增加了2~3倍),分子动力学计算模拟显示,TFSAM不仅可以使锂离子从PEO聚合物骨架中脱离,还可以将它们重新偶联到阴离子上,促进锂离子更快地传输。类似地,Wang等[99]通过引入多种锂盐,双(三氟甲基磺酰基)亚胺锂LiTFSI和二氟(草酸)硼酸锂(LiDFOB)削弱了“Li+溶剂化”,阴离子和Li+浓度的增加能够削弱聚合物单体之间的静电排斥,使聚合物链段形成了暴露更多的锂离子结合位点的球形构象,改善了锂离子链间转移,有助于增强离子传输并稳定界面形态,60 ℃时离子电导率为1.78×10-4 S ·cm-1,锂离子迁移数为0.67。最近对盐阴离子的分子结构进行设计也引起了研究人员兴趣。Xia等[100]以LiTFSI为原料合成了一种不对称功能锂盐LiFEA,与传统的锂盐不同,LiFEA保留了LiTFSI中的1个强吸电子CF3SO2-基团且连接1个负电荷离域的氮原子, 并引入了具有给电子能力的醚骨架,可以捕获迁移的Li+,类似两性离子的结构。它具有较大的偶极矩和较高的给体数,作为添加剂可以提高碳酸基电解质的锂离子迁移数,高达0.78(1.0 mol ·L-1 LiFEA添加量)。
展望未来的发展,为了在弱配位电解质基础上进一步实现Li+传输与聚合物链段的弛豫解耦并解决阴离子迁移带来的浓差极化问题,有必要延续PIS SPEs和SIPEs设计思路,提高离子电导率的同时能提高阳离子选择性。用带电荷的聚盐(如聚阳离子、聚阴离子或聚两性离子)代替常见的中性聚醚/聚酯是个比较理想的选择,优势体现在以下2点:(1)锂离子在此类聚合物中传导机制类似离子跳跃机制,迁移活化能大大降低;(2)聚合物链段与阴离子中的离子-离子相互作用能有效限制阴离子的迁移。
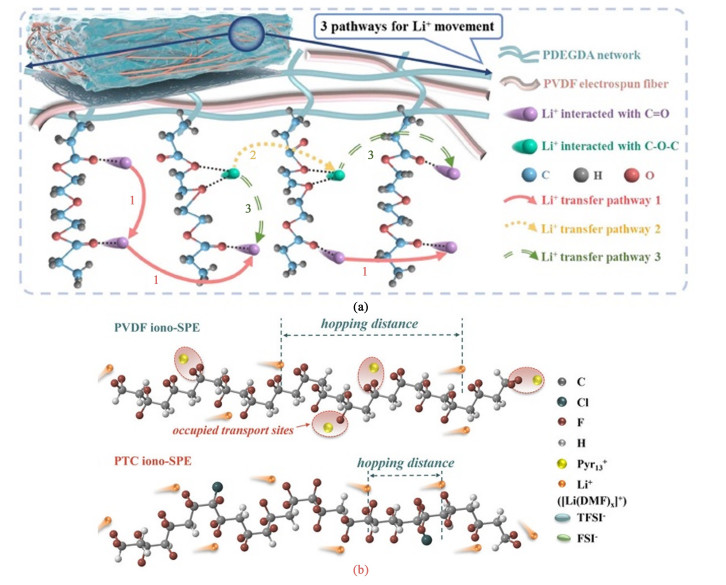
3.3 高分子结构设计无论是增强聚合物链段运动动力学还是弱配位电解质的设计均是通过引入其他添加材料来改善聚合物电解质的性能,这不得不考虑材料之间的相容性,以及多种材料共同构建的体系的复杂性。事实上,目前的各种策略离实现真正的Li+传输与聚合物链段的弛豫解耦还很远,因此对聚合物链段的高分子结构进行合理设计以促进锂离子传导仍具备巨大的研究价值。高分子结构设计原理的关键是引入特定的官能团来溶剂化Li+同时增强骨架与阴离子相互作用以增加锂离子迁移数。Zhang等[101]通过在准固态电解质构建了含叔胺官能团(NR3)的三维聚合物骨架,由于NR3基团与Li+配位强度高于酯溶剂的羰基(C=O)基团,因此Li+可以在聚合物的NR3上有序快速地扩散,从而将准固态电解质的离子电导率显著提高到3.69 mS ·cm-1。Xu等[102]利用2D-MOF中取代基的给电子效应有效地限制了ClO4-的移动,提高了PEO的力学性能和锂离子迁移数(0.36~0.64)。同时,官能团的增加构建了具有多重离子传输路径的电解质。Lin等[103]在聚偏氟乙烯骨架(PVDF FMs)中进行二甘醇二丙烯酸酯(DEGDA)的原位热引发聚合来制备复合聚合物电解质,其中含有2种偶极(C=O和C—O)并生成了3条传输路径,如图 8(a)所示,实现了1.41×10-4 S ·cm-1的高离子电导率和0.076 eV低能量势垒下的锂离子迁移。
|
| 图 8 (a) PDEGDA/PVDF FMs QSPEs中Li+的多重离子传输路径示意图[103]; (b) Li+在PVDF iono-SPE和PTC iono-SPE中沿分子链传输的示意图[104] Fig.8 (a)Schematic illustration of multiple transport pathways for Li+ in PDEGDA/PVDF FMs QSPEs[103]; (b) Schematic diagram of Li+ transport along molecular chains in PVDF iono-SPE and PTC iono-SPE[104] |
| |
此外对聚合物结构设计还能缩短相邻偶极子间的Li+跃迁距离。Liu等[104]报道了一种基于聚(偏氟乙烯-三氟乙烯-三氟氯乙烯)(P-(VDF-TrFE-CTFE),PTC)的聚合物电解质,如图 8(b)所示。PTC的介电常数(~40.2)明显高于PVDF(~11.7),有利于锂离子-阴离子团簇的解离,并在25 ℃时将PTC iono-SPE的离子电导率提高到5.75×10-4 S ·cm-1。具有局部极性结构的PTC对Pyr13+的吸附能较Li+低,这降低了Pyr13+占据Li+跳跃位点的可能性,并将Li+迁移活化能从PVDF iono-SPE的0.35 eV降低到PTC iono-SPE的0.25 eV。高介电常数和对Pyr13+的低吸附能的PTC结构有效提高了聚合物相中Li+的传输效率,缩小了离子液体与聚合物相之间的离子迁移差距。对聚合物结构设计除了实现良好的离子传输性能之外还能够促成电解质应用的多样性,比如自修复[105]、可折叠[106]、低温下工作能力[107, 108]。然而,锂离子的传导机制和迁移途径会随着聚合物结构的变化变得更复杂。这些体系中存在大量的相互作用,包括离子-偶极相互作用和偶极-偶极相互作用,很难用简单的模型来描述这一过程。因此,揭示Li+在不同高分子结构设计下的传导过程并开发新的模型来解释其传导机制是固态电池发展的另一个潜在方向。
4 结语聚合物基固体电解质被认为是固态电池最有前途的电解质,已被广泛研究。这些材料将取代液体电解质,以最大限度地减少电池中潜在的安全隐患,并能匹配高容量的电极材料以实现高能量密度。本论文综述了聚合物电解质中的离子传导机理,包括“salt-in-polymer”电解质、“polymer-in-salt”电解质和单离子传导电解质,讨论了相关的传导模型以深入了解离子传导机理。然而,各种策略设计下的聚合物基固态电解质的多样性和复杂性带来的离子传导机制仍比较模糊,未来研究的范围是巨大的。随着新型理论工具和先进表征技术的发展,有理由期待在聚合物基固体电解质中离子传导机制的理解方面取得重要突破。对于未来的发展,设计高性能聚合物基电解质不仅需要关注离子电导率和界面稳定性的优化,还需要设计具有特定结构的锂盐和聚合物,促使Li+传导与聚合物链的松弛解耦从而构建Li+的高选择性传输路径。固态聚合物电解质中的离子传导机理的研究可以为优化锂离子的传输性能提供指导,将进一步促进聚合物电解质在高安全性和高能量密度电池中的深入发展。
| [1] |
LEE M J, HAN J, LEE K, et al. Elastomeric electrolytes for high-energy solid-state lithium batteries[J]. Nature, 2022, 601(7892): 217-222. DOI:10.1038/s41586-021-04209-4 |
| [2] |
YE L, LI X. A dynamic stability design strategy for lithium metal solid state batteries[J]. Nature, 2021, 593(7858): 218-222. DOI:10.1038/s41586-021-03486-3 |
| [3] |
WU Y, WANG S, LI H, et al. Progress in thermal stability of all-solid-state-Li-ion-batteries[J]. InfoMat, 2021, 3(8): 827-853. DOI:10.1002/inf2.12224 |
| [4] |
CHANG Z, YANG H, ZHU X, et al. A stable quasi-solid electrolyte improves the safe operation of highly efficient lithium-metal pouch cells in harsh environments[J]. Nature Communications, 2022, 13(1): 1510. DOI:10.1038/s41467-022-29118-6 |
| [5] |
JANEK J, ZEIER W G. Challenges in speeding up solid-state battery development[J]. Nature Energy, 2023, 8: 230-240. DOI:10.1038/s41560-023-01208-9 |
| [6] |
HODGE I M, INGRAM M D, WEST A R. Impedance and modulus spectroscopy of polycrystalline solid electrolytes[J]. Journal of Electroanalytical Chemistry and Interfacial Electrochemistry, 1976, 74(2): 125-143. DOI:10.1016/S0022-0728(76)80229-X |
| [7] |
陈立坤, 胡懿, 马家宾, 等. Li+电池固态聚合物电解质研究进展[J]. 化学工业与工程, 2020, 37(1): 2-16. CHEN Likun, HU Yi, MA Jiabin, et al. Research progress of solid polymer electrolytes for lithium-ion batteries[J]. Chemical Industry and Engineering, 2020, 37(1): 2-16. DOI:10.13353/j.issn.1004.9533.20191908 (in Chinese) |
| [8] |
LIANG H, WANG L, WANG A, et al. Tailoring practically accessible polymer/inorganic composite electrolytes for all-solid-state lithium metal batteries: A review[J]. Nano-Micro Letters, 2023, 15(1): 42. DOI:10.1007/s40820-022-00996-1 |
| [9] |
HOU W, GUO X, SHEN X, et al. Solid electrolytes and interfaces in all-solid-state sodium batteries: Progress and perspective[J]. Nano Energy, 2018, 52: 279-291. DOI:10.1016/j.nanoen.2018.07.036 |
| [10] |
LIU M, ZHANG S, VAN ECK E R H, et al. Improving Li-ion interfacial transport in hybrid solid electrolytes[J]. Nature Nanotechnology, 2022, 17(9): 959-967. DOI:10.1038/s41565-022-01162-9 |
| [11] |
CHENG Z, LIU T, ZHAO B, et al. Recent advances in organic-inorganic composite solid electrolytes for all-solid-state lithium batteries[J]. Energy Storage Materials, 2021, 34: 388-416. DOI:10.1016/j.ensm.2020.09.016 |
| [12] |
LI J, CAI Y, WU H, et al. Polymers in lithium-ion and lithium metal batteries[J]. Advanced Energy Materials, 2021, 11(15): 2003239. DOI:10.1002/aenm.202003239 |
| [13] |
DING P, LIN Z, GUO X, et al. Polymer electrolytes and interfaces in solid-state lithium metal batteries[J]. Materials Today, 2021, 51: 449-474. DOI:10.1016/j.mattod.2021.08.005 |
| [14] |
刁庆宇, 刘吉源, 王列, 等. 固态电解质离子传输机制研究进展[J]. 化学工业与工程, 2024, 41(1): 71-82. DIAO Qingyu, LIU Jiyuan, WANG Lie, et al. Research progress on ion transport mechanism in solid-state electrolytes[J]. Chemical Industry and Engineering, 2024, 41(1): 71-82. DOI:10.13353/j.issn.1004.9533.20220352 (in Chinese) |
| [15] |
WU D, CHEN L, LI H, et al. Solid-state lithium batteries-from fundamental research to industrial progress[J]. Progress in Materials Science, 2023, 139: 101182. DOI:10.1016/j.pmatsci.2023.101182 |
| [16] |
ZHANG Z, CHEN H, HU Z, et al. Ion conduction path in composite solid electrolytes for lithium metal batteries: From polymer rich to ceramic rich[J]. Frontiers in Energy, 2022, 16(5): 706-733. DOI:10.1007/s11708-022-0833-9 |
| [17] |
FENTON D E, PARKER J M, WRIGHT P V. Complexes of alkali metal ions with poly(ethylene oxide)[J]. Polymer, 1973, 14(11): 589. |
| [18] |
ARMAND M B, CHABAGNO J M, DUCLOT M J. Fast ion transport in solids[J]. Electrodes and Electrolytes, 1979, 131: 2944-2955. |
| [19] |
SONG Z, CHEN F, MARTINEZ-IBAÑEZ M, et al. A reflection on polymer electrolytes for solid-state lithium metal batteries[J]. Nature Communications, 2023, 14(1): 4884. DOI:10.1038/s41467-023-40609-y |
| [20] |
DIDDENS D, HEUER A, BORODIN O. Understanding the lithium transport within a rouse-based model for a PEO/LiTFSI polymer electrolyte[J]. Macromolecules, 2010, 43(4): 2028-2036. DOI:10.1021/ma901893h |
| [21] |
SETHURAMAN V, MOGURAMPELLY S, GANESAN V. Ion transport mechanisms in lamellar phases of salt-doped PS-PEO block copolymer electrolytes[J]. Soft Matter, 2017, 13(42): 7793-7803. DOI:10.1039/C7SM01345K |
| [22] |
SETHURAMAN V, MOGURAMPELLY S, GANESAN V. Multiscale simulations of lamellar PS-PEO block copolymers doped with LiPF6 ions[J]. Macromolecules, 2017, 50(11): 4542-4554. DOI:10.1021/acs.macromol.7b00125 |
| [23] |
BORODIN O, SMITH G D. Molecular dynamics simulations of poly(ethylene oxide)/LiI melts. 1. Structural and conformational properties[J]. Macromolecules, 1998, 31(23): 8396-8406. DOI:10.1021/ma980838v |
| [24] |
ZHANG D, MENG X, HOU W, et al. Solid polymer electrolytes: Ion conduction mechanisms and enhancement strategies[J]. Nano Research Energy, 2023, 2: e9120050. DOI:10.26599/NRE.2023.9120050 |
| [25] |
STAUNTON E, ANDREEV Y G, BRUCE P G. Structure and conductivity of the crystalline polymer electrolyte β-PEO6: LiAsF6[J]. Journal of the American Chemical Society, 2005, 127(35): 12176-12177. DOI:10.1021/ja053249v |
| [26] |
STOEVA Z, MARTIN-LITAS I, STAUNTON E, et al. Ionic conductivity in the crystalline polymer electrolytes PEO6: LiXF6, X=P, As, Sb[J]. Journal of the American Chemical Society, 2003, 125(15): 4619-4626. DOI:10.1021/ja029326t |
| [27] |
LIGHTFOOT P, MEHTA M A, BRUCE P G. Crystal structure of the polymer electrolyte poly(ethylene oxide)3: LiCF3SO3[J]. Science, 1993, 262(5135): 883-885. DOI:10.1126/science.262.5135.883 |
| [28] |
MARZANTOWICZ M, DYGAS J R, KROK F, et al. In situ microscope and impedance study of polymer electrolytes[J]. Electrochimica Acta, 2006, 51(8/9): 1713-1727. |
| [29] |
GOLODNITSKY D, STRAUSS E, PELED E, et al. Review—On order and disorder in polymer electrolytes[J]. Journal of the Electrochemical Society, 2015, 162(14): A2551-A2566. DOI:10.1149/2.0161514jes |
| [30] |
DEVAUX D, BOUCHET R, GLÉ D, et al. Mechanism of ion transport in PEO/LiTFSI complexes: Effect of temperature, molecular weight and end groups[J]. Solid State Ionics, 2012, 227: 119-127. DOI:10.1016/j.ssi.2012.09.020 |
| [31] |
ORÄDD G, EDMAN L, FERRY A. Diffusion: A comparison between liquid and solid polymer LiTFSI electrolytes[J]. Solid State Ionics, 2002, 152: 131-136. |
| [32] |
ZARDALIDIS G, IOANNOU E, PISPAS S, et al. Relating structure, viscoelasticity, and local mobility to conductivity in PEO/LiTf electrolytes[J]. Macromolecules, 2013, 46(7): 2705-2714. DOI:10.1021/ma400266w |
| [33] |
XUE Z, HE D, XIE X. Poly(ethylene oxide)-based electrolytes for lithium-ion batteries[J]. Journal of Materials Chemistry A, 2015, 3(38): 19218-19253. DOI:10.1039/C5TA03471J |
| [34] |
RATNER M A, SHRIVER D F. Ion transport in solvent-free polymers[J]. Chemical Reviews, 1988, 88(1): 109-124. DOI:10.1021/cr00083a006 |
| [35] |
ROBITAILLE C D, FAUTEUX D. Phase diagrams and conductivity characterization of some PEO-LiX electrolytes[J]. Journal of the Electrochemical Society, 1986, 133(2): 315-325. DOI:10.1149/1.2108569 |
| [36] |
BALLARD D G H, CHESHIRE P, MANN T S, et al. Ionic conductivity in organic solids derived from amorphous macromolecules[J]. Macromolecules, 1990, 23(5): 1256-1264. DOI:10.1021/ma00207a006 |
| [37] |
GAUTHIER M, FAUTEUX D, VASSORT G, et al. Behavior of polymer electrolyte batteries at 80~100 ℃ and near room temperature[J]. Journal of Power Sources, 1985, 14(1/2/3): 23-26. |
| [38] |
CHIODELLI G. Ionic conduction and thermal properties of poly (ethylene oxide)-lithium tetrafluoroborate films[J]. Solid State Ionics, 1988, 28/29/30: 1009-1013. |
| [39] |
FRECH R, CHINTAPALLI S, BRUCE P G, et al. Crystalline and Amorphous Phases in the Poly(ethylene oxide)-LiCF3SO3 System[J]. Macromolecules, 1999, 32(3): 808-813. DOI:10.1021/ma9812682 |
| [40] |
VALLÉE A, BESNER S, PRUD'HOMME J. Comparative study of poly(ethylene oxide) electrolytes made with LiN(CF3SO2)2, LiCF3SO3 and LiClO4: Thermal properties and conductivity behaviour[J]. Electrochimica Acta, 1992, 37(9): 1579-1583. DOI:10.1016/0013-4686(92)80115-3 |
| [41] |
TAN S, YUE J, TIAN Y, et al. In-situ encapsulating flame-retardant phosphate into robust polymer matrix for safe and stable quasi-solid-state lithium metal batteries[J]. Energy Storage Materials, 2021, 39: 186-193. DOI:10.1016/j.ensm.2021.04.020 |
| [42] |
DONG T, ZHANG J, XU G, et al. A multifunctional polymer electrolyte enables ultra-long cycle-life in a high-voltage lithium metal battery[J]. Energy & Environmental Science, 2018, 11(5): 1197-1203. |
| [43] |
QIAO L, RODRIGUEZ PEÑA S, MARTÍNEZ-IBAÑEZ M, et al. Anion π-π stacking for improved lithium transport in polymer electrolytes[J]. Journal of the American Chemical Society, 2022, 144(22): 9806-9816. DOI:10.1021/jacs.2c02260 |
| [44] |
CROCE F, APPETECCHI G B, PERSI L, et al. Nanocomposite polymer electrolytes for lithium batteries[J]. Nature, 1998, 394: 456-458. DOI:10.1038/28818 |
| [45] |
ZHOU Q, MA J, DONG S, et al. Intermolecular chemistry in solid polymer electrolytes for high-energy-density lithium batteries[J]. Advanced Materials, 2019, 31(50): e1902029. DOI:10.1002/adma.201902029 |
| [46] |
CHEN L, LI Y, LI S, et al. PEO/garnet composite electrolytes for solid-state lithium batteries: From "ceramic-in-polymer" to "polymer-in-ceramic"[J]. Nano Energy, 2018, 46: 176-184. DOI:10.1016/j.nanoen.2017.12.037 |
| [47] |
LI Z, HUANG H, ZHU J, et al. Ionic conduction in composite polymer electrolytes: Case of PEO: Ga-LLZO composites[J]. ACS Applied Materials & Interfaces, 2019, 11(1): 784-791. |
| [48] |
YANG X, LIU J, PEI N, et al. The critical role of fillers in composite polymer electrolytes for lithium battery[J]. Nano-Micro Letters, 2023, 15(1): 74. DOI:10.1007/s40820-023-01051-3 |
| [49] |
ZHAO T, ZHENG X, WANG D, et al. A quasi-solid-state polyether electrolyte for low-temperature sodium metal batteries[J]. Advanced Functional Materials, 2023, 33(48): 2304928. DOI:10.1002/adfm.202304928 |
| [50] |
YANG H, LIU Z, WANG Y, et al. Multiscale structural gel polymer electrolytes with fast Li+ transport for long-life Li metal batteries[J]. Advanced Functional Materials, 2023, 33(1): 2209837. DOI:10.1002/adfm.202209837 |
| [51] |
ZHANG F, SUN Y, WANG Z, et al. Highly conductive polymeric ionic liquid electrolytes for ambient-temperature solid-state lithium batteries[J]. ACS Applied Materials & Interfaces, 2020, 12(21): 23774-23780. |
| [52] |
YUE Y, ZHENG B, NI J, et al. All-polymer solar cells with 17% efficiency enabled by the "end-capped" ternary strategy[J]. Advanced Science, 2022, 9(32): e2204030. DOI:10.1002/advs.202204030 |
| [53] |
ZHANG Y, WANG Z, PAN Y, et al. Tailoring a multi-system adaptable gel polymer electrolyte for the realization of carbonate ester and ether-based Li-SPAN batteries[J]. Energy & Environmental Science, 2024, 17(7): 2576-2587. |
| [54] |
LU X, WANG Y, XU X, et al. Polymer-based solid-state electrolytes for high-energy-density lithium-ion batteries-review[J]. Advanced Energy Materials, 2023, 13(38): 2301746. DOI:10.1002/aenm.202301746 |
| [55] |
ZHAO Y, BAI Y, LI W, et al. Design strategies for polymer electrolytes with ether and carbonate groups for solid-state lithium metal batteries[J]. Chemistry of Materials, 2020, 32(16): 6811-6830. DOI:10.1021/acs.chemmater.9b04521 |
| [56] |
TOMINAGA Y. Ion-conductive polymer electrolytes based on poly(ethylene carbonate) and its derivatives[J]. Polymer Journal, 2017, 49(3): 291-299. DOI:10.1038/pj.2016.115 |
| [57] |
MACKANIC D G, MICHAELS W, LEE M, et al. Crosslinked poly(tetrahydrofuran) as a loosely coordinating polymer electrolyte[J]. Advanced Energy Materials, 2018, 8(25): 1800703. DOI:10.1002/aenm.201800703 |
| [58] |
SÅNGELAND C, YOUNESI R, MINDEMARK J, et al. Towards room temperature operation of all-solid-state Na-ion batteries through polyester-polycarbonate-based polymer electrolytes[J]. Energy Storage Materials, 2019, 19: 31-38. DOI:10.1016/j.ensm.2019.03.022 |
| [59] |
WEBB M A, JUNG Y, PESKO D M, et al. Systematic computational and experimental investigation of lithium-ion transport mechanisms in polyester-based polymer electrolytes[J]. ACS Central Science, 2015, 1(4): 198-205. DOI:10.1021/acscentsci.5b00195 |
| [60] |
ANGELL C A, LIU C, SANCHEZ E. Rubbery solid electrolytes with dominant cationic transport and high ambient conductivity[J]. Nature, 1993, 362: 137-139. DOI:10.1038/362137a0 |
| [61] |
MANUEL STEPHAN A. Review on gel polymer electrolytes for lithium batteries[J]. European Polymer Journal, 2006, 42(1): 21-42. DOI:10.1016/j.eurpolymj.2005.09.017 |
| [62] |
TONG B, SONG Z, WU H, et al. Ion transport and structural design of lithium-ion conductive solid polymer electrolytes: A perspective[J]. Materials Futures, 2022, 1(4): 042103. DOI:10.1088/2752-5724/ac9e6b |
| [63] |
ANGELL C A. Mobile ions in amorphous solids[J]. Annual Review of Physical Chemistry, 1992, 43: 693-717. DOI:10.1146/annurev.pc.43.100192.003401 |
| [64] |
FORSYTH M, SUN J, MACFARLANE D R, et al. Compositional dependence of free volume in PAN/LiCF3SO3 polymer-in-salt electrolytes and the effect on ionic conductivity[J]. Journal of Polymer Science Part B: Polymer Physics, 2000, 38(2): 341-350. DOI:10.1002/(SICI)1099-0488(20000115)38:2<341::AID-POLB6>3.0.CO;2-S |
| [65] |
ANGELL C A. Concepts and conflicts in polymer electrolytes: The search for ion mobility[J]. Electrochimica Acta, 2019, 313: 205-210. DOI:10.1016/j.electacta.2019.03.193 |
| [66] |
CHENG S, SMITH D M, LI C. How does nanoscale crystalline structure affect ion transport in solid polymer electrolytes?[J]. Macromolecules, 2014, 47(12): 3978-3986. DOI:10.1021/ma500734q |
| [67] |
LI Z, FU J, ZHOU X, et al. Ionic conduction in polymer-based solid electrolytes[J]. Advanced Science, 2023, 10(10): e2201718. DOI:10.1002/advs.202201718 |
| [68] |
GAO H, GRUNDISH N S, ZHAO Y, et al. Formation of stable interphase of polymer-in-salt electrolyte in all-solid-state lithium batteries[J]. Energy Material Advances, 2020, 2020: 1932952. |
| [69] |
AZIZ S B, WOO T J, KADIR M F Z, et al. A conceptual review on polymer electrolytes and ion transport models[J]. Journal of Science: Advanced Materials and Devices, 2018, 3(1): 1-17. DOI:10.1016/j.jsamd.2018.01.002 |
| [70] |
YANG J, LI R, ZHANG P, et al. Crosslinked polymer-in-salt solid electrolyte with multiple ion transport paths for solid-state lithium metal batteries[J]. Energy Storage Materials, 2024, 64: 103088. DOI:10.1016/j.ensm.2023.103088 |
| [71] |
HE Z, FAN L. Poly(ethylene carbonate)-based electrolytes with high concentration Li salt for all-solid-state lithium batteries[J]. Rare Metals, 2018, 37(6): 488-496. DOI:10.1007/s12598-018-1017-y |
| [72] |
ZHANG W, KOVERGA V, LIU S, et al. Single-phase local-high-concentration solid polymer electrolytes for lithium-metal batteries[J]. Nature Energy, 2024, 9: 386-400. DOI:10.1038/s41560-023-01443-0 |
| [73] |
DIEDERICHSEN K M, MCSHANE E J, MCCLOSKEY B D. Promising routes to a high Li+ transference number electrolyte for lithium ion batteries[J]. ACS Energy Letters, 2017, 2(11): 2563-2575. DOI:10.1021/acsenergylett.7b00792 |
| [74] |
MA Q, ZHANG H, ZHOU C, et al. Single lithium-ion conducting polymer electrolytes based on a super-delocalized polyanion[J]. Angewandte Chemie (International Ed), 2016, 55(7): 2521-2525. DOI:10.1002/anie.201509299 |
| [75] |
FONG K D, SELF J, DIEDERICHSEN K M, et al. Ion transport and the true transference number in nonaqueous polyelectrolyte solutions for lithium ion batteries[J]. ACS Central Science, 2019, 5(7): 1250-1260. DOI:10.1021/acscentsci.9b00406 |
| [76] |
SAVOIE B M, WEBB M A, MILLER T F. Enhancing cation diffusion and suppressing anion diffusion via lewis-acidic polymer electrolytes[J]. The Journal of Physical Chemistry Letters, 2017, 8(3): 641-646. DOI:10.1021/acs.jpclett.6b02662 |
| [77] |
BOUCHET R, MARIA S, MEZIANE R, et al. Single-ion BAB triblock copolymers as highly efficient electrolytes for lithium-metal batteries[J]. Nature Materials, 2013, 12(5): 452-457. DOI:10.1038/nmat3602 |
| [78] |
GAO J, WANG C, HAN D, et al. Single-ion conducting polymer electrolytes as a key jigsaw piece for next-generation battery applications[J]. Chemical Science, 2021, 12(40): 13248-13272. DOI:10.1039/D1SC04023E |
| [79] |
DOYLE M, FULLER T F, NEWMAN J. The importance of the lithium ion transference number in lithium/polymer cells[J]. Electrochimica Acta, 1994, 39(13): 2073-2081. DOI:10.1016/0013-4686(94)85091-7 |
| [80] |
ZHANG H, LI C, PISZCZ M, et al. Single lithium-ion conducting solid polymer electrolytes: Advances and perspectives[J]. Chemical Society Reviews, 2017, 46(3): 797-815. DOI:10.1039/C6CS00491A |
| [81] |
CHAZALVIEL J. Electrochemical aspects of the generation of ramified metallic electrodeposits[J]. Physical Review A, Atomic, Molecular, and Optical Physics, 1990, 42(12): 7355-7367. DOI:10.1103/PhysRevA.42.7355 |
| [82] |
BOLINTINEANU D S, STEVENS M J, FRISCHKNECHT A L. Atomistic simulations predict a surprising variety of morphologies in precise ionomers[J]. ACS Macro Letters, 2013, 2(3): 206-210. DOI:10.1021/mz300611n |
| [83] |
HALL L M, STEVENS M J, FRISCHKNECHT A L. Dynamics of model ionomer melts of various architectures[J]. Macromolecules, 2012, 45(19): 8097-8108. DOI:10.1021/ma301308n |
| [84] |
WANG Y, SUN Q, ZOU J, et al. Simultaneous high ionic conductivity and lithium-ion transference number in single-ion conductor network polymer enabling fast-charging solid-state lithium battery[J]. Small, 2023, 19(43): 2303344. DOI:10.1002/smll.202303344 |
| [85] |
HE D, WANG D, ZOU D, et al. Anion-tethered single lithium-ion conducting polyelectrolytes through UV-induced free radical polymerization for improved morphological stability of lithium metal anodes[J]. Angewandte Chemie, 2023, 135(38): e202308309. DOI:10.1002/ange.202308309 |
| [86] |
LIU J, PICKETT P D, PARK B, et al. Non-solvating, side-chain polymer electrolytes as lithium single-ion conductors: Synthesis and ion transport characterization[J]. Polymer Chemistry, 2020, 11(2): 461-471. DOI:10.1039/C9PY01035A |
| [87] |
HAN S, WEN P, WANG H, et al. Sequencing polymers to enable solid-state lithium batteries[J]. Nature Materials, 2023, 22(12): 1515-1522. DOI:10.1038/s41563-023-01693-z |
| [88] |
LU F, LI G, YU Y, et al. Zwitterionic impetus on single lithium-ion conduction in solid polymer electrolyte for all-solid-state lithium-ion batteries[J]. Chemical Engineering Journal, 2020, 384: 123237. DOI:10.1016/j.cej.2019.123237 |
| [89] |
HU J, HE P, ZHANG B, et al. Porous film host-derived 3D composite polymer electrolyte for high-voltage solid state lithium batteries[J]. Energy Storage Materials, 2020, 26: 283-289. DOI:10.1016/j.ensm.2020.01.006 |
| [90] |
WU N, CHIEN P H, LI Y, et al. Fast Li+ conduction mechanism and interfacial chemistry of a NASICON/polymer composite electrolyte[J]. Journal of the American Chemical Society, 2020, 142(5): 2497-2505. DOI:10.1021/jacs.9b12233 |
| [91] |
BAE J, LI Y, ZHANG J, et al. A 3D nanostructured hydrogel-framework-derived high-performance composite polymer lithium-ion electrolyte[J]. Angewandte Chemie, 2018, 130(8): 2118-2122. DOI:10.1002/ange.201710841 |
| [92] |
CHEN H, ADEKOYA D, HENCZ L, et al. Stable seamless interfaces and rapid ionic conductivity of Ca-CeO2/LiTFSI/PEO composite electrolyte for high-rate and high-voltage all-solid-state battery[J]. Advanced Energy Materials, 2020, 10(21): 2000049. DOI:10.1002/aenm.202000049 |
| [93] |
LI Q, WANG X, ZHU S, et al. Fast Li-ion conduction enabled by graphite fluoride flakes in solid polymer electrolyte[J]. Rare Metals, 2023, 42(10): 3337-3344. DOI:10.1007/s12598-023-02375-0 |
| [94] |
YUAN Y, CHEN L, LI Y, et al. Functional LiTaO3 filler with tandem conductivity and ferroelectricity for PVDF-based composite solid-state electrolyte[J]. Energy Materials and Devices, 2023, 1(1): 9370004. DOI:10.26599/EMD.2023.9370004 |
| [95] |
WEN K, XIN C, GUAN S, et al. Ion-dipole interaction regulation enables high-performance single-ion polymer conductors for solid-state batteries[J]. Advanced Materials, 2022, 34(32): e2202143. DOI:10.1002/adma.202202143 |
| [96] |
PENG H, LONG T, PENG J, et al. Molecular design for in-situ polymerized solid polymer electrolytes enabling stable cycling of lithium metal batteries[J]. Advanced Energy Materials, 2024, 14(22): 2400428. DOI:10.1002/aenm.202400428 |
| [97] |
YU X, ZHAO L, LI Y, et al. Weakening ionic coordination for high ionic conductivity composite solid electrolytes[J]. ACS Energy Letters, 2024, 9(5): 2109-2115. DOI:10.1021/acsenergylett.4c00636 |
| [98] |
HOFFKNECHT J P, WETTSTEIN A, ATIK J, et al. Coordinating anions "to the rescue" of the lithium ion mobility in ternary solid polymer electrolytes plasticized with ionic liquids[J]. Advanced Energy Materials, 2023, 13(1): 2202789. DOI:10.1002/aenm.202202789 |
| [99] |
WANG C, ZHAO X, LI D, et al. Anion-modulated ion conductor with chain conformational transformation for stabilizing interfacial phase of high-voltage lithium metal batteries[J]. Angewandte Chemie (International Ed), 2024, 63(19): e202317856. DOI:10.1002/anie.202317856 |
| [100] |
XIA Y, ZHOU P, KONG X, et al. Designing an asymmetric ether-like lithium salt to enable fast-cycling high-energy lithium metal batteries[J]. Nature Energy, 2023, 8: 934-945. DOI:10.1038/s41560-023-01282-z |
| [101] |
ZHANG Q, LIU Z, SONG X, et al. Ordered and fast ion transport of quasi-solid-state electrolyte with regulated coordination strength for lithium metal batteries[J]. Angewandte Chemie (International Ed), 2023, 62(30): e202302559. DOI:10.1002/anie.202302559 |
| [102] |
XU L, XIAO X, TU H, et al. Engineering functionalized 2D metal-organic frameworks nanosheets with fast Li+ conduction for advanced solid Li batteries[J]. Advanced Materials, 2023, 35(38): e2303193. DOI:10.1002/adma.202303193 |
| [103] |
LIN W, ZHENG X, MA S, et al. Quasi-solid polymer electrolyte with multiple lithium-ion transport pathways by in situ thermal-initiating polymerization[J]. ACS Applied Materials & Interfaces, 2023, 15(6): 8128-8137. |
| [104] |
LIU J, WU Z, STADLER F J, et al. High dielectric poly(vinylidene fluoride)-based polymer enables uniform lithium-ion transport in solid-state ionogel electrolytes[J]. Angewandte Chemie International Edition, 2023, 62(26): e202300243. DOI:10.1002/anie.202300243 |
| [105] |
CHEN K, SUN Y, ZHANG X, et al. A self-healing and nonflammable cross-linked network polymer electrolyte with the combination of hydrogen bonds and dynamic disulfide bonds for lithium metal batteries[J]. Energy & Environmental Materials, 2023, 6(4): e12568. |
| [106] |
GUO D, SHINDE D B, SHIN W, et al. Foldable solid-state batteries enabled by electrolyte mediation in covalent organic frameworks[J]. Advanced Materials, 2022, 34(23): e2201410. DOI:10.1002/adma.202201410 |
| [107] |
LIN Z, GUO X, WANG Z, et al. A wide-temperature superior ionic conductive polymer electrolyte for lithium metal battery[J]. Nano Energy, 2020, 73: 104786. DOI:10.1016/j.nanoen.2020.104786 |
| [108] |
HUANG X, HUANG S, WANG T, et al. Polyether-b-amide based solid electrolytes with well-adhered interface and fast kinetics for ultralow temperature solid-state lithium metal batteries[J]. Advanced Functional Materials, 2023, 33(27): 2300683. DOI:10.1002/adfm.202300683 |
 2025, Vol. 42
2025, Vol. 42