2. 中国石油天然气股份有限公司天然气销售湖北分公司, 武汉 430077
2. Petrochina Company Limited Natural gas sales Hubei Branch, Wuhan 430077, China
由于工业的快速发展以及人类对汽车需求的不断增长导致大气污染急剧增加,环境问题逐渐走进公众的视野[1]。在所有污染物中,CO作为大气中的主要污染物之一,会严重影响人类的身体健康并对环境造成不可逆转的破坏[2, 3],因此CO的消除变得尤为重要。通过CO催化氧化技术将CO转化为CO2是目前节能高效的方法之一[4-7]。催化剂作为CO催化氧化技术的核心部分,关于催化剂的研究越来越广泛;其中,贵金属催化剂因其吸附性强、抗毒性强、氧化效率高的特点被广泛应用于CO催化氧化反应中,且在CO催化氧化领域取得了不错的效果[8, 9]。
Ru基催化剂在低温氧化反应中表现出较好的催化性能,因此对其研究越来越多[10-15]。Oh等[16]将不同贵金属(Ru、Rh、Pt和Pb)负载在γ-Al2O3上,并应用在CO优先氧化中。结果发现,较其它3种催化剂,在相同条件下Ru/γ-Al2O3催化剂具有较好的低温催化活性。Gonzalez等[17]制备了不同Ru负载量的Ru(x)-CeO2(x=1.5和3.0)催化剂并应用在CO催化氧化中。结果发现,与参比样CeO2相比,低负载量的(1.5%,质量分数)的Ru(1.5)-CeO2催化剂低温催化活性较好。这可能是因为少量Ru的掺杂促进了CeO2表面氧空位的形成,进而提高催化剂活性。
载体作为催化剂的重要部分,直接影响催化剂结构、性质和催化性能。Weiher等[18]研究了负载在Al2O3、TiO2和SiO2上的Au催化剂并应用于CO催化氧化反应中。结果发现Au/Al2O3催化剂的金团簇电子结构发生变化促进了CO在金团簇上的吸附,进而提高了催化活性。Lou等[19]通过将单个Pt原子分别负载在高还原性Fe2O3、可还原性ZnO和不可还原性γ-Al2O3上,并用于CO催化氧化反应。研究发现,3种不同载体的化学性质、单金属原子与载体之间的相互作用直接影响了催化剂的催化性能,单个Pt原子负载在高还原性Fe2O3上的CO催化氧化性能较好。Li等[20]将负载在SiO2纳米球和CeO2纳米棒上的Ru基催化剂的CO催化氧化性能进行对比,发现负载在CeO2纳米棒上的Ru基催化剂具有较好的低温催化氧化性能,这是因为Ru与CeO2纳米棒界面形成Ru—O—Ce键,Ru物种均匀地分散在载体表面,从而提高了CO催化氧化性能。基于以上结果,选择合适的载体对于进一步提高Ru基催化剂的CO催化氧化性能尤为重要。
本研究采用沉积沉淀法制备了以CeO2、拟薄水铝石[AlO(OH)]、γ-Al2O3和ZrO2为载体的Ru基催化剂,并通过机械球磨对催化剂进行处理。用XRD、H2-TPR、BET和XPS等表征方法对催化剂进行表征,探讨了载体差异对催化剂结构、性质以及CO催化氧化性能的影响。
1 实验部分 1.1 主要试剂试剂:RuCl3(陕西开达化工,分析纯);AlO(OH)、γ-Al2O3、ZrO2、CeO2、NaOH(以上均为国药集团,分析纯)。
1.2 催化剂的制备将49.60 g CeO2 (d=50 nm)和300 mL去离子水在烧杯中混合并剧烈搅拌2 h。在避光并保持剧烈搅拌状态下,向混合液中滴加19 mL的RuCl3水溶液(0.1 mol ·L-1),待全部滴加后继续搅拌30 min,之后将配置好的NaOH水溶液(0.1 mol ·L-1)缓慢滴加到上述混合液中,当混合液pH=7时停止滴加并继续搅拌30 min后,避光静置2.5 h。将混合液抽滤并反复洗涤,直至无氯离子残留后(取1.5 mL滤液和1 mL的0.6 mol ·L-1 AgNO3水溶液震荡混合,无白色沉淀即为无氯离子残留),将得到的样品在80 ℃下干燥17 h,不需要焙烧得到Ru/CeO2催化剂。
取上述Ru/CeO2催化剂在全方位行星式球磨机(南京弛顺科技发展有限公司的PMQW04型)中以300 r ·min-1的转数球磨4 h得到Ru/CeO2-BM催化剂。并用相同的方法将Ru负载到拟薄水铝石[AlO(OH)]、γ-Al2O3和ZrO2上,得到不同载体负载的Ru基催化剂,未球磨的催化剂分别命名为Ru/CeO2、Ru/AlO(OH)、Ru/γ-Al2O3和Ru/ZrO2,球磨后的催化剂分别命名为Ru/CeO2-BM、Ru/AlO(OH)-BM、Ru/γ-Al2O3-BM和Ru/ZrO2-BM。
1.3 催化剂的表征 1.3.1 X射线粉末衍射(XRD)采用德国Bruker公司的D8 Advance型X射线衍射仪检测样品物相组成,测试条件:Cu_Kα1靶,入射波长λ=0.154 nm,管电压40 kV,管电流40 mA,10°~90°扫描。催化剂平均粒径由Scherrer公式(1)计算。
| $ D=\frac{K \lambda}{F \cos \theta} $ | (1) |
式(1)中:D表示测得样品晶粒大小;K是Scherrer常数;λ是X射线波长;F是测得样品衍射峰的半峰宽;θ是测得样品的衍射角。
1.3.2 表面性质分析(BET)采用贝士德科技(北京)有限公司的BSD-PM型高性能比表及微孔分析仪对比表面积和孔体积进行检测。根据BET多点法对催化剂比表面积进行计算,根据BJH法对催化剂的孔体积和孔径进行计算。
1.3.3 程序升温还原分析(H2-TPR)采用中国浙江泛泰科技有限公司FINESORB-3010型化学吸附仪进行测试。取30 mg催化剂在5% H2-Ar条件下进行程序升温还原(50~550 ℃),升温速率为10 ℃ ·min-1。
1.3.4 X射线光电子能谱(XPS)采用美国塞默飞世尔公司Thermo 250i型光电子能谱仪进行测试,测试条件:Al射线激发源,结合能使用测试催化剂的污染碳(C 1s结合能为284.6 eV)进行校正。
1.3.5 高分辨透射电镜(HR-TEM)采用日本电子公司的JEOL-2100F型高分辨透射电镜观察催化剂的形貌和晶格条纹。测试前,将催化剂样品加入乙醇形成溶液,经超声振荡分散均匀后,滴在镍片上等待测试。
1.4 催化剂的评价CO催化氧化性能评价在湖南华思仪器有限公司制造的固定床反应装置进行。称取40~80目的催化剂0.2 g置于内径为6 mm的石英管反应器中,以200 mL ·min-1的流速通入反应气(体积分数为0.6% CO、1.5% O2、97.9% Ar),空速为60 000 h-1。从30 ℃以1 ℃ ·min-1的升温速率升到200 ℃,反应后尾气由科尔塔公司的MOT500型在线气体检测仪检测CO浓度。
CO转化率X(CO)按式(2)计算。
| $ X(\mathrm{CO})=\frac{c(\mathrm{CO})_{\mathrm{in}}-c(\mathrm{CO})_{\text {out }}}{c(\mathrm{CO})_{\mathrm{in}}} \times 100 \% $ | (2) |
式(2)中:c(CO)in表示初始CO的浓度;c(CO)out表示反应后CO的浓度。
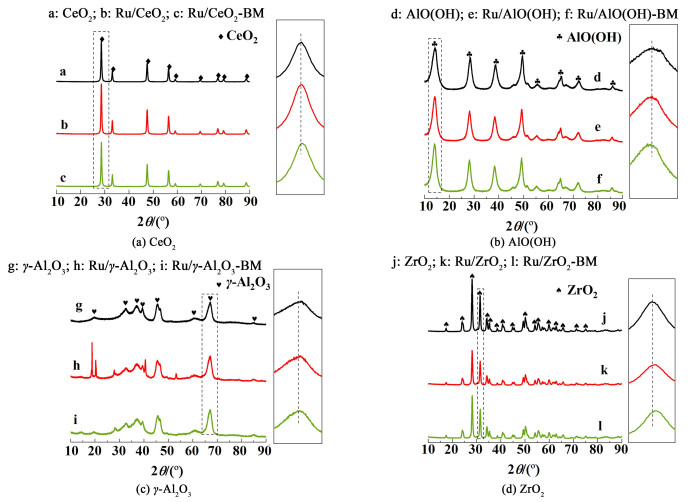
2 结果与讨论 2.1 XRD表征为了探究不同载体对Ru基催化剂晶体结构的影响,进行了XRD表征。图 1为不同载体Ru基催化剂的XRD谱图及晶面放大图。
|
| 图 1 不同载体的Ru基催化剂XRD图及晶面放大图 Fig.1 XRD diagrams of ruthenium-based catalysts with different supports |
| |
由图 1可见,与标准库中的标准卡片对比,不同载体的Ru基催化剂均未出现Ru物种的特征衍射峰,说明Ru物种可能以高分散的状态存在,或进入载体晶格中形成固溶体,或以上2种方式并存[21, 22]。固溶体的形成可以通过衍射峰的位置偏移进一步证明,高分散Ru物种的存在可以通过H2-TPR表征(图 2)结果进一步证明。
|
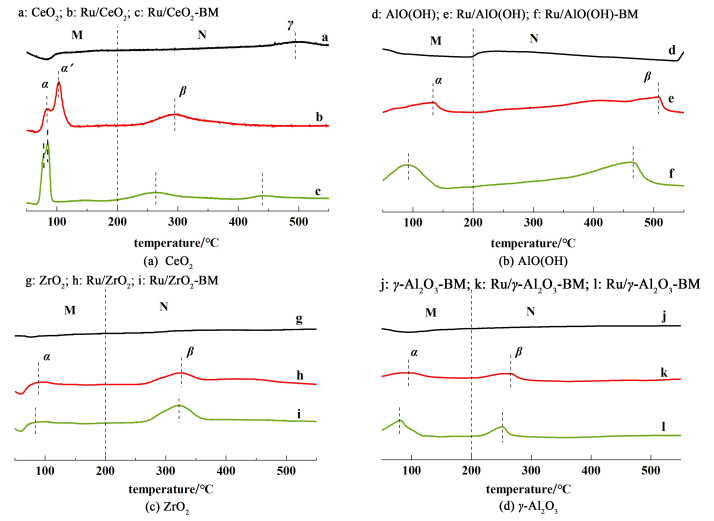
| 图 2 不同载体的Ru基催化剂H2-TPR图 Fig.2 H2-TPR diagrams of ruthenium-based catalysts with different supports |
| |
表 1为根据Scherrer公式计算出不同载体和不同载体Ru基催化剂的晶胞参数。
| Catalysts | Cell parameter/Å | ||
| a | b | c | |
| CeO2 | 0.541 0 | 0.541 0 | 0.541 0 |
| Ru/CeO2 | 0.540 8 | 0.540 8 | 0.540 8 |
| Ru/CeO2-BM | 0.540 7 | 0.540 7 | 0.540 7 |
| AlO(OH) | 0.285 9 | 1.224 0 | 0.369 1 |
| Ru/AlO(OH) | 0.286 7 | 1.224 1 | 0.369 3 |
| Ru/AlO(OH)-BM | 0.287 0 | 1.225 1 | 0.369 7 |
| γ-Al2O3 | 0.792 4 | 0.792 4 | 0.792 4 |
| Ru/γ-Al2O3 | 0.794 0 | 0.794 0 | 0.794 0 |
| Ru/γ-Al2O3-BM | 0.793 5 | 0.793 5 | 0.793 5 |
| ZrO2 | 0.514 4 | 0.521 0 | 0.531 1 |
| Ru/ZrO2 | 0.514 3 | 0.520 9 | 0.530 7 |
| Ru/ZrO2-BM | 0.514 2 | 0.520 6 | 0.530 7 |
结合图 1和表 1,与标准库中AlO(OH)(PDF#74-1895)和γ-Al2O3(PDF#79-1558)标准卡对比,以AlO(OH)和γ-Al2O3为载体的Ru基催化剂特征衍射峰的2θ角均向低角度偏移,催化剂的晶胞参数大于载体的晶胞参数,出现这种现象的原因可能是由于Ru3+(0.068 nm)和Ru4+(0.062 nm)的离子半径大于Al3+(0.039 nm)离子半径,部分Ru3+或Ru4+进入到AlO(OH)和γ-Al2O3晶体内部形成了Ru-O-Al固溶体造成的。与标准库中的CeO2(PDF#78-0694)和ZrO2(PDF#86-1451)标准卡对比,以CeO2和ZrO2为载体的Ru基催化剂所出现的特征衍射峰的2θ均向高角度偏移,催化剂的晶胞参数均小于载体的晶胞参数,这种可能是因为Ru3+(0.068 nm)和Ru4+(0.062 nm)的离子半径小于Ce4+(0.087 nm)、Ce3+(0.102 nm)和Zr4+(0.130 nm)的离子半径,部分Ru3+或Ru4+进入到CeO2和ZrO2晶体内部形成了Ru-O-Ce和Ru-O-Zr固溶体造成的。
2.2 BET表征表 2为不同载体的Ru基催化剂的比表面积、孔容积和平均孔径。
| Catalysts | SBET/m2·g-1 | Pore volume/mL·g-1 | Average pore size/nm |
| CeO2 | 31.8 | 0.115 | 14.5 |
| Ru/CeO2 | 31.3 | 0.136 | 17.4 |
| Ru/CeO2-BM | 36.3 | 0.129 | 14.2 |
| AlO(OH) | 245.9 | 0.373 | 6.1 |
| Ru/AlO(OH) | 239.8 | 0.323 | 5.3 |
| Ru/AlO(OH)-BM | 242.9 | 0.345 | 5.7 |
| ZrO2 | 41.7 | 0.202 | 19.3 |
| Ru/ZrO2 | 42.2 | 0.289 | 27.4 |
| Ru/ZrO2-BM | 43.4 | 0.230 | 21.2 |
| γ-Al2O3 | 151.2 | 1.230 | 34.4 |
| Ru/γ-Al2O3 | 175.0 | 0.733 | 16.5 |
| Ru/γ-Al2O3-BM | 177.5 | 0.523 | 12.0 |
由表 2可知,不同载体的Ru基催化剂经球磨处理后,比表面积分别增大了5.0、3.1、1.2和2.5 m2 ·g-1,说明球磨提高了Ru基催化剂的比表面积。
2.3 H2-TPR表征图 2为不同载体和不同载体Ru基催化剂的H2-TPR谱图。
由图 2可知,不同载体的Ru基催化剂在50~200 ℃(M区间)和200~550 ℃(N区间)产生还原峰。
在图 2(a)中,对Ru/CeO2和Ru/CeO2-BM催化剂的各个还原峰进行归属,M区间α和α'峰归属为高分散Ru物种的还原,N区间β峰归属为Ru-O-Ce固溶体的还原,γ峰归属为表面CeO2的还原。在图 2(b)和图 2(d)中,M区间α峰归属为高分散Ru物种还原,N区间β峰归属为Ru-O-Al固溶体的还原。图 2(c)中,M区间α峰归属为高分散Ru物种的还原,N区间β峰归属为Ru-O-Zr固溶体还原。
为了进一步说明载体对Ru基催化剂的影响,将各个Ru基催化剂的还原峰温度列于表 3。由表 3可知,不同载体的Ru基催化剂α峰对应的还原温度不同,其原因可能是载体的差异影响Ru物种的分散,进而影响了Ru物种与载体之间的相互作用[23]。另外,从表 3还可以看出Ru基催化剂经球磨处理后的α峰都向低温方向移动,这可能是球磨处理使得Ru物种分散度提高造成的,β峰也向低温方向移动,可能在球磨过程中,部分Ru—O—M(M=Al, Zr和Ce)固溶体结构被破坏形成金属Ru氧化物[24]和M。
| Catalysts | Location of reduction peak/℃ | ||
| α peak | β peak | γ peak | |
| Ru/CeO2 | 83 | 295.1 | - |
| Ru/CeO2-BM | 78.2 | 262.2 | 496.4 |
| Ru/AlO(OH) | 133.4 | 507.8 | - |
| Ru/AlO(OH)-BM | 92.8 | 465.9 | - |
| Ru/ZrO2 | 89.4 | 326.1 | - |
| Ru/ZrO2-BM | 83.9 | 322.1 | - |
| Ru/γ-Al2O3 | 94.8 | 265.6 | - |
| Ru/γ-Al2O3-BM | 79.5 | 252.1 | - |
| 注:“-”为未测出。 | |||
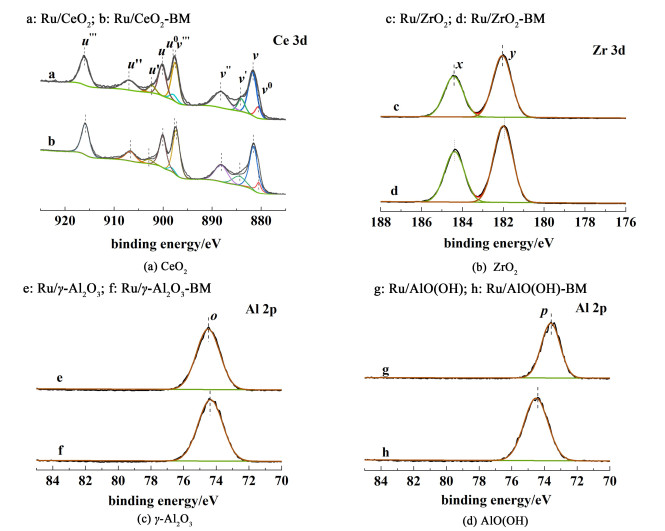
图 3(a)为Ru/CeO2和Ru/CeO2-BM催化剂的Ce 3d X射线光电子能谱。由图 3(a)可知,Ru/CeO2和Ru/CeO2-BM催化剂均出现了10个Ce 3d自旋轨道的特征峰,并将10个特征峰与文献[25]对比可知,u峰和v峰分别对应Ce 3d3/2和Ce 3d5/2能级,其中v0、v'、u0和u'归属于Ce3+,v、v″、v'''、u、u″和u'''均归属于Ce4+。Ru/CeO2和Ru/CeO2-BM催化剂中,Ce4+和Ce3+的相互转换能够有效地促进催化剂表面氧空位的形成,而氧空位的产生有利于CO催化氧化[26],这可能是以CeO2为载体的Ru基催化剂相较其它催化剂活性较好的原因之一。
|
| 图 3 不同载体的XPS谱图 Fig.3 XPS spectra of Ru-based catalysts with different supports |
| |
图 3(b)为Ru/ZrO2和Ru/ZrO2-BM催化剂的Zr 3d X射线光电子能谱。由图 3(b)可知,Ru/ZrO2和Ru/ZrO2-BM催化剂均出现了2个Zr 3d自旋轨道的特征峰。与文献[27]对比可知,x归属于Zr4+的电子结合能,y归属于Zr4+的电子结合能,说明催化剂表面的Zr主要以Zr4+的形式存在。
图 3(c)和3图(d)分别为以γ-Al2O3和AlO(OH)为载体Ru基催化剂的Al 2p X射线光电子能谱。图 3(c)和3图(d)中催化剂均出现1个Al 2p自旋轨道的特征峰,将该特征峰与NIST标准数据库对比可知,73.5~74.5 eV处的特征峰o和p可归属为Al3+。说明以γ-Al2O3和AlO(OH)为载体Ru基催化剂表面Al主要以Al3+形式存在。
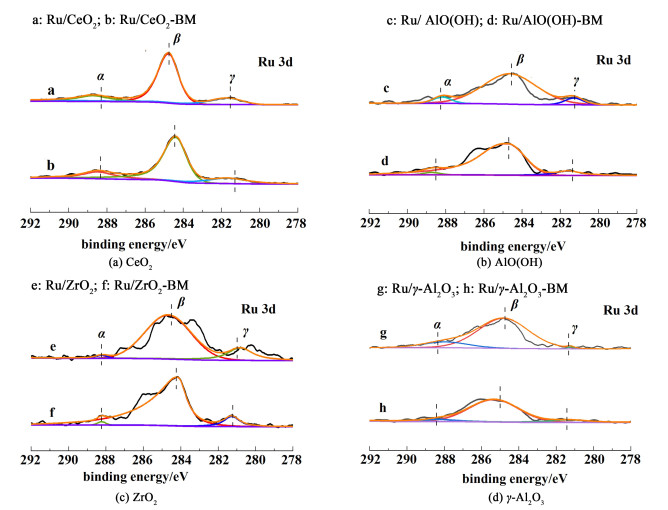
图 4为不同载体的Ru催化剂的Ru 3d X射线光电子能谱。
|
| 图 4 Ru/CeO2催化剂Ru 3d XPS谱图 Fig.4 Ru 3d XPS spectrum of Ru/CeO2 catalyst |
| |
由图 4可知,所有催化剂均出现了3个Ru 3d自旋轨道的特征峰,即α(288.0 eV)、β(284.8 eV)和γ(281.3 eV)。将3个特征峰与NIST标准数据库对比可知,α特征衍射峰归属于Ru 3d3/2自旋轨道特征峰,β特征衍射峰归属于C 1s自旋轨道特征峰,γ特征衍射峰归属于Ru 3d5/2自旋轨道特征峰。其中Ru 3d3/2自旋轨道和部分的C 1s自旋轨道重合,所以通过Ru 3d5/2自旋轨道来判断Ru原子在不同催化剂上的氧化态。负载在不同载体上的Ru基催化剂γ特征衍射峰出现在281.3 eV附近,归属于Ru 3d5/2自旋轨道的Ru3+物种,说明不同载体制备的Ru基催化剂的表面Ru物种主要以Ru3+的状态存在。Ru3+在烘干的过程中会发生歧化反应,反应方程式如式(3)所示,生成Ru0和Ru4+,XPS没有检测到Ru0和Ru4+的原因可能是Ru0和Ru4+含量太低[24]。
| $ 4 \mathrm{Ru}(\mathrm{OH})_3=\mathrm{Ru}+3 \mathrm{RuO}_2+6 \mathrm{H}_2 \mathrm{O} $ | (3) |
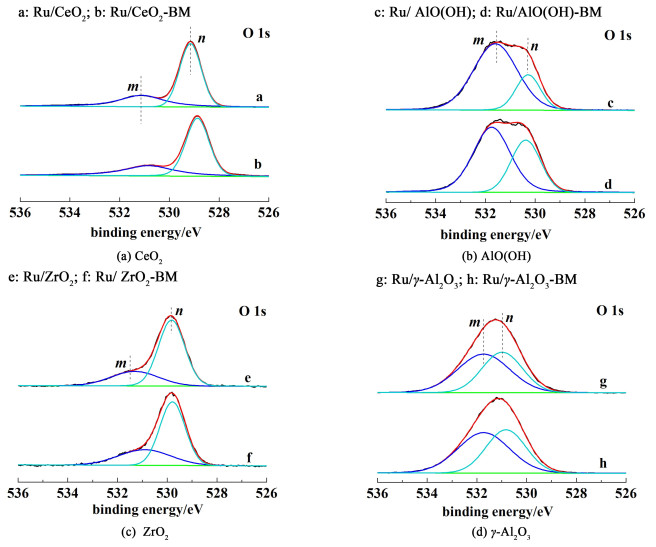
图 5为不同载体的Ru基催化剂的O 1s X射线光电子能谱。
|
| 图 5 催化剂O 1s XPS谱图 Fig.5 O 1s XPS spectrum of catalyst |
| |
由图 5可知,所有催化剂均出现了2个O 1s自旋轨道的特征峰,将2个特征峰与NIST标准数据库对比可知,531.8~530.8 eV处的特征峰m可归属为催化剂表面吸附氧,530.8~528.9 eV处的特征峰n可归属为催化剂中晶格氧[28]。
2.5 HR-TEM表征图 6是Ru/CeO2-BM催化剂的高分辨透射电镜(HR-TEM)以及mapping图。

|
| 图 6 Ru/CeO2-BM催化剂的TEM图 Fig.6 TEM diagram of Ru/CeO2-BM catalyst |
| |
从图 6中可知,Ru/CeO2-BM催化剂是不规则的多边形颗粒,并且颗粒分布在10~30 nm内。通过高分辨透射电镜中可以清晰地看到Ru/CeO2-BM催化剂的晶格条纹,通过测定晶格条纹之间的晶格间距可得出Ru/CeO2-BM催化剂对应的CeO2晶面。图 6中的晶格间距d=0.32 nm,对应着CeO2(111)晶面。
从图 6中没有观察到Ru物种的颗粒,这可能是由于低Ru含量或Ru物种在CeO2载体表面上的良好分散。显然,TEM数据与XRD结果一致。从图 6中可以看出,Ce、O和Ru在催化剂之间均匀分布,进一步表明Ru物种在催化剂表面的高度分散。
2.6 CO催化氧化性能的评价为了比较不同载体的Ru基催化剂的活性,对催化剂活性做出如下定义,定义当CO浓度在1×10-5以下视为对环境无害。定义T50为催化剂转化率为50%时的反应温度。
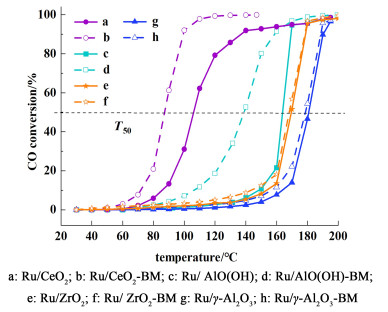
图 7为不同载体的Ru基催化剂在CO催化氧化反应中的CO转化曲线。
|
| 图 7 不同载体负载的Ru催化剂上CO的转化率与反应温度的关系 Fig.7 The relationship between CO conversion rate and reaction temperature on Ru catalysts with various carriers |
| |
从图 7可以看出,CO转化率随着反应温度的升高而增加,活性顺序为:Ru/CeO2-BM>Ru/CeO2>Ru/AlO(OH)-BM>Ru/AlO(OH)> Ru/ZrO2-BM>Ru/ZrO2>Ru/γ-Al2O3-BM>Ru/γ-Al2O3,说明不同载体对Ru基催化剂CO催化氧化活性有影响,可能是因为Ru物种与载体之间的相互作用不同导致的。为了更好的比较不同载体Ru基催化剂性能,在表 4中列出了不同载体负载的Ru基催化剂的T50数据。由表 4可以发现,Ru基催化剂球磨后CO低温催化活性均有一定程度的提高,Ru/CeO2-BM、Ru/AlO(OH)-BM、Ru/ZrO2-BM和Ru/γ-Al2O3-BM催化剂的T50分别降低了19、25、2和3 ℃。Ru/CeO2-BM催化剂在反应温度为147 ℃时,其CO的浓度就降低到了1×10-5以下,CO转化率达到99.9%,且T50温度最低为87 ℃。结合前文XRD、H2-TPR、XPS和HR-TEM等分析结果可知,Ru/CeO2-BM催化剂中Ru物种的分散性好,Ru与Ce的相互作用形成了Ru-O-Ce固溶体,Ce4+和Ce3+的相互转换能够有效地促进其表面氧空位的形成,从而提高了催化剂的低温催化活性。因此,Ru/CeO2-BM催化剂的低温催化性能较好。
| Catalyst | T/℃ | CO concentration/×10-6 | T50%/℃ |
| Ru/CeO2 | 195 | 93 | 106 |
| Ru/CeO2-BM | 147 | 9 | 87 |
| Ru/AlO(OH) | 195 | 109 | 163 |
| Ru/AlO(OH)-BM | 199 | 9 | 138 |
| Ru/ZrO2 | 200 | 119 | 170 |
| Ru/ZrO2-BM | 200 | 32 | 168 |
| Ru/γ-Al2O3 | 195 | 221 | 181 |
| Ru/γ-Al2O3-BM | 195 | 186 | 178 |
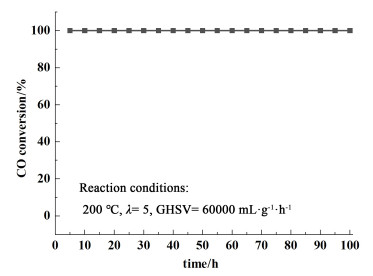
催化剂的稳定性也是评价催化剂CO催化氧化性能的一个重要指标。因此对Ru/CeO2-BM催化剂在恒定反应条件下进行了100 h的CO催化氧化性能评价。如图 8所示,在100 h内,CO转化率均保持在100%,没有明显的失活,这表明Ru/CeO2-BM催化剂具有优异的稳定性。
|
| 图 8 Ru/CeO2-BM催化剂的稳定性曲线 Fig.8 Stability curve of Ru/CeO2-BM catalyst |
| |
为了将本研究的催化剂和文献报道的催化剂更好地比较,将100 ℃时各催化剂的CO转化率列于表 5。其中,反应速率R指的是反应温度为100 ℃时,每1 g贵金属每1 s转化CO物质的量,根据反应速率快慢可以较直观地看出催化剂中贵金属利用情况。计算公式为式(4)。
| $ R=\frac{G c(\mathrm{CO}) X(\mathrm{CO})}{22.4 \times 3600 W_{\mathrm{M}}} \times 1000 $ | (4) |
| Catalyst | WM/% | X(CO)/% | Feeding gas composition | GHSV/(mL·g-1·h-1) | R/(μmol·g-1·s-1) |
| Ru/CeO2-BM | 0.38 | 92.0 | 0.6%CO-1.5%O2-97.9%Ar | 60 000 | 1080.8 |
| Ru/AlO(OH)-BM | 0.38 | 7.2 | 0.6%CO-1.5%O2-97.9%Ar | 60 000 | 84.6 |
| Ru/ZrO2-BM | 0.38 | 3.4 | 0.6%CO-1.5%O2-97.9%Ar | 60 000 | 39.9 |
| Ru/γ-Al2O3-BM | 0.38 | 1.6 | 0.6%CO-1.5%O2-97.9%Ar | 60 000 | 18.8 |
| Ru(3)-CeO2[17] | 3.00 | 33.0 | 1%CO-1%O2-98%N2 | 302 703 | 412.9 |
| 0.3Pt/CeO2[29] | 0.30 | 70.0 | 1%CO-1%O2-98%N2 | 9 600 | 277.8 |
| Pd/CeO2-rod[30] | 1.00 | 18.0 | 2%CO-2%O2-96%He | 60 000 | 267.9 |
式(4)中:G代表体积空速mL ·g-1 ·h-1;c(CO)代表原料气中CO的体积分数;X(CO)代表在100 ℃时的CO转化率;WM代表催化剂中贵金属的质量分数。
由表 5可以看出,Ru/CeO2-BM催化剂在100 ℃时的CO转化率高于其它催化剂,贵金属反应速率为1 080.8 μmol ·g-1 ·s-1,也达到了较高水平,优于文献报道的其它贵金属催化剂。此外,本实验反应尾气中的CO含量是通过CO检测器测定,因此所计算的CO转化率比文献更精确。由此可以说明Ru/CeO2-BM催化剂在CO催化氧化反应中值得进一步研究。
3 结论本研究采用沉积沉淀法制备了负载型的Ru基催化剂,表征和评价结果显示,不同载体主要影响催化剂活性组分和载体之间的相互作用以及氧空位的产生,进而影响了催化材料的催化活性,且存在明显的载体效应。CO催化氧化性能的实验结果表明,Ru/CeO2-BM催化剂表现出了较好的低温性能,在反应温度为147 ℃、氧过量系数为5、空速为60 000 h-1的条件下,CO浓度降低到1×10-5以下,CO转化率达到99.9%。Ru/CeO2-BM催化剂中Ru物种分散性好,相互作用强,能够产生氧空位,因此Ru/CeO2-BM催化剂表现出优良的低温催化性能。该结果明显优于文献报道的其它贵金属催化剂,该催化剂很值得在此基础上做进一步的研究。
| [1] |
ROUHANI M, KORD S, MIRJAFARY Z. Ga-doped phagraphene as a superior media for sensing of carbon monoxide: A detailed theoretical investigation[J]. Physica E: Low-Dimensional Systems and Nanostructures, 2020, 116: 113710. DOI:10.1016/j.physe.2019.113710 |
| [2] |
柴澍靖, 李静, 白雪芹, 等. 水热法制备SnO2纳米颗粒的CO氧化性能[J]. 化学工业与工程, 2017, 34(5): 19-24. CHAI Shujing, LI Jing, BAI Xueqin, et al. CO oxidation performance over SnO2 nanoparticles prepared with hydrothermal method[J]. Chemical Industry and Engineering, 2017, 34(5): 19-24. (in Chinese) |
| [3] |
ZHAO Y, HU J, TAN Z, et al. Ambient carbon monoxide and increased risk of daily hospital outpatient visits for respiratory diseases in Dongguan, China[J]. Science of the Total Environment, 2019, 668: 254-260. DOI:10.1016/j.scitotenv.2019.02.333 |
| [4] |
刘娅琼, 吕倩, 孟明. 制备参数对Au/TiO2催化剂上CO低温氧化性能的影响[J]. 化学工业与工程, 2013, 30(5): 1-6. LIU Yaqiong, LYU Qian, MENG Ming. Effect of preparation parameters on the CO low-temperature oxidation performance of Au/TiO2 catalysts[J]. Chemical Industry and Engineering, 2013, 30(5): 1-6. (in Chinese) |
| [5] |
AN N, LI S, DUCHESNE P N, et al. Size effects of platinum colloid particles on the structure and CO oxidation properties of supported Pt/Fe2O3 catalysts[J]. The Journal of Physical Chemistry C, 2013, 117(41): 21254-21262. DOI:10.1021/jp404266p |
| [6] |
金石山, 张大山, 冯旭浩, 等. Ni含量对NiO/CeO2催化剂催化CO氧化性能的影响[J]. 燃料化学学报, 2022, 50(8): 1034-1040. JIN Shishan, ZHANG Dashan, FENG Xuhao, et al. Effect of Ni content on catalytic oxidation of CO over NiO/CeO2 catalyst[J]. Journal of Fuel Chemistry and Technology, 2022, 50(8): 1034-1040. (in Chinese) |
| [7] |
JIANG Y, ZHANG D, ZHANG C, et al. Preparation of Cu0.1-xNixCe0.9O2-y catalyst by ball milling and its CO catalytic oxidation performance[J]. International Journal of Hydrogen Energy, 2023, 48(33): 12385-12395. DOI:10.1016/j.ijhydene.2022.12.183 |
| [8] |
HARUTA M, YAMADA N, KOBAYASHI T, et al. Gold catalysts prepared by coprecipitation for low-temperature oxidation of hydrogen and of carbon monoxide[J]. Journal of Catalysis, 1989, 115(2): 301-309. DOI:10.1016/0021-9517(89)90034-1 |
| [9] |
HARUTA M, DATÉ M. Advances in the catalysis of Au nanoparticles[J]. Applied Catalysis A: General, 2001, 222(1/2): 427-437. |
| [10] |
SREETHAWONG T, SUKJIT D, OURAIPRYVAN P, et al. Oxidation of oxygenated volatile organic compound over monometallic and bimetallic Ru-Au catalysts[J]. Catalysis Letters, 2010, 138(3): 160-170. |
| [11] |
KAMIUCHI N, MITSUI T, MUROYAMA H, et al. Catalytic combustion of ethyl acetate and nano-structural changes of ruthenium catalysts supported on tin oxide[J]. Applied Catalysis B: Environmental, 2010, 97(1/2): 120-126. |
| [12] |
PARK J N, SHON J K, JIN M, et al. Room-temperature CO oxidation over a highly ordered mesoporous RuO2 catalyst[J]. Reaction Kinetics, Mechanisms and Catalysis, 2011, 103(1): 87-99. DOI:10.1007/s11144-011-0284-5 |
| [13] |
CHIN S, ALEXEEV O S, AMIRIDIS M D. Preferential oxidation of CO under excess H2 conditions over Ru catalysts[J]. Applied Catalysis A: General, 2005, 286(2): 157-166. DOI:10.1016/j.apcata.2005.02.031 |
| [14] |
HUANG B, KOBAYASHI H, YAMAMOTO T, et al. A CO adsorption site change induced by copper substitution in a ruthenium catalyst for enhanced CO oxidation activity[J]. Angewandte Chemie (International Ed), 2019, 58(8): 2230-2235. DOI:10.1002/anie.201812325 |
| [15] |
ANIL C, MADRAS G. Catalytic behaviour of Mn2.94M0.06O4-δ (M=Pt, Ru and Pd) catalysts for low temperature water gas shift (WGS) and CO oxidation[J]. International Journal of Hydrogen Energy, 2020, 45(17): 10461-10474. DOI:10.1016/j.ijhydene.2019.04.117 |
| [16] |
OH S H, SINKEVITCH R M. Carbon monoxide removal from hydrogen-rich fuel cell feedstreams by selective catalytic oxidation[J]. Journal of Catalysis, 1993, 142(1): 254-262. DOI:10.1006/jcat.1993.1205 |
| [17] |
GONZALEZ-A E, RANGEL R, SOLÍS-GARCIA A, et al. FTIR investigation under reaction conditions during CO oxidation over Ru(x)-CeO2 catalysts[J]. Molecular Catalysis, 2020, 493: 111086. DOI:10.1016/j.mcat.2020.111086 |
| [18] |
WEIHER N, BUS E, DELANNOY L, et al. Structure and oxidation state of gold on different supports under various CO oxidation conditions[J]. Journal of Catalysis, 2006, 240(2): 100-107. DOI:10.1016/j.jcat.2006.03.010 |
| [19] |
LOU Y, LIU J. CO oxidation on metal oxide supported single Pt atoms: The role of the support[J]. Industrial & Engineering Chemistry Research, 2017, 56(24): 6916-6925. |
| [20] |
LI J, LIU Z, WANG R. Support structure and reduction treatment effects on CO oxidation of SiO2 nanospheres and CeO2 nanorods supported ruthenium catalysts[J]. Journal of Colloid and Interface Science, 2018, 531: 204-215. DOI:10.1016/j.jcis.2018.07.046 |
| [21] |
卢畅, 张财顺, 刘道胜, 等. CuO-SiO2-CeO2催化剂的设计、制备及性能研究[J]. 石油化工高等学校学报, 2022, 35(1): 29-34. LU Chang, ZHANG Caishun, LIU Daosheng, et al. Design, preparation and performance of CuO-SiO2-CeO2 catalyst[J]. Journal of Petrochemical Universities, 2022, 35(1): 29-34. (in Chinese) |
| [22] |
XING Y, WU J, ZHANG C, et al. Mn-induced Cu/Ce catalysts with improved performance for CO preferential oxidation in H2/CO2-rich streams[J]. International Journal of Hydrogen Energy, 2023, 48(54): 20667-20679. DOI:10.1016/j.ijhydene.2023.03.043 |
| [23] |
杨昕毓, 孙舒, 石岩, 等. 水热时间对CuO/CeO2催化甲醇水蒸气重整制氢的影响[J]. 石油化工高等学校学报, 2023, 36(2): 63-69. YANG Xinyu, SUN Shu, SHI Yan, et al. Effects of hydrothermal reaction time on the performance of CuO/CeO2 catalyst for hydrogen production from steam reforming methanol[J]. Journal of Petrochemical Universities, 2023, 36(2): 63-69. (in Chinese) |
| [24] |
ZHANG Y. Preparation and characterization of Ru/Al2O3 catalysts by adsorption-precipitation-activation method and selective hydrogenation of dimethyl maleate to dimethyl succinate[J]. Material Science and Engineering with Advanced Research, 2015, 1(1): 31-37. DOI:10.24218/msear.2015.05 |
| [25] |
DING Y, WANG Z, GUO Y, et al. A novel method for the synthesis of CexZr1-xO2 solid solution with high purity of κappa phase and excellent reactive activity[J]. Catalysis Today, 2019, 327: 262-270. DOI:10.1016/j.cattod.2018.04.040 |
| [26] |
李树娜, 石奇, 李小军, 等. 金属掺杂Ce-M(M=Fe、Ni和Cu)催化剂的CO低温氧化性能研究[J]. 燃料化学学报, 2017, 45(6): 707-713. LI Shuna, SHI Qi, LI Xiaojun, et al. Low temperature CO oxidation over the ceria oxide catalysts doped with Fe, Ni and Cu[J]. Journal of Fuel Chemistry and Technology, 2017, 45(6): 707-713. (in Chinese) |
| [27] |
SHI Z, TAN Q, WU D. Ternary copper-cerium-zirconium mixed metal oxide catalyst for direct CO2 hydrogenation to methanol[J]. Materials Chemistry and Physics, 2018, 219: 263-272. DOI:10.1016/j.matchemphys.2018.08.038 |
| [28] |
康玉姝, 王丽宝, 李永志, 等. 水热合成时间对Cu/Ce-Zr催化水气变换反应性能的影响[J]. 燃料化学学报(中英文), 2023, 51(6): 776-782. KANG Yushu, WANG Libao, LI Yongzhi, et al. Effect of hydrothermal synthesis time on the performance of Cu/Ce-Zr catalysts for catalytic water-gas shift reaction[J]. Journal of Fuel Chemistry and Technology, 2023, 51(6): 776-782. (in Chinese) |
| [29] |
LIU H, WANG Y, JIA A, et al. Oxygen vacancy promoted CO oxidation over Pt/CeO2 catalysts: A reaction at Pt-CeO2 interface[J]. Applied Surface Science, 2014, 314: 725-734. DOI:10.1016/j.apsusc.2014.06.196 |
| [30] |
SPEZZATI G, BENAVIDEZ A D, DELARIVA A T, et al. CO oxidation by Pd supported on CeO2(100) and CeO2(111) facets[J]. Applied Catalysis B: Environmental, 2019, 243: 36-46. DOI:10.1016/j.apcatb.2018.10.015 |
 2025, Vol. 42
2025, Vol. 42





