2. 常州大学生物过程工程实验室, 江苏 常州 213164;
3. 石油和化工行业连续流技术工程实验室, 江苏 常州 213164
2. Laboratory of Bioprocess Engineering, Changzhou University, Changzhou 213164, Jiangsu, China;
3. Engineering Laboratory of Continuous Flow Technology in Petroleum and Chemical Industry, Changzhou University, Changzhou 213164, Jiangsu, China
β-石竹烯是一种双环结构的倍半萜类化合物(如图 1),广泛存在于各种植物提取的精油中[1]。β-石竹烯在治疗人类重大疾病,如肿瘤、心脑血管疾病、艾滋病等方面具有良好的应用潜力[2],但目前对于β-石竹烯抗氧化能力研究还较少。除此之外,β-石竹烯等倍半萜类化合物可以降低燃料黏度,提高生物燃料的十六烷值,使其满足航空燃料的需求,被认为是未来最具发展前景的高能量密度航空燃料之一[3]。植物提取精油组成成分非常复杂,含有多种萜类、醇类、酮类、酚类和烷烃类等化合物[4],且其中β-石竹烯含量较少,后续分离纯化困难。近年来,随着植物天然产物合成生物学的发展,利用微生物细胞工厂定向合成稀有植物天然化合物成为了实现这类目标化合物定向合成及规模化生产的新策略。
|
| 图 1 β-石竹烯结构式 Fig.1 β-Caryophyllene structure |
| |
目前,倍半萜类化合物的提取分离方法主要有直接压榨法、溶剂提取法、水蒸气蒸馏法、超临界萃取法等[5],通常会针对不同的生物体而采用不同的提取方法,如从植物提取和从海洋生物或微生物中提取所采用的方法可能完全不同。其中溶剂萃取法是从发酵液或者微藻培养液中提取目标化合物最常见的方法之一,但由于发酵液和细胞培养液中组分复杂,导致该方法通常选择性不佳,影响后续分离纯化效果[6]。因此,为了提高提取效率和产品中β-石竹烯的质量分数,针对产品及待分离液特点,开发新型的分离纯化工艺具有实际意义。目前,大孔树脂和硅胶柱是常用的分离纯化手段。大孔树脂因其吸附能力强、安全可靠、绿色无污染以及可再生等优点而被广泛应用于分离纯化领域。檀琪[7]使用AB-8型树脂有效提高了桦褐孔菌中萜类化合物的纯化率。大孔树脂联用硅胶柱纯化工艺近年来也获得了广泛的认可,该方法比单一使用大孔树脂分离效果更加突出。王飞飞[8]等使用HPD-600大孔树脂结合制备液相分离巴黎皂苷Ⅱ和薯蓣皂苷,质量分数在95%以上。姚禹民[9]使用大孔树脂-正相硅胶柱色谱法制备了闹羊花中二萜类主要药效成分,且浓缩干燥后含量≥50%。
本研究采用转基因集胞藻培养液为原料,以减压浓缩结合乙醇提取获得含有β-石竹烯的乙醇水混合液,通过HPD-100型大孔树脂联合C18球形硅胶柱分离纯化出β-石竹烯单一成分,借助质谱技术对组分进行了鉴定,并利用液相色谱法对β-石竹烯进行了定量以及纯度分析,结合抗氧化能力测试和分子对接方法验证其抗氧化能力,为倍半萜类化合物的分离纯化及活性研究提供了一种新思路。
1 材料与方法 1.1 原料与试剂转基因集胞藻,中科院青岛能源所提供;β-石竹烯标准品(质量分数≥97%),购自上海思域化工科技有限公司;大孔吸附树脂(ADS-5、HPD-100、D101、X-5、AB-8、HPD-500),购自天津允开树脂科技有限公司;无水乙醇、无水甲醇、柠檬酸、磷酸氢二钠、氢氧化钠、盐酸、氯化钾购自阿拉丁(上海)生物试剂公司,均为分析纯。
1.2 实验设备旋转蒸发仪RE-52AA,上海亚荣生化仪器厂;恒温振荡器,苏州捷美电子有限公司;岛津液相色谱仪LC-20A,岛津企业管理(中国)有限公司;伊利特BETASIL系列C18色谱柱(4.6 mm×250 mm),大连伊利特分析仪器有限公司;安捷伦7890-5975C,安捷伦科技(中国)有限公司;SHZ-Ⅱ型循环水式真空泵,上海亚荣生化仪器厂;精密电子天平,上海越平科学仪器(苏州)制造有限公司;PHS-3C数显酸度计,上海雷磁仪器有限公司;BT100-2J蠕动泵,保定融柏恒流泵制造有限公司;BSZ-160自动部分收集器,绍兴上虞艾科仪器设备有限公司;C18球形硅胶柱,常州三泰生物科技公司。
1.3 实验方法 1.3.1 β-石竹烯粗提液的制备按照文献[10]方法培养转基因集胞藻,培养周期结束后获得集胞藻培养液;培养液在4 000 r ·min-1的条件下离心,取离心后的上清液;参照文献[11]方法,对离心后上清液进行减压浓缩得浓缩液并进一步过滤,最后用5倍体积72%(如无特殊注明均指质量分数)的乙醇水溶液对浓缩后的滤液进行提取,得到乙醇浓度为60%,β-竹烯含量为0.72 mg ·mL-1,质量分数为35.8%的粗提液。
1.3.2 大孔树脂的筛选考察了6种常用的大孔树脂,其基本参数如表 1所示。新购的大孔树脂需经预处理去掉残留杂质[12]。
| 树脂型号 | 性质 | 比表面积/(m2·g-1) | 平均粒径/mm |
| ADS-5 | 非极性 | 90~150 | 0.30~1.25 |
| HPD-100 | 非极性 | ≥650 | 0.30~1.25 |
| D101 | 非极性 | 500~550 | 0.30~1.25 |
| X-5 | 弱极性 | 500~600 | 0.30~1.25 |
| AB-8 | 弱极性 | 480~520 | 0.13~0.14 |
| HPD-500 | 极性 | 570~600 | 0.06~0.08 |
准确称取经预处理的大孔树脂各2 g置于150 mL锥形瓶中,加入50 mL β-石竹烯粗提液,放置于恒温摇床中150 r ·min-1常温振荡12 h。吸附结束后,取上清液测定β-石竹烯残留量。取按照上述方法吸附饱和的大孔树脂2 g置于一定浓度的120 mL乙醇水溶液中振荡12 h,充分解吸后过滤,测定解吸液中β-石竹烯的浓度。大孔树脂的吸附率和解吸率按照公式(1)和公式(2)计算:
| $ W_1=\frac{\left(c_1-c_2\right) V}{c_1 V} \times 100 \% $ | (1) |
| $ W_2=\frac{c_3 V_1}{\left(c_1-c_2\right) V} \times 100 \% $ | (2) |
式(1)和式(2)中:W1和W2分别为吸附率和解吸率;c1、c2和c3分为样品液、吸附液和解吸液中β-石竹烯浓度,g ·L-1;V和V1分别为吸附液和解吸液体积,mL。
1.3.3 不同温度和pH值对HPD-100型大孔树脂静态吸附的影响(1) 温度影响:准确称取2 g经预处理的HPD-100大孔树脂6份,置于150 mL三角瓶中,各加入50 mL的β-石竹烯粗提液,在不同温度条件下吸附12 h。(2) pH值影响:在最适宜吸附温度下,分别用柠檬酸-磷酸氢二钠缓冲液和盐酸-氯化钾缓冲液调节不同pH值后吸附12 h。测定上述全部实验吸附前后溶液浓度计算吸附率。然后在最适宜吸附条件下进行静态吸附实验,按照1.3.2计算吸附率绘制静态吸附曲线。
1.3.4 HPD-100型大孔树脂静态解吸附实验取6份按照1.3.3中静态吸附方法达到吸附饱和的HPD-100树脂,每份2 g,分别加入三角瓶中。选用不同浓度乙醇水溶液作为解吸液,各取80 mL至三角瓶中,常温振荡12 h后取上清液测定β-石竹烯含量。按照1.3.2计算解吸率,绘制解吸动力学曲线。
1.3.5 不同上样流速对HPD-100树脂动态吸附性能的影响准确称取8 g树脂,湿法装柱,使用蒸馏水清洗3个柱体积后进行粗提液上样。控制流速分别为2、4、6、8 BV ·h-1(单位时间流经单位体积树脂的平均液量),流出液用自动收集器按4 mL ·管-1进行收集,使用HPLC检测β-石竹烯浓度,当流出液浓度达到上样浓度10%,此时认定为泄漏点,绘制上样流速与吸附率的关系曲线。
1.3.6 确定最适宜上样量根据最适宜上样流速上样,每4 mL为1管收集流出液,按照1.4.2的方法间隔测定β-石竹烯浓度,绘制泄漏曲线。
1.3.7 洗脱速度对大孔树脂动态解吸性能的影响准确称取经过预处理的HPD-100树脂8 g,湿法装柱,按照1.3.5所述方法以2 BV ·h-1的上样速度进行动态吸附至饱和,用3倍柱体积的蒸馏水冲洗树脂床后,使用无水乙醇分别以2、4、6、8 BV ·h-1的流速进行洗脱,每4 mL为一管收集洗脱液,测定洗脱液中β-石竹烯浓度,绘制洗脱曲线,确定最适宜洗脱流速。
1.3.8 C18柱分离C18球形硅胶柱选用粒径15 mm,孔径100 Å的硅胶填料。流动相选用色谱级甲醇。将大孔树脂分离后的样品液进行减压浓缩,浓缩体积为原液的1/10,用浓缩液进行上样,上样量为5 mL,流速1 mL ·min-1,每管收集1 mL,按照1.4.2的方法进行定量。
1.4 分析方法 1.4.1 GC-MS分析使用气质联用仪进行定性分析,检测条件如下,色谱柱:HP-5MS(30 m×250 mm×0.25 mm);离子源:EI源;载气:高纯He;进样口温度240 ℃;进样量:0.5 μL;分流比:200∶1;色谱柱流速:1.2 mL ·mL-1;柱温:70 ℃,保持3 min,以10 ℃ ·min-1升温至280 ℃保持5 min;离子源温度:230 ℃;MS四极杆温度:150 ℃。
1.4.2 HPLC检测及标准曲线的绘制取β-石竹烯标准品,以乙醇作为溶剂分别配置浓度为0.4、0.6、0.8、1.0、1.2 g ·L-1的标准品溶液;使用HPLC进行检测,检测选用C18色谱柱(4.6 mm×250 mm),以色谱级甲醇为流动相,设置检测波长220 nm,流速0.65 mL ·min-1,柱温25 ℃,进样量20 μL。
1.5 抗氧化能力 1.5.1 细胞外抗氧化能力 1.5.1.1 DPPH清除能力测定参照文献[13]方法,用无水乙醇配置不同浓度的β-石竹烯溶液,以相同浓度的BHT为对照。在2 mL 0.2 mmol ·L-1 DPPH自由基溶液(95%乙醇溶解)中加入2 mL β-石竹烯溶液,混匀,室温避光反应30 min。空白为2 mL样品加2 mL 95%乙醇,对照为2 mL DPPH加2 mL 95%乙醇。所有样品均在517 nm波长处测定吸光度并按公式(3)计算DPPH清除能力。
| $ W_3=\frac{\left(A_{\mathrm{b}}-A_{\mathrm{s}}\right)}{A_{\mathrm{b}}} \times 100 \% $ | (3) |
式(3)中:W3为DPPH清除率;As和Ab分别代表样品和空白的吸光度。
1.5.1.2 ABTS清除能力测定参照文献[13]方法,用无水乙醇配置不同浓度的β-石竹烯溶液,以相同浓度的BHT为对照。将5 mL 7 mmol ·L-1 ABTS溶液与88 μL 140 mmol ·L-1过硫酸钾溶液混合,在20 ℃下放置20 h,加入约3倍体积的75%乙醇(体积分数),在734 nm波长处的吸光度为0.70 (±0.02),得到ABTS自由基。样品由9.8 mL稀释的ABTS自由基溶液和0.2 mL 1 mg ·mL-1 β-石竹烯组成。以0.2 mL蒸馏水和9.8 mL稀释的ABTS自由基溶液的混合物为空白,0.2 mL β-石竹烯和9.8 mL蒸馏水为对照。所有混合物在室温下放置0.5 h,用分光光度计在734 nm处测定并按公式(4)计算。
| $ W_4=\frac{A_{\mathrm{b}}-\left(A_{\mathrm{s}}-A_{\mathrm{c}}\right)}{A_{\mathrm{b}}} \times 100 \% $ | (4) |
式(4)中:W4为ABTS清除率;As、Ac和Ab分别表示样品、对照和空白的吸光度。
1.5.1.3 ·O2-清除能力测定参照文献[13]方法,用无水乙醇配置不同浓度的β-石竹烯溶液,以相同浓度的BHT为对照。1.5 mL β-石竹烯,依次加入0.5 mL 300 μmol ·L-1 NBT,0.5 mL 468 μmol ·L-1 NADH,0.5 mL 60 μmol ·L-1 PMS,震荡混匀,25 ℃水浴5 min,560 nm波长测定吸光值,以缓冲液代替样品作为空白对照,并按公式(5)计算。
| $ W_5=\frac{A_0-A_1}{A_2-A_1} \times 100 \% $ | (5) |
式(5)中:W5为·O2-清除率;A0、A1和A2分别代表实验组、空白组和对照组的OD值。
1.5.2 细胞内抗氧化能力 1.5.2.1 MTT法检测PC12细胞存活率取对数生长期的PC12细胞,以每孔1×105个·mL-1的密度接种于在96孔细胞培养板中,预培养24 h后,吸去孔内培养基,加入100 μL含有不同浓度的β-石竹烯的无血清培养液,同时设置对照组和空白组,每组4个重复。β-石竹烯处理24 h后,每孔加入10 μL MTT溶液,继续培养4 h,吸弃上清液,向所有孔内加入100 μL Formazan溶解液,混匀后放回细胞培养箱中4 h左右,直至在倒置显微镜中观察没有紫色晶体。使用酶标仪测定各孔在570 nm波长处的吸光度,存活率如公式(6)。
| $ W_6=\frac{A_0-A_1}{A_2-A_1} \times 100 \% $ | (6) |
式(6)中:W6为PC12细胞存活率;A0、A1和A2分别代表实验组、空白组和对照组的OD值。
1.5.2.2 细胞内ROS含量测定将PC12细胞以每孔1×105个·mL-1的密度接种于无菌的全黑96孔板中,待细胞生长融合至80%左右时,加入100 μL含有不同浓度的β-石竹烯的无血清培养液,处理24 h后,吸弃旧的培养液,分别加入100 μL浓度为10 μmol ·mL-1的荧光探针,在培养箱中孵育20 min。使用PBS缓冲液清洗1~2次以除去未进入细胞的探针。最后,每孔加入100 μL PBS缓冲液,在避光条件下使用荧光酶标仪分别检测荧光强度,激发和发射波长分别为495和529 nm,计算PC12细胞内ROS水平[14],如公式(7)。
| $ W_7=\frac{A_0-A_1}{A_2-A_1} \times 100 \% $ | (7) |
式(7)中:W7为ROS清除率;A0、A1和A2分别代表实验组、空白组和对照组OD值。
1.5.3 分子对接PDB数据库下载SOD(PDB ID:1E9O)、CAT(PDB ID;3QJ4)、POD(PDB ID;1M9Q)、GPX(PDB ID;6ELW)。使用Pymol 2.3.0去除蛋白结晶水、原始配体等,将蛋白结构导入AutoDocktools(v1.5.6)进行加氢、计算电荷、分配电荷、指定原子类型并保存为“pdbqt”格式。使用POCASA 1.1预测蛋白结合位点,采用AutoDock Vina1.1.2进行对接[15]。
1.6 数据处理试验重复3次,数据采用Origin 9.0和AutoDock Vina1.1.2进行分析处理。
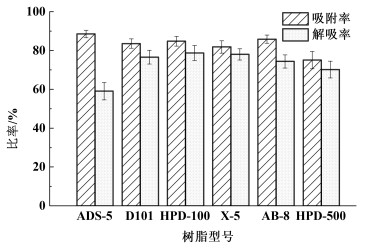
2 结果与讨论 2.1 同型号树脂对β-石竹烯的静态吸附与解吸效果本研究首先选取了6种常见的大孔树脂,分别比较了其对样品粗提液中目标化合物的吸附和解吸效果,结果如图 2所示。
|
| 图 2 6种大孔树脂的吸附率与解吸率 Fig.2 Adsorption and desorption rates of 6 macroporous resins |
| |
由图 2可知,除HPD-500以外,其它5种树脂吸附率均高于80%,这可能是因其与β-石竹烯的极性差异较大而导致吸附效果较差[16]。与此同时,从解吸效果可以看出,HPD-100与X-5的解吸率较高,分别为78.7%和78.0%,而ADS-5虽然吸附率最高,但其解吸率仅为59.1%,远远低于其它型号树脂。综合考虑不同型号树脂的吸附与解吸效果,选用HPD-100树脂进行后续分离纯化实验。
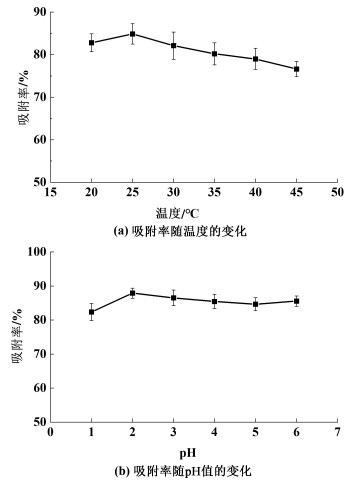
2.2 温度和pH值对树脂静态吸附效果的影响温度和pH值对大孔树脂静态吸附率的影响结果见图 3。
|
| 图 3 温度和pH值对大孔树脂静态吸附率的影响 Fig.3 Effects of temperature and pH on static adsorption rate of macroporous resin |
| |
由图 3(a)可知,最适宜吸附温度为25 ℃,此时吸附率可达84.9%。温度影响吸附质(β-石竹烯)分子的热运动,温度越高,热运动越强[17],因此从20升高到25 ℃时可以促进吸附质向吸附剂进行扩散。当进一步提高吸附温度后,吸附质热运动继续加强,容易挣脱吸附剂的束缚而发生解吸附现象,从而导致吸附量呈下降趋势。由图 3(b)可知,当pH值为2.0时,HPD-100型树脂对β-石竹烯的静态吸附率达到最高值,为87.8%。
2.3 不同浓度乙醇水溶液对HPD-100解吸率的影响大孔树脂对β-石竹烯的吸附具有可逆性,且解吸效果受解吸剂种类和浓度影响。考虑到常用的有机溶剂,如丙酮、二氯甲烷和乙酸乙酯等,对树脂可能存在损伤并且有一定的环境污染风险[18],本研究优先选用不同浓度的乙醇水溶液作为解吸剂,考察乙醇浓度对解吸率的影响。
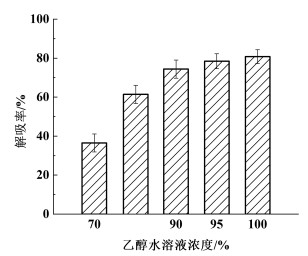
由图 4可知,随着解吸剂中乙醇浓度的增大解吸率逐渐提高。乙醇能够使大孔树脂得到充分溶胀,促进产物溶出,同时β-石竹烯在乙醇中溶解度也较高。因此,解吸剂中乙醇浓度增大有利于增加β-石竹烯的溶解性,使得大孔树脂与β-石竹烯之间的作用力减小,从而提高解吸率。当使用无水乙醇作为解吸剂时,解吸率最高可达80.8%。
|
| 图 4 解吸剂中乙醇浓度对大孔树脂静态解吸率的影响 Fig.4 Effects of different ethanol concentrations on static adsorption rate of macroporous resin |
| |
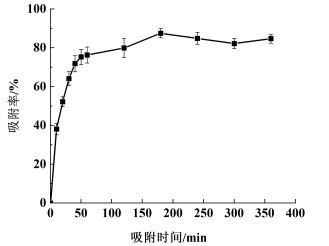
β-石竹烯在HPD-100树脂上的吸附率随吸附时间的变化如图 5所示。
|
| 图 5 HPD-100树脂的静态吸附动力学曲线 Fig.5 Kinetic curve of HPD-100 static adsorption process |
| |
由图 5可见,在吸附开始后的1 h内,HPD-100树脂对β-石竹烯的吸附率快速上升,达到76.3%,说明此时树脂上的吸附位点被快速饱和。当吸附时间为3 h,此时吸附率达到最高为87.8%,此后随时间延长,吸附率逐渐趋于平稳,说明此时已经基本达到吸附平衡状态[19]。因此,在操作过程中可以选择吸附时间为3 h。
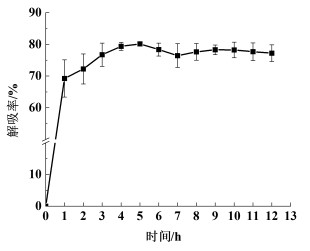
2.4.2 静态解吸动力学取按照1.3.3方法操作达到静态吸附饱和的HPD-100大孔树脂进行解吸实验。随着解吸时间的延长,其解吸率变化趋势如图 6所示。
|
| 图 6 静态解吸动力学曲线 Fig.6 Kinetic curve of static desorption |
| |
在解吸附操作开始后的1 h内,解吸率快速提升,达到69.2%,而后解吸率增加趋势减缓,在5 h时达到最高值80.8%。随着时间延长,解吸率在小范围内有一定波动,说明被洗脱下来的目标产物仍存在重复吸附到HPD-100树脂上的可能性。
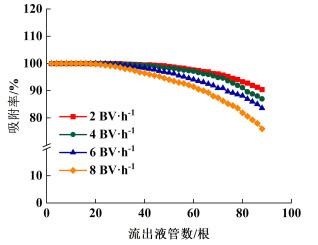
2.5 HPD-100树脂的动态吸附与解吸附 2.5.1 上样流速对吸附的影响上样流速影响目标物与大孔树脂的接触时间,从而影响吸附率,测定结果见图 7。
|
| 图 7 不同上样流速对大孔树脂动态吸附率的影响 Fig.7 Effects of different loading flow rates on dynamic adsorption rate of macroporous resin |
| |
由图 7可知,在不同上样流速下,收集到的前16管收集液中均未检测到β-石竹烯,说明此时进样液中所有β-石竹烯均可被HPD-100树脂完全吸附。随着上样量的增加,上样流速越大的样品组其吸附率下降越快。综合考虑上样时间和吸附率变化,采用变流速方式[20]上样,在上样量为5 BV前采用高流速8 BV ·h-1进行上样以缩短吸附时间,此后转换成低流速2 BV ·h-1继续上样,以增大树脂吸附量。
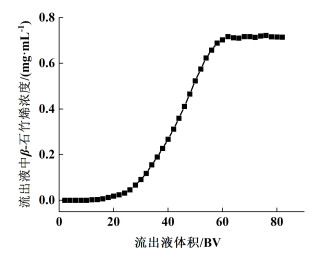
2.5.2 泄漏曲线的绘制用2 BV ·h-1的上样流速进样,收集流出液并对流出液中样品浓度进行测定,结果见图 8。
|
| 图 8 HPD-100大孔树脂泄漏曲线 Fig.8 Leakage curve of HPD-100 macroporous resin |
| |
由图 8可知,当树脂床体积一定时,初始流出液中未检测到β-石竹烯,说明目标产物完全被树脂所吸附。随后,流出液中β-石竹烯的浓度逐渐增大,当收集液达到28 BV时,流出液中目标产物浓度为0.073 g ·L-1,达到上样液浓度的10%,此时为泄漏点。因此,确定28 BV为最适宜上样体积。
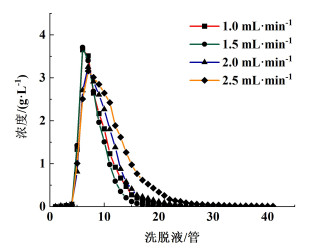
2.5.3 洗脱流速对解吸过程的影响洗脱流速对解吸过程的影响见图 9。
|
| 图 9 洗脱流速对HPD-100大孔树脂动态解吸率的影响 Fig.9 Effects of elution flow rates on the dynamic desorption rate of the HPD-100 macroporous resin |
| |
由图 9可知,洗脱液前几管β-石竹烯浓度较低,是因为树脂柱中残留的水分对洗脱液进行了稀释,随后洗脱剂中β-石竹烯的浓度逐渐增大。洗脱流速为1.0和1.5 mL ·min-1时洗脱效果较好。相比较而言,当洗脱流速为1.5 mL ·min-1时,洗脱曲线峰型较窄,无明显拖尾现象。此流速下只需要84 mL(7 BV)溶剂就能完成洗脱,解吸效果最好。洗脱流速达到2 mL ·min-1时,所需溶剂体积约为1.5 mL ·min-1流速下的2倍。综合考虑洗脱时间和洗脱溶剂用量,确定1.5 mL ·min-1为最适宜洗脱流速。
2.6 目标产物的C18柱分离纯化本研究采用制备色谱(C18球形柱)对动态解吸洗脱液中的目标产物进行进一步的分离纯化。结果见图 10。
|
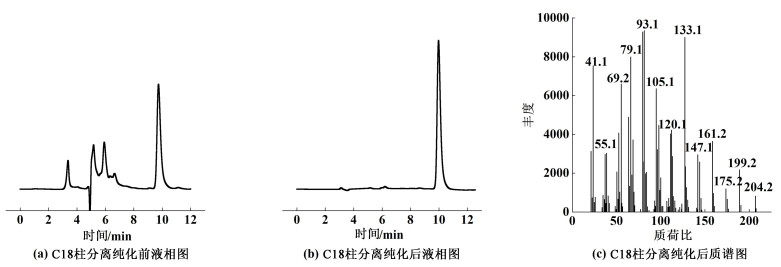
| 图 10 C18柱分离纯化前后液相和气质联用检测图谱 Fig.10 HPLC and GC-MS results before and after C18 column separation and purification |
| |
由图 10(a)对比β-石竹烯标准品的液相图谱可知,β-石竹烯出峰时间约为10 min,但是经大孔树脂分离纯化后的液体样品中仍然存在部分杂质。相比较而言,浓缩后的洗脱液经过C18柱进一步纯化后液相色谱图上的杂质峰基本被去除,β-石竹烯纯度得到了明显提高,此时质量分数达到99.0%,相较未纯化前提高了51.2%。如图 10(c)将C18柱流出液样品进行质谱分析进一步验证了收集到的样品为β-石竹烯。
2.7 抗氧化能力 2.7.1 细胞外抗氧化图 11考察了β-石竹烯的体外抗氧化能力随浓度变化情况并与BHT进行对比。
|
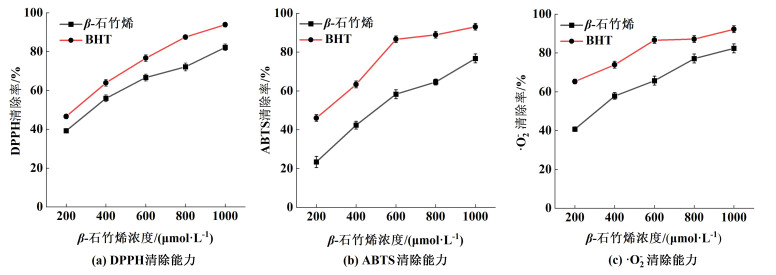
| 图 11 β-石竹烯的体外抗氧化能力 Fig.11 Antioxidant capacity of β-caryophyllene in vitro |
| |
如图 11所示,β-石竹烯和BHT的抗氧化能力均随着浓度增加而有所提升,当其浓度为1 000 μmol ·L-1时,β-石竹烯对DPPH、ABTS和·O2-的清除能力分别为82.2%、76.7%和82.4%,略低于对照样BHT的93.9%、93.0%和92.3%,说明β-石竹烯也具有一定的抗氧化能力。
2.7.2 细胞内抗氧化测试了细胞内抗氧化能力,结果见图 12。
|
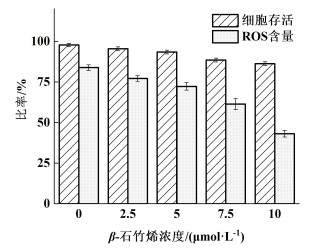
| 图 12 β-石竹烯的细胞内抗氧化能力 Fig.12 Intracellular antioxidant capacity of β-caryophyllene |
| |
如图 12所示,经β-石竹烯处理24 h后,PC12细胞存活率均在85%以上,说明在本实验中选用的β-石竹烯浓度对PC12细胞无明显毒副作用。ROS形成为氧的正常代谢的天然副产物,在细胞信号传导和体内平衡中具有重要作用。在不同浓度条件下检测ROS的含量,发现随着β-石竹烯浓度升高,ROS含量有所下降,添加10 μmol ·L-1的β-石竹烯样品ROS含量降低了40.8%,证明其具有细胞内抗氧化效果。
2.7.3 分子对接消除ROS的抗氧化体系分为酶系和非酶系,酶系有超氧化物歧化酶(SOD)、过氧化氢酶(CAT)、谷胱甘肽过氧化物酶(GPX)和过氧化物酶(POD)等,可下调活性氧的产生水平。
因此,本研究采用分子对接模拟的方法研究β-石竹烯的抗氧化机制,分别与SOD(PDB ID:1E9O)、CAT(PDB ID;3QJ4)、POD(PDB ID;1M9Q)、GPX(PDB ID;6ELW)进行分子对接(如图 13,粉色虚线表示疏水作用力)。小分子β-石竹烯与POD、CAT、GPX、SOD蛋白之间的结合能分别为-27.61、-29.71、-25.52和-23.43 kJ ·mol-1。通常配体与靶蛋白的结合能小于0,则配体和受体蛋白可以自发结合,如果结合能小于-20.92 kJ ·mol-1,表明活性成分与靶点具有较强的亲和活性,因此说明4对对接之间均具有较强的亲和活性。
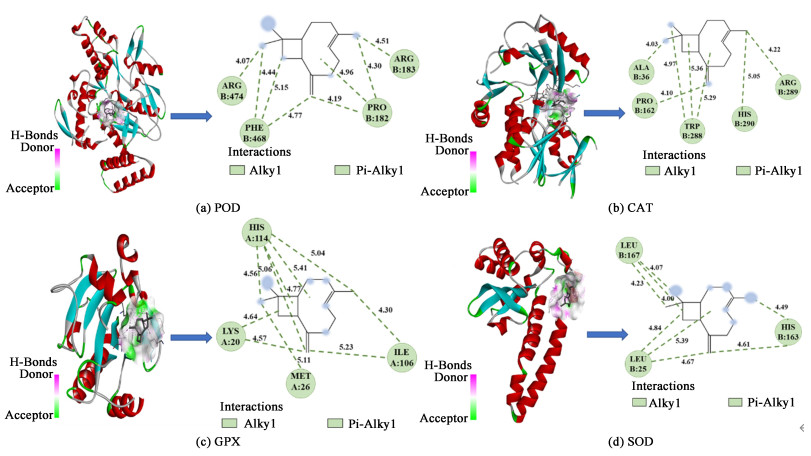
|
| 图 13 β-石竹烯的分子对接酶 Fig.13 Molecular docking of β-carnation |
| |
通过对静态吸附和解吸性能的比较,筛选出对粗提液中β-石竹烯吸附效果最好的HPD-100型大孔树脂。同时探讨了多种影响因素对树脂吸附和解吸附性能的影响,得出大孔树脂动态分离纯化最佳条件为:上样溶液pH值为2.0,上样温度25 ℃,依次用8和2 BV ·h-1流速上样,采用无水乙醇以1.5 mL ·min-1流速进行洗脱。树脂洗脱液经浓缩后,再以上样量5 mL,流速1 mL ·min-1通过C18柱进一步分离纯化,成功得到β-石竹烯单一组分,且质量分数达到99.0%,较粗提液提高了63.2%,表明该分离方法效果显著。抗氧化能力测试和分子对接模拟结果表明β-石竹烯可能通过结合酶发挥其抗氧化活性,β-石竹烯与SOD、CAT、POD、GPX均有良好的亲和活性。本研究为倍半萜类化合物的分离纯化与抗氧化性研究提供了参考。
| [1] |
LEE H Y, KO M J. Thermal decomposition and oxidation of β-caryophyllene in black pepper during subcritical water extraction[J]. Food Science and Biotechnology, 2021, 30(12): 1527-1533. DOI:10.1007/s10068-021-00983-z |
| [2] |
SKÖLD M, KARLBERG A T, MATURA M, et al. The fragrance chemical beta-caryophyllene-air oxidation and skin sensitization[J]. Food and Chemical Toxicology: an International Journal Published for the British Industrial Biological Research Association, 2006, 44(4): 538-545. DOI:10.1016/j.fct.2005.08.028 |
| [3] |
DAHHAM S S, TABANA Y M, IQBAL M A, et al. The anticancer, antioxidant and antimicrobial properties of the sesquiterpene β-caryophyllene from the essential oil of aquilaria crassna[J]. Molecules, 2015, 20(7): 11808-11829. DOI:10.3390/molecules200711808 |
| [4] |
HARVEY B G, MEYLEMANS H A, GOUGH R V, et al. High-density biosynthetic fuels: The intersection of heterogeneous catalysis and metabolic engineering[J]. Physical Chemistry Chemical Physics, 2014, 16(20): 9448-9457. DOI:10.1039/C3CP55349C |
| [5] |
AMIRI H, MESHKAT AL SADAT M H, LARI Y H. Chemical composition of the essential oil of Eremostachys Laevigata bung[J]. DARU: Journal of Pharmaceutical Sciences, 2007, 15(1): 34-40. |
| [6] |
DÍAZ-MAROTO M C, DÍAZ-MAROTO I J, SÁNCHEZ-PALOMO E, et al. Volatile components and key odorants of fennel (Foeniculum vulgare mill.) and thyme (Thymus vulgaris L.) oil extracts obtained by simultaneous distillation-extraction and supercritical fluid extraction[J]. Journal of Agricultural and Food Chemistry, 2005, 53(13): 5385-8389. DOI:10.1021/jf050340+ |
| [7] |
檀琪, 阮文辉, 杨官娥, 等. 大孔吸附树脂纯化桦褐孔菌三萜类化合物工艺优化[J]. 食品工业, 2021, 42(3): 142-146. TAN Qi, RUAN Wenhui, YANG Guane, et al. Optimization of purification of triterpenoids from inonotus obliquus by macro-porous resin[J]. The Food Industry, 2021, 42(3): 142-146. (in Chinese) |
| [8] |
WANG F, MA X, QU L. Combined application of macroporous resins and preparative high-performance liquid chromatography for the separation of steroidal saponins from stems and leaves of Paris polyphylla[J]. Chromatographia, 2021, 84(10): 917-925. DOI:10.1007/s10337-021-04073-4 |
| [9] |
姚禹民, 房鑫, 张继全, 等. 大孔树脂-正相硅胶柱色谱法制备闹羊花二萜有效部位[J]. 中国医药工业杂志, 2019, 50(12): 1444-1449. YAO Yumin, FANG Xin, ZHANG Jiquan, et al. Preparation of diterpenoid fraction from fruits of rhododendron molle G. don by macroporous resin combined with normal-phase silica gel column chromatography[J]. Chinese Journal of Pharmaceuticals, 2019, 50(12): 1444-1449. (in Chinese) |
| [10] |
IIJIMA H, WATANABE A, SUKIGARA H, 等. Simultaneous increases in the levels of compatible solutes by cost-effective cultivation of Synechocystis sp. PCC 6803[J]. Biotechnology and Bioengineering, 2020, 117(6): 1649-1660. |
| [11] |
宋爱荣, 赵晨, 孙效乐, 等. 桑黄菌中一种新的桉烷型倍半萜的分离技术: CN103113194A[P]. 2013-05-22 SONG Airong, ZHAO Chen, SUN Xiaole, et al. Technology for separating novel eudesmane sesquiterpenes from Phellinus igniarius: CN103113194A[P]. 2013-05-22 (in Chinese) |
| [12] |
罗磊, 姬青华, 马丽苹, 等. NKA-9大孔树脂对绿豆皮黄酮的纯化研究[J]. 中国食品学报, 2019, 19(6): 157-167. LUO Lei, JI Qinghua, MA Liping, et al. Studies on purification of total flavonoids from mung bean hull using NKA-9 macroporous resin[J]. Journal of Chinese Institute of Food Science and Technology, 2019, 19(6): 157-167. (in Chinese) |
| [13] |
DINARDO A, SUBRAMANIAN J, SINGH A. Investigation of antioxidant content and capacity in yellow European plums[J]. International Journal of Fruit Science, 2018, 18(1): 99-116. DOI:10.1080/15538362.2017.1381873 |
| [14] |
LIANG R, CHENG S, DONG Y, et al. Intracellular antioxidant activity and apoptosis inhibition capacity of PEF-treated KDHCH in HepG2 cells[J]. Food Research International, 2019, 121: 336-347. DOI:10.1016/j.foodres.2019.03.049 |
| [15] |
REN G, SUN H, GUO J, et al. Molecular mechanism of the interaction between resveratrol and trypsin via spectroscopy and molecular docking[J]. Food & Function, 2019, 10(6): 3291-3302. |
| [16] |
吴红艳, 石岩, 李秀鑫, 等. 大孔树脂纯化万寿菊花中叶黄素的工艺优化[J]. 食品与机械, 2022, 38(9): 153-158. WU Hongyan, SHI Yan, LI Xiuxin, et al. Optimization of purification process of lutein from Marigold by macroporous resin[J]. Food & Machinery, 2022, 38(9): 153-158. (in Chinese) |
| [17] |
高丽, 张昭, 李静. 大孔树脂精制荷叶黄酮的工艺研究[J]. 粮食与油脂, 2021, 34(3): 67-69, 89. GAO Li, ZHANG Zhao, LI Jing. Research on the technology of refining flavonoidfrom lotus leaf by macroporous adsorption resin[J]. Cereals & Oils, 2021, 34(3): 67-69, 89. (in Chinese) |
| [18] |
李晓玲, 王世清, 王文亮, 等. 大孔树脂纯化脂溶性玉米黄色素[J]. 中国食品学报, 2014, 14(9): 164-169. LI Xiaoling, WANG Shiqing, WANG Wenliang, et al. Purification of liposoluble maize yellow pigment by macroporous resin[J]. Journal of Chinese Institute of Food Science and Technology, 2014, 14(9): 164-169. (in Chinese) |
| [19] |
曹艳, 金佳秀, 巩卫琪, 等. 大孔树脂法纯化覆盆子中黄酮化合物[J]. 食品安全质量检测学报, 2022, 13(7): 2137-2143. CAO Yan, JIN Jiaxiu, GONG Weiqi, et al. Purification of flavonoids from Rubus chingii Hu extraction by macroporous resin[J]. Journal of Food Safety & Quality, 2022, 13(7): 2137-2143. (in Chinese) |
| [20] |
谢三都, 方豪, 黄东东. 大孔树脂纯化柿子黄色素工艺优化[J]. 中国调味品, 2021, 46(12): 167-171. XIE Sandu, FANG Hao, HUANG Dongdong. Optimization of purification process of persimmon yellow pigment by macroporous resin[J]. China Condiment, 2021, 46(12): 167-171. (in Chinese) |
 2025, Vol. 42
2025, Vol. 42





