在碳材料上掺杂杂原子特别是氮原子可以有效提高氧化剂去除有机污染物的催化活性,而杂原子在提供活性位点、增加缺陷边缘和增强电子转移方面发挥了很大的作用[1]。然而,虽然无金属碳催化剂解决了金属离子的二次污染问题,但原始碳材料固有的化学惰性使其催化活性受到限制,这仍是一个迫切有待解决的问题。
近年来,过渡金属,如铁、钴、铜和锰以及氮掺杂碳(M-N-C) 催化剂已成为复合催化剂的新兴的研究方向,并被证实是填补均相和多相催化剂之间间隔的桥梁[2, 3]。M-N-C催化剂相较于传统的均相金属离子、氧化物和负载碳金属材料具有更好的稳定性和重复使用性,并且它们比无金属碳材料具有更高的反应活性[4]。氮掺杂可以有效地克服碳材料的化学惰性,M-N-C中的氮原子还可以作为Lewis碱,与作为Lewis酸的过渡金属结合,两者间产生的配位作用确保金属位点可以牢固锚定[5]。由于氮元素的固定功能,M-N-C催化材料中的金属位点可以达到极高的分散度,从而发挥最大的活性作用。特别是M-N-C为能量中心提供了明确的结构,方便从原子尺度上直观地揭示了催化剂结构和反应机理之间的关系,为定制具有高活性的高活性催化剂提供了重要的参考。
基于氧化剂为高碘酸钠(NaIO4) 的新型高级氧化技术因其高效稳定、操作简便等特点逐渐引起了学者们的关注和研究。高碘酸盐是一种新型的氧化剂,可以有效地产生高活性的自由基。其氧化还原电位为1.6 V[6],具有较强的氧化还原能力。与一般的氧化剂相比,高碘酸盐在pH值为2~9的范围内相对稳定,同时具有相对效率高、污染少、成本低的特点,因而被认为是一种拥有巨大潜力的氧化剂[7]。
Du等[8]在2019年进行的实验中发现,均相的Mn2+对高碘酸盐的活化有着卓越的表现。当pH=9.5时,把1 mmol ·L-1的Mn2+用来活化1 mmol ·L-1的IO4-,反应在1 min以内可以完全降解浓度为0.1 mmol ·L-1的BPA溶液[8]。Mn2+/IO4-去除水中有机污染物具有反应速率快、氧化剂利用率高(氧化剂与污染物的物质的量之比仅为2)等特点,是一种新颖有效的高级氧化水处理技术。然而Mn2+在自然界中通常是以液态的形式存在,这不便于运输和循环利用。因此,开发非均相的不同结构、晶型的锰基催化剂用来活化高碘酸盐将会是今后研究的热点。
本工作使用相同的反应原料,在不同温度下制备了2种不同晶型的Mn-N-C材料,通过活化高碘酸盐产生的活性氧物种来降解双酚A (BPA); 旨在进一步研究过渡金属氮掺杂碳催化剂的性能和机理。
1 实验 1.1 实验药品双酚A(BPA,质量分数为99%,下同)、无水乙醇(AR, 99%)、高碘酸钠(NaIO4, 98%)、乙酰丙酮锰[Mn(acac)3, 98%]、氢氧化钠(NaOH, 98%)、呋喃甲醇(FFA, 98%)、Nafion(5%)、三聚氰胺(Melamine, 99%)购自上海阿拉丁生化科技股份有限公司。氮化锰(Mn4N, N 8%)购自上海麦克林生化科技有限公司。甲醇(MeOH, 99%)购自天津科密欧试剂有限公司。硫酸(H2SO4, 98%)购自天津市元立化工有限公司。对苯醌(p-BQ,99%)购自阿达玛斯试剂有限公司。
1.2 催化剂的制备将0.353 g乙酰丙酮锰[Mn(acac)3]和3.153 g三聚氰胺(Melamine)加入50 mL无水乙醇中,并在加热套搅拌器中以600 r ·min-1的搅拌速率搅拌12 h,在常温条件下是2种物质尽可能的均匀混合。待样品均匀地分布在无水乙醇后,将温度保持在60 ℃,使无水乙醇完全蒸发掉,得到土黄色的混合物前驱体。将得到的前驱体进行研磨,在刚玉舟中放在管式炉中高温煅烧。管式炉中的升温程序先从常温以5 ℃ ·min-1的升温速率升到550 ℃,在此温度下保存2 h,然后再将温度分别升高到800和1 100 ℃,继续在对应温度下保温2 h,使得样品完全碳化,煅烧过程全程以N2作为保护气体,流量设置为150 mL ·min-1。
1.3 催化剂的表征采用Smartlab Rigaku X型射线衍射仪对材料的晶面,物质组成进行分析测试。采用Thermo Scientific Apreo S型扫描电子显微镜和FEI TF20型透射电子显微镜观察样品的微观形貌。采用Thermo ESCALAB 250XI型X射线光电子能谱用于检测分析材料的碳、氮、氧和锰等元素的价态分布情况等信息。采用U3000型高效液相色谱仪对固定时间所取得的样品进行色谱分析,得到目标物的相对含量采用CHI660E电化学工作站对实验的开路电压测定,判断反应过程是否存在直接电子转移过程(DET)。使用电感耦合等离子质谱仪(ICP-MS)测量催化剂的金属含量。
1.4 催化剂的催化氧化性能评价本实验使用100 mL, 2×10-5的BPA水溶液作为目标污染物。实验时,先将10 mg催化剂加入污染物水溶液之中,然后进行2 min的超声,使得催化剂对BPA的吸附达到平衡。之后在污染物水溶液加入10 mg NaIO4,加入的同时使用秒表进行计时,在0、2、5、10、15、20、30和40 min时刻进行取样,取样时每次从反应体系中取得0.5 mL反应液体,迅速加到含有0.5 mL的甲醇中。甲醇可以快速淬灭·OH、SO4·-和O2·-自由基,再将1 mL混合液体用注射器吸取,通过0.45 μm的滤膜过滤到液相小瓶中,滤膜可以过滤掉催化剂颗粒,使得非自由基反应过程终止。使用高效液相色谱仪进行BPA浓度的分析,所取得的0 min试样对应着2×10-5 BPA溶液的峰面积,以相对峰面积作为剩余BPA浓度的判断依据。液相色谱仪的流动相为[m(甲醇) ∶m(水)=7 ∶3],流速为1.0 mL ·min-1,检测波长为280 nm。循环稳定性测试中,将反应完成的催化剂过滤出来,经过醇洗、水洗去除催化剂表面可能吸附的中间产物,暴露出活性位点。再将得到的催化剂进行冻干处理,冻干后进行称量,加入相对体积的2×10-5的BPA溶液,按照上述性能测试步骤重复进行。
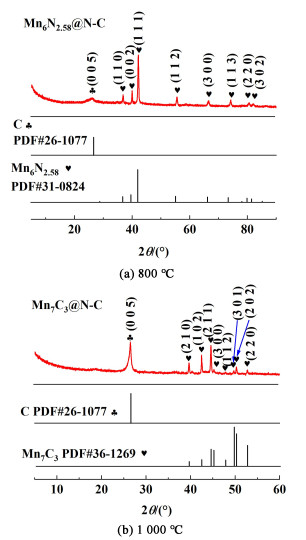
2 实验结果与讨论 2.1 催化剂的表征结果 2.1.1 催化剂的X射线衍射仪(XRD)表征结果对合成的2种Mn-N-C催化剂进行XRD的谱图分析,结果如图 1(a)所示,对于800 ℃条件下所碳化得到的材料,其X射线衍射谱图中出现了36.7°、39.5°、41.8°、55.1°、66.1°、73.3°、79.8°和81.4°的衍射峰,分别对应着晶体Mn6N2.58 (PDF#31-0824)的(110)、(002)、(111)、(112)、(300)、(113)、(220)和(302)晶面,这说明合成的催化剂含有Mn6N2.58晶体,出现在26.6°的衍射峰为石墨C衍射峰(PDF#26-1077),所对应的晶面为(005)晶面。在图 1(b)中为1 100 ℃条件下所碳化得到的催化剂,该谱图在39.7°、42.5°、44.6°、45.2°、47.9°、49.8°、50.3°和52.8°出现了衍射峰,分别对应Mn7C3(PDF#36-1269)的(210)、(102)、(211)、(300)、(112)、(301)、(202)和(220)晶面。26.6°的衍射峰为C的衍射峰,对应着(005)晶面。
|
| 图 1 催化剂的XRD图像 Fig.1 XRD images of catalysts |
| |
为了对材料的微观形貌做进一步的了解,对催化剂进行了扫描电镜和透射电镜的分析,Mn6N2.58@ N-C的扫描电镜实验结果如图 2(a)所示,可以看出,Mn6N2.58@N-C的表面拥有较多的褶皱,这样的疏松、层状的表面结构会有利于对BPA分子的吸附作用[9],从而有利于催化氧化反应的进行。Mn7C3@N-C的扫描电镜结果,如图 2(c)所示,催化剂表面出现了丰富的孔道结构,这种蜂窝状的表面结构会有利于反应物及其中间产物进入材料内部,可以充分利用材料的活性位点,并加快反应过程,提高反应活性。

|
| 图 2 Mn6N2.58@N-C的SEM (a)和TEM (b),Mn7C3@N-C的SEM (c)和TEM (d) Fig.2 SEM (a) and TEM (b) of Mn6N2.58@N-C and Mn7C3@N-C SEM (c) and TEM (d) |
| |
图 2(b)显示的是Mn6N2.58@N-C的透射电镜图,很清晰地看到Mn6N2.58晶体整体被碳氮层所包裹,这样的结构可以有效地降低离子浸出,从而提高催化剂的稳定性,减少金属离子对水体的污染[10]。如图 2(d)显示,亦可以看出被氮掺杂碳所包裹的Mn7C3晶体颗粒,可以看出晶体的结晶度并不是很高,这反映在上述的XRD图像中的晶体相对于石墨的衍射峰强并不明显。上述2种晶体均处于被碳氮层包裹状态,碳氮层的存在会有利于加强电子传输、降低离子浸出[1, 11]。
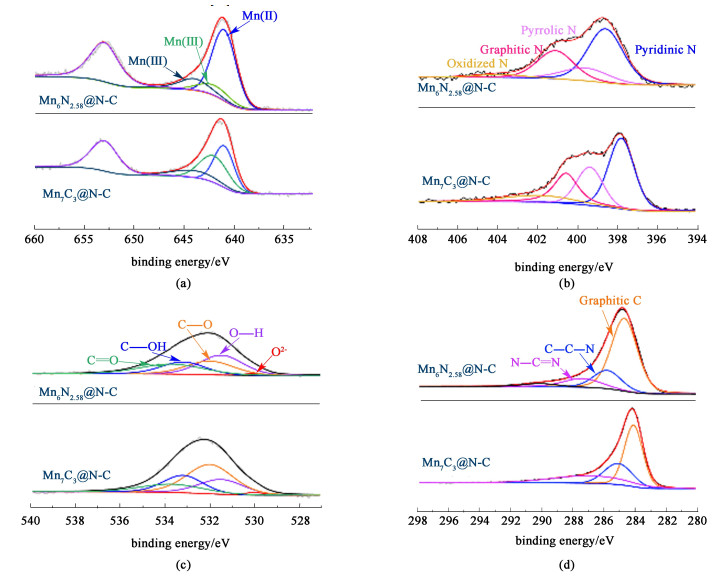
2.1.3 催化剂的X射线能谱(XPS)分析利用XPS对个元素进行了单独分峰,具体的分峰结果如图 3所示,具体的各组分含量在表 1列出。Mn 2p轨道在642和653 eV处有2个峰,分别对应于Mn 2p3/2和Mn 2p1/2。Mn 2p3/2在结合能为641、642和644 eV时可分为3个组分,分别对应着Mn2+、Mn3+和Mn4+[12]。可以看出Mn6N2.58@N-C的Mn2+、Mn3+和Mn4+分别占比为69.7%、19.3%和17.0%。相较于Mn7C3@N-C的48.7%,40.2%和11.1%来说,Mn6N2.58@N-C中Mn2+拥有更大的占比,更高的Mn2+占比可能是导致其性能和稳定性更好的主要原因。前人的研究解释了锰基催化剂活化高碘酸盐的机理[13],认为高碘酸盐的活化伴随着锰的氧化还原转化,根据Wang等[14]之前的早期研究,Mn2+与NaIO4混合会产生4价锰氧化物。这种锰形成的变化也暗示为反应溶液从2价锰无色到Mn-O(OH)2的棕色中间产物,同时产生O2·-,这种颜色变化与我们实际测试的现象相同。此外,高碘酸盐与O2·-之间的反应,会生成无毒无色的IO3-和1O2,4价锰会进一步被IO4-还原,生成Mn2+。在Mn2+/IO4-反应体系催化氧化降解BPA的过程中,高碘酸盐和碘酸盐同步形成进行还原分解。通过在高碘酸盐中加入碘酸盐的摩尔浓度,观察到碘的质量平衡良好,这表明高碘酸盐完全被还原为碘酸盐,并且在反应过程中没有产生其他碘的副产物[15]。这一结果表明,在降解过程中并未产生有毒的中间产物,并且高碘酸盐与Mn2+结合可原位生成高价Mn4+以及O2·-和1O2降解BPA,这个结果和我们淬灭实验所确定的活性氧物种是一致的。具体降解机理如下所示。
| $ \begin{gathered} \mathrm{Mn}^{2+}+2 \mathrm{IO}_4^{-}+\mathrm{O}_2+3 \mathrm{H}_2 \mathrm{O} \rightarrow \mathrm{Mn}-\mathrm{O}(\mathrm{OH})_2+ \\ 2 \mathrm{IO}_3^{-}+4 \mathrm{H}^{+}+2 \mathrm{O}_2^{·-} \end{gathered} $ | (1) |
| $ \mathrm{Mn-O}(\mathrm{OH})_2 \rightarrow \mathrm{MnO}_2+\mathrm{H}_2 \mathrm{O} $ | (2) |
| $ \mathrm{IO}_4^{-}+2 \mathrm{O}_2^{.-}+\mathrm{H}_2 \mathrm{O} \rightarrow \mathrm{IO}_3^{-}+2^1 \mathrm{O}_2+2 \mathrm{OH}^{-} $ | (3) |
| $ 2 \mathrm{O}_2^{.-}+2 \mathrm{H}_2 \mathrm{O} \rightarrow{ }^1 \mathrm{O}_2+\mathrm{H}_2 \mathrm{O}_2+2 \mathrm{OH}^{-} $ | (4) |
| $ \mathrm{Mn}-\mathrm{O}(\mathrm{OH})_2+\mathrm{IO}_4^{-} \rightarrow \mathrm{Mn}-(\mathrm{OH})_2+\mathrm{IO}_3^{-}+{ }^1 \mathrm{O}_2 $ | (5) |
在图 3(b)中我们将氮分别在398.6、399.6、401.1和403.9 eV分为4个组分[16],它们分别对应着吡啶氮(Pyridinic N)、吡咯氮(Pyrrolic N)、石墨氮(Graphitic N)和氧化氮(Oxidized N),各个物种的占比分别为37.5%、26.9%、15.0%和20.6%。图 3(c)中显示了5种氧物种,它们分别是O2-、O—H、C—O、C—OH和C=O,分别在530.0、531.5、532.0、533.2和533.7 eV的特征峰位置上,据报道,更多的O2-意味着存在的氧空位(Oxygen vacancy, OV)越少。O2-在所有氧物种中的比率(O2-/O)可以反映OV的含量[17]。2种Mn-N-C材料的O2-/O分别为4.5%和44.3%,这说明Mn6N2.58@N-C具有更高的表面OV浓度,因此其对阳离子的吸收能力增加,从而产生更好的催化性能,这和性能测试的结果是一致的。图 3 (d)中碳被分为3个组分,分别是石墨碳、C=C—N和N—C=N,对应的特征峰位置分别在285.0、286.0和288 eV[18]。
|
| 图 3 Mn-N-C催化剂的XPS图像Mn (a);N 1s (b);O 1s (c);C 1s (d) Fig.3 XPS images of Mn-N-C catalyst Mn (a); N 1s (b); O 1s (c); C 1s (d) |
| |
| component | mole fraction/% | ||
| Mn6N2.58@N-C | Mn7C3@N-C | ||
| N 1s | Pyridinic N | 54.2 | 37.5 |
| Pyrrolic N | 13.4 | 26.9 | |
| Graphitic N | 28.8 | 15.0 | |
| Oxidized N | 3.6 | 20.6 | |
| C 1s | Graphitic C | 77.8 | 50.3 |
| CC—N | 14.2 | 33.8 | |
| N—CN | 8.0 | 15.9 | |
| O 1s | O—H | 30.5 | 22.1 |
| O2- | 4.5 | 17.3 | |
| C—O | 26.8 | 33.7 | |
| C—OH | 13.7 | 15.9 | |
| CO | 24.5 | 11.0 | |
| Mn 2p | Mn2+ | 69.7 | 48.7 |
| Mn3+ | 13.3 | 40.2 | |
| Mn4+ | 17.0 | 11.1 | |
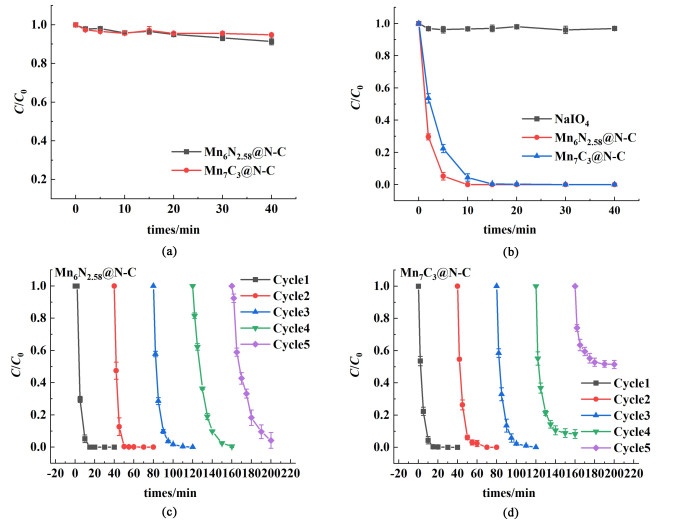
图 4 (a)中进行了吸附试验的测试,结果表明,2种Mn-N-C催化剂吸附的BPA < 10%。图 4(b)中进行了降解性能的测试,测试以NaIO4为氧化剂,在没有添加催化剂而仅有氧化剂的条件下,只有约14%的BPA减少量,这说明氧化剂本身对于污染物的降解很有限,结合加入催化剂的曲线,可以看出Mn6N2.58@N-C的可以在2 min内降解超过60%的2×10-5的双酚A溶液,并且在10 min之内将双酚A完全降解掉。而Mn7C3@N-C在2 min内也可以降解掉40%以上的双酚A,20 min之内降解100%的污染物。性能测试表明了2种Mn-N-C催化剂对活化高碘酸盐降解双酚A的过程均具有优异的催化氧化效果,其中Mn6N2.58@N-C拥有更加优异的性能。本实验中,我们分别对Mn6N2.58@N-C和Mn7C3@N-C进行了5次的循环试验,实验结果如图 4(b)所示,Mn6N2.58@N-C在前3轮循环过程中均可在20 min之内降解掉所有污染物,即使在第5次循环中依旧可以在40 min之内降解掉99%以上的双酚A, 这说明该催化剂具有良好的稳定性。Mn7C3@N-C的循环测试结果如图 4(c)所示,前3次循环中也可以在20 min之内降解掉所有的BPA,在第5次循环复用中,40 min的降解时间内也可以去除47%的BPA,催化剂的性能在前3次重复中可以保持稳定但后续出现明显的性能下降。使用电感耦合等离子体质谱(ICP-MS) 测试了催化剂使用前后的Mn的含量,表 2中分别给出了使用前和使用5次后催化剂中Mn元素的质量分数,结果表明,2种催化剂使用前后均出现了Mn元素含量的明显下降,这可能是由于在多次重复利用中,催化剂出现了离子的浸出从而导致性能下降。
|
| 图 4 (a) 催化剂的吸附实验测试;(b)催化剂的吸附性能测试;(c)Mn6N2.58@N-C的稳定性测试;(d)Mn7C3@N-C的稳定性测试 Fig.4 Adsorption experiment test of catalyst (a); performance test (b); stability test of Mn6N2.58@N-C (c); stability test of Mn7C3@N-C of catalysts (d) |
| |
| Samples | Mn6N2.58@N-C中 Mn的质量分数/% |
Mn7C3@N-C中 Mn的质量分数/% |
| Fresh | 21.61 | 22.47 |
| Used 5th | 18.23 | 14.45 |
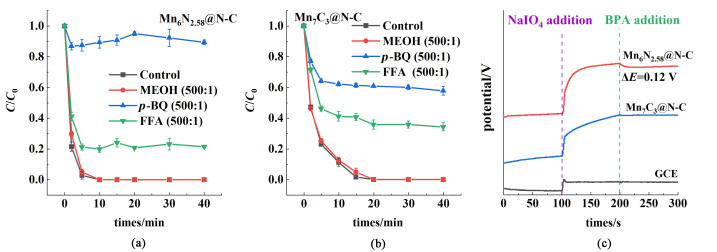
自由基猝灭实验被用来检测反应体系中产生的各类自由基[19-21]。甲醇(MEOH)通常被添加到反应体系中,用来做羟基自由基(·OH)的猝灭剂[19, 22]。它和·OH具有较高的反应速率,因此可以迅速地消耗反应过程中产生的·OH。同理,使用对苯醌(p-BQ)用来猝灭反应过程中生成的超氧自由基(O2·-)[23]。呋喃甲醇(FFA)与单线氧(1O2)有着较高的反应速率而被应用于1O2的猝灭[24]。在本节中,为了探究Mn-N-C催化剂的反应机理,我们分别使用上述3种猝灭剂对催化剂进行了自由基猝灭实验。对Mn6N2.58@N-C来说,反应体系中添加的甲醇与氧化剂NaIO4的添加量物质的量之比为500 ∶1,其降解效果和对照组的降解曲线基本一致[图 5(a)],因此认为反应体系中并不存在·OH。而在p-BQ猝灭O2·-的实验中,降解速率出现了明显的降低,40 min的降解过程中,在第1个取样点2 min以后,几乎停止降解,最终也只有约12%的BPA被除去,这说明反应体系中有较高浓度的O2·-。实验使用了物质的量之比500 ∶1的FFA对1O2进行检测,出现了明显的抑制效果,说明Mn6N2.58/NaIO4体系中,存在部分1O2。如图 5(b)所示,Mn7C3@N-C中的抑制过程也呈现与上述相同的结果。因此2种Mn-N-C材料在活化高碘酸盐过程中具有相同的活性氧物种。同时,在碳基催化剂的降解中,常常会伴随着直接电子转移过程(Direct Electron Transfer,DET)。在该过程中,催化剂的表面会发生由污染物BPA到氧化剂NaIO4电子转移,而不产生自由基,实验使用开路电位测试(Open-Circuit Potential, OCP)来验证这一过程的存在。这一过程中,我们使用了未涂抹催化剂的玻碳电极(Glassy Carbon Electrode, GCE)作为对比样,使用滴加了含有催化剂的Ink的玻碳电极作为目标样。在100 s时,在电解池中一次性注入2 mL NaIO4溶液,因为高碘酸钠是一种强电解质,因此,它的加入会导致开路电压的显著变化,这是由于催化剂和NaIO4之间有一定的相互作用,从而导致电子重新排布[25]。待到电势稳定后,对反应体系注入5 mL的1×10-4的BPA溶液,BPA作为有机物分在水体环境中几乎不再电离,因此引起的电位变化主要由于直接电子转移所引起的,可以观察电位变化,来判断反应体系是否存在DET过程[25, 26]。实验结果如图 5(c)所示,添加Mn6N2.58@N-C的玻碳电极出现了约为0.012 V的电位变化,这表明BPA向Mn6N2.58@N-C/NaIO4复合物的电子转移过程[27]。而Mn7C3@N-C中并未出现明显变化,这说明只有Mn6N2.58@N-C中存在着DET过程。
|
| 图 5 Mn6N2.58@N-C的猝灭实验(a); Mn7C3@N-C的猝灭实验(b)和OCP测试(c) Fig.5 Mn6N2.58@N-C Quenching experiment (a); Mn7C3@N-C Quenching experiment (b) and OCP test (c) |
| |
从上述结论中我们可以总结出,Mn6N2.58@N-C催化氧化BPA的过程是由自由基O2·-和非自由基1O2所共同主导的过程,并且在该过程中伴随着直接电子转移过程。而Mn7C3@N-C的催化氧化过程是由自由基O2·-和非自由基1O2共同主导,并不存在直接电子转移途径。
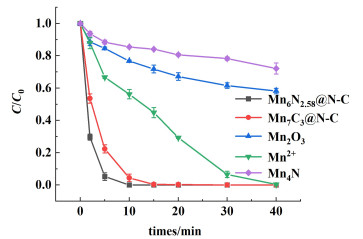
2.4 常见含锰催化剂的性能对比为了验证本试验所制备的催化剂的性能表现的优异性,我们分别选取了一些常见的锰系催化剂(Mn4N、Mn2O3和MnCl2)进行BPA降解的性能比较。如图 6所示,5种催化剂中表现最差的是Mn4N,在10 min内仅可以降解8%左右的BPA分子,即使在40 min的完整测试时间内也仅仅可以降解掉约28%的BPA。而常被用于催化氧化的锰的氧化物(Mn2O3),在40 min的去除效率为60%,这和我们所制备的Mn-N-C催化剂具有明显的性能差异。均相的MnCl2在除去本实验制备的Mn-N-C催化剂外,表现出了最好的降解效果,可以在40 min内将BPA分子完全氧化掉,这个结果和相关的研究报道相吻合[8]。本实验制备的Mn-N-C催化剂在降解速率还是降解效果上都大大超过传统的锰系催化剂,这说明本实验的催化剂有着优异的催化氧化能力,具有较强的实际利用价值。
|
| 图 6 常见锰系催化剂性能对比 Fig.6 Performance comparison of common manganese based catalysts |
| |
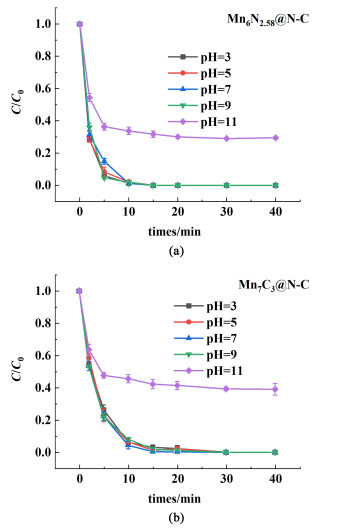
催化反应条件是催化剂性能的关键因素,本节测试了不同初始pH值条件下(pH=3~11),催化剂活化NaIO4降解目标污染物BPA的性能测试。结果如图 7所示,在pH=3~9的范围内,2种Mn-N-C催化剂的性能基本没有变化,而在pH=11时,2种催化剂均出现了明显的性能下降。这是由于在溶液碱性较强时,催化剂的表面也可能会带上负电荷,从而排斥IO4-,造成催化性能的下降[28]。
|
| 图 7 不同初始pH条件下的性能测试(a) Mn6N2.58@N-C;(b) Mn7C3@N-C Fig.7 Performance testing under different initial pH conditions (a) Mn6N2.58@N-C; (b) Mn7C3@N-C |
| |
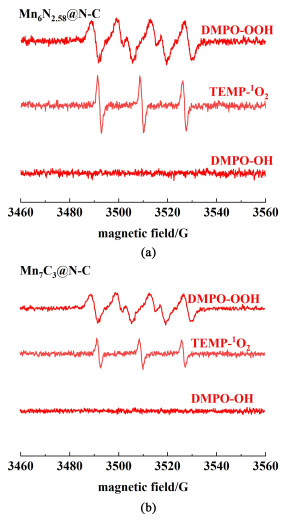
为了进一步研究Mn-N-C/NaIO4系统中的ROSs,本节进行了电子顺磁共振(EPR)测试。经过5 min的降解反应后,检测溶液中的自由基。DMPO和TEMP作为探针化合物,可与自由基形成自旋加合物,来分别证明·OH、O2·-和1O2的存在[29-32]。Mn6N2.58@N-C和Mn7C3@N-C检测结果分别如图 8(a)和图 8(b)所示。结果表明,2种Mn-N-C材料可观察到DMPO-OOH和TEMP-1O2的典型EPR特征峰信号,这证明了反应体系中O2·-和1O2的存在。
|
| 图 8 EPR测试(a) Mn6N2.58@N-C;(b) Mn7C3@N-C Fig.8 EPR test (a) Mn6N2.58@N-C; (b) Mn7C3@N-C |
| |
利用乙酰丙酮锰和三聚氰胺在不同的煅烧温度下制备了2种不同的Mn-N-C材料,分别是Mn6N2.58@N-C和Mn7C3@N-C,2种锰系材料在活化NaIO4降解BPA分子的过程中都表现出了良好的降解效果,在3次的循环利用内也都表现出了优异的稳定性。在TEM中,可以明显地看出2种晶体均处于碳氮层的包裹之中,这样的包裹结构可以有效地降低离子浸出,提高电子转移速率,并为催化剂的结构稳定性提供了支撑。猝灭实验表明了这2种催化剂的主要活性氧物种为O2·-和1O2,这与曾经所发表的锰系催化剂活化高碘酸盐的工作结论相同。进一步通过XPS的测试,证明了两者间的性能差异主要是由于其主要活化作用的Mn2+含量不同所引起的。制备的Mn-N-C材料不但具有优异的催化性能还具有较好的稳定性,这会在实际应用过程中有很大的优势。综上所述,本研究的Mn-N-C材料是一种制备简单,性能优异,稳定性好的锰系催化剂,这为过渡金属催化剂的研究提供了补充。
| [1] |
FAN X, YU Y, DONG S, et al. Heteroatoms-doped biochar derived from deciduous resource as persulfate catalysts for efficient degradation of phenol[J]. Journal of Water Process Engineering, 2022, 48: 102866. DOI:10.1016/j.jwpe.2022.102866 |
| [2] |
CAO S, CHEN H, DONG B, et al. Nitrogen-rich metal-organic framework mediated Cu-N-C composite catalysts for the electrochemical reduction of CO2[J]. Journal of Energy Chemistry, 2021, 54: 555-563. DOI:10.1016/j.jechem.2020.06.038 |
| [3] |
陈立功, 白国义, 许正双, 等. 三乙烯二胺的合成催化剂的筛选[J]. 天津大学学报(自然科学与工程技术版), 2000, 33(5): 638-640. CHEN Ligong, BAI Guoyi, XU Zhengshuang, et al. Selection of catalysts for synthesis of triethylenediamine[J]. Journal of Tianjin University (Science and Technology), 2000, 33(5): 638-640. (in Chinese) |
| [4] |
ZHAO Z, ZHOU W, LIN D, et al. Construction of dual active sites on diatomic metal (FeCo-N/Cx) catalysts for enhanced Fenton-like catalysis[J]. Applied Catalysis B: Environmental, 2022, 309: 121256. DOI:10.1016/j.apcatb.2022.121256 |
| [5] |
LI J, ZHAO S, ZHANG L, et al. Cobalt single atoms embedded in nitrogen-doped graphene for selective oxidation of benzyl alcohol by activated peroxymonosulfate[J]. Small, 2021, 17(16): 2004579. DOI:10.1002/smll.202004579 |
| [6] |
LEE C H, YOON J. Application of photoactivated periodate to the decolorization of reactive dye: Reaction parameters and mechanism[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2004, 165(1/2/3): 35-41. |
| [7] |
CHADI N E, MEROUANI S, HAMDAOUI O, et al. H2O2/periodate (IO4-): A novel advanced oxidation technology for the degradation of refractory organic pollutants[J]. Environmental Science: Water Research & Technology, 2019, 5(6): 1113-1123. |
| [8] |
DU J, TANG S, LING H, et al. Insights into periodate oxidation of bisphenol A mediated by Manganese[J]. Chemical Engineering Journal, 2019, 369: 1034-1039. DOI:10.1016/j.cej.2019.03.158 |
| [9] |
王静, 汪恂, 陈沾, 等. 镧、钇共掺杂纳米ZnO的制备及处理染料废水研究[J]. 工业水处理, 2017, 37(1): 82-85, 94. WANG Jing, WANG Xun, CHEN Zhan, et al. Research on the preparation of La and Y co-doped nano-ZnO and its application to the treatment of wastewater containing dyestuff[J]. Industrial Water Treatment, 2017, 37(1): 82-85, 94. (in Chinese) |
| [10] |
易学睿. 过渡金属基电催化剂的表面结构设计及性能研究[D]. 北京: 北京化工大学, 2021 YI Xuerui. Study on surface structure design and properties of transition metal-based electrocatalysts[D]. Beijing: Beijing University of Chemical Technology, 2021 (in Chinese) |
| [11] |
OH W D, DONG Z, LIM T T. Generation of sulfate radical through heterogeneous catalysis for organic contaminants removal: Current development, challenges and prospects[J]. Applied Catalysis B: Environmental, 2016, 194: 169-201. DOI:10.1016/j.apcatb.2016.04.003 |
| [12] |
FANG H, WANG C, LI D, et al. Fabrication of Ag@Ag2O-MnOx composite nanowires for high-efficient room-temperature removal of formaldehyde[J]. Journal of Materials Science & Technology, 2021, 91: 5-16. |
| [13] |
WANG Z, BAO J, DU J, et al. Sulfamethoxazole degradation by alpha-MnO2/periodate oxidative system: Role of MnO2 crystalline and reactive oxygen species[J]. Environmental Science and Pollution Research, 2022, 29(29): 44732-44745. DOI:10.1007/s11356-022-18901-z |
| [14] |
YANG B, CHAN S, CHANG W, et al. Surface enrichment in mixed oxides of Cu, Co, and Mn, and its effect on CO oxidation[J]. Journal of Catalysis, 1991, 130(1): 52-61. DOI:10.1016/0021-9517(91)90091-H |
| [15] |
LONG Y, DAI J, ZHAO S, et al. Atomically dispersed cobalt sites on graphene as efficient periodate activators for selective organic pollutant degradation[J]. Environmental Science & Technology, 2021, 55(8): 5357-5370. |
| [16] |
CHEN J, LI H, FAN C, et al. Dual single-atomic Ni-N4 and Fe-N4 sites constructing Janus hollow graphene for selective oxygen electrocatalysis[J]. Advanced Materials, 2020, 32(30): 2003134. DOI:10.1002/adma.202003134 |
| [17] |
ZHANG H, LI C, LYU L, et al. Surface oxygen vacancy inducing peroxymonosulfate activation through electron donation of pollutants over cobalt-zinc ferrite for water purification[J]. Applied Catalysis B: Environmental, 2020, 270: 118874. DOI:10.1016/j.apcatb.2020.118874 |
| [18] |
XIONG Y, DONG J, HUANG Z, et al. Single-atom Rh/N-doped carbon electrocatalyst for formic acid oxidation[J]. Nature Nanotechnology, 2020, 15(5): 390-397. DOI:10.1038/s41565-020-0665-x |
| [19] |
DONG Q, WANG J, DUAN X, et al. Self-assembly of 3D MnO2/N-doped graphene hybrid aerogel for catalytic degradation of water pollutants: Structure-dependent activity[J]. Chemical Engineering Journal, 2019, 369: 1049-1058. DOI:10.1016/j.cej.2019.03.139 |
| [20] |
DUAN X, SUN H, WANG S. Metal-free carbocatalysis in advanced oxidation reactions[J]. Accounts of Chemical Research, 2018, 51(3): 678-687. DOI:10.1021/acs.accounts.7b00535 |
| [21] |
YANG M, ZHANG Z, LIN K. One-step fabrication of cobalt-embedded carbon nitride as a magnetic and efficient heterogeneous catalyst for activating oxone to degrade pollutants in water[J]. Separation and Purification Technology, 2019, 210: 1-9. DOI:10.1016/j.seppur.2018.07.086 |
| [22] |
ZHOU Y, JIANG J, GAO Y, et al. Activation of peroxymonosulfate by benzoquinone: A novel nonradical oxidation process[J]. Environmental Science & Technology, 2015, 49(21): 12941-12950. |
| [23] |
ZENG H, DENG L, ZHANG H, et al. Development of oxygen vacancies enriched CoAl hydroxide@hydroxysulfide hollow flowers for peroxymonosulfate activation: A highly efficient singlet oxygen-dominated oxidation process for sulfamethoxazole degradation[J]. Journal of Hazardous Materials, 2020, 400: 123297. DOI:10.1016/j.jhazmat.2020.123297 |
| [24] |
LI H, TIAN J, ZHU Z, et al. Magnetic nitrogen-doped nanocarbons for enhanced metal-free catalytic oxidation: Integrated experimental and theoretical investigations for mechanism and application[J]. Chemical Engineering Journal, 2018, 354: 507-516. DOI:10.1016/j.cej.2018.08.043 |
| [25] |
TAN W, REN W, WANG C, et al. Peroxymonosulfate activated with waste battery-based Mn-Fe oxides for pollutant removal: Electron transfer mechanism, selective oxidation and LFER analysis[J]. Chemical Engineering Journal, 2020, 394: 124864. DOI:10.1016/j.cej.2020.124864 |
| [26] |
AHN Y Y, BAE H, KIM H I, et al. Surface-loaded metal nanoparticles for peroxymonosulfate activation: Efficiency and mechanism reconnaissance[J]. Applied Catalysis B: Environmental, 2019, 241: 561-569. DOI:10.1016/j.apcatb.2018.09.056 |
| [27] |
WANG J, DUAN X, GAO J, et al. Roles of structure defect, oxygen groups and heteroatom doping on carbon in nonradical oxidation of water contaminants[J]. Water Research, 2020, 185: 116244. DOI:10.1016/j.watres.2020.116244 |
| [28] |
LI B, MA B, WEI M, et al. Synthesis of Co-NC catalysts from spent lithium-ion batteries for Fenton-like reaction: Generation of singlet oxygen with ~100% selectivity[J]. Carbon, 2022, 197: 76-86. DOI:10.1016/j.carbon.2022.06.029 |
| [29] |
WU X, ZHAO Q, GUO F, et al. Porous g-C3N4 and α-FeOOH bridged by carbon dots as synergetic visible-light-driven photo-Fenton catalysts for contaminated water remediation[J]. Carbon, 2021, 183: 628-640. DOI:10.1016/j.carbon.2021.07.006 |
| [30] |
WU X, LIU T, NI W, et al. Engineering controllable oxygen vacancy defects in iron hydroxide oxide immobilized on reduced graphene oxide for boosting visible light-driven photo-Fenton-like oxidation[J]. Journal of Colloid and Interface Science, 2022, 623: 9-20. DOI:10.1016/j.jcis.2022.04.094 |
| [31] |
WU X, ZHAO Q, ZHANG J, et al. 0D carbon dots intercalated Z-scheme CuO/g-C3N4 heterojunction with dual charge transfer pathways for synergetic visible-light-driven photo-Fenton-like catalysis[J]. Journal of Colloid and Interface Science, 2023, 634: 972-982. DOI:10.1016/j.jcis.2022.12.052 |
| [32] |
YU X, WU X, GUO F, et al. Visible-light-assisted activation of peroxymonosulfate (PMS) over CoOx@C/g-C3N4 composite for efficient organic pollutant degradation[J]. Journal of Alloys and Compounds, 2023, 948: 169702. DOI:10.1016/j.jallcom.2023.169702 |
 2025, Vol. 42
2025, Vol. 42





