硝酸硫康唑是一种抑制真菌生长的常用药物,能够抑制真菌细胞膜麦角甾醇的生物合成,影响细胞膜的通透性。可用于治疗浅表和深部真菌病,如皮肤和指甲癣、阴道白色念珠菌病、胃肠真菌感染等,以及由白色念珠菌、类球孢子菌、组织胞浆菌等引起的全身感染[1, 2]。在制备硝酸硫康唑原料药的过程中,使用的硫酸烷基酯类试剂硫酸二甲酯、硫酸二乙酯容易在成品中残留。硫酸二甲酯和硫酸二乙酯是已知的具有致癌致畸作用的试剂[3, 4],ICH M7分类为2类[5, 6],需要作为基因毒性杂质进行研究控制[7, 8]。因此针对其痕量残留建立一个快速、高效的检测方法至关重要。
目前针对硫酸二甲酯、硫酸二乙酯的检测方法已有报道,如李一婧等[9]用气相色谱火焰光谱法检测新型抗结核药物E-10-(4-三氟甲氧基苯基)-2, 10-二氢-3-(2-甲氧基-3-吡啶)氨基-2-(反-4-甲氧基环己基)亚胺吩嗪中硫酸二甲酯和硫酸二乙酯残留;吴楚林等[10]用气相色谱-质谱联用测定化妆品中硫酸二甲酯和硫酸二乙酯。但使用气相色谱火焰光谱法或气相色谱-质谱联用法检测痕量硫酸二甲酯和硫酸二乙酯,需要制备高浓度样品[11, 12],直接进样不可取,存在严重的污染问题,影响衬管、气相毛细管色谱柱[13, 14];且在高温加热过程中,硫酸烷基酯类试剂经常会与高浓度的主成分发生烷基化反应,导致回收率偏低[15],影响样品检测的准确度。Alzaga等[16]通过使用五氟苯硫酚作为衍生化试剂,使目标化合物衍生成更稳定的待分析物,顶空进样,但空白样中会有来自五氟苯硫酚甲基衍生物的高度干扰,影响低浓度水平加标回收率。
通过衍生化反应得到稳定的衍生化产物,提高灵敏度[17],降低样品制备浓度,减小污染,是一个很好的控制策略[18, 19]。本研究使用的LC-MS法,与气相毛细管色谱柱相比,液相色谱柱通常可以耐受更高的样品量[20, 21],故系统引起污染的问题较少[22];另外,使用三乙胺作为衍生化试剂,对硫酸二甲酯和硫酸二乙酯衍生化,可以提高灵敏度,降低样品制备浓度,并且在空白中对衍生物的干扰极小,在低、中、高3个浓度水平下的加标回收率均良好。本研究将衍生化与LC-MS法相结合,建立了一种快速测定硝酸硫康唑中硫酸二甲酯、硫酸二乙酯的分析方法,满足硝酸硫康唑中基因毒性杂质硫酸二甲酯、硫酸二乙酯痕量检测要求,为市场监管部门对硝酸硫康唑原料药中硫酸烷基酯类的痕量监测提供了技术支持。
1 实验部分 1.1 仪器与试剂LC-QQQ 1290II-G6470B三重串联四极杆液质联用仪;数显恒温水浴锅;2~20 μL、20~200 μL、100~1 000 μL和0.5~5 mL移液器;MS205DU电子天平、XP6电子天平、XPR2电子天平。
硫酸二甲酯对照品,美国SINCO公司,批号:21-09-0801,质量分数为96.92%;硫酸二乙酯对照品,日本TCI公司,批号:Z6PGH-BE,质量分数为99.7%;实验用水,超纯水,自制;甲酸铵,德国Sigma-Aldrich公司,LC-MS级;甲酸,美国Fisher公司,LC-MS级;乙腈,德国Merck公司,LC-MS级;三乙胺,上海阿拉丁生化科技股份有限公司,色谱级;硝酸硫康唑,山东京卫制药有限公司,批号:221031-0904、221107-2902、221110-2901、221121-1601、221121-2903、221124-2902、221130-0101、221201-2901、2212909-4和2212909-5。
1.2 色谱条件与质谱条件 1.2.1 色谱条件流动相A:20 mmol ·L-1甲酸铵溶液-甲酸(1 000 ∶1);流动相B:乙腈;流动相:流动相A-流动相B(10 ∶90);色谱柱:Waters Atlantis HILIC Silica(2.1 mm×50 mm,3 μm);流速:0.2 mL ·min-1;柱温:20 ℃;进样体积:1 μL;进样器温度:5 ℃。
1.2.2 质谱条件离子源:AJS ESI;极性:正;干燥气流量:8 L ·min-1;干燥气温度:300 ℃;喷雾器压力:2.41×105 Pa;鞘气流量:11 L ·min-1;鞘气温度:325 ℃;毛细管电压:3 500 V;喷嘴电压:0 V;加速电压:3 V;扫描模式:MRM;驻留时间:250 ms;碎裂电压:100 V;碰撞能量:25 eV;硫酸二甲酯衍生物离子对:116.1→72.1;硫酸二乙酯衍生物离子对:130.0→86.1。
1.3 实验方法衍生化试剂:精密量取三乙胺5 mL,置50 mL量瓶中,加水,置2~8 ℃溶解,转移至室温,稀释至刻度,摇匀,即得衍生化试剂。
空白溶液:精密量取乙腈1 mL及衍生化试剂100 μL,置2 mL液相进样小瓶,50 ℃下水浴加热15 h,待测定。
900 ng ·mL-1对照品贮备液:分别取硫酸二甲酯、硫酸二乙酯约9 mg,精密称定,置20 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀;精密量取20 μL,置10 mL量瓶中,用乙腈稀释至刻度,摇匀,即得。
9 ng ·mL-1对照品溶液:精密量取900 ng ·mL-1对照品贮备液100 μL,置10 mL量瓶中,用乙腈稀释至刻度,摇匀;精密量取上述溶液1 mL及衍生化试剂100 μL,置2 mL液相进样小瓶中,在50 ℃下水浴加热15 h,待测定。
供试品溶液:取硝酸硫康唑约30 mg,精密称定,置10 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀;精密量取1 mL,置10 mL量瓶中,用乙腈稀释至刻度,摇匀;精密量取上述溶液1 mL及衍生化试剂100 μL,置2 mL液相进样小瓶中,50 ℃下水浴加热15 h,待测定。
所配制的空白溶液、对照品溶液及供试品溶液在1.2项色谱条件与质谱条件下进行分析,采用外标法进行数据处理,即可得到硫酸二甲酯和硫酸二乙酯的含量。
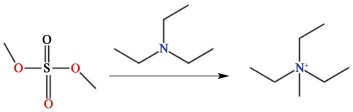
2 结果与讨论 2.1 空白干扰的处理采用三乙胺将硫酸二甲酯衍生化,衍生化产物三乙基甲基季铵盐在质谱正离子模式下响应较为灵敏。通过LC-MS法检测衍生化产物的方法间接检测硫酸二甲酯的含量。硫酸二甲酯衍生化机理如图 1所示。
|
| 图 1 硫酸二甲酯衍生化机理 Fig.1 Derivatization mechanism of dimethyl sulfate |
| |
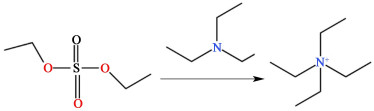
根据上述衍生化机理,硫酸二乙酯经三乙胺衍生化后,衍生物为四乙基季铵盐。硫酸二乙酯衍生化机理如图 2所示。
|
| 图 2 硫酸二乙酯衍生化机理 Fig.2 Derivatization mechanism of diethyl sulfate |
| |
衍生化试剂三乙胺中含有少量的三乙基甲基季铵盐,即空白溶剂中能检出三乙基甲基季铵盐而产生干扰。因其含量相对较少,且在三乙胺加入量固定的情况下,空白溶剂中目标物的峰面积可重现,可以通过从对照品溶液或者供试品溶液中扣除空白溶液中面积的方法,去除干扰。
2.2 前处理条件的优化加标供试品溶液:取硝酸硫康唑约30 mg,精密称定,置10 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀;精密量取上述溶液1 mL及“ 1.3 ”项下900 ng ·mL-1对照品贮备液100 μL,置10 mL量瓶中,用乙腈稀释至刻度,摇匀;精密量取1 mL及衍生化试剂100 μL,置2 mL液相进样小瓶中,50 ℃下水浴加热15 h,待测定。
衍生化时间和温度会影响到衍生化是否完全,因此考察50 ℃下水浴加热15 h、50 ℃下水浴加热14.5 h、50 ℃下水浴加热15.5 h、45 ℃下水浴加热15 h、55 ℃下水浴加热15 h,不同衍生化条件下衍生化产物的变化。不同衍生化条件的峰面积与衍生化(50 ℃,15 h)条件下相比,加标供试品溶液中硫酸二乙酯衍生物峰面积比值为90.3%~97.4%,硫酸二甲酯衍生物峰面积比值为93.9%~98.0%。以上证明50 ℃下水浴加热15 h衍生化条件下已经衍生完全。
2.3 控制限度硝酸硫康唑原料药用于国内上市制剂硝酸硫康唑喷雾剂,为皮肤外用制剂,原研药(美国上市剂型为外用溶液、乳膏)说明书中未规定最大日剂量,用法为直接喷施本品少量并均匀分布于患处及其周围皮肤,1日2次。经文献检索,未查询到本品制剂以及本品用于给药途径为皮肤外用的其他原研制剂的最大日剂量。山东京卫制药有限公司喷雾剂规格为1%,包装规格分别为每瓶10 mL、每瓶30 mL。为了严格控制本品质量,计算遗传毒性杂质限度时,最大日剂量按每日使用5 mL(10 g ·L-1、50 mg)计算。硫酸二甲酯和硫酸二乙酯是已知的具有致癌致畸作用的化合物,ICH M7分类为2类,需要作为基因毒性杂质进行研究。ICH M7中收载硫酸二甲酯的PDE为1.5 μg ·d-1,本研究以30 μg ·g-1作为硝酸硫康唑中硫酸二甲酯的控制限度;参照硫酸二甲酯,以30 μg ·g-1作为硝酸硫康唑中硫酸二乙酯的控制限度。
2.4 质谱解析硫酸二甲酯衍生化产物的质谱图中,m/z 116.1为[M+H]+离子,在碎裂电压为100 V时响应最高;m/z 72.1为主要碎片离子,在碰撞能量为25 eV时响应最高。因此,选择m/z 116.1→72.1作为MRM扫描模式下的定量离子对。
硫酸二乙酯衍生化产物的质谱图中,m/z 130.0为[M+H]+离子,在碎裂电压为100 V时响应最高;m/z 86.1为主要碎片离子,在碰撞能量为25 eV时响应最高。因此,选择m/z 130.0→86.1作为MRM扫描模式下的定量离子对。
2.5 专属性空白溶液:精密量取乙腈1 mL及衍生化试剂100 μL,置2 mL液相进样小瓶,50 ℃下水浴加热15 h,待测定。
硫酸二甲酯溶液:取硫酸二甲酯约9 mg,精密称定,置20 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀;精密量取20 μL,置10 mL量瓶中,用乙腈稀释至刻度,摇匀;精密量取100 μL,置10 mL量瓶中,用乙腈稀释至刻度,摇匀;精密量取1 mL及衍生化试剂100 μL,置2 mL液相进样小瓶,50 ℃下水浴加热15 h,待测定。
硫酸二乙酯溶液:取硫酸二乙酯约9 mg,精密称定,置20 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀;精密量取20 μL,置10 mL量瓶中,用乙腈稀释至刻度,摇匀;精密量取100 μL,置10 mL量瓶中,用乙腈稀释至刻度,摇匀;精密量取1 mL及衍生化试剂100 μL,置2 mL液相进样小瓶,50 ℃下水浴加热15 h,待测定。
加标供试品溶液:取硝酸硫康唑约30 mg,精密称定,置10 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀;精密量取上述溶液1 mL及“ 1.3 ”项下900 ng ·mL-1对照品贮备液100 μL,置10 mL量瓶中,用乙腈稀释至刻度,摇匀;精密量取1 mL及衍生化试剂100 μL,置2 mL液相进样小瓶,50 ℃下水浴加热15 h,待测定。
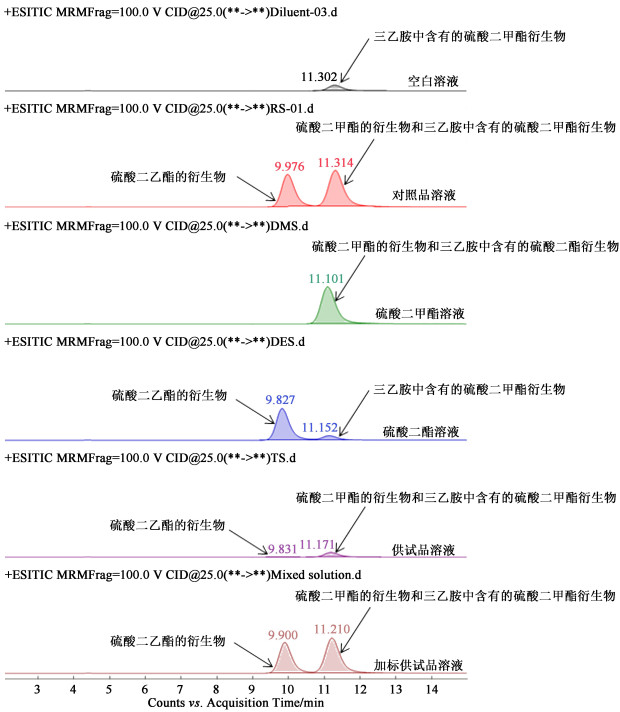
取空白溶液、硫酸二甲酯溶液、硫酸二乙酯溶液、“ 1.3 ”项下9 ng ·mL-1对照品溶液、“ 1.3 ”项下供试品溶液及加标供试品溶液进样,考察专属性,谱图对比情况如图 3所示。衍生化试剂三乙胺中含有少量的三乙基甲基季铵盐(即硫酸二甲酯衍生物),因此在衍生化后的所有溶液中也会存在,因其含量较少,可通过扣除衍生化后乙腈中面积的方法去除干扰。乙腈与供试品不干扰硫酸二甲酯衍生物、硫酸二乙酯衍生物检查,分离度均不小于1.5。表明该方法专属性良好。
|
| 图 3 专属性考察谱图对比 Fig.3 Comparison of mass spectrogram of specificity |
| |
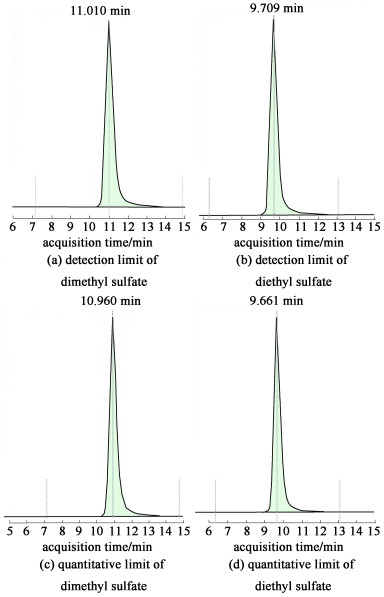
用乙腈对“ 1.3 ”项下的900 ng ·mL-1对照品贮备液逐级稀释,配制成系列质量浓度的线性溶液,浓度为1.8、4.5、9、10.8、13.5 ng ·mL-1;分别精密量取1 mL及衍生化试剂100 μL,置2 mL液相进样小瓶,50 ℃下水浴加热15 h。采用本方法对线性溶液进行分析。以目标化合物的质量浓度为横坐标(x,ng ·mL-1),峰面积为纵坐标(y)绘制标准曲线,线性方程如表 1所示,线性相关系数r均大于0.99,表明在1.8~13.5 ng ·mL-1范围内,硫酸二甲酯及硫酸二乙酯的衍生物线性良好。逐步稀释,考察检测限及定量限,结果如图 4所示。检测限浓度为0.54 ng ·mL-1,信噪比大于3;定量限浓度为1.8 ng ·mL-1,信噪比大于10;表明硫酸二甲酯及硫酸二乙酯的衍生物检测限、定量限良好。
| 参数 | 硫酸二甲酯 | 硫酸二乙酯 |
| 线性方程 | y=21384.640x- 2989.110 | y=23845.541x+ 34110.671 |
| 范围/(ng·mL-1) | 1.8~13.5 | 1.8~13.5 |
| r | 0.999 7 | 0.998 9 |
| 检测限/(ng·mL-1) | 0.54 | 0.54 |
| 定量限/(ng·mL-1) | 1.8 | 1.8 |
|
| 图 4 检测限、定量限质谱图 Fig.4 Mass spectrogram of detection limit and quantitative limit |
| |
取硝酸硫康唑约30 mg,精密称定9份,分别置10 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀;精密量取1 mL,置10 mL量瓶中,精密量取“ 1.3 ”项下900 ng ·mL-1对照品贮备液20 μL、100 μL、120 μL置上述量瓶中,用乙腈稀释至刻度,摇匀,即得低(1.8 ng ·mL-1,3份)、中(9 ng ·mL-1,3份)、高(10.8 ng ·mL-1,3份)3个浓度的加标供试品溶液;精密量取1 mL及衍生化试剂100 μL,置2 mL液相进样小瓶,50 ℃下水浴加热15 h,进样,考察准确度。结果如表 2和表 3所示,在上述3个加标水平下,硫酸二甲酯衍生物回收率为80.3%~102.3%,回收率的RSD值为8.5%;硫酸二乙酯衍生物回收率为90.3%~100.0%,回收率的RSD值为3.2%。表明该方法准确度良好。
| 化合物 | 加入量/ ng | 测得量/ ng | 回收率/ % | 平均回收率/% | RSD/ % |
| 硫酸二甲酯 | 18.180 | 14.590 | 80.3 | 92.2 | 8.5 |
| 18.180 | 14.940 | 82.2 | |||
| 18.180 | 15.590 | 85.8 | |||
| 90.901 | 86.160 | 94.8 | |||
| 90.901 | 84.510 | 93.0 | |||
| 90.901 | 85.340 | 93.9 | |||
| 109.082 | 107.390 | 98.4 | |||
| 109.082 | 107.900 | 98.9 | |||
| 109.082 | 111.580 | 102.3 |
| 化合物 | 加入量/ ng | 测得量/ ng | 回收率/ % | 平均回收率/% | RSD/ % |
| 硫酸二乙酯 | 19.047 | 17.200 | 90.3 | 94.7 | 3.2 |
| 19.047 | 17.520 | 92.0 | |||
| 19.047 | 18.080 | 94.9 | |||
| 95.233 | 89.510 | 94.0 | |||
| 95.233 | 88.560 | 93.0 | |||
| 95.233 | 89.790 | 94.3 | |||
| 114.280 | 109.280 | 95.6 | |||
| 114.280 | 111.940 | 98.0 | |||
| 114.280 | 114.300 | 100.0 |
按照“ 2.5 ”项下加标供试品溶液制备方法,平行制备6份,考察重复性。不同时间,不同人员进行重复性试验。6份加标供试品溶液中硫酸二甲酯含量的RSD值为1.6%,硫酸二乙酯含量的RSD值为1.6%。表明该方法重复性良好。计算12份加标供试品溶液中硫酸二甲酯含量的RSD值为5.2%,硫酸二乙酯含量的RSD值为5.6%。表明该方法中间精密度良好。
2.8 稳定性取“ 1.3 ”项下9 ng ·mL-1对照品溶液、供试品溶液及“ 2.5 ”项下加标供试品溶液,连续进行48 h稳定性分析,峰面积与0 h比值为均在0.70~1.25范围内,表明9 ng ·mL-1对照品溶液、供试品溶液及加标供试品溶液在48 h内稳定性良好。
2.9 样品测定按“ 1.3 ”项下制备硝酸硫康唑供试品溶液,照“ 1.2 ”项下色谱条件与质谱条件进行检测,记录提取离子流图。结果如表 4所示,硫酸二甲酯、硫酸二乙酯均有检出,残留量均未超过其控制限度(30 μg ·g-1)。
| 批号 | 硫酸二甲酯含量/ (μg·g-1) | 硫酸二乙酯含量/ (μg·g-1) |
| 221031-0904 | 1.1 | 0.6 |
| 221107-2902 | 1.2 | 1.1 |
| 221110-2901 | 2.9 | 1.5 |
| 221121-1601 | 1.0 | 0.9 |
| 221121-2903 | 0.9 | 1.2 |
| 221124-2902 | 0.7 | 1.1 |
| 221130-0101 | 0.8 | 0.9 |
| 221201-2901 | 0.7 | 0.8 |
| 2212909-4 | 0.7 | 0.7 |
| 2212909-5 | 0.6 | 1.6 |
本研究将衍生化与LC-MS法相结合,建立了一种快速测定硝酸硫康唑中痕量硫酸烷基酯类基因毒性杂质(包括硫酸二甲酯、硫酸二乙酯)的分析方法。本方法流动相A为20 mmol ·L-1甲酸铵溶液-甲酸(1 000 ∶1),流动相B为乙腈,HILIC色谱柱(2.1 mm×50 mm,3 μm),流速0.2 mL ·min-1、柱温20 ℃,流动相A-流动相B(10 ∶90)等度洗脱,采用多反应监测(MRM)模式定量检测。同时,考察了温度及时间对衍生化的影响。该方法操作简单、快速,提高了灵敏度,成本低,专属性强;硫酸二甲酯回收率为80.3%~102.3%,回收率的RSD值为8.5%;硫酸二乙酯回收率为90.3%~100.0%,回收率的RSD值为3.2%,准确度良好;硫酸二甲酯、硫酸二乙酯重复性RSD均为1.6%,中间精密度RSD分别为5.2%、5.6%,精密度良好。本方法满足硝酸硫康唑中基因毒性杂质硫酸二甲酯、硫酸二乙酯痕量检测要求,为市场监管部门对原料药中硫酸烷基酯类的痕量监测提供了技术支持。
| [1] |
许玉成. 硝酸硫康唑(Sulconazole Nitrate)[J]. 国外医药.合成药.生化药.制剂分册, 1987, 3: 173-174. |
| [2] |
王美芳, 李邻峰, 程海燕, 等. 1%硝酸硫康唑喷雾剂治疗足癣及鞋袜用药对预防复发的作用[J]. 中国真菌学杂志, 2018, 13(3): 164-167. WANG Meifang, LI Linfeng, CHENG Haiyan, et al. Efficacy of 1% sulconazole nitrate spray in the treatment of tinea pedis and preventive effect of spraying the shoes and socks[J]. Chinese Journal of Mycology, 2018, 13(3): 164-167. DOI:10.3969/j.issn.1673-3827.2018.03.008 (in Chinese) |
| [3] |
刘咏梅, 陆强. 3例职业性急性硫酸二甲酯中毒临床特点分析[J]. 中国工业医学杂志, 2024, 37(1): 53-55. |
| [4] |
根加甫·阿尔布斯力, 石梦迪, 戴平, 等. 硫酸二甲酯致背部皮肤灼伤1例报道[J]. 中国工业医学杂志, 2023, 36(5): 417-418. GENJIAPU Aerbusili, SHI Mengdi, DAI Ping, et al. A case report of skin burn in back caused by dimethyl sulfate[J]. Chinese Journal of Industrial Medicine, 2023, 36(5): 417-418. (in Chinese) |
| [5] |
冯萌萌, 王虹, 陈佩瑾. 气相色谱-质谱法测定土壤中硫酸二甲酯和硫酸二乙酯的残留量[J]. 广东化工, 2020, 47(9): 186-187, 185. FENG Mengmeng, WANG Hong, CHEN Peijin. Determination of dimethyl sulfate and diethyl sulfate residues in soil by gas chromatography-mass spectrometry[J]. Guangdong Chemical Industry, 2020, 47(9): 186-187, 185. DOI:10.3969/j.issn.1007-1865.2020.09.085 (in Chinese) |
| [6] |
International Conference on Harmonization of Technical Requirements for Registration of Pharmaceuticals for Human Use(ICH). Assessment and Control of DNA Reactive (Mutagenic) Impurities in Pharmaceuticals to Limit Potentical Carcinogenic Risk M7(R1). 2015
|
| [7] |
李栋, 赵海英. 9例急性硫酸二甲酯中毒护理体会[J]. 中国工业医学杂志, 2022, 35(1): 91-95. |
| [8] |
汪生, 倪悦泠, 陆宇婷, 等. 顶空气相色谱法测定塞来昔布中硫酸二乙酯基因毒性杂质[J]. 中国新药杂志, 2018, 27(20): 2437-2441. WANG Sheng, NI Yueling, LU Yuting, et al. Determination of the diethyl sulphate genotoxic impurity in celecoxib by headspace gas chromatography[J]. Chinese Journal of New Drugs, 2018, 27(20): 2437-2441. (in Chinese) |
| [9] |
李一婧, 张婷婷, 李彤, 等. 气相色谱火焰光度法检测TBI-166中硫酸二甲酯和硫酸二乙酯残留量[J]. 药物分析杂志, 2016, 36(10): 1847-1851. |
| [10] |
吴楚森, 王斌, 王莉, 等. 气相色谱-质谱联用测定化妆品中硫酸二甲酯与硫酸二乙酯[J]. 分析测试学报, 2018, 37(1): 70-75. WU Chusen, WANG Bin, WANG Li, et al. Determination of dimethyl sulfate and diethyl sulfate in cosmetics by GC-MS[J]. Journal of Instrumental Analysis, 2018, 37(1): 70-75. DOI:10.3969/j.issn.1004-4957.2018.01.011 (in Chinese) |
| [11] |
毕富春, 吴国旭. 44种有机磷杀虫剂的气相色谱分析[J]. 化学工业与工程, 2001, 18(3): 156-160. BI Fuchun, WU Guoxu. Gas chromatography of 44 organophosphorus insecticides[J]. Chemical Industry and Engineering, 2001, 18(3): 156-160. DOI:10.3969/j.issn.1004-9533.2001.03.007 (in Chinese) |
| [12] |
张韻慧, 吴金国, 张雅慧, 等. 毛细管气相色谱法测定强心滴丸中的冰片含量[J]. 化学工业与工程, 2007, 24(3): 215-217, 271. ZHANG Yunhui, WU Jinguo, ZHANG Yahui, et al. Quantitative determination of borneol in Qiangxin dripping pills by capillary gas chromatography[J]. Chemical Industry and Engineering, 2007, 24(3): 215-217, 271. DOI:10.3969/j.issn.1004-9533.2007.03.007 (in Chinese) |
| [13] |
袁玉兵, 樊顺东, 梁花. GC-MS法测定纺织品中硫酸二乙酯的方法研究[J]. 中国纤检, 2023(8): 70-72. YUAN Yubing, FAN Shundong, LIANG Hua. Study on determination of diethyl sulfate in textiles by GC-MS[J]. China Fiber Inspection, 2023(8): 70-72. (in Chinese) |
| [14] |
鲍美玲, 陈海霞, 秦琴, 等. GC-MS法同时测定9-氨基米诺环素盐酸盐中的硫酸二甲酯和硫酸二异丙酯[J]. 海峡药学, 2018, 30(9): 51-53. BAO Meiling, CHEN Haixia, QIN Qin, et al. Simultaneous determination of dimethyl sulfate and diisopropyl sulfate in 9-amino minocycline hydrochloride by GC-MS[J]. Strait Pharmaceutical Journal, 2018, 30(9): 51-53. (in Chinese) |
| [15] |
吴健华. 硫酸二甲酯检验方法研究及化工分析难题的应对策略[J]. 化工设计通讯, 2022, 48(11): 100-102. WU Jianhua. Research on dimethyl sulfate inspection method and coping strategies for difficult problems in chemical analysis[J]. Chemical Engineering Design Communications, 2022, 48(11): 100-102. (in Chinese) |
| [16] |
ALZAGA R, RYAN R W, TAYLOR-WORTH K, et al. A generic approach for the determination of residues of alkylating agents in active pharmaceutical ingredients by in situ derivatization-headspace-gas chromatography-mass spectrometry[J]. Journal of Pharmaceutical and Biomedical Analysis, 2007, 45(3): 472-479. |
| [17] |
杨亚琴, 李圆圆, 曹秀, 等. 衍生化-气相色谱法测定谷物籽粒中三氯吡氧乙酸残留量[J]. 农药, 2024, 63(3): 191-195, 227. YANG Yaqin, LI Yuanyuan, CAO Xiu, et al. Determination of triclopyr residue in cereal seeds by gas chromatography with derivatization[J]. Agrochemicals, 2024, 63(3): 191-195, 227. (in Chinese) |
| [18] |
戴琛, 汪瑾, 卢亚萍. 衍生化UPLC-MS法测定酸性植物激素[J]. 植物学报, 2022, 57(4): 500-507. DAI Chen, WANG Jin, LU Yaping. Determination of acidic plant hormones by derivative UPLC-MS[J]. Chinese Bulletin of Botany, 2022, 57(4): 500-507. (in Chinese) |
| [19] |
汪建飞, 索绪斌, 张涵. 衍生化法测定γ-氨基丁酸的含量及稳定性研究[J]. 化学研究与应用, 2022, 34(4): 909-914. WANG Jianfei, SUO Xubin, ZHANG Han. Determination and stability of γ-aminobutyric acid by derivatization[J]. Chemical Research and Application, 2022, 34(4): 909-914. (in Chinese) |
| [20] |
石蕾, 李伟松, 师浩淳, 等. 草酸二甲酯和草酸的反相高效液相色谱分析[J]. 化学工业与工程, 2016, 33(2): 91-95. SHI Lei, LI Weisong, SHI Haochun, et al. Determination of dimethyl oxalate and oxalic acid by reversed-phase high performance liquid chromatography[J]. Chemical Industry and Engineering, 2016, 33(2): 91-95. DOI:10.13353/j.issn.1004.9533.20141058 (in Chinese) |
| [21] |
王林, 吴佳豪, 许凌. 溶剂解吸-高效液相色谱法测定染料车间空气中的硫酸二甲酯[J]. 预防医学情报杂志, 2023, 39(6): 698-703. WANG Lin, WU Jiahao, XU Ling. Determination by solvent desorption-high performance liquid chromatography dimethyl sulfate in the air of dye workshop[J]. Journal of Preventive Medicine Information, 2023, 39(6): 698-703. (in Chinese) |
| [22] |
李晶, 张琦, 刘净. 气质联用和液质联用在农药残留检测中的运用[J]. 食品安全导刊, 2022(18): 165-167, 171. |
 2025, Vol. 42
2025, Vol. 42





