2. 赤峰瑞阳化工有限公司, 内蒙古 赤峰 024076;
3. 内蒙古自治区多元醇化工新材料企业重点实验室, 内蒙古 赤峰 024076;
4. 中低品位磷矿及其共伴生资源高效利用国家重点实验室, 贵阳 550016
2. Chifeng Ruiyang Chemical Co., Ltd., Chifeng, Inner Mongolia 024076, China;
3. Key Laboratory of Polyol Chemical New Materials Enterprises of Inner Mongolia Autonomous Region, Chifeng, Inner Mongolia 024076, China;
4. National Key Laboratory for Efficient and Comprehensive Utilization of Medium and Low Grade Phosphate Rock and Its Associated Resources, Guiyang 550016, China
绿色化学正在成为21世纪的发展前沿,在设计合理的合成过程时,避免使用有害物质和产生有毒废物,引起了科研工作者极大的关注。在这种背景下,近年来,离子液体(Ionic liquid,IL)作为一种绿色溶剂,已经快速成为一种有前途的替代反应介质。
离子液体是完全由阳离子和阴离子组成的液体盐。碱性离子液体可作为溶剂[1],并且其稳定性[2]和电导率极好[3],有独特的无蒸汽性和可重复使用性,为开发环保的碱性催化剂提供了新的可能性,在一些催化有机反应中,含咪唑阳离子的离子液体可以作为强介质,不仅可以促进催化剂的回收,而且可以提高反应速率和提高选择性[4]。
目前,碱性离子液体已成功地应用于有机反应催化剂,例如在Knovenagel反应、Adol反应、酯化反应、曼尼希反应、Markovnikov反应、Herry反应等[5-11]。碱性离子液体作为环保溶剂[12]和催化剂,具有高活性、选择性和易于回收,可取代传统的碱,如KOH、NaOH、Ca(OH)2、K2CO3、NaHCO3、NaOAc、三乙胺或四丁基乙酸铵[13],由此为催化三羟甲基丙烷的合成提供了可能性。
三羟甲基丙烷(Trimethylolpropane,TMP)是一种三元醇。三羟甲基丙烷主要用于醇酸树脂、聚氨酯、不饱和树脂、聚酯树脂、涂料等领域,也可用于合成航空润滑油、增塑剂、表面活性剂、润湿剂、炸药和印刷油墨等[14-17],还可用作纺织助剂和聚氯乙烯树脂的热稳定剂。目前生产主要方法为Cannizzaro法和催化加氢法,前者催化剂主要为无机催化剂(NaOH、KOH等);后者则需要在反应的不同阶段变换催化剂,先是三乙胺或离子交换树脂后为特殊金属(如:Ni系、Cu系催化剂)[18-23]。反应结束后处理程序复杂,且实验中的催化剂转化成无机盐成为副产物(甲酸钙、甲酸钠),影响产品质量。
研究发现碱性离子液体可用于合成TMP[24],对比使用Ca(OH)2等碱性催化剂,减少了许多后处理步骤以及副产物的生成,且碱性离子液体可以进行回收率利用,符合绿色化工生产。因此本论文拟采用咪唑类离子液体[Bmmim]OH作为催化剂代替传统的Ca(OH)2催化剂,以甲醛和正丁醛为原料合成TMP,并以Box-Behnken响应面法探究其最适宜生产工艺条件。
1 实验 1.1 实验材料与仪器材料:[Bmmim]Br,分析纯,安徽泽开科技有限公司;甲醇,乙醇,甲醛,正丁醛,分析纯,赤峰瑞阳化工有限公司;KOH,三氯甲烷,无水硫酸钠,分析纯,国药集团化学试剂有限公司;1, 6-己二醇,分析纯,上海麦克林生化科技有限公司;乙醚,分析纯,成都市科隆化学品有限公司。
仪器:安捷伦7890B气相色谱仪,真空泵,DF-101S集热式恒温加热磁力搅拌器,傅里叶变换红外光谱仪,泵头TG-1 BT100-3J型Longerpump蠕动泵。
1.2 实验方法 1.2.1 [Bmmim]OH的制备将0.1 mol KOH 5.61 g溶于适量甲醇中,待溶解完毕后加入0.1 mol[Bmmim]Br 23.315 g,此时溶液呈白色,室温下剧烈搅拌反应24 h[25],减压蒸馏2 h除去溶剂甲醇,得到粗[Bmmim]OH。后用乙醚洗涤,得[Bmmim]OH纯品,收率为87.39%。
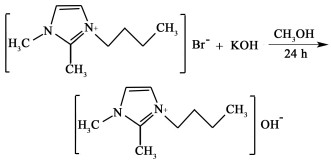 |
(1) |
三羟甲基丙烷的合成中会发生以下反应:
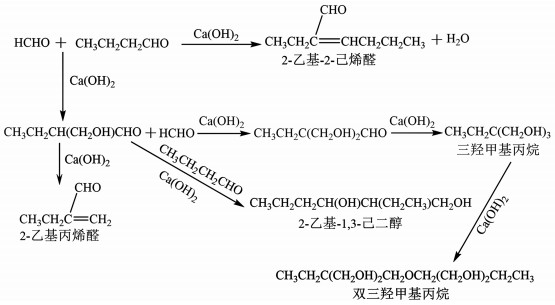 |
(2) |
称取甲醛加入1 L反应器中,加入适量[Bmmim]OH离子液体,BT100-3J型蠕动泵30 ℃下匀速流加正丁醛,反应2 h,流加完毕后,升温至70 ℃反应4 h。通过旋转蒸发仪连续升温45~60 ℃去除水后,加入三氯甲烷结晶,在50 ℃下对结晶物减压干燥3 h,所得到的固体在乙酸乙酯中进一步再结晶,最终的TMP产物为白色固体。
1.2.3 表征采用FT-IR对合成的[Bmmim]OH纯品和TMP进行表征。配制0.43 g ·L-1 2-乙基丙烯醛、1.02 g ·L-1 2-乙基-2-己烯醛、2.42 g ·L-1 2-乙基-1, 3-己二醇、2.69 g ·L-1内标1, 6-己二醇和12.24 g ·L-1三羟甲基丙烷成混合标准品。并用气相色谱仪内标法对TMP及其副产物浓度进行定性和定量分析[26]。
1.2.4 单因素实验以Cannizzaro反应时间、投料速度和原料物质的量之比为单因素,以TMP产物浓度为目标考察其影响。
1.2.5 Box-Behnken响应面法优化实验根据DESIGN-Expert 12.0中Box-Behnken响应面法设计要求进行实验,并对数据进行模拟拟合,得出最适宜参数组合。
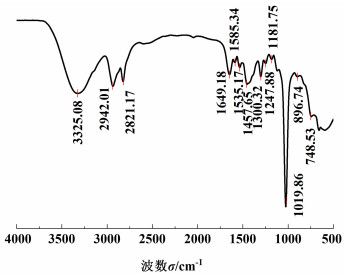
2 结果与讨论 2.1 表征结果[Bmmim]OH离子液体和TMP的FT-IR光谱图如图 1和图 2所示。
|
| 图 1 [Bmmim]OH离子液体红外光谱 Fig.1 FT-IR spectra of [Bmmim] OH ionic liquid |
| |
|
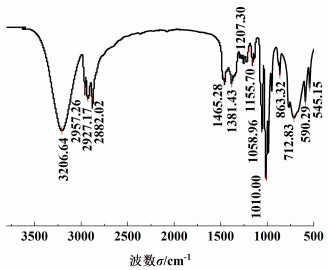
| 图 2 三羟甲基丙烷红外光谱 Fig.2 FT-IR spectra of trimethylolpropane |
| |
由图 1可知,3 325.08 cm-1为离子液体中醇羟基O—H吸收峰,2 942.01和2 821.17 cm-1的为咪唑环侧链上的—CH2—和—CH3基团的伸缩振动,1 649.18 cm-1处为咪唑环上的—C C—双键伸缩振动吸收峰,在1 535.17 cm-1处为咪唑环骨架C—N伸缩振动吸收峰,1 457.65 cm-1处吸收峰为咪唑环上侧链—CH2CH2CH2CH3中—CH2—的C—H面内弯曲振动吸收峰[27],在896.74和748.53 cm-1分别为咪唑环上C—H面内和面外弯曲振动峰,因此证明实验合成了[Bmmim]OH离子液体。
由图 2可知,3 206.64 cm-1为羟基的特征吸收,2 957.26、2 927.17和2 882.02 cm-1为—CH3和—CH2—伸缩振动吸收峰,1 381.43、1 207.30和1 155.70 cm-1为烷基上的C—H吸收峰,1 058.96和1 010.00 cm-1处吸收峰为醇羟基上的C—O伸缩振动。由此可见,实验成功合成了TMP。
通过图 3(b)可知各组分出峰时间,经过内标法的计算在反应结束后各组分浓度如下:2- 乙基丙烯醛浓度为0.04 g ·L-1、2-乙基-2-己烯醛为0.49 g ·L-1、2-乙基-1, 3-己二醇为0.26 g ·L-1、三羟甲基丙烷为12.22 g ·L-1。

|
| 图 3 三羟甲基丙烷合成中气相色谱图 Fig.3 Gas chromatogram of TMP synthesis |
| |
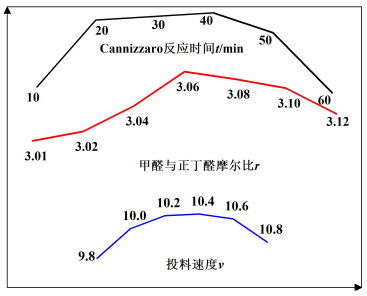
本研究分别考察了Cannizzaro反应时间:10、20、30、40、50和60 min,甲醛与正丁醛物质的量之比:3.01、3.02、3.04、3.06、3.08、3.10,3.12,投料速度:9.80、10.00、10.20、10.40、10.60和10.80,对于TMP生成浓度的影响,结果如图 4所示。
|
| 图 4 单因素实验结果 Fig.4 Single factor experiment results |
| |
由图 4可知,随着时间增加,TMP质量浓度增加,等到达平衡状态之后,时间的增加会降低TMP的质量浓度,因为随着反应中TMP的增加,以TMP作为反应底物分子间脱水会产生双三羟甲基丙烷。而甲醛与正丁醛物质的量之比不断增加,在超过了理论物质的量之比3 ∶1的情况下,增加甲醛会增加正丁醛的转化率,而当甲醛过量时,各种副产物都会增加,而TMP不再会有增加的趋势,反而降低。在投放正丁醛的速度过快时,正丁醛会瞬时过量,会增大正丁醛自缩合成2-乙基-1, 3-己二醇。
因此在单因素的基础上选择Cannizzaro反应时间:20~40 min,n(甲醛)/n(正丁醛):3.06~3.10,投料速度:10.20~10.60。以上条件作为响应面实验的水平。
2.3 Box-Behnken响应面结果与讨论根据单因素影响实验,本研究选择响应面因素水平如表 1所示。
| 因素 | 编码 | 各水平取值 | ||
| -1 | 0 | 1 | ||
| Cannizzaro反应时间t/min | X1 | 20 | 30 | 40 |
| 甲醛与正丁醛物质的量之比r | X2 | 3.06 | 3.08 | 3.10 |
| 投料速度v/(r·min-1) | X3 | 10.20 | 10.40 | 10.60 |
将上述因素水平输入Design-Expert 12软件中,得到以下实验记录表,实验设计及结果见表 2,响应面回归模型方差分析结果见表 3。以TMP浓度为Y进行拟合得到了回归方程为:
| $ \begin{gathered} Y=12.82+0.1663 X_1-1.16 X_2+0.3561 X_3- \\ 0.7465 X_1 X_2+0.8075 X_1 X_3+0.3367 X_2 X_3- \\ 1.48 X_1^2-1.09 X_2^2-0.8555 X_3^2 \end{gathered} $ | (3) |
| 序号 | Cannizzaro 反应时间 t/min |
甲醛与正丁醛 物质的量 之比r |
投料 速度v/ (r·min-1) |
TMP 浓度c/ (g·L-1) |
| 1 | 30 | 3.10 | 10.20 | 9.191 |
| 2 | 40 | 3.08 | 10.20 | 9.256 |
| 3 | 30 | 3.06 | 10.60 | 11.893 |
| 4 | 40 | 3.10 | 10.40 | 8.577 |
| 5 | 20 | 3.08 | 10.20 | 10.794 |
| 6 | 30 | 3.06 | 10.20 | 12.057 |
| 7 | 30 | 3.08 | 10.40 | 12.795 |
| 8 | 40 | 3.06 | 10.40 | 12.515 |
| 9 | 30 | 3.08 | 10.40 | 12.639 |
| 10 | 30 | 3.08 | 10.40 | 12.665 |
| 11 | 30 | 3.10 | 10.60 | 10.374 |
| 12 | 20 | 3.10 | 10.40 | 9.482 |
| 13 | 40 | 3.08 | 10.60 | 11.786 |
| 14 | 20 | 3.08 | 10.60 | 10.094 |
| 15 | 30 | 3.08 | 10.40 | 12.825 |
| 16 | 20 | 3.06 | 10.40 | 10.434 |
| 17 | 30 | 3.08 | 10.40 | 13.177 |
| 项目 | 平方和 | df | 均方 | F值 | P值 |
| 模型 | 36.47 | 9 | 4.05 | 66.04 | <0.000 1 |
| X1-Cannizzaro反应时间 | 0.221 1 | 1 | 0.221 1 | 3.6 | 0.099 5 |
| X2-甲醛与正丁醛物质的量之比 | 10.75 | 1 | 10.75 | 175.24 | <0.000 1 |
| X3-投料速度 | 1.01 | 1 | 1.01 | 16.53 | 0.004 8 |
| X1X2 | 2.23 | 1 | 2.23 | 36.33 | 0.000 5 |
| X1X3 | 2.61 | 1 | 2.61 | 42.51 | 0.000 3 |
| X2X3 | 0.453 6 | 1 | 0.453 6 | 7.39 | 0.029 8 |
| X12 | 9.25 | 1 | 9.25 | 150.75 | <0.000 1 |
| X22 | 4.97 | 1 | 4.97 | 80.92 | <0.000 1 |
| X32 | 3.08 | 1 | 3.08 | 50.22 | 0.000 2 |
| 残差 | 0.429 5 | 7 | 0.061 4 | ||
| 失拟项 | 0.244 7 | 3 | 0.081 6 | 1.76 | 0.292 6 |
| 纯误差 | 0.184 9 | 4 | 0.046 2 | ||
| 总计 | 36.9 | 16 |
由表 3可知,模型F值为66.04,P值<0.000 1, 说明该模型显著。失拟项P值为0.292 6>0.05,表明模型误差在可允许范围内, 失拟项不显著。实验R2=0.988 4, 与校正值R2=0.973 4差值小于0.2,说明该模型可信度高,以及信噪比22.674>4,模型的变异系数为2.21%且小于10%,表明该模型精密度和准确度高。并且由表 3显示一次项X2、二次项X1和X2的P值<0.000 1,表明其非常显著。而一次项X1,和Cannizzaro反应时间、甲醛与正丁醛物质的量之比、投料速度(P值<0.05)交互作用对TMP浓度的影响显著。一次项X1-Cannizzaro反应时间P值>0.05,表明其对于TMP浓度影响不显著。
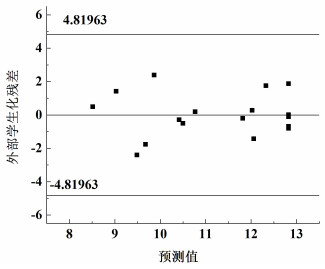
2.3.2 残差分析模型和数据的相关性与可靠性可以通过残差来检验。
在图 5中为残差正态分布图,其中实验数据点均匀分布在直线两侧,分布规律正常,表明标准偏差与实际值差别很小,模型呈正态分布。而图 6为残差与上升的预测响应值之间的关系,可得残差随机分布,残差与拟合值不相关,说明该模型适应性良好。

|
| 图 5 残差正态图 Fig.5 Normal plot of residuals |
| |
|
| 图 6 残差与预测值关系图 Fig.6 Residuals vs the predicted |
| |
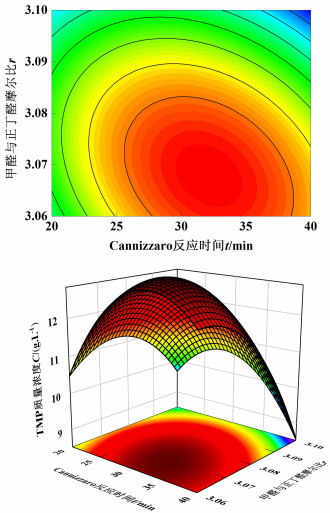
为更清晰了解各因素相交互作用的影响,本论文分析了其等高线图和三维图,如图 6~图 8所示。
|
| 图 7 Cannizzaro反应时间与甲醛正丁醛物质的量之比交互作用 Fig.7 Interaction between Cannizzaro reaction time and molar ratio of formaldehyde to butanal |
| |
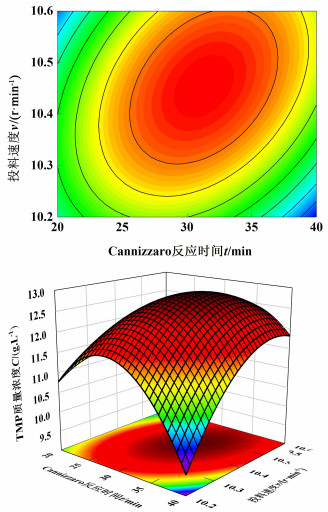
|
| 图 8 Cannizzaro反应时间与投料速度交互作用 Fig.8 Interaction between Cannizzaro reaction time and feeding speed |
| |
在3D图中,曲面坡度越陡,说明对于TMP质量浓度的影响越强。等高线越趋于圆形,两相交互对TMP质量浓度影响不显著;等高线越趋于椭圆形,则交互作用对TMP影响显著。
由图 7可见,当固定投料速度时,Cannizzaro反应时间与甲醛正丁醛物质的量之比交互作用的等高线图为椭圆形,且三维图坡度陡峭,说明其交互作用对TMP浓度的影响作用大且显著。随着Cannizzaro反应时间增加,物质的量之比对TMP质量浓度强度先增大后减小,这是因为当Cannizzaro反应时间短时,HCHO与中间产物2, 2-二羟甲基丁醛歧化反应未达到平衡状态,而当达到平衡状态时,TMP会自缩合生成副产物双三羟甲基丙烷。
图 8为Cannizzaro反应时间与投料速度交互作用的等高线图和三维图,并且分别为椭圆形和陡峭状,表明其交互作用对于TMP质量浓度影响强且显著。当固定HCHO和CH3CH2CH2CHO物质的量之比时,随着Cannizzaro反应时间增加,投料速度增大使TMP质量浓度先增加后减小,原因是当投料速度加快,正丁醛自缩合生成2-乙基-1, 6-己二醇。
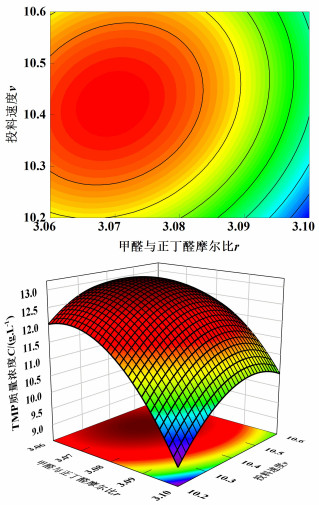
从图 9可知,甲醛正丁醛物质的量之比与投料速度交互作用的等高线呈椭圆形,但没有上述交互作用强烈;三维图坡度陡峭,说明其交互影响强且较为显著。在固定Cannizzaro反应时间下,随着甲醛与正丁醛物质的量之比增加,投料速度对TMP影响先增大由减弱,且投料速度在10.30~10.50最适宜,原因是正丁醛与甲醛的羟醛缩合反应达到一个相互平衡的状态,合成中间产物CH3CH2C(CH2OH)2CHO。
|
| 图 9 甲醛正丁醛物质的量之比与投料速度交互作用 Fig.9 Interaction between molar ratio of formaldehyde and butyraldehyde and feeding rate |
| |
由Design-Expert 12.0推荐的最适宜合成条件为:Cannizzaro反应时间:37.21 min、甲醛正丁醛物质的量之比:3.074、投料速度:10.45 r ·min-1,其最佳的TMP质量浓度为12.744 g ·L-1。
2.3.4 模型实验验证根据响应曲面最佳实验结果,Cannizzaro反应时间:37.21 min、n(甲醛)/n(正丁醛)为3.074、投料速度:10.45 r ·min-1,分别进行3次实验。3次实验的平均值为12.406 g ·L-1,平行实验的RSD为0.22%<2%,与预测值的偏差率为2.65%,表明此建立的模型可信度高。
3 结论(1)[Bmmim]Br与KOH在常温状态下可反应制得[Bmmim]OH离子液体,且产率为87.39%。
(2) 在分别考察了单因素Cannizzaro反应时间、甲醛与正丁醛物质的量之比、投料速度后,实验结果表明最适宜Cannizzaro反应时间为40 min,最适宜范围为20~40 min;最适宜n(甲醛)/n(正丁醛)为3.06,最适宜范围为3.06~3.10;最适宜投料速度为10.40 r ·min-1,最适宜范围为10.20~10.60 r ·min-1。
(3) 在Box-Behnken曲面分析法优化[Bmmim]OH催化合成三羟甲基丙烷实验中,实验结果分析发现,最适宜合成条件为Cannizzaro反应时间:37.21 min、n(甲醛)/n(正丁醛)为3.074、投料速度:10.45 r ·min-1,其最适宜的TMP质量浓度为12.744 g ·L-1。显著性关系:甲醛正丁醛物质的量之比>投料速度>Cannizzaro反应时间。
(4) 模型实验验证结果表明,实验值与预测值偏差率为2.65%,说明模型可信度高,预测准确。
| [1] |
LETHESH K C, EVJEN S, VENKATRAMAN V, et al. Highly efficient cellulose dissolution by alkaline ionic liquids[J]. Carbohydrate Polymers, 2020, 229: 115594. DOI:10.1016/j.carbpol.2019.115594 |
| [2] |
MEEK K M, NYKAZA J R, ELABD Y A. Alkaline chemical stability and ion transport in polymerized ionic liquids with various backbones and cations[J]. Macromolecules, 2016, 49(9): 3382-3394. DOI:10.1021/acs.macromol.6b00434 |
| [3] |
WU X, SANG X, LI Z, et al. Study on physicochemical properties and basicity of carbanion-functionalized ionic liquids[J]. Journal of Molecular Liquids, 2020, 312: 113405. DOI:10.1016/j.molliq.2020.113405 |
| [4] |
CHAUDHARY S, MILTON M D. Dicationic imidazolium salts as fluorescent probes for selective detection of Fe3+ ion in pure aqueous media[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2018, 356: 595-602. DOI:10.1016/j.jphotochem.2018.02.003 |
| [5] |
FEKRI L Z. Ionic liquid [BDBDMIm](Br3)2 as a new efficient brominating agent in the synthesis of γ-butyrolactones[J]. Russian Journal of General Chemistry, 2018, 88(5): 1009-1014. DOI:10.1134/S1070363218050286 |
| [6] |
HU Y, REN M, KAZEMNEJADI M. Metal- and solvent-free transesterification and aldol condensation reactions by a homogenous recyclable basic ionic liquid based on the 1, 3, 5-triazine framework[J]. ChemistryOpen, 2021, 10(8): 775-783. DOI:10.1002/open.202100091 |
| [7] |
TEIMURI-MOFRAD R, RAHIMPOUR K, REZAEI H, et al. Study of new synthesized ferrocenyl ionic liquids in oxidative esterification reaction[J]. Synthetic Communications, 2018, 48(12): 1425-1435. DOI:10.1080/00397911.2018.1450883 |
| [8] |
PRABHAKARA M D, MAITI B. Ionic liquid-immobilized proline(s) organocatalyst-catalyzed one-pot multi-component Mannich reaction under solvent-free condition[J]. Research on Chemical Intermediates, 2020, 46(4): 2381-2401. DOI:10.1007/s11164-020-04096-w |
| [9] |
CHEN X, LI X, SONG H, et al. Solvent-free aza-Markovnikov and aza-Michael additions promoted by a catalytic amount of imidazolide basic ionic liquids[J]. Tetrahedron Letters, 2011, 52(28): 3588-3591. DOI:10.1016/j.tetlet.2011.04.117 |
| [10] |
JAGADALE M, NAIKWADE A, SALUNKHE R, et al. An ionic liquid gel: A heterogeneous catalyst for Erlenmeyer-Plochl and Henry reactions[J]. New Journal of Chemistry, 2018, 42(13): 10993-11005. DOI:10.1039/C8NJ00367J |
| [11] |
高歌, 靳海波. 咪唑类离子液体催化合成碳酸丙烯酯[J]. 化学工业与工程, 2014, 31(1): 14-18, 62. GAO Ge, JIN Haibo. Synthesis of propylene carbonate in the presence of catalysts of N, N'-dialkylimidazolium-based ionic liquids[J]. Chemical Industry and Engineering, 2014, 31(1): 14-18, 62. (in Chinese) |
| [12] |
YE C, XIAO J, TWAMLEY B, et al. Basic ionic liquids: Facile solvents for carbon-carbon bond formation reactions and ready access to palladium nanoparticles[J]. European Journal of Organic Chemistry, 2007(30): 5095-5100. |
| [13] |
HAJIPOUR A R, RAFIEE F. Basic ionic liquids. A short review[J]. Journal of the Iranian Chemical Society, 2009, 6(4): 647-678. DOI:10.1007/BF03246155 |
| [14] |
NIE J, SHEN J, SHIM Y Y, et al. Synthesis of trimethylolpropane esters by base-catalyzed transesterification[J]. European Journal of Lipid Science and Technology, 2020, 122(3): 1900207. DOI:10.1002/ejlt.201900207 |
| [15] |
罗丹, 陈家玲, 周正, 等. 双丙甘醇/角鲨烷/三羟甲基丙烷三辛酸葵酸酯复合纳米乳头皮养护及毛发修复功效研究[J]. 香料香精化妆品, 2021(5): 71-76. LUO Dan, CHEN Jialing, ZHOU Zheng, et al. Research on scalp care and hair repair efficacy of dipropylene glycol/squalane/trimethylolpropane trieaprylic caprate complex nanoemulsion[J]. Flavour Fragrance Cosmetics, 2021(5): 71-76. (in Chinese) |
| [16] |
郭晓峰. 三羟甲基丙烷三(3-巯基丙酸酯)的合成与应用研究[D]. 北京: 北京化工大学, 2022 GUO Xiaofeng. Study on synthesis and application of trimethylolpropane tris (3-mercaptopropionic acid ester)[D]. Beijing: Beijing University of Chemical Technology, 2022(in Chinese) |
| [17] |
KIRPLUKS M, VANAGS E, ABOLINS A, et al. High functionality bio-polyols from tall oil and rigid polyurethane foams formulated solely using bio-polyols[J]. Materials, 2020, 13(8): 1985. DOI:10.3390/ma13081985 |
| [18] |
NIE J, SHIM Y Y, SHEN J, et al. Characterization of trimethylolpropane-based biolubricant[J]. European Journal of Lipid Science and Technology, 2020, 122(7): 2000025. DOI:10.1002/ejlt.202000025 |
| [19] |
EOM S S, KO D H, MOON J J, et al. Method for preparing trimethylolproane: US7253326[P]. 2007-08-07
|
| [20] |
LAEMMLE G J, MILLIGAN J G, PEPPEL W J. Trimethylolethane from propionaldehyde and formaldehyde[J]. Industrial & Engineering Chemistry, 1960, 52(1): 33-36. |
| [21] |
IMMEL O, SCHWARZ H H, QUAST H, et al. Process for the preparation of trimethylolpropane: US4514578[P]. 1985-04-30
|
| [22] |
MULLER D, WAGNER P, SCHWEGLER B, et al. Preparation of trimethylolpropane: US20030139631[P]. 2003-07-24
|
| [23] |
张卫红, 冯亚青, 董宁, 等. 三羟甲基丙烷的合成研究[J]. 化学工业与工程, 1998, 15(2): 14-18, 23. ZHANG Weihong, FENG Yaqing, DONG Ning, et al. The synthesis of trimethylolpropane[J]. Chemical Industry and Engineering, 1998, 15(2): 12-16, 21. (in Chinese) |
| [24] |
龙金星, 袁正求, 马浩, 等. 碱性离子液体催化合成三羟甲基丙烷[J]. 物理化学学报, 2015(2): 337-343. LONG Jinxing, YUAN Zhengqiu, MA Hao, et al. Catalytic synthesis of trimethylolpropane in the presence of basic ionic liquid[J]. Acta Physico-Chimica Sinica, 2015(2): 337-343. (in Chinese) |
| [25] |
孙健, 伞影, 谢宁, 等. 碱性离子液体催化Friedlander反应合成2, 3-二苯基-1, 8-萘啶的研究[J]. 现代化工, 2022, 42(2): 167-171. SUN Jian, SAN Ying, XIE Ning, et al. Synthesis of 2, 3-diphenyl-1, 8-naphthyridine by Friedlander reaction catalyzed by basic ionic liquids[J]. Modern Chemical Industry, 2022, 42(2): 167-171. (in Chinese) |
| [26] |
解田, 全宏冬, 伍庆, 等. 一种三羟甲基丙烷及其副产物的检测方法: CN113917019B[P]. 2022-05-27 XIE tian, QUAN Hongdong, WU Qing, et al. Method for detecting trimethylolpropane and byproducts thereof: CN113917019B[P]. 2022-05-27(in Chinese) |
| [27] |
YAMADA T, MIZUNO M. Characteristic spectroscopic features because of cation-anion interactions observed in the 700~950 cm-1 range of infrared spectroscopy for various imidazolium-based ionic liquids[J]. ACS Omega, 2018, 3(7): 8027-8035. |
 2024, Vol. 41
2024, Vol. 41





