2. 中国建筑设计研究院工程设计研究院, 北京 100044;
3. 南京师范大学化学与材料科学学院, 江苏省物质循环与污染控制重点实验室, 南京 210023;
4. 北京科技大学能源与环境工程学院, 北京 100083
2. Engineering Design and Research Institute, China Architecture Design & Research Group, Beijing 100044, China;
3. School of Chemistry and Materials Science, Jiangsu Provincial Key Laboratory of Materials Cycling and Pollution Control, Nanjing Normal University, Nanjing 210023, China;
4. School of Energy and Environmental Engineering, University of Science and Technology Beijing, Beijing 100083, China
自20世纪90年代,部分专家学者提出源分离生态卫生排水概念[1-5],旨在将传统的以污水处理达标排放为目标的排水系统转变为以污水及其中污染物质的资源化利用为目标的分散式分流分质处理系统。与传统污水排放系统相比,源分离生态卫生排水系统更为复杂,需要从便器系统、管路系统、资源化系统和废物处置系统等多方面进行综合管理和调控[6]。其中任何一个环节出现问题都可能会影响到整个排水系统的正常运行。
随着源分离生态卫生排水概念的提出,这一领域迅速引起了国内外专家学者的关注,研究方向主要集中于新型卫生设施系统的开发、源分离污水资源化回收技术、源分离系统碳排放等方面,曹睿等[7]对农村生活污水传统处理与源分离处理的碳排放进行了分析,发现源分离方案的直接碳排放与间接碳排放均低于传统方案,减少排放的同时产生了可观的碳补偿。段文俊等[8]以尿液作为液体肥料施用为目标进行了源分离尿液碱性稳定化研究,结果显示pH值越高、温度越低,尿液越稳定。Randall等[9]将氢氧化钙作为稳定剂,用以抑制尿液中尿素水解,达到稳定尿液的效果。刘铭等[10]对当前源分离尿液资源化处理技术进行了梳理与分析,表明现阶段单一技术仍无法实现黄水中多种物质或能量的同时处理与再利用,回收效果与成本是主要限制因素。
尽管当前关于源分离生态卫生排水领域的研究已经取得了显著的进展,但是关于源分离污水输送的研究是匮乏的。在黄水输送系统中,新鲜尿液中的尿素在微生物脲酶的作用下发生水解,在这一过程中黄水的pH值由6.2左右升高至9.1左右,导致黄水中钙、镁离子与磷酸盐等离子发生反应形成固体,沉积在黄水输送系统中[11, 12]。研究人员[13, 14]在源分离排水系统工程案例中发现大量磷基固体沉积在黄水收集器及黄水运输管道中,造成一定程度的管道堵塞,增加了排水管道的维护成本。此外,磷基固体在黄水输送系统中的沉积一定程度上导致黄水中磷元素的流失,降低了污水中营养元素资源化回收率,成为了当前黄水输送系统规模化推广应用的主要挑战之一[15]。
针对磷基矿物在输送系统中的沉积问题,本研究系统性地评估了磷基矿物在黄水收集和运输过程中的沉积特性,分析了pH值、n(Ca)/n(Mg)、柠檬酸盐、转速等各类因素对磷基矿物结晶特性的影响, 旨在为黄水输送系统的设计及优化提供试验和理论基础,有助于推进人类排泄物资源化的研究,尤其是对未来城镇污水排放系统的建设与发展、推进我国“厕所革命”具有重要的意义和价值。
1 材料与方法 1.1 自配黄水由于真实黄水的理化指标不稳定,研究人员通常会使用自配黄水来替代真实黄水进行相关试验研究[16-18]。在本研究所有的结晶实验中,均使用自配黄水来代替真实黄水。本研究针对自配黄水做出以下假设:(ⅰ)黄水已完全水解;(ⅱ)由于黄水中的有机络合物对结晶沉淀的影响可以忽略不计,因此自配黄水的配方中不包含有机络合物;(ⅲ)为了避免黄水中的钙、镁离子在结晶实验进行前与黄水中的磷酸盐等物质发生反应,在配置黄水时将黄水中的钙、镁成分单独配置,在结晶实验开始时单独加入。自配黄水的合成配方如表 1所示[12, 16-19]。
| 成分 | 物质的量浓度/(mol·L-1) | 质量浓度/(g·L-1) |
| CaCl2·2H2O | 0.004 6 | 0.676 29 |
| NaH2PO4·2H20 | 0.024 0 | 3.744 24 |
| MgCl2·6H2O | 0.003 9 | 0.792 91 |
| NaCl | 0.037 6 | 2.197 34 |
| KCl | 0.056 0 | 4.174 80 |
| Na2SO4 | 0.016 0 | 2.272 64 |
| NH4OH (conc.) | 0.311 9 | 10.928 98 |
| NH4HCO3 | 0.266 7 | 21.085 30 |
| NaOH | 0.023 7 | 0.948 00 |
用以结晶实验的结晶系统包括6组1 L的玻璃反应器,采用可控制转速的六联搅拌器(MY3000-6M)对反应溶液进行搅拌。所有的结晶反应均在室温条件(19±1) ℃下进行。采用哈希HQ30d便携式pH测定仪监测记录溶液pH值和温度,并通过使用氢氧化钠(2 mol ·L-1)和盐酸溶液(2 mol ·L-1)调节反应溶液的pH值。参考先前鸟粪石结晶实验[20-23],所有结晶实验的反应时间控制为90 min,沉淀时间控制为30 min,待结晶反应结束后,采用真空抽滤装置将溶液中的结晶颗粒通过0.45 μm滤膜进行过滤,为了避免结晶产物中鸟粪石的挥发,将收集到的结晶产物在23 ℃条件下的真空干燥箱中干燥,以进行后续的表征工作。本工作研究了pH值、n(Ca)/n(Mg)、柠檬酸盐、转速对黄水中磷基矿物结晶特性的影响。所有用于结晶反应的自配黄水在实验前均进行离子浓度分析检查,以确保实验的准确性。结晶实验的控制条件见补充材料。
1.3 主要理化指标及分析方法本工作主要分析的理化指标有pH值、钾离子、铵根离子、钠离子、硫酸根离子、氯离子、磷酸根离子、镁离子、钙离子、总悬浮固体等,其中pH值采用哈希HQ30d便携式pH测定仪测定,钾离子、铵根离子、钠离子、硫酸根离子、氯离子、镁离子和钙离子浓度采用离子色谱法(赛默飞ICS-600离子色谱仪)测定,磷酸根离子采用分光法(北京普析T9S紫外可见分光光度计)测定,总悬浮固体采用烘干减重法测定。此外,分别使用日本理学Smartlab-9kw X射线衍射仪、德国LEO1450扫描电子显微镜、赛默飞NORAN System7能谱仪等仪器对结晶产物的物相、结构、表观形态、元素种类和元素含量等指标进行表征。
1.4 初始过饱和度指数计算本研究基于Visual MINTEQ软件对初始过饱和度指数进行计算。Visual MINTEQ是美国环境保护署(EPA)开发的一款用于解决化学平衡的计算机程序,可以计算水中无机离子和络合物的形态,评估溶解相或沉淀相对水化学的影响,研究常见氧化还原对的平衡物种,模拟滴定过程中水样化学成分的变化。Visual MINTEQ根据给定的参数文件,包括离子初始浓度、溶液pH值、温度等,通过平衡反应方程和平衡常数,进行重复迭代计算,从而最终计算出溶液体系达到平衡时,溶液中各物质的化学形态和浓度。
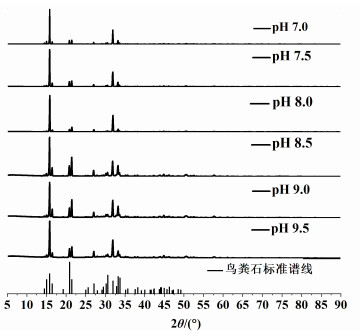
2 结果与讨论 2.1 pH值对磷基矿物结晶特性的影响研究在黄水输送系统中,受微生物脲酶的影响,黄水中的尿素会发生水解,导致黄水的pH值由6.2增加至9.1左右[19],因此,本工作探究了pH值对黄水中磷基矿物结晶特性的影响。不同pH值条件下黄水中结晶产物的XRD分析结果如图 1所示,结果显示在不同pH值条件下形成的结晶产物的衍射峰均与标准鸟粪石的特征峰相匹配,表明所有的结晶产物均以鸟粪石为主。研究发现,随pH值的增加,结晶产物衍射峰的强度表现出先增大后减小的趋势,在pH值为7.5时衍射峰的强度达到最大值。当pH值由8.0增加至8.5时,衍射峰的强度显著降低,并且在衍射图谱中观察到了明显的背景噪声,而随着pH值的进一步增加,背景噪声更加显著。XRD分析结果表明pH值会影响黄水结晶产物中鸟粪石晶体的强度和纯度,当pH值在7到8之间,结晶产物中鸟粪石的纯度较高,当pH值大于8.5时,鸟粪石的纯度开始下降。
|
| 图 1 在不同pH值条件下结晶产物的XRD分析结果 Fig.1 XRD results of crystallization products under different pH |
| |
结晶产物的SEM-EDS分析结果(见补充材料)证实了XRD的分析结果。当pH值为7时,结晶产物为形状规则的多面体晶体,以Mg-P化合物(鸟粪石)为主。当pH值升高至7.5时,结晶产物仍以形状规则的多面体鸟粪石晶体为主,但是,在鸟粪石晶体表面观察到了形状不规则的附着物,EDS分析表明附着物的主要成分为Ca-P化合物。随着pH值的进一步增加,鸟粪石晶体的生长过程受到强烈影响,在晶体表面观察到大量的裂纹及残缺,晶体形态也发生显著变化,由规则的多面体晶体转变为形状不规则的晶体,并且晶体表面被大量的无定形Ca-P化合物覆盖。此外,SEM分析结果显示鸟粪石晶体的粒径呈现出先增大后减小的趋势。
pH值对黄水中磷基矿物结晶特性的影响本质上归因于pH值变化引起的磷基矿物相初始过饱和度指数的变化。在本研究中,鸟粪石被确定为唯一生成的Mg-P化合物,而Ca-P化合物大多数以无定形形式存在[12, 23, 24],主要有无定形磷酸钙[ACP,Ca3(PO4)2]、磷酸三钙[TCP,Ca3(PO4)2]、磷酸八钙[OCP,Ca4H(PO4)3 ·3H2O(s)]、无水磷酸二钙[DCPA,CaHPO4(s)]、羟基磷灰石[HAP,Ca10(PO4)6(OH)2]、磷酸二钙二水合物[DCPD,CaHPO4 ·2H2O(s)]。基于Visual MINTEQ软件,计算了不同pH值条件下鸟粪石和几种潜在的Ca-P化合物的初始过饱和度指数,如表 2所示。
| pH | MAP | HAP | OCP | ACP | DCPA | DCPD | TCP |
| 7.0 | 1.596 | 11.345 | 3.866 | 2.415 | 1.198 | 0.877 | 3.507 |
| 7.5 | 2.164 | 13.455 | 5.021 | 3.504 | 1.265 | 0.943 | 4.595 |
| 8.0 | 2.667 | 15.263 | 5.892 | 4.397 | 1.243 | 0.921 | 5.488 |
| 8.5 | 3.107 | 16.624 | 6.39 | 5.017 | 1.121 | 0.800 | 6.108 |
| 9.0 | 3.437 | 17.396 | 6.412 | 5.281 | 0.878 | 0.557 | 6.372 |
| 9.5 | 3.600 | 17.750 | 6.100 | 5.294 | 0.551 | 0.231 | 6.386 |
计算结果表明HAP、OCP、ACP及TCP的初始过饱和度指数在pH值7.0~8.0的区间内迅速增大,而在pH值8.0~9.5的区间内,尽管也观察到了增加的趋势,但增加值相对较小。初始过饱和度指数的计算结果与SEM-EDS的分析结果相一致。在pH值为7.0时,Ca-P化合物的初始过饱和度指数相对较低,SEM-EDS的分析结果显示结晶产物中仅含有少量的Ca-P化合物,观察到的结晶产物主要为形状规则的鸟粪石晶体。而当pH值增加至8.0时,由于Ca-P化合物的初始过饱和度指数在pH值7.0~8.0的区间内迅速增大,导致结晶产物中Ca-P化合物的比例迅速增加,降低了结晶产物中鸟粪石的纯度。
结晶产物中Ca-P化合物比例的增加显著改变了鸟粪石晶体的形态,这可能是由于Ca-P化合物干扰了鸟粪石晶体的结晶反应[25]。不同比容的Ca-P化合物在鸟粪石晶体表面的共沉淀和共结晶影响了鸟粪石晶体的形态,导致鸟粪石晶体结构内产生相对较大的张力,导致晶体裂纹、不规则表面、残缺的出现[26]。
由于成核和晶体生长之间的竞争关系,不同pH值条件下鸟粪石初始过饱和度指数的变化对鸟粪石晶体的粒径大小有直接影响,通常在高过饱和度的条件下,鸟粪石晶体的成核率较高,导致体系中形成数量更多、但粒径更小的晶体[27]。然而,当过饱和度指数较低时,鸟粪石晶体的成核过程消耗了体系中可用于结晶反应的大部分离子,导致参与鸟粪石晶体生长过程的离子较少,使得鸟粪石晶体的生长过程受限、粒径相对较小。在这种情况下,增加反应体系的初始高饱和度指数,有助于补充用于鸟粪石晶体生长过程的离子数量,从而有利于更大粒径的鸟粪石晶体的形成。因此,当溶液的初始pH值由7.0增加至7.5时,观察到鸟粪石晶体粒径的增大。然而,随着溶液初始pH值的进一步增加,鸟粪石晶体的初始过饱和度指数进一步增大,增加了体系中鸟粪石晶体的成核率,导致鸟粪石晶体粒径的减小。Ronteltap等[27]在研究pH值对鸟粪石结晶的影响时也观察到了类似的现象,验证了本文的观点,其研究结果显示当pH值由7.0增加至10.0时,鸟粪石晶体的粒径呈现出先增大后减小的趋势,在pH值为8.0时达到最大粒径。此外,体系中存在的钙离子也会影响鸟粪石晶体的粒径,这可能是因为钙离子阻碍了鸟粪石晶体的生长位点,抑制了鸟粪石晶体的生长[23]。
因此,在其他结晶条件恒定的情况下,初始pH值的增加迅速增大了黄水中Ca-P化合物的过饱和度指数,使其在黄水结晶产物中的比例迅速增大,并对鸟粪石晶体的生长过程产生强烈的影响。此外,初始pH值的改变导致鸟粪石初始过饱和度指数的变化,对鸟粪石晶体的粒径大小产生显著影响。
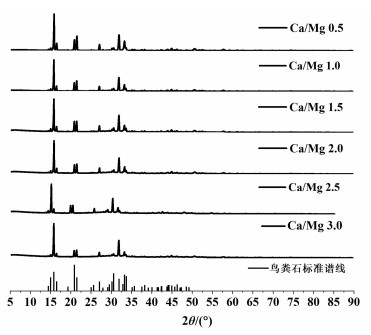
2.2 n(Ca)/n(Mg)对磷基矿物结晶特性的影响研究钙离子是生活污水中阻碍鸟粪石晶体成核和生长的代表性离子[20]。尽管已有大量的研究报道了不同废水中钙对鸟粪石结晶的影响[26, 28-31],但是仍缺少系统性的研究以评估黄水中存在的钙离子会对结晶产物中鸟粪石晶体生长过程的影响。因此,本节研究了黄水中不同浓度的钙离子对结晶产物的影响,不同n(Ca)/n(Mg)下黄水中结晶产物的XRD分析结果如图 2所示。结果显示在不同n(Ca)/n(Mg)下形成的结晶产物的衍射峰均与标准鸟粪石的特征峰相匹配,表明所有的结晶产物均以鸟粪石为主。研究发现,随着n(Ca)/n(Mg)的增加,结晶产物衍射峰的强度显著降低,并且当n(Ca)/n(Mg)大于1时,开始在衍射图谱中观察到了明显的背景噪声,并且背景噪声随n(Ca)/n(Mg)的进一步增大而变得更加显著。XRD分析结果表明黄水中存在的钙离子会影响黄水结晶产物中鸟粪石晶体的强度和纯度。当n(Ca)/n(Mg)小于1时,结晶产物中鸟粪石的纯度较高,随着n(Ca)/n(Mg)的增加,鸟粪石的纯度开始下降。
|
| 图 2 不同n(Ca)/n(Mg)下结晶产物的XRD分析结果 Fig.2 XRD results of crystallization products under different Ca/Mg molar ratio |
| |
不同n(Ca)/n(Mg)下结晶产物的SEM-EDS分析结果(见补充材料)显示当n(Ca)/n(Mg)为0.5时,结晶产物为具有高纵横比的针状晶体,以Mg-P化合物(鸟粪石)为主。随着n(Ca)/n(Mg)的增加,晶体的纵横比降低,变得更短,更厚,呈不规则状。同时结晶产物中Mg-P化合物的比例下降,而Ca-P化合物的比例升高。Yan等[24]在研究n(Ca)/n(Mg)对鸟粪石结晶的影响时观察到了类似的现象,当n(Ca)/n(Mg)较低时,鸟粪石晶体倾向于沿纵轴生长,最终形成针状晶体,然而,随着n(Ca)/n(Mg)的增加,鸟粪石晶体的形态,包括其大小和形状,发生了显著变化,由规则的针状晶体变为不规则状晶体,并且表面被无定形Ca-P化合物覆盖。
钙离子通常是通过竞争反应体系中的磷酸根离子或通过直接干扰鸟粪石晶体的生长过程来影响鸟粪石的形成[20]。由于Ca-P化合物的溶解度比Mg-P化合物的更低,导致当体系中钙、镁离子共存时,Ca-P化合物比Mg-P化合物更易于成核,同时在动力学上阻碍鸟粪石晶体的成核过程[23]。先前的研究表明,当体系中初始Mg/N/P摩尔比恒定为1 ∶1 ∶1时,增加的n(Ca)/n(Mg)会抑制鸟粪石晶体的形成,并且在n(Ca)/n(Mg)超过2的情况下,鸟粪石的结晶会被钙离子完全抑制[24]。然而,在黄水中,相对于钙、镁离子,磷酸盐是“过量”的。如表 3所示,基于Visual MINTEQ软件,计算了不同n(Ca)/n(Mg)下当黄水中Ca-P化合物完全析出后的鸟粪石的过饱和度指数,结果表明即使黄水中所有的钙离子优先与磷酸盐反应形成Ca-P化合物,黄水中仍有足够的磷酸盐可与镁离子发生反应而生成鸟粪石。
| n(Ca)/n(Mg) | MAP |
| 0.5 | 3.517 |
| 1.0 | 3.498 |
| 1.5 | 3.477 |
| 2.0 | 3.454 |
| 2.5 | 3.431 |
| 3.0 | 3.405 |
| a假设黄水中Ca-P化合物已经完全结晶析出。 | |
因此,在黄水中,Ca-P化合物和Mg-P化合物之间并不存在明显的竞争关系,钙离子主要是参与影响鸟粪石晶体的生长过程,XRD与SEM-EDS的分析结果验证了这一观点,即使在高n(Ca)/n(Mg)条件下,结晶产物中仍存在一定比例的鸟粪石晶体。鸟粪石晶体在结晶产物中的比例下降的原因主要是因为随着钙离子浓度的增加,黄水中形成了更多的Ca-P化合物。
2.3 柠檬酸盐对磷基矿物结晶特性的影响研究柠檬酸盐是健康人尿的重要组成成分,其24 h的正常排泄量在0.000 5~0.005 0 mol之间,当尿液中的柠檬酸盐含量较低时,会增加钙类结石在人体中出现的风险[32]。当前关于柠檬酸盐对黄水中磷基矿物结晶特性影响的研究比较局限,因此本节研究了柠檬酸盐对黄水中磷基矿物结晶特性的影响。
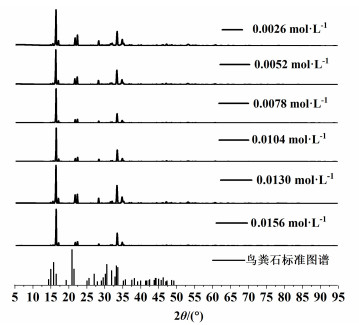
不同柠檬酸盐浓度下黄水中结晶产物的XRD分析结果如图 3所示,结果显示在不同柠檬酸盐浓度下形成的结晶产物的衍射峰均与标准鸟粪石的特征峰相匹配,表明所有的结晶产物均以鸟粪石为主。研究发现,随柠檬酸盐浓度增加,结晶产物衍射峰的强度整体上呈升高的趋势,并且背景噪声随柠檬酸盐浓度的增加而逐渐消失。表明柠檬酸盐的存在会抑制结晶产物中无定形Ca-P化合物的形成,进而增加了鸟粪石晶体的强度和纯度。
|
| 图 3 不同柠檬酸盐浓度下结晶产物的XRD分析结果 Fig.3 XRD results of crystallization products under different citrate concentrations |
| |
结晶产物的SEM-EDS分析结果证实了XRD的分析结果(见补充材料),不同柠檬酸盐浓度下结晶产物的SEM-EDS分析结果表明当反应体系中柠檬酸盐的浓度较低时,受Ca-P化合物的影响,结晶产物呈不规则状,在晶体表面观察到大量的无定形Ca-P化合物。随着柠檬酸盐浓度的升高,晶体表面的无定形物开始减少,晶体的纵横比增加。当柠檬酸盐的浓度大于0.013 mol ·L-1时,在结晶产物中观察到了大量的具有X型形态的典型鸟粪石晶体[21, 22],并且晶体表面无附着物痕迹。EDS的分析结果表明结晶产物中钙元素的含量随着柠檬酸盐浓度的升高而不断降低,说明柠檬酸盐抑制了结晶产物中Ca-P化合物的形成。柠檬酸盐对Ca-P化合物结晶的抑制作用主要归因于其在晶体活性生长位点上的吸附,阻碍了Ca-P化合物的形成[33]。
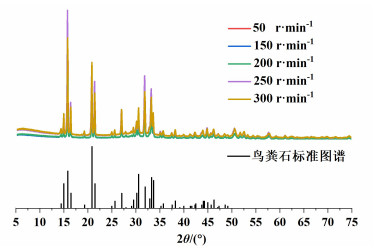
2.4 转速对磷基矿物结晶特性的影响研究搅拌通常是影响鸟粪石结晶的重要参数之一,当结晶反应器的搅拌型性能较弱时,可能导致反应器中溶液混合不均匀,产生局部的高过饱和度,使结晶过程更倾向于成核过程[34]。本工作探究了同一结晶反应器内转速对黄水磷基矿物结晶特性的影响。不同转速条件下结晶产物的XRD分析结果如图 4所示,结果显示不同转速下形成的结晶产物的衍射图谱无明显差别,衍射峰均与标准鸟粪石的特征峰相匹配,并且在所有的衍射图谱中均观察到了由于Ca-P化合物的存在导致的背景噪声。XRD的分析结果说明转速对结晶产物的晶体构成无明显影响,不同转速条件下,结晶产物均由鸟粪石晶体及Ca-P化合物组成。
|
| 图 4 不同转速条件下结晶产物的XRD分析结果 Fig.4 XRD results of crystallization products under different rotational speeds |
| |
不同转速条件下结晶产物的SEM-EDS分析结果(见补充材料)表明转速对结晶产物的晶体形态、粒径均无明显影响。然而,在Ronteltap等[27]研究研究转速对黄水中结晶产物晶体形态、粒径的影响时,镁溶液以12 mL ·h-1的流量连续泵入结晶反应器,在具有更强混合性能的结晶反应器中得到了平均粒径更大的鸟粪石晶体,导致研究结果不同的主要原因是由于当结晶反应器的混合性能不佳时,会导致反应器内部离子分布不均匀,产生局部的高过饱和度。在本研究中,钙、镁离子是以溶液的形式一次性加入结晶反应器,当钙、镁离子加入后,成核反应立刻发生,迅速消耗了结晶反应器内的钙、镁离子,导致体系中磷基矿物的过饱和度指数迅速下降,结晶反应由成核过程迅速转变为晶体生长过程,此时不同转速条件下的结晶反应均以晶体生长为主,因此,在不同转速条件下,观察到了相似晶体形态、粒径的结晶产物。
3 结论基于磷基矿物在黄水输送过程中的沉积问题,本工作系统性地评估了pH值、n(Ca)/n(Mg)、柠檬酸盐、转速等因素对磷基矿物结晶特性的影响。初始pH值的增加引起了黄水中磷基矿物相初始过饱和度指数的变化,随着初始pH值的增加,黄水中HAP、OCP、ACP及TCP等Ca-P化合物的初始过饱和度指数迅速增大,使黄水结晶产物中Ca-P化合物的比例增高,鸟粪石晶体比例下降,在这一过程中,Ca-P化合物干扰了鸟粪石晶体的结晶反应,鸟粪石晶体的生长过程受到强烈影响,晶体表面出现大量裂纹及残缺,晶体形态发生显著变化,由规则的多面体晶体转变为形状不规则的晶体,表面被大量的无定形Ca-P化合物覆盖。
在黄水中,Ca-P化合物和Mg-P化合物之间并不存在明显的竞争关系,钙离子主要是参与影响鸟粪石晶体的生长过程,在高n(Ca)/n(Mg)初始条件下,结晶产物中仍存在一定比例的鸟粪石晶体。此外,研究结果显示柠檬酸盐对结晶产物中Ca-P化合物的形成由一定的抑制作用,主要归因于其在晶体活性生长位点上的吸附,阻碍了Ca-P化合物的形成。在本研究中,转速对磷基矿物的结晶特性,包括晶体构成、晶体形态以及晶体粒径均无显著影响。
本研究系统性地阐明了黄水输送过程中pH值变化、n(Ca)/n(Mg)等因素对磷基矿物结晶特性的影响,一方面为源分离黄水输送系统的搭建提供理论依据,另一方面明晰了源分离黄水输送过程中导致管道结垢堵塞的主要因素,为管道结垢缓解控制措施的研究提供理论参考。
| [1] |
GAJUREL D R, LI Z, OTTERPOHL R. Investigation of the effectiveness of source control sanitation concepts including pre-treatment with Rottebehaelter[J]. Water Science and Technology, 2003, 48(1): 111-118. DOI:10.2166/wst.2003.0029 |
| [2] |
PAHL-WOSTL C, SCHÖNBORN A, WILLI N, et al. Investigating consumer attitudes towards the new technology of urine separation[J]. Water Science and Technology: A Journal of the International Association on Water Pollution Research, 2003, 48(1): 57-65. DOI:10.2166/wst.2003.0015 |
| [3] |
VINNERÅS B, JÖNSSON H. The performance and potential of faecal separation and urine diversion to recycle plant nutrients in household wastewater[J]. Bioresource Technology, 2002, 84(3): 275-282. DOI:10.1016/S0960-8524(02)00054-8 |
| [4] |
LARSEN T A, GUJER W. The concept of sustainable urban water management[J]. Water Science and Technology, 1997, 35(9): 3-10. DOI:10.2166/wst.1997.0326 |
| [5] |
LARSEN T A, GUJER W. Separate management of anthropogenic nutrient solutions (human urine)[J]. Water Science and Technology, 1996, 34(3/4): 87-94. |
| [6] |
李子富. 城镇污水处理源头控制技术及进展[J]. 建设科技, 2013(2): 32-35. LI Zifu. Source control technology and progress of urban sewage treatment[J]. Building Technology, 2013(2): 32-35. DOI:10.3969/j.issn.1671-3915.2013.02.011 (in Chinese) |
| [7] |
曹睿, 封莉, 杜子文, 等. 农村生活污水传统处理与源分离处理碳排放比较[J]. 环境科学, 2024(8): 1-13. CAO Rui, FENG Li, DU Ziwen, et al. Comparison of carbon emissions between traditional treatment and source separation treatment of rural domestic sewage[J]. Environmental Science, 2024(8): 1-13. (in Chinese) |
| [8] |
段文俊, 陆茵, 孙利利, 等. 我国高寒旱地区源分离尿液碱性稳定化研究[J]. 环境卫生工程, 2023, 31(3): 1-8. DUAN Wenjun, LU Yin, SUN Lili, et al. Study on alkaline stabilization of source-separated urine in alpine-cold and water shortage area of China[J]. Environmental Sanitation Engineering, 2023, 31(3): 1-8. (in Chinese) |
| [9] |
RANDALL D G, KRÄHENBüHL M, KÖPPING I, et al. A novel approach for stabilizing fresh urine by calcium hydroxide addition[J]. Water Research, 2016, 95: 361-369. DOI:10.1016/j.watres.2016.03.007 |
| [10] |
刘铭, 熊霞, 魏珞宇, 等. 源分离尿液废水资源化处理研究进展[J]. 中国沼气, 2023, 41(1): 3-12. LIU Ming, XIONG Xia, WEI Luoyu, et al. Biogas institute of ministry of agriculture and rural affairs[J]. China Biogas, 2023, 41(1): 3-12. (in Chinese) |
| [11] |
UDERT K M, LARSEN T A, BIEBOW M, et al. Urea hydrolysis and precipitation dynamics in a urine-collecting system[J]. Water Research, 2003, 37(11): 2571-2582. DOI:10.1016/S0043-1354(03)00065-4 |
| [12] |
UDERT K M, LARSEN T A, GUJER W. Estimating the precipitation potential in urine-collecting systems[J]. Water Research, 2003, 37(11): 2667-2677. DOI:10.1016/S0043-1354(03)00071-X |
| [13] |
LIENERT J, LARSEN T A. High acceptance of urine source separation in seven European countries: A review[J]. Environmental Science & Technology, 2010, 44(2): 556-566. |
| [14] |
HELLSTRÖM D, JOHANSSON E. Swedish experiences with urine separating systems[J]. Wasser Und Boden, 1999, 51(11): 26-29. |
| [15] |
YAN Z, CHENG S, ZHANG J, et al. Precipitation in urine source separation systems: Challenges for large-scale practical applications[J]. Resources, Conservation and Recycling, 2021, 169: 105479. DOI:10.1016/j.resconrec.2021.105479 |
| [16] |
XU K, LI J, ZHENG M, et al. The precipitation of magnesium potassium phosphate hexahydrate for P and K recovery from synthetic urine[J]. Water Research, 2015, 80: 71-79. DOI:10.1016/j.watres.2015.05.026 |
| [17] |
ZHANG R, SUN P, BOYER T H, et al. Degradation of pharmaceuticals and metabolite in synthetic human urine by UV, UV/H2O2, and UV/PDS[J]. Environmental Science & Technology, 2015, 49(5): 3056-3066. |
| [18] |
SUN P, LI Y, MENG T, et al. Removal of sulfonamide antibiotics and human metabolite by biochar and biochar/H2O2 in synthetic urine[J]. Water Research, 2018, 147: 91-100. DOI:10.1016/j.watres.2018.09.051 |
| [19] |
UDERT K M, LARSEN T A, GUJER W. Fate of major compounds in source-separated urine[J]. Water Science and Technology: A Journal of the International Association on Water Pollution Research, 2006, 54(11/12): 413-420. |
| [20] |
LE CORRE K S, VALSAMI-JONES E, HOBBS P, et al. Impact of calcium on struvite crystal size, shape and purity[J]. Journal of Crystal Growth, 2005, 283(3/4): 514-522. |
| [21] |
LIU Y, QU H. Interplay of digester supernatant composition and operating pH on impacting the struvite particulate properties[J]. Journal of Environmental Chemical Engineering, 2017, 5(4): 3949-3955. DOI:10.1016/j.jece.2017.07.065 |
| [22] |
SHADDEL S, UCAR S, ANDREASSEN J P, et al. Engineering of struvite crystals by regulating supersaturation-Correlation with phosphorus recovery, crystal morphology and process efficiency[J]. Journal of Environmental Chemical Engineering, 2019, 7(1): 102918. DOI:10.1016/j.jece.2019.102918 |
| [23] |
LIU X, WANG J. Impact of calcium on struvite crystallization in the wastewater and its competition with magnesium[J]. Chemical Engineering Journal, 2019, 378: 122121. DOI:10.1016/j.cej.2019.122121 |
| [24] |
YAN H, SHIH K. Effects of calcium and ferric ions on struvite precipitation: A new assessment based on quantitative X-ray diffraction analysis[J]. Water Research, 2016, 95: 310-318. DOI:10.1016/j.watres.2016.03.032 |
| [25] |
MORAGASPITIYA C, RAJAPAKSE J, MILLAR G J. Effect of Ca/Mg ratio and high ammoniacal nitrogen on characteristics of struvite precipitated from waste activated sludge digester effluent[J]. Journal of Environmental Sciences (China), 2019, 86: 65-77. DOI:10.1016/j.jes.2019.04.023 |
| [26] |
HUTNIK N, KOZIK A, MAZIENCZUK A, et al. Phosphates (Ⅴ) recovery from phosphorus mineral fertilizers industry wastewater by continuous struvite reaction crystallization process[J]. Water Research, 2013, 47(11): 3635-3643. DOI:10.1016/j.watres.2013.04.026 |
| [27] |
RONTELTAP M, MAURER M, HAUSHERR R, et al. Struvite precipitation from urine-Influencing factors on particle size[J]. Water Research, 2010, 44(6): 2038-2046. DOI:10.1016/j.watres.2009.12.015 |
| [28] |
PASTOR L, MARTI N, BOUZAS A, et al. Sewage sludge management for phosphorus recovery as struvite in EBPR wastewater treatment plants[J]. Bioresource Technology, 2008, 99(11): 4817-4824. DOI:10.1016/j.biortech.2007.09.054 |
| [29] |
LEE S H, YOO B H, KIM S K, et al. Enhancement of struvite purity by re-dissolution of calcium ions in synthetic wastewaters[J]. Journal of Hazardous Materials, 2013, 261: 29-37. DOI:10.1016/j.jhazmat.2013.06.072 |
| [30] |
YE Z, CHEN S, WANG S, et al. Phosphorus recovery from synthetic swine wastewater by chemical precipitation using response surface methodology[J]. Journal of Hazardous Materials, 2010, 176(1/2/3): 1083-1088. |
| [31] |
BARBOSA S G, PEIXOTO L, MEULMAN B, et al. A design of experiments to assess phosphorous removal and crystal properties in struvite precipitation of source separated urine using different Mg sources[J]. Chemical Engineering Journal, 2016, 298: 146-153. DOI:10.1016/j.cej.2016.03.148 |
| [32] |
JOHRI N, JAEGER P, ROBERTSON W, et al. Renal stone disease[J]. Medicine, 2011, 39(7): 371-377. DOI:10.1016/j.mpmed.2011.04.005 |
| [33] |
CAO X D, HARRIS W. Carbonate and magnesium interactive effect on calcium phosphate precipitation[J]. Environmental Science & Technology, 2008, 42(2): 436-442. |
| [34] |
MERSMANN A. Crystallization technology handbook[M]. Florida, United States: CRC Press, 2001.
|
 2024, Vol. 41
2024, Vol. 41





