由于纺织品、染色和印刷等各种工业应用对亚甲基蓝(MB)废水的处理不足,未达标的MB废水流入水体,会使水变色并污染[1]。MB废水由于其化学性质对人类健康、动物和植物生态系统造成严重后果,尤其是它具有致癌性[2]。为去除废水中的污染物,人们探索了许多技术,吸附法具有效率高、处理简单、成本低等优点,被证明是一种更适合去除污染物的方法[3]。
传统的磁性生物炭,由于磁性介质的阻塞,磁性生物炭通常表现出较低的比表面积和较小的孔隙体积,因此对污染物的去除效率相对较低[4]。对磁性生物炭进行改性,提高其物理和化学性能,以提高其吸附的效率,受到了越来越多的关注[5]。为改善磁性生物炭的性能,开发了许多技术,如酸碱改性、表面功能改性、氧化和元素掺杂等。在这些方法中,元素掺杂是改变磁性生物炭性质从而提高吸附性能的有效方法。
Chin等[6]报道掺杂了金属(Ce、Cu、Co和Mn)的改性磁性生物炭的比表面积以及羰基和羧基的数量大大增加,提高了对汞的去除效率。Liang等[7]发现,与未修饰形式相比,Cr(Ⅵ)的去除率得到了提高。有报告表明,在样品中添加氯化锌可以增加磁性活性炭的表面积,从而影响吸附剂的吸附能力[8]。
受这些研究的启发,这项工作利用醋酸锌对椰棕磁性生物炭进行改性。对改性磁性生物炭做了批量吸附实验,验证了其优异的吸附性能。此外,还通过各种表征方法揭示了改性磁性生物炭的物理化学特性。
1 材料与方法 1.1 实验材料椰棕从海南大学附近水果店购买。醋酸锌[(CH3COO)2Zn]、三氯化铁(FeCl3)和氢氧化钠(NaOH)由上海麦克林生化公司提供。亚甲基蓝(MB)由阿拉丁股份有限公司提供。盐酸、氯化钠、氯化钙、氯化镁、硝酸钠、碳酸钠、硫酸钠、磷酸乙醇、乙酸等均购自西龙科技有限公司。所有化学试剂均为分析试剂级。
1.2 生物炭的制备原始生物炭的制备:称取10 g制备好的椰棕粉末放入刚玉方舟中,然后放入通有氮气保护气的管式炉中进行热解,以5 ℃·min-1速率升温至600 ℃,保温1 h。对椰棕原炭,命名为BC600。
磁性生物炭的制备:将10 g氯化铁完全溶解在含有30 mL超纯水的50 mL烧杯中。将溶解后的氯化铁和10 g椰棕置于500 mL玛瑙球磨罐中,进行球磨。球磨后进行热裂解,同原始生物炭的制备方法一样。制备好的磁性生物炭命名为FBC600。
改性磁性生物炭的制备:将10 g氯化铁和10 g醋酸锌完全溶解在含有30 mL超纯水的50 mL烧杯中。将溶解后的混合物和10 g椰棕置于500 mL玛瑙球磨罐中,进行球磨。接下来的步骤与磁性生物炭的制备方法一样。制备好的改性磁性生物炭根据醋酸锌用量命名:加入5 g醋酸锌命名为0.5MBC600、加入10 g醋酸锌命名为MBC600和加入20 g醋酸锌命名为2MBC600。
1.3 生物炭的表征生物炭中的有机元素(C、H、O和N)由德国Elementar公司的有机元素分析仪(Vario EL cube)测量,无机元素(Fe和Zn)由美国安捷伦公司的电耦合等离子体原子发射光谱仪(Agilent ICPOES730)测量;物理分析(BET)通过美国麦克公司的物理吸附仪(ASAP 2460)测试的;傅里叶变换红外光谱仪(Bruker Tensor 27)测试生物炭的红外光谱;生物炭表面的电荷性质通过Zeta电位分析仪(Zetasizer Nano ZS)测量;为了确定改性后生物炭磁性的强弱,通过超导干涉量子仪(MPMS(SQUID)XL-7)在正负4T的条件下测量生物炭的磁滞回线;生物炭表面的形貌、孔道结构和元素分布等扫描电子显微镜(Phenom Prox)进行测试为了确定生物炭的结构,可以通过拉曼光谱(In Via,Renishaw plc)中的拉曼位移来测量:为了获得生物炭的成分以及C和Fe原子的结构形态,使用X射线衍射仪对生物炭的晶体结构进行分析;生物炭表面的元素组成和元素价态是通过X射线光电子能谱仪(Thermo Scientific Escalab 250Xi)表征的。
1.4 生物炭的吸附实验所有吸附是0.5 g·L-1的生物炭和MB溶液在180 r·min-1的振荡速度下在目标时间内进行的。通过紫外分光光度计在665 nm波长下测定MB的浓度。为了确保实验的准确性,所有吸附都进行了3次,并使用了平均值。吸附量qe由方程(1)确定。
| $q_{\mathrm{e}}=\left(c_0-c_{\rm{e}}\right) V / m$ | (1) |
式(1)中:qe为生物炭对MB的吸附量,mg·g-1;c0为MB的初始浓度,mg·g-1;ce为吸附时MB的平衡浓度,mg·g-1;V为被吸MB的体积,L;m是生物炭的质量,g。
在目标时间内研究了生物炭的动力学,对伪一级动力学模型公式(2)和伪二级动力学模型公式(3)进行拟合;在15、25和35 ℃温度下,研究了温度对生物炭吸附能力的影响(吸附72 h),将实验得出的等温线数据通过Langmuir公式(4)模型和Freundlich公式(5)模型进行拟合。研究了共存离子(50 mmol·L-1)如(Na+、Mg2+、Ca2+、Cl-、NO3-、CO32-、SO42-和PO43-)对生物炭吸附性能的影响。
| $q_{\mathrm{t}}=q_{\mathrm{e}}\left[1-\exp \left(-k_1 t\right)\right]$ | (2) |
式(2)中:qt表示时间为t的吸附量,mg·g-1;qe表示为平衡吸附量,mg·g-1;k1为伪一级动力学吸附模型的吸附常数。
| $q_{\mathrm{t}}=\left(q_{\mathrm{e}}^2 k_2 t\right) /\left(l+q_{\mathrm{e}} k_2 t\right)$ | (3) |
式(3)中:qt表示时间为t的吸附量,mg·g-1;qe表示为平衡吸附量,mg·g-1;k2为伪二级动力学吸附模型的吸附常数。
| $q_{\mathrm{e}}=\left(K_{\mathrm{L}} q_{\max } c_{\mathrm{e}}\right) /\left(1+K_{\mathrm{L}} c_{\mathrm{e}}\right)$ | (4) |
式(4)中:ce表示吸附达到平衡时污染物的浓度,mg·L-1;qe和qmax分别表示生物炭对污染物的平衡吸附量和最大吸附量,mg·g-1;KL是Langmuir吸附亲和常数。
| $q_{\mathrm{e}}=K_{\mathrm{F}} c_{\mathrm{e}}^{(1 / n)}$ | (5) |
式(5)中:ce表示吸附达到平衡时污染物的浓度,mg·L-1;qe表示生物炭对污染物的平衡吸附量,mg·g-1;KF是Freundlich吸附亲和常数;n表示多相性指数。
1.5 再生实验再生实验是将200 mg吸附后MB的MBC600分别加入400 mL乙醇/乙酸(质量比9∶1,下同)洗脱液中,在25 ℃的恒温振荡器中以180 r·min-1振荡解吸24 h。
2 结果与讨论 2.1 生物炭的表征 2.1.1 元素组成和物理分析如表 1所示,BC600主要由C、H和O元素组成,磁性生物炭FBC600和MBC600由C、H、O和Fe元素组成。与FBC600相比,MBC含有更多的Fe和O元素。此外,MBC600还含有0.6%的Zn元素。这表明(CH3COO)2Zn作为改性剂,促进含氧基团的形成和更多的Fe元素负载在生物炭上。改性后,MBC600的比表面积(SSA)和孔隙体积(PV)分别为799.7 m2·g-1和0.46 cm3·g-1,远大于FBC600。总之,(CH3COO)2Zn作为改性剂大大的提高了磁性生物炭的物理性质。
| 生物炭 | 元素组成/% | 表面分析 | |||||
| C | H | O | Fe | Zn | SSA/(m2·g-1) | PV/(cm3·g-1) | |
| BC600 | 71.9 | 2.7 | 18.66 | 0 | 0 | 39.1 | 0.02 |
| FBC600 | 52.8 | 1.3 | 17.10 | 24.4 | 0 | 381.4 | 0.27 |
| MBC600 | 47.6 | 1.1 | 19.54 | 31.1 | 0.6 | 799.7 | 0.46 |
| SSA:比表面积,m2·g-1;PV:孔隙体积,cm3·g-1。 | |||||||
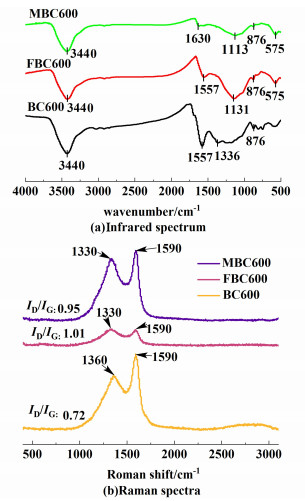
对傅里叶变换红外光谱图 1(a)进行了分析,在3 440 cm-1处的峰值是O—H的伸缩振动。1 557~1 630 cm-1处的峰值属于芳香族C=C基团的伸缩振动吸收峰[9, 10]。1 140 cm-1处的峰值可归因于C—OH/C—O—C伸展振动[11]。与FBC600相比,MBC600在1 557~1 630 cm-1和1 140 cm-1处的峰值减小,可能是由于(CH3COO)2Zn的加入,使MBC600中C=C官能团的数量减少。876 cm-1附近的条带可归因于芳香基团的C—H振动[12]。575 cm-1处的峰值属于Fe—O伸展振动,这表明MBC600和FBC600成功的负载了Fe元素[13]。拉曼光谱如图 1(b)。可以观察到1 330 cm-1左右的D峰和1 590 cm-1左右的G峰。ID/IG的比值可以评估生物炭的结构完整性和晶体质量。MBC600和FBC600的ID/IG比值分别为0.91和1.02,表明改性后的磁性生物炭的结构缺陷多,晶格质量差[14]。
|
| 图 1 生物炭的红外和拉曼光谱 Fig.1 Infrared and Raman spectra of biochar |
| |
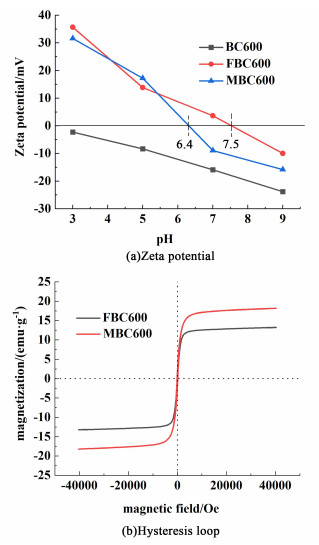
图 2(a)是所制备生物炭的Zeta电位与pH值的关系。随着pH值的增加,Zeta电位逐渐降低。由于羟基的存在,BC600显示出很强的负电位[15]。由于阳离子的存在,MBC600和FBC600显示出更高的电位,FBC600的零点电荷pH值为7.5,MBC600的零点电荷pH值为6.4。磁滞回线图 2(b)显示,MBC600和FBC600饱和磁化强度分别为13.20和18.8 emu·g-1,与FBC600相比,MBC600表现出更高的饱和磁化强度。
|
| 图 2 生物炭的磁滞回线和Zeta电位 Fig.2 Hysteresis loop and zeta potential of biochar |
| |
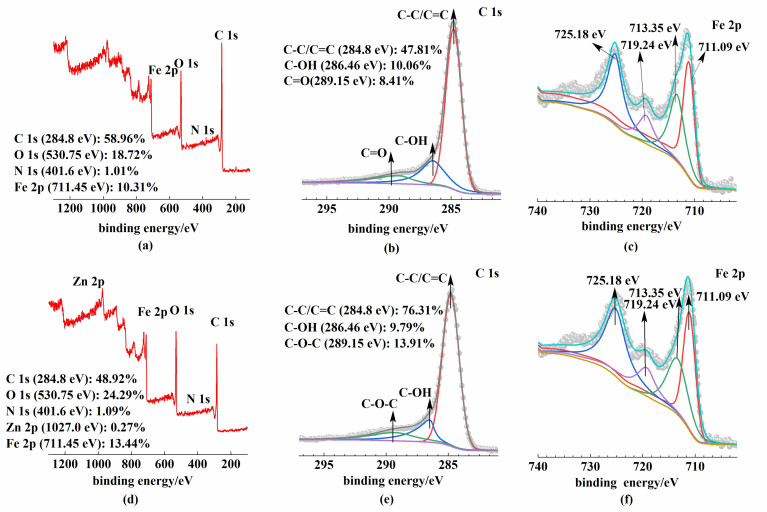
XPS分析如图 3所示,如图 3(a)和图 3(d),在FBC600和MBC600上检测到Fe元素,MBC600上还有少量的Zn元素。如图 3(b)和图 3(e),在2种磁性生物炭的C1s光谱中,289.2、286.5和284.8 eV处的峰分别是C—O—C、C—OH和C=C/C—C的基团[16, 17],由于(CH3COO)2Zn的加入,MBC600含有更多的C—O—C和C—OH基团。这些含氧基团是吸附亚甲基蓝的主要位点[8]。如图 3(f)是MBC600的Fe 2p光谱,711.09 eV处的结合能是Fe2+的特征峰,而713.35 eV处的结合能属于Fe3+的特征峰。719.24 eV处的结合能是Fe2+和Fe3+的卫星峰。这证实了在MBC600中形成了Fe3O4颗粒[18],没有锌光谱可能是由于锌含量极少。
|
| 图 3 生物炭的XPS光谱: (a~c)FBC600;(d~f)MBC600 Fig.3 XPS spectra of biochar: (a—c)FBC600;(d—f)MBC600 |
| |
扫描电镜SEM图像如图 4所示,图 4(a)和图 4(b)是FBC600的SEM图像,图 4(c)和图 4(d)是MBC600的SEM图像。FBC600和MBC600均表现出粗糙表面和不同尺寸的颗粒,这表明金属氧化物的成功的负载。与FBC600相比,MBC600具有更丰富的介孔,因此比表面积和孔隙体积较大,这与上述讨论一致。

|
| 图 4 生物炭的SEM图像 Fig.4 SEM image of biochar |
| |
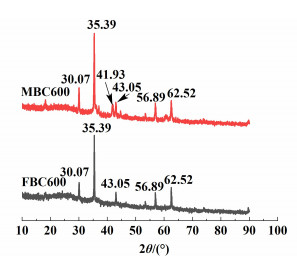
XRD图谱如图 5所示,FBC600和MBC600中没有纤维素、半纤维素和碳的衍射峰,这表明椰棕几乎分解成了无定形碳[19]。在2θ=30.07°、35.39°、43.05°、56.89°和62.52°处出现的衍射峰分别对应于Fe3O4的(220)、(311)、(400)、(511)和(440)晶面。与FBC600相比,MBC600衍射峰中Fe3O4的强度增加,这表明随着(CH3COO)2Zn的改性,Fe3O4的含量增加,这与元素分析结果一致。
|
| 图 5 生物炭的XRD图谱 Fig.5 XRD spectra of biochar |
| |
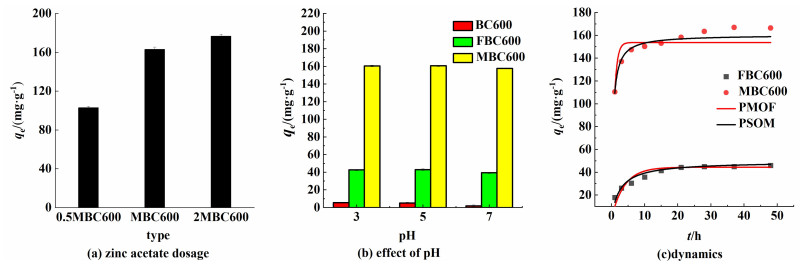
如图 6(a)所示,研究了醋酸锌的用量对吸附性能的影响。0.5MBC、MBC和2MBC是椰棕、氯化铁和醋酸锌的质量比为2∶2∶1、1∶1∶1、1∶1∶2的条件下制备的,0.5MBC600对MB的吸附量为103 mg·g-1。当醋酸锌的用量增加1倍时,很明显了提高了对MB的吸附量,此时MBC600对MB吸附量为163 mg·g-1。当醋酸锌的用量增大到2倍时,此时2MBC对MB的吸附量为176 mg·g-1。质量比为1∶1∶1从增大1∶1∶2时,对MB的吸附量提高量很低。质量比为1∶1∶1更具有性价比,后续实验用MBC600。如图 6(b)所示,研究了初始pH值对磁性生物炭吸附能力的影响。pH值在3~10的范围内,MB的吸附量随pH值的增加变化得很小。MBC600对MB的吸附能力远远高于和FBC600和BC600。在相同的pH值下,MBC600的吸附量比FBC600大得多,这可能是由于其含氧基团数量多和较高的比表面积。FBC600和MBC600的零点电荷pH值分别为7.5和6.4,溶液中的pH值低于零点电荷pH值时,吸附剂MBC600和FBC600带正电荷,会对阳离子染料MB产生排斥作用。但pH值在3~7的酸性环境,MBC600和FBC600对MB的吸附量很高,pH值在7~10的弱碱性环境中,MBC600和FBC600对MB的吸附量轻微变化。因此,静电作用对MB的吸附影响小。MBC600和FBC600在pH值为5时对MB的吸附量最大,分别为160和42.97 mg·g-1,溶液的初始pH值设定为5最适宜。
|
| 图 6 初始pH值的影响和吸附动力学 Fig.6 Effect of initial pH and adsorption kinetics |
| |
由于BC600对MB吸附量极低,因此只在25 ℃下对FBC600和MBC600进行了48 h的动力学吸附实验。如图 6(c)和表 2所示,在初始阶段,由于吸附位点丰富,MBC600和FBC600对MB的吸附速度很快。随着吸附时间的延长,由于吸附位点被占据,吸附量缓慢增加,直至达到吸附平衡。吸附平衡时,MBC600对亚甲基蓝的最大吸附量为166 mg·g-1,FBC600对亚甲基蓝的最大吸附量为45.86 mg·g-1。伪二阶模型(PSOM)得到的R2值高于由伪一阶模型(PFOF)得到的R2值,由PSOM模型计算得到的qe值更接近于实验qe值,这说明MB在MBC600和FBC600上的吸附可以用PSOM模型来描述[20]。这意味着吸附速率主要受化学吸附控制的过程[21]。
| 生物炭 | c0/(mg·g-1) | qe, exp/(mg·g-1) | 伪一级动力学 | 伪二级动力学 | |||||
| Qe/(mg·g-1) | k1 | R2 | Qe/(mg·g-1) | k2/(min-1) | R2 | ||||
| FBC600 | 100 | 45.86 | 44.45 | 0.258 | 0.914 | 49.48 | 0.007 | 0.961 | |
| MBC600 | 100 | 166.41 | 153.79 | 1.250 | 0.890 | 160.43 | 0.013 | 0.976 | |
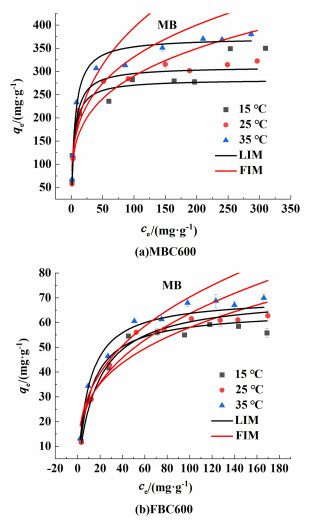
吸附等温线如图 7所示,在初始阶段,吸附量随着MB的初始浓度增加而增加,直至达到动态平衡。随着温度从25升至35 ℃,MBC600对MB的吸附量从322.16升至380.33 mg·g-1,FBC600对MB的吸附量从61.2升至71.8 mg·g-1。由Langmuir和Freundlich等温线模型拟合[22]。如表 3所示,Langmuir模型对MB吸附的R2值大于Freundlich模型的R2值,这说明Langmuir模型匹配MB的吸附,MB在MBC600和FBC600上的吸附主要是单分子层吸附,且MBC600对MB的吸附量远大于FBC600。在25 ℃时MBC600对亚甲基蓝吸附量高于大多数报告值(表 4)。
|
| 图 7 吸附等温线 Fig.7 Adsorption isotherms |
| |
| 生物炭 | 温度/℃ | qm exp/(mg·g-1) | Langmuir model | Freundlich model | |||||
| Qm | KL | R2 | KF | 1/n | R2 | ||||
| 15 | 322.16 | 282.76 | 0.176 | 0.991 | 87.20 | 0.327 | 0.874 | ||
| MBC600 | 25 | 344.06 | 307.92 | 0.200 | 0.997 | 76.02 | 0.293 | 0.847 | |
| 35 | 380.33 | 373.15 | 0.216 | 0.992 | 94.51 | 0.272 | 0.841 | ||
| 15 | 61.20 | 64.88 | 0.074 | 0.987 | 13.96 | 0.309 | 0.882 | ||
| FBC600 | 25 | 66.40 | 70.97 | 0.079 | 0.992 | 12.14 | 0.359 | 0.926 | |
| 35 | 71.80 | 70.23 | 0.085 | 0.989 | 13.55 | 0.357 | 0.927 | ||
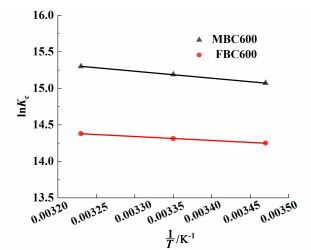
吸附热力学参数(ΔH°和ΔS°)是通过lnKc对1/T的拟合直线的斜率和截距求出[23],如图 8所示。ΔG°可由热力学第三定律得出。如表 5所示,ΔH°为正值,表明MBC600和FBC600吸附MB的过程为吸热过程。ΔS°也为正,表明MB吸附到2种磁性生物炭上后,体系的混乱程度增加。ΔG°为负值,且随吸附温度的升高而升高,说明MBC600和FBC600吸附MB是自发的,具有热力学特性。
|
| 图 8 生物炭对MB吸附的lnKc对1/T的拟合直线 Fig.8 Fitting straight line of lnKc to 1/T for MB adsorption by biochar |
| |
| 生物炭 | T/K | ΔG°/(kJ·mol-1) | ΔH°/(kJ·mol-1) | ΔS°/(J·mol-1·K-1) |
| 288 | -36.08 | |||
| MBC600 | 298 | -36.50 | 7.97 | 152.89 |
| 308 | -39.18 | |||
| 288 | -34.12 | |||
| FBC600 | 298 | -34.26 | 4.50 | 134.02 |
| 308 | -34.43 | |||
| 注:ΔGθ=-RTlnKc;lnKc= | ||||
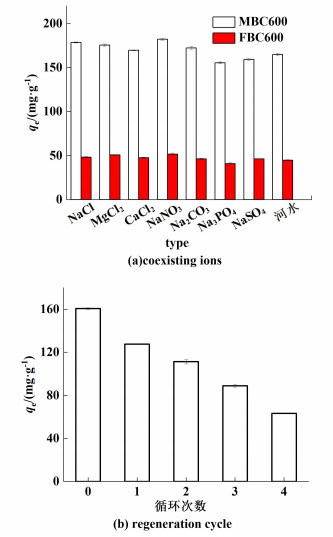
在工业废水中含有一定量的矿物质,可能对吸附产生负面影响[19]。矿物离子会通过改变生物炭的表面特性来影响目标污染物的吸附能力[29]。实验使用阳离子(Na+、Mg2+和Ca2+)和阴离子(NO3-、CO32-、SO42-和PO43-)以50 mmol·L-1浓度来研究对生物炭吸附性能的影响,结果如图 9(a)所示,MB在MBC600上的吸附,加入SO42-和PO43-会轻微降低吸附性能,而加入Na+、Mg2+、NO3-、CO32-和Ca2+则会稍微地增加吸附量。对于MB在FBC600上的吸附,这些离子的加入则会轻微影响吸附性能。生物炭的可再利用性是用作吸附材料的一个关键参数,进行了可再利用性测试。经探究,MB的最适宜脱附剂是乙醇/乙酸(9∶1,体积比)。由于MBC600的吸附量大于FBC600,因此只对MBC600进行了可重复使用性测试,结果如图 9(b)所示。随着循环次数的增加,MBC600对MB吸附能力逐渐降低,从160.9降至为63.3 mg·g-1,吸附能力的下降可能是MB的不完全不完全或某些吸附位点的不可逆效应[30]。但是,MBC600仍然有中等的吸附能力,可以回收再利用。
|
| 图 9 共存离子对生物炭的影响和再生循环 Fig.9 Effect of coexisting ions on biochar and regeneration cycle |
| |
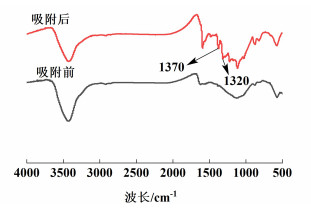
用红外表征MBC600对MB吸附后生物炭,以阐述吸附机理。如图 10,在吸附MB后的MBC600上1 370和1 320 cm-1处出现了峰,这对应C—N基团[31]。这表明吸附过程中,MB与含氧基团发生氢键作用。由于MBC600含有大量的—OH活性基团,MB可以通过这些基团的阳离子交换而被吸附。
|
| 图 10 MBC600吸附MB后的红外光谱 Fig.10 Infrared spectrum of MBC600 after MB adsorption |
| |
(1) 采用(CH3COO)2Zn对椰棕磁性生物炭进行改性,在600 ℃热裂解制备改性磁性生物炭MBC600。通过磁滞回线、元素分析、XRD、XPS、FIRT等进行表征发现,MBC600的饱和磁化强度为18.18 emu·g-1,比表面积提升为799.7 mg·g-1,孔隙体积增至为0.46 cm3·g-1,都远大于未改性的磁性生物炭,且含氧基团的数量也大于未改性的磁性生物炭。
(2) MBC600在25 ℃的条件下对MB的最大吸附量为344.06 mg·g-1,通过伪一级动力学模型和伪二级动力学模型对动力学进行拟合,发现MBC600对MB吸附速率主要受化学吸附控制的过程。通过Langmuir模型和Freundlich模型对热力学进行拟合,发现MBC600对MB的吸附主要是单层均匀化学吸附。
(3) 对MBC600进行了离子共存实验,发现大多数共存离子对MB的吸附能力影响较小。通过再生实验,经4次循环后,MBC600对MB有相对较好的再生性能。MB的吸附是通过氢键作用、阳离子交换而实现。
| [1] |
王栋, 夏晓露, 刘汇洋, 等. 毛细管微反应器降解亚甲基蓝废水试验研究[J]. 化学工业与工程, 2022, 39(4): 65-70. WANG Dong, XIA Xiaolu, LIU Huiyang, et al. Experimental study on the degradation of methylene blue wastewater by capillary microreactor[J]. Chemical Industry and Engineering, 2022, 39(4): 65-7. (in Chinese) |
| [2] |
SUTAR S, PATIL P, JADHAV J. Recent advances in biochar technology for textile dyes wastewater remediation: A review[J]. Environmental Research, 2022, 209: 112841. DOI:10.1016/j.envres.2022.112841 |
| [3] |
马紫珺, 马宏瑞, 朱超, 等. 改性市政污泥对水中苯酚的吸附性能研究[J]. 化学工业与工程, 2023, 40(2): 85-93. MA Zijun, MA Hongrui, ZHU Chao, et al. Municipal sludge modification and their adsorption performance for phenol in wastewater[J]. Chemical Industry and Engineering, 2023, 40(2): 85-93. DOI:10.13353/j.issn.1004.9533.20220345 (in Chinese) |
| [4] |
YI Y, HUANG Z, LU B, et al. Magnetic biochar for environmental remediation: A review[J]. Bioresource Technology, 2020, 298: 122468. DOI:10.1016/j.biortech.2019.122468 |
| [5] |
REGUYAL F, SARMAH A K, GAO W. Synthesis of magnetic biochar from pine sawdust via oxidative hydrolysis of FeCl2 for the removal sulfamethoxazole from aqueous solution[J]. Journal of Hazardous Materials, 2017, 321: 868-878. DOI:10.1016/j.jhazmat.2016.10.006 |
| [6] |
CHIN J, HENG Z, TEOH H C, et al. Recent development of magnetic biochar crosslinked chitosan on heavy metal removal from wastewater: Modification, application and mechanism[J]. Chemosphere, 2022, 291: 133035. DOI:10.1016/j.chemosphere.2021.133035 |
| [7] |
LIANG J, CHEN Y, CAI M, et al. One-pot pyrolysis of metal-embedded biochar derived from invasive plant for efficient Cr(Ⅵ) removal[J]. Journal of Environmental Chemical Engineering, 2021, 9(4): 105714. DOI:10.1016/j.jece.2021.105714 |
| [8] |
WU Z, WANG X, YAO J, et al. Synthesis of polyethyleneimine modified CoFe2O4-loaded porous biochar for selective adsorption properties towards dyes and exploration of interaction mechanisms[J]. Separation and Purification Technology, 2021, 277: 119474. DOI:10.1016/j.seppur.2021.119474 |
| [9] |
LIMA D R, LIMA E C, THUE P S, et al. Comparison of acidic leaching using a conventional and ultrasound-assisted method for preparation of magnetic-activated biochar[J]. Journal of Environmental Chemical Engineering, 2021, 9(5): 105865. DOI:10.1016/j.jece.2021.105865 |
| [10] |
ZHANG R, ZHENG X, CHEN B, et al. Enhanced adsorption of sulfamethoxazole from aqueous solution by Fe-impregnated graphited biochar[J]. Journal of Cleaner Production, 2020, 256: 120662. DOI:10.1016/j.jclepro.2020.120662 |
| [11] |
SHEN Y, XIAO Y, ZHANG H, et al. Synthesis of magnetic biochar-supported Fe-Cu bimetallic catalyst from pulp and paper mill wastes for the Fenton-like removal of rhodamine B dye[J]. Chemical Engineering Journal, 2023, 477: 146823. DOI:10.1016/j.cej.2023.146823 |
| [12] |
LIANG S, SHI S, ZHANG H, et al. One-pot solvothermal synthesis of magnetic biochar from waste biomass: Formation mechanism and efficient adsorption of Cr(Ⅵ) in an aqueous solution[J]. The Science of the Total Environment, 2019, 695: 133886. DOI:10.1016/j.scitotenv.2019.133886 |
| [13] |
DUAN S, MA W, PAN Y, et al. Synthesis of magnetic biochar from iron sludge for the enhancement of Cr (Ⅵ) removal from solution[J]. Journal of the Taiwan Institute of Chemical Engineers, 2017, 80: 835-841. DOI:10.1016/j.jtice.2017.07.002 |
| [14] |
SHIN D, CHOI Y S, HONG B. Graphene-enhanced Raman spectroscopy reveals the controlled photoreduction of nitroaromatic compound on oxidized graphene surface[J]. ACS Omega, 2018, 3(9): 11084-11087. DOI:10.1021/acsomega.8b01285 |
| [15] |
QU J, SHI J, WANG Y, et al. Applications of functionalized magnetic biochar in environmental remediation: A review[J]. Journal of Hazardous Materials, 2022, 434: 128841. DOI:10.1016/j.jhazmat.2022.128841 |
| [16] |
CAI W, WEI J, LI Z, et al. Preparation of amino-functionalized magnetic biochar with excellent adsorption performance for Cr(Ⅵ) by a mild one-step hydrothermal method from peanut hull[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2019, 563: 102-111. |
| [17] |
SUN Y, WANG T, HAN C, et al. Facile synthesis of Fe-modified lignin-based biochar for ultra-fast adsorption of methylene blue: Selective adsorption and mechanism studies[J]. Bioresource Technology, 2022, 344: 126186. DOI:10.1016/j.biortech.2021.126186 |
| [18] |
SUN C, CHEN T, HUANG Q, et al. Enhanced adsorption for Pb(Ⅱ) and Cd(Ⅱ) of magnetic rice husk biochar by KMnO4 modification[J]. Environmental Science and Pollution Research, 2019, 26(9): 8902-8913. DOI:10.1007/s11356-019-04321-z |
| [19] |
WEN Q, CHEN Y, RAO X, et al. Preparation of magnesium Ferrite-Doped magnetic biochar using potassium ferrate and seawater mineral at low temperature for removal of cationic pollutants[J]. Bioresource Technology, 2022, 350: 126860. DOI:10.1016/j.biortech.2022.126860 |
| [20] |
HU Y, ZHU Y, ZHANG Y, et al. An efficient adsorbent: Simultaneous activated and magnetic ZnO doped biochar derived from camphor leaves for ciprofloxacin adsorption[J]. Bioresource Technology, 2019, 288: 121511. DOI:10.1016/j.biortech.2019.121511 |
| [21] |
REVELLAME E D, FORTELA D L, SHARP W, et al. Adsorption kinetic modeling using pseudo-first order and pseudo-second order rate laws: A review[J]. Cleaner Engineering and Technology, 2020, 1: 100032. DOI:10.1016/j.clet.2020.100032 |
| [22] |
AL-GHOUTI M A, DA'ANA D A. Guidelines for the use and interpretation of adsorption isotherm models: A review[J]. Journal of Hazardous Materials, 2020, 393: 122383. DOI:10.1016/j.jhazmat.2020.122383 |
| [23] |
LIMA E C, HOSSEINI-BANDEGHARAEI A, MORENO-PIRAJÁN J C, et al. A critical review of the estimation of the thermodynamic parameters on adsorption equilibria. Wrong use of equilibrium constant in the Van't Hoof equation for calculation of thermodynamic parameters of adsorption[J]. Journal of Molecular Liquids, 2019, 273: 425-434. DOI:10.1016/j.molliq.2018.10.048 |
| [24] |
RUBANGAKENE N O, ELKADY M, ELWARDANY A, et al. Effective decontamination of methylene blue from aqueous solutions using novel nano-magnetic biochar from green pea peels[J]. Environmental Research, 2023, 220: 115272. DOI:10.1016/j.envres.2023.115272 |
| [25] |
PRABAKARAN E, PILLAY K, BRINK H. Hydrothermal synthesis of magnetic-biochar nanocomposite derived from avocado peel and its performance as an adsorbent for the removal of methylene blue from wastewater[J]. Materials Today Sustainability, 2022, 18: 100123. DOI:10.1016/j.mtsust.2022.100123 |
| [26] |
ZENG H, QI W, ZHAI L, et al. Magnetic biochar synthesized with waterworks sludge and sewage sludge and its potential for methylene blue removal[J]. Journal of Environmental Chemical Engineering, 2021, 9(5): 105951. DOI:10.1016/j.jece.2021.105951 |
| [27] |
EL-SHAFIE A S, RAHMAN E, GADELHAK Y, et al. Techno-economic assessment of waste mandarin biochar as a green adsorbent for binary dye wastewater effluents of methylene blue and basic fuchsin: Lab- and large-scale investigations[J]. Spectrochimica Acta Part A, Molecular and Biomolecular Spectroscopy, 2024, 306: 123621. DOI:10.1016/j.saa.2023.123621 |
| [28] |
YAN N, HU B, ZHENG Z, et al. Twice-milled magnetic biochar: A recyclable material for efficient removal of methylene blue from wastewater[J]. Bioresource Technology, 2023, 372: 128663. DOI:10.1016/j.biortech.2023.128663 |
| [29] |
LI J, HU J, SHENG G, et al. Effect of pH, ionic strength, foreign ions and temperature on the adsorption of Cu(Ⅱ) from aqueous solution to GMZ bentonite[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2009, 349(1/2/3): 195-201. |
| [30] |
KANG K, HU Y, KHAN I, et al. Recent advances in the synthesis and application of magnetic biochar for wastewater treatment[J]. Bioresource Technology, 2023, 390: 129786. DOI:10.1016/j.biortech.2023.129786 |
| [31] |
ZHANG A, LI X, XING J, et al. Adsorption of potentially toxic elements in water by modified biochar: A review[J]. Journal of Environmental Chemical Engineering, 2020, 8(4): 104196. DOI:10.1016/j.jece.2020.104196 |
 2024, Vol. 41
2024, Vol. 41





