随着化石燃料的短缺及能源需求的增长,全球环境问题已经日益严重,使得清洁能源和可持续发展被更多人重视[1]。氢气作为可再生清洁能源,具有高能量密度、清洁环保、资源丰富等优点,可广泛应用于各个行业[2]。近年来,国家极其重视氢能的发展,地方及中央相继推出众多政策,促进氢能发展。氢气的制备方法主要为煤制氢、天然气制氢、电解水制氢等。其中,电解水制氢技术以水作为反应底物,由可再生能源(太阳能、风能等)驱动,整个过程完全绿色无污染,被研究者认为是最理想的制氢方式之一。电解水制氢分为阴极的析氢反应(Hydrogen evolution reaction,HER)和阳极的析氧反应(Oxygen evolution reaction,OER)2个半反应。其中,HER是反应速率较快的两电子过程,但OER是动力学迟缓的四电子反应过程,使得电解水制氢电耗较高,制约着电解水制氢技术的发展。
在过去的几十年里,研究人员通过设计制备高性能OER/HER电催化剂来提高电解水制氢性能。通过对催化剂形貌控制、表面修饰、缺陷工程、相变和元素掺杂等方法来增加催化剂表面暴露活性位点数量及改善活性位点本征活性,以此提高催化性能[3]。然而,目前通过催化剂的设计和改性以提高电解水制氢性能已逐渐进入瓶颈,难以取得重大进展。尽管近年来发展了利用有机物氧化反应代替OER的方法,使得电解水制氢性能有所上升,电耗有所下降,但如何进一步提升性能及降低电耗成为了目前的科研难题。
最近,在电解水反应体系中引入外场(光场、磁场、弹性应力场、重力场等)已被证明是提升电解水活性的有效策略[4]。引入外场可改善反应传质及改变反应动力学从而显著提高电解水性能。例如:利用光辅助的光热效应及局域表面等离子体共振效应(LSPR),可降低电解水制氢起始电位、提高电流密度并且改变反应路径以提高选择性。此外,磁场诱导的洛伦兹力和电子极化也能提高电子的传输效率,有利于提高电催化剂的电催化效率。因此将外场辅助策略与电解水制氢结合成为目前该领域一个新兴研究方向。本综述重点介绍了通过外场辅助强化电解水制氢反应的最新进展,包括HER、OER及电解水制氢耦合有机物氧化。最后对外场辅助电解水制氢的发展进行了总结及展望,希望能够为电解水制氢的未来发展提供一些借鉴。
1 外场辅助增强电解水制氢的原理 1.1 光辅助增强原理 1.1.1 局部表面等离子体共振效应(LSPR)LSPR效应是指当光照射到贵金属纳米颗粒表面时,表面上的自由电子集体振荡,产生表面等离子激元。当振荡频率接近入射光的频率时,会产生共振效应,使表面电子的集体振动进一步增强[5-7]。贵金属颗粒(如:铂、金和银等)等都具有此效应,一部分非贵金属也同样具有这种效应(如铋、铝和铜等)[8]。此外,LSPR的共振频率可以通过改变金属纳米结构的形状、尺寸、介电环境以及金属介电函数得到进一步增强[9]。
1.1.2 光热效应与传统的光催化和热催化不同,光辅助策略的光热效应可在微纳尺度使催化剂局部温度增加,将热量集中在催化剂的活性位点附近,从而大幅提高反应速率,并且通过避免对整个反应器系统加热以进一步降低反应能耗[10]。一般来说,光热效应有3种不同的机制:等离子体金属的局部加热、半导体的非辐射弛豫和分子的热振动(图 1)。
金属材料中的光热效应主要是由其LSPR效应产生:当共振频率波长的光照射到金属材料的表面时,金属材料中会发生电磁辐射并激发处于未被占据状态的电子引起电子振荡,进而使金属局部表面温度迅速升高。半导体的非辐射弛豫是指:在光激发下,当半导体吸收等于或大于带隙能量的光子时,会产生电子-空穴对。随后,光电子通过非辐射或辐射弛豫返回到较低的能态,能量则通过晶格振动以热的形式释放。分子的热振动是指:当光子能量与分子中的电子跃迁能相匹配时,分子的光激发使电子从最高的占据分子轨道(HOMO)跃迁到最低的未占据分子轨道(LUMO),随后光电子在基态弛豫,并通过电子-振动耦合在分子中产生热量[11-14]。
1.2 磁辅助增强原理磁场和电催化的结合被认为是一种新兴、有前景的增强电催化性能的策略。一般来说,磁场增强电催化的效应包括磁热效应、磁流体效应和微磁流体效应、麦克斯韦应力效应、开尔文力效应以及自旋选择性效应[15]。此外,磁场的各种效应可以同时存在于磁场中,从而协同强化电催化性能。
磁场增强电催化性能的可能机制如下:(1)磁热效应是由高频交变磁场(AMF)激活磁性纳米粒子(MNPs)而形成的,广泛应用于磁热疗。磁性纳米颗粒在磁场诱导下产生的热在电极上是局部化的,因此可以在不加热电解液的情况下提高局部微区温度,改善电催化动力学,从而提高电解水制氢效率[16];(2)磁流体效应和微磁流体效应分别是磁场与局部电流密度相互作用引起的宏观对流和微观对流,由洛伦兹力驱动。这2种效应对电催化系统的影响主要针对气体逸出电极[17];(3)麦克斯韦应力是指由磁场与元件中的偶极矩相互作用产生的一种力。在均匀磁场中,顺磁液滴会产生正负电荷,从而削弱顺磁液滴的磁性。然后,来自磁场的应力导致顺磁液滴的横向或纵向拉伸(磁致伸缩)[18];(4)开尔文力可从2个方面影响电化学反应:一是加速顺磁性材料的传质,从而提高反应速率;二是使扩散层变薄,从而增大电流密度[19]。此外,开尔文力还可以通过对顺磁性气体氧气的吸引实现氧富集,避免反磁性物质N2或H2O在电极表面的“堵塞”现象,从而为氧的传输提供更多的通道[20];(5)自旋选择性效应是一个新兴研究方向,指手性分子可以通过优先的自旋取向转移电子,这种现象被称为手性诱导自旋选择性效应。施加磁场可以使2个自旋态相互转换,从而改变产物选择性,且磁场还可以诱导吸附在催化剂表面的中间体发生自旋翻转,从而优化反应路径提高反应效率[15]。
1.3 其他外场除光、磁场被用于电解水制氢外,还有其他外场被应用于该反应中,例如:外加弹性应变是提高电解水反应性能的一种有效途径,当金属表面受到压缩或拉伸应变时,d带中心将发生移动,从而改变反应物和中间物种在金属表面的吸附能[21]。此外,在电解水制氢的过程中,产生的氢气和氧气会附着在催化剂表面或分散在电解液中,从而在电解槽中引起较高的欧姆电压降,降低反应性能[22]。通过高重力加速度可以增加相间滑移速度和对流速度,以实现超重力场下的气-液/气-固快速分离,降低欧姆压降和电解水制氢过电位。
2 外场辅助策略在增强电解水性能方面的进展 2.1 外场辅助增强HER 2.1.1 光辅助策略增强HER电解水制氢是一种很有前景的绿色生产氢气的方法,其在阴极发生HER产生氢气。近年来,众多研究人员在电解水的过程中引入光场,通过光辅助策略提高HER电流密度,降低反应电压,从而提高析氢效率。
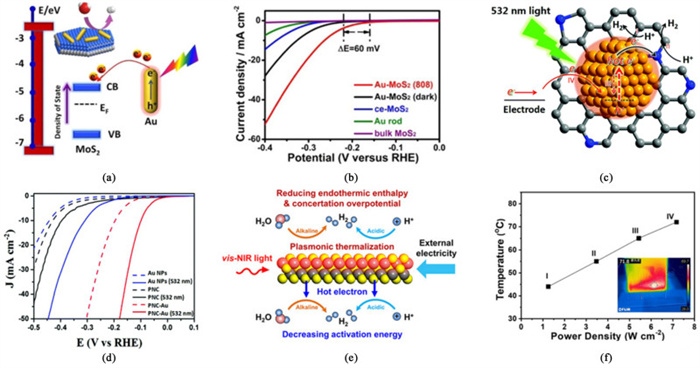
等离子体纳米材料(如Au、Ag和Pt等)有着近场增强、互补光吸收以及在结界面处能加速光生载流子分离等优点,将其引入催化剂中再通过光辅助策略可显著提升HER性能。例如,南京大学夏兴华团队[23]合成了负载金纳米棒的硫化钼纳米片催化剂(Au-MoS2),并将其用于HER反应。在波长为808 nm的激光照射下,Au-MoS2的HER性能得到了显著提升,起始电位降低至-0.16 V vs. RHE[图 2(b)]。其性能提升机理为:在激光的照射下,
|
| 图 2 (a) Au-MoS2的能级图示意图;(b) 在几种催化剂上得到的HER极化曲线[23];(c) HER在PNC-Au上的电子转移示意图;(d) 几种催化剂在0.5 mol·L-1 H2SO4电解液中得到的HER极化曲线[24];(e) LSPR诱导的光热效应和热电子效应对提高MXenes的电催化HER性能的积极贡献示意图;(f) 电极温度与NIR光功率之间的相关性。插图是Ti3C2Tx MXenes电极的典型红外图像[25] Fig.2 (a) Schematic illustration of energy level diagram of Au-MoS2; (b) HER polarization curves obtained on several catalysts as indicated[23]; (c) Schematic illustration of electron transfer for HER over PNC-Au; (d) HER polarization curves obtained from several catalysts as indicated in 0.5 mol·L-1 H2SO4 electrolyte[24]; (e) Schematic illustration of the positive contribution of the LSPR-induced photothermal and hot-electron effect to improve the electrocatalytic HER performance of MXenes; (f) Correlation between the electrode temperature and NIR light power. The inset is a typical infrared image of the Ti3C2Tx MXene electrode[25] |
| |
Au会产生热电子使MoS2中的载流子密度增加,从而提高HER性能[图 2(a)]。该工作强调了贵金属的LSPR效应如何提高HER性能,同时证明了等离子体强化电催化性能的可行性,为通过光辅助策略增强半导体材料的电催化性能提供了新思路。
此外,中国科学院大学张健团队[24]合成了多孔N掺杂炭负载Au纳米颗粒的电催化剂(PNC-Au),并通过光辅助策略(LSPR效应)使其HER的电流密度提升4倍以上,在电流密度为10 mA·cm-2时,过电位显著降低至99 mV[图 2(d)]。HER的性能增强原因为:在光激发下,等离子体Au纳米粒子会发生LSPR效应从而产生热电子,而PNC可高效转移电荷,从而加速热电子的转移[图 2(c)]。另外,PNC和Au纳米颗粒之间的协同作用促进了Au等离子体驱动的电荷分离和转移,从而强化了HER性能。该工作为通过光辅助策略设计更高效率的电解水制氢系统提供了新的途径。
北京化工大学邱介山团队[25]证明了,MXenes可以通过LSPR在可见光-近红外区域诱导的光热效应和热电子效应降低HER的势垒,从而增强HER活性。基于此他们制备了Ti3C2Tx MXenes电催化剂,并表现出最高的光热效率和最好的HER活性[图 2(e)]。通过系列实验证明了性能提升机理为:光热效应可以降低HER的吸热焓和过电势,而热电子效应可以降低HER的活化能同时提高法拉第效率(FE)。
山西师范大学许小红课题组[26]制备了具有丰富界面的垂直排列的WS2/N-WC和MoS2/N-MoC异质结构纳米片,在酸性溶液中用于高效的光辅助析氢电催化剂。这些独特的异质结构可以为HER提供丰富的界面和活性部位。在酸性溶液中,WS2/N-WC和MoS2/N-MoC异质结构电催化剂在10 mA·cm-2处的过电位分别为0.120和0.122 V,表现出优异的光辅助电催化活性。这种高HER活性是由不同相界丰富的活性中心的电催化协同作用和对紫外可见光的吸收产生的。这种界面工程可能是提高二维材料导电性的一般方法,可以扩展到更多的材料,并在HER以外的其他反应中得到应用。
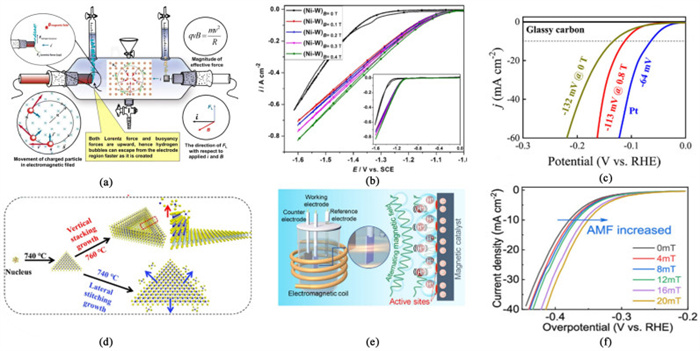
2.1.2 磁辅助策略增强HER近年来研究人员发现,引入外磁场是提高电催化剂HER性能的可行策略。例如,Hegde团队[27]采用电沉积技术合成了具有特定成分的电活性Ni-W合金催化剂,并将其用于HER反应[图 3(a)]。在外加磁场下,Ni-W合金的HER起始电位发生了明显下降[图 3(b)]。机理研究表明:施加磁辅助后,磁流体效应使得来源于气泡阻力的欧姆降降低,从而提高了HER活性。北京科技大学王守国团队[28]成功合成了铁磁性的碗状MoS2催化剂,并将其用于HER反应。当恒定外电压为-150 mV时,磁辅助的HER电流密度是没有磁场的2倍[图 3(c)]。机理研究表明:在外加垂直磁场的作用下,铁磁性的MoS2催化剂可以加速电子从玻碳电极到活性中心的转移,从而提高HER性能[图 3(d)]。这种磁辅助强化HER方法不仅适用于MoS2,也适用于其他铁磁性二维材料。而华东理工大学马巍课题组[29]用简单的低温介导液相剥离和梯度离心法制备了单层、双层、3层和多层MoS2薄片。在中等磁场和不加磁场的情况下,测试单片MoS2的HER催化性能。结果表明,与双层、3层和多层MoS2薄膜相比,单层MoS2薄膜表现出最高的HER性能和最大的磁增强(~300%)。作者研究发现,通过减少MoS2片层的层数,大量暴露的边缘位置和硫空位会加速HER的反应动力学,同时提高了铁磁性。中国科学院大学霍军涛团队[30]制备了Fe-Co-Ni-P-B催化剂,并研究交变磁场对HER性能的影响。结果表明,施加交变磁场可以显著提高其HER的催化效率,在20 mT的磁场中,电流密度提高了27%[图 3(e)和图 3 (f)]。系列实验表明,电荷与交变磁场之间的洛伦兹相互作用对提高电荷转移效率起到了关键作用,其作用远强于加热的效果。该工作为磁辅助策略为提高非贵金属Ni、Co、Fe及其化合物等磁性催化剂的HER活性提供了一定的借鉴作用。
|
| 图 3 (a) 镍钨合金涂层上磁场诱导HER的实验装置原理图;(b)特定成分的Ni-W合金的CV响应显示出HER效率的提高[27];(c)在外加垂直磁场和不外加垂直磁场的情况下,单片碗状MoS2的极化曲线;(d)二硫化钼薄片的横向拼接和垂直堆积生长示意图[28];(e)磁辅助电催化HER示意图;(f) 不同强度AMFs下的LSV曲线[30] Fig.3 (a) The schematic of the experimental setup used for magnetic field-induced HER on Ni-W alloy coating; (b) CV responses of the Ni-W alloy of a specific composition showing improvement in HER efficiency[27]; (c) Polarization curves of individual bowl-like MoS2 flakes with and without an external vertical magnetic field and Pt; (d) The schematic illustration of lateral stitching and vertical stacking growth of MoS2 flakes[28]; (e) Schematic diagram of magnetically assisted electrocatalysis of HER; (f) LSV curves under AMFs of different intensities[30] |
| |
外加弹性应变是提高电解水反应性能的一种有效途径。北京大学郭少军团队[31]提出了一种通过控制MoS2壳层数来精确调节Co9S8/MoS2核/壳纳米晶体表面张力以提高HER活性的策略。调节优化后,其HER在10 mA·cm-2时过电位仅为97 mV,Tafel斜率为71 mV·dec-1。机理研究表明:Co9S8/1L MoS2核/壳纳米晶体的3.5%的大拉伸表面应变可以优化带隙使其更接近费米能级,从而有利于氢的吸附和快速扩散过程。该工作首次证明了拉伸应变可改善纳米材料的电催化性能。此外,中国科学院王明涌团队[32]利用超重力场强化了HER性能。机理研究表明:在超重力场条件下,形成气泡核的临界半径比正常重力条件下小很多,而浮力大很多。超重力场使氢气泡更容易形成并可以迅速脱离电极表面,使电极表面的气体覆盖率显著降低,从而可保留更多的活性位点,进而提高HER性能。且在较高电流密度下,超重力场对HER的增强作用更加明显。该工作表明,应用超重力场有望大幅度降低电解水制氢、氯碱电解及生产重水的能耗。
外场对HER反应性能的增强总结于表 1。
| 催化剂 | 反应性能 | 外场辅助 |
| Au-MoS2[23] | -160 mV(vs. RHE, 起始电位) | 光辅助 |
| PNC-Au[24] | 99 mV(η, 10 mA·cm-2) | 光辅助 |
| Ti3C2Tx MXenes[25] | 128 mV(η, 起始电位) | 光辅助 |
| WS2/N-WC MoS2/N-MoC[26] | 120 mV(η, 起始电位) 122 mV(η, 起始电位) | 光辅助 |
| Ni-W合金[27] | -1 010 mV(vs. RHE, 起始电位) | 磁辅助 |
| 碗状MoS2[28] | -113 mV(vs. RHE, 10 mA·cm-2) | 磁辅助 |
| 单层MoS2[29] | -310 mV(η, -10 mA·cm-2) | 磁辅助 |
| Fe-Co-Ni-P-B[30] | -350 mV(η, -10 mA·cm-2) | 磁辅助 |
| Co9S8/MoS2[31] | 97 mV(η, 10 mA·cm-2) | 弹性应变 |
电解水制氢在阳极发生OER产生氧气,然而该过程为四电子转移过程,动力学缓慢,过电位高。近年来,研究人员发现通过光辅助策略可有效增强等离子体纳米材料的OER反应动力学,降低过电位。
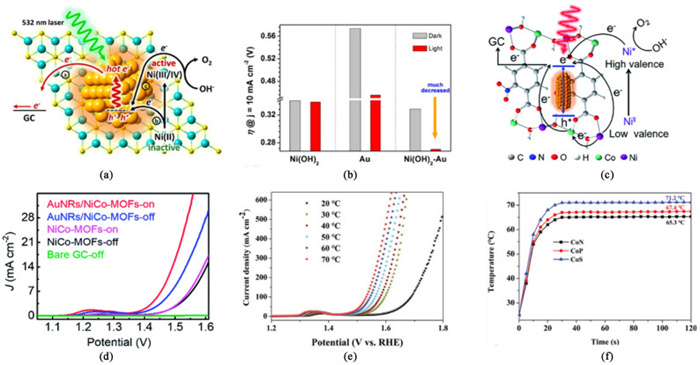
河北大学叶金花团队[33]首次通过光辅助策略强化OER性能。他们制备了Au纳米颗粒修饰的Ni(OH)2纳米片电催化剂Ni(OH)2-Au。在光照的条件下,该催化剂的OER电流密度提升了4倍以上,且在10 mA·cm-2的电流密度下,反应过电位从330降低至270 mV,Tafel斜率降低至35 mV·dec-1[图 4(b)]。机理研究表明:在光照的条件下,Au纳米颗粒的热电子效应促进了NiⅢ/Ⅳ活性物质的生成并提高了电荷转移,从而显著提高了OER活性[图 4(a)]。此外,他们还在CoO-Au和FeOOH-Au催化剂上也观察到了LSPR增强的OER催化作用,表明该策略具有普遍性。这些结果表明,通过LSPR效应强化OER性能的可能性,为设计更节能的电解水制氢系统开辟了新的途径。
|
| 图 4 (a) 在532 nm激光照射下,Ni(OH)2-Au电极中可能发生的电子转移路径示意图;(b)Ni(OH)2-Au杂化催化剂与对照样品在光照和不光照条件下10 mA·cm-2电流密度所需过电位(η)的比较[33];(c)在808 nm光照射下,AuNRs和NiCo-MOFs之间的电子转移路径示意图;(d)不同催化剂修饰电极在1.0 mol·L-1 KOH电解液中808 nm光照下的LSV曲线[34];(e) 在1 mol·L-1 KOH溶液中,不同电解质温度下Co3O4电极的LSV曲线;(f)CoN、CoP和CoS电极的温度-时间图[36] Fig.4 (a) Schematic electron transfer paths likely to occur in the Ni(OH)2-Au electrode under 532 nm laser irradiation responsible for the OER catalysis; (b) Comparison of overpotentials (η) required for a 10 mA·cm-2 current density over Ni(OH)2-Au hybrid catalysts and control samples with and without light irradiation[33]; (c) Schematic electron transfer paths occurring between AuNRs and NiCo-MOFs under 808 nm light irradiation; (d) LSV curves of the electrodes modified with different catalysts in 1.0 mol·L-1 KOH electrolyte with 808 nm light on or off as indicated[34]; (e) LSV polarization curves of Co3O4 electrode under various electrolyte temperatures in 1 mol·L-1 KOH solution; (f) Temperature-time plots of CoN, CoP, and CoS electrodes[36] |
| |
南京大学夏兴华团队[34]制备了Au纳米棒-2D超薄金属-有机框架(NiCo-MOF)复合电催化剂(AuNRs/NiCo-MOFs),该催化剂在光辅助策略下,表现出优异的OER电催化性能,电流密度为10 mA·cm-2时,过电位降低至240 mV,Tafel斜率降低至69 mV·dec-1[图 4(d)]。机理研究表明:在LSPR激发下,Au纳米粒子产生的热空穴在合适的偏压下会被注入到催化剂的Ni活性中心,从而显著地增加NiCo-MOF中高价Ni*活性位点的生成。此外,由局域表面等离子体共振产生的热电子则会转移到外电路中形成电流,这使得OER过程中能级更好匹配,从而降低反应过电位。通过这2种机制的协同作用,降低了OER的活化能,从而提高了OER活性[图 4(c)]。该工作凸显了贵金属等离子体的LSPR效应在促进MOF材料的OER性能方面的重要性,为提高MOF材料的固有电催化活性开辟了一条新途径。此外,复旦大学陈彧团队[35]合成的Au-MnO2催化剂也有类似的光辅助增强OER活性机制。
此外,通过光热效应提高反应温度也是一种提高OER性能的有效方法。中国地质大学刘学琴团队[36]证明了Co3O4电催化剂通过光热效应显著增强了OER性能[图 4(e)]。由于Co3O4是一种典型的p型半导体,其价带内空穴密度较高,因此,在近红外光照射下,空穴的集体震荡会产生光热效应。光热效应引起的电极温度升高使得电子传输速度加快,有利于加快反应动力学和气泡释放。其他类似的Co基催化剂(如CoN、CoP和CoS)也因光热效应而表现出增强的OER性能[图 4(f)]。该工作为通过光热效应强化OER性能开辟了一种新的优化方法。
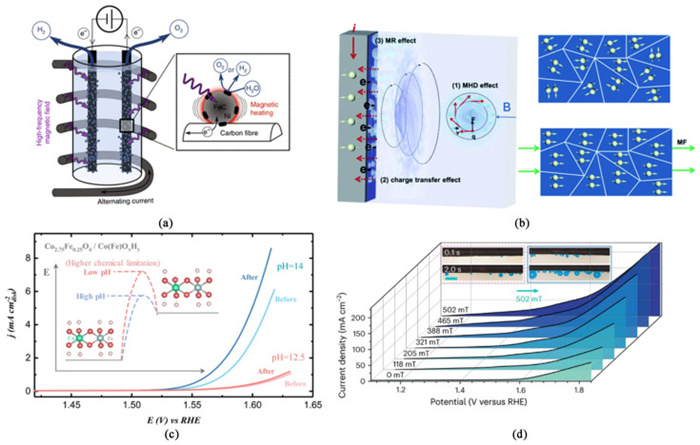
2.2.2 磁辅助策略增强OER在过去的几年中,磁辅助策略已经成功地应用于OER中,以降低反应过电位和增加反应动力学,这证明了磁辅助增强OER策略的可行性。例如,Chatenet团队[37]首次将磁辅助策略应用于提高OER性能,并且证明了通过使用非贵金属催化剂的磁热效应可以改善与电解水有关的电催化反应[图 5(a)]。在高频交变磁场的作用下,FeC-Ni纳米颗粒催化剂会产生磁热效应加热局部活性位点,从而降低OER和HER的过电位。在20 mA·cm-2的电流密度下,OER和HER的过电位分别降低了200和100 mV。这种动力学增强相当于电解槽温度上升约200 ℃,但实际上只提高了5 ℃。所以作者认为该性能提升不仅是因为磁热效应,还有其他不确定的机制需要探索。哈尔滨工业大学徐平团队[38]研究了外加磁场对镍基催化剂[Ni(OH)2、NiO和Ni]OER性能的影响[图 5(b)]。结果表明,在1.4 T的外加磁场下,Ni在10 mA·cm-2的OER过电位可降低20 mV。机理研究表明:在外加磁场下,自旋电子散射引起的磁阻效应是影响表观电催化活性(以过电位表示)的主要因素。该工作对全面理解磁辅助增强OER性能有着重要参考意义,有助于合理设计高效“磁效应”催化剂。最近,南洋理工大学的徐梽川团队[39]通过电化学重构建立了稳定的顺磁性羟基氧化物层/铁磁层界面,并利用界面处的自旋钉扎效应改变表面羟基氧化物(厚度约为4 nm)的磁结构,从而极大地提高了催化剂的本征活性[图 5(c)]。机理研究表明:在磁场中,铁磁畴与顺磁(羟基)氢氧化物层界面处存在自旋钉扎效应,从而使催化剂在OER过程中发生可控的表面重构,即通过磁场使自旋电子排列得更整齐,从而提高OER活性。该工作为利用自旋钉扎效应设计高性能OER催化剂提供了新的思路。新加坡国立大学吕炯课题组[40]合成一系列单原子自旋催化剂(SASCs),该催化剂由嵌入在MoS2主体中的替位磁性原子组成。其中Ni1/MoS2采用了扭曲的四方结构,促使其与附近的S原子以及邻近的Ni1位发生铁磁耦合,从而产生了全局室温铁磁性这种耦合有利于OER反应中的自旋选择性电荷转移,从而产生三重态O2。此外,在~0.5 T的弱磁场下,OER反应的磁电流比Ni1/MoS2提高2 880%[图 5(d)],在海水和纯水裂解池中都具有良好的活性和稳定性。动态现场原位表征和理论计算结果表明,OER性能的增强,是因为磁场调节S(p)-Ni(d)杂化引起的场诱导的自旋排列和S活性中心上的自旋密度优化,从而优化了自由基中间体的吸附能,从而降低了整个反应势垒。
|
| 图 5 (a) 在产生AMF的线圈内运行的AWE电池的一般表示,理想情况下,电池由可再生电力供电[37];(b)铁磁材料的磁矩变化示意图:在没有外磁场(MF)的情况下,各畴的磁矩都是随机定向的,当施加适当的磁场时,所有的磁矩都与磁场对齐[38];(c)重建的Co2.75Fe0.25O4在0.5 T磁场下,在pH值为12.5和14下磁化15 min前后的LSV。插图是不同pH值下脱氢在Co位上生成负氧的示意图[39];(d)Ni1/MoS2在不同磁场下的线性扫描伏安曲线。插图显示了Ni1/MoS2作为OER催化剂在1.65 V无磁场(左)和有磁场(右)的裂水室中的照片[40] Fig.5 (a) General representation of the AWE cell operating inside the coil that generates the AMF, the cell being, ideally, powered with renewable electricity[37]; (b) Schematic illustration of the magnetic moment change of ferromagnetic materials: the magnetic moment of every domain is randomly oriented in the absence of an external magnetic field (MF), and when a proper magnetic field is applied, all magnetic moments align with the field[38]; (c) The LSV of the reconstructed Co2.75Fe0.25O4 before and after magnetization in magnetic field of 0.5 T for 15 min under pH of 12.5 and 14. The inset is a schematic illustration of dehydrogenation under different pH for generating negatively charged oxygen on Co site[39]; (d) Linear scan voltammetry curves of Ni1/MoS2 under different magnetic fields.Inset shows photo images of Ni1/MoS2 as OER catalysts in water splitting cells at 1.65 V without (left) and with (right) magnetic fields[40] |
| |
外场对OER反应性能的增强总结于表 2。
近年来,研究人员发现,通过将有机物氧化反应来代替OER过程,可以降低电解水过电位、降低反应能耗、提高产氢效率,同时在阳极得到高附加值产物。另外,近期研究证明通过光辅助策略可进一步提高电解水制氢耦合有机物氧化反应活性,但该领域目前仍处于初期阶段,相关报道较少。
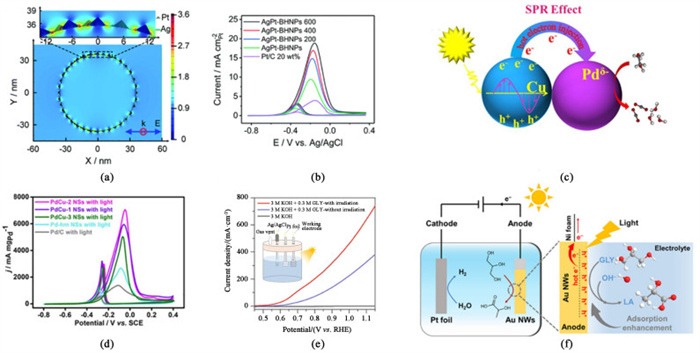
西安交通大学杨生春团队[41]合成了具有超薄壳层的银铂双金属中空纳米粒子(AgPt-BHNPs)。且通过光辅助策略可显著提高其甲醇氧化反应活性。机理研究表明,在光照的条件下,LSPR诱导的光热效应导致了催化剂局部温度的升高,从而显著地加速了甲醇氧化过程[图 6(b)]。此外,由于Ag物种的等离子体激元效应引起的表面电荷不均匀,导致AgPt-BHNPs中Pt的d带中心偏移,从而抑制了甲醇氧化过程中CO的吸附,提高了AgPt-BHNPs的抗CO中毒性能[图 6(a)]。该工作揭示了等离子体增强甲醇氧化的本质,并为利用光辅助策略提高电解水制氢耦合有机物氧化反应活性开辟了道路。
|
| 图 6 (a) 在LSPR激发波长为500 nm时的局部电场增强(|E|/|E0|)轮廓;(b)AgPt-BHNPs和商业Pt/C催化剂的电催化性能。[41];(c)SPR促进了EGOR的作用机制;(d) 3种催化剂以及Pd-hm NSs和商品Pd/C在1 mol·L-1 KOH+ 1 mol·L-1乙二醇光照条件下的CV曲线[42];(e)在3 mol·L-1 KOH中,以10 mV·s-1的扫描速率,Au NWs的LSV曲线。插图:用于甘油氧化的石英电池和三电极系统的示意图;(f)光辅助电催化耦合甘油氧化示意图[43] Fig.6 (a) local electric field enhancement (|E|/|E0|) contours at an LSPR excitation wavelength of 500 nm; (b) Electrocatalytic performance of the AgPt-BHNPs and commercial Pt/C catalysts[41]; (c) SPR promoted mechanism of EGOR; (d) CV curves of three catalysts as well as Pd-hm NSs and commercial Pd/C in 1 mol·L-1 KOH+ 1 mol·L-1 EG in the condition with light[42]; (e) LSV curves of Au NWs at a scan rate of 10 mV·s-1 in 3 mol·L-1 KOH with or without 0.3 mol·L-1 GLY and with or without light irradiation. Inset: schematic illustration of the quartz cell and three-electrode system used for GLY oxidation; (f) Schematic diagram of photoassisted electrocatalysis coupled glycerol oxidation[43] |
| |
苏州大学杜玉扣团队[42]通过简单的共还原策略,成功合成了PdCu-2 NSs催化剂。在光照的条件下,该催化剂表现出显著提高的乙二醇氧化质量活性(7 547 mA·mg-1)和电流密度(14.3 mA·cm-2),且具有最优的稳定性[图 6(d)]。机理研究表明,乙二醇氧化性能提升的机理为:由于Cu的LSPR效应促进了电子从Cu向Pd的转移,从而改变了Pd的电子结构,进而增强了Pd的电催化能力[图 6(c)]。该工作揭示了等离子体Cu辅助Pd电催化乙二醇氧化的反应机理,为开发新型高效的液体燃料电池提供了新思路。
本课题组[43]合成了一种泡沫镍负载Au纳米线(Au NWs)的电催化剂,并将其应用到甘油电催化氧化制乳酸中。通过光辅助策略,Au NWs的甘油氧化电流密度高达387 mA·cm-2(0.95 V vs. RHE),相较于黑暗条件提高了2.2倍,且乳酸选择性高达80%[图 6(e)]。通过系列研究表明,光辅助在提高甘油电氧化性能方面起着双重作用:光辅助可以通过光热效应提高电解质的温度,从而提高电流密度;同时LSPR效应可以促进甘油仲羟基在Au表面的吸附,从而提高乳酸选择性[图 6(f)]。该工作为光辅助策略用于大电流密度下电解水制氢耦合甘油氧化开辟了一个新的路径。
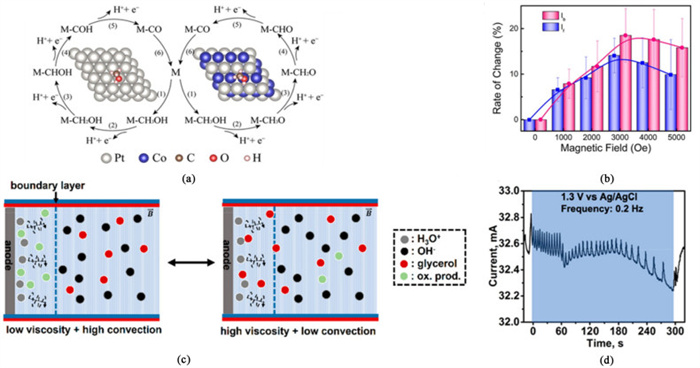
2.3.2 磁辅助策略增强电解水制氢耦合有机物氧化在过去的几年里,通过外场辅助策略提高电催化有机物氧化性能已成为一个新的研究热点方向,然而,有关磁辅助提高有机物电催化氧化性能的相关报道仍然较少。北京科技大学王守国团队[44]制备了Co42Pt58 TONPs催化剂用于电催化甲醇氧化(MOR)。性能测试结果表明,在外加3 000 Oe(1 Oe=80 A·m-1)的磁场下,Co42Pt58 TONPs的甲醇氧化性能提升最明显,甲醇氧化速相较于无磁条件提升了14.1%[图 7(b)]。机理研究表明:磁场可以抑制电子自旋的熵并且通过强量子自旋交换相互作用降低甲醇和水的活化势垒,促进Pt上COad的和Co上OHad的产生,从而加速CO2的生成并降低CO对Pt的毒害[图 7(a)]。哈佛大学Whitesides团队[45]论证了在甘油电催化氧化过程中施加静磁场可以通过洛伦兹力增加传质,并对静态磁场下甘油氧化过程产生振荡行为[图 7(d)]。该振荡行为由2个步骤耦合:一是甘油的氧化降低了阳极附近甘油的局部浓度;二是在低局部浓度的条件下,磁场的存在又增加了甘油传质速率,从而增加了阳极附近甘油的局部浓度[图 7(c)]。这种振荡行为使甘油酸的选择性提高了2.1倍。该工作为磁辅助甘油氧化开辟了道路,并对提高产物选择性提供了新思路。
|
| 图 7 (a) MOR在Pt和CoPt板上的首选反应途径;(b) 不同磁场条件下与无磁场条件下If和Ib的变化率[44];(c)利用磁场产生电化学振荡的示意图;(d)在交叉电位附近施加磁场产生的振荡行为[45] Fig.7 (a) Preferred reaction pathways of MOR on Pt and CoPt slabs; (b) The rates of change for If and Ib peaks at various magnetic fields compared with the occasion without magnetic fields[44]; (c) Schematic depiction of how this work uses magnetic fields to generate electrochemical oscillations; (d) that application of a magnetic field near the crossover potential could generate oscillatory behavior[45] |
| |
其它场辅助策略用于促进电解水制氢耦合有机物氧化仍处于初期开发阶段,目前文献报道较少。苏州大学黄小青团队[46]利用应变效应和配体效应合成了一系列具有富PtNi外壳和Pd核的三金属PtNiPd纳米线。在形态生长过程中,形成的超薄PtNi纳米线作为种子,然后沉积Pd,从而还原Pt和Ni使其向外扩散形成PtNi壳层。在电催化乙二醇氧化反应(EGOR)和甘油氧化反应(GOR)方面,PtNi0.56Pd1.42纳米线表现出最高的活性和稳定性,EGOR的比活性和质量活性分别为0.97 mA·cm-2和0.54 A·mg-1, 为该系列催化剂的2倍以上;GOR比活性和质量活性分别为0.44 mA·cm-2和0.24 A·mg-1,是商业Pt/C催化剂催化GOR的2.75倍。该工作为应变效应提高电解水制氢耦合有机物氧化性能开辟了道路。
3 结论和展望在设计高效电催化剂提高电解水制氢性能逐渐进入瓶颈期后,通过外场辅助提高电解水制氢反应性能是一种十分有前景的新兴策略。如,光辅助策略可通过LSPR效应及光热效应降低反应过电位,加快反应速率,并可提高电解水制氢耦合有机物氧化的产物选择性。磁辅助策略则是通过磁热效应、磁流体效应和微磁流体效应、麦克斯韦应力效应、开尔文力效应以及自旋选择性效应提高电解水制氢反应性能。本综述重点介绍了通过外场辅助增强电解水制氢反应的最新进展,包括HER、OER、电解水制氢耦合有机物氧化。
虽然目前电解水制氢已有较多报道,但外场辅助电解水制氢领域仍处于起步阶段,仍有大量工作需研究人员进行更加详细的探索。具体如下:(1)理论上单一外场会产生多种效应,但是目前报道的有关多种效应的协同作用的机理仍然比较模糊,因此需要研究者进行更加深入的探索,从而才能更好地利用外场辅助来提高电解水制氢性能;(2)目前应用单一场地报道较多,但如果将光场、磁场等相结合,利用2种或多种场的多种不同效应协同提升电解水制氢的性能可能会是一个有效的策略;(3)目前关于适合外场的催化剂的报道也不是很多,因此需要合理设计外场响应电催化剂,以最大限度的提高对外场的响应;(4)需要深入了解外场增强电解水制氢的机理,从而更好地设计和优化反应体系。相信随着研究的不断深入,未来会有越来越多的外场辅助电解水制氢研究,外场辅助电解水制氢的机理也会有更深层次的研究和诠释。
| [1] |
ALI Z S O, LARACHI F, ABATZOGLOU N, et al. Hydrogen production by glycerol steam reforming catalyzed by Ni-promoted Fe/Mg-bearing metallurgical wastes[J]. Applied Catalysis B: Environmental, 2017, 219: 183-193. DOI:10.1016/j.apcatb.2017.07.039 |
| [2] |
YAN Y, XIA B, XU Z, et al. Recent development of molybdenum sulfides as advanced electrocatalysts for hydrogen evolution reaction[J]. ACS Catalysis, 2014, 4(6): 1693-1705. DOI:10.1021/cs500070x |
| [3] |
JIAO Y, ZHENG Y, JARONIEC M, et al. Design of electrocatalysts for oxygen- and hydrogen-involving energy conversion reactions[J]. Chemical Society Reviews, 2015, 44(8): 2060-2086. DOI:10.1039/C4CS00470A |
| [4] |
YAO J, HUANG W, FANG W, et al. Promoting electrocatalytic hydrogen evolution reaction and oxygen evolution reaction by fields: Effects of electric field, magnetic field, strain, and light[J]. Small Methods, 2020, 4(10): 2000494. DOI:10.1002/smtd.202000494 |
| [5] |
VALENTI M, JONSSON M P, BISKOS G, et al. Plasmonic nanoparticle-semiconductor composites for efficient solar water splitting[J]. Journal of Materials Chemistry A, 2016, 4(46): 17891-17912. DOI:10.1039/C6TA06405A |
| [6] |
YAO G, LIU Q, ZHAO Z. Studied localized surface plasmon resonance effects of Au nanoparticles on TiO2 by FDTD simulations[J]. Catalysts, 2018, 8(6): 236. DOI:10.3390/catal8060236 |
| [7] |
LI Y, WEI J, SUN Z, et al. Greatly enhanced photocurrent density in bismuth ferrite films by Localized Surface Plasmon Resonance effect[J]. Applied Surface Science, 2022, 583: 152571. DOI:10.1016/j.apsusc.2022.152571 |
| [8] |
王海召, 陈雪冰, 张静, 等. 具有LSPR效应非贵金属的研究进展[J]. 当代化工研究, 2022(24): 22-24. WANG Haizhao, CHEN Xuebing, ZHANG Jing, et al. Research progress of non-precious metals with LSPR effect[J]. Modern Chemical Research, 2022(24): 22-24. (in Chinese) |
| [9] |
宋艳东. 基于Au、Ag三明治结构的表面等离子共振增强MoS2光电性能的研究[D]. 辽宁阜新: 辽宁工程技术大学, 2022 SONG Yandong. Enhanced photodetector performance of MoS2 via surface plasmon resonance coupling of Au and Ag nanoparticles with sandwich structure[D]. Liaoning Fuxin: Liaoning Technical University, 2022 (in Chinese) |
| [10] |
孟祥钰, 詹琦, 武亚南, 等. 光热效应增强的Au/RGO/Na2Ti3O7光催化加氢性能[J]. 高等学校化学学报, 2022, 43(3): 136-147. MENG Xiangyu, ZHAN Qi, WU Yanan, et al. Photothermal enhanced photocatalytic hydrogenation performance of Au/RGO/Na2Ti3O7[J]. Chemical Journal of Chinese Universities, 2022, 43(3): 136-147. (in Chinese) |
| [11] |
张小燕. 光热效应增强的钴基氧化物/N-rGO双功能氧电极催化剂的设计、制备及其性能研究[D]. 浙江温州: 温州大学, 2021 ZHANG Xiaoyan. Design, preparation of cobalt-based oxide coupled with N-rGO bifunctional materials and their photothermal-enhanced electrocatalytic performance[D]. Zhejiang Wenzhou: Wenzhou University, 2021 (in Chinese) |
| [12] |
IRSHAD M S, ARSHAD N, WANG X B. Nanoenabled photothermal materials for clean water production[J]. Global Challenges, 2021, 5(1): 2000055. DOI:10.1002/gch2.202000055 |
| [13] |
RINGE E, LANGILLE M R, SOHN K, et al. Plasmon length: A universal parameter to describe size effects in gold nanoparticles[J]. The Journal of Physical Chemistry Letters, 2012, 3(11): 1479-1483. DOI:10.1021/jz300426p |
| [14] |
IRSHAD M S, ABBAS A, QAZI H H, et al. Role of point defects in hybrid phase TiO2 for resistive random-access memory (RRAM)[J]. Materials Research Express, 2019, 6(7): 076311. DOI:10.1088/2053-1591/ab17b5 |
| [15] |
ZHANG Y, LIANG C, WU J, et al. Recent advances in magnetic field-enhanced electrocatalysis[J]. ACS Applied Energy Materials, 2020, 3(11): 10303-10316. DOI:10.1021/acsaem.0c02104 |
| [16] |
SEO B, JOO S H. A magnetic boost[J]. Nature Energy, 2018, 3(6): 451-452. DOI:10.1038/s41560-018-0157-5 |
| [17] |
LIN M, HOURNG L W, HSU J S. The effects of magnetic field on the hydrogen production by multielectrode water electrolysis[J]. Energy Sources, Part A: Recovery, Utilization, and Environmental Effects, 2017, 39(3): 352-357. DOI:10.1080/15567036.2016.1217289 |
| [18] |
DODOO J, STOKES A A. Field-induced shaping of sessile paramagnetic drops[J]. Physics of Fluids, 2020, 32(6). |
| [19] |
SHI J, XU H, LU L, et al. Study of magnetic field to promote oxygen transfer and its application in zinc-air fuel cells[J]. Electrochimica Acta, 2013, 90: 44-52. DOI:10.1016/j.electacta.2012.11.088 |
| [20] |
MATSUSHIMA H, ⅡDA T, FUKUNAKA Y, et al. PEMFC performance in a magnetic field[J]. Fuel Cells, 2008, 8(1): 33-36. DOI:10.1002/fuce.200700050 |
| [21] |
SETHURAMAN V A, VAIRAVAPANDIAN D, LAFOURESSE M C, et al. Role of elastic strain on electrocatalysis of oxygen reduction reaction on Pt[J]. The Journal of Physical Chemistry C, 2015, 119(33): 19042-19052. DOI:10.1021/acs.jpcc.5b06096 |
| [22] |
BALZER R J, VOGT H. Effect of electrolyte flow on the bubble coverage of vertical gas-evolving electrodes[J]. Journal of the Electrochemical Society, 2003, 150(1): E11. DOI:10.1149/1.1524185 |
| [23] |
SHI Y, WANG J, WANG C, et al. Hot electron of Au nanorods activates the electrocatalysis of hydrogen evolution on MoS2 nanosheets[J]. Journal of the American Chemical Society, 2015, 137(23): 7365-7370. DOI:10.1021/jacs.5b01732 |
| [24] |
ZHANG H, LI Y, LI M, et al. Boosting electrocatalytic hydrogen evolution by plasmon-driven hot-electron excitation[J]. Nanoscale, 2018, 10(5): 2236-2241. DOI:10.1039/C7NR08474A |
| [25] |
WU X, WANG J, WANG Z, et al. Boosting the electrocatalysis of MXenes by plasmon-induced thermalization and hot-electron injection[J]. Angewandte Chemie International Edition, 2021, 60(17): 9416-9420. DOI:10.1002/anie.202016181 |
| [26] |
WANG L, YANG R, FU J, et al. Vertically aligned W(Mo)S2/N-W(Mo)C-based light-assisted electrocatalysis for hydrogen evolution in acidic solutions[J]. Rare Metals, 2023, 42(5): 1535-1544. DOI:10.1007/s12598-022-02250-4 |
| [27] |
ELIAS L, CHITHARANJAN H A. Effect of magnetic field on HER of water electrolysis on Ni-W alloy[J]. Electrocatalysis, 2017, 8(4): 375-382. DOI:10.1007/s12678-017-0382-x |
| [28] |
ZHOU W, CHEN M, GUO M, et al. Magnetic enhancement for hydrogen evolution reaction on ferromagnetic MoS2 catalyst[J]. Nano Letters, 2020, 20(4): 2923-2930. DOI:10.1021/acs.nanolett.0c00845 |
| [29] |
SUN Z, ZHAO S, GU Z, et al. Understanding correlation between magnetism and electrocatalytic hydrogen evolution based on intrinsic properties of single MoS2 entity[J]. The Journal of Physical Chemistry Letters, 2023, 14(30): 6765-6771. DOI:10.1021/acs.jpclett.3c01165 |
| [30] |
CAI L, HUO J, ZOU P, et al. Key role of Lorentz excitation in the electromagnetic-enhanced hydrogen evolution reaction[J]. ACS Applied Materials & Interfaces, 2022, 14(13): 15243-15249. |
| [31] |
ZHU H, GAO G, DU M, et al. Atomic-scale core/shell structure engineering induces precise tensile strain to boost hydrogen evolution catalysis[J]. Advanced Materials, 2018, 30(26): 1707301. DOI:10.1002/adma.201707301 |
| [32] |
WANG M, WANG Z, GUO Z. Understanding of the intensified effect of super gravity on hydrogen evolution reaction[J]. International Journal of Hydrogen Energy, 2009, 34(13): 5311-5317. DOI:10.1016/j.ijhydene.2009.05.043 |
| [33] |
LIU G, LI P, ZHAO G, et al. Promoting active species generation by plasmon-induced hot-electron excitation for efficient electrocatalytic oxygen evolution[J]. Journal of the American Chemical Society, 2016, 138(29): 9128-9136. DOI:10.1021/jacs.6b05190 |
| [34] |
HU W, SHI Y, ZHOU Y, et al. Plasmonic hot charge carriers activated Ni centres of metal-organic frameworks for the oxygen evolution reaction[J]. Journal of Materials Chemistry A, 2019, 7(17): 10601-10609. DOI:10.1039/C9TA00847K |
| [35] |
XU J, GU P, BIRCH D J S, et al. Plasmon-promoted electrochemical oxygen evolution catalysis from gold decorated MnO2 nanosheets under green light[J]. Advanced Functional Materials, 2018, 28(31): 1801573. DOI:10.1002/adfm.201801573 |
| [36] |
JIN B, LI Y, WANG J, et al. Promoting oxygen evolution reaction of co-based catalysts (Co3O4, CoS, CoP, and CoN) through photothermal effect[J]. Small, 2019, 15(44): 1903847. DOI:10.1002/smll.201903847 |
| [37] |
NIETHER C, FAURE S, BORDET A, et al. Improved water electrolysis using magnetic heating of FeC-Ni core-shell nanoparticles[J]. Nature Energy, 2018, 3(6): 476-483. DOI:10.1038/s41560-018-0132-1 |
| [38] |
ZHANG Y, GUO P, LI S, et al. Magnetic field assisted electrocatalytic oxygen evolution reaction of nickel-based materials[J]. Journal of Materials Chemistry A, 2022, 10(4): 1760-1767. DOI:10.1039/D1TA09444K |
| [39] |
WU T, REN X, SUN Y, et al. Spin pinning effect to reconstructed oxyhydroxide layer on ferromagnetic oxides for enhanced water oxidation[J]. Nature Communications, 2021, 12: 3634. DOI:10.1038/s41467-021-23896-1 |
| [40] |
SUN T, TANG Z, ZANG W, et al. Ferromagnetic single-atom spin catalyst for boosting water splitting[J]. Nature Nanotechnology, 2023, 18(7): 763-771. DOI:10.1038/s41565-023-01407-1 |
| [41] |
BI J, CAI H, WANG B, et al. Localized surface plasmon enhanced electrocatalytic methanol oxidation of AgPt bimetallic nanoparticles with an ultra-thin shell[J]. Chemical Communications, 2019, 55(27): 3943-3946. DOI:10.1039/C9CC00331B |
| [42] |
ZHANG K, WANG C, YOU H, et al. Advanced Plasmon-driven ethylene glycol oxidation over 3D ultrathin Lotus-like PdCu nanosheets[J]. Chemical Engineering Journal, 2022, 438: 135666. DOI:10.1016/j.cej.2022.135666 |
| [43] |
YAN Y, WANG Q, HAO P, et al. Photoassisted strategy to promote glycerol electrooxidation to lactic acid coupled with hydrogen production[J]. ACS Applied Materials & Interfaces, 2023, 15(19): 23265-23275. |
| [44] |
ZHU M, WANG Y, WU Y, et al. Greatly enhanced methanol oxidation reaction of CoPt truncated octahedral nanoparticles by external magnetic fields[J]. Energy & Environmental Materials, 2023, 6(5): 12403. |
| [45] |
GAO R, KODAIMATI M S, HANDY K M, et al. Generating oscillatory behavior by applying a magnetic field during electrocatalytic oxidation of glycerol[J]. The Journal of Physical Chemistry C, 2022, 126(42): 18159-18169. DOI:10.1021/acs.jpcc.2c05145 |
| [46] |
ZHANG N, FENG Y, ZHU X, et al. Superior bifunctional liquid fuel oxidation and oxygen reduction electrocatalysis enabled by PtNiPd core-shell nanowires[J]. Advanced Materials, 2017, 29(7): 1603774. DOI:10.1002/adma.201603774 |
 2024, Vol. 41
2024, Vol. 41






