2. 天津大学机械工程学院, 天津 300350;
3. 中国电子科技集团公司第十八研究所 化学与物理电源重点实验室, 天津 300384
2. School of Mechanical Engineering, Tianjin University, Tianjin 300350, China;
3. Key Laboratory of Chemical and Physical Power Supply, 18 th Research Institute of China Electronics Technology Corporation, Tianjin 300384, China
随着全球化石燃料消费量不断增加,随之带来的气候变化及环境污染都会对人类社会的发展造成严峻挑战,而发展可再生能源的储存和转换技术是应对这些挑战的有效策略[1]。在现有的储能和转换系统中,锂离子电池由于具有高能量密度、低自放电率、较长循环寿命和质量轻等优点,被视为最方便和高效的储能器件,已广泛地占据了储能和动力设备市场[2]。目前,商业化的锂离子电池大多使用易挥发性和易燃的有机电解液,并且存在电解液泄漏,易发生起火爆炸等一系列安全隐患[3]。因此,寻找更加安全稳定的新型电解质已成为未来锂离子电池技术发展的目标。
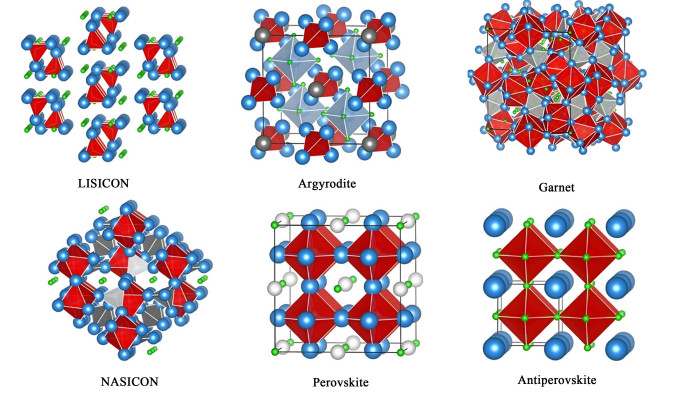
近年来,全固态锂金属电池因其具有安全性高、能量密度大、循环性能好、工作温度范围宽和回收方便等优点,成为了当前储能系统的研究热点之一[4]。固态电解质主要分为无机固态电解质(ISE)、聚合物固态电解质(SPE)和复合固态电解质(CPE)[5]。其中,无机固态电解质又可分为锂超离子导体(LISICON)[6, 7]、钠超离子导体(NASICON)[8, 9]、硫银锗矿型(Argyrodite)[10]、钙钛矿型(Perovskite)[11]、反钙钛矿型(Antiperovskite)[12]和石榴石型(Garnet)[13, 14]等类型。图 1为几种常见无机电解质的典型结构族(锂原子以绿色球体标记)。聚合物固态电解质主要有聚氧化乙烯(PEO)[15, 16]、聚偏氟乙烯(PVDF)[17]、聚丙烯腈(PAN)[18]、聚甲基丙烯酸甲酯(PMMA)[19]、聚碳酸亚乙烯酯(PVC)[20]、聚偏氟乙烯-六氟丙烯共聚物(PVDF-HFP)[21]等类型。复合固态电解质一般是由无机电解质颗粒与聚合物电解质进行复合所得到的。表 1总结了常见固态电解质的室温离子电导率。
| 固态电解质 | 类型 | 离子电导率/(S·cm-1) | Ref. |
| Li10GeP2S12 | LISICON | 1.20×10-2 | [24] |
| Li1.3Al0.3Ti1.7(PO4)3 | NASICON | 10-4~10-3 | [25] |
| Li6.5La3Zr1.5Ta0.5O12 | 石榴石 | 7.19×10-4 | [26] |
| Li0.33La0.557TiO3 | 钙钛矿 | 1.00×10-3 | [27] |
| Li3OCl | 反钙钛矿 | 2.00×10-3 | [28] |
| Li5.6PS4.6I1.4 | 硫银锗矿 | 2.04×10-3 | [29] |
| PEO(60 ℃) | 聚合物 | 2.20×10-4 | [30] |
| PEO/PVDF(60 ℃) | 聚合物 | 5.56×10-4 | [31] |
| PMA/PEO(65 ℃) | 聚合物 | 2.05×10-4 | [32] |
| PVDF-HFP(70 ℃) | 聚合物 | 7.20×10-4 | [33] |
| PEO/LLZTO | 复合 | 1.10×10-4 | [34] |
| PVDF/LLZTO | 复合 | 5.00×10-4 | [35] |
| PVDF/LLTO | 复合 | 5.30×10-4 | [36] |
| PVDF-HFP/LLZO | 复合 | 9.50×10-4 | [37] |
由于各种类型固态电解质的材料化学组成和微观结构存在着差异,其性能提升的策略也不相同。在保证锂电池循环稳定性的前提下,最大化地提升离子电导率是新型固态电解质研发的关键[22]。本论文首先介绍了不同类型固态电解质的离子传输机制,总结了影响固态电解质离子电导率的各种因素,综述了提高锂离子传输速率的技术途径及其最新研究进展。
1 固态电解质离子传输 1.1 离子传输机理固态电解质本质上是一种离子导体,电解质中的离子发生迁移是由电化学体系中的化学梯度和电化学梯度所驱动的,它的电流密度(j)可以用所有离子通量的总和来加以描述[38]。
| $j=F \sum\nolimits_i z_i N_i$ | (1) |
式(1)中:F表示法拉第常数;Ni表示物质i的通量;该物质的电荷数为zi(假设为1,后续计算忽略)。理想电解质溶液中的离子通量可以用Nernst-Planck方程来加以描述,它描述了溶质物质通过扩散、迁移和对流的通量[39]:
| $N_i=-D_i c_i-F \mu_i c_i \varphi_i+c_i u$ | (2) |
式(2)中:ci表示离子i的浓度;Di表示扩散系数;μi表示迁移率;φi表示电解质电位;u表示离子传输对流速度。将Nernst-Planck方程(2) 代入电流密度表达式(1)后,可以得到式(3):
| $J=-F \sum\nolimits_i D_i c_i-F^2 \varphi_i \sum\nolimits_i \mu_i c_i+F u \sum\nolimits_i c_i$ | (3) |
在固态电解质中,离子浓度梯度较小,扩散项和对流项可忽略不计,故公式(3)经简化后可得到电解质的电导率(σ)为:
| $\sigma=-\frac{j}{\varphi_i}=F^2 \sum\nolimits_i u_i c_i$ | (4) |
式(4)中,迁移率与扩散系数的关系为:
| $u_i=D_i / R T$ | (5) |
由式(4)可知,高离子电导率需要良好的离子迁移率和足够的解离离子对,二者缺一不可。因此,设计高离子导电性的固态电解质时,既要考虑如何促进锂盐离子对的解离,还要考虑如何降低离子运动过程中遇到的阻力。此外,虽然阳离子和阴离子的迁移对总电流均有贡献,但在大多数固态电解质中,产生输运电流的载流子主要是阳离子[40]。因此,有效的离子电导率一般是指固态电解质中金属阳离子的迁移速率。
1.2 无机固态电解质的离子传输大多数无机电解质(ISE)都具有配位多面体的周期性结构,锂离子的迁移扩散会在其骨架内存在的缺陷中进行。缺陷则主要包括点缺陷、线缺陷、平面缺陷、体积缺陷和电子缺陷等,其中,点缺陷在ISE的离子传输过程中起着重要作用。典型的点缺陷有肖特基缺陷和弗伦克尔缺陷[41]。
在ISE中,锂离子的传输机制主要包括空位机制和间隙机制。空位机制通常是由依靠肖特基缺陷产生的大量空位,供锂离子跃迁迁移。当1个锂离子迁移后,在原来的位置会产生1个新的空位,这样不断地循环往复,进而实现锂离子的连续输运。间隙机制则是间隙离子通过弗伦克尔缺陷进行扩散,锂离子连续置换相邻的有效位点,从而实现在分子骨架之间进行扩散[42]。此外,电解质的晶格可能在边界和界面附近处发生扭曲,锂离子会根据电位差重新移动排布,并产生额外的界面电荷传输路径[图 2(b)][40]。
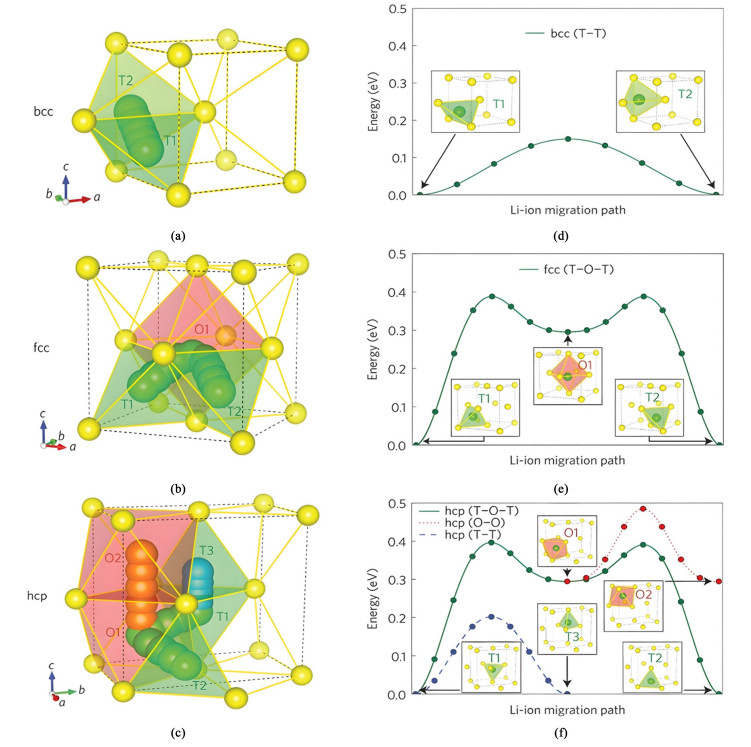
超离子导体型电解质通常具有无序的亚晶格结构,亚晶格中存在锂离子空位和间隙空位。从头算分子动力学模拟(AIMD)的结果表明,锂离子在超离子导体中,如硫化物电解质(LGPS)、钠超离子导体(LATP),会表现出多离子的协同迁移机制,即多个离子一起跃迁到各自下一个邻近的位置,而不是每个离子孤立地越过能垒进行迁移[43]。超离子导体离子传输动力学与晶格的静态结构和相关运动有关,如晶格极化率、阴离子堆积方式、活化能及指前因子、迁移离子亚晶格的排布无序化、晶体骨架的柔软度等[44]。Wang等[45]认为特定阴离子排列的拓扑结构是决定锂离子迁移率的一个关键因素,通过计算各种阴离子主体的锂离子迁移能垒可以发现,相比于面心立方(fcc)和六方最密(hcp)阴离子亚晶格结构,具有体心立方(bcc)阴离子的亚晶格结构具有最低的迁移能垒和最高的离子导电性(图 3)。
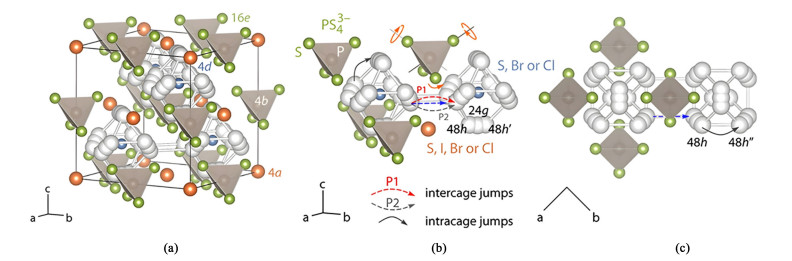
在硫银锗矿型电解质中,锂离子的迁移扩散过程会受晶体结构和缺陷化学等多种因素的影响,如图 4所示Hanghofer等[46]选择立方Li6PS5X (X=Cl, Br, I)电解质为研究对象,总结了硫银锗矿电解质中锂离子迁跃的3种类型:(1)锂离子可在相邻位点[图 4(c)中48 h和4 8h″位点]之间进行跃迁;(2)在“锂离子笼内”跳跃(p1);(3)在“锂离子笼间”跳跃(p2)。3种离子跃迁方式一起组成了Li6PS5X电解质内的锂离子传导过程。
钙钛矿结构的电解质和反钙钛矿结构相类似,但在相同位点上的电荷会发生反转,两者本身可观的离子电导率也源于晶体结构中存在空隙和缺陷。Baktash等[47]研究了缺陷分布对Li3OCl结构的影响。研究结果表明,缺陷分布起着重要的作用,它可以改变锂离子在Li3OCl中的扩散行为,可以调节Li3OCl固态电解质中的离子电导率。Emly等[48]从第一性原理出发,研究了2种反钙钛矿Li3OX(X=Cl, Br)的离子输运机制。计算结果表明,反钙钛矿Li3OCl中单个锂空位沿八面体棱边的迁移势垒为0.367 eV,小于八面体顶点跳跃的1.021 eV。间隙锂以哑铃型离子对形式迁移,迁移势垒更低。
石榴石结构电解质的离子传输与锂离子浓度有非常紧密的关系。相比于四方相石榴石型电解质,立方相结构的电解质因八面体位置有更高的锂离子浓度,具有更高的离子电导率[49]。Ramzy等[50]指出,对于不同石榴石体系,电导率与锂离子浓度为线性增加关系。Han等[51]用高温中子衍射(HTND)方法研究了立方石榴石型Li7La3Zr2O12中锂离子位移的三维间隙路径从室温到600 ℃的演化过程,并采用最大熵法(MEM)估计了锂核密度分布,观察了温度对锂离子迁移的影响。研究结果表明,在石榴石型的骨架中,锂离子的传导途径仅限于通过间隙空间的四面体位置进行扩散。
总之,ISE中的离子传输具有以下4个重要特征[41]:(1)锂离子的扩散倾向于通过间隙或空位的协同迁移机制。(2)ISE结构中骨架单元的排列和组成的差异,会导致传输势能面的分布方式不相同,从而影响离子电导率。(3)锂离子的迁移能垒与扩散路径有关,锂离子扩散途径中的传导通路增加,使锂离子迁移能垒降低,提高了离子电导率。(4)锂离子迁移率与锂离子亚晶格的无序度、骨架中主体原子的极化率及成键特性等相关。
1.3 聚合物固态电解质的离子传输聚合物固态电解质的离子导电相是通过将碱金属盐,如双三氟甲磺酰亚胺锂(LITFSI)等,与高分子聚合物基体进行络合而形成的。离子的传输主要依赖于聚合物链的节段弛豫过程,聚合物链段的弛豫有助于聚合物与阳离子之间配位键的破坏和形成,为阳离子的迁移提供自由体积,从而促进金属阳离子发生迁移[52]。
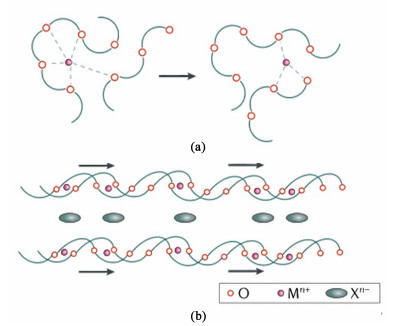
聚合物固态电解质的离子迁移主要在非结晶相中发生,以PEO为例,离子传输通常发生在玻璃化转变温度(Tg)以上的非结晶相区域。Zhao等[40]认为在非结晶相中,1个锂离子约与5个醚氧(EO)键形成弱配位,从而引起的阳离子(Mn+)的链内跳跃运动。而在结晶相中, 聚合物链折叠成圆柱形隧道,锂离子在聚合物链内发生传递,而阴离子(Xn-)则在聚合物链外迁移(图 5)。Brooks等[53]研究了PEO聚合物电解质离子扩散机制。分子动力学模拟(MD)的结果表明,在360 K时链内扩散是锂离子最可能的扩散路径,在更高的温度下链间扩散更为有利。他们还计算了锂离子在PEO基体中扩散的均方位移(MSD)。计算结果表明,柔性聚合物对锂离子的吸附过多,而刚性聚合物可以加快锂离子的扩散。
从PEO的导电机理可以看出,SPE中的离子电导率主要取决于以下因素[54]:(1)锂盐在聚合物基质中的溶解度。聚合物中锂离子浓度的增加,会提高其离子电导率。(2)聚合物链的迁移率。聚合物柔韧性的增加,同时分子内力、分子间力和结晶度的降低,会在一定程度上促进SPE离子电导率的提高。
1.4 复合固态电解质的离子传输1998年,Croce等[55]研究了纳米颗粒对PEO基聚合物电解质离子电导率的影响,由此开启了将颗粒应用于复合固态电解质设计和制备的快速发展阶段。复合固态电解质的填料包括惰性和活性2种类型,这2种类型的填料均可以提高聚合物电解质的离子导电性[56]。
Fan等[57]认为惰性颗粒能够提高复合电解质的离子导电性,主要归因于下面2种机制。首先,填料颗粒降低了聚合物基体的结晶度,颗粒表面和聚合物链之间的路易斯酸碱相互作用也会在动力学上抑制了聚合物链的结晶度,增强了聚合物链段的运动性,进而增加了锂离子的迁移率。其次,填料颗粒和锂盐之间的路易斯酸碱相互作用会促进锂盐的解离,增加了可移动锂离子的浓度。此外,填料颗粒和聚合物之间形成的界面层,也可以成为离子传输的快速路径。与惰性颗粒相比,活性颗粒在增强离子导电性方面更加有效。在复合固态电解质中,活性颗粒不仅起到惰性颗粒的作用,即通过路易斯酸碱相互作用在聚合物和颗粒之间的界面层内创建锂离子传输路径,而且活性颗粒作为锂离子导体,本身也可以促进锂离子的传输。因此,活性填料已成为当今研究的热点。
Zheng等[58]用立方相Li7La3Zr2O12(LLZO)石榴石和PEO进行复合制备了一种复合电解质,并组装成锂对称电池。通过同位素标记和核磁共振波谱法(NMR),监测电池循环期间复合电解质中7Li被金属电极中6Li替代的情况,以发现LLZO/PEO复合电解质中的锂离子传输路径。实验结果表明,LLZO陶瓷相更有利于锂离子通过,而不是PEO-LLZO界面或PEO基体相。Chen等[59]通过无溶剂热压法制备了一系列的PEO/Garnet复合固体电解质。他们发现,随着LLZTO含量的增加,复合固体电解质的形态由“陶瓷在聚合物中”(ceramic-in-polymer)逐渐过渡到“聚合物在陶瓷中”(polymer-in-ceramic)。同时电解质中的导锂通道也由单一聚合物导锂通道向聚合物和LLZTO双相导锂通道转变(图 6)。
Gupta等[60]考虑了LLZTO-CPE中的3种可能的锂离子传输路径:(1)通过聚合物基体;(2)通过聚合物和无机相界面;(3)通过无机填料相。他们原以为聚合物的离子电导率较低,同时CPE中无机组分的含量不高,路径(2)应是锂离子主要的传输路径。但是实验结果表明,路径(2)的传输阻抗要高于路径(1),因此实际情况则是路径(1)为CPE中主要的离子传输路径。他们认为,如果能增强路径(2)的离子传输速率,就可以大幅度地提高CPE的离子电导率。PEO与LLZTO之间的高界面阻抗是影响CPE离子电导率的主要因素,而LLZTO表面的杂质和PEO与LLZTO之间的锂离子浓度差则是产生高界面阻抗的主要原因。
如上所述,CPE中的锂离子传输可以通过聚合物相、通过无机相和通过无机/聚合物界面相等不同的途径。当然,由于复合固态电解质内部的离子传输机制非常复杂,仍需更多实验与模拟揭示其具体的传输行为。可以肯定的是,聚合物链和填料的界面在创建快速离子传输通道中起着关键作用,而合理的电解质结构及填料的均匀分散程度都是影响CPE离子导电性的重要因素[61]。
2 固态电解质的设计和研究进展为了提高固态电解质的离子电导率,各国的科研工作者正在努力开发各种新型固态电解质。下面按照固态电解质的结构类型,分别介绍各种固态电解质的最新研究进展。
2.1 无机固态电解质ISE的晶体结构是影响其离子电导率的一个重要因素。近年来,研究人员针对ISE的晶体结构的优化提出了许多有效的提升策略,包括改进制备方法,如高温固相反应、熔融淬火、共沉淀、机械化学以及气相反应等;掺杂不同的化合物或引入不同的元素离子,如氧化物、硫化物、卤化物及较大离子半径的阳离子等[62]。
为了深究超离子导体的组成结构与锂离子电导率的关系,Liang等[63]利用固相烧结法制备了一系列Li3-3xM1+xCl6(-0.14<x≤0.2, M=Tb, Dy, Ho, Y, Er, Tm)的氯化物超离子导体。他们发现,随着x值的增大,该电解质结构的空间群会从三方相(P-3m1)转变为正交(Pnma)。P-3m1和Pnma空间群都是由Cl-阴离子的hcp结构组成,但它们的阳离子(包括Li+和M3+)排列不同。在不同的Li-M-Cl体系中,向Pnma相的转变过程中会降低了锂离子扩散的活化能垒,增加锂离子的扩散速率。新的正交相材料如Li2.73Ho1.09Cl6的室温离子电导率更高,是三方相材料Li3HoCl6(0.3×10-3 S·cm-1)的4倍以上。合理改变ISE的空间群的结构可以提高超离子导体的离子电导率。
典型的硫银锗矿类硫化物电解质(Li6PS5Cl)可通过Li、P、S位的杂原子取代的方法来改善其离子电导率[64-66]。除此之外,氯元素含量对Li6PS5Cl的晶体结构也会有较大的影响。Zeng等[67]探究了Li7-xPS6-xClx体系中Cl-含量对其微观组织、Li|SE界面演化和抗锂枝晶能力的影响。实验结果表明,对于中、高程度的氯含量,Cl-离子不是完全位于Argyrodite晶格内,而是倾向于形成LiCl存在于晶粒表面,并相互连接构成LiCl纳米壳框架。在电化学循环过程中,LiCl纳米壳中的Cl-会迁移到锂金属负极和电解质界面(Li|SE)上,重新形成高质量的LiCl基的自限制界面层,从而有效地抑制了负极电解质界面处的电化学副反应和锂枝晶生长,并改善了锂离子传输。
Mo等[68]报道了一种无铅有机-无机卤化物钙钛矿MASr0.8Li0.4Cl3(MA=甲基铵,分子式为CH3NH2)电解质,该钙钛矿电解质具有高度对称的晶体结构和良好的成分可调性。通过密度泛函理论计算,证明了杂化钙钛矿框架可以允许快速的锂离子迁移而不破坏其晶体结构。他们同时系统研究了MASr1-xLi2xCl3(x=0.1, 0.2, 0.3, 0.4)中不同锂含量对锂离子迁移速率的影响,发现当锂含量为x=0.2时,MASr0.8Li0.4Cl3的离子电导率最高(7.0×10-6 S·cm-1),即可以通过平衡MASr0.8Li0.4Cl3中的锂离子和Sr空位来降低离子的跃迁能垒,以实现锂离子的快速传输。
石榴石型固态电解质的制备通常需要高于1 100 ℃的烧结温度,以实现致密化并获得高于0.1 mS·cm-1的室温离子电导率。当前普遍使用Al2O3、Li3BO3和Li4SiO4等烧结助剂来降低石榴石电解质的烧结温度[69, 70]。Chen等[71]采用原子层沉积(ALD)技术在陶瓷颗粒表面均匀地引入一层纳米非晶氧化铝涂层作为烧结助剂,这种烧结助剂包覆层的方法,可提高烧结助剂的分布均匀度和烧结活性,可以成功地将石榴石电解质的烧结温度降至1 000 ℃以下。石榴石型电解质在980 ℃温度条件下烧结后,表现出较高的室温离子电导率(0.13 mS·cm-1)。
2.2 聚合物固态电解质聚合物链运动、锂离子与聚合物链的解离能和锂离子的传输路径是影响SPE离子电导率的几个关键因素。以PEO为例,主要有3种策略提高其离子电导率:(1)使用增塑剂促进锂盐解离,降低聚合物的结晶度,改善聚合物链运动活性;(2)使用新型锂盐添加剂,抑制阴离子传输,提高了锂离子迁移数从而提高有效离子电导率。(3)改善聚合物本征分子内部结构,开发具有优化离子导电框架的SPE。
Xu等[72]提出了一种PEO基固体电解质的设计方案。他们使用丁二腈(SN)作为增塑剂,通过调节丁二腈和PEO的物质的量之比,构建了一种具有连续锂离子传输通道的均相固态聚合物电解质(Homo-SPE)。通过调节丁二腈(SN)和PEO的摩尔比,可以使PEO基固体电解质呈均相,同时抑制了PEO的结晶,降低了EO与锂离子之间的亲和力,即在均匀的固态聚合物电解质中,形成了锂离子传输的快速通道,使离子电导率提高了100倍。
Arrese-Igor等[73]开发了一种由聚碳酸丙烯酯(PPC)和聚环氧乙烷(PEO)所组成的双层聚合物电解质(DLPE)。他们通过布鲁斯-文森特(Bruce-Vincent)方法和脉冲梯度核磁共振(PFG-NMR)方法测量了锂离子迁移数。实验结果表明,添加聚4-苯乙烯磺酰(三氟甲基磺酰)亚胺锂盐(LiPSTFSI)后,阴离子(TFSI-)与聚苯乙烯链的键合可以极大提高锂离子迁移数,抑制了阴离子在负极表面的积累,降低了副反应的发生,从而表现出良好的锂离子传输性能。
Wen等[74]同时引发1,3-二氧环烷(DOL)和三羟甲基丙烷三缩水甘油醚(TTE),在超薄垂直多孔聚合物膜(LP)中进行阳离子开环交联聚合,成功地制备了一种超薄交联固体聚合物电解质[poly(DOL-TTE)-LP]。所得到的三维网络交联结构可大幅度减少聚合物固态电解质中局部分子链间的结晶度和末端易氧化羟基地数量,使其具有较高的室温离子电导率。
2.3 复合固态电解质无机填料的性能是影响复合固态电解质离子电导率的关键因素。无机填料与聚合物基体之间的相互作用和结合方式是近年来研究的热点。目前,固态电解质主要有3种设计思路:(1)向聚合物基体中添加惰性或活性填料;(2)构建有机/无机双层或多层结构;(3)向三维无机骨架中填充有机相组分。
Wang等[75]将碘化锂(LiI)作为双功能添加剂引入到PEO基电解质中,以提高其离子电导率并在Li/PEO间构建一层稳定的界面。实验结果表明,碘离子与PEO链上的氢原子之间会产生强烈的静电相互作用,形成大量I—H键,使PEO链发生交联,降低了PEO的结晶度,从而改善了锂离子的传输速率。
Zhang等[76]利用静电纺丝技术制备了PAN/LLZTO纤维网络材料,将其作为填料与PEO聚合物相结合,制备了一种三维纤维网络增强的PEO基固态电解质(PPL)。其中,3D骨架结构的纤维/陶瓷网络材料能够均匀地分布在PEO聚合物基体中,显著降低了PEO聚合物的结晶度,从而成功构建了连续的锂离子传输通道,使其具有较高的离子电导率(1.76×10-4 S·cm-1, 30 ℃)。
Wang等[30]利用NaCl作为模板制备了一种三维互连多孔结构的LATP框架,然后将PEO和LiTFSI引入到多孔陶瓷孔隙中,构建了一种复合电解质(CPE-3D)。这种由LATP框架增强的CPE表现出高的离子传导性和机械强度。由于三维互连多孔LATP框架和PEO电解质之间形成了长程连续的锂离子传输通道,CPE-3D的离子电导率在60 ℃时为7.47×10-4 S·cm-1,明显高于PEO(2.2×10-4 S·cm-1)。
3 总结与展望全固态锂电池具有高安全性、高能量密度、易加工、机械和热稳定性良好等优点,在未来储能技术领域表现出巨大的应用前景[77]。固态电解质作为其中的重要组成部分,目前仍然存在诸多技术障碍,限制了其快速发展。本论文介绍了不同固态电解质的离子传输机制,综述了当前最新的研究进展,为高离子电导率固态电解质材料的设计提供了理论依据。除本文总结的改进策略外,未来高性能固态电解质的开发,还应关注以下2个方面。
(1) 固态电解质体系的理论研究。尽管当前有大量理论模型阐述固态电解质中的导电机理,但这些阐释一方面不够具有普遍性,很多计算过程要依赖引入经验常数,与实验数据存在较大的出入。另一方面,随着金属有机框架材料(MOF)和共价有机框架(COF)等新型材料在固态电解质中得到应用,许多新的离子输运机制需要去进一步揭示。
(2) 多种改进策略相结合。全固态电池体系在商业化进程中依旧存在着诸多问题,采用单一技术手段无法解决问题,需要采用多种举措。如无机固态电解质存在着固-固相接触差、电解质片脆裂、对空气敏感等缺点。上述问题可通过综合掺杂、包覆、与聚合物复合等多种方式实现其性能的提升。还有,聚合物固态电池存在工作温度高、易短路和能量密度低等缺点。上述缺点可通过结合共聚、接枝、掺杂和复合等多种改进方式加以完善。复合固态电解质则存在着填料颗粒团聚和颗粒与聚合物基体相容性差等缺陷。上述问题可通过统筹新型制备工艺如热压、静电纺丝和3D打印等技术来加以改进。
| [1] |
ZHENG Y, YAO Y, OU J, et al. A review of composite solid-state electrolytes for lithium batteries: Fundamentals, key materials and advanced structures[J]. Chemical Society Reviews, 2020, 49(23): 8790-8839. DOI:10.1039/D0CS00305K |
| [2] |
马华, 从长杰, 王驰伟. 储能用锂离子动力电池研究进展[J]. 化学工业与工程, 2014, 31(3): 26-33. MA Hua, CONG Changjie, WANG Chiwei. Research progress on lithium-ion batteries for energy storage application[J]. Chemical Industry and Engineering, 2014, 31(3): 26-33. (in Chinese) |
| [3] |
陈立坤, 胡懿, 马家宾, 等. Li+电池固态聚合物电解质研究进展[J]. 化学工业与工程, 2020, 37(1): 2-16. CHEN Likun, HU Yi, MA Jiabin, et al. Research progress of solid polymer electrolytes for lithium-ion batteries[J]. Chemical Industry and Engineering, 2020, 37(1): 2-16. (in Chinese) |
| [4] |
HE L, SUN Q, CHEN C, et al. Failure mechanism and interface engineering for NASICON-structured all-solid-state lithium metal batteries[J]. ACS Applied Materials & Interfaces, 2019, 11(23): 20895-20904. |
| [5] |
许卓, 郑莉莉, 陈兵, 等. 固态电池复合电解质研究综述[J]. 储能科学与技术, 2021, 10(6): 2117-2126. XU Zhuo, ZHENG Lili, CHEN Bing, et al. Overview of research on composite electrolytes for solid-state batteries[J]. Energy Storage Science and Technology, 2021, 10(6): 2117-2126. (in Chinese) |
| [6] |
ZHANG Q, CAO D, MA Y, et al. Sulfide-based solid-state electrolytes: Synthesis, stability, and potential for all-solid-state batteries[J]. Advanced Materials, 2019, 31(44): e1901131. DOI:10.1002/adma.201901131 |
| [7] |
LEE J E, PARK K H, KIM J C, et al. Universal solution synthesis of sulfide solid electrolytes using alkahest for all-solid-state batteries[J]. Advanced Materials, 2022, 34(16): 2200083. DOI:10.1002/adma.202200083 |
| [8] |
RAJAGOPALAN R, ZHANG Z, TANG Y, et al. Understanding crystal structures, ion diffusion mechanisms and sodium storage behaviors of NASICON materials[J]. Energy Storage Materials, 2021, 34: 171-193. DOI:10.1016/j.ensm.2020.09.007 |
| [9] |
JIAN Z, HU Y, JI X, et al. NASICON-structured materials for energy storage[J]. Advanced Materials, 2017, 29(20): 1601925. |
| [10] |
FANG H, JENA P. Argyrodite-type advanced lithium conductors and transport mechanisms beyond paddle-wheel effect[J]. Nature Communications, 2022, 13(1): 1-11. |
| [11] |
ZHENG N, ZHANG C, LV Y, et al. Low-temperature synthesis of lithium lanthanum titanate/carbon nanowires for fast-charging Li-ion batteries[J]. ACS Applied Materials & Interfaces, 2022, 14(9): 11330-11338. |
| [12] |
QI H, XIE A, ZUO R. Local structure engineered lead-free ferroic dielectrics for superior energy-storage capacitors: A review[J]. Energy Storage Materials, 2022, 45: 541-567. DOI:10.1016/j.ensm.2021.11.043 |
| [13] |
ABOUALI S, YIM C H, MERATI A, et al. Garnet-based solid-state Li batteries: From materials design to battery architecture[J]. ACS Energy Letters, 2021, 6(5): 1920-1941. DOI:10.1021/acsenergylett.1c00401 |
| [14] |
CHEN S, NIE Z, TIAN F, et al. The influence of surface chemistry on critical current density for garnet electrolyte[J]. Advanced Functional Materials, 2022, 32(23): 2113318. DOI:10.1002/adfm.202113318 |
| [15] |
FENG J, WANG L, CHEN Y, et al. PEO based polymer-ceramic hybrid solid electrolytes: A review[J]. Nano Convergence, 2021, 8(1): 2. DOI:10.1186/s40580-020-00252-5 |
| [16] |
CHOO Y, HALAT D M, VILLALUENGA I, et al. Diffusion and migration in polymer electrolytes[J]. Progress in Polymer Science, 2020, 103: 101220. DOI:10.1016/j.progpolymsci.2020.101220 |
| [17] |
WU Y, LI Y, WANG Y, et al. Advances and prospects of PVDF based polymer electrolytes[J]. Journal of Energy Chemistry, 2022, 64: 62-84. DOI:10.1016/j.jechem.2021.04.007 |
| [18] |
ZHOU D, HE Y, LIU R, et al. In situ synthesis of a hierarchical all-solid-state electrolyte based on nitrile materials for high-performance lithium-ion batteries[J]. Advanced Energy Materials, 2015, 5(15): 1500353. DOI:10.1002/aenm.201500353 |
| [19] |
YAO Y, WANG X, DONG C, et al. Constructing effective interface for room-temperature beta-Al2O3 based sodium metal batteries[J]. Journal of Power Sources, 2022, 523: 231034. DOI:10.1016/j.jpowsour.2022.231034 |
| [20] |
YANG H, LIU Q, WANG Y, et al. An interlayer containing dissociated LiNO3 with fast release speed for stable lithium metal batteries with 400 Wh·kg-1 energy density[J]. Small, 2022, 18(25): 2202349. |
| [21] |
JIANG Y, XU C, XU K, et al. Surface modification and structure constructing for improving the lithium ion transport properties of PVDF based solid electrolytes[J]. Chemical Engineering Journal, 2022, 442: 136245. |
| [22] |
ZHU F, ISLAM M S, ZHOU L, et al. Single-atom-layer traps in a solid electrolyte for lithium batteries[J]. Nature Communications, 2020, 11(1): 1-9. |
| [23] |
XIA W, ZHAO Y, ZHAO F, et al. Antiperovskite electrolytes for solid-state batteries[J]. Chemical Reviews, 2022, 122(3): 3763-3819. DOI:10.1021/acs.chemrev.1c00594 |
| [24] |
SU H, JIANG Z, LIU Y, et al. Recent progress of sulfide electrolytes for all-solid-state lithium batteries[J]. Energy Materials, 2022. |
| [25] |
ZHU J, ZHAO J, XIANG Y, et al. Chemomechanical failure mechanism study in NASICON-type Li1.3Al0.3Ti1.7(PO4)3 solid-state lithium batteries[J]. Chemistry of Materials, 2020, 32(12): 4998-5008. DOI:10.1021/acs.chemmater.9b05295 |
| [26] |
YANG L, TAO X, HUANG X, et al. Efficient mutual-compensating Li-loss strategy toward highly conductive garnet ceramics for Li-metal solid-state batteries[J]. ACS Applied Materials & Interfaces, 2021, 13(47): 56054-56063. |
| [27] |
LV R, KOU W, GUO S, et al. Preparing two-dimensional ordered Li0.33La0.557TiO3 crystal in interlayer channel of thin laminar inorganic solid-state electrolyte towards ultrafast Li+ transfer[J]. Angewandte Chemie International Edition, 2022, 61(7). |
| [28] |
BRAGA M H, FERREIRA J A, STOCKHAUSEN V, et al. Novel Li3ClO based glasses with superionic properties for lithium batteries[J]. Journal of Materials Chemistry A, 2014, 2(15): 5470-5480. |
| [29] |
LIU Y, PENG H, SU H, et al. Ultrafast synthesis of I-rich lithium argyrodite glass-ceramic electrolyte with high ionic conductivity[J]. Advanced Materials, 2022, 34(3): 2107346. DOI:10.1002/adma.202107346 |
| [30] |
WANG G, LIU H, LIANG Y, et al. Composite polymer electrolyte with three-dimensional ion transport channels constructed by NaCl template for solid-state lithium metal batteries[J]. Energy Storage Materials, 2022, 45: 1212-1219. |
| [31] |
LI J, ZHU K, WANG J, et al. Optimisation of conductivity of PEO/PVDF-based solid polymer electrolytes in all-solid-state Li-ion batteries[J]. Materials Technology, 2022, 37(4): 240-247. |
| [32] |
ZHOU W, WANG Z, PU Y, et al. Double-layer polymer electrolyte for high-voltage all-solid-state rechargeable batteries[J]. Advanced Materials, 2019, 31(4): 1805574. DOI:10.1002/adma.201805574 |
| [33] |
JIE J, LIU Y, CONG L, et al. High-performance PVDF-HFP based gel polymer electrolyte with a safe solvent in Li metal polymer battery[J]. Journal of Energy Chemistry, 2020, 49: 80-88. DOI:10.1016/j.jechem.2020.01.019 |
| [34] |
GUO Q, XU F, SHEN L, et al. Poly(ethylene glycol) brush on Li6.4La3Zr1.4Ta0.6O12 towards intimate interfacial compatibility in composite polymer electrolyte for flexible all-solid-state lithium metal batteries[J]. Journal of Power Sources, 2021, 498: 229934. DOI:10.1016/j.jpowsour.2021.229934 |
| [35] |
ZHANG X, LIU T, ZHANG S, et al. Synergistic coupling between Li6.75La3Zr1.75Ta0.25O12 and poly(vinylidene fluoride) induces high ionic conductivity, mechanical strength, and thermal stability of solid composite electrolytes[J]. Journal of the American Chemical Society, 2017, 139(39): 13779-13785. DOI:10.1021/jacs.7b06364 |
| [36] |
LI B, SU Q, YU L, et al. Li0.35La0.55TiO3 nanofibers enhanced poly(vinylidene fluoride)-based composite polymer electrolytes for all-solid-state batteries[J]. ACS Applied Materials & Interfaces, 2019, 11(45): 42206-42213. |
| [37] |
LI Y, ZHANG W, DOU Q, et al. Li7La3Zr2O12 ceramic nanofiber-incorporated composite polymer electrolytes for lithium metal batteries[J]. Journal of Materials Chemistry A, 2019, 7(7): 3391-3398. |
| [38] |
陶祖贻, 杨更亮. Nernst-Planck方程和离子交换反应动力学[J]. 离子交换与吸附, 1990, 6(2): 137-145. TAO Zuyi, YANG Gengliang. Nernst Planck equation and ion exchange reaction kinetics[J]. Ion exchange and adsorption, 1990, 6(2): 137-145. (in Chinese) |
| [39] |
ROOIJ D. Electrochemical methods: Fundamentals and applications[J]. Anti-Corrosion Methods and Materials, 2003, 50(5). |
| [40] |
ZHAO Q, STALIN S, ZHAO C, et al. Designing solid-state electrolytes for safe, energy-dense batteries[J]. Nature Reviews Materials, 2020, 5(3): 229-252. |
| [41] |
ZHANG B, TAN R, YANG L, et al. Mechanisms and properties of ion-transport in inorganic solid electrolytes[J]. Energy Storage Materials, 2018, 10: 139-159. |
| [42] |
YANG H, WU N. Ionic conductivity and ion transport mechanisms of solid-state lithium-ion battery electrolytes: A review[J]. Energy Science & Engineering, 2022, 10(5): 1643-1671. |
| [43] |
NODA Y, NAKANO K, TAKEDA H, et al. Computational and experimental investigation of the electrochemical stability and Li-ion conduction mechanism of LiZr2(PO4)3[J]. Chemistry of Materials, 2017, 29(21): 8983-8991. DOI:10.1021/acs.chemmater.7b01703 |
| [44] |
ZHANG Z, NAZAR L F. Exploiting the paddle-wheel mechanism for the design of fast ion conductors[J]. Nature Reviews Materials, 2022, 7(5): 389-405. |
| [45] |
WANG Y, RICHARDS W D, ONG S P, et al. Design principles for solid-state lithium superionic conductors[J]. Nature Materials, 2015, 14(10): 1026-1031. |
| [46] |
HANGHOFER I, GADERMAIER B, WILKENING H M R. Fast rotational dynamics in argyrodite-type Li6PS5X (X: Cl, Br, I) as seen by 31P nuclear magnetic relaxation—On cation-anion coupled transport in thiophosphates[J]. Chemistry of Materials, 2019, 31(12): 4591-4597. |
| [47] |
BAKTASH A, DEMIR B, YUAN Q, et al. Effect of defects and defect distribution on Li-diffusion and elastic properties of anti-perovskite Li3OCl solid electrolyte[J]. Energy Storage Materials, 2021, 41: 614-622. DOI:10.1016/j.ensm.2021.06.039 |
| [48] |
EMLY A, KIOUPAKIS E, VAN DER VEN A. Phase stability and transport mechanisms in antiperovskite Li3OCl and Li3OBr superionic conductors[J]. Chemistry of Materials, 2013, 25(23): 4663-4670. DOI:10.1021/cm4016222 |
| [49] |
GUO Y, WU S, HE Y, et al. Solid-state lithium batteries: Safety and prospects[J]. eScience, 2022, 2(2): 138-163. DOI:10.1016/j.esci.2022.02.008 |
| [50] |
RAMZY A, THANGADURAI V. Tailor-made development of fast Li ion conducting garnet-like solid electrolytes[J]. ACS Applied Materials & Interfaces, 2010, 2(2): 385-390. |
| [51] |
HAN J, ZHU J, LI Y, et al. Experimental visualization of lithium conduction pathways in garnet-type Li7La3Zr2O12[J]. Chemical Communications, 2012, 48(79): 9840-9842. DOI:10.1039/c2cc35089k |
| [52] |
JR D, BALSARA N P. Polymer electrolytes[J]. Annual Review of Materials Research, 2013, 43: 503-525. DOI:10.1146/annurev-matsci-071312-121705 |
| [53] |
BROOKS D J, MERINOV B V, GODDARD W A Ⅲ, et al. Atomistic description of ionic diffusion in PEO-LiTFSI: Effect of temperature, molecular weight, and ionic concentration[J]. Macromolecules, 2018, 51(21): 8987-8995. DOI:10.1021/acs.macromol.8b01753 |
| [54] |
MENG N, LIAN F, CUI G. Macromolecular design of lithium conductive polymer as electrolyte for solid-state lithium batteries[J]. Small, 2021, 17(3): 2005762. DOI:10.1002/smll.202005762 |
| [55] |
CROCE F, APPETECCHI G B, PERSI L, et al. Nanocomposite polymer electrolytes for lithium batteries[J]. Nature, 1998, 394(6692): 456-458. |
| [56] |
MENG N, ZHU X, LIAN F. Particles in composite polymer electrolyte for solid-state lithium batteries: A review[J]. Particuology, 2022, 60: 14-36. DOI:10.1016/j.partic.2021.04.002 |
| [57] |
FAN L, HE H, NAN C. Tailoring inorganic-polymer composites for the mass production of solid-state batteries[J]. Nature Reviews Materials, 2021, 6(11): 1003-1019. |
| [58] |
ZHENG J, TANG M, HU Y. Lithium ion pathway within Li7La3Zr2O2-polyethylene oxide composite electrolytes[J]. Angewandte Chemie, 2016, 128(40): 12726-12730. DOI:10.1002/ange.201607539 |
| [59] |
CHEN L, LI Y, LI S, et al. PEO/garnet composite electrolytes for solid-state lithium batteries: From "ceramic-in-polymer" to "polymer-in-ceramic"[J]. Nano Energy, 2018, 46: 176-184. DOI:10.1016/j.nanoen.2017.12.037 |
| [60] |
GUPTA A, SAKAMOTO J. Controlling ionic transport through the PEO-LiTFSI/LLZTO interface[J]. The Electrochemical Society Interface, 2019, 28(2): 63-69. DOI:10.1149/2.F06192if |
| [61] |
JI X, ZHANG Y, CAO M, et al. Advanced inorganic/polymer hybrid electrolytes for all-solid-state lithium batteries[J]. Journal of Advanced Ceramics, 2022, 11(6): 835-861. |
| [62] |
KWAK H, WANG S, PARK J, et al. Emerging halide superionic conductors for all-solid-state batteries: Design, synthesis, and practical applications[J]. ACS Energy Letters, 2022, 7(5): 1776-1805. DOI:10.1021/acsenergylett.2c00438 |
| [63] |
LIANG J, VAN DER MAAS E, LUO J, et al. A series of ternary metal chloride superionic conductors for high-performance all-solid-state lithium batteries[J]. Advanced Energy Materials, 2022, 12(21): 2103921. DOI:10.1002/aenm.202103921 |
| [64] |
SCHNEIDER H, SEDLMAIER S J, DU H, et al. Stabilization of highly conductive lithium argyrodites by means of lithium substitution: The case of Li6Fe0.5PS6[J]. ChemistrySelect, 2019, 4(12): 3351-3354. DOI:10.1002/slct.201803388 |
| [65] |
TAN D, WU E, NGUYEN H, et al. Elucidating reversible electrochemical redox of Li6PS5Cl solid electrolyte[J]. ACS Energy Letters, 2019, 4(10): 2418-2427. DOI:10.1021/acsenergylett.9b01693 |
| [66] |
ZHANG Z, SUN Y, DUAN X, et al. Design and synthesis of room temperature stable Li-argyrodite superionic conductors via cation doping[J]. Journal of Materials Chemistry A, 2019, 7(6): 2717-2722. DOI:10.1039/C8TA10790D |
| [67] |
ZENG D, YAO J, ZHANG L, et al. Promoting favorable interfacial properties in lithium-based batteries using chlorine-rich sulfide inorganic solid-state electrolytes[J]. Nature Communications, 2022, 13(1): 1-13. |
| [68] |
MO H, YIN Y, LUO J, et al. Lead-free solid-state organic-inorganic halide perovskite electrolyte for lithium-ion conduction[J]. ACS Applied Materials & Interfaces, 2022, 14(15): 17479-17485. |
| [69] |
WAKUDKAR P, DESHPANDE A V. Effect of Li4SiO4 addition in Li6.22Al0.16La3Zr1.7Ta0.3O12 garnet type solid electrolyte for lithium ion battery application[J]. Ceramics International, 2019, 45(16): 20113-20120. DOI:10.1016/j.ceramint.2019.06.276 |
| [70] |
SHIN R H, SON S I, HAN Y, et al. Sintering behavior of garnet-type Li7La3Zr2O12-Li3BO3 composite solid electrolytes for all-solid-state lithium batteries[J]. Solid State Ionics, 2017, 301: 10-14. DOI:10.1016/j.ssi.2017.01.005 |
| [71] |
CHEN S, HU X, BAO W, et al. Low-sintering-temperature garnet oxides by conformal sintering-aid coating[J]. Cell Reports Physical Science, 2021, 2(9): 100569. DOI:10.1016/j.xcrp.2021.100569 |
| [72] |
XU S, SUN Z, SUN C, et al. Homogeneous and fast ion conduction of PEO-based solid-state electrolyte at low temperature[J]. Advanced Functional Materials, 2020, 30(51): 2007172. |
| [73] |
ARRESE-IGOR M, MARTINEZ-IBAÑEZ M, PAVLENKO E, et al. Toward high-voltage solid-state Li-metal batteries with double-layer polymer electrolytes[J]. ACS Energy Letters, 2022, 7(4): 1473-1480. DOI:10.1021/acsenergylett.2c00488 |
| [74] |
WEN S, LUO C, WANG Q, et al. Integrated design of ultrathin crosslinked network polymer electrolytes for flexible and stable all-solid-state lithium batteries[J]. Energy Storage Materials, 2022, 47: 453-461. DOI:10.1016/j.ensm.2022.02.035 |
| [75] |
WANG H, HOU T, CHENG H, et al. Bifunctional LiI additive for poly(ethylene oxide) electrolyte with high ionic conductivity and stable interfacial chemistry[J]. Journal of Energy Chemistry, 2022, 71: 218-224. DOI:10.1016/j.jechem.2022.02.041 |
| [76] |
ZHANG Z, ZHANG G, CHAO L. Three-dimensional fiber network reinforced polymer electrolyte for dendrite-free all-solid-state lithium metal batteries[J]. Energy Storage Materials, 2021, 41: 631-641. |
| [77] |
FU Z, CHEN X, ZHANG Q. Review on the lithium transport mechanism in solid-state battery materials[J]. WIREs Computational Molecular Science, 2022. DOI:10.1002/wcms.1621 |
 2024, Vol. 41
2024, Vol. 41