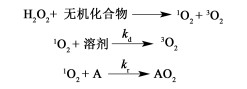
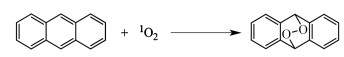1O2是一种应用广泛的活性氧(Reactive oxygen species,ROS),相比于其他ROS,1O2与有机物反应时,表现出更好的选择性和更高的反应活性[1]。因此,其在生物化学、有机化学、环境保护与光动力疗法等领域表现出重要的应用价值。1924年1O2被Lewisin[2]首次提出,但并未引起人们的关注。在较长的一段时间里,1O2的研究一直没有取得较大的进展。直到1963年,1O2被Khan以及Kasha等[3]发现存在于在次氯酸-过氧化氢反应体系中,其判断方法是通过观察到反应过程中的红色化学发光现象。紧接着,1964年,Foote等[4]证实1O2是光氧化中的主要氧化活性组分。这些研究成果为接下来的研究奠定了基础,极大地推动了1O2的研究进展。自此,有关高能1O2的性能及应用才逐渐被许多课题组所研究[5]。
几十年来,人们致力于1O2的制备和应用开发,本论文基于目前发表的研究结果,总结了1O2的制备方法与其在有机合成方面的应用,提出了过往研究中的优点与不足,并对其未来的发展趋势提出了展望。
1 单线态氧的制备经研究发现,氧分子的电子性质由π分子轨道的6个电子决定,用分子轨道处理氧分子与实验研究均表明氧分子内有2个不成对的电子,其电子排布为[KK(σ2s)2(σ2s*)2(σ2pz)2(π2px)2(π2py)2(π2px*)1(π2py*)1][6]。由于氧分子最外层的2个电子自旋平行且分别在2个不同轨道,因此氧分子具有顺磁性。三线态氧是处于基态的氧分子,一般用3∑g-(3O2)表示。当3∑g-的2个未成对电子受到一定能量激发后,由自旋平行变为自旋相反,当这2个电子占据同一个π2p*轨道时,为较稳定的第一激发态1O2,表示为1Δg (1O2)。当氧分子吸收的能量足够大时,这2个反向平行的电子会占据不同的分子轨道,达到最高能量激发态,即第2激发态1∑g+(1O2)。相比于3∑g-的能量,1Δg和1∑g+能量更高,分别为95 kJ ·mol-1和158 kJ ·mol-1[6]。但因1∑g+能量较高,使得其稳定性较差,因此1Δg的寿命相较于1∑g+更长,使其能参与溶液中的化学反应,是较为重要的1O2。人们通常所说的1O2即为第一激发态1Δg(1O2)。
基于其产生原理,制备1O2的有效途径有很多,包括酶催化法[7]、物理法[8]和化学法[9]。其中,酶催化法是指经酶催化反应产生1O2的方法,大多发生在生物体系中[10]。如嗜酸性粒细胞中过氧化物酶催化氧化蛋白质生成3-溴酪氨酸和3,5-二溴酪氨酸[11],大豆中脂肪氧合酶催化亚油酸氧化或制备[12],乳过氧化物酶或髓过氧化物酶催化硫氰酸盐离子氧化产生硫氰酸根离子[13]等。本研究侧重于1O2在合成化学方面的应用,因此主要论述了最常用的物理法和化学法这2种合成方法。
1.1 物理法物理法一般是指将其他形式的能量(如电能和光能)转化为1O2中化学能的合成方法,主要包括微波/射频放电法[14]与光敏化方法[15]。
1.1.1 微波/射频放电法微波或射频放电法是一种高频放电技术,指通过放电,使得微波中的能量转移到含氧气体(如O2、CO2或NO2)中,进而产生1O2的制备方法,由Foner和Hudson首次报道[16]。Javier等[17]也在低压下通过微波放电技术,成功从H2与CO2的混合气体中制备出1O2。但此方法转化率低,只有10%~20%,且反应过程中会产生氧原子与臭氧等物质,使得产物的成分更加复杂,1O2更易淬灭,因此对于此方法的应用研究较少。
1.1.2 光敏化法与放电法不同,光敏化法以廉价易得的氧气为原料,以光为能量来源,操作简单,可控性较强,因此成为较常用的1O2制备方法[18]。其原理为光敏化剂通过特定波长的光辐射,吸收能量成为激发态的单线态光敏剂。但单线态光敏剂不稳定,会通过发射荧光或者系间窜越成为激发态三线态光敏剂,而后激发态的三线态光敏剂可与基态氧发生反应,将能量转移给氧分子,使基态氧吸收能量成为1O2,而自身经过系间跨越回到三线态[19]。
从光敏化原理可知,反应过程中用到的光敏剂是一种能够吸收光并能将能量传递给基态氧的物质,是光敏化法制备1O2的核心。因此,光敏剂的选择至关重要,经大量研究发现,性能优良的光敏剂需要具有以下特点[20]:(1)在激发光源的光谱区(UV-Vis范围)吸收系数较高;(2)三线态具有较高的三线态能(Er≥95 kJ ·mol-1),且能传递给基态氧;(3)三线态需具有高的量子产率(ΦT>0.4)和较长的寿命(ΓT>1 μs);(4)有较好的光稳定性。
近几年来,光敏化制备1O2的方法成为人们研究的热点,多种物质被发现可作为光敏剂用于1O2的制备[21]。常用的光敏剂可分为以下4种:(1)四吡咯化合物[21];(2)芳香类[22];(3)半导体[23];(4)过渡金属配合物[24]。
1.1.2.1 四吡咯化合物此类光敏剂中,最常用的是卟啉和酞菁[25]。从结构来看,卟啉和酞菁都具有4个吡咯与异吲哚氮原子,属于环状四吡咯化合物。四吡咯类化合物拥有较大的π共轭体系,使其具有较高的光学活性和良好的光热稳定性。此类物质在日光下便能吸收光能进而激发为三线态,三线态分子具有的三线态能(Er≥95 kJ ·mol-1)足以将基态氧激发为1O2。除日光外,在UV-Vis范围内的许多波长能够被卟啉等四吡咯化合物吸收利用。
1999年,Nazeeruddin等[26]首次将酞菁用于光敏化反应。但人们发现酞菁在反应过程中容易发生聚集,不利于反应的进行[27]。因此,Sundstrom等[28]与Kimura等[29]分别通过酪氨酸取代法及在酞菁的外围苯环上添加三联苯酚醚集团的方法,抑制了酞菁的聚集。而卟啉类化合物中却很少出现这种聚集现象,其中,血卟啉[30]是较为成熟的光敏剂,其三线态量子产率很高,为0.83,相应地,反应过程中的1O2量子产率也很高,为0.65。虽然卟啉拥有较高的光学活性,但其性质却不易调控。且包括血卟啉在内的部分四吡咯化合物具有特殊的性质,即能在光敏化后一段时间内分解[31]。这对于医学方面的应用是有利的,但是却不利于其工业化方面的应用。
因此,人们进一步研究发现,由于此类化合物具有的特殊的吡咯结构,使其可以与金属元素络合,形成多种配合物[32],从而使其具有更高的化学稳定性,并可在合成过程中对其性质进行定向调控。
卟啉的金属化合物于1934年,由Ficsher等[33]首次发现,通过复杂的操作步骤从叶绿素与血红素化合物中提取出来,但此方法仅限于实验室。次年,Rothemund等[34]首次通过化学合成方法制备出四苯基卟啉,为卟啉化合物的工业化制备与应用提供了可能。
近几年,金属有机多孔骨架材料(Metal-organic frameworks,MOFs)成为人们的研究热点,MOFs的研究推动了卟啉与酞菁在光催化领域的应用研究进展[35, 36]。2015年,Zhou课题组[18]合成的光敏剂SO-PCN和PC-PCN,是以卟啉和Zn(NO3)2 ·6H2O等为原料制得。令人惊喜地发现,SO-PCN能够可逆控制1O2的生成。同年Jiang等[37]在Zhou的基础上,制备出PCN-222,并将其用于光催化还原CO2,取得了较好的效果。特殊地,卤族原子取代的二吡咯也是良好的光敏剂,如氮杂氟硼二吡咯(Aza-BODIPY),因其在长波长区域(>650 nm)具有强烈的吸收能力,且光稳定性好,合成简单,所以近年来受到广泛重视[38]。吴清华等[39]发现卤族原子取代位置不同,其效果也不同,2, 6-位取代时会更高效地产生1O2,且双溴化与四溴化的Aza-BODIPY能较快地产生1O2。该发现为光敏剂的合成与选择提供了新的思路。
1.1.2.2 芳香类常见的光敏剂,如玫瑰红(RB)亚甲基蓝(MB)及曙红(EO)等,大部分都属于芳香类[40]。此类物质包括芳香烃及芳香烃的衍生物,具有1个或多个苯环,其特殊的结构,使得其在光催化过程中,能够更好地实现能量转移。其中,醌类化合物常作为非质子溶剂中的光敏剂,如1, 8-二羟基蒽醌,其1O2量子产率可以达到0.69[41]。此外,氧杂蒽在可见光的绿色区域有较强的吸收谱带,在光催化中有较高的1O2量子产率,如孟加拉玫瑰的1O2量子产率为0.76[42]。在芳香类光敏剂中,卤素取代物的种类对其光催化活性有较大的影响,卤原子越大越有利于1O2的生成。因此,包含曙红B在内的四碘氧杂蒽衍生物相较于其他卤素取代物,有较强的光催化活性[43]。
1.1.2.3 半导体半导体纳米微晶(Semiconductor nanocrystal)的本质是一种三维团簇,它的光催化原理不同于传统的有机光敏剂[21]。当半导体在所需波长光的照射下,其价带电子会吸收光能而被激发到导带,从而在价带处产生空穴,形成电子空穴对。Samia课题组[44]在将半导体材料CdSe与酞箐染料结合参与反应的过程中,首次发现了半导体材料的光敏性,但该结合物难溶于水。后期,人们在此基础上选择水溶性的半导体与多种有机光敏剂结合,使得结合物能够溶于水,但反应过程中的量子产率较低,只有0.10~0.43[45]。经过研究后发现,部分半导体可直接作为光敏剂产生1O2。例如,TiO2便是一种优秀的光敏剂,得益于其化学性质稳定、价格低廉以及环境友好的优点,常用于涂料、空气净化以及化妆品制备,具有较高的商业价值[46]。但此类半导体的光利用率低,对氧分子的活化能力较弱且会同时催化产生多种ROS。针对此类问题,可通过在半导体表面加入氧空位或负载金属活性位点等方法进行改善[47]。如叶新辉[48]通过在BiOBrov上负载Fe位点,使得催化产物中只有1O2,从表征结果来看,1O2产率提升了75%左右,但降低了1O2的平均寿命。且参与的有机硫化物氧化制备亚砜的反应,最终的转化率与选择性几乎达到了100%。
1.1.2.4 过渡金属配合物除可作为半导体的金属配合物外,其他的部分无机配合物也可作为光敏剂,如Ru(Ⅱ)的金属配合物[49]。由于Ru(Ⅱ)的金属配合物在UV-Vis光谱区有较强的光吸收,因此其三线态具有较长的寿命,更利于1O2的合成,是一种常用的无机光敏剂;并且可以通过改变Ru(Ⅱ)的金属配合物中的配体,提高1O2的量子产率,如Ru(dpds)34-在CH3OD中的量子产率可达到1.0。除Ru外,Cr及Pt等过渡金属配合物也常被用作光敏化反应[50, 51]。因不同金属三线态具有的能量不同,所以其制备1O2的能力也不同,选择合适的金属配合物,对于光敏化反应至关重要。
由上可知,物理法制备1O2操作过程大多都较为复杂,且需要使用电能、光能等额外的能量。因此仍需寻找一些操作简单,环境友好的1O2制备方法。
1.2 化学法化学法制备1O2是指通过化学反应来实现的制备方法,此方法参与的反应基本无需额外的能量便可发生。1963年,Khan和Kasha[3]采用的次氯酸-过氧化氢反应制备1O2的方法,是化学法制备1O2的开端。近几十年,人们开发出多种原料用于制备1O2,如过氧化氢(H2O2)[52]、内过氧化物[53]和过氧自由基[54]等。其中,H2O2与内过氧化物最为常用。
1.2.1 H2O2制备1O2H2O2是一种基础的绿色化学品,常被用来作为制备1O2的原料。可通过2种途径来制备1O2,一种是被氧化剂氧化发生氧化反应[55],另一种是与金属及其配合物作用发生自身歧化反应[56]。其中,H2O2与氧化剂HClO的反应已被详细研究,在一定条件下基本可以定量生成1O2。Miyamoto等[57]使用同位素示踪法发现,1O2全部来自H2O2,而不是ClO-与H2O,其研究结果如图 1所示。
在此制备方法中,在反应体系中引入了Cl-等杂质,不利于产物的分离,且会引发副反应。添加氧化剂后,也增加了实验的危险性,不符合绿色合成的宗旨。相较于氧化剂氧化法,H2O2自身歧化分解,安全性更高,反应后的产物更易于提取,其反应机理如图 2所示。
早期,Gekhman等[58]发现H2O2在含有钒化合物的CF3COOH的溶液中,可以释放出的1O2,进而将N2氧化为N2O。Aubry[59]对此反应类型做了系统的研究,以推导出的1O2产率计算公式,计算出了元素周期表中各个H2O2-M体系的1O2产率,总结出了金属及其化合物与H2O2反应制备1O2的分布规律。其中,H2O2-Mo[60]和H2O2-La[61]体系的研究最为广泛。
H2O2和MoO42-在碱性条件下可以定量生成1O2,反应过程中会生成多种Mo的过氧配合物[MoOn(O2)4-n2-(n=0~3)],1O2便是由Mo的过氧配合物释放得到的[62]。但这些Mo的过氧配合物并不都能产生1O2,Aubry等通过采用紫外光谱和动力学研究等方法得出MoO2(O2)22-是产生1O2的前驱体,但却没有意识到紫外光谱无法准确区分出MoO3(O2)2-、MoO2(O2)22-和MoO(O2)32-。Nardello等[63]通过95MoNMR分析和动力学研究等方法,准确验证出只有MoO(O2)32-是产生1O2的主要前驱体;且当H2O2与Mo的摩尔比为3时,最有利于MoO(O2)32-的产生,即最有利于释放1O2。
H2O2-La体系中,相较于La单质,氧化镧等镧的配合物更加难以研究。因为过氧化物中间体的鉴定比较繁琐,且作用于H2O2分解速率的相关参数数量较高。Pierlot等[64]利用NIR检测器,分别研究了La(NO3)3、La2O3及La(OH)3参与的1O2制备过程;并判断出La(NO3)3分解H2O2时,原位生成的过氧化合物的比表面积更大,使得其催化H2O2分解的速度是其他2种镧配合物的60倍。
由此可知,H2O2与金属氧化物作用时生成的多种中间体,为有机合成及实验分析造成了巨大的阻碍,且催化剂在反应后不易于回收利用。因此,人们尝试将此类催化剂负载于分子筛等载体上,进而提高其化学稳定性。
Wahlen等[65]通过将La高度分散于载体材料来提高催化剂的反应活性,实验过程中,采用(1)分解H2O2的活性;(2)香茅醇和1O2的反应;(3)光学法等多种方法综合评价了催化剂的活性,其反应机理如图 3所示。
在此基础上,Wahlen等[66]又做了其他尝试,将钼酸根通过离子交换负载于层状双羟基上,制得Mo-LDH,用于催化H2O2生成1O2。发现非均相的Mo-LDH与均相钼酸盐相比,化学稳定性更高,更易从反应介质中回收,且便于重复使用。此外,Mo-LHD还可应用于非质子性溶剂。且在LDHs表面上Mo原子的活性远高于NaMoO4溶液中Mo原子的活性。
但载体催化剂的制备方法较为复杂,且成本较高,不利于提高其工业应用价值。Aubry等[60]合成的一种能储存1O2的试剂CaO2 ·2H2O2,在较低温度下便能生成1O2,且很容易通过过滤回收再生利用,制备方法简单,可被应用于多种溶剂中的有机合成反应。但是CaO2 ·2H2O2的储存温度较为苛刻,为-80 ℃,此缺点限制了其应用价值。
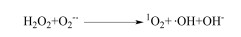
此外,除以上2种反应类型外,人们发现H2O2还会与超氧化物发生如图 4所示的Haber-Weiss反应[67],但还未成功将其应用于有机物的制备中。
内过氧化物一般是指由环芳烃捕捉1O2得到的中间体。此类物质在加热或紫外光照射下,表现出释放1O2的特性[68]。1926年,Dufraisse等[69]首次发现了这种现象,并对其进行了大量研究,他称这种现象为“碳与氧的不稳定结合”。人们又发现4-二甲氧基-9, 10-二苯基蒽在室温下即可释放1O2,这种异常反应是由于二氧桥所在的特殊位置导致的[70]。Fidder等[71]研究发现,吸收能量后蒽的内过氧化物在跃迁过程中,O—O键更易断裂,进而释放出1O2。稠环类过氧化物相对容易制备并且种类丰富,是制备1O2的有效路径。
1.2.3 其他除以上2种合成方法外,过硫酸盐活化是环境治理中常用的制备1O2的方法[72]。但反应过程中会伴随多种ROS的生成,选择性较差,不利于有机反应。经过研究发现,在碱性条件下生成的1O2较多,但也不能避免其他ROS的生成[73]。
1O2还可由其他过氧化物反应制得,如过氧自由基的Russell反应[74],过氧亚硝基化合物与过氧叔丁醇(t-BuOOH)的反应[54],以及过氧酸盐的热分解[75]等。臭氧加热分解或臭氧化物在低温下分解[76]也可产生1O2。
2 单线态氧的应用因1O2具有亲电性,使其对有机物有较强的反应能力,且对底物的选择性高,是化学合成中一种重要的反应试剂。1O2主要与不饱和化合物发生反应,但其将氧原子引入烯烃、二烯烃或芳香族等有机物,需采用不同的反应途径,主要包括1,3-加成反应[77]、1,2-环加成反应[78]和1,4-环加成反应[69]。
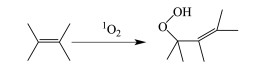
2.1 与烯烃的1,3-加成反应1O2与烯烃的1,3-加成反应又被称为1O2与烯烃的ene反应,这类反应由Schenck在1943年首次报道,故也被称为Schenck反应[79]。当具有烷基取代基的烯烃与1O2反应后,会生成相应的氢过氧化物,同时双键发生移动,到α位[80]。其中,1O2与单烯烃的反应机理如图 5所示。
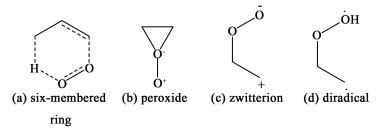
自发现1O2与烯烃的ene反应后,人们便投入了对其机理的探究。但关于反应过程中生成的中间态的争议却持续了很长时间。其中,主要对以下几种结构(图 6)展开了讨论[81]。
普遍认为,此类反应是逐步或协同向烯烃与二烯烃中加入氧。Davies与Schiesser[82]找到了2条反应路径。一种是生成六元环过渡态,另一种是生成三元环过渡态,也就是中间态为过氧化物。通过计算发现,除氮化氢外,这2条反应路径在各种情况下的能垒相同。但Inagaki与Fukui[83]更倾向于在反应的第1阶段生成了类似过氧化合物的复合物。Harding等[84]计算后,却排除了过氧化合物作为反应中间体的可能性,并表明1,4-自由基是这类反应中唯一可能形成的高能中间体。然而,这些作者都不能排除这类反应是协同反应的可能性。因此,Yamaguchi[84]在之前研究的基础上判断出,作为ene反应的中间体,双自由基相较于过氧化合物更加稳定,并间接证明了此类反应不是协同反应。
随着对ene反应机理认识的加深,人们将其更多的应用于有机物的合成[58, 77]。如使1O2与3-烷基环丙烯反应,生成相应的氢过氧化物[85],还可进一步脱水后生成更有应用价值的醌。
近几年,随着对1O2化学反应的深入研究,以四大反应类型为依据,通过热力学与反应动力学计算,判断反应类型的方法,受到越来越多研究工作者的青睐。牛涛[77]探究1O2与氯代酚的作用机理时,便是采用了这种方法。研究过程中,通过Gaussian计算,从热力学上发生的可能性以及反应动力学最终判断出,1O2与氯代酚发生的是ene反应。综上可知,1O2与烯烃的ene反应对有机物的合成方面具有重要意义。
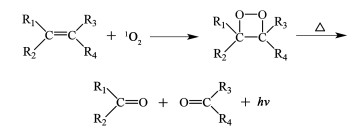
2.2 与富电子烯烃的1,2-环加成反应1O2不仅可与单烯烃发生1,3-加成反应,还可与富电子烯烃发生如图 7所示的1,2-加成反应[86]。如图 7所示,反应后碳碳双键断裂,生成了立体构型不变的1,2-二氧环丁烷。因此,此类反应又被称为[2+2]环加成反应。
但生成的四元环过氧化物具有较强的灵敏性,在加热条件下会发生有趣的化学发光反应,最终分解为羰基化合物[78]。
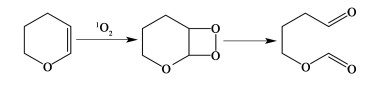
如果参与反应的碳碳双键,位于如图 8所示的环状有机物,在氧加到双键两侧后,最终会分裂成二醛类结构的化合物[85],为合成二醛类化合物提供了一种有效地合成路径,具有重要的应用价值。
以上反应都是1O2与富电子烯烃反应生成二氧杂环丁烷,但Bartlett[85]发现,1O2与亚金刚基金刚烷反应除生成二氧杂环丁烷外,还会生成环氧化合物。这是因为溶剂与中间体过氧化物发生了还原反应,使中间体无法重排成二氧杂环丁烷。此发现说明,1,2-环加成反应也是制备环氧化合物的有效途径,且可以通过选择合适的溶剂来调控环氧化合物的选择性。
由于此类物质与1O2反应较为灵敏,反应活化能低,且在1O2、H2O2、O2-·、OH·与ClO-这些活性氧同时存在时,会与1O2进行选择性反应[87, 88]。因此,常作为化学发光探针的其中一种,用于检测1O2,在一定程度上能够较好地减少底物对信号的干扰。
2.3 与共轭二烯烃的1,4-环加成反应在制备1O2的方法中提到,芳烃可与1O2反应,进而生成内过氧化物。此类反应由Dufraisse等[69]首次发现并大量研究。后来,这种1O2与芳烃或共轭二烯烃的反应,被称为1,4-环加成反应,又叫[4+2]环加成反应[89],与Diels-Alder反应类似,因此,该类反应的反应机理未能引起人们的重视。但Aubry等[90]发现其与Diels-Alder反应并不完全相同。具体表现为,有机物中,1O2的加入是通过单步协同机制发生的,具有对称的过渡结构,表现出从有机供体到氧的显著电荷转移。
除了探究1O2与有机物1,4-环加成反应的机理,人们还进一步确定了该类反应,反应速率常数的主要影响因素[89]。由于1O2本身具有的亲电性,其与芳香烃的反应会受到底物结构、空间位阻及溶剂的影响[91]。
虽然1O2与有机物的1,4-环加成反应与Diels-Alder反应并不完全相同,但是却有很多相似之处。其中较为重要的是,同一物质在1,4-环加成反应与Diels-Alder反应中的活性相对应。如,蒽与二烯烃亲和物和1O2都有较强的的反应性[92]。因此,可通过这一特性,预测某物质与1O2的反应活性,对1O2的应用有重要的指导意义。
通常来说,1,4-环加成产物相比于1,3-加成反应和1,2-环加成反应的产物具有较强的稳定性。表现为,其可在室温下分离和纯化,为其工业化应用提供了可能。但生成的桥环过氧化物大多不稳定,受热易分解,生成具有较高应用价值的二醛类或二酮类物质[93]。其中最为经典的是蒽及其衍生物与1O2的反应[94],反应过程中会生成蒽的内过氧化物,其反应原理如图 9所示。
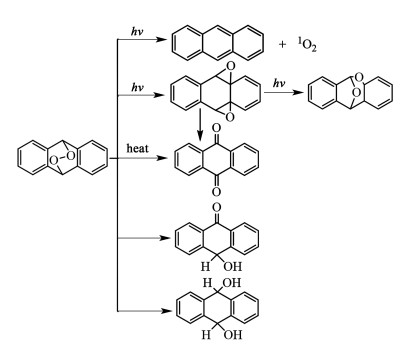
但内过氧化物不稳定会发生进一步的转化,Fidder等[71]对蒽的内过氧化物的转化方式进行了系统的研究。如图 10所示,除了释放出1O2后重新变为蒽,蒽的内过氧化物还可以再加热条件下生成蒽醌或其他蒽醌的衍生物。蒽醌作为制备H2O2的原料,有较高的合成价值。
由于蒽环与1O2反应后,生成的内过氧化物会产生较强的荧光,因此该反应类型已被开发为化学法测定1O2收率的常见方法之一[95]。如2004年,Ma等[96]以富电子的四硫磺戊烯与蒽为原料,得到了蒽衍生物探针。2018年,Sun等[97]设计了含有不同荧光团的探针,并仅通过一步取代反应便可轻松制得。此类探针在多种ROS同时存在的情况下,对1O2表现出高选择性并发生会强烈的化学发光反应。
2.4 与硫类、肽类化合物的反应1O2具有的特殊的亲电性,使得其还会与含有杂原子(N、S、P、Se等)的有机化合物发生反应[98]。如图 11所示,1O2会与硫醇或硫醚反应生成亚砜和砜类化合物[99]。由半导体催化制备的1O2,参与的有机硫化物氧化制亚砜的反应,转化率与选择性接近100%[48]。
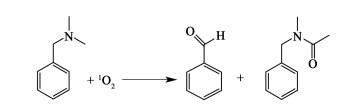
1O2与胺类反应机理如图 12所示,此过程中1O2的物理淬灭与氧化反应同时发生[100]。
除上述反应类型外,1O2还可与酚类[101]如苯酚、双酚A等发生较为复杂的反应。
3 总结与展望综述了自1O2被发现以来,研究者对于其认识、研究以及利用的发展进程。我们认识到,与其他ROS相比,1O2的选择性较好,活性更高,因此具有更大的研究价值。
制备方面:(1)物理法制备1O2中,光敏化法作为主要的制备方法,能够将太阳能加以利用,符合当下“双碳”背景的要求。(2)化学法制备1O2中,H2O2因其环保性,常作为1O2制备的原料。但其与金属化合物反应后,会形成多种过氧化物,反应体系较为复杂,因此还有较大的探究与优化空间。
应用方面:(1) 光敏化法应用于有机合成领域时,常用的四吡咯化合物、芳香类催化剂,其大部分反应转化率与选择性较低,限制了该方法的应用推广。在绿色化发展的要求下,迫切需要找到一种能够有效提高光催化氧化反应转化率和选择性的方法。(2)相比于四吡咯化合物、芳香类催化剂,半导体催化剂在有机合成领域表现出更大的催化潜力,通过负载金属位点,在一定程度上改善了半导体催化剂光利用率低,与对氧分子的活化能力较弱,且会同时催化产生多种ROS的问题。但其催化剂的制备过程较为复杂,影响了其工业化的进展。因此,进一步优化制备过程,降低催化剂制备的生产成本至关重要。(3)化学法中,H2O2与金属化合物体系制备1O2,是一种较为绿色的合成方法。但在其应用于有机氧化反应过程中,生成的中间体种类多,使得催化剂不易分离与回收。因此,金属化合物与载体结合的载体催化剂是未来化学法制备1O2工业化的突破要点。(4)通过1O2与有机物的反应,设计新的实验路线,能够高效、绿色和便捷的制备醇、环氧及羰基等化合物。
| [1] |
ZHANG J, CHEN P, GAO W, et al. Melamine-cyanurate supramolecule induced graphitic N-rich graphene for singlet oxygen-dominated peroxymonosulfate activation to efficiently degrade organic pollutants[J]. Separation and Purification Technology, 2021, 265: 118474. DOI:10.1016/j.seppur.2021.118474 |
| [2] |
HO R Y N, LIEBMAN J F, VALENTINE J S. Overview of the energetics and reactivity of oxygen[M]//Active Oxygen in Chemistry. Dordrecht: Springer Netherlands, 1995
|
| [3] |
KHAN A U, KASHA M. Red chemiluminescence of molecular oxygen in aqueous solution[J]. The Journal of Chemical Physics, 1963, 39(8): 2105-2106. DOI:10.1063/1.1734588 |
| [4] |
FOOTE C S, WEXLER S. Olefin oxidations with excited singlet molecular oxygen[J]. Journal of the American Chemical Society, 1964, 86(18): 3879-3880. DOI:10.1021/ja01072a060 |
| [5] |
QUINTANO M M, ROCHA W R. Computational insights into the reactivity of chlorpyrifos and chlorpyrifos-methyl toward singlet oxygen[J]. Journal of Molecular Modeling, 2021, 27(10): 282. |
| [6] |
HONG P, WU Z, YANG D, et al. Efficient generation of singlet oxygen (1O2) by hollow amorphous Co/C composites for selective degradation of oxytetracycline via Fenton-like process[J]. Chemical Engineering Journal, 2021, 421: 129594. DOI:10.1016/j.cej.2021.129594 |
| [7] |
LIU X, TIAN M, LI C, et al. Polyvinylpyrrolidone-stabilized Pt nanoclusters as robust oxidase mimics for selective detection of ascorbic acid[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2021, 625: 126985. DOI:10.1016/j.colsurfa.2021.126985 |
| [8] |
BHAT I A, SOMAN R, CHANDRA B, et al. 10, 15-Bis(ethoxycarbonyl)-5-(4-methoxycarbonylphenyl) B(Ⅲ) subchlorin: A photosensitizer with high singlet oxygen producing efficiency[J]. Journal of Porphyrins and Phthalocyanines, 2021, 25(10/12): 1015-1021. |
| [9] |
STANLEY C P, STOCKER R. Regulation of vascular tone and blood pressure by singlet molecular oxygen in inflammation[J]. Current Opinion in Nephrology and Hypertension, 2021, 30(2): 145-150. |
| [10] |
BASHIR F, REHMAN A U, SZABÓ M, et al. Singlet oxygen damages the function of Photosystem Ⅱ in isolated thylakoids and in the green alga Chlorella sorokiniana[J]. Photosynthesis Research, 2021, 149(1/2): 93-105. |
| [11] |
WU W, CHEN Y, D'AVIGNON A, et al. 3-bromotyrosine and 3, 5-dibromotyrosine are major products of protein oxidation by eosinophil peroxidase: Potential markers for eosinophil-dependent tissue injury in vivo[J]. Biochemistry, 1999, 38(12): 3538-3548. DOI:10.1021/bi982401l |
| [12] |
KANOFSKY J R, AXELROD B. Singlet oxygen production by soybean lipoxygenase isozymes[J]. Journal of Biological Chemistry, 1986, 261(3): 1099-1104. DOI:10.1016/S0021-9258(17)36059-3 |
| [13] |
AUNE T M, THOMAS E L. Accumulation of hypothiocyanite ion during peroxidase-catalyzed oxidation of thiocyanate ion[J]. European Journal of Biochemistry, 1977, 80(1): 209-214. |
| [14] |
AI M, DU H, LV S, et al. Effective removal of 2, 4, 6-trichlorophenol by FeSx/talc composite under microwave[J]. Journal of Environmental Chemical Engineering, 2021, 9(4): 105287. |
| [15] |
SUN Y, SUN L, FENG D, et al. An in situ one-pot synthetic approach towards multivariate zirconium MOFs[J]. Angewandte Chemie International Edition, 2016, 55(22): 6471-6475. DOI:10.1002/anie.201602274 |
| [16] |
FONER S N, HUDSON R L. Metastable oxygen molecules produced by electrical discharges[J]. The Journal of Chemical Physics, 1956, 25(3): 601-602. DOI:10.1063/1.1743000 |
| [17] |
DE LA FUENTE J F, MORENO S H, STANKIEWICZ A I, et al. Reduction of CO2 with hydrogen in a non-equilibrium microwave plasma reactor[J]. International Journal of Hydrogen Energy, 2016, 41(46): 21067-21077. DOI:10.1016/j.ijhydene.2016.08.032 |
| [18] |
PARK J, FENG D, YUAN S, et al. Photochromic metal-organic frameworks: Reversible control of singlet oxygen generation[J]. Angewandte Chemie International Edition, 2015, 54(2): 430-435. DOI:10.1002/anie.201408862 |
| [19] |
HASEGAWA R, IWAKIRI S, KUBO Y J. Synthesis and triplet sensitization of bis(arylselanyl)BOPHYs; potential application in triplet-triplet annihilation upconversion[J]. New Journal of Chemistry, 2021, 45(13): 6091-6099. DOI:10.1039/D1NJ00721A |
| [20] |
OPATA M R, DREUW A. Embelin's versatile photochemistry makes it a potent photosensitizer for photodynamic therapy[J]. The Journal of Physical Chemistry B, 2021, 125(14): 3527-3537. DOI:10.1021/acs.jpcb.1c00330 |
| [21] |
TSAY J M, TRZOSS M, SHI L, et al. Singlet oxygen production by peptide-coated quantum dot-photosensitizer conjugates[J]. Journal of the American Chemical Society, 2007, 129(21): 6865-6871. DOI:10.1021/ja070713i |
| [22] |
SAITA S, ANZAI M, MORI N, et al. Controlled aggregation of methylene blue in silica-methylene blue nanocomposite for enhanced 1O2 generation[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2021, 617: 126360. DOI:10.1016/j.colsurfa.2021.126360 |
| [23] |
LI R, OU X, ZHANG L, et al. Photocatalytic oxidation of NO on reduction type semiconductor photocatalysts: Effect of metallic Bi on CdS nanorods[J]. Chemical Communications, 2021, 57(78): 10067-10070. DOI:10.1039/D1CC03516A |
| [24] |
MULAZZANI Q G, SUN H, HOFFMAN M Z, et al. Quenching of the excited states of ruthenium(Ⅱ)-diimine complexes by oxygen[J]. The Journal of Physical Chemistry, 1994, 98(4): 1145-1150. DOI:10.1021/j100055a017 |
| [25] |
BRUCE G, SAMPERI M, AMABILINO D B, et al. Singlet oxygen generation from porphyrin-functionalized hexahedral polysilicon microparticles[J]. Journal of Porphyrins and Phthalocyanines, 2019, 23(1/2): 223-233. |
| [26] |
NAZEERUDDIN M K, HUMPHRY-BAKER R, GRÃTZEL M, et al. Efficient near IR sensitization of nanocrystalline TiO2 films by ruthenium phthalocyanines[J]. Chemical Communications, 1998(6): 719-720. DOI:10.1039/a708834e |
| [27] |
LIN K, DOANE T, WANG L, et al. Laser spectroscopic assessment of a phthalocyanine-sensitized solar cell as a function of dye loading[J]. Solar Energy Materials and Solar Cells, 2014, 126: 155-162. DOI:10.1016/j.solmat.2014.03.025 |
| [28] |
HE J, BENKÖ G, KORODI F, et al. Modified phthalocyanines for efficient near-IR sensitization of nanostructured TiO2 electrode[J]. Journal of the American Chemical Society, 2002, 124(17): 4922-4932. DOI:10.1021/ja0178012 |
| [29] |
KIMURA M, NOMOTO H, MASAKI N, et al. Dye molecules for simple Co-sensitization process: Fabrication of mixed-dye-sensitized solar cells[J]. Angewandte Chemie International Edition, 2012, 51(18): 4371-4374. |
| [30] |
ZHANG J, SHI C, SHAN F, et al. From biology to biology: Hematoporphyrin-melanin nanoconjugates with synergistic sonodynamic-photothermal effects on malignant tumors[J]. Chemical Engineering Journal, 2021, 408: 127282. DOI:10.1016/j.cej.2020.127282 |
| [31] |
DEROSA M C, CRUTCHLEY R J. Photosensitized singlet oxygen and its applications[J]. Coordination Chemistry Reviews, 2002, 233/234: 351-371. DOI:10.1016/S0010-8545(02)00034-6 |
| [32] |
ÖNAL E, TÜNCEL Ö, ALBAKOUR M, et al. Synthesizing and evaluating the photodynamic efficacy of asymmetric heteroleptic A7B type novel lanthanide bis-phthalocyanine complexes[J]. RSC Advances, 2021, 11(11): 6188-6200. |
| [33] |
CHANG C. Paul rothemund and S. Ferguson MacDonald, and their namesake reactions-The influence of the Fischer school on my life in porphyrin chemistry[J]. Israel Journal of Chemistry, 2016, 56(2/3): 130-143. |
| [34] |
ROTHEMUND P. Formation of porphyrins from pyrrole and aldehydes[J]. Journal of the American Chemical Society, 1935, 57(10): 2010-2011. |
| [35] |
CHEN Y, LI A, HUANG Z, et al. Porphyrin-based nanostructures for photocatalytic applications[J]. Nanomaterials, 2016, 6(3): 51. DOI:10.3390/nano6030051 |
| [36] |
FARAJZADEH N, ATMACA G Y, ERDOǦMUŞ A, et al. Comparatively singlet oxygen efficiency by sono-photochemical and photochemical studies of new lutetium (Ⅲ) phthalocyanines[J]. Dyes and Pigments, 2021, 190: 109325. DOI:10.1016/j.dyepig.2021.109325 |
| [37] |
LIU Y, HOWARTH A J, HUPP J T, et al. Selective photooxidation of a mustard-gas simulant catalyzed by a porphyrinic metal-organic framework[J]. Angewandte Chemie, 2015, 127(31): 9129-9133. DOI:10.1002/ange.201503741 |
| [38] |
王昭昀, 张萍, 张敏, 等. 喹啉取代的氟硼二吡咯染料类三价铁离子荧光探针的合成与性能[J]. 应用化学, 2018, 35(1): 46-52. WANG Zhaoyun, ZHANG Ping, ZHANG Min, et al. Synthesis and properties of quinoline substituted boron dipyrromethene based ferric ion probe[J]. Chinese Journal of Applied Chemistry, 2018, 35(1): 46-52. (in Chinese) |
| [39] |
吴清华, 崔救恩, 焦莉娟, 等. 溴代氮杂氟硼二吡咯类近红外吸收光敏剂的合成, 光物理性质及其产生单线态氧性能研究[J]. 安徽工程大学学报, 2020, 35(3): 1-8, 52. WU Qinghua, CUI Jiuen, JIAO Lijuan, et al. Synthesis, photophysical and singlet oxygen generation properties of near-infrared absorbed brominated aza-BODIPY derivatives[J]. Journal of Anhui Polytechnic University, 2020, 35(3): 1-8, 52. (in Chinese) |
| [40] |
LUTKUS L V, RICKENBACH S S, MCCORMICK T M. Singlet oxygen quantum yields determined by oxygen consumption[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2019, 378: 131-135. DOI:10.1016/j.jphotochem.2019.04.029 |
| [41] |
GUTIÉRREZ I, BERTOLOTTI S G, BIASUTTI M A, et al. Quinones and hydroxyquinones as generators and quenchers of singlet molecular oxygen[J]. Canadian Journal of Chemistry, 1997, 75(4): 423-428. DOI:10.1139/v97-048 |
| [42] |
REDMOND R W, GAMLIN J N. A compilation of singlet oxygen yields from biologically relevant molecules[J]. Photochemistry and Photobiology, 1999, 70(4): 391-475. |
| [43] |
BENKOVICS G, AFONSO D, DARCSI A, et al. Novel β-cyclodextrin-eosin conjugates[J]. Beilstein Journal of Organic Chemistry, 2017, 13: 543-551. |
| [44] |
SAMIA A C S, CHEN X, BURDA C. Semiconductor quantum dots for photodynamic therapy[J]. Journal of the American Chemical Society, 2003, 125(51): 15736-15737. DOI:10.1021/ja0386905 |
| [45] |
MA J, CHEN J, IDOWU M, et al. Generation of singlet oxygen via the composites of water-soluble thiol-capped CdTe quantum Dots Sulfonated aluminum phthalocyanines[J]. The Journal of Physical Chemistry B, 2008, 112(15): 4465-4469. DOI:10.1021/jp711537j |
| [46] |
CHEN C, ZHU X, WEN X, et al. Coupling N2 and CO2 in H2O to synthesize urea under ambient conditions[J]. Nature Chemistry, 2020, 12(8): 717-724. |
| [47] |
WU D, YE L, YUE S, et al. Alkali-induced in situ fabrication of Bi2O4-decorated BiOBr nanosheets with excellent photocatalytic performance[J]. The Journal of Physical Chemistry C, 2016, 120(14): 7715-7727. DOI:10.1021/acs.jpcc.6b02365 |
| [48] |
叶新辉. 二维溴氧化铋半导体表面氧空位与金属位点的构筑及其光催化氧气分子活化的研究[D]. 天津: 天津理工大学, 2021 YE Xinhui. Construction of oxygen vacancies and metal sites on the surface of two-dimensional bismuth oxybromide semiconductor and its photocatalytic activation of oxygen molecules[D]. Tianjin: Tianjin University of Technology, 2021 (in Chinese) |
| [49] |
LI J, LIU L. On the synthesis and characterization of Ru(Ⅱ)-doped polymer fibers: Polymer immobilization effect on Ru(Ⅱ) emitter photophysical performance and singlet oxygen generation[J]. Journal of Luminescence, 2021, 238: 118224. |
| [50] |
LI W, YANG S, WANG W, et al. Simultaneous removal of Cr(Ⅵ) and acid Orange 7 from water in pyrite-persulfate system[J]. Environmental Research, 2020, 189: 109876. DOI:10.1016/j.envres.2020.109876 |
| [51] |
SHAFIKOV M Z, SULEYMANOVA A F, KUTTA R J, et al. Dual emissive dinuclear Pt(Ⅱ) complexes and application to singlet oxygen generation[J]. Journal of Materials Chemistry C, 2021, 9(17): 5808-5818. DOI:10.1039/D1TC00282A |
| [52] |
SCISCENKO I, ARQUES A, VARGA Z, et al. Significant role of iron on the fate and photodegradation of enrofloxacin[J]. Chemosphere, 2021, 270: 129791. DOI:10.1016/j.chemosphere.2021.129791 |
| [53] |
TURKSOY A, YILDIZ D, AYDONAT S, et al. Mechanochemical generation of singlet oxygen[J]. RSC Advances, 2020, 10(16): 9182-9186. DOI:10.1039/D0RA00831A |
| [54] |
MIYAMOTO S, MARTINEZ G R, MARTINS A P B, et al. Direct evidence of singlet molecular oxygen[O2(1Δg)] production in the reaction of linoleic acid hydroperoxide with peroxynitrite[J]. Journal of the American Chemical Society, 2003, 125(15): 4510-4517. |
| [55] |
TIAN S, LI Y, ZENG H, et al. Cyanide oxidation by singlet oxygen generated via reaction between H2O2 from cathodic reduction and OCl- from anodic oxidation[J]. Journal of Colloid and Interface Science, 2016, 482: 205-211. |
| [56] |
CASTRO J, FERNÁNDEZ F, OLIVARES F, et al. Electrodes based on zeolites modified with cobalt and/or molybdenum for pesticide degradation: Part Ⅱ—2, 4, 6-trichlorophenol degradation[J]. Journal of Solid State Electrochemistry, 2021, 25(1): 117-131. |
| [57] |
TSUKAGOSHI K, FUKUMOTO K, NAKAJIMA R, et al. Characterization of chemiluminescence from singlet oxygen under laminar flow conditions in a micro-channel and its quenching with beverages[J]. Talanta, 2007, 72(2): 607-611. DOI:10.1016/j.talanta.2006.11.022 |
| [58] |
GEKHMAN A E, STOLYAROV I P, SHESTAKOV A F, et al. Oxidation of molecular nitrogen with hydrogen peroxide[J]. Russian Chemical Bulletin, 2003, 52(3): 768-770. |
| [59] |
AUBRY J M. Search for singlet oxygen in the decomposition of hydrogen peroxide by mineral compounds in aqueous solutions[J]. Journal of the American Chemical Society, 1985, 107(21): 5844-5849. DOI:10.1021/ja00307a002 |
| [60] |
PIERLOT C, NARDELLO V, SCHRIVE J, et al. Calcium peroxide diperoxohydrate as a storable chemical generator of singlet oxygen for organic synthesis[J]. ChemInform, 2002, 33(38): 46. DOI:10.1002/chin.200238046 |
| [61] |
NARDELLO V, BARBILLAT J, MARKO J, et al. Lanthanum(Ⅲ)-catalyzed disproportionation of hydrogen peroxide: A heterogeneous generator of singlet molecular oxygen—1O2 (1Δg)—In near-neutral aqueous and organic media for peroxidation of electron-rich substrates[J]. Chemistry-A European Journal, 2003, 9(2): 435-441. DOI:10.1002/chem.200390045 |
| [62] |
JARY W, POCHLAUER P, FALK H, et al. Singlet oxygen oxidation of organic substrates: US20040156776[P]. 2004-08-12
|
| [63] |
NARDELLO V, MARKO J, VERMEERSCH G, et al. 90Mo NMR and kinetic studies of peroxomolybdic intermediates involved in the catalytic disproportionation of hydrogen peroxide by molybdate ions[J]. Inorganic Chemistry, 1995, 34(20): 4950-4957. DOI:10.1021/ic00124a007 |
| [64] |
PIERLOT C, BARBILLAT J, NARDELLO-RATAJ V, et al. Optimisation of the chemical generation of singlet oxygen (1O2, 1Δg) from the hydrogen peroxide-lanthanum(Ⅲ) catalytic system using an improved NIR spectrometer[J]. Photochemical & Photobiological Sciences, 2009, 8(7): 1024-1031. |
| [65] |
RAO A V S, RAVISHANKAR H N, RAMASARMA T. Vanadium catalysis in bromoperoxidation reaction[J]. Archives of Biochemistry and Biophysics, 1996, 334(1): 121-134. DOI:10.1006/abbi.1996.0437 |
| [66] |
WAHLEN J, DE VOS D E, GROOTHAERT M H, et al. Synergism between molybdenum and lanthanum in the disproportionation of hydrogen peroxide into singlet oxygen[J]. Journal of the American Chemical Society, 2005, 127(49): 17166-17167. DOI:10.1021/ja0547026 |
| [67] |
KHAN A U, KASHA M. Singlet molecular oxygen in the Haber-Weiss reaction[J]. Proceedings of the National Academy of Sciences of the United States of America, 1994, 91(26): 12365-12367. |
| [68] |
BLOODWORTH A J, EGGELTE H J. Face selectivity in the reduction with dideuteriodiimide of endoperoxides derived from the singlet oxygenation of 1,3-cycloalkadienes[J]. Journal of the Chemical Society, 1984, 12: 2069-2072. |
| [69] |
MOUREAU C, DUFRAISE C, DEAN P M. A dissociable organic peroxide. The peroxide of rubrene[J]. Comptes Rendus, 1926, 182: 1584-1587. |
| [70] |
DUFRAISSE C, VELLUZ L. Labile union of O with C. Photoöxidation of variously substituted dimethoxy-ms-diphenylanthracenes[J]. Bulletin de la Societe Chimique de France, 1942, 9: 171-184. |
| [71] |
FIDDER H, LAUER A, FREYER W, et al. Photochemistry of anthracene-9, 10-endoperoxide[J]. The Journal of Physical Chemistry A, 2009, 113(22): 6289-6296. DOI:10.1021/jp901073s |
| [72] |
RAO L, YANG Y, CHEN L, et al. Highly efficient removal of organic pollutants via a green catalytic oxidation system based on sodium metaborate and peroxymonosulfate[J]. Chemosphere, 2020, 238: 124681-124687. |
| [73] |
KHAN A, ZHANG K K, SUN P, et al. High performance of the A-Mn2O3 nanocatalyst for persulfate activation: Degradation process of organic contaminants via singlet oxygen[J]. Journal of Colloid and Interface Science, 2021, 584: 885-899. DOI:10.1016/j.jcis.2020.10.021 |
| [74] |
MIYAMOTO S, MARTINEZ G R, MEDEIROS M H G, et al. Singlet molecular oxygen generated from lipid hydroperoxides by the Russell mechanism: Studies Using 18O-labeled linoleic acid hydroperoxide and monomol light emission measurements[J]. Journal of the American Chemical Society, 2003, 125(20): 6172-6179. DOI:10.1021/ja029115o |
| [75] |
NIU Q, MENDENHALL G D. Yields of singlet molecular oxygen from peroxyl radical termination[J]. Journal of the American Chemical Society, 1992, 114(1): 165-172. DOI:10.1021/ja00027a024 |
| [76] |
MUÑOZ F, MVULA E, BRASLAVSKY S E, et al. Singlet dioxygen formation in ozone reactions in aqueous solution[J]. Journal of the Chemical Society, Perkin Transactions 2, 2001(7): 1109-1116. DOI:10.1039/b101230o |
| [77] |
牛涛. 单线态氧与氯代酚作用机理的理论研究[D]. 江苏无锡: 江南大学, 2008 NIU Tao. Theoretical study on the interaction mechanism between singlet oxygen and chlorophenol[D]. Jiangsu Wuxi: Jiangnan University, 2008 (in Chinese) |
| [78] |
刘剑波, 宋心琦. 分子氧、活性氧与生命[J]. 大学化学, 1994, 9(5): 26-33. LIU Jianbo, SONG Xinqi. Molecular oxygen, active oxygen and life[J]. University Chemistry, 1994, 9(5): 26-33. (in Chinese) |
| [79] |
KEARNS D R. Physical and chemical properties of singlet molecular oxygen[J]. Chemical Reviews, 1971, 71(4): 395-427. DOI:10.1021/cr60272a004 |
| [80] |
张建成, 王夺元. 现代光化学[M]. 北京: 化学工业出版社, 2006.
|
| [81] |
GAJEWSKI J J. Hydrocarbon thermal isomerizations[M]. New York: Academic Press, 1981.
|
| [82] |
DAVIES A G, SCHIESSER C H. A PM3 study of the reactions of propene with singlet oxygen and other enophiles[J]. Tetrahedron, 1991, 47(9): 1707-1726. |
| [83] |
INAGAKI S, FUKUI K. Mechanism of[2+2]cycloaddition and related reactions between electron donors and electron acceptors. Perepoxide quasi-intermediate and its roles in the reactions of 1. DELTA. g molecular oxygen with olefins[J]. Journal of the American Chemical Society, 1975, 97(26): 7480-7484. DOI:10.1021/ja00859a015 |
| [84] |
HARDING L B, GODDARD W A. The mechanism of the ene reaction of singlet oxygen with olefins[J]. Chemischer Informationsdienst, 1980, 11(2): 439-449. |
| [85] |
马炳生, 潘荣欣, 王立夫. 单线态氧及其在有机合成中的应用[J]. 高师理科学刊, 1998, 18(1): 26-30. MA Bingsheng, PAN Rongxin, WANG Lifu. Singlet oxygen and its application of organic synthesis[J]. Journal of Science of Teachers College and University, 1998, 18(1): 26-30. (in Chinese) |
| [86] |
DINACHE A, SMARANDACHE A, SIMON A, et al. Photosensitized cleavage of some olefins as potential linkers to be used in drug delivery[J]. Applied Surface Science, 2017, 417: 136-142. DOI:10.1016/j.apsusc.2017.03.177 |
| [87] |
MACMANUS-SPENCER L A, MCNEILL K. Quantification of singlet oxygen production in the reaction of superoxide with hydrogen peroxide using a selective chemiluminescent probe[J]. Journal of the American Chemical Society, 2005, 127(25): 8954-8955. DOI:10.1021/ja052045b |
| [88] |
MACMANUS-SPENCER L A, LATCH D E, KRONCKE K M, et al. Stable dioxetane precursors as selective trap-and-trigger chemiluminescent probes for singlet oxygen[J]. Analytical Chemistry, 2005, 77(4): 1200-1205. DOI:10.1021/ac048293s |
| [89] |
XI T, LI X, ZHANG Q, et al. Enhanced catalytic oxidation of 2, 4-dichlorophenol via singlet oxygen dominated peroxymonosulfate activation on CoOOH@Bi2O3 composite[J]. Frontiers of Environmental Science & Engineering, 2020, 15(4): 1-11. |
| [90] |
AUBRY J M, PIERLOT C, RIGAUDY J, et al. Reversible binding of oxygen to aromatic compounds[J]. Accounts of Chemical Research, 2003, 36(9): 668-675. DOI:10.1021/ar010086g |
| [91] |
SEIP M, BRAUER H D. Endoperoxide formation of helianthrene with triplet molecular oxygen. A spin-forbidden reaction[J]. Journal of the American Chemical Society, 1992, 114(12): 4486-4490. DOI:10.1021/ja00038a007 |
| [92] |
LIU X, DAI P, GU T, et al. Cyclometalated iridium(Ⅲ) complexes containing an anthracene unit for sensing and imaging singlet oxygen in cellular mitochondria[J]. Journal of Inorganic Biochemistry, 2020, 209: 111106. DOI:10.1016/j.jinorgbio.2020.111106 |
| [93] |
GROSSMAN J N, KOWAL S F, STUBBS A D, et al. Anthracene and pyrene photooxidation kinetics in saltwater environments[J]. ACS Earth and Space Chemistry, 2019, 3(12): 2695-2703. DOI:10.1021/acsearthspacechem.9b00218 |
| [94] |
LIU K, LALANCETTE R A, JÄKLE F. Tuning the structure and electronic properties of B-N fused dipyridylanthracene and implications on the self-sensitized reactivity with singlet oxygen[J]. Journal of the American Chemical Society, 2019, 141(18): 7453-7462. DOI:10.1021/jacs.9b01958 |
| [95] |
尹红菊, 钱琦文, 张绪尖. 蒽环类物质检测单线态氧的研究新进展[J]. 曲靖师范学院学报, 2016, 35(3): 27-34. YIN Hongju, QIAN Qiwen, ZHANG Xujian. Recent progress in detection of singlet oxygen by fluorescent probes containing anthracene ring[J]. Journal of Qujing Normal University, 2016, 35(3): 27-34. (in Chinese) |
| [96] |
LI X, ZHANG G, MA H, et al. 4, 5-dimethylthio-4'-[2-(9-anthryloxy)ethylthio]tetrathiafulvalene, a highly selective and sensitive chemiluminescence probe for singlet oxygen[J]. Journal of the American Chemical Society, 2004, 126(37): 11543-11548. DOI:10.1021/ja0481530 |
| [97] |
SUN M, KRISHNAKUMAR S, ZHANG Y, et al. Singlet oxygen probes made simple: Anthracenylmethyl substituted fluorophores as reaction-based probes for detection and imaging of cellular 1O2[J]. Sensors and Actuators B: Chemical, 2018, 271: 346-352. DOI:10.1016/j.snb.2018.05.063 |
| [98] |
ROEINFARD M, ZAHEDIFAR M, DARROUDI M, et al. Synthesis of graphene quantum dots decorated with Se, Eu and Ag As photosensitizer and study of their potential to use in photodynamic therapy[J]. Journal of Fluorescence, 2021, 31(2): 1-7. |
| [99] |
FALKOWSKI M, KUCINSKA M, PISKORZ J, et al. Synthesis of sulfanyl porphyrazines with bulky peripheral substituents-Evaluation of their photochemical properties and biological activity[J]. Journal of Photochemistry and Photobiology A: Chemistry, 2021, 405: 112964. DOI:10.1016/j.jphotochem.2020.112964 |
| [100] |
BACIOCCHI E, DEL GIACCO T, LAPI A. Oxygenation of benzyldimethylamine by singlet oxygen. Products and mechanism[J]. Organic Letters, 2004, 6(25): 4791-4794. DOI:10.1021/ol047876l |
| [101] |
QI C, LIU X, MA J, et al. Activation of peroxymonosulfate by base: Implications for the degradation of organic pollutants[J]. Chemosphere, 2016, 151: 280-288. |
 2024, Vol. 41
2024, Vol. 41