氯乙烯(VCM)作为工业生产聚氯乙烯(PVC)的单体,在工业上主要采取乙炔氢氯化法和乙烯法生产[1]。由于国内多煤少气的资源环境,主要采取乙炔氢氯化法生产氯乙烯,工业用氯化汞(HgCl2)催化剂。然而,由于汞容易在反应过程中流失,严重污染环境,因此探求工业化乙炔氢氯化无汞催化剂的工作日渐紧迫[2, 3]。
近些年来,随着Huchings等[4]将金属阳离子标准电极电势同催化活性联系在一起,指出电极电势与催化活性正相关,并成功预测金(Au)基催化剂的高活性以来,无汞催化剂的研究取得了极大的进展。目前主要的研究集中在Au[5-7]、Ru[8, 9]、Pd[10, 11]等贵金属和Cu[12, 13]等非贵金属,通过对载体进行杂原子掺杂改性、多金属协同作用以及液相均相催化[14, 15]等来提高催化活性。尽管Pd基催化剂具备极高的初始活性,但目前的研究较少,主要是由于活性组分Pd易流失以及易积碳[10, 16],这就导致催化剂在反应中稳定性较差。因此,提高Pd基催化剂稳定性是其工业化应用的主要技术难题。
到目前为止,乙炔氢氯化Pd基催化剂的研究主要集中在载体改性及多金属协同策略,以此提高催化剂稳定性。例如,王璐等[17]以NFY分子筛为载体,通过添加KCl作为助剂,制备Pd-K/NFY双金属催化剂,结果表明,添加钾能有效提高Pd/NFY催化剂的催化稳定性,稳定更多的活性位点(Pd2+基团),抑制碳沉积。李小年等[10]通过引入氯化1-丁基-3-甲基咪唑氯盐离子液体,利用离子液体对Pd物种的吸附作用,降低Pd物种在反应过程中的流失,以此来提高催化剂的稳定性,其制备的0.5Pd-10IL/AC催化剂,在160 ℃和740 h-1的乙炔空速下,C2H2转化率达到98.6%,VCM选择性达到99.8%以上。包信和等[18]通过制备氮掺杂碳材料作为乙炔氢氯化反应载体,制备Pd基催化剂,研究发现氮掺杂可以减少催化剂上的碳沉积,使其比未掺杂催化剂更加稳定,而且碳结构中掺杂的氮杂原子更容易稳定Pd活性物种,从而提高Pd基催化剂的活性和长期稳定性。配体改性作为一种提高金属催化活性的方法已经在Au[19]、Ru[8, 20]等催化剂中被广泛采用,尤其是含N配体改性,可以显著提高催化活性和稳定性。1, 8-二氮杂环[5, 4, 0]十一烯-7(DBU)由于具备独特的分子结构和极强的碱性,已经被证明是一种优良的Ru基催化剂改性配体,而且其自身对HCl的强吸附和对C2H2的弱吸附也使其具备一定的乙炔氢氯化活性[21, 22]。尽管研究已经证明氮位点可以改进PdCl2催化剂的活性,稳定催化剂,但含N有机配体改性Pd基催化剂在乙炔氢氯化反应中罕见报道。
基于以上原因,我们选取DBU作为Pd基催化剂的配体,研究含N配体对Pd基催化剂催化性能的影响,通过TG、XPS、TPD、TEM等分析研究了催化剂活性、稳定性以及配体对催化剂的影响,并通过第一性原理(DFT)计算对催化机理进行理论分析。
1 实验部分 1.1 试剂与仪器椰壳炭(AC),分析纯,福建鑫森炭业;二氯化钯(PdCl2),Pd质量分数为59.5%,1, 8-二氮杂环[5, 4, 0]十一烯-7(DBU),质量分数为98%,天津希恩思奥普德科技有限公司;氢氧化钠(NaOH),分析纯,天津杰尔正化工贸易有限公司;氮气(N2),体积分数为99.999%,氢气(H2),体积分数为99.999%,乙炔(C2H2),体积分数为99.99%,天津六方工业气体经销有限公司;氯化氢(HCl),体积分数为99.9%,山东言赫化工有限公司。
1.2 催化剂的制备采用简易湿法浸渍技术制备催化剂[9]。以0.5Pd-10DBU-AC为例。首先将0.0168 g前驱体PdCl2溶于稀盐酸中,随后加入0.2 g DBU,放置超声下20 min,得到淡黄色澄清溶液。然后在其中加入1.8 g经过酸洗预处理的AC,接着将混合物超声处理60 min。随后,样品于80 ℃下保持6 h,最终在80 ℃下缓慢干燥6 h后,120 ℃下干燥处理6 h。得到的催化剂记为0.5Pd-10DBU-AC,其中Pd的质量分数为0.5%,配体的质量分数为10%。依照上述方法依次制备了不同Pd质量分数及配体含量的催化剂。另外,只制备了Pd质量分数在0.5%的无配体催化剂Pd-AC,以及只负载10%DBU的DBU-AC催化剂。
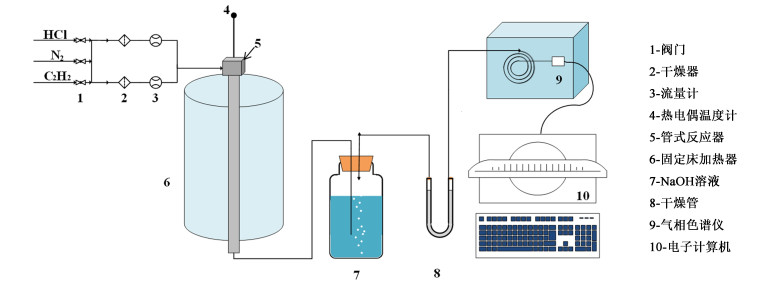
1.3 催化性能测试对催化剂活性和稳定性的评价在固定床反应器进行,评价装置如图 1所示。具体操作过程为:首先将2 mL催化剂装填入反应管中,连通管路后首先用N2在反应温度下吹扫装置60 min,后打开HCl阀门通入HCl预先活化催化剂30 min,最后通入C2H2反应气开始反应。控制反应条件为:160 ℃,乙炔空速360 h-1,HCl与C2H2流量比为1.2∶1.0。反应后的气体经过NaOH溶液吸收残余HCl气体后干燥,后通入在线气相色谱分析确定组成。C2H2转化率(XA)以及VCM选择性(SV)计算如公式(1)和公式(2)所示。
| $ X_{\mathrm{A}}=1-\varphi_{\mathrm{A}} $ | (1) |
| $ S_{\mathrm{v}}=\frac{\varphi_{\mathrm{vC}}}{1-\varphi_{\mathrm{A}}} $ | (2) |
|
| 图 1 催化活性评价装置图 Fig.1 The schematic diagram of catalytic activity evaluation equipment |
| |
式(1)和式(2)中:φA和φVC分别代表反应后气体中C2H2和VCM的体积分数。
1.4 催化剂表征催化剂的比表面积及孔结构参数由中国彼奥德公司的SSA-7000型仪器测定,采用BET方法;X射线光电子能谱(XPS)由美国Thermo公司的Nexsa型仪器测定;透射电子显微镜(TEM)图像由日本电子JEM 2100F型拍摄得到;热重分析(TG)采用德国耐驰STA 449 F5型仪器测试得到;电感耦合等离子体光谱(ICP-OES)由日本安捷伦公司ICP OES 730型仪器测试;紫外-可见分光光谱(UV-vis)由美国安捷伦的Cary Series UV-vis spectrophotometer型仪器测试。
1.5 DFT计算本研究所有理论计算都基于Gaussian09软件包实现[23]。对计算结果采取DFT-D3进行矫正[24]。结构优化在B3LYP-D3/def2-svp的计算级别下进行[25, 26],对所有优化结构进行振动分析以确定没有虚频,波函数分析在Multiwfn软件包中进行[27],采用可视化软件CYLview显示[28]。吸附能(Eads)的计算如公式(3)所示。
| $ E_{\mathrm{ads}}=E_{\mathrm{RC}}-E_{\mathrm{R}}-E_{\mathrm{C}} $ | (3) |
式(3)中:ER和EC分别为反应物和催化剂的总能量;ERC为反应物和催化剂复合结构的总能量。
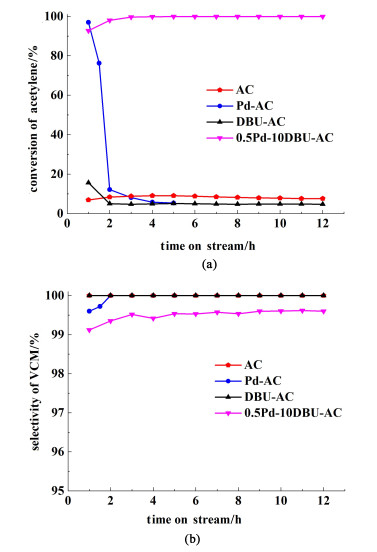
2 结果与讨论 2.1 催化性能评价首先,在160 ℃,乙炔空速为360 h-1的条件下对催化剂进行活性评价,分别测试AC、10DBU-AC、Pd-AC以及0.5Pd-10DBU-AC的活性,以此来确定DBU配体的引入对Pd基催化剂的影响,活性测试结果如图 2所示,其中纯活性炭催化转化率仅有8%,这可能是由载体本身的缺陷位点和官能团带来的[29],而DBU-AC的转化率较纯活性炭略有降低,为4%左右,这说明DBU本身活性很低,且负载后覆盖了活性炭表面的活性基团,降低了催化剂转化率。而Pd-AC初始活性很高,达到96%,但其在1 h后就下降至10%,随后更下降至5%左右,这与Pd催化高活性和极低的稳定性结果相吻合。而在DBU配体引入后,0.5Pd-10DBU-AC的活性可达到99%,并且正在12 h内转化率基本没有下降,实验结果证明DBU配体的引入可极大地提高催化剂的稳定性,这可能是由DBU中N物种与活性中心Pd之间产生的相互作用引起的。此外,所有的催化剂选择性均超过99%,证明几乎无副产物产生。值得注意的是,对于Pd-AC催化剂,我们记录了其反应前后的质量变化,由于其2 h后活性几乎完全丧失,故称量了反应前和反应2 h后的质量变化,结果为0.84 g到反应后1.23 g,其质量增加了46%,作为对比,0.5Pd-10DBU-AC催化剂反应前后质量由0.88 g增加至0.96 g,质量增加了9%,因此推测Pd基催化剂催化乙炔氢氯化失活较快可能是由于积碳导致的。
|
| 图 2 催化剂的(a)乙炔转化率XA;(b) 氯乙烯选择性SV Fig.2 (a) Conversion of acetylene and (b) selectivity to VCM of different catalysts |
| |
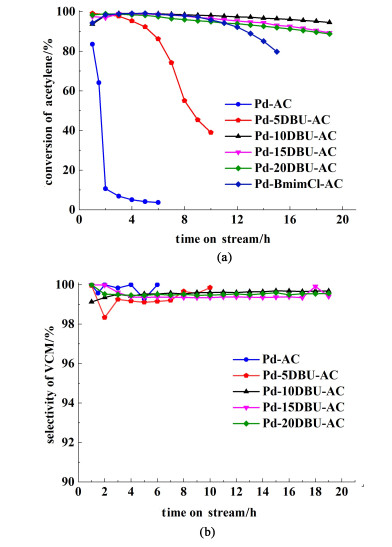
由于配体的加入可以改善催化活性,但过多的配体容易堵塞活性炭孔道,降低催化剂的性能,因此,进一步研究了不同配体添加量对催化剂活性的影响。选用一定配体浓度梯度的Pd基催化剂进行了催化性能评价,采用乙炔空速为720 h-1,结果如图 3所示。刚开始随着DBU配体含量的增加,催化剂活性和稳定性逐渐增加,当配体含量超过10%时,催化剂活性和稳定性有一定的下降,即最优的配体添加量为10%,此时催化剂转化率可达99%,且在20 h后只下降了5%。另外,所有的催化剂均表现出极佳的选择性,都超过了99%。DBU的引入可以显著提高Pd基催化剂的稳定性,且配体含量为10%时,稳定性最好。值得注意的是,对比已报道的咪唑基离子液体改性催化剂时[10],在同样制备和测试条件下,当DBU掺入量超过10%后的Pd基催化剂失活速率均优于已报到咪唑基离子液体的改性结果,说明DBU是一种极佳的Pd基催化剂改性材料。
|
| 图 3 不同DBU含量的催化剂的(a)乙炔转化率XA;(b) 氯乙烯选择性SV Fig.3 (a) Conversion of acetylene and (b) selectivity to VCM of Pd-xDBU-AC catalysts |
| |
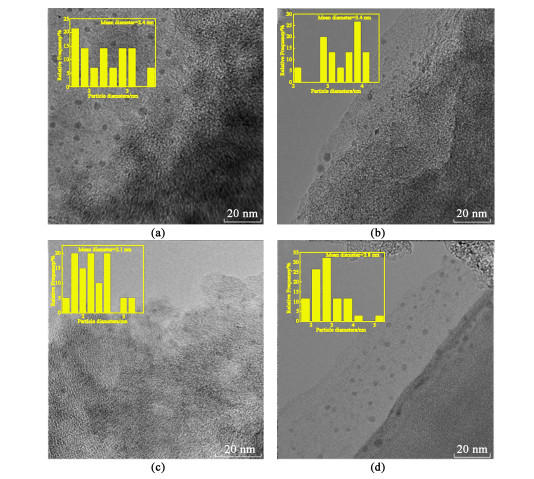
根据前人的研究[10, 30, 31],配体的引入往往会改善金属活性中心的分散程度,以此提高催化剂的活性。图 4统计了在透射电子显微镜下催化剂表面Pd颗粒的平均粒径,其中Pd-AC的平均粒径为2.4 nm,反应2 h后平均粒径增加至3.4 nm,这说明在反应过程中Pd纳米颗粒存在一定的团聚现象,这可能是Pd基催化剂迅速失活的一个原因。而对比加入配体后的催化剂,反应前粒径为2.1 nm,小于Pd-AC催化剂中Pd颗粒粒径,说明DBU配体的引入有助于Pd物种的分散,而反应20 h后0.5Pd-10DBU-AC中粒径平均为2.8 nm,尽管也存在一定的团聚现象,但远小于不加配体时的增幅,即配体的引入一定程度上可以抑制反应过程中Pd物种的团聚,从而提高Pd基催化剂稳定性。
|
| 图 4 催化剂粒径统计(a) 反应前0.5Pd-AC;(b) 反应后0.5Pd-AC;(c) 反应前0.5Pd10-DBU-AC;(d) 反应后0.5Pd-10DBU-AC Fig.4 The particle diameter distribution of (a) fresh 0.5Pd-AC; (b) used 0.5Pd-AC; (c) fresh 0.5Pd10-DBU-AC; (d) used 0.5Pd10-DBU-AC |
| |
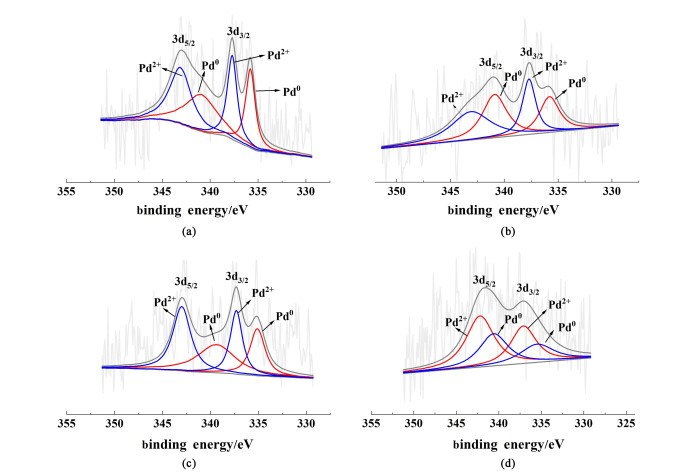
为研究Pd基催化剂中Pd组分的结构特征和价态,对新鲜的Pd基催化剂和用过的Pd基催化剂进行了XPS表征,结果如图 5所示。光谱显示了宽分辨的自旋双态,对应于Pd 3d5/2和Pd 3d3/2能级的Pd原子[11, 30]。其中,能量为337.5 eV的Pd 3d5/2为离子Pd2+的能态,另一种结合能较低的Pd态为335.1 eV,为金属Pd0物种。具体的价态分布信息列于表 1。其中,对于Pd-AC催化剂,在反应2 h后催化剂中Pd2+物种含量降低了4.5%,说明反应过程中一定量的高价Pd物种被还原了,这可能是由于乙炔等还原性气体导致的。而引入DBU配体后,反应前Pd2+物种含量与Pd-AC催化剂中含量基本相等,这说明DBU配体的引入并没有通过提高Pd2+含量而提高催化剂催化活性,这与反应刚开始时二者催化活性接近相一致。反应后0.5Pd-10DBU-AC催化剂中Pd2+物种含量较反应前还增加了6.2%,这可能是由于反应过程中HCl的活化导致的,但这也充分地证明DBU的引入有助于抑制Pd2+被还原为Pd0的过程,从而提高Pd基催化剂的稳定性。XPS的结果和催化活性实验结果相吻合,证明DBU能够稳定Pd物种价态,从而提高催化剂的稳定性。此外,新鲜的0.5Pd-10DBU-AC催化剂中Pd 3d5/2轨道电子较Pd-AC催化剂向结合能低的方向偏移约0.4 eV,这可能是DBU与Pd之间存在相互作用,增加了Pd2+的电子云密度,从而抑制了Pd2+物种的还原[32]。
|
| 图 5 不同催化剂的XPS谱图:(a) 新鲜的Pd-AC催化剂;(b) 反应后的Pd-AC催化剂;(c) 新鲜的0.5Pd-10DBU-AC催化剂;(d) 反应后的0.5Pd-10DBU-AC催化剂 Fig.5 XPS spectra and simulation of (a) fresh Pd-AC; (b) used Pd-AC; (c) fresh 0.5Pd-10DBU-AC; (d) used 0.5Pd-10DBU-AC |
| |
| Catalysts | The percentage of different Pd species/% | |
| Pd0 | Pd2+ | |
| Fresh Pd-AC | 48.7 | 51.3 |
| Used Pd-AC | 53.2 | 46.8 |
| Fresh 0.5Pd-10DBU-AC | 47.2 | 52.8 |
| Used 0.5Pd-10DBU-AC | 41.1 | 58.9 |
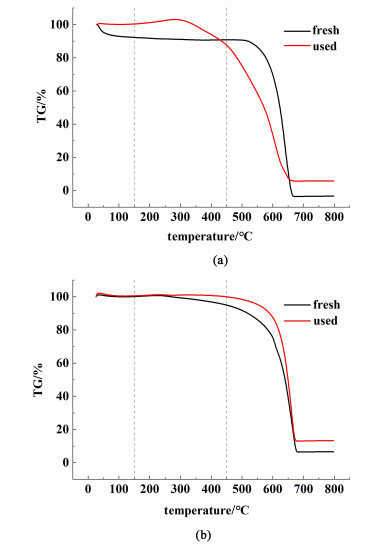
2.1中催化剂活性评价中,我们测量了催化剂反应前后的质量变化,判断积碳是Pd基催化剂失活的主要原因,对于Pd-AC催化剂,其反应后质量从0.84 g增加至1.23 g,质量增加了46%,如果增加质量全为积碳的话,其积碳量换算为31.7%。采用热重(TG)分析催化剂反应前后的积碳量。具体的分析结果如图 6所示。根据已有文献报道[10, 30, 33],认为催化剂在150~450 ℃内的质量损失为积碳燃烧。此时Pd-AC催化剂积碳量为10.6%,0.5Pd-10DBU-AC催化剂积碳量为4.5%。对于Pd-AC催化剂TG结果与催化剂质量增加数值之间存在的巨大差异,认为是由于催化剂反应后其孔道结构被大量堵塞,其内部积碳无法顺利燃烧,积碳的燃烧并没有完全体现在TG曲线150~450 ℃范围内,这也与图 6 (a)中使用后催化剂的TG失量曲线相吻合,即其积碳燃烧失量与活性炭载体燃烧失量相重合。对于Pd-AC催化剂,其使用后TG曲线在150 ℃之前没有失量,即不存在水分和小分子化合物引起的质量变化,因此,我们认为Pd-AC催化剂反应2 h后积碳量与质量增加量一致,积碳量换算为31.7%。而对于0.5Pd-10DBU-AC催化剂,其反应后的TG曲线失量分界明显,认为150~400 ℃之间的失量为其积碳的燃烧,其积碳量为4.5%。积碳结果表明,DBU配体的引入可以极大地降低催化剂的积碳量,而这也是Pd-AC催化剂失活的重要原因。
|
| 图 6 反应前后催化剂的热重分析:(a) Pd-AC;(b) 0.5Pd-10DBU-AC Fig.6 TG results of fresh and used catalysts: (a) Pd-AC; (b) 0.5Pd-10DBU-AC |
| |
通过BET测试进一步分析催化剂前后的孔结构参数变化。如表 2所示,当DBU配体引入之后,催化剂的比表面积(SBET)和总孔容(Vtotal)有所减少,说明配体成功掺入活性炭中。反应前后催化剂比表面积及总孔容的变化一定程度上可以反映催化剂的积碳程度[8, 21, 33],因此可以用比表面积和总孔容的变化比例来对比积碳程度。对于Pd-AC催化剂,其反应2 h后比表面积和总孔容分别下降98%和99%,积碳严重堵塞孔道结构。而DBU掺入催化剂反应20 h后,比表面积和总孔容只分别下降55%和48%,这说明DBU掺入后催化剂积碳的程度明显降低。BET结果与活性数据相吻合,这也侧面证明积碳是Pd基催化剂失活的重要原因。
| catalysts | SBET/(m2·g-1) | Vtotal/(cm3·g-1) | ΔS/% | ΔV/% | |||
| Fresh | Used | Fresh | Used | ||||
| Pd-AC | 1 424 | 33 | 0.81 | 0.06 | 98 | 99 | |
| 0.5Pd-10DBU-AC | 982 | 440 | 0.48 | 0.25 | 55 | 48 | |
参考之前的文献[10, 16, 17, 32],认为Pd基催化剂失活的另一重要原因是气相溶出挥发性钯乙炔配合物带来的Pd物种流失,并且流失往往达到40%以上。但是此前的文献均是以ICP-OES的结果直接判断的,并未在此过程中考虑积碳导致催化剂质量变化,从而引起Pd物种质量含量变化的影响。因此我们对反应前后的催化剂进行了ICP-OES分析,结果如表 3所示。不考虑因积碳带来的催化剂质量变化影响时,Pd-AC催化剂反应2 h后中Pd物种流失量为37.8%,而对0.5Pd-10DBU-AC催化剂,反应20 h后Pd物种流失4.0%。考虑反应前后催化剂质量变化,消除积碳影响后,Pd-AC催化剂反应后Pd物种流失为6.9%,远低于通常文献中的约50%的流失量[10, 16, 34],这意味着造成Pd基催化剂迅速失活的主要原因是积碳,Pd物种流失。而0.5Pd-10DBU-AC催化剂反应前后Pd物种无损失,证明DBU对Pd物种有锚定效果,可以提高Pd物种的稳定性。
| Catalysts | Nominal loading/% | Results of ICP/% | Loss ratio of Pd/% | Carbon deposition/% | Loss ratio of Pd After removing the effect of carbon deposition/% | |
| Fresh | Used | |||||
| Pd-AC | 0.5 | 0.43 | 0.27 | 37.81 | 31.7 | 6.9 |
| 0.5Pd-10DBU-AC | 0.5 | 0.40 | 0.38 | 4.04 | 4.5 | 0.0 |
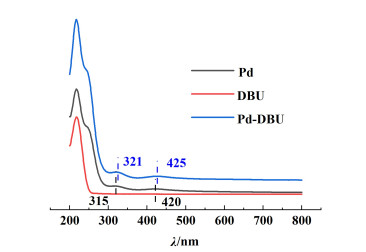
此外,通过紫外-可见分光光度法来观测Pd和DBU之间可能存在的配位。结果如图 7所示,其中321和425 nm的紫外吸收峰为钯(Ⅱ)的d-d跃迁[35-37]。在Pd-DBU的紫外谱图中,2个特征峰都有一定程度的蓝移,这也意味着Pd和DBU之间存在配位作用[38]。
|
| 图 7 Pd、DBU以及Pd-DBU的紫外吸收谱图 Fig.7 UV-vis absorption spectroscopy of Pd, DBU and Pd-DBU |
| |
上述结果已经说明Pd基催化剂失活原因及配体改性的效果,本研究用DFT模拟进一步分析Pd基催化剂失活及改性的机理,具体优化后的分子结构及吸附能如图 8所示。

|
| 图 8 分子间吸附结构及其吸附能:PdCl2吸附(a) HCl和(b) C2H2;DBU吸附(c) HCl和(d) C2H2;DBU-PdCl2团簇吸附(e) HCl和(f) C2H2;(g) DBU吸附PdCl2 Fig.8 The optimized geometries and adsorption energies of (a) HCl and (b) C2H2 absorbed on PdCl2; (c) HCl and (d) C2H2 absorbed on DBU; (e) HCl and (f) C2H2 absorbed on DBU-PdCl2; (g) PdCl2 absorbed on DBU |
| |
由图 8可以发现,PdCl2对C2H2的吸附能为117.9 kJ ·mol-1,强于对HCl的吸附能81.1 kJ ·mol-1,因此在反应过程中,PdCl2会优先吸附C2H2物种。而对于DBU配体而言,其对HCl的吸附能(91.7 kJ ·mol-1),远强于对C2H2的吸附能(35.3 kJ ·mol-1)。之前的研究表明HCl的吸附和活化是乙炔氢氯化反应的重要步骤[39, 40],在反应中如果不能及时吸附活化HCl,会导致C2H2之间的自聚引起积碳和还原高价Pd物种。此外吸附能差的绝对值|Eads(C2H2)- Eads(HCl)|与钯催化剂的稳定性呈负相关[40]。对于Pd-AC催化剂,其活性中心Pd对于HCl和C2H2的吸附能分别达到-81.1和-117.9 kJ ·mol-1,|Eads(C2H2)-Eads(HCl)|差值为36.8 kJ ·mol-1。而加入DBU后,配位结构Pd-DBU对HCl的吸附能为-110.5 kJ ·mol-1,超过了其对C2H2的吸附能-93.3 kJ ·mol-1,吸附能差值|Eads(C2H2)-Eads(HCl)|为17.2 kJ ·mol-1。这些结果表明,理论上在反应过程中,催化剂会优先吸附HCl物种,这有利于乙炔氢氯化反应的进行,避免因为C2H2过度吸附而形成积碳。值得注意的是,PdCl2和DBU之间的吸附能可以达到232.3 kJ ·mol-1,远大于Pd同C2H2的吸附能,这意味着PdCl2同DBU的配位作用强于C2H2对PdCl2的配位作用,有利于锚定Pd物种,不易产生Pd-C2H2配合物使Pd物种在反应过程中流失。
基于前线轨道理论,本研究初步讨论了Pd基催化剂乙炔氢氯化过程中的催化机理。图 9和表 4展示了反应过程中催化剂分子的最高占据轨道(HOMO)和最低未占据轨道(LUMO)的信息。根据前线轨道理论分子间电子转移规律,电子转移难易程度主要由HOMO和LUMO之间能量差来衡量,由表 4数据计算可得,C2H2的HOMO和HCl的LUMO能量差(8.50 eV)低于HCl的HOMO和C2H2的LUMO能量差(9.60 eV),这说明反应过程中电子主要倾向于从乙炔转移向氯化氢。当催化剂参与反应后,对于单纯PdCl2物种,显然其LUMO与C2H2的能量差(2.69 eV)小于与HCl的能量差(3.36 eV),即PdCl2更易接受C2H2的电子形成配位结构。而当电子从PdCl2的HOMO轨道转移时,与HCl的LUMO轨道能量更接近,即更易转移到HCl的反键轨道δ*。对于只存在DBU时,其2种轨道能量差同C2H2与HCl的轨道能量差基本接近,即单纯DBU不会降低反应中电子转移能量差,对于反应基本没有贡献,这也与前文中DBU-AC活性十分微弱的结果相一致。而当PdCl2同DBU配位时,配位分子结构的HOMO和LUMO同PdCl2的轨道结构相似,即配位后的前线轨道依然主要位于PdCl2分子附近。同时,DBU配位后Pd团簇的HOMO和LUMO能量均升高,这一方面增加了其与C2H2间电子转移能量差,也降低了其与HCl间电子转移能量差,而后者是整个电子传输过程中能量差较大的部分。电子转移能量的下降有利于乙炔氢氯化反应的发生,这从微观层面解释了DBU配体影响Pd催化反应的过程机理。

|
| 图 9 不同配位结构的前线轨道:(a) PdCl2-HOMO;(b) PdCl2-LUMO;(c) DBU-HOMO;(d) DBU-LUMO;(e) PdCl2-DBU-HOMO;(f) PdCl2-DBU-LUMO Fig.9 The frontier molecular orbital of (a) PdCl2-HOMO; (b) PdCl2-LUMO; (c) DBU-HOMO; (d) DBU-LUMO; (e) PdCl2-DBU-HOMO; (f) PdCl2-DBU-LUMO |
| |
| Molecular | The frontier molecular orbital energies/eV | |
| HOMO | LUMO | |
| HCl | -8.64 | 0.53 |
| C2H2 | -7.97 | 0.96 |
| PdCl2 | -7.72 | -5.28 |
| DBU | -5.51 | 0.91 |
| Pd-DBU | -6.15 | -3.30 |
(1) 通过湿法浸渍技术制备了DBU配位Pd基催化剂,极大地改善了Pd基催化剂活性和稳定性,优化后的催化剂0.5Pd-10DBU-AC在160 ℃,乙炔空速720 h-1,氯化氢与乙炔流量比为1.2时,转化率达到99%,20 h内只下降了5%。
(2) TEM表征结果证明DBU配体可以减缓Pd颗粒在反应过程中的团聚,XPS结果证明DBU可以稳定Pd2+物种,活性实验结果、TG、BET和ICP-OES证明Pd基催化剂失活的主要原因为积碳,配体的引入可以明显降低积碳程度,且DBU可以锚定Pd物种,抑制其在反应过程中的流失。
(3) 通过DFT计算,分析了Pd基催化剂失活和配体改性的机理,配体的引入不仅可以增强对Pd物种的吸附,阻止Pd物种流失,还可以通过增强对HCl的吸附和活化,同时削弱Pd物种向HCl提供电子的能量差,促进乙炔氢氯化反应的发生,减少积碳,计算结果与实验相一致,这也为Pd基催化剂进一步的发展提供了思路。
| [1] |
JOHNSTON P, CARTHEY N, HUTCHINGS G J. Discovery, development, and commercialization of gold catalysts for acetylene hydrochlorination[J]. Journal of the American Chemical Society, 2015, 137(46): 14548-14557. DOI:10.1021/jacs.5b07752 |
| [2] |
ZHONG J, XU Y, LIU Z. Heterogeneous non-mercury catalysts for acetylene hydrochlorination: Progress, challenges, and opportunities[J]. Green Chemistry, 2018, 20(11): 2412-2427. DOI:10.1039/C8GC00768C |
| [3] |
XU H, LUO G. Green production of PVC from laboratory to industrialization: State-of-the-art review of heterogeneous non-mercury catalysts for acetylene hydrochlorination[J]. Journal of Industrial and Engineering Chemistry, 2018, 65: 13-25. DOI:10.1016/j.jiec.2018.05.009 |
| [4] |
HUTCHINGS G. Vapor phase hydrochlorination of acetylene: Correlation of catalytic activity of supported metal chloride catalysts[J]. Journal of Catalysis, 1985, 96(1): 292-295. DOI:10.1016/0021-9517(85)90383-5 |
| [5] |
MALTA G, KONDRAT S A, FREAKLEY S J, et al. Deactivation of a single-site gold-on-carbon acetylene hydrochlorination catalyst: An X-ray absorption and inelastic neutron scattering study[J]. ACS Catalysis, 2018, 8(9): 8493-8505. DOI:10.1021/acscatal.8b02232 |
| [6] |
MALTA G, KONDRAT S A, FREAKLEY S J, et al. Identification of single-site gold catalysis in acetylene hydrochlorination[J]. Science, 2017, 355(6332): 1399-1403. DOI:10.1126/science.aal3439 |
| [7] |
CHEN Z, CHEN Y, CHAO S, et al. Single-atom AuI-N3 site for acetylene hydrochlorination reaction[J]. ACS Catalysis, 2020, 10(3): 1865-1870. DOI:10.1021/acscatal.9b05212 |
| [8] |
LI Y, WANG F, HU J, et al. A study on the rules of ligands in highly efficient Ru-amide/AC catalysts for acetylene hydrochlorination[J]. Catalysis Science & Technology, 2021, 11(22): 7347-7358. |
| [9] |
SHANG S, ZHAO W, WANG Y, et al. Highly efficient Ru@IL/AC to substitute mercuric catalyst for acetylene hydrochlorination[J]. ACS Catalysis, 2017, 7(5): 3510-3520. DOI:10.1021/acscatal.7b00057 |
| [10] |
ZHAO J, YUE Y, SHENG G, et al. Supported ionic liquid-palladium catalyst for the highly effective hydrochlorination of acetylene[J]. Chemical Engineering Journal, 2019, 360: 38-46. DOI:10.1016/j.cej.2018.11.179 |
| [11] |
WANG B, YUE Y, JIN C, et al. Hydrochlorination of acetylene on single-atom Pd/N-doped carbon catalysts: Importance of pyridinic-N synergism[J]. Applied Catalysis B-Environmental, 2020, 272. |
| [12] |
WANG B, ZHANG T, LIU Y, et al. Phosphine-oxide organic ligand improved Cu-based catalyst for acetylene hydrochlorination[J]. Applied Catalysis A: General, 2022, 630: 118461. DOI:10.1016/j.apcata.2021.118461 |
| [13] |
REN Y, WU B, WANG F, et al. Chlorocuprate(i) ionic liquid as an efficient and stable Cu-based catalyst for hydrochlorination of acetylene[J]. Catalysis Science & Technology, 2019, 9(11): 2868-2878. |
| [14] |
姚世康, 张旭斌, 王富民, 等. 稳定的钌基离子液体催化液相乙炔氢氯化[J]. 化学工业与工程, 2022, 39(4): 9-21. YAO Shikang, ZHANG Xubin, WANG Fumin, et al. A stable Ru-based ionic liquid as a catalyst for hydrochlorination of acetylene in liquid phase[J]. Chemical Industry and Engineering, 2022, 39(4): 9-21. DOI:10.13353/j.issn.1004.9533.20210337 (in Chinese) |
| [15] |
QIN G, SONG Y, JIN R, et al. Gas-liquid acetylene hydrochlorination under nonmercuric catalysis using ionic liquids as reaction media[J]. Green Chemistry, 2011, 13(6): 1495. DOI:10.1039/c1gc15041c |
| [16] |
SONG Q, WANG S, SHEN B, et al. Palladium-based catalysts for the hydrochlorination of acetylene: Reasons for deactivation and its regeneration[J]. Petroleum Science and Technology, 2010, 28(18): 1825-1833. DOI:10.1080/10916460903160842 |
| [17] |
WANG L, WANG F, WANG J. Effect of K promoter on the stability of Pd/NFY catalysts for acetylene hydrochlorination[J]. Catalysis Communications, 2016, 83: 9-13. DOI:10.1016/j.catcom.2016.04.020 |
| [18] |
LI P, DING M, HE L, et al. The activity and stability of PdCl2/C-N catalyst for acetylene hydrochlorination[J]. Science China Chemistry, 2018, 61(4): 444-448. DOI:10.1007/s11426-017-9154-x |
| [19] |
LI Y, ZHANG C, ZHANG H, et al. Effects of N-, P-, or O-containing ligands on gold-based complex catalysts for acetylene hydrochlorination[J]. Applied Catalysis a-General, 2021, 612. |
| [20] |
LI H, WU B, WANG F, et al. Achieving efficient and low content Ru-based catalyst for acetylene hydrochlorination based on N, N'-dimethylpropyleneurea[J]. Chemcatchem, 2018, 10(18): 4090-4099. DOI:10.1002/cctc.201801000 |
| [21] |
LI Y, WANG F, WU B, et al. Competing on the same stage: Ru-based catalysts modified by basic ligands and organic chlorine salts for acetylene hydrochlorination[J]. Catalysis Science & Technology, 2022, 12(16): 5086-5096. |
| [22] |
DONG X, LIU G, CHEN Z, et al. Activated carbon supported nitrogen-containing diheterocycle mercury-free catalyst for acetylene hydrochlorination[J]. Molecular Catalysis, 2022, 525: 112366. DOI:10.1016/j.mcat.2022.112366 |
| [23] |
FRISCH G W T, SCHLEGEL H B, SCUSERIA G E, et al. GAUSSIAN 09 (Revision D.01)[M]. Wallingford Ct: Gaussian, Inc., 2016.
|
| [24] |
GRIMME S, ANTONY J, EHRLICH S, et al. A consistent and accurate ab initio parametrization of density functional dispersion correction (DFT-D) for the 94 elements H-Pu[J]. The Journal of Chemical Physics, 2010, 132(15): 154104. DOI:10.1063/1.3382344 |
| [25] |
MIEHLICH B, SAVIN A, STOLL H, et al. Results obtained with the correlation energy density functionals of Becke and Lee, Yang and Parr[J]. Chemical Physics Letters, 1989, 157(3): 200-206. DOI:10.1016/0009-2614(89)87234-3 |
| [26] |
EICHKORN K, WEIGEND F, TREUTLER O, et al. Auxiliary basis sets for main row atoms and transition metals and their use to approximate Coulomb potentials[J]. Theoretical Chemistry Accounts, 1997, 97(1): 119-124. |
| [27] |
LU T, CHEN F. Multiwfn: A multifunctional wavefunction analyzer[J]. Journal of Computational Chemistry, 2012, 33(5): 580-592. DOI:10.1002/jcc.22885 |
| [28] |
ABBOTT A P, CAPPER G, DAVIES D L, et al. Ionic liquids based upon metal halide/substituted quaternary ammonium salt mixtures[J]. Inorganic Chemistry, 2004, 43(11): 3447-3452. DOI:10.1021/ic049931s |
| [29] |
LIU Y, ZHANG H, DONG Y, et al. Characteristics of activated carbons modulate the catalytic performance for acetylene hydrochlorination[J]. Molecular Catalysis, 2020, 483. |
| [30] |
LONG Z, WANG L, YAN H, et al. Design of choline chloride modified USY zeolites for palladium-catalyzed acetylene hydrochlorination[J]. RSC Advances, 2022, 12(16): 9923-9932. DOI:10.1039/D2RA01142E |
| [31] |
HE H, ZHAO J, WANG B, et al. Design strategies for the development of a Pd-based acetylene hydrochlorination catalyst: Improvement of catalyst stability by nitrogen-containing ligands[J]. RSC Advances, 2019, 9(37): 21557-21563. DOI:10.1039/C9RA02572C |
| [32] |
WANG L, WANG F, WANG J. Enhanced stability of hydrochlorination of acetylene using polyaniline-modified Pd/HY catalysts[J]. Catalysis Communications, 2016, 74: 55-59. DOI:10.1016/j.catcom.2015.10.027 |
| [33] |
HU J, WANG F, LI Y, et al. Enhanced catalytic performance of oxidized Ru supported on N-doped mesoporous carbon for acetylene hydrochlorination[J]. Applied Catalysis a-General, 2021, 623. |
| [34] |
ZHANG M, WANG L, YAN H, et al. Palladium-halloysite nanocomposites as an efficient heterogeneous catalyst for acetylene hydrochlorination[J]. Journal of Materials Research and Technology, 2021, 13: 2055-2065. DOI:10.1016/j.jmrt.2021.06.006 |
| [35] |
BON V V, ORYSYK S I, PEKHNYO V I, et al. Synthesis and spectroscopic investigations of Rh(Ⅲ) and Pd(Ⅱ) complex compounds with N-(pyridine-2-yl)morpholine-4-carbothioamide[J]. Polyhedron, 2007, 26(13): 2935-2941. DOI:10.1016/j.poly.2007.01.042 |
| [36] |
CORBI P P, CAGNIN F, MASSABNI A C. Chemical and spectroscopic studies of a new palladium(Ⅱ) complex with N-acetyl-L-cysteine[J]. Journal of Coordination Chemistry, 2008, 61(22): 3666-3673. DOI:10.1080/00958970802108809 |
| [37] |
何武强. 硼氢化钠还原氯钯酸制备纳米钯[J]. 河北化工, 2010(12): 28-29. HE Wuqiang. Prepare palladium nano acid by sodium borohydride reduction of palladium chloride[J]. Hebei Chemical Engineering and Industry, 2010(12): 28-29. (in Chinese) |
| [38] |
CAI M, ZHANG H, MAN B, et al. Synthesis of a vinyl chloride monomer via acetylene hydrochlorination with a ruthenium-based N-heterocyclic carbene complex catalyst[J]. Catalysis Science & Technology, 2020, 10(11): 3552-3560. |
| [39] |
胡嘉琦, 王富民, 张旭斌. 氮氧吡啶-钌基催化剂催化乙炔氢氯化的研究[J]. 化学工业与工程, 2023, 40(4): 1-14. HU Jiaqi, WANG Fumin, ZHANG Xubin. Study on Ru-based catalysts coordinated with pyridine N-oxide for acetylene hydrochlorination[J]. Chemical Industry and Engineering, 2023, 40(4): 1-14. DOI:10.13353/j.issn.1004.9533.20210342 (in Chinese) |
| [40] |
CEN Y, YUE Y, WANG S, et al. Adsorption behavior and electron structure engineering of Pd-based catalysts for acetylene hydrochlorination[J]. Catalysts, 2019, 10(1): 24. DOI:10.3390/catal10010024 |
 2023, Vol. 40
2023, Vol. 40





