1. 河北工业大学化工学院/海水资源高效利用化工技术教育部工程硏究中心,天津 300130;
2. 河北省现代海洋化工技术协同创新中心,天津 300130;
3. 河北工业大学化工学院/化工节能过程集成与资源利用国家-地方联合工程实验,天津 300130
收稿日期: 2022-02-19; 修改日期: 2022-03-17
基金项目: 河北省重点研发计划项目(19274003D)
作者简介:
杨婷,(1997-),女,硕士研究生,现从事资源利用及环保方面的研究.
Research on resource utilization technology of saline wastewater in antibiotic production
1. School of Chemical Engineering, Hebei University of Technology, Engineering Research Center for Chemical Technology of the Efficient Utilization of Seawater Resources, Tianjin 300130, China;
2. Collaborative Innovation Center of Hebei Modern Marine Chemical Technology, Tianjin 300130, China;
3. School of Chemical Engineering, Hebei University of Technology, Chemical Energy Conservation Process Integration and Resource Utilization National-Local Joint Engineering Laboratory, Tianjin 300130, China
抗生素生产中产生的含盐废水作为一种典型的制药废水,不仅含盐度高,且含有大量有机物,甚至是有毒物质。近年来,因抗生素废水未经妥善处理后排出,对水体中的微生物及水生动植物造成了严重危害[1, 2]。因此,如何妥善处理含抗生素废水已成为关乎人类健康和命运的重要问题[3]。目前高盐水处理技术主要为膜法和蒸发法,膜法(如纳滤、微滤、超滤、反渗透)处理过程中会额外引入二次污染物,同时系统本身会产生高盐度的浓水;蒸发法是将含盐废水通过外加热源进行蒸发浓缩、结晶分离,从而实现回收冷凝水、最大减量化的目的,但该技术需要外加热源,能耗较高。机械式蒸汽再压缩技术(Mechanical vapor recompression,MVR),是利用蒸发系统自身产生的二次蒸汽及其能量,将低品位的蒸汽经压缩机的机械做功提升为高品位的蒸汽热源,如此循环向蒸发系统提供热能,从而减少对外界能源的需求。在高盐废水处理中,MVR技术常与其他方法形成组合工艺,从而达到高盐废水处理的较佳效果[4]。对于含盐废水中组分盐的回收利用,国内在技术能耗[5, 6]、成本[7]、再利用和环境危害等方面的研究仍有待提升。本研究设计“MVR蒸发+冷却结晶”组合工艺对抗生素生产中含盐废水进行处理,旨在回收NaCl和KCl,以实现对废水进行深度处理和资源化利用。本研究重点考察了不同蒸发温度和不同蒸发水量条件对获得NaCl和KCl的效果与质量,以期为抗生素生产中含盐废水的资源化利用提供参考。
1 实验材料与方法
1.1 实验仪器与试剂
集热式恒温加热磁力搅拌器(DF-101S)、电热鼓风干燥箱(FCD-3000)、台式过滤离心机(TD5G)、X射线衍射仪(D8 Discover)、红外光谱仪(TENSOR 27);某制药厂青霉素生产废水、四苯基硼酸钠、十六烷基三甲基溴化铵、硝酸银。
1.2 实验分析方法
采用红外光谱、X射线衍射(XRD)、化学滴定等分析表征法。
1.3 条件实验步骤
1.3.1 条件实验实施主要理论依据
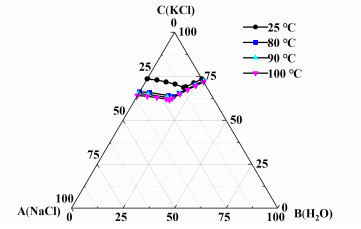
依据25、80、90和100 ℃条件下K+,Na+//Cl--H2O三元体系相平衡数据[8],绘制相图,如图 1所示。借助相图,由初始物料组成进行计算,得出80 ℃下NaCl和KCl共饱点对应单位质量原料液中理论蒸发去水质量与理论含水质量之比为81.04%,结合实际实验操作,选择蒸水量条件为73.00%~86.00%;在90 ℃条件下,NaCl和KCl共饱点对应为81.55%,选择蒸水量条件为73.00%~86.00%;在100 ℃条件,NaCl和KCl共饱点对应为81.74%,选择蒸水量条件为78.00%~87.00%。
1.3.2 实验工艺流程
实验整体工艺流程如图 2所示,蒸发去除部分水后保温沉降,过滤所得粗盐(粗NaCl),用饱和NaCl溶液(洗盐液)洗涤分离得产品盐(精NaCl)。过滤所得清液进行冷却,析出固体后过滤得粗钾(粗KCl),使用饱和KCl溶液(洗钾液)洗涤,分离得产品钾(精KCl);析钾母液回头进入蒸发工段,洗液成分达到NaCl或KCl饱和浓度后,将洗水回头进入蒸发工段,进行钠、钾分离。
1.3.3 实验具体操作步骤
根据某制药厂废水化学组成配制模拟废水进行蒸发实验。称取2 kg模拟废水置于搪瓷杯中,分别在80、90和100 ℃条件下常压恒温蒸发,蒸发水量分别控制为73.00%~87.00%、78.00%~86.00%、78.00%~88.00%。将蒸发浓缩后的母液恒温沉降5 min,迅速保温过滤获得粗盐和清液。粗盐用质量比1∶1的饱和NaCl洗涤,固液分离得到精NaCl;清液冷却至室温(25 ℃),过滤得到粗KCl,经质量比为1∶1的饱和KCl溶液洗涤后,得到精KCl。洗盐液和洗钾液饱和后回头蒸发。对精NaCl和精KCl进行分析,考察主要成分含量。
1.4 实验数据处理过程
| We=(G0−Gt)/(G0ED)×100% |
(1) |
式(1)中:We为水分蒸发量,%;G0为初始模拟废水的质量,kg;Gt为t时刻模拟废水的质量,kg;ED为原始废液中水分质量占比,%(化学滴定后求得)。
2 实验结果与讨论
2.1 原料初步检测结果
2.1.1 废水红外光谱
将某制药厂青霉素生产废水进行红外光谱分析,所得谱图如图 3所示。从图 3(b)可以得出,3 413 cm-1处的峰可能为O—H基的伸缩振动或是—NH2的反对称伸缩振动峰;2 925 cm-1可能是CH3的C—H伸缩振动或是—CH2—的反对称伸缩振动;1 645 cm-1可能为C C伸缩振动,由于3 100~3 000 cm-1和1 000~650 cm-1未出现苯环C C的特征吸收峰,所以由此推断为普通烯烃C C;1 483 cm-1为CH2的C—H弯曲振动;1 020 cm-1可能是—OH弯曲振动伴随着C O伸缩振动或是S—O的反对称伸缩振动;576 cm-1可能是PO43-面内弯曲振动。经过红外光谱的分析后推测该废水中可能含有醇类、酚类、胺类、硫酸盐、磷酸盐和有机酸类物质[9-12]。
2.1.2 废水烘干物的XRD结果
为进一步了解废水中的主要成分,测得某制药厂废水经过烘干后固体的XRD图谱如图 4所示。
由图 4可知,烘干物的XRD结果与NaCl和KCl标准峰基本吻合,证实废水中的无机盐成分以NaCl和KCl为主。NaCl的峰最高,说明NaCl晶相含量应当相对要高;图 4中的衍射峰峰型尖锐,表明NaCl和KCl的结晶度较好[13, 14]。
2.1.3 化学滴定结果
为获得废水中NaCl和KCl的精确含量,对废水进行化学滴定。测定结果为C(K+)=12.68 g·L-1,C(Cl-)=51.74 g·L-1,推算出C(NaCl)=66.25 g·L-1(由Cl-和K+浓度近似推算),C(KCl)=24.21 g·L-1。
2.2 产品盐检测结果
图 5所示为粗盐、产品NaCl和KCl的XRD图谱,与NaCl和KCl的标准卡片进行对比,发现粗盐的主要成分为NaCl,但含有一部分KCl;而产品NaCl中并未发现KCl的衍射峰,可以证明产品NaCl的纯度较高,具体是否达到国家标准可通过化学滴定进一步证实。产品KCl的峰型尖锐且与KCl衍射峰高度吻合,说明在经过洗钾液洗涤后的产品KCl纯度和结晶度均较高[15]。
2.3 不同温度下模拟废水蒸发实验结果
2.3.1 不同蒸发温度条件下的最适宜蒸水量
表 1为青霉素模拟废水分别在80、90和100 ℃下常压恒温蒸发的实验结果。
表 1 模拟废水在不同温度(80、90和100 ℃)下的蒸发实验结果
Table 1 Experimental results of simulated waste water evaporation at different temperatures (80, 90, 100 ℃)
| We/% |
80 ℃ |
| 90 ℃ |
| 100 ℃ |
| C(NaCl)/% |
YNaCl/% |
YKCl/% |
| C(NaCl)/% |
YNaCl/% |
YKCl/% |
| C(NaCl)/% |
YNaCl/% |
YKCl/% |
| 79.00(±0.50) |
85.27 |
94.91 |
93.41 |
| 87.73 |
97.23 |
91.79 |
| 95.11 |
96.72 |
92.66 |
| 81.00(±0.50) |
95.50 |
95.37 |
95.18 |
| 95.61 |
96.85 |
91.44 |
| 95.41 |
95.07 |
94.61 |
| 83.00(±0.50) |
88.49 |
95.18 |
93.94 |
| 83.19 |
97.17 |
91.58 |
| 91.00 |
96.31 |
90.86 |
| 85.00(±0.50) |
78.32 |
95.43 |
93.04 |
| 77.18 |
96.70 |
90.86 |
| 83.84 |
92.24 |
90.70 |
| 注:CKCl—粗盐/母液中KCl含量,质量分数(化学滴定测得);CNaCl—粗盐/母液中NaCl含量,质量分数(化学滴定测得);YNaCl—NaCl纯度,质量分数(实际精NaCl质量/理论精NaCl质量);YKCl—KCl纯度,质量分数(实际精KCl质量/理论精KCl质量)。 |
如表 1所示,在80、90和100 ℃下,蒸发量为(78.00±0.50)%~(85.00±0.50)%时,所得精NaCl质量分数维持在92.24%~97.23%,精KCl质量分数维持在90.86%~95.41%,多数满足工业盐国家标准(GB/T 5462—2015)中工业湿盐一级品主指标要求[16],即NaCl(g/100 g)≥95.00,KCl国家标准(GB/T 7118—2008)中一级品主指标,即KCl(g/100 g)≥90.00[17]。在考察的3个温度下,随着蒸水量的增加,蒸发所得的粗盐中NaCl含量均呈现先升高后降低的趋势;在蒸发量为(81.00±0.50)%时粗盐中NaCl的含量最高,80、90和100 ℃的粗盐NaCl最高含量分别为95.50%、91.61%和95.41%,此时粗盐中KCl含量最低,即在此蒸水量下NaCl和KCl的分离效果最好。根据相图(图 1)可知,80 ℃时NaCl和KCl共饱和点对应理论蒸水量为81.04%,即蒸发水量为81.04%时NaCl分离效果最好。同理,结合90和100 ℃的对应理论蒸水量为81.55%和81.74%,通过条件实验的探索,确定优选实验条件为(81.00±0.50)%。
当蒸水量超过81.50%时,在粗盐母液中冷却结晶得到的粗KCl较少(80 ℃析出13.00 g,90 ℃析出10.00 g,100 ℃析出5.00 g),这是由于在高温蒸发下,废水在结束蒸发转移过程中降温速度较快,KCl因温度下降而直接在粗盐中产生结晶,导致粗盐母液中KCl析出较少。此时考虑使用辅助加热过滤的方式,以减少在转移过程因降温导致的KCl析出,以达到预期分离效果。
2.3.2 不同温度下的NaCl收率
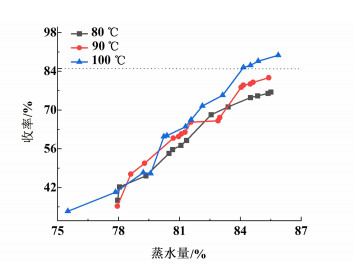
在废水资源化利用过程中,不仅需要考虑分离效果[Y(NaCl)≥95.00%,Y(KCl)≥90.00%],同时要选择获得NaCl收率较高(收率≥85.00%)的蒸水量和蒸发温度,所以对不同蒸发温度下的NaCl收率进行了统计分析,所得结果见图 6。
如图 6所示,在3个温度下,随着蒸水量的升高,NaCl的收率皆呈上升趋势;80 ℃时NaCl收率在共饱和点对应蒸水量81.04%之前上升缓慢,之后变化幅度较大,分析其缘由是析出的粗盐质量越来越多,其所含的NaCl质量也在逐步提升,故NaCl的收率上升幅度较大。90 ℃时的情况同80 ℃基本一致。100 ℃时的NaCl收率一直平稳上升,且100 ℃下的NaCl收率大于80和90 ℃,原因是100 ℃时析出的粗盐质量相对较多,因此NaCl收率相应会增加。如图 6可知,在蒸水量为84.15%~85.86%之间时,100 ℃下的NaCl收率维持在85.00%~89.00%之间,相比80 ℃和90 ℃能更快满足收率85.00%的要求。
2.3.3 能耗估算
实现废水资源化利用的同时,更需要结合实际生产过程考虑经济性和节能性,由此探究了在不同的温度下的能耗差异。根据式(2)和式(3)进行计算,比较80 ℃、90 ℃和100 ℃下的能耗差异。
式(2)和式(3)中:F为溶液加料量,kg·s-1;W为单位时间水分蒸发量,kg·s-1;w0和w为料液与完成液(产物)的溶质质量分数,%;D为加热蒸汽消耗量,kg·s-1;r0为加热蒸汽的汽化热,J·g-1,t0和t为加料液与完成液的温度,℃;r1为二次蒸汽的汽化热,J·g-1。
定义W/D为每千克加热蒸汽所蒸发的水量(kg)为加热蒸汽的经济性,以此衡量蒸发过程的能耗[18]。计算出80、90和100 ℃的能耗(经济性)分别为0.79、0.80和0.82,即随着蒸发温度的升高,能耗在增大,100 ℃下的能耗最高。
2.4 优选操作条件下的母液循环实验
由图 6与能耗估算可知,在3个温度下,100 ℃条件下虽然能够得到最佳粗盐收率,但是相对而言能耗也最高,考虑到在实验过程中析钾母液在过滤出产品盐后就未参与后续步骤,以及在使用饱和溶液洗涤后也无其他应用。最终选用90 ℃作为蒸发温度,将析钾母液以及洗水与废水进行循环。参考图 6中90 ℃未进行循环时蒸水量(81.50±0.50)%下NaCl收率未达到85.00%要求的情况,加入母液和洗水进行循环蒸发,通过相图计算确定了在母液循环操作模式下以90 ℃和85.00%蒸水量进行模拟废水的蒸发实验。
表 2为90 ℃下将模拟废水(起始循环母液蒸水量为83.80%下所得)进行母液循环的实验结果,证实了90 ℃下蒸水量为(85.00±0.50)%的循环实验能够满足NaCl收率高于85.00%,且能耗相较于100 ℃更低。由表 2的母液循环结果可知,在90 ℃下蒸水量维持在85.80%~87.07%时,NaCl收率维持在87.39%~91.94%,NaCl质量分数基本达到95.00%以上,KCl质量分数在90.32%~92.17%;在90 ℃下循环蒸水量约为(85.00±0.50)%时,NaCl的收率为88.64%,NaCl和KCl的质量分数都达到了国家标准要求。实验结果证明,在(85.00±0.50)%蒸水量下进行母液循环时能够在满足最低能量消耗和最佳分离效果的前提下,同时达到预期指标要求:NaCl收率≥85.00%,w(NaCl)≥95.00%,w(KCl)≥90.00%。
表 2 90 ℃下母液循环实验结果
Table 2 Experimental results of mother liquor circulation conditions at 90 ℃
| 循环实验次数 |
We/% |
母液加入量 |
| 母液滤出量 |
| 粗盐 |
FNaCl/% |
YNaCl/% |
YKCl/% |
| m/g |
C(NaCl)/% |
C(KCl)/% |
| m/g |
C(NaCl)/% |
C(KCl)/% |
| m/g |
C(NaCl)/% |
C(KCl)/% |
| 1 |
86.52 |
159.80 |
20.67 |
10.23 |
| 160.00 |
17.54 |
11.64 |
| 146.80 |
79.23 |
14.97 |
87.78 |
95.67 |
91.15 |
| 2 |
86.97 |
154.88 |
17.54 |
11.64 |
| 158.80 |
17.51 |
11.74 |
| 157.20 |
78.48 |
19.80 |
88.65 |
94.55 |
90.56 |
| 3 |
86.81 |
153.30 |
22.51 |
11.74 |
| 152.12 |
16.85 |
11.66 |
| 155.10 |
79.19 |
19.54 |
91.33 |
95.82 |
91.44 |
| 4 |
85.80 |
147.30 |
16.85 |
11.66 |
| 172.20 |
21.56 |
12.84 |
| 137.90 |
85.07 |
10.05 |
88.64 |
95.80 |
90.61 |
| 5 |
86.05 |
168.10 |
21.56 |
12.84 |
| 168.73 |
20.96 |
12.15 |
| 144.73 |
80.67 |
13.98 |
87.39 |
96.24 |
92.17 |
| 6 |
87.07 |
163.62 |
20.96 |
12.15 |
| 155.10 |
17.14 |
10.89 |
| 160.40 |
75.95 |
20.01 |
91.94 |
95.11 |
90.32 |
| 7 |
86.73 |
150.40 |
17.14 |
10.89 |
| 157.44 |
17.21 |
11.89 |
| 150.30 |
79.86 |
18.41 |
90.58 |
94.98 |
90.40 |
3 结论
通过红外光谱、XRD、化学滴定确定了废水的主要成分;根据K+,Na+//Cl--H2O体系相图以及废水初始物料组成计算得到获得KCl和NaCl的理论蒸发水量,并进行了实验验证;考察了蒸发温度和蒸水量对蒸发效果的影响,确定了最适宜蒸发条件。从工艺的探究过程和实验结果可以得出以下结论:(1)从节能减排的角度考虑,采用母液循环的操作模式进行废水中盐的回收,所得NaCl和KCl产品纯度均能达到国家标准的指标要求,即NaCl(g/100 g)≥95.00、KCl(g/100 g)≥90.00,且整个生产过程无废液排放。(2)通过实验确定了最适宜操作条件:蒸发温度为90 ℃、蒸水量为(85.00±0.50)%、结晶温度为25 ℃。研究结果可为含盐废水的资源化利用提供指导和参考。
 2023, Vol. 40
2023, Vol. 40