2. 天津大陆制氢设备有限公司, 天津 301609
2. Tianjin Mainland Hydrogen Equipment Co., Ltd., Tianjin 301609, China
开发清洁的可再生能源是应对全球变暖与化石能源短缺危机的有效途径[1]。氢具有燃烧热值高、清洁无污染等特点,是未来最有可能替代化石燃料的零碳能源载体[2, 3]。在众多的制氢技术中,电解水制氢技术可以利用太阳能、风能、水等可再生能源[3],生产过程高效环保,具有广阔的发展前景。目前,较为成熟电解水制氢技术是质子交换膜电解水(PEMWE)和碱性电解水(AWE)。PEMWE电解效率高,产氢纯度高,但需使用资源短缺的贵金属催化剂,这限制了PEMWE的大规模使用。相较之下,AWE能以非贵金属作为催化剂,极大降低制氢成本[4, 5],已成为当前备受关注的电解水技术。
隔膜是碱性电解槽的核心组件,主要作用是分隔阴阳两极和传导离子[6]。因此,一般要求隔膜具有良好的离子传递能力、化学稳定性、阻气性和机械稳定性。最早用于碱性电解槽的石棉隔膜因致癌性和在高温碱液中不稳定等问题被限制使用。为了开发石棉替代品,同时也为了进一步提高隔膜的性能,多孔陶瓷[7, 8]、聚合物膜[9-12]、阴离子交换膜[13-16]和离子溶剂化膜[17-19]等已被广泛研究。其中,阴离子交换膜成为近年来的研究热点。阴离子交换膜阻隔气体的性能优异,但离子导电率低和在高温碱液中易降解是其发展面临的主要挑战。相比而言,多孔隔膜,尤其是包括Zirfon UTP-500膜和聚苯硫醚隔膜在内的商业化隔膜不仅耐腐蚀性好而且离子电导率较高,但大孔隙和高孔隙率导致其阻气性较差[20, 21]。
聚苯硫醚(PPS)、聚四氟乙烯(PTFE)和聚砜(PSU)具有出色的碱稳定性,被视为碱性电解水隔膜的优选材料。然而,这些聚合物膜亲水性差,容易导致气泡粘附,不仅使溶液电阻增加,电解效率降低,而且加剧气体交叉,易引发爆炸危险。为解决这一难题,近些年,不少学者开展了新型复合隔膜的研究,并取得了一些进展。Stojadinovic等[22]将硫酸钡(BaSO4)沉淀至聚苯硫醚膜表面,制备了BaSO4/PPS复合隔膜,Cho等[23]采用共混法制备了纤维素纳米晶体(CNCs)/ZrO2/PSU复合隔膜,这些复合膜的离子电导率和阻气性都优于Zirfon PERL膜,但无机盐在膜表面易脱落和纳米颗粒的团聚问题尚存。Wang等[24]采用以PTFE为基底,以层状双金属氢氧化物(LDH)作为填充物,利用多孔填充法制备了PTFE/LDH复合膜,LDH赋予了复合膜低面电阻、高耐碱性和超亲水表面,但电解产生的气体纯度不高。
PVA是典型的凝胶材料,具有优异的亲水性、柔韧性、阻气性和化学稳定性,已被广泛用于燃料电池、锌空气电池和电容器等领域[25-27]。Kim等[28]采用超声波喷涂法在Zirfon PERL膜表面形成交联PVA表层,降低了气体渗透率,同时面电阻无大幅增加。本研究采用多孔填充策略,以多孔PPS无纺布为基膜,以PVA作为凝胶填充物,利用刮涂法将PVA完全填充至基膜孔隙内,通过化学交联,制备出PVA填充PPS交联复合膜。PVA填充PPS交联复合膜表现出高离子传导率、低气体渗透率和良好的碱稳定性。
1 实验部分 1.1 实验材料聚苯硫醚无纺布(厚90~100 μm,孔隙率为70%)来自东丽纤维研究所(中国)有限公司。聚乙烯醇树脂(PVA-124,醇解度99%,平均聚合度2 400~2 500,可乐丽)购自国药集团化学试剂有限公司。戊二醛(GA,50%水溶液)购自上海阿拉丁生化科技股份有限公司。丙酮(CH3COCH3)为分析纯,购自天津市大茂化学试剂厂。氢氧化钾(KOH)、无水甲醇(CH3OH)、无水乙醇(CH3CH2OH)均为分析纯,均购自天津市科密欧化学试剂有限公司。盐酸(HCl,36%~38%)为分析纯,购自天津市利安隆博华医药化学有限公司。Nafion溶液(D-520,杜邦)、Pt/C催化剂(20% Pt,Johnson Matthey)、去离子水(≥3 MΩ×cm)购自天津市永清源蒸馏水经营部。Zirfon UTP-500膜[厚度:500(±20) μm]购自AGFA公司。
1.2 PVA填充PPS交联复合膜的制备PVA填充PPS交联复合膜采用刮涂法制备。依次使用丙酮、乙醇、去离子水对聚苯硫醚无纺布进行超声清洗15 min,去除其孔隙中残留的添加剂和气泡,干燥后作为基膜。取2.0 g PVA添加到18 g去离子水中,在90 ℃下磁力搅拌4 h,混合均匀后,静置一夜脱气泡,配成10%的凝胶态铸膜液。将基膜铺展在干净的水平玻璃板上,用刮刀将铸膜液均匀刮涂在基膜外表面,使铸膜液充分浸润到基膜的孔隙之中,80 ℃干燥至恒质量,重复刮涂、干燥步骤3次,使凝胶完全填充至基膜孔隙内。将干燥后的填充复合膜从水平玻璃板上揭下,浸泡在含0.12%盐酸、7%戊二醛的甲醇溶液(交联溶液)中,在40 ℃下交联反应1.5 h,取出复合膜用去离子水中洗去膜表面残留的交联溶液,经80 ℃真空干燥后,得到PVA填充PPS交联复合膜(PPS-PVA)。
1.3 PVA交联膜的制备PVA交联膜采用溶液浇铸法制备。取2.0 g PVA添加到38 g去离子水中,在90 ℃下磁力搅拌4 h,混合均匀后,静置一夜脱气泡,配成质量分数为5%的铸膜液。取8.0 g铸膜液缓缓倒入水平玻璃膜池,于60 ℃干燥12 h取出。将干燥后的PVA膜从玻璃膜池上揭下,依照同样的方法,浸泡在上述交联溶液中,在40 ℃下交联反应1.5 h后取出,洗去膜表面残留的交联溶液,经80 ℃真空干燥后,得到PVA交联膜(PVA)。
1.4 表征与测试采用场发射扫描电子电镜(FESEM, Regulus 8100, Japan)对样品膜的表面和断面微观形貌进行观察。其中,样品在液氮中冷冻脆断以获得新鲜的膜断面,所有样品在测试前均进行喷金处理。
将干燥的样品膜切成约2 cm×1 cm的矩形,测量样品膜的长边边长、厚度和质量。将膜浸泡在不同温度的20% KOH中24 h后,取出样品膜,迅速用滤纸擦除附着在膜表面的液体,并测量湿态样品膜的长边边长、厚度和质量。样品膜的吸液率(WU)和溶胀率(SR)数据可由下列公式计算得到:
| $ W_{\mathrm{U}}=\frac{W_{\mathrm{w}}-W_{\mathrm{d}}}{W_{\mathrm{d}}} \times 100 \% $ | (1) |
| $ S_{\mathrm{R} 1}=\frac{L_{\mathrm{w}}-L_{\mathrm{d}}}{L_{\mathrm{d}}} \times 100 \% $ | (2) |
| $ S_{\mathrm{R} 2}=\frac{T_{\mathrm{w}}-T_{\mathrm{d}}}{T_{\mathrm{d}}} \times 100 \% $ | (3) |
式(1)~(3)中:Ww和Wd分别为样品膜湿态和干态的质量;SR1为水平方向膜的溶胀率;Lw和Ld为样品膜湿态和干态的长边边长;SR2为垂直方向膜的溶胀率;Tw和Td为样品膜湿态和干态的厚度。
使用四电极测试体系[29],利用交流阻抗法测试膜在KOH溶液中的离子电导率。裁剪一张2 cm×2 cm的样品膜放入20% KOH溶液中,浸泡24 h后取出,用数显千分尺测厚规测量膜厚,将膜夹在H型电池之间(直径1.5 cm),用硅橡胶垫片进行密封,向池中加满20% KOH溶液,排除气泡。每个半电池包含1个泡沫镍电极和1个连接到饱和甘汞参比电极的玻璃鲁金毛细管,且毛细管尖端靠近膜放置。使用电化学工作站(PARSTAT 2273, AMETEK)在10 mV的振荡电压、2 MHz到1 Hz的频率扫描下测试阻抗R1。测试完毕,取出样品膜,测试2根鲁金毛细管之间的溶液阻抗R0。使用公式(4)计算离子电导率σ,使用公式(5)计算膜的面电阻Rs。
| $ \sigma=\frac{\delta}{R_{\mathrm{s}} A} $ | (4) |
| $ R_{\mathrm{s}}=A\left(R_1-R_0\right) $ | (5) |
式(4)~(5)中:σ是电导率mS·cm-1;δ是膜的厚度,cm;Rs是膜的面电阻mΩ·cm2;R1是夹膜时测的阻抗,mΩ;R0是去膜时测的溶液阻抗; A是有效膜面积,cm2。
为了考察膜的碱稳定性,裁剪2 cm×1 cm的干膜样品,称质量后,浸泡在装有30% KOH溶液的密封聚丙烯塑料盒中,每隔4 d换1次新鲜的碱液,每间隔一段时间取出样品膜,用去离子水清洗至中性,干燥后称质量,并测量膜的长边边长和厚度。膜的溶胀率数据可由公式(2)和公式(3)计算得到,膜中PVA的质量变化率(RW)可由式(6)计算。
| $ R_{\mathrm{W}}=\frac{w_1-w_2}{w_1} \times 100 \% $ | (6) |
式(6)中w1和w2分别为浸泡碱液前后干膜中PVA的质量。
用配备有衰减全反射(ATR)附件的傅里叶变换红外光谱仪(FTIR-650型,天津港东)对浸泡60 ℃、30% KOH溶液不同时间的PPS-PVA膜进行表征。测试样品均是从碱液中取出后用去离子水清洗至中性再经过干燥所得。每个样品扫描32次,分辨率为4 cm-1,光谱范围为4 000~650 cm-1。
将在去离子水中浸泡至饱和态的湿膜切成3 cm×1 cm的矩形样品,室温下通过MUF-1050型万能拉伸试验机以5 mm·min-1的拉伸速率测量膜的拉伸强度。
采用电化学方法[30]测量膜的氢气渗透率。氢气渗透率是由氢氧化反应(HOR)极限电流确定的。取0.08 g Pt/C催化剂,加入40 μL Nafion溶液、1 mL去离子水和5 mL乙醇进行混合,经超声分散后得到催化剂墨水,用喷枪将催化剂墨水均匀喷涂在4 cm×4 cm的碳纸整平层上,得到负载量为1 mg Pt·cm-2的Pt/C催化剂的电极。将其剪裁成2 cm×2 cm的样品分别用作阴、阳电极。将在30% KOH中浸泡一夜的待测膜夹在阴阳2电极之间,组装到单电池中。测试前,阴极、阳极2室均用加湿过的N2吹扫1 h,以排除空气。然后将阴极室切换为加湿过的H2吹扫30 min,之后调节2极室的背压,稳定30 min后,通过线性伏安扫描法测试获得不同温度条件下待测膜的氢气渗透极限电流。线性扫描区间为-0.1~1.0 V,扫描速率为1 mV·s-1。由公式(7)计算氢气渗透率。
| $ K=\frac{i}{2 F P} $ | (7) |
式(7)中: K是氢气渗透率,mol·(cm-2·s-1·kPa-1);i是扣除了短路电流后[30]确定的氢气渗透极限电流密度值,mA·cm-2;F是法拉第常数,96 485 C·mol-1;P是氢气分压差,kPa。
碱性水电解实验在装配有PPS-PVA膜的单个零间隙电解槽(活性面积:2 cm×2 cm)中进行,以Zirfon UTP-500膜(简称Zirfon膜)作为参考。阴极和阳极催化剂分别使用本课题组自制的多孔镍负载碳载铂[31]和多孔镍铁合金[32],阴阳2极室内30% KOH的电解液均由蠕动泵以40 mL·min-1的流速进行循环。在200 mA·cm-2的电流密度、频率范围为100 000~1 Hz,振幅为5 mV的条件下得到电化学阻抗谱(EIS)。在70 ℃的温度条件下测试得到电解池极化曲线。
2 结果与讨论通过扫描电子显微镜对PPS基膜和PPS-PVA膜的形态进行了观察。图 1(a)是PPS基膜表面的SEM图,图 1(b)和图 1(c)是PPS-PVA膜表面的SEM图。PPS基膜表面粗糙、多孔,而PPS-PVA膜表面光滑致密,没有明显的孔隙。如图 1(d)所示,由复合膜断面的SEM可知,PVA已被成功填充至PPS基膜的孔隙中。

|
| 图 1 (a) PPS基膜的平面SEM图;(b)~(c) PPS-PVA膜的平面SEM图;(d) PPS~PVA膜的断面SEM图 Fig.1 SEM image of (a) PPS porous membrane; (b)~(c) the surface of PPS-PVA membrane; (d) the cross-section of PPS-PVA membrane |
| |
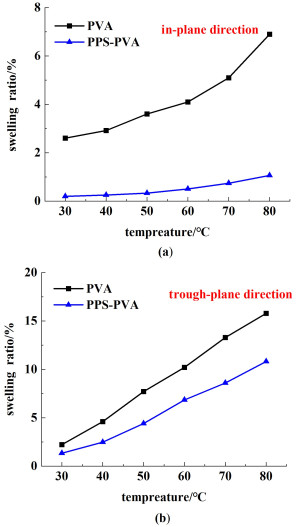
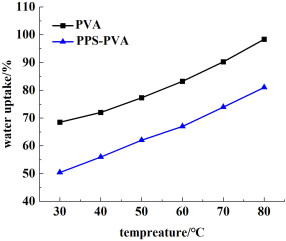
图 2示出了PVA膜和PPS-PVA膜在20% KOH中的溶胀率。与PVA膜相比,在基底膜孔隙内的PVA溶胀受到了限制,PPS-PVA膜的溶胀显著降低。PVA膜和PPS-PVA膜在20% KOH中的吸液率示于图 3。与PVA膜相比,由于PPS-PVA膜中PVA含量较少且PPS基膜材料本身亲水性较差,因而PPS-PVA膜的吸液率较低。
|
| 图 2 PVA膜和PPS-PVA膜在20% KOH中的溶胀率(a) 水平方向膜的溶胀率;(b) 垂直方向膜的溶胀率 Fig.2 Swelling ratio of PVA membrane and PPS-PVA membrane in 20% KOH (a) Swelling ratio of the membranes in-plane direction; (b) Swelling ratio of the membranes through-plane direction |
| |
|
| 图 3 PVA膜和PPS-PVA膜在20% KOH中的吸液率 Fig.3 Water uptake of PVA membrane and PPS-PVA membrane in 20% KOH |
| |
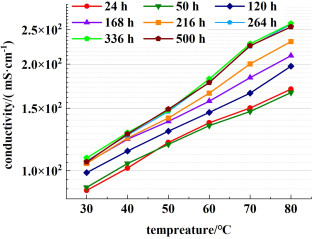
在20% KOH中测试PPS-PVA膜的离子电导率随温度的变化曲线,如图 4所示。复合膜仅靠PVA吸收到膜结构中的电解质溶液传输离子,故其离子传导率与吸液率成正相关。温度升高,膜的吸液率增加,80 ℃时离子电导率可达170 mS·cm-1。为了评估复合膜的稳定性,将浸泡在60 ℃、20% KOH溶液中不同时间的复合膜取出,在20% KOH中测试其离子电导率的变化曲线。由图 4可知,随着浸泡时间的增加,一方面,PVA凝胶不断吸液溶胀,高电解质吸收率有利于离子迁移,电导率不断增加,另一方面,在碱处理过程中,伴随有PVA小分子的溶出,约260 h后趋于稳定,电导率不再变化。由公式(5)计算得到PPS-PVA膜的面电阻低于Zirfon膜的面电阻,如表 1所示。
|
| 图 4 60 ℃、20% KOH浸泡不同时间后PPS-PVA膜的电导率随温度的变化曲线 Fig.4 Variation curve of electrical conductivity with temperature of PPS-PVA membrane after soaking in 20% KOH at 60 ℃ for different time |
| |
| Tempe-rature/℃ | Zirfon RS1/(mΩ·cm2) | PPS-PVA(as prepared)RS2/(mΩ·cm2) | PPS-PVA(aged)RS3/(mΩ·cm2) |
| 30 | 346 | 302 | 230 |
| 40 | 315 | 261 | 185 |
| 50 | 275 | 221 | 157 |
| 60 | 246 | 189 | 137 |
| 70 | 218 | 174 | 94 |
| 80 | 182 | 151 | 89 |
| 注:as prepared指将膜浸泡在60 ℃、20% KOH中24 h;aged指将膜浸泡在60 ℃、20% KOH中500 h。 | |||
为了进一步评估PPS-PVA膜的稳定性,将其浸泡在60 ℃、30% KOH溶液中进行碱处理后,测量复合膜的溶胀率、膜中PVA的质量变化率、膜的红外图谱和机械性能。
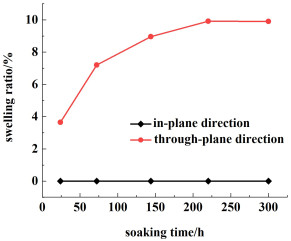
经过碱处理不同时间后的膜的溶胀率测试结果如图 5所示,随着碱处理时间的增加,PPS-PVA膜水平方向的尺寸没有变化,垂直方向的溶胀率从3.7%增加到9.9%,约220 h后趋于稳定, 表现出良好的碱稳定性和尺寸稳定性。
|
| 图 5 60 ℃、30% KOH浸泡不同时间后PPS-PVA膜的溶胀率 Fig.5 Swelling ratio of PPS-PVA membrane after soaking in 30% KOH at 60 ℃ for different time |
| |
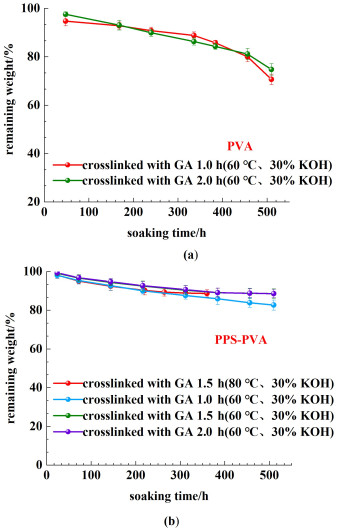
碱处理前后PPS-PVA膜中PPS的质量不变,根据公式(6)计算得到膜中PVA的质量变化率示于图 6。与GA交联2 h的PVA膜随着碱处理时间的增加,其质量呈加速趋势减小,500 h后,质量损失高达30%,如图 6(a)所示。与之相比,仅与GA交联1.5 h的PPS-PVA膜在经过碱液处理500 h后其中的PVA的质量仍能保持在初始值的88%左右,如图 6(b)所示,表现出良好的碱稳定性。对比60和80 ℃碱液中复合膜中PVA的质量损失,可以发现,前期复合膜中PVA在80 ℃下的质量损失更大,这是由于其在高温条件下溶胀更严重,相同时间内更多的小分子会溶出至碱液。但是,膜中PVA的质量更快趋于稳定(约250 h),且与60 ℃下的结果基本一致,约为初始质量的88%。由此可知,PVA的交联度是影响膜稳定性的主要因素。
|
| 图 6 30% KOH溶液浸泡不同时间后膜中PVA的质量变化率(a) PVA膜;(b) PPS-PVA膜 Fig.6 Remaining weight ratio of PVA in the membranes after soaking in 30% KOH for different time(a) PVA membrane; (b) PPS-PVA membrane |
| |
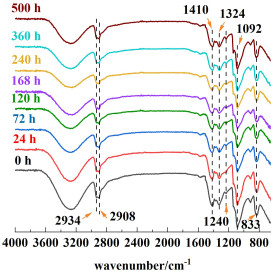
对比PPS-PVA膜在60 ℃、30% KOH中碱处理500 h前后的红外谱图,示于图 7。由于在孔填充过程中PPS基膜表面形成了几十微米的PVA表层,因此内层的PPS特征峰不明显。从图 7中可观察到PVA的典型光谱:2 934和2 908 cm-1分别对应—CH2—基团的对称和不对称伸缩振动吸收峰,1 410 cm-1对应—CH2—基团的C—H弯曲振动吸收峰,1 324 cm-1对应C—H变形振动吸收峰,1 092 cm-1对应C—O基团的伸缩振动吸收峰,1 240 cm-1对应C—O—C伸缩振动吸收峰,833 cm-1对应C—C基团伸缩振动吸收峰。它们均未发生变化,由此推测PPS-PVA膜的失质量可能是由于PVA交联不彻底导致的部分溶解。
|
| 图 7 60 ℃、30% KOH浸泡不同时间后PPS-PVA膜的红外谱图 Fig.7 ATR-FTIR spectra of PPS-PVA membrane after soaking in 30% KOH at 60 ℃ for different time |
| |
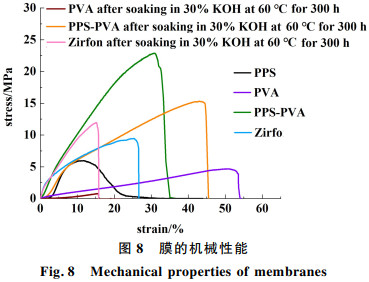
在室温下测试湿态膜水平方向的拉伸性能,结果如图 8所示。PVA膜具有较高的断裂伸长率54%。PPS-PVA膜的拉伸强度可达23 MPa,远高于Zirfon膜的拉伸强度值。PPS-PVA强度的提高或是2者协同作用的结果——PPS纤维网络限制了PVA的溶胀,PVA的填充强化了在PPS纤维之间力的传导和分配。分别将PVA膜、PPS-PVA膜和Zirfon膜浸泡在60 ℃、30% KOH中处理300 h后测试其机械性能,结果发现,PVA膜吸液溶胀严重,机械强度较差,断裂伸长率和拉伸强度大幅下降。而PPS-PVA膜的拉伸强度和断裂伸长率分别是碱处理前膜的67%和1.36倍,并且显著高于碱处理后Zirfon膜的拉伸强度和断裂伸长率。因此,PPS-PVA膜具有良好的碱稳定性和机械性能。
|
| 图 8 膜的机械性能 Fig.8 Mechanical properties of membranes |
| |
|
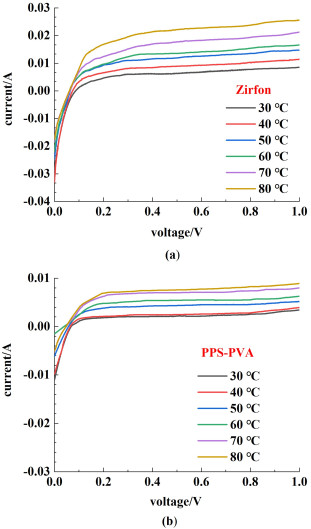
| 图 9 膜在完全加湿状态,PH2=0.2 MPa,PN2=0.15 MPa,不同温度下的氢气渗透测试(a) Zirfon膜;(b) PPS-PVA膜 Fig.9 The hydrogen permeation test of the membrane in the fully humidified state, PH2=0.2 MPa, PN2=0.15 MPa, at different temperatures(a) Zirfon membrane; (b) PPS-PVA membrane |
| |
采用电化学测量方法,分别测试等压和差压条件下Zirfon膜和PPS-PVA膜的氢气渗透极限电流。由公式(7)计算得到膜的氢气渗透率随温度的变化,结果示于表 2。氢气渗透随着温度的增加而加剧,80 ℃等压条件下,PPS-PVA膜的氢气渗透率为3.5×10-8 mol·cm-2·s-1·kPa-1,低于Zirfon膜的值7.9×10-8 mol·cm-2·s-1·kPa-1。当阴阳两极室气体存在0.05 MPa的压差后,与等压条件下的测试结果相比,80 ℃时膜的气体渗透率增加了约43%,而Zirfon膜增加了约90%。故可以说明PPS-PVA膜的阻气性优于Zirfon膜的阻气性。
| Temperature/℃ | Zirfon | PPS-PVA | |||
| Ka1/(mol·cm-2·s-1·kPa-1) | Kb1/(mol·cm-2·s-1·kPa-1) | Ka2/(mol·cm-2·s-1·kPa-1) | Kb2/(mol·cm-2·s-1·kPa-1) | ||
| 30 | 2.72×10-8 | 4.08×10-8 | 9.85×10-9 | 1.44×10-8 | |
| 40 | 3.81×10-8 | 5.57×10-8 | 1.14×10-8 | 1.64×10-8 | |
| 50 | 4.47×10-8 | 8.07×10-8 | 2.02×10-8 | 2.71×10-8 | |
| 60 | 5.80×10-8 | 1.04×10-7 | 2.62×10-8 | 3.40×10-8 | |
| 70 | 6.76×10-8 | 1.26×10-7 | 3.21×10-8 | 4.56×10-8 | |
| 80 | 7.92×10-8 | 1.51×10-7 | 3.47×10-8 | 4.98×10-8 | |
| Ka1和Ka2是在等压条件(PH2=PN2=0.2 MPa)测得的膜的氢气渗透率,Kb1和Kb2是在差压条件下(PH2=0.2 MPa,PN2=0.15 MPa)测得的膜的氢气渗透率。 | |||||
对经过80 ℃、30% KOH处理300 h后的膜进行氢气渗透率测试,结果如表 3所示。与表 2中碱处理前膜的氢气渗透率比较可知,碱处理后PPS-PVA膜的氢气渗透率未有大幅增加,说明PPS-PVA膜具有较好的稳定性。
| Temperature/℃ | Zirfon | PPS-PVA | |||
| Ib3/(mA·cm-2) | Kb3/(mol·cm-2·s-1·kPa-1) | Ib4/(mA·cm-2) | Kb4/(mol·cm-2·s-1·kPa-1) | ||
| 30 | 1.59 | 4.12×10-8 | 0.57 | 1.48×10-8 | |
| 40 | 2.18 | 5.64×10-8 | 0.66 | 1.70×10-8 | |
| 50 | 3.20 | 8.30×10-8 | 1.08 | 2.78×10-8 | |
| 60 | 4.14 | 1.07×10-7 | 1.35 | 3.51×10-8 | |
| 70 | 5.03 | 1.30×10-7 | 1.82 | 4.71×10-8 | |
| 80 | 6.08 | 1.58×10-7 | 2.02 | 5.23×10-8 | |
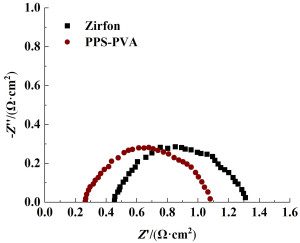
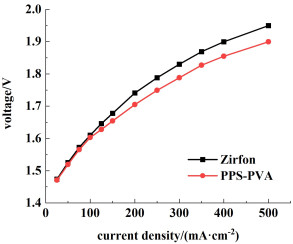
如图 10所示,比较了分别由PPS-PVA膜和Zirfon膜组装的电池在200 mA·cm-2下的Nyquist图。基于PPS-PVA膜的电池电阻约为0.26 Ω·cm2低于基于Zirfon膜的电池电阻(0.45 Ω·cm2)。在70℃、30% KOH测试条件下,分别由PPS-PVA膜和Zirfon膜组装的电池的极化曲线如图 11所示。在500 mA·cm-2的电流密度下,由PPS-PVA膜组装的电池的电压为1.91 V,优于使用Zirfon膜时的电压1.96 V。
|
| 图 10 分别由PPS-PVA膜和Zirfon膜组装的电池在200 mA·cm-2下的奈奎斯特图 Fig.10 Nyquist plots of cells assembled by PPS-PVA and Zirfon membranes at 200 mA·cm-2, respectively |
| |
|
| 图 11 在70 ℃、30% KOH条件下,分别由PPS-PVA膜和Zirfon膜组装的电池的极化曲线 Fig.11 Polarization curves of cells assembled by PPS-PVA membrane and Zirfon membrane in 30% KOH at 70 ℃, respectively |
| |
在本研究中,我们成功制备了一种新型凝胶填充复合膜用于碱性水电解。以高机械强度的PPS作为支撑骨架,限制了凝胶的溶胀,显著提高了PPS-PVA膜的稳定性。同时,PPS-PVA膜具有低面电阻(150 mΩ·cm2)和低氢气渗透率(3.5×10-8 mol·cm-2·s-1·kPa-1)。凝胶填充复合膜的策略为碱性水电解新型隔膜的设计和优化提供了一条可行的途径。
| [1] |
CHI J, YU H. Water electrolysis based on renewable energy for hydrogen production[J]. Chinese Journal of Catalysis, 2018, 39(3): 390-394. DOI:10.1016/S1872-2067(17)62949-8 |
| [2] |
YU H, YI B. Hydrogen for energy storage and hydrogen production from electrolysis[J]. Chinese Journal of Engineering Science, 2018. DOI:10.15302/J-SSCAE-2018.03.009 |
| [3] |
MANDAL M. Recent advancement on anion exchange membranes for fuel cell and water electrolysis[J]. ChemElectroChem, 2021, 8(1): 36-45. DOI:10.1002/celc.202001329 |
| [4] |
LI D, PARK E J, ZHU W, et al. Highly quaternized polystyrene ionomers for high performance anion exchange membrane water electrolysers[J]. Nature Energy, 2020, 5(5): 378-385. DOI:10.1038/s41560-020-0577-x |
| [5] |
URSUA A, GANDIA L M, SANCHIS P. Hydrogen production from water electrolysis: Current status and future trends[J]. Proceedings of the IEEE, 2012, 100(2): 410-426. DOI:10.1109/JPROC.2011.2156750 |
| [6] |
万磊, 徐子昂, 王培灿, 等. 电解水制氢的耐碱离子膜研究进展[J]. 化工进展, 2022, 41(3): 1556-1568. WAN Lei, XU Ziang, WANG Peican, et al. Progress of alkaline-resistant ion membranes for hydrogen production by water electrolysis[J]. Chemical Industry and Engineering Progress, 2022, 41(3): 1556-1568. DOI:10.16085/j.issn.1000-6613.2021-2217 (in Chinese) |
| [7] |
WENDT H, HOFMANN H. Cermet diaphragms and integrated electrode-diaphragm units for advanced alkaline water electrolysis[J]. International Journal of Hydrogen Energy, 1985, 10(6): 375-381. DOI:10.1016/0360-3199(85)90063-1 |
| [8] |
IVANOVA Y A, FREITAS C, LOPES D V, et al. Cellular zirconia ceramics processed by direct emulsification[J]. Journal of the European Ceramic Society, 2020, 40(5): 2056-2062. DOI:10.1016/j.jeurceramsoc.2020.01.005 |
| [9] |
ROSA V M, SANTOS M B F, DA SILVA E P. New materials for water electrolysis diaphragms[J]. International Journal of Hydrogen Energy, 1995, 20(9): 697-700. DOI:10.1016/0360-3199(94)00119-K |
| [10] |
KERRES J, EIGENBERGER G, REICHLE S, et al. Advanced alkaline electrolysis with porous polymeric diaphragms[J]. Desalination, 1996, 104(1/2): 47-57. |
| [11] |
OTERO J, SESE J, MICHAUS I, et al. Sulphonated polyether ether ketone diaphragms used in commercial scale alkaline water electrolysis[J]. Journal of Power Sources, 2014, 247: 967-974. DOI:10.1016/j.jpowsour.2013.09.062 |
| [12] |
AILI D, HANSEN M K, ANDREASEN J W, et al. Porous poly(perfluorosulfonic acid) membranes for alkaline water electrolysis[J]. Journal of Membrane Science, 2015, 493: 589-598. DOI:10.1016/j.memsci.2015.06.057 |
| [13] |
VENGATESAN S, SANTHI S, JEEVANANTHAM S, et al. Quaternized poly (styrene-co-vinylbenzyl chloride) anion exchange membranes for alkaline water electrolysers[J]. Journal of Power Sources, 2015, 284: 361-368. DOI:10.1016/j.jpowsour.2015.02.118 |
| [14] |
LIU Z, SAJJAD S D, GAO Y, et al. The effect of membrane on an alkaline water electrolyzer[J]. International Journal of Hydrogen Energy, 2017, 42(50): 29661-29665. DOI:10.1016/j.ijhydene.2017.10.050 |
| [15] |
PARK E J, CAPUANO C B, AYERS K E, et al. Chemically durable polymer electrolytes for solid-state alkaline water electrolysis[J]. Journal of Power Sources, 2018, 375: 367-372. DOI:10.1016/j.jpowsour.2017.07.090 |
| [16] |
HU X, HUANG Y, LIU L, et al. Piperidinium functionalized aryl ether-free polyaromatics as anion exchange membrane for water electrolysers: Performance and durability[J]. Journal of Membrane Science, 2021. DOI:10.1016/j.memsci.2020.118964 |
| [17] |
KRAGLUND M, AILI D, JANKOVA K, et al. Zero-gap alkaline water electrolysis using ion-solvating polymer electrolyte membranes at reduced KOH concentrations[J]. Journal of the Electrochemical Society, 2016, 163(11): F3125-F3131. DOI:10.1149/2.0161611jes |
| [18] |
AILI D, WRIGHT A G, KRAGLUND M R, et al. Towards a stable ion-solvating polymer electrolyte for advanced alkaline water electrolysis[J]. Journal of Materials Chemistry A, 2017, 5(10): 5055-5066. DOI:10.1039/C6TA10680C |
| [19] |
HU B, HUANG Y, LIU L, et al. A stable ion-solvating PBI electrolyte enabled by sterically bulky naphthalene for alkaline water electrolysis[J]. Journal of Membrane Science, 2022. DOI:10.1016/j.memsci.2021.120042 |
| [20] |
DE GROOT M T, VREMAN A W. Ohmic resistance in zero gap alkaline electrolysis with a Zirfon diaphragm[J]. Electrochimica Acta, 2021. DOI:10.1016/j.electacta.2020.137684 |
| [21] |
LEE H I, DUNG D T, KIM J, et al. The synthesis of a Zirfon-type porous separator with reduced gas crossover for alkaline electrolyzer[J]. International Journal of Energy Research, 2020, 44(3): 1875-1885. DOI:10.1002/er.5038 |
| [22] |
STOJADINOVIC J, LA MANTIA F. Woven or nonwoven web: US11035046[P]. 2021-06-15
|
| [23] |
LEE J W, LEE J H, LEE C, et al. Cellulose nanocrystals-blended zirconia/polysulfone composite separator for alkaline electrolyzer at low electrolyte contents[J]. Chemical Engineering Journal, 2022. DOI:10.1016/j.cej.2021.131149 |
| [24] |
WAN L, XU Z, WANG B. Green preparation of highly alkali-resistant PTFE composite membranes for advanced alkaline water electrolysis[J]. Chemical Engineering Journal, 2021. DOI:10.1016/j.cej.2021.131340 |
| [25] |
MERLE G, HOSSEINY S S, WESSLING M, et al. New cross-linked PVA based polymer electrolyte membranes for alkaline fuel cells[J]. Journal of Membrane Science, 2012, 409/410: 191-199. DOI:10.1016/j.memsci.2012.03.056 |
| [26] |
LIN Z, LU Y, LAI C, et al. Polyvinyl alcohol-based gel electrolytes with high water content for flexible zinc-air batteries with high rate capability[J]. Journal of the Electrochemical Society, 2021. DOI:10.1149/1945-7111/ac2ac4 |
| [27] |
ALIPOORI S, MAZINANI S, ABOUTALEBI S H, et al. Review of PVA-based gel polymer electrolytes in flexible solid-state supercapacitors: Opportunities and challenges[J]. Journal of Energy Storage, 2020. DOI:10.1016/j.est.2019.101072 |
| [28] |
SOHEE K, HEE H J, JINOK Y, et al. Highly selective porous separator with thin skin layer for alkaline water electrolysis[J]. Journal of Power Sources, 2022. DOI:10.1016/j.jpowsour.2022.231059 |
| [29] |
LU S, ZHUANG L, LU J. Homogeneous blend membrane made from poly(ether sulphone) and poly(vinylpyrrolidone) and its application to water electrolysis[J]. Journal of Membrane Science, 2007, 300(1/2): 205-210. |
| [30] |
ZHANG J, GASTEIGER H, GU W. Electrochemical measurement of the oxygen permeation rate through polymer electrolyte membranes[J]. Journal of the Electrochemical Society, 2013, 160(6): F616-F622. DOI:10.1149/2.081306jes |
| [31] |
葛升. 静态供水水电解装置研究[D]. 天津: 天津大学, 2021 GE Sheng. Study on static water supply electrolysis device[D]. Tianjin: Tianjin University, 2021 (in Chinese) |
| [32] |
葛升, 闵洛夫, 费洪达, 等. 一步电沉积制备高活性高稳定镍铁合金析氧电催化剂[J]. 化学工业与工程, 2022, 39(2): 41-49. GE Sheng, MIN Luofu, FEI Hongda, et al. Highly efficient and durable Ni-Fe alloy catalyst towards OER via one-step electrodeposition[J]. Chemical Industry and Engineering, 2022, 39(2): 41-49. (in Chinese) |
 2023, Vol. 40
2023, Vol. 40




