在约85%的医药产品中,活性医药成分(Active pharmaceutical ingredients,API)以结晶状态的形式存在,结晶是贯穿医药开发和制剂开发过程的极其关键和重要的一环[1]。不同多晶型、纯度、粒度和粒度分布(Crystal size distribution, CSD)等的晶态产物常体现出溶解度、溶出度和生物利用度等不同的理化性质,影响结晶工艺及下游工艺,进而影响技术操作、设备设计、开发成本等,最终影响药物的疗效和可开发性[2]。在新药和新制剂的研发中,应对药物的结晶过程控制予以特别关注,研究产物晶型、纯度和CSD等的调控方法可以为剂型和工艺的设计提供理论指导,是新药研发以及开发高质量仿制药的关键,也是药物结晶领域的一大挑战。
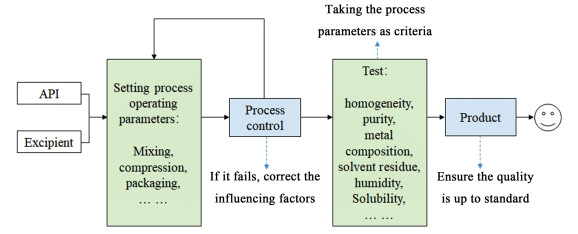
溶液结晶法是目前纯化和分离API最重要和常用的方法,如能充分开展溶液结晶的过程控制研究、发展过程控制策略,从而稳健控制结晶过程,最终实现晶体晶型、粒度和CSD等的高度可控,将对丰富药物结晶调控策略及药物结晶工业的发展具有重要意义,也是整个结晶工业的发展前沿[3]。然而,结晶是受各种因素影响的复杂动态过程,如结晶物的物性、溶剂、添加剂、过饱和度、pH值、温度、晶种和流场等[4]。控制1个或多个上述参数可能无法实现特定晶体产物的可控制备,另一方面,结晶过程机理复杂,涉及成核、生长、聚结和破碎等多种动力学行为。在以往的研究中,普遍使用试错法(Trial-and-error)进行药物开发。然而,该方法的盲目性显著降低了研发的经济性及高效性。最典型的是“质量源于检测(Quality by testing, QbT)”研究理念在药物结晶中的应用,即将最终产品的重复性检测输入结晶产品中,通过确定结晶过程输入和输出的关系优化产品质量。然而研究人员逐渐意识到该理念在效率和灵活度方面的欠缺,最重要的是,无法明确影响结晶过程的关键性因素[5]。为了突破结晶过程动态变化的“黑匣子”,2004年,美国食品与药品管理委员会(US Food and Drug Administration, FDA)建议将过程分析技术(Process analysis technology, PAT)运用到医药产品制造行业中,形成一套全面主动的药物研发方法。PAT集合了多种现代过程分析表征手段,已被广泛运用于化工产品的分析制备过程。通过对生产过程中的关键性参数进行周期性、持续性的检测采集、数据分析及反馈控制,确保最终产品的质量达到要求(图 1)[6, 7]。这种全新的设计理念是在“质量源于设计(Quality by design, QbD)”的基础上建立的,不但能够通过对关键状态变量的识别以及对关键过程参数的调控,确保药物研发及生产过程的稳健性和药物产品的一致性,还能够有效缩短药物的研发周期,可降低原料浪费,使研发效率得以提高[8-10]。
|
| 图 1 QbD指导的质量控制流程图 Fig.1 Quality control guided by QbD |
| |
结晶过程涉及多种学科,并且机理复杂,建立相应的过程模型或控制模型具有十分大的挑战性,也是研究领域和工业领域中的瓶颈问题之一[11]。针对此现状,本研究结合计算机编程技术,提出将PAT技术应用于结晶过程研究中,设计与构建结晶过程监控系统(Crystallizaiton process monitoring and control system, CPMCS)[12, 13],预期达到以下目标:1)基于光谱法、色谱法及其他过程分析仪,组装结晶过程关键过程参数(Critical process parameters, CPPs)的信息分析及管理工具;2)根据以上信息,构建晶体生产过程的控制系统。本研究所述系统的开发通过对“QbD”思想的演绎,建立一个可评估并且调控晶态产品质量的在线研究平台,对结晶过程整体规律的探索及理解具有指导意义。
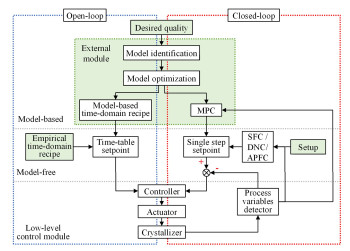
1 CPMCS的开发 1.1 CPMCS的理论构架和模块设计针对溶液结晶中最普遍的冷却、溶析结晶过程,CPMCS设计了2种控制模块:开环控制和闭环反馈控制。前者通常采用时域工艺策略,在实验开始前预设降温方案或反溶剂添加方案[14]。后者包括无模型的闭环反馈控制及模型预测控制(Model predictive control, MPC)[15]。广泛使用的无模型闭环反馈控制之一是过饱和度反馈控制(Supersaturation feedback control, SFC)[16],该方法必须基于一系列结晶热力学参数并配有提前建立的浓度检测模型。直接成核控制(Direct nucleation control, DNC)[17]也属于无模型闭环反馈控制;但与SFC不同的是,DNC完全基于实时粒数信号,并且允许不经任何校正直接应用;最后,本研究在所开发系统的无模型闭环反馈控制中补充加入了晶型反馈控制(Active polymorphic feedback control, APFC)[18]。由于需要对不同晶型进行有效鉴别,该方法采用光谱法,需事先对多晶型的Raman光谱进行研究,若定量控制需结合化学计量学进行建模,定性控制则相对简捷,但需结合反溶剂调控以削弱温度调控所引发的滞后。对于MPC控制,本研究开发的过程检测系统设有MPC模块接口,可结合已有的结晶过程模拟和优化工作实现MPC功能,即根据结晶的实时状态参数(如过饱和度、温度等),通过过程模型实时设定控制变量,从而达到反馈控制的目的。
所开发系统的控制模块设计见图 2,主要功能包含:1)用户可采用开路控制通过模型优化获得的工艺策略,或采用经验式工艺策略;2)可通过预留的MPC模块实现反馈控制;3)可采用无模型闭环反馈控制(SFC、DNC或APFC),获得趋近于预设标准的晶体产品。
|
| 图 2 控制模块的结构设计 Fig.2 Structure of control module |
| |
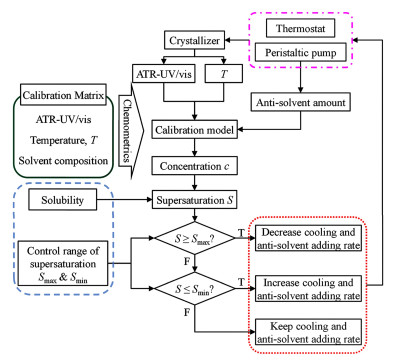
本研究所开发系统中,面向冷却、溶析结晶的SFC模块原理如图 3所示。需提前建立好浓度检测模型。在实际操作中,首先获取晶浆温度,同时基于初始投料比,以一定滴加速率泵入反溶剂,开启对结晶体系溶剂组成的实时监测。接下来,结合浓度监测模型、溶液温度和在线ATR-UV/vis实时采集的光谱强度,获得体系内当前溶质浓度并进而得到实时过饱和度。然后,将过饱和度与预设的浓度上、下限进行比对,根据是否超过或低于预设范围来调整温度或反溶剂的量。
|
| 图 3 SFC在冷却、溶析结晶过程中的应用原理图 Fig.3 Diagram of SFC for cooling, anti-solvent crystallization |
| |
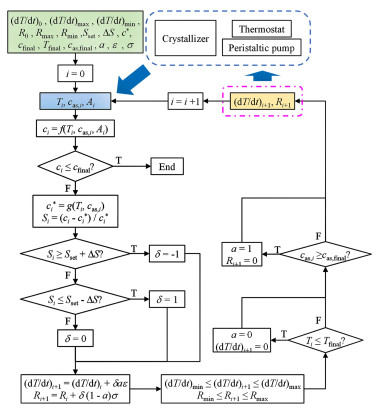
实际SFC的逻辑流程图如图 4。先设定初始操作参数和控制参数并调整步长,涉及参数如表 1中“初始操作参数和控制参数”所示。需要注意的是,此处引入了1个操作比例a,这是因为当冷却结晶和溶析结晶耦合时,必须考虑到2者的操作速度,因此定义a为耦合结晶过程中降温速率和反溶剂添加速率的比值。接下来进行反溶剂的添加并开始按初始降温速率执行冷却结晶操作。该阶段需对结晶釜内的多种状态参数进行持续性实时监测,涉及参数列于表 1中“实时监测状态参数”一栏。以上状态参数可通过计算转化为实时浓度ci。需要注意的是,UV/vis信号波动会产生较大噪音,进而影响过饱和度的计算结果。因此,SFC的循环速率不宜过高。除此之外,应在单次循环内多次采集光谱信号以降低噪音。例如,将SFC循环速率控制为1 min·次-1,实时UV/vis信号采集时间设定为2 s;连续不间断采集中对单次输入的UV/vis光谱Ai取最近10~20次的数据平均处理,降低噪音的影响。同时,在实际操作过程中,可通过调整操作比例a的值,对冷却结晶和溶析结晶进行调节以使结晶釜内的温度和反溶剂量处于可控范围内。
|
| 图 4 冷却、溶析结晶过程SFC程序流程图 Fig.4 Logic diagram of SFC basing on cooling, anti-solvent crystallization |
| |
| 参数名称 | 符号 |
| 初始操作参数和控制参数 | |
| 初始降温速率 | (dT/dt)0 |
| 降温速率区间 | (dT/dt)min, (dT/dt)max |
| 降温速率步长 | ε |
| 初始反溶剂添加速率 | R0 |
| 反溶剂添加速率区间 | Rmin, Rmax |
| 反溶剂添加速率步长 | σ |
| 过饱和度预设值 | Sset |
| 过饱和度波动区间 | ΔS |
| 结晶终点处溶质浓度,反溶剂浓度,温度 | cfinal, cas, fina, Tfinal |
| 溶解度函数 | c* |
| 冷却\溶析结晶操作比例 | a |
| 实时监测状态参数 | |
| 反溶剂浓度 | cas, i |
| 结晶釜内温度 | Ti |
| ATR-UV/vis信号强度 | Ai |
DNC模块的目的是获得粒度较大的晶体产品。由于结晶工艺的理论收率不变,减少终点颗粒数目是增大粒度的有效手段。一般情况下可采取温度调节法或反溶剂加入量调节法,其原理是控制结晶过程中的成核驱动力,即过饱和度。借助聚焦光散射测量(Focused beam reflectance measurement, FBRM)等技术检测粒数或平均粒度的变化,通过对比预设范围的上、下限,确定调整方向。以CSD为控制目标,将弦长分布(Chord length distribution, CLD)计算的均方平均弦长作为辅助控制目标,如式(1)所示。
| $ L_{[3, 2]}=\sum\limits_{i=1}^k n_i L_i^3 / \sum\limits_{i=1}^k n_i L_i^2 $ | (1) |
式(1)中:L[3,2]代表均方平均弦长;Li为i时刻所测得的弦长。
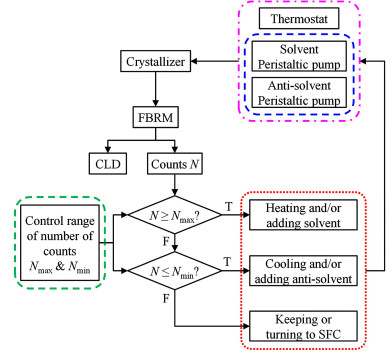
DNC原理如图 5所示。在实际操作过程中不存在添加晶种的操作,因此所有的晶核来源均为初级成核,即过结晶初始阶段的饱和度全部用于爆发成核。同时应结合FBRM、浊度仪或颗粒成像测量(Particle vision measurement, PVM)等技术监测成核,根据粒数变化率判断爆发成核是否发生。一旦观察到结晶釜内发生爆发成核,应立即停止反溶剂的添加,此后转入常规控制。为了降低滞后性,可采用比例-微分控制器进行调控。
|
| 图 5 DNC在冷却、溶析结晶过程中的应用原理图 Fig.5 Diagram of DNC for cooling, anti-solvent crystallization |
| |
相比SFC,DNC策略的结晶终点判据较为复杂。若通过温度控制进行粒数控制,则以终点温度为判据即可。若采用添加反溶剂/溶剂的方式,则需设置一个总体积(或液位)的上限值和终点反溶剂浓度的下限值,控制DNC过程溶剂和反溶剂的加入量,而后以终点温度和反溶剂浓度共同作为终点判据。DNC策略趋向于在较高的过饱和度下进行,容易导致溶剂包藏、纯度下降、颗粒聚集等问题。因此可结合SFC辅助进行控制,但因此也加大了浓度建模校正的工作量。
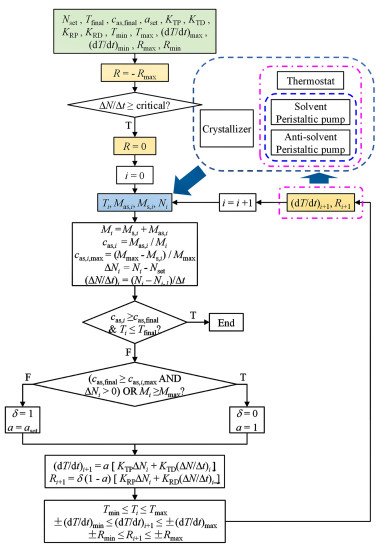
DNC的操作流程如图 6所示。首先设置一定的操作参数及控制参数,具体参数列于表 2。然后,加入反溶剂控制爆发成核,通过粒数的变化率检测爆发成核的发生。随后,在进入循环的同时开启对结晶状态参数的实时监测,检测每一次循环过程中的颗粒数目和晶浆温度,如表 2所示。根据蠕动泵的操作参数计算得到溶剂和反溶剂的加入量Ms, i和Mas, i。为了实现对最终晶体粒度的控制,若溶剂和反溶剂总加入量Mi到达上限Mmax,或者当前粒数Ni高于Nset同时理论反溶剂终点最大浓度cas, i, max低于预设的终点反溶剂浓度cas, final时,停止蠕动泵工作。对于新的升温/降温速率(dT/dt)i+1及溶剂/反溶剂添加速率Ri+1,若超出预设范围,则强制调整到边界值,作为一种保护。若晶浆温度Ti和反溶剂浓度cas, i达到了终点,则停止控制。与SFC模块类似,由于是冷却和溶析的耦合结晶过程,需引入操作比例a。
|
| 图 6 冷却、溶析结晶过程DNC程序流程图 Fig.6 Logic diagram of DNC for cooling, anti-solvent crystallization |
| |
| 参数名称 | 符号 |
| 初始操作参数和控制参数 | |
| 粒数预设值 | Nset |
| 反溶剂浓度 | cas, final |
| 结晶终点温度 | Tfinal |
| 降温速率区间 | (dT/dt)min, (dT/dt)max |
| 温度区间 | Tmin, Tmax |
| 反溶剂添加速率区间 | Rmin, Rmax |
| 冷却\溶析结晶操作比例 | a |
| 控制器相关设定参数 | KRP、KTP、KTD、KRD |
| 实时监测状态参数 | |
| 颗粒数目 | Ni |
| 晶浆温度 | Ti |
APFC模块用于诱导药物的目标多晶型。多晶型现象指同种化学分子具有2种或2种以上的晶体结构,不同晶型的API常体现不同的理化性质。充分开展药物晶型研究、发展晶型调控策略是开发高质量仿制药的关键,也是新药研发和评审过程中极为重要的内容。然而多晶型的选择性成核尚未形成成熟理论,其机理仍存在较大盲区,影响因素复杂多样。对药物特定多晶型的诱导和深入研究仍然是晶体产品控制中具有挑战性的一环。本研究所开发系统中的APFC无模型控制策略在得到预期晶型的同时,很有可能出现非预期晶型以伴随成核的形式析出。因此,与DNC类似,有必要在非预期晶型析出后采用溶解法消除。另外,由于过饱和度对晶型存在较大影响,通常在APFC的基础上结合SFC策略以维持目标晶型的生长。
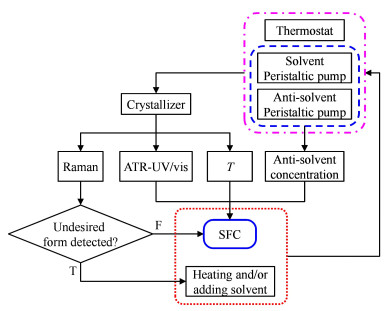
本系统构建的APFC原理如图 7所示。由于是SFC辅助APFC的模型框架,因此引入了Raman和ATR-UV/vis光谱技术,对目标晶型的控制通过定性考察Raman光谱中出现的对应特征峰执行。具体逻辑流程图与DNC类似,此处不做详述。
|
| 图 7 APFC在冷却、溶析结晶过程中的应用原理图 Fig.7 Diagram of APFC for cooling, anti-solvent crystallization |
| |
本研究采集了不同溶液温度下,药物溶液中ATR-UV光谱最大吸收波长处的吸光度值,以及相同溶液温度条件下的ATR-UV光谱最大吸收波长λmax随浓度的变化。采用多元数据处理软件SIMCA-P 11.5,对以上数据进行偏最小二乘法(PLS)回归,通过压缩-中心化(Scaled & Centere)数据并设定自变量X及因变量Y建立数据集(Dataset)。基于霍特林T2分布(Hotelling T2)检测结果得到置信椭圆(Confidence ellipse),选择椭圆内的数据作为工作集(Workset),剩余数据用于模型校验。随后,采用所选工作集进行数据的回归建模。
1.6 CPMCS开环控制实验步骤本研究以5’-核苷酸二钠的结晶过程为研究对象,对CPMCS的开环控制模块进行考察。5’-核苷酸二钠由5’-肌苷酸二钠(IMP)和5’-鸟苷酸二钠(GMP)2种核苷酸衍生物按质量比1∶1组成,简称为IMP & GMP。通常由乙醇-水体系中的反溶剂结晶制备。本研究针对IMP & GMP产品粒度分布不理想的问题,围绕粒数衡算模型进行结晶动力学研究。考虑到实际过程为间歇操作,无进出料,因此晶浆体积恒定。并假定:1)晶体生长速率符合ΔL定律[19],即晶体的生长速度与粒度无关;2)CSD变化不受晶体的破碎与聚结的影响,仅与初级成核及之后的生长相关。根据以上条件,粒数衡算方程可简化为式(2)。
| $ \frac{\partial n}{\partial t}+G \frac{\partial n}{\partial L}=0 $ | (2) |
式(2)中:n代表晶体粒数密度;L代表晶体粒度;G代表晶体生长速率;t代表操作时间。通过测定结晶过程晶体粒数密度及CSD变化趋势,即可求得生长速率。在无进出料且不考虑晶体的聚结和破碎的前提下,成核速率可由晶浆中晶体粒数密度随时间的变化率求得。
本研究通过考察不同因素对结晶过程中CSD变化的影响,明确影响结晶能力的关键性因素,建立晶体成核速率、生长速率与操作条件间的数理关系。实际开环控制IMP & GMP的结晶时,首先考察了乙醇浓度和降温速率的影响。配制50 ℃的IMP & GMP饱和乙醇-水溶液,总体积500 mL。保持釜内物料混合充分。实时采集FBRM和ATR-UV/vis数据以获得结晶釜内实时浓度,然后按预设降温速率冷却结晶。开环控制所采用的工艺可以是基于过程建模优化得到的工艺,也可是无模型的经验式工艺。观察到晶体析出后立即增大ATR-UV/vis和FBRM的数据收集频率。溶液温度降至结晶终点温度时停止实验。
随后考察反溶剂滴加速率和溶液温度的影响。先配制一定温度下的饱和溶液,并设定溶析结晶终点时的乙醇浓度,所需乙醇根据水的质量推算,终点体积应控制在650 mL以下。在高于溶解温度3 ℃以上恒温一段时间,并采用合适的搅拌速率以保证物料充分混合后完全溶解。然后开启蠕动泵滴加反溶剂,同时采集ATR-UV/vis和FBRM数据,记录反应时间。数据采集速率可随晶体的析出逐渐增大。当反溶剂添加完毕即停止实验,并且记录用时。根据整个过程的用时及乙醇总量可得反溶剂浓度随时间的变化曲线,以上数据用于之后的ATR-UV/vis光谱浓度计算。
1.7 CPMCS闭环控制实验步骤为了验证CPMCS对冷却、溶析结晶的闭环控制效果,以β-蒿甲醚(下称蒿甲醚)溶析结晶过程为例,以非线性预测控制(Nonlinear model predict control, NMPC)和移动窗(Moving horizon estimation, MHE)耦合的方法构建结晶过程控制模型,对NMPC-MHE方法进行准确性验证。
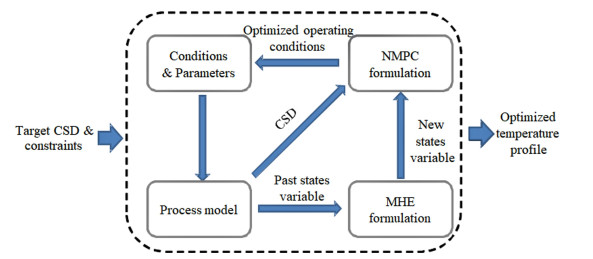
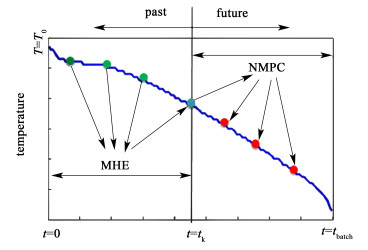
NMPC方法与MHE方法的工作原理如图 8所示,在任意的在每个时间点,MHE方法根据tk之前的已知的测量值与预测值估计tk时刻的状态变量
|
| 图 8 固定间歇时间下NMPC-MHE方法的工作原理 Fig.8 Working principle of the NMPC-MHE formulation for fixed batch time |
| |
具体操作时,首先配制具有一定初始浓度的溶液,设定好搅拌速度使物料充分混合,并设定恒温水浴的温度高于饱和温度3 ℃以保证溶液完全澄清。开启FBRM,调节参数使在初始溶液中FBRM显示的颗粒数小于150,设定数据的实时采集步长为15 s。待结晶釜中的溶质完全溶解后,开启降温程序至预设的饱和温度,此后恒温搅拌1 h。开启蠕动泵,向体系加入反溶剂并记录开始时刻。通过恒温水浴,根据最优降温曲线控制结晶釜温度。每隔30 s取上层清液后采用重量法分析溶液的浓度。本研究通过对配点进行优化求解,从而得出最适宜操作变量。
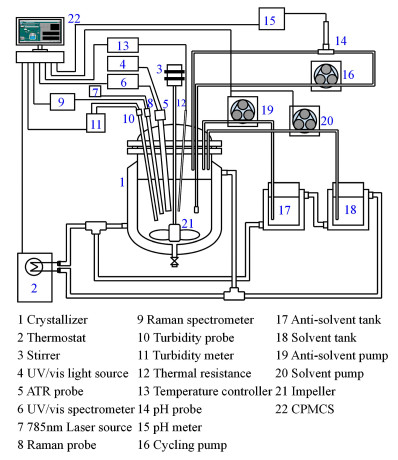
2 案例研究 2.1 CPMCS系统的实施和界面本研究基于LabVIEW平台开发结晶控制系统的配套软件。最终所构建的硬件系统和人机交互界面分别如图 9和图 10所示。所开发系统的软件核心包括通讯控制、时间控制、反馈控制和数据分析等模块。所有信号均集成显示于软件主界面,包括溶剂/反溶剂参数、温度、浊度和粒度等。考虑到设备的更替和二次开发等问题,均采用模块化的形式编写所涉及的硬件功能及数据处理,增强了软件通用性。各实验仪器或设备通过弹出式窗口操控。如需对硬件及功能进行改动,则应重新编写对应模块后接入CPMCS。
|
| 图 9 CPMCS硬件结构示意图 Fig.9 Diagram of instruments of CPMCS |
| |

|
| 图 10 所开发系统的人机交互界面 Fig.10 Graphic user interface of developed system |
| |
溶液浓度在线检测人机互动界面和ATR-UV/vis光谱仪参数设置界面如图 11所示。由于系统集成了多种PAT工具,实际应用时需考虑多设备间通讯信号的时间同步性,因此采用主动请求的通讯机制实现硬件设备采集任务的精确控制。程序采用多生产者/多消费者模式构建数据采集和分析框架。允许用户通过键盘和鼠标等设备操纵软件的图标或菜单,进而执行调用M文件、启动实验程序、选择实验操作命令等。

|
| 图 11 (a) 浓度在线检测和(b)ATR-UV/vis光谱仪参数设置界面 Fig.11 (a) The interface for solution concentration monitoring and (b) Instrument parameter setting of ATR-UV/vis spectroscopy |
| |
IMP & GMP是一种重要的食品添加剂。国内IMP & GMP产品质量差,结晶机制不清晰,缺乏深入的结晶过程动力学研究[20]。本研究基于所构建的CPMCS系统,结合ATR-UV/vis和FBRM在线技术,测定了考察不同降温曲线和反溶剂添加速率对结晶成核、生长动力学的影响,考察采用不同条件时的结晶动力学参数,以此为基础优化操作路线,实现了对结晶过程的开环控制[21]。
2.2.1 FBRM CLD处理本研究选用矩量变换法处理粒度分布数据,直接基于FBRM测得的CLD代替CSD进行动力学参数计算。为克服非线性偏微分方程转换所导致的结果误差较大,且差异性随着矩量阶次的升高越来越大等问题[22],采用零阶、一阶矩量的矩量变换法对CLD数据进行计算[23, 24]。处理后得到FBRM第j个数据点对应的晶体成核速率B和生长速率G:
| $ B_{\text {exp }, j}=\left[\frac{\mathrm{d} \mu_0 / \mathrm{d} t}{m_{\text {water }}+m_{\text {EtOH }}}\right]_j=\frac{\Delta \mu_{0, j} / \theta_j}{\left[m_{\text {water }}+m_{\text {EtOH }}\right]_j} $ | (3) |
| $ G_{\exp , j}=\left[\frac{\mathrm{d}\left(\mu_1 / \mu_0\right)}{\mathrm{d} t}\right]_j=\left[\frac{\mathrm{d} D_{[1, 0]}}{\mathrm{d} t}\right]_j=\frac{\Delta D_{[1, 0], j}}{\theta_j} $ | (4) |
式(3)和式(4)中:D[1,0]代表由μ0和μ1计算得到的平均粒度;μ0和μ1为粒数密度函数n对FBRM弦长r的零阶和一阶矩量;θ是单次离散采样时间。
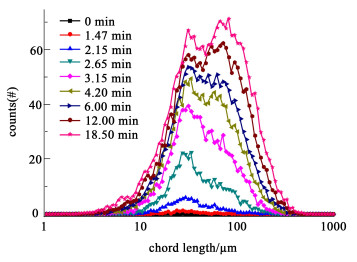
2.2.2 IMP & GMP结晶动力学结晶的成核和生长过程机理非常复杂,尚没有统一的模型可完整描述成核过程,实际应用一般采用经验方程进行描述。本论文采用Arrhenius方程描述成核速率常数、生长速率常数与溶液温度的关系。对于溶析结晶过程,则将成核、生长速率级数与反溶剂浓度进行关联。在Matlab上采用lsqcurvefit函数,对采用不同降温和反溶剂添加策略时的结晶动力学参数进行非线性回归,完整结果见[12, 21],本论文中主要对其中一组实验进行阐述。图 12展示了当溶剂中不添加乙醇,并且降温速率采取1.0 ℃·min-1时,结晶过程的温度、浓度及成核、生长速率变化曲线。由图 12可知,在冷却结晶初始期间检测到爆发成核,IMP & GMP的浓度发生骤降,同时温度曲线中形成了成核放热平台,对应Δμ0/θ和ΔD[1,0]/θ可见峰值。对应过程CLD变化见图 13,CLD的剧烈变化是由于在结晶初期发生的爆发成核,曲线随后逐渐变平缓伴随着结晶釜内的晶核持续生长,大颗粒增多。
本研究对爆发成核阶段之后的动力学数据进行回归,采用不同降温速率及乙醇含量时的完整拟合结果详见[12, 21]。通过数据分析,发现存在一些问题:1)虽然拟合效果基本良好,但部分拟合结果中活化能数据为正值,对应吸热,但实验中发现IMP & GMP的晶核形成以及晶体生长过程均放热,与实际现象不符;2)拟合结果中的一些参数并没有体现出规律性的变化趋势。以上问题可能是因为溶液结晶的干扰因素非常多,是一个高度非线性、时变性并且机理复杂的物理和化学过程,许多工艺参数如结晶釜内的温度、局部溶质浓度等经常波动。以上因素直接导致了在回归动力学方程参数时,根据非线性优化过程的初值而反映结晶釜内的真实情况是具有很大挑战性的,难以通过拟合获得满意的效果。因此,在实际应用中,以上非线性求解的方法很难反映体系的全部实际情况及结晶过程的明确机制,仅具有一定的参考性和指导性。本研究的目的在于通过结晶动力学数据提出一种针对IMP & GMP冷却、溶析结晶的控制及优化手段,故不针对动力学方程拟合模型的关联进行深入探讨。
综上,该方法可准确捕捉IMP & GMP冷却结晶过程中各组分浓度变化及爆发成核等,能满足实际需求。
2.3 蒿甲醚结晶过程的闭环控制本研究针对疟疾特效药蒿甲醚溶析结晶所得产物粒度分布不理想的问题,采用NMPC和MHE耦合的方法,从结晶动力学研究入手,通过对过程模型进行适当的优化得到控制模型,从而提出了一种控制蒿甲醚溶析结晶过程以优化结晶产物CSD的有效策略[25]。
2.3.1 控制模型的建立首先建立溶析结晶控制过程的模型框架,如图 14所示。在实验前先设定目标CSD,以最小化过程模型预测的CSD间的差距为目标函数,同时设置对应的限制条件,包括操作变量的范围以及其他状态变量的约束等,然后开始第1次循环。基于粒数衡算方程,在每个时间点形成过程模型,结合PAT设备实时测得的结晶状态变量和操作条件,采用NMPC法对模型药物的溶析结晶过程进行模拟,得到初始优化后的操作参数。接下来参照其进行降温操作及反溶剂的添加。在此阶段根据已有的状态变量和测量值,采用MHE方法估算当前的状态变量,并继续由NMPC进行模拟预测,不断对操作参数进行修正和优化。重复以上循环过程直到结晶终点,通过不断更新得到最优操作曲线,从而获得粒度分布合理,标准方差小的蒿甲醚结晶产品。
在实施过程中采用Radau配点法结合Ipopt工具箱[26],将计算的时间范围划分为一定步长的若干区间,然后将配置点离散在各个区间,从而将NMPC转化为非线性规划问题,可高效求解方程。
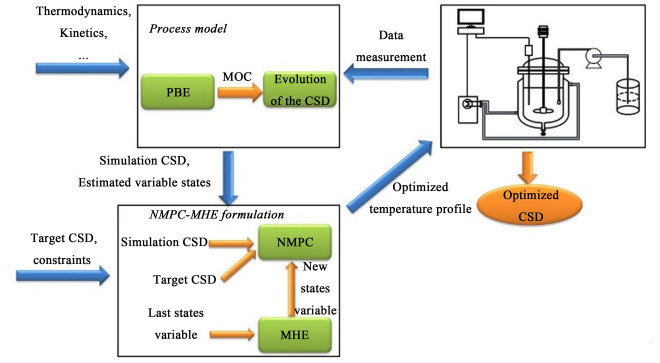
2.3.2 模型的封装和接入本研究以代码的形式将整个模型的建立及求解存于M文件中,然后写入Matlab软件的tool box,接入所开发的CPMCS系统即可建立针对溶析结晶过程的控制系统。封装后的控制通过建立的图形用户界面(Graphical user interface, GUI) 执行。点击即可调用Matlab,无需读取内部代码即可方便用户输入结晶过程模拟和控制参数,其预测控制流程图见图 15。
首先在过程模型(Process model)中输入其他物性数据,并进行基础结晶热力学、动力学参数的设定。根据以上信息即可初步计算得到结晶过程得的CSD演变;接下来输入目标CSD及相应的操作约束,由NMPC-MHE方法给出最优操作条件;最后,根据以上最优操作路线,通过水浴及蠕动泵等调节相应的结晶操作参数,同时结合FBRM等对体系内的状态变量进行实时监测,反馈至NMPC-MHE模型后不断优化操作参数,重复循环以上步骤不断接近目标CSD,最终得到最优操作变量,获得理想的结晶产品。
在实际操作时,用户需要打开GUI界面,单击下一步后进入结晶热力学、动力学参数输入界面。输入后单击下一步进入过程参数输入界面,人为设定NMPC-MHE法求解过程中的所需信息,包括条件约束(结晶釜内实际温度、反溶剂添加速率和搅拌速率的操作范围等)和目标CSD。初次循环开始后,开启实时测量以获取结晶过程的状态变量(浓度和粒度),以便在MHE估计状态变量的过程中修正模型噪音,提升模型精度。单击下一步后进行NMPC-MHE计算,其结果存储于Matlab的Workspace。
3 结论本研究以结晶过程的优化及结晶产品的质量控制为目标,基于QbD思路,结合PAT技术,借助LabVIEW平台,自主开发构建了包含3种无模型控制策略和闭环MPC控制策略的多参数反馈调控结晶系统。对5’-核苷酸二钠溶析/冷却结晶体系和蒿甲醚溶析结晶体系进行了动力学研究。结果表明,所开发的CPMCS系统实现了对溶液结晶过程关键参数的监测,有助于结晶过程模型的建立,所提出的基于结晶过程动力学参数的调控策略可基本满足实际应用需求。多参数反馈调控结晶系统在工业结晶过程工艺开发及优化、产品质量控制等方面的应用,值得关注。
| [1] |
LOH N D, SEN S, BOSMAN M, et al. Multistep nucleation of nanocrystals in aqueous solution[J]. Nature Chemistry, 2017, 9(1): 77-82. DOI:10.1038/nchem.2618 |
| [2] |
SOSSO G C, CHEN J, COX S J, et al. Crystal nucleation in liquids: Open questions and future challenges in molecular dynamics simulations[J]. Chemical Reviews, 2016, 116(12): 7078-7116. DOI:10.1021/acs.chemrev.5b00744 |
| [3] |
WANTHA L. Kinetics of the solution-mediated polymorphic transformation of organic compounds[J]. Current Pharmaceutical Design, 2018, 24(21): 2383-2393. DOI:10.2174/1381612824666180601093228 |
| [4] |
邢晓红, 欧阳金波, 周利民, 等. 限域空间内的结晶研究进展[J]. 化学工业与工程, 2022, 39(5): 39-48. XING Xiaohong, OUYANG Jinbo, ZHOU Limin, et al. Research progress of crystallization in confined space[J]. Chemical Industry and Engineering, 2022, 39(5): 39-48. (in Chinese) |
| [5] |
SZILÁGYI B, BORSOS Á, PAL K, et al. Experimental implementation of a Quality-by-Control (QbC) framework using a mechanistic PBM-based nonlinear model predictive control involving chord length distribution measurement for the batch cooling crystallization of L-ascorbic acid[J]. Chemical Engineering Science, 2019, 195: 335-346. DOI:10.1016/j.ces.2018.09.032 |
| [6] |
ZHANG T, SZILÁGYI B, GONG J, et al. Novel semibatch supersaturation control approach for the cooling crystallization of heat-sensitive materials[J]. AIChE Journal, 2020. DOI:10.1002/aic.16955 |
| [7] |
LIONBERGER R A, LEE S L, LEE L M, et al. Quality by design: Concepts for ANDAs[J]. The AAPS Journal, 2008, 10(2): 268-276. DOI:10.1208/s12248-008-9026-7 |
| [8] |
KACKER R, SALVADOR P M, STURM G S J, et al. Microwave assisted direct nucleation control for batch crystallization: Crystal size control with reduced batch time[J]. Crystal Growth & Design, 2016, 16(1): 440-446. |
| [9] |
BÖTSCHI S, RAJAGOPALAN A K, MORARI M, et al. Feedback control for the size and shape evolution of needle-like crystals in suspension. I. concepts and simulation studies[J]. Crystal Growth & Design, 2018, 18(8): 4470-4483. |
| [10] |
YANG Y, PAL K, KOSWARA A, et al. Application of feedback control and in situ milling to improve particle size and shape in the crystallization of a slow growing needle-like active pharmaceutical ingredient[J]. International Journal of Pharmaceutics, 2017, 533(1): 49-61. DOI:10.1016/j.ijpharm.2017.09.050 |
| [11] |
赵绍磊, 王灵宇, 吴送姑. 药物多晶型的研究进展[J]. 化学工业与工程, 2018, 35(3): 12-21. ZHAO Shaolei, WANG Lingyu, WU Songgu. Progress in the research of pharmaceutical polymorph[J]. Chemical Industry and Engineering, 2018, 35(3): 12-21. DOI:10.3969/j.issn.1006-7906.2018.03.003 (in Chinese) |
| [12] |
李炳辉. 基于实时监测的5'-呈味核苷酸二钠反溶剂结晶过程研究[D]. 广州: 华南理工大学, 2019 LI Binghui. The study of disodium 5'-ribonucleotide anti-solvent crystallization based on real-time monitoring platform[D]. Guangzhou: South China University of Technology, 2019 (in Chinese) |
| [13] |
唐凯. 多参数反馈调控结晶系统的初步开发[D]. 广州: 华南理工大学, 2014 TANG Kai. Primary development of multi-parameter feedback regulation and control system for crystallization[D]. Guangzhou: South China University of Technology, 2014 (in Chinese) |
| [14] |
NAGY Z K, FUJIWARA M, BRAATZ R D. Modelling and control of combined cooling and antisolvent crystallization processes[J]. Journal of Process Control, 2008, 18(9): 856-864. DOI:10.1016/j.jprocont.2008.06.002 |
| [15] |
ABU BAKAR M R, NAGY Z K, SALEEMI A N, et al. The impact of direct nucleation control on crystal size distribution in pharmaceutical crystallization processes[J]. Crystal Growth & Design, 2009, 9(3): 1378-1384. |
| [16] |
SALEEMI A N, RIELLY C D, NAGY Z K. Comparative investigation of supersaturation and automated direct nucleation control of crystal size distributions using ATR-UV/vis spectroscopy and FBRM[J]. Crystal Growth & Design, 2012, 12(4): 1792-1807. |
| [17] |
SALEEMI A, RIELLY C, NAGY Z K. Automated direct nucleation control for in situ dynamic fines removal in batch cooling crystallization[J]. CrystEngComm, 2012, 14(6): 2196-2203. DOI:10.1039/c2ce06288g |
| [18] |
SIMONE E, SALEEMI A N, TONNON N, et al. Active polymorphic feedback control of crystallization processes using a combined Raman and ATR-UV/vis spectroscopy approach[J]. Crystal Growth & Design, 2014, 14(4): 1839-1850. |
| [19] |
FALOLA A, BORISSOVA, A, WA NG, X. Extended method of moment for general population balance models including size dependent growth rate, aggregation and breakage kernels[J]. Computers & Chemical Engineering, 2013, 56: 1-11. |
| [20] |
LI B, SONG Y, SUN L, et al. Measurement of disodium 5'-inosinate and disodium 5'-guanylate in aqueous ethanol by attenuated total reflection ultraviolet method[J]. Chemical Engineering & Technology, 2019, 42(11): 2376-2385. |
| [21] |
ZHAO W, LI B, LIU S, et al. Kinetic study of complicated anti-solvent and cooling crystallization of disodium 5'-ribonucleotide[J]. Particuology, 2023, 73: 103-112. DOI:10.1016/j.partic.2022.05.001 |
| [22] |
BRAATZ R D. Advanced control of crystallization processes[J]. Annual Reviews in Control, 2002, 26(1): 87-99. |
| [23] |
TRIFKOVIC M, SHEIKHZADEH M, ROHANI S. Multivariable real-time optimal control of a cooling and antisolvent semibatch crystallization process[J]. AIChE Journal, 2009, 55(10): 2591-2602. |
| [24] |
FUJIWARA M, NAGY Z K, CHEW J W, et al. First-principles and direct design approaches for the control of pharmaceutical crystallization[J]. Journal of Process Control, 2005, 15(5): 493-504. |
| [25] |
SUN L, SONG Y, LI B, et al. A modified method for modelling, optimization and control of an anti-solvent crystallization process[J]. Chemical Engineering Science, 2020. DOI:10.1016/j.ces.2019.115253 |
| [26] |
WÄCHTER A, BIEGLER L T. On the implementation of an interior-point filter line-search algorithm for large-scale nonlinear programming[J]. Mathematical Programming, 2006, 106(1): 25-57. |
 2023, Vol. 40
2023, Vol. 40