2. 天津大学化工学院, 天津 300350
2. School of Chemical Engineering and Technology, Tianjin University, Tianjin 300350, China
超滤是一种将溶液进行净化、分离或浓缩的膜分离技术,主要用于截留悬浮固体、去除有机物并高效降低水体浊度[1],具有设备体积小、结构简单、投资费用低和易于实施等优势,被广泛应用于膜法水处理中[2]。然而超滤过程中由于滞留颗粒、胶体、大分子有机污染物和无机结垢造成的膜孔堵塞和膜污染加剧会导致超滤膜渗透通量下降[3],使超滤膜水处理效率降低。膜污染会导致更高的运行成本,缩短超滤膜使用寿命,这成为限制其发展的主要因素[4]。其中,天然有机物被认为是超滤滤膜污染的主要原因[5]。在水生环境中溶解的天然有机物主要是由腐殖质贡献的[6],腐殖质是低到中等分子量的难降解阴离子大分子物质,而腐植酸(HA)为腐殖质的重要组分之一。因此,如何维持高渗透通量和减轻天然有机物中腐殖质带来的膜污染对提高超滤膜水分离效率具有重要意义。
目前已有多种方法用于强化超滤膜法水处理过程,包括超滤膜改性[7, 8]、注气[9-11]和超声辅助[12, 13]等。超滤膜亲水性、孔隙率、表面粗糙度以及机械强度在膜分离过程中起着重要作用[14, 15],Erdal等[7]通过将聚砜与聚[2, 2'-(间苯撑)-5, 5'-二苯并咪唑]共混制备了新型聚砜复合超滤膜,其孔隙率、亲水性和热稳定性等膜特性都显著提高,这种复合膜与原始聚砜膜相比,牛血清白蛋白截留效率提高了33%,水通量增大了127 L ·m-2 ·h-1。Cui和Wrigh[16]观察到,在超滤过程中将空气注入进料流后,葡聚糖渗透通量可增加60%,染色葡聚糖渗透通量可增加113%,BSA溶液渗透通量可增加91%,同时截留效率可提高5%~10%。Muthukumaran等[12]在对乳清蛋白超滤过程中采用超声波辅助发现,超声波对渗透通量的增强系数在1.2~1.7之间。
近年来,微纳米气泡(MNBs)(直径为1.0 nm~102 μm)[17]在饮用水[18, 19]和废水[20, 21]处理方面引起广泛研究兴趣。由于其寿命长、面积体积比大和传质效率高等优势在超滤膜法水处理中表现出很好的应用潜力。在平板陶瓷膜超滤HA溶液之后鼓入微纳米气泡可以在不到6 h内完成膜清洗,渗透通量恢复到初始水平[22]。在对膜表面蛋白质去除中,电化学处理20 s产生的纳米气泡使蛋白质覆盖率降低26%~34%,此外膜表面预吸附的蛋白质也被电化学产生的纳米气泡去除[23],这说明微纳米气泡不仅可以用来去污,也可以用来防止膜表面污染。
本研究选用HA作为天然有机物模型污染物,在进料溶液和聚偏氟乙烯(PVDF)超滤膜污染去除过程中鼓入微纳米气泡(MNBs),研究直接鼓入微纳米气泡和预沉积微纳米气泡滤层对超滤渗透通量、截留效率的影响,以及微纳米气泡对膜污染去除效果。
1 实验材料与方法 1.1 实验材料和仪器设备聚偏氟乙烯(PVDF)超滤平板膜购自中科瑞阳膜技术(北京)有限公司,其截留相对分子质量为100 kDa,用于超滤实验的有效膜面积为1.81×10-3 m2。腐植酸(HA)购自上海阿拉丁生化科技股份有限公司,药品为分析纯,无需进一步纯化即可使用。实验用水均为去离子水。
微纳米气泡发生器(ZJC-NM-200L)购自上海河森保环境技术有限公司,电子天平(TD10001)购自天马衡基仪器有限公司,UV(V-6300)全扫购自上海市美谱达仪器有限公司,聚焦离子束电子束双束显微镜(FIBDBM, Crossbeam 550)购自德国Zeiss公司。
1.2 通量和截留效率分析超滤膜渗透通量计算方程式为:
| $ J=\frac{V}{A t} $ | (1) |
式(1)中:J为超滤膜的渗透通量,L ·m-2·h-1;V为渗透液体积,L;t为超滤时间,h;A是超滤膜有效过滤面积,m2。
超滤膜截留效率的计算式为:
| $ R_{\mathrm{e}}=\left(1-\frac{C_{\mathrm{e}}}{C_0}\right) \times 100 \% $ | (2) |
式(2)中:Re为截留效率, %;Ce和C0分别为进料溶液出水和进水浓度,mg ·L-1。
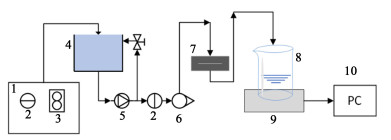
1.3 超滤实验本研究在死端过滤模式下将超滤单元与微纳米气泡发生器耦合来进行实验,工艺流程如图 1所示。为避免搅动对微纳米气泡造成干扰,在超滤时未加搅拌装置。
|
| 1—微纳米气泡发生器; 2—压力表; 3—空气流量计; 4—储料罐; 5—驱动泵; 6—液体转子流量计; 7—膜评价池; 8—烧杯; 9—电子天平; 10—电脑 图 1 超滤实验流程 Fig.1 The ultrafiltration experimental process |
| |
超滤操作流程如下。
(1) 在实验开始前将超滤膜在纯水中浸泡24 h以去除超滤膜表面的甘油等生产杂质。每个超滤膜在超滤循环开始前先以去离子水30 mL ·min-1的流速运行10 min,以达到稳定的渗透通量。
(2) 称量100.0 mg HA溶解于去离子水中,定容至100 mL容量瓶,制得1.0 g ·L-1 HA储备液,放在4 ℃的黑暗环境中储存,并在3 d内使用。
(3) 将储备液置于室温,用去离子水稀释至5.0 mg ·L-1制得工作溶液。用工作溶液润洗微纳米气泡发生器和超滤装置。
(4) 在超滤前,将储罐中的进料溶液送入微纳米气泡发生器处理10 min,控制微纳米气泡发生器空气流量为80 mL ·min-1,以产生含有大量微纳米气泡的溶液。
(5) 然后将含有微纳米气泡的HA工作溶液送入超滤膜评价池进行超滤分离实验。在超滤分离过程中,通过调节回流保持跨膜压差为恒压0.1 MPa,由泵驱动通过平板超滤膜的滤液。超滤膜渗透通量由与计算机相连的电子天平定时进行连续数据采集。
用J/J0的归一化通量(J0是纯水的渗透通量,J为进料溶液渗透通量)表示通量随时间的变化,每次超滤循环都选择新的并且通量相近的超滤膜进行实验,超滤膜的平均纯水通量为408.7(±8.9) L ·m-2 ·h-1。所有超滤实验均在25(±1) ℃下进行,并至少重复3次,记录平均值。
微纳米气泡减轻膜污染实验流程如下。
(1) 为使通量变化更显著,将储备液稀释至50.0 mg ·L-1,然后重复超滤操作流程中步骤(5)得到污染超滤膜。
(2) 用微纳米气泡发生器处理去离子水10 min,控制微纳米气泡发生器空气流量为80 mL ·min-1,制得微纳米气泡水。
(3) 清洗操作:将污染超滤膜在去离子水或微纳米气泡水中浸泡5 min,取出污染超滤膜再次进行超滤操作流程中步骤(5)。
(4) 反洗操作:将污染超滤膜反面朝上置于膜评价池中,调节超滤膜跨膜压差为0.2 MPa,控制膜评价池进水流量为30 mL ·min-1,用去离子水或微纳米气泡水作为进料溶液超滤反洗5 min。
1.4 HA浓度测定在样品通过0.45 μm孔径的针孔过滤器(Millipore,中国)过滤后,HA的浓度通过使用UV全扫(Mapada UV-6300,中国)在254 nm处测定。
1.5 滤饼层厚度测定将带有滤饼层的超滤膜自然晾干后通过离子束电子束双束切割超滤膜表面后利用聚焦离子束电子束双束显微镜(Crossbeam 550,德国)测定滤饼层厚度。
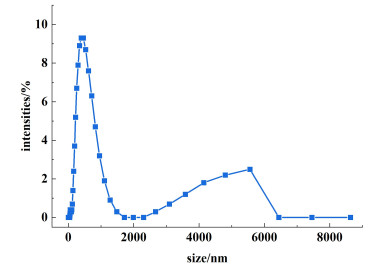
2 实验结果和讨论 2.1 微纳米气泡尺寸分布为了探究微纳米气泡发生器产生的气泡尺寸,通过对微纳米气泡发生器产生的气泡进行动态光散射测量分析(DLS)得到去离子水中微纳米气泡尺寸分布,如图 2所示。结果表明,微纳米气泡发生器产生的气泡尺寸分布在43.82~1 484 nm和2.6~5.6 μm之间,微纳米气泡发生器产生的气泡为微纳米气泡[17]。
|
| 图 2 微纳米气泡尺寸分布 Fig.2 Size distribution of MNBs |
| |
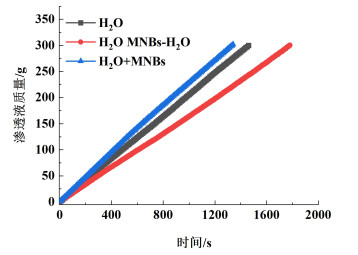
为比较不同微纳米气泡工艺处理超滤膜对去离子水的透过性,考察了向去离子水中直接鼓入MNBs(H2O+MNBs)和预沉积MNBs(H2O MNBs-H2O)后H2O渗透液质量随时间变化,实验结果如图 3所示。其中H2O MNBs-H2O为用微纳米气泡发生器在空气流量为80 mL ·min-1条件下处理去离子水10 min,将此微纳米气泡水(H2O+MNBs)超滤10 min,在超滤膜表面预沉积MNBs滤层,之后进行纯水超滤实验,测量其渗透液质量随时间变化。图 3显示,H2O、H2O MNBs-H2O和H2O+MNBs收集300 g渗透液所需时间分别为1 460、1 780和1 340 s,根据方程式(1)计算其渗透通量分别为408.7、335.2和445.3 L ·m-2 ·h-1。结果表明向去离子水中鼓入微纳米气泡使渗透通量增大了8.9%。而在超滤膜表面预沉积微纳米气泡滤层使去离子水渗透通量降低了18.0%。这是因为预沉积的微纳米气泡在超滤膜表面形成新的滤层,使过滤阻力增大,导致渗透通量下降。
|
| 图 3 不同微纳米气泡工艺渗透液质量随时间变化 Fig.3 The variation of permeate quality with time |
| |
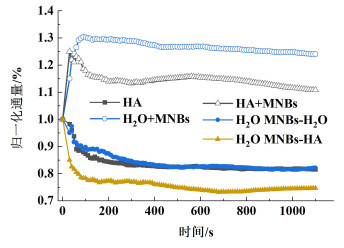
为研究不同MNBs处理工艺对HA溶液超滤过程中归一化通量的影响,通过J/J0计算了超滤时间为20 min内分别向H2O和HA溶液中直接鼓入MNBs和预沉积MNBs归一化通量变化(图 4)。结果表明,直接向H2O中鼓入微纳米气泡(H2O+MNBs)归一化通量峰值增大到1.3,超滤结束时其归一化通量为1.24,而H2O MNBs-H2O的归一化通量降低到0.8(图 4),这与图 3结果一致,结果表明直接向H2O中鼓入MNBs可以有效提高其归一化通量。
|
| 图 4 不同微纳米气泡工艺归一化通量随时间变化 Fig.4 The variation of naomalized flux with MNBs input with time |
| |
直接向HA溶液中鼓入MNBs(HA+MNBs)的归一化通量峰值为1.2,超滤结束后归一化通量下降到1.1;无微纳米气泡时归一化通量下降到0.8,而提前在超滤膜表面预沉积微纳米气泡滤层后超滤HA溶液(H2O MNBs-HA),其归一化通量低于无微纳米气泡时的归一化通量,超滤结束时归一化通量下降到0.7(图 4)。结果表明,向HA溶液中鼓入MNBs可有效提高其归一化通量,与H2O+MNBs相比,HA+MNBs归一化通量峰值下降了10%,这是由于HA堵塞了超滤膜孔,造成膜污染,导致渗透通量下降。
以上结果表明在进料溶液中鼓入MNBs后超滤渗透通量有效提高了10%~30%,这与Dayarathne等[24]观察到的结果一致,在反渗透过程中连续投加微纳米气泡(150~250 nm)时,渗透通量增加了24.6%。Wang等[25]提出,在微滤过程中,当气体流量从0.3增加到1.0 L ·min-1时,局部临界通量从23%增加到54%。而预沉积微纳米气泡滤层导致更大过滤阻力,使渗透通量降低了20%。
2.3 微纳米气泡对截留效率和膜污染影响为研究微纳米气泡强化过程对HA去除效率影响,通过对超滤过程中膜前和膜后HA溶液浓度测定,利用方程式(2)计算了超滤膜对HA的截留效率,结果如图 5所示。结果表明,HA的截留效率为39.1%,向HA溶液中鼓入微纳米气泡之后(HA+MNBs)的截留效率为61.1%,相较于HA提高了22.0%。H2O MNBs-HA的截留效率为41.6%,相较于HA截留效率提高了2.5%(图 5)。这说明直接鼓入MNBs和预沉积MNBs滤层均可有效提高HA的截留效率。这是由于MNBs具有负电界面,根据扩散双层理论[26],在扩散层中存在大量H+,溶液中MNBs吸引HA聚集,导致超滤膜有效截留聚集后的HA。

|
| 图 5 HA、H2O MNBs-HA、HA+MNBs截留效率 Fig.5 The variation of rejection coefficient to HA, H2O MNBs-HA, HA+MNBs |
| |
此外,Cui和Wrigh[16]观察到,在超滤过程中将空气注入进料流后,牛血清白蛋白(BSA)溶液截留效率提高5%~10%。Dayarathne等[24]观察到在反渗透过程中连续投加微纳米气泡(150~250 nm)时,截留效率增加0.8%。
HA、H2O MNBs-HA、HA+MNBs超滤循环结束后污染超滤膜实物图如图 6所示,从图 6中可以看出超滤结束后污染超滤膜表面颜色依次加深,说明超滤膜表面截留污染物量依次增加。这与图 5结果一致,污染超滤膜表面颜色随截留效率增大而加深。

|
| 图 6 HA、H2O MNBs-HA、HA+MNBs污染超滤膜 Fig.6 The fouled UF membrane after UF process of HA, H2O MNBs-HA, HA+MNBs |
| |
采用聚焦离子束电子束双束显微镜进一步分析了HA+MNBs和HA污染超滤膜表面滤饼层厚度,如图 7所示。结果表明,鼓入MNBs后污染膜表面滤饼层厚度为436.7(±18.6) nm[图 7(a)],无MNBs超滤膜表面滤饼层厚度为288.0(±9.7) nm[图 7(b)],这是因为鼓入MNBs增强了超滤膜归一化通量(图 4),超滤膜水分离效率提高,这加速了膜表面滤饼层的形成。

|
| 图 7 滤饼层厚度 Fig.7 The thickness of cake layer |
| |
超滤过程中由于污染物在膜孔和膜表面积累,很容易导致超滤膜渗透性下降[27]。超滤膜污染仍然是超滤膜法水处理技术广泛应用的主要障碍,定期清洗污染后的超滤膜仍是超滤中重要步骤,以去除污染物,恢复操作生产力[4]。膜污染包括可逆污染和不可逆污染,可逆污染通过一定的清洗方法可以去除,但清洗后仍残留的污染为不可逆污染,而不可逆污染不可用水力手段清洗去除[4]。研究表明,HA对超滤膜的污染以不可逆污染为主,HA大分子与膜表面之间存在静电作用力,其对超滤膜造成污染后不经过化学清洗难以全部去除[28, 29],孙丽华等[29]对20 mg ·L-1 HA污染超滤膜经水力反冲洗后归一化通量恢复了15%。然而化学清洗虽然能够有效去除膜污染,但频繁地化学清洗会造成膜材料损伤,缩短膜材料使用寿命[30]。因此开发新型环保的膜去污工艺对超滤膜法水处理技术的发展具有重要意义。
为研究H2O+MNBs清洗和反洗对HA污染超滤膜通量的恢复情况,考察了纯H2O和H2O+MNBs清洗和反洗前后归一化通量变化,结果如图 8所示。纯水清洗(H2O cleaning)即将污染超滤膜在纯水中浸泡5 min,纯水清洗后超滤HA(50 mg ·L-1)归一化通量恢复了7%[图 8(a)];微纳米气泡水清洗(H2O+MNBs cleaning)即将污染超滤膜浸泡在微纳米气泡水中5 min,微纳米气泡水清洗后超滤HA归一化通量恢复了28%[图 8(b)]。在纯水反洗(H2O BW)和微纳米气泡水反洗(H2O+MNBs BW)之后,HA归一化通量分别恢复了18%和43%[图 8(c)和8(d)]。结果表明,微纳米气泡水清洗和反洗去污工艺相较于纯水对污染超滤膜渗透通量恢复分别增强了21%和25%。这主要是由于微纳米气泡在坍塌过程中会产生活性氧化物种,例如羟基自由基[31],产生的羟基自由基能够通过氧化反应或水力冲刷减轻或去除膜表面上积聚的污垢[22]。此外,反洗过程中跨膜压差会提供更大的水力冲洗作用,从而更好的去除膜污染。

|
| 图 8 污染膜清洗或反洗后归一化通量变化 Fig.8 The variation of normalized flux of fouling membrane after cleaning or backwashing(BW) |
| |
1) 向进料溶液中直接鼓入微纳米气泡可有效增强超滤分离效率,其归一化通量增大了10%~30%,截留效率提高了2.5%~22.0%;而在超滤膜表面预沉积微纳米气泡滤层使归一化通量降低20%,截留效率提高仅2.5%,不利于超滤膜过程的增强。
2) HA+MNBs超滤污染膜表面滤饼层厚度为436.7(±18.6) nm,无MNBs时滤饼层厚度为288.0(±9.7) nm。H2O+MNBs清洗和反洗污染超滤膜后HA归一化通量分别恢复了28%和43%,与纯H2O清洗和反洗相比提高了21%和25%,MNBs有效增强了超滤膜污染的去除效果。
| [1] |
WARSINGER D M, CHAKRABORTY S, TOW E W, et al. A review of polymeric membranes and processes for potable water reuse[J]. Progress in Polymer Science, 2018, 81: 209-237. DOI:10.1016/j.progpolymsci.2018.01.004 |
| [2] |
季伟, 李十中. 鼓泡超滤法用于木糖生产过程的探讨[J]. 化学工业与工程, 2007, 24(1): 52-55. JI Wei, LI Shizhong. Application of gas sparging to the production process of xylose by ultrafiltration[J]. Chemical Industry and Engineering, 2007, 24(1): 52-55. DOI:10.3969/j.issn.1004-9533.2007.01.014 (in Chinese) |
| [3] |
AHMED F, LALIA B S, KOCHKODAN V, et al. Electrically conductive polymeric membranes for fouling prevention and detection: A review[J]. Desalination, 2016, 391: 1-15. DOI:10.1016/j.desal.2016.01.030 |
| [4] |
SHI X, TAL G, HANKINS N P, et al. Fouling and cleaning of ultrafiltration membranes: A review[J]. Journal of Water Process Engineering, 2014, 1: 121-138. DOI:10.1016/j.jwpe.2014.04.003 |
| [5] |
KAIYA Y, ITOH Y, FUJITA K, et al. Study on fouling materials in the membrane treatment process for potable water[J]. Desalination, 1996, 106(1/2/3): 71-77. |
| [6] |
YUAN W, ZYDNEY A L. Humic acid fouling during ultrafiltration[J]. Environmental Science and Technology, 2000, 34(23): 5043-5050. DOI:10.1021/es0012366 |
| [7] |
EREN E, SARIHAN A, EREN B, et al. Preparation, characterization and performance enhancement of polysulfone ultrafiltration membrane using PBI as hydrophilic modifier[J]. Journal of Membrane Science, 2015, 475: 1-8. DOI:10.1016/j.memsci.2014.10.010 |
| [8] |
ZHAO Y, LU J, LIU X, et al. Performance enhancement of polyvinyl chloride ultrafiltration membrane modified with graphene oxide[J]. Journal of Colloid and Interface Science, 2016, 480: 1-8. DOI:10.1016/j.jcis.2016.06.075 |
| [9] |
CABASSUD C, LABORIE S, DURAND-BOURLIER L, et al. Air sparging in ultrafiltration hollow fibers: Relationship between flux enhancement, cake characteristics and hydrodynamic parameters[J]. Journal of Membrane Science, 2001, 181(1): 57-69. DOI:10.1016/S0376-7388(00)00538-X |
| [10] |
MERCIER M, FONADE C, LAFFORGUE-DELORME C. How slug flow can enhance the ultrafiltration flux in mineral tubular membranes[J]. Journal of Membrane Science, 1997, 128(1): 103-113. DOI:10.1016/S0376-7388(96)00317-1 |
| [11] |
TAITEL Y, BARNEA D, DUKLER A E. Modelling flow pattern transitions for steady upward gas-liquid flow in vertical tubes[J]. AIChE Journal, 1980, 26(3): 345-354. DOI:10.1002/aic.690260304 |
| [12] |
MUTHUKUMARAN S, KENTISH S E, ASHOKKUMAR M, et al. Mechanisms for the ultrasonic enhancement of dairy whey ultrafiltration[J]. Journal of Membrane Science, 2005, 258(1/2): 106-114. |
| [13] |
CHAI X, KOBAYASHI T, FUJⅡ N. Ultrasound effect on cross-flow filtration of polyacrylonitrile ultrafiltration membranes[J]. Journal of Membrane Science, 1998, 148(1): 129-135. DOI:10.1016/S0376-7388(98)00145-8 |
| [14] |
曲连续, 张犇, 张庆男, 等. PAN超滤膜的常压介质阻挡放电等离子体亲水改性[J]. 化学工业与工程, 2013, 30(1): 38-41, 52. QU Lianxu, ZHANG Ben, ZHANG Qingnan, et al. Hydrophilic modification of polyacrylonitrile ultrafiltration membrane via atmospheric dielectric barrier discharge(DBD) plasma[J]. Chemical Industry and Engineering, 2013, 30(1): 38-41, 52. DOI:10.13353/j.issn.1004.9533.2013.01.010 (in Chinese) |
| [15] |
郭春刚, 吕经烈, 张召才, 等. PVDF-TiO2复合中空纤维膜的制备与表征[J]. 化学工业与工程, 2013, 30(6): 5-10. GUO Chungang, LYU Jinglie, ZHANG Zhaocai, et al. Preparation and characterization of PVDF-TiO2 composite hollow fiber membrane[J]. Chemical Industry and Engineering, 2013, 30(6): 5-10. DOI:10.3969/j.issn.1006-7906.2013.06.002 (in Chinese) |
| [16] |
CUI Z, WRIGHT K I T. Gas-liquid two-phase cross-flow ultrafiltration of BSA and dextran solutions[J]. Journal of Membrane Science, 1994, 90(1/2): 183-189. |
| [17] |
TEMESGEN T, BUI T T, HAN M, et al. Micro and nanobubble technologies as a new horizon for water-treatment techniques: A review[J]. Advances in Colloid and Interface Science, 2017, 246: 40-51. DOI:10.1016/j.cis.2017.06.011 |
| [18] |
BATAGODA J H, HEWAGE S D A, MEEGODA J N. Nano-ozone bubbles for drinking water treatment[J]. Journal of Environmental Engineering and Science, 2019, 14(2): 57-66. DOI:10.1680/jenes.18.00015 |
| [19] |
REUTER F, LAUTERBORN S, METTIN R, et al. Membrane cleaning with ultrasonically driven bubbles[J]. Ultrasonics Sonochemistry, 2017, 37: 542-560. DOI:10.1016/j.ultsonch.2016.12.012 |
| [20] |
DENG S, JOTHINATHAN L, CAI Q, et al. FeOx@GAC catalyzed microbubble ozonation coupled with biological process for industrial phenolic wastewater treatment: Catalytic performance, biological process screening and microbial characteristics[J]. Water Research, 2021. DOI:10.1016/j.watres.2020.116687 |
| [21] |
WANG Y, WANG J, DING Y, et al. In situ generated micro-bubbles enhanced membrane antifouling for separation of oil-in-water emulsion[J]. Journal of Membrane Science, 2021. DOI:10.1016/j.memsci.2020.119005 |
| [22] |
KHALED A A A, SUN C, HUA L, et al. Colloidal properties of air, oxygen, and nitrogen nanobubbles in water: Effects of ionic strength, natural organic matters, and surfactants[J]. Environmental Engineering Science, 2018, 35(7): 720-727. DOI:10.1089/ees.2017.0377 |
| [23] |
WU Z, CHEN H, DONG Y, et al. Cleaning using nanobubbles: Defouling by electrochemical generation of bubbles[J]. Journal of Colloid and Interface Science, 2008, 328(1): 10-14. DOI:10.1016/j.jcis.2008.08.064 |
| [24] |
DAYARATHNE H N P, CHOI J, JANG A. Enhancement of cleaning-in-place (CIP) of a reverse osmosis desalination process with air micro-nano bubbles[J]. Desalination, 2017, 422: 1-4. DOI:10.1016/j.desal.2017.08.002 |
| [25] |
WANG J, FANE A, CHEW J W. Effect of bubble characteristics on critical flux in the microfiltration of particulate foulants[J]. Journal of Membrane Science, 2017, 535: 279-293. DOI:10.1016/j.memsci.2017.04.047 |
| [26] |
MEEGODA J N, HEWAGE S A, BATAGODA J H. Application of the diffused double layer theory to nanobubbles[J]. Langmuir: the ACS Journal of Surfaces and Colloids, 2019, 35(37): 12100-12112. DOI:10.1021/acs.langmuir.9b01443 |
| [27] |
GAO W, LIANG H, MA J, et al. Membrane fouling control in ultrafiltration technology for drinking water production: A review[J]. Desalination, 2011, 272(1/2/3): 1-8. |
| [28] |
JONES K L, O'MELIA C R. Protein and humic acid adsorption onto hydrophilic membrane surfaces: Effects of pH and ionic strength[J]. Journal of Membrane Science, 2000, 165(1): 31-46. DOI:10.1016/S0376-7388(99)00218-5 |
| [29] |
孙丽华, 俞天敏, 田海龙, 等. 典型有机物与超滤膜界面作用及膜污染机制研究[J]. 环境科学学报, 2016, 36(2): 530-536. SUN Lihua, YU Tianmin, TIAN Hailong, et al. Interaction of typical organic matters on ultrafiltration membrane and the mechanism of membrane fouling[J]. Acta Scientiae Circumstantiae, 2016, 36(2): 530-536. (in Chinese) |
| [30] |
TIAN J, XU Y, CHEN Z, et al. Air bubbling for alleviating membrane fouling of immersed hollow-fiber membrane for ultrafiltration of river water[J]. Desalination, 2010, 260(1/2/3): 225-230. |
| [31] |
LIU S, OSHITA S, KAWABATA S, et al. Identification of ROS produced by nanobubbles and their positive and negative effects on vegetable seed germination[J]. Langmuir: The ACS Journal of Surfaces and Colloids, 2016, 32(43): 11295-11302. DOI:10.1021/acs.langmuir.6b01621 |
 2022, Vol. 39
2022, Vol. 39





