近年来,随着各种芳香族有机化合物在工业上的大规模应用,水污染等环境问题变得日益严重。这些芳香族有机化合物本身具有较强的毒性和难降解性,一旦排放到环境中,就会对生态环境以及人类健康产生重大威胁[1-3]。例如,广泛用于制备聚碳酸酯和环氧树脂的中间体原料双酚A(BPA),不仅能够直接破坏水体生态系统平衡,而且能够通过食物链传播转移到人类自身,干扰人体的内分泌系统[4, 5]。因此,为适应绿色清洁可持续发展战略,高效降解残留有机污染物已经成为一项重大课题。
与传统的水处理方法如物理吸附、膜过滤和生物降解等相比,高级氧化工艺(AOPs)能够通过产生强氧化性物质来有效降解水中有机污染物[6-8]。其中,基于过一硫酸盐(PMS)的高级氧化工艺(AOPs)因其能够产生具有更高氧化还原电位(2.5~3.1 eV)和较宽的pH值(2.0~8.0)适用范围的硫酸根自由基(SO4·-)而被广泛应用[2, 9-11]。为提高PMS的活化效率,研究人员陆续探索了能量活化、过渡金属活化和非金属碳活化等活化方式[3, 12-14]。然而能量活化过程会导致能量损失,造成能量浪费。金属基活化容易导致有毒金属浸出,引发二次污染。与上述方法相比,碳基催化剂具有环境友好、热稳定性好等优点,在水体有机污染物的绿色修复中具有广阔的应用前景[1, 7, 15]。
以往的研究表明碳基催化剂在活化PMS中表现出的活性较低,因此通过改性提高其催化活性至关重要[16]。近年来,对碳材料进行杂原子(如N、B、S或者P)掺杂成为提高碳材料催化性能的研究热点[1, 17]。其中氮原子与碳原子具有相似的原子半径,易于掺杂进而获得较高的负载,同时2者具有不同的电负性有利于调整局部电子结构,因此氮原子掺杂是碳材料改性的理想选择[18]。具体而言,氮原子掺杂具有如下优势:(1)产生更多的缺陷位点和官能团;(2)通过sp2共轭激活sp2碳的π电子进而增强电子迁移率;(3)改变与掺杂N原子相邻的局部碳原子的电子密度[7, 18]。然而,对于氮掺杂碳基催化剂,过一硫酸盐活化过程中起增强碳催化作用的主要活性位点仍然存在争议,因此探索其活性位点对于活化PMS过程的理解也有着积极意义。
在本项工作中,我们使用原位聚合法制备了氮掺杂的中空多孔碳球(NHPS),并将其运用于PMS活化降解BPA体系。在此基础上,通过动力学分析,并结合SEM、HRTEM、BET、XPS、Raman等多种表征手段对催化剂的主要活性位点进行了初步探索,结果表明石墨氮是主要的活性位点。此外还利用猝灭实验和电化学测试对PMS活化过程中的活性氧物种进行了研究,进一步确定超氧自由基(O2·-)是NHPC-800/PMS体系中的负责BPA降解的主要活性物种。
1 实验部分 1.1 实验材料正硅酸乙酯[Si(OC2H5)4];氨水(NH4OH, AR, 质量分数为25%~28%;乙醇(C2H6O,AR);氢氧化钠(NaOH);过一硫酸盐(2KHSO5 ·3KHSO4 ·K2SO4)等购自上海阿拉丁;盐酸多巴胺(C8H11NO2 ·HCl)购自上海西格玛;甲醇(MeOH)、叔丁醇(TBA)、呋喃甲醇(FFA)、对苯醌(p-BQ),色谱纯等购自天津元立化工有限公司。
1.2 催化剂制备首先,将70 mL乙醇,10 mL去离子水,2.8 mL氨水在室温下(25 ℃)搅拌5 min。然后,将2.8 mL正硅酸乙酯逐滴加入上述混合溶液中并不断搅拌。30 min后加入400 mg盐酸多巴胺,并将混合物在室温下搅拌12 h。将反应溶液离心(12 000 r ·min-1) 并使用去离子水和无水乙醇交替洗涤3次,所得前驱体于60 ℃真空干燥箱干燥12 h。将干燥后的产物置于管式炉中氮气氛围下,以2 ℃ ·min-1的速率分别升温到700、800和900 ℃并保温5 h。待自然降温后,取出样品于2 mol ·L-1的NaOH溶液中,80 ℃下搅拌12 h以除去模板。对悬浊液进行抽滤并用去离子水进行洗涤,将滤饼置于60 ℃鼓风干燥箱中充分干燥,收集干燥后的样品。
1.3 双酚A降解的性能测试选取过硫酸氢钾(PMS)为氧化剂,双酚A(BPA)为模型污染物,测试所制备材料的催化性能。BPA降解的性能测试实验于室温(25 ℃)下在100 mL螺口瓶中进行,具体的操作过程如下:首先将5 mg催化剂加入到含有100 mL BPA(20×10-6)溶液的螺口瓶中,并通过超声的方式使其分散均匀。随后将螺口瓶置于磁力搅拌器上以300 r ·min-1的速度均匀搅拌,加入30 mg过硫酸氢钾(PMS)开始降解反应。反应过程中,每隔一段时间使用移液枪移取0.5 mL反应溶液并将其与0.5 mL甲醇充分混合,使用0.22 μm的滤膜过滤混合溶液除去固体催化剂,将所得液体注入液相色谱仪的进样瓶中,使用高效液相色谱仪进行分析。对于猝灭实验,则是在加入PMS前向溶液中添加适量的猝灭剂,其他步骤同上。对于稳定性实验,每轮稳定性实验循环后对反应溶液迅速过滤并用去离子水和无水乙醇对催化剂交替洗涤3次,以备下次使用。
1.4 电化学测试电化学测量在CHI760电化学工作站上进行,主要包括工作电极的准备工作和测试2部分。工作电极的准备工作:首先将5 mg的催化剂溶解在475 μL无水乙醇和475 μL去离子水的混合溶液中,再滴加50 μL的Nafion溶液并超声30 min使催化剂均匀分散,然后移取5 μL分散液滴于玻碳电极的表面,室温下干燥以备测试。开路电位的测试:以负载催化剂的玻碳电极为工作电极、Ag/AgCl电极为参比电极、碳棒作为对电极组成三电极体系进行开路电位测试。采用开路电压-时间模型(OCPT)测试了材料在不同电解质条件下的开路电压值变化。测试过程中,将PMS和BPA依次加入超纯水中监测开路电位(OCP)的变化,PMS和BPA的最终质量浓度和质量分数分别为1 g·L-1和10×10-6。
1.5 催化剂表征X射线衍射(XRD)图谱由Bruker Nonius D8 FOCUS X射线仪器获得。拉曼光谱由Horiba LabRAM HR Evolution(532 nm激光激发)获得。X射线光电子能谱(XPS)由Thermo ESCALAB 250XI光谱仪记录。Brunauer-Emmett-Teller(BET)比表面积由Bjbuilder SSA-7000仪器获得。通过扫描电子显微镜(SEM,Hitachi S8100)和透射电子显微镜(TEM,JEM-F200)获得样品的形态。像差校正的高角度环形暗场扫描透射电子显微镜(AC HAADF-STEM)和X射线光谱(EDS)映射由JEOL JEM-ARM200F STEM/TEM仪器完成。
2 结果与讨论 2.1 材料表征与分析利用原位聚合法制备了二氧化硅(SiO2)/聚多巴胺(PDA)原位共聚复合颗粒[19],后经过高温煅烧(700、800和900 ℃)和模板刻蚀,得到氮掺杂的中空多孔碳球(N-doping hollow porous carbon spheres),分别记为NHPC-700、NHPC-800和NHPC-900。
图 1为氮掺杂中空多孔碳球(NHPC-800)的SEM、TEM图以及相应的mapping元素分布图。

|
| 图 1 NHPC-800的(a)、(b)SEM图、(c)TEM图及(d)元素分布图 Fig.1 (a); (b) SEM images of NHPC-800; (c) TEM image of NHPC-800; (d) EDX elemental mapping images of NHPC-800 |
| |
如图 1(a)和图 1(b)所示,NHPC-800呈均匀的球状形态,粒径为200 nm左右,同时根据几处破碎的粒子可以初步判断其中空结构。TEM[图 1(c)]进一步证明了样品NHPC-800具有彼此交联的均匀中空球形结构,与SEM图像结果相一致。图 1(d)为NHPC-800的mapping图,可以看出C、N和O 3种元素均匀分布,证实了杂原子N成功地掺杂到了C基底中。
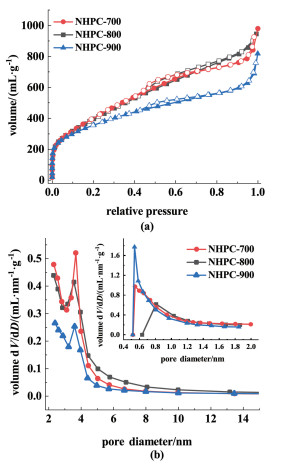
图 2(a)和图 2(b)分别为氮掺杂中空多孔碳球(NHPC)的氮气吸附-脱附曲线以及相应的孔径分布曲线。
|
| 图 2 NHPC-700、NHPC-800和NHPC-900的(a)氮气吸附-脱附曲线和(b)孔径分布曲线 Fig.2 (a) Nitrogen adsorption-desorption cure; (b) corresponding pore size distribution of NHPC-700, NHPC-800, NHPC-900 |
| |
由图 2(a)可以看出,NHPC的吸脱附曲线呈现出明显的I型和IV型等温线组合的形式。当相对压力P/P0在0~0.1之间时,吸附曲线急剧增加,说明所制备的样品中存在丰富的微孔结构,而相对压力(P/P0)在0.4~1.0时,吸附曲线所表现出的滞后循环说明样品中存在介孔结构,与图 2(b)的孔径分布曲线相对应。NHPC-700、NHPC-800和NHPC- 900的比表面积分别为1 530、1 480和1 277 m2·g-1,且其孔径分布主要集中在0.6~1.2 nm的微孔以及4 nm左右的介孔。各样品所具有的大比表面积以及多级孔结构得益于原位二氧化硅模板的生成和原位聚合过程中二氧化硅初级粒子的造孔作用。以上结果充分说明采用原位聚合方法制备的样品具有较大的比表面积以及多级孔径结构,有利于后续催化氧化反应的进行。
图 3为氮掺杂的中空多孔碳球(NHPC)样品的拉曼(Raman)光谱。

|
| 图 3 NHPC-700、NHPC-800和NHPC-900的拉曼光谱 Fig.3 The Raman spectra of NHPC-700, HNPC-800, NHPC-900, respectively |
| |
如图 3所示,所有样品均在1 330和1 590 cm-1处出现了明显的D峰和G峰。D峰反映了碳层中的缺陷和无序度[20],G峰则代表碳结构中sp2杂化碳的平面振动[21]。D峰和G峰的强度比值一定程度上能够反映材料的缺陷程度。随着热解温度的升高,部分掺杂的N原子被去除从而产生了更多的缺陷,但与此同时材料的石墨化程度也会提高,因此不同热解温度下的NHPC表现出接近的ID/IG值,即不同热解温度下的NHPC-700、NHPC-800和NHPC-900 3种材料具有相似的缺陷程度。
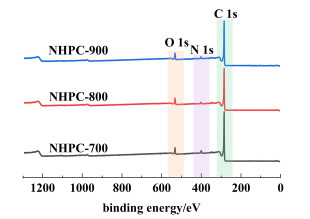
采用X射线光电子能谱(XPS)对样品的表面元素组成及化学状态进行详细分析。NHPC的XPS全谱图(图 4)中出现了明显的C 1s、N 1s以及O 1s的峰,说明样品中存在C、N和O 3种元素,其中氮掺杂中空多孔碳球(NHPC)中的N和O元素主要来源于前驱体多巴胺的炭化过程。
|
| 图 4 NHPC-700、NHPC-800和NHPC-900的XPS总谱 Fig.4 The XPS spectra of NHPC-700, NHPC-800, NHPC-900, respectively |
| |
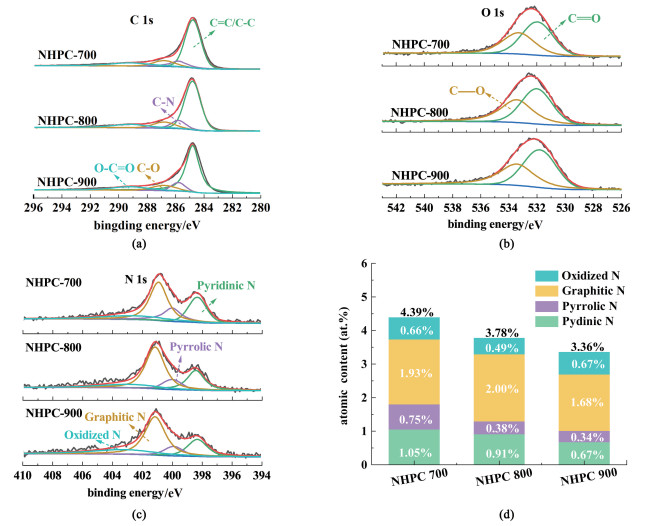
C 1s的高分辨率图谱[图 5(a)]中,289.1、287.0、285.6和284.8 eV处分别对应C=O、C—O、C—N和C—C 4个特征峰。在O 1s的高分辨率图谱[图 5(b)]中,于531.5和533.5 eV处出现了分别对应C=O和C—O的2个特征峰。这些吸电子基团可以调节相邻碳原子的电荷分布,提高BPA在碳材料上的吸附能力。由N 1s的高分辨率图谱[图 5(c)],可以观察到吡啶N(398.3 eV)、吡咯N(400.0 eV)、石墨N(401.0 eV)以及氧化N(403.0 eV) 4个特征峰[22, 23]。我们进一步分析了不同样品中的各类N含量。如图 5(d)所示,NHPC-700、NHPC- 800和NHPC-900中的摩尔分数分别为4.39%、3.78%和3.36%,呈现出随热解温度的升高,N掺杂含量在逐步下降的趋势。这与文献中所报道的高温退火温度下(>500 ℃)C—N键的断裂会导致碳材料中部分N的损失现象相符[24]。与此同时,观察到样品中石墨N的含量随着煅烧温度呈现出先增加后降低的趋势,在NHPC-800中达到2.00%的极值。石墨N具有较高的热稳定性,高温下吡啶N和吡咯N易于转化成更稳定的石墨N[8, 20]。因此,当热解温度由700 ℃上升到900 ℃时,石墨N在样品中的含量占比呈现上升的趋势,但热解温度偏高会造成样品中部分N原子的损失[25]。综合上所述,NHPC-800中石墨N的含量最高,而吡啶N和吡咯N在NHPC-700、NHPC-800和NHPC-900中的含量则都是呈现逐步降低的趋势。
|
| 图 5 NHPC-700、NHPC-800和NHPC-900的(a)高分辨率C 1s谱;(b)高分辨率O 1s谱;(c)高分辨率N 1s谱;(d)不同N种类的摩尔分数 Fig.5 (a) High-resolution C 1s spectra; (b) high-resolution O 1s spectra; (c) high-resolution of N 1s spectra; (d) the atomic percentage of different nitrogen species of NHPC-700, NHPC-800, NHPC-900 |
| |
为了对比研究不同样品的催化活性,选取过硫酸氢钾(PMS)为氧化剂,对NHPC-700、NHPC-800和NHPC-900进行BPA降解的催化性能测试。
从图 6(a)中可以看出,NHPC催化剂对BPA的吸附较弱,30 min的时间吸附量少于20%,并且单独的PMS对BPA几乎不表现出氧化活性。然而当NHPC与PMS同时加入到含有污染物BPA的溶液中时,BPA的降解速率得到大幅度提升。值得注意的是,NHPC-800/PMS体系表现出最优异的BPA降解性能,能够在30 min之内去除100%的BPA。然而,NHPC-700/PMS和NHPC-900/PMS体系在30 min之内分别完成了90%和50%的BPA的降解。为更直观比较不同催化剂的催化性能,我们通过拟一级动力学对不同体系的BPA降解的表观反应速率常数(kobs)进行拟合[图 6(b)]。NHPC-800/PMS体系中BPA的kobs为0.10 min-1,分别是NHPC-700/ PMS体系和NHPC-900/PMS体系kobs的1.43倍和5.00倍,体现出NHPC-800优异的PMS活化性能。

|
| 图 6 NHPC-700、NHPC-800、NHPC-900的(a)BPA吸附和降解曲线和(b)相应的表观反应速率常数(kobs) Fig.6 (a) BPA adsorption and degradation on NHPC-700, NHPC-800, NHPC-900; (b) the corresponding apparent reaction rate constant |
| |
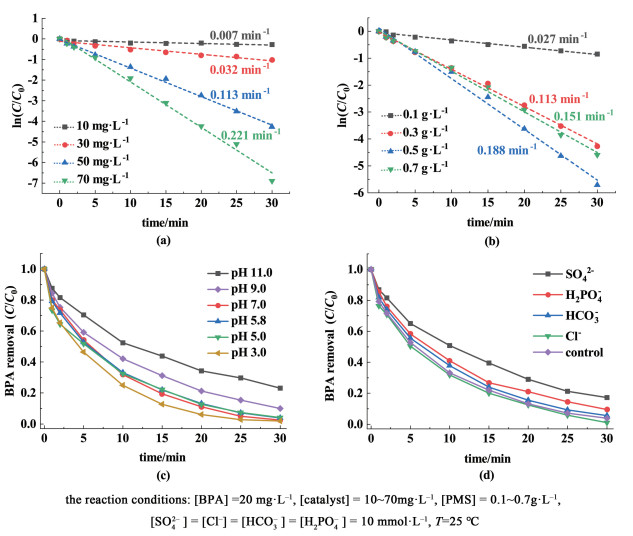
图 7(a)和图 7 (b)展示了不同浓度催化剂添加量以及氧化剂PMS浓度对BPA降解性能的影响。
|
| 图 7 (a) 不同催化剂浓度下和(b)不同PMS浓度下BPA降解的拟一级动力学拟合;(c)不同初始pH值下BPA降解曲线;(d)不同无机阴离子存在下BPA的降解曲线 Fig.7 The pseudo-first-order kinetic fitting on BPA degradation on (a)different catalysts dosages; (b)PMS concentration; effect of (c)initial pH; (d) inorganic anions on BPA degradation |
| |
从图 7(a)可以看出,当体系中催化剂浓度从10 mg ·L-1增加到70 mg ·L-1时,BPA的降解速率不断增加。其相应的降解反应速率(kobs)由0.007 min-1提升到0.221 min-1,这表明反应活性物种的生成量与催化剂用量成正比。对于PMS浓度的影响,BPA的降解效率随着PMS的浓度的增加呈现先增后降低的趋势[图 7(b)]。当PMS的溶液浓度从0.1 g ·L-1提高到0.5 g ·L-1时,相应的BPA的降解反应速率(kobs)从0.027 min-1增加到0.188 min-1,说明随着PMS添加量的增加,有更多的活性氧物种被激活从而提高了BPA降解速率;但是当PMS的溶液浓度从0.5 g ·L-1提高到0.7 g ·L-1时,其kobs下降至0.151 min-1,说明当体系中PMS浓度过高时会产生自我抑制现象,高浓度的PMS反而会阻碍BPA与活性氧物种的接触导致其降解速率大大降低[26]。接下来测定了NHPC-800/PMS体系不同初始pH值(3~11)下BPA的降解曲线[如图 7(c)所示],未调节的BPA反应溶液的初始pH值为5.8。实验结果表明,当BPA反应溶液的初始pH值在3~7范围内波动时,BPA能够在30 min内被完全去除;而当初始溶液的pH值进一步增加到9或11时,BPA的降解受到了抑制,但是仍能去除80%以上BPA。以上结果表明,NHPC-800/PMS体系在酸性、中性以及碱性条件下均具有优异的BPA降解性能,其中碱性条件下的催化性能的下降可能是因为OH-与HSO5-在催化剂表面存在一定的竞争吸附现象。此外,探究了不同无机阴离子存在下对BPA降解的影响[图 7(d)]。一般来说,废水中的无机阴离子能够被PMS活化产生的SO4·-和·OH氧化,因此无机阴离子的存在可能会与BPA竞争SO4·-和·OH从而对BPA的降解产生负面影响。当NHPC-800/PMS体系分别添加10 mmol ·L-1 Cl-、HCO3-和H2PO4-时,BPA的降解速率几乎不受影响。相比之下,NHPC-800/PMS体系中SO42- (10 mmol ·L-1)的存在使得BPA的降解效率降低,这种抑制作用有可能是因为溶液中一定量的SO42-使得SO4·-/SO42-的氧化还原电位降低,进而影响了其他ROS的生成,从而抑制了BPA的降解。在NHPC-800/PMS体系中,Cl-、HCO3-和H2PO4-的存在对BPA降解的影响甚微,因此PMS活化过程可能不是由SO4·-或者·OH主导。
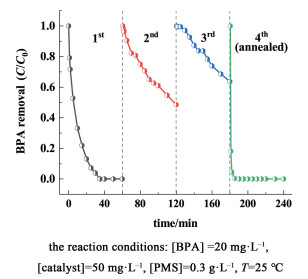
2.3 稳定性测试除了材料催化活性外,通过稳定性循环实验评估了材料NHPC-800的稳定性。如图 8所示,经过水洗和醇洗处理,NHPC-800催化剂的性能在3次稳定性循环实验中逐渐下降,在60 min的反应时间内依次催化降解了100%、50%和40%的BPA。NHPC-800催化性能在稳定性循环实验中逐步下降,可能是氧化环境中样品表面化学性质发生变化以及活性位点被吸附在样品表面的中间产物所覆盖而导致[17, 27]。热处理能够去除所述被覆盖中间体并恢复催化剂上的活性位点[28]。为恢复样品活性,收集3轮循环实验之后的样品在800 ℃ N2氛围下高温退火5 h,实验结果表明在第4次循环测试中,热处理过后的样品仍可达到100%的BPA降解率,说明样品活性能够通过简单热处理得到有效恢复。
|
| 图 8 NHPC-800的稳定性测试 Fig.8 The stability test of NHPC-800 |
| |
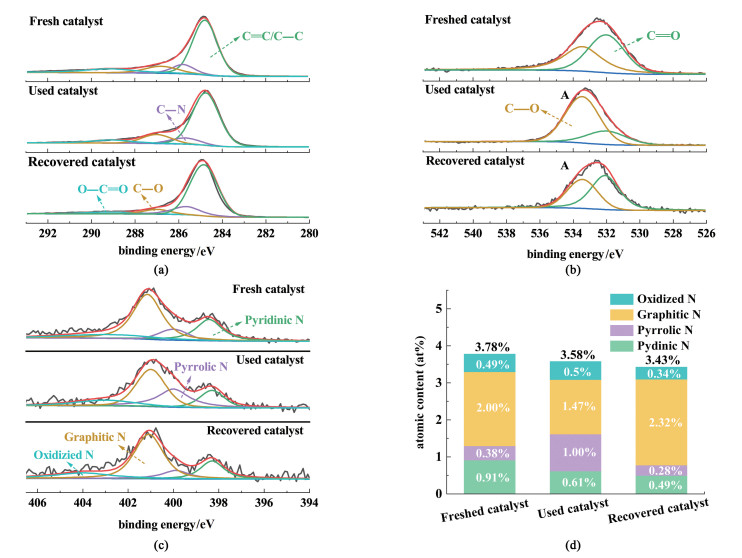
为探究原因,我们对反应前、反应后和热处理后催化剂进行XPS表征和Raman测试。由图 9(a)可知,反应后的C—O含量由7.78%(摩尔分数,下同)上升到12.58%,热处理后C—O含量由12.58%降到6.43%。结合O1s的高分辨率图谱可知催化剂参与反应过程中,其表面的C—O含量增加,说明催化剂表面发生了化学变化,结合反应前后的C、N、O元素含量的变化(表 1)以及反应后的催化剂缺陷水平的明显降低(图 10),可知催化剂在高氧化环境中被氧化,碳骨架上生成许多含氧官能团[6]。由高分辨率的N 1s图谱9(c)和相应各构型氮含量[图 9(d)]可知,石墨N从2.00% 降低到1.47%,而热处理后其含量上升到2.32%。石墨N含量的变化与反应前、后和热处理后催化能力的变化一致。因此,碳材料表面化学性质的改变(含氧官能团的增加)以及石墨N含量的下降是催化剂性能下降的原因。经过热处理(800 ℃,5 h),部分不稳定的吡啶N和吡咯N在高温下再一次转化成石墨N,结合热处理前后的C、N、O元素含量的变化(表 1)以及热处理后催化剂缺陷水平的恢复(图 10)可知催化剂表面化学性质得以恢复,同时由于热处理后的石墨N的含量相比未使用的催化剂的含量大大上升,因此其催化性能得到有效提升。
|
| 图 9 反应前催化剂、反应后催化剂、再生催化剂的(a) 高分辨率C 1s谱;(b) 高分辨率O 1s谱;(c) 高分辨率N 1s谱;(d)不同N种类的含量(原子百分比) Fig.9 (a) High-resolution C 1s spectra; (b) high-resolution O 1s spectra; (c) high-resolution of N 1s spectra; (d) the atomic percentage of different nitrogen species of fresh catalyst, used catalyst and recovered catalyst, respectively |
| |

|
| 图 10 反应前催化剂、反应后催化剂、再生催化剂的拉曼光谱 Fig.10 The Raman spectra of fresh catalyst, used catalyst and recovered catalyst, respectively |
| |
| Cat. | n(C)/% | n(N)/% | n(O)/% |
| Fresh cat. | 88.89 | 3.78 | 7.33 |
| Used cat. | 81.39 | 3.58 | 15.03 |
| Recovered cat. | 91.83 | 3.43 | 4.74 |
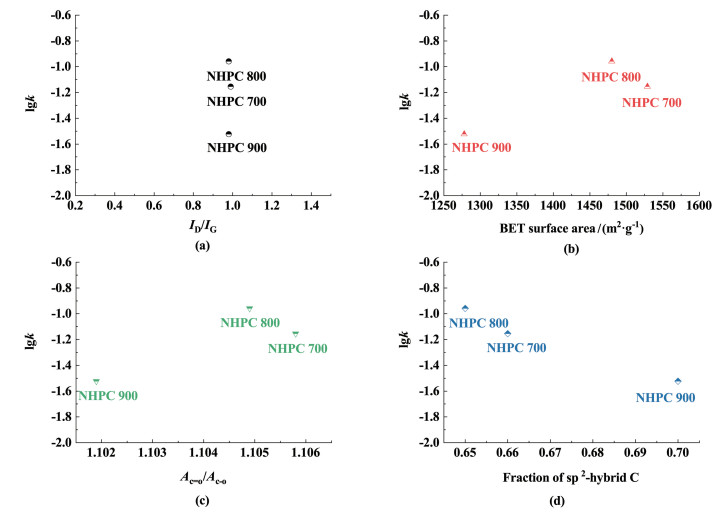
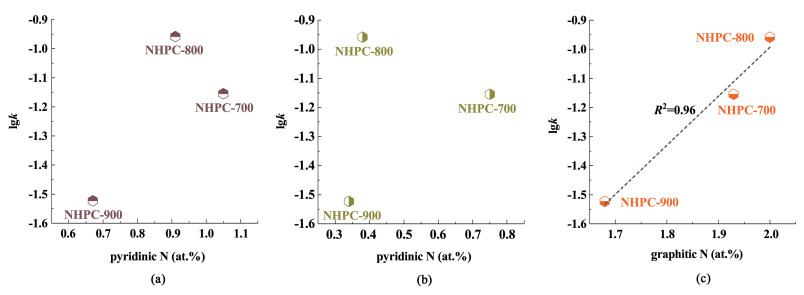
先前的研究表明,缺陷位点、sp2杂化碳以及纳米碳上的酮基C=O在非金属催化剂中对PMS活化具有很高的活性[16, 29, 30]。为了探究NHPC-800具有优异性能的原因,我们对BPA在对数坐标下的降解速率(lgk)与NHPC-800的结构参数进行了分析。由图 11(a)所示,3种样品拥有接近的ID/IG(≈0.98),但是其降解反应速率却表现出较大差别,这说明缺陷位点不是其主要活性位点。如图 11(b)所示,降解速率(lgk)与样品的催化剂比表面积没有表现出正相关的趋势,NHPC-700拥有最大的比表面积(1 570 m2 ·g-1),但是其催化降解反应速率却低于比表面积为1 430 m2 ·g-1的NHPC-800,即催化剂比表面积未对催化性能产生决定性影响。因此,NHPC的催化活性可能取决于碳和杂原子掺杂的本征构型以及催化位点的优化电子结构[16, 29]。我们进一步研究了C=O和C—O的原子比(AC=O/AC—O),sp2杂化碳占比与lgk的关系。如图 11(c)和图 11(d)所示,随着AC=O/AC—O或者sp2杂化碳占比的提高,lgk值呈现出先增加再减少的趋势或者逐渐降低的趋势,说明纳米碳上的酮基C=O,以及sp2杂化碳皆不是NHPC-800的主要活性位点。氮原子掺杂能够通过调节惰性碳质材料的自旋密度和电荷分布来改善其催化性能[8, 27, 31]。在氮掺杂过程中所形成的石墨N、吡咯N以及吡啶N通常对催化活性起着至关重要的作用,因此,探究NHPC中所含N的种类和含量具有重要意义。如图 12所示,lgk值与石墨N的含量密切相关,随着样品种石墨N含量的增加,其相应的BPA降解速率也在不断增加,其相关的拟合系数为0.96。然而吡啶N、吡咯N的含量与性能关系并没有发现类似规律。相比于NHPC-700和NHPC-900,催化活性最高的NHPC-800所含的吡咯N和吡啶N的含量皆不是最高。综合以上结果表明,石墨N是氮掺杂中空多孔碳球(NHPC)在过硫酸盐活化中的主要活性位点。
|
| 图 11 对数坐标下的BPA降解速率(lgk)与(a)拉曼ID/IG;(b)比表面积;(c)AC=O/AC—O比值;(d)sp2杂化碳的占比 Fig.11 BPA degradation rate in a log scale (lgk) versus (a) the Raman ID/IG ratio; (b) the BET surface area; (c) the AC=O/AC—O ratio, (d) the sp2-hybrid C content of the as-prepared carbon samples |
| |
|
| 图 12 对数坐标下的BPA降解速率(lgk)与样品中(a)吡啶N含量;(b)吡咯N含量;(c)石墨N含量 Fig.12 BPA degradation rate in a log scale (lgk) versus the content of (a) pyridinic N; (b) pyrrolic N; (c) graphitic N |
| |
通过化学猝灭实验进一步确定HNPC-800/PMS体系的活性氧物种,进一步探究NHPC-800激活PMS氧化降解双酚A过程的作用机制。本实验采用甲醇(EtOH)、叔丁醇(TBA)和呋喃甲醇(FFA),对苯醌(p-BQ)作为自由基猝灭剂,猝灭剂的加入能够抑制相应的活性氧物种与目标污染物的反应。活性氧物种在对BPA降解的贡献可以通过分析猝灭剂加入前后的动力学来判断。据文献报道,EtOH是SO4·-和·OH的有效猝灭剂[17, 32, 33],TBA比EtOH更疏水,倾向于吸附在催化剂表面,是·OH的有效清除剂[5, 27]。
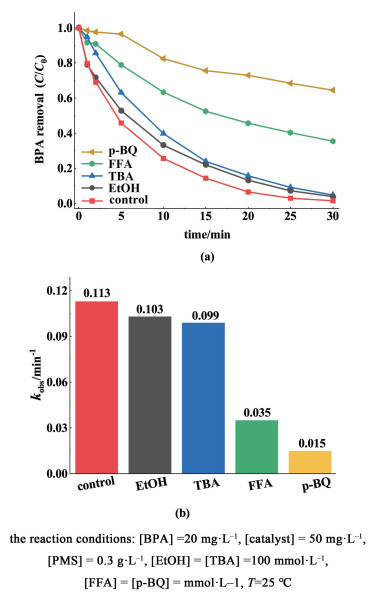
如图 13(a)所示,当100 mmol L-1 EtOH和TBA分别加入体系中,它们几乎无法抑制BPA降解,相应的表观反应速率[图(13(b)]也反映了SO4·-和·OH并不是该体系中主要参与反应的活性氧物种。接下来在体系中引入单线氧(1O2) 的猝灭剂FFA,可以检测到10 mmol ·L-1 FFA的加入对BPA的降解产生了明显的抑制作用,在30 min内只有60%的BPA被降解,这表明1O2在BPA的降解中具有一定的作用。当向体系中加入10 mmol ·L-1 O2·-的抑制剂p-BQ时,BPA的降解被抑制的效果更加明显,在30 min时间内仅有30%的BPA被有效降解,这表明O2·-在BPA降解中起主要作用。
|
| 图 13 (a) 不同猝灭剂对BPA降解的影响;(b)不同猝灭体系下相应的表观反应速率 Fig.13 (a) Effect of various quenching agents on BPA degradation; (b)the corresponding Pseudo-first order reaction rate constants in different quenching systems |
| |
计算表观反应速率发现[图 13(b)],猝灭剂FFA和p-BQ的加入使得kobs由0.113 min-1分别降低到0.035和0.015 min-1。综合上述分析,在NHPC-800/PMS体系中,O2·-和单线氧1O2皆对BPA的降解具有重要作用,其中O2·-是主要的活性物种。
考虑到猝灭实验仅能识别PMS活化过程中活性氧物种,并不能对其中直接电子转移过程的非自由基路径进行识别。我们利用电化学测试对直接电子转移过程进行了深入研究[6, 34]。开路电位测试能够直接揭示电子转移过程,已经被广泛应用于类似体系的非自由基途径探索[35, 36]。图 14展示了连续向超纯水中注入PMS和BPA后,在负载NHPC-800的玻碳电极上监测到的开路电位响应。在注入PMS后,负载NHPC-800的玻碳电极的电位出现明显的上升,这归因于催化剂与PMS之间的相互作用(即电子转移过程),表明2者可能生成了亚稳态的中间体[35-37]。当在体系中注入污染物BPA时,在电极上引起的开路电位的变化是非常微弱的,说明作为电子供体的BPA与作为电子受体的亚稳态中间体之间几乎不存在直接的电子传递过程[38, 39]。上述电化学测试表明,在NHPC-800/PMS体系中,直接的电子转移过程在PMS氧化过程中的作用是可忽略的。综上所述,可以证实以NHPC-800为催化剂的BPA降解过程是一个以O2·-为主导,1O2参与的高级氧化过程。

|
| 图 14 NHPC-800的开路电位测试 Fig.14 Open-circuit potential curves of NHPC-800 |
| |
主要研究了氮掺杂碳基催化剂活化PMS的主要活性位点和反应机理。首先采用原位聚合法合成了氮掺杂的中空多孔碳球(NHPC),通过改变其热解温度,制备了具有相似结构缺陷、sp2杂化碳含量、氧官能团的NHPC-700、NHPC-800和NHPC-900,其中NHPC-800对PMS活化降解BPA表现出最优异的催化性能。结合动力学分析、自由基猝灭实验以及电化学测试对其进一步分析,确定了石墨N位点是PMS活化降解BPA过程中的主要的活性位点,超氧自由基(O2·-)是参与BPA降解过程的主要活性氧物种。同时,热处理可以通过去除部分不利于电子传递的氧官能团和再生石墨N来恢复催化剂活性,再生后的催化剂性能优于未使用的催化剂。本研究为合理设计制备氮掺杂碳基催化剂,促进其在实际应用中的高效催化提供了一定指导。
| [1] |
ZHU S, HUANG X, MA F, et al. Catalytic removal of aqueous contaminants on N-doped graphitic biochars: Inherent roles of adsorption and nonradical mechanisms[J]. Environmental Science & Technology, 2018, 52(15): 8649-8658. |
| [2] |
LI X, HUANG X, XI S, et al. Single cobalt atoms anchored on porous N-doped graphene with dual reaction sites for efficient Fenton-like catalysis[J]. Journal of the American Chemical Society, 2018, 140(39): 12469-12475. DOI:10.1021/jacs.8b05992 |
| [3] |
QIAN K, CHEN H, LI W, et al. Single-atom Fe catalyst outperforms its homogeneous counterpart for activating peroxymonosulfate to achieve effective degradation of organic contaminants[J]. Environmental Science & Technology, 2021, 55(10): 7034-7043. |
| [4] |
HAN Q, WANG H, DONG W, et al. Degradation of bisphenol A by ferrate(VI) oxidation: Kinetics, products and toxicity assessment[J]. Chemical Engineering Journal, 2015, 262: 34-40. DOI:10.1016/j.cej.2014.09.071 |
| [5] |
LUO H, ZENG Y, HE D, et al. Application of iron-based materials in heterogeneous advanced oxidation processes for wastewater treatment: A review[J]. Chemical Engineering Journal, 2021. DOI:10.1016/j.cej.2020.127191 |
| [6] |
WANG J, LI B, LI Y, et al. Facile synthesis of atomic Fe-N-C materials and dual roles investigation of Fe-N4 sites in Fenton-like reactions[J]. Advanced Science (Weinheim, Baden-Wurttemberg, Germany), 2021. DOI:10.1002/advs.202101824 |
| [7] |
CHEN X, OH W D, HU Z, et al. Enhancing sulfacetamide degradation by peroxymonosulfate activation with N-doped graphene produced through delicately-controlled nitrogen functionalization via tweaking thermal annealing processes[J]. Applied Catalysis B: Environmental, 2018, 225: 243-257. DOI:10.1016/j.apcatb.2017.11.071 |
| [8] |
LI X, WANG J, DUAN X, et al. Fine-tuning radical/nonradical pathways on graphene by porous engineering and doping strategies[J]. ACS Catalysis, 2021, 11(8): 4848-4861. DOI:10.1021/acscatal.0c05089 |
| [9] |
KOHANTORABI M, MOUSSAVI G, GIANNAKIS S. A review of the innovations in metal- and carbon-based catalysts explored for heterogeneous peroxymonosulfate (PMS) activation, with focus on radical vs. non-radical degradation pathways of organic contaminants[J]. Chemical Engineering Journal, 2021. DOI:10.1016/j.cej.2020.127957 |
| [10] |
HE Y, ZHANG J, ZHOU H, et al. Synergistic multiple active species for the degradation of sulfamethoxazole by peroxymonosulfate in the presence of CuO@FeOx@Fe0[J]. Chemical Engineering Journal, 2020. DOI:10.1016/j.cej.2019.122568 |
| [11] |
张笑丛, 王琮, 吴松海. 不同形貌氧化钴活化过一硫酸盐降解硝基酚[J]. 化学工业与工程, 2020, 37(6): 38-47. ZHANG Xiaocong, WANG Cong, WU Songhai. Degradation of nitrophenols in wastewater by peroxymonosulfate activated by cobalt oxide with different morphologies[J]. Chemical Industry and Engineering, 2020, 37(6): 38-47. (in Chinese) |
| [12] |
JIANG N, XU H, WANG L, et al. Nonradical oxidation of pollutants with single-atom-Fe(Ⅲ)-activated persulfate: Fe(V) being the possible intermediate oxidant[J]. Environmental Science & Technology, 2020, 54(21): 14057-14065. |
| [13] |
LIU N, LU N, YU H, et al. Degradation of aqueous bisphenol A in the CoCN/Vis/PMS system: Catalyst design, reaction kinetic and mechanism analysis[J]. Chemical Engineering Journal, 2021. DOI:10.1016/j.cej.2020.127228 |
| [14] |
马晓, 王燕, 李国兵, 等. CoCo-PBA@CuFe-LDH活化过一硫酸盐降解阿特拉津[J]. 化学工业与工程, 2021, 38(2): 9-18. MA Xiao, WANG Yan, LI Guobing, et al. Activation peroxymonosulfate by CoCo-PBA@CuFe-LDH for the degradation of atrazine[J]. Chemical Industry and Engineering, 2021, 38(2): 9-18. (in Chinese) |
| [15] |
DUAN X, SUN H, WANG Y, et al. N-doping-induced nonradical reaction on single-walled carbon nanotubes for catalytic phenol oxidation[J]. ACS Catalysis, 2015, 5(2): 553-559. DOI:10.1021/cs5017613 |
| [16] |
ZHANG M, HAN C, CHEN W, et al. Active sites and reaction mechanism for N-doped carbocatalysis of phenol removal[J]. Green Energy & Environment, 2020, 5(4): 444-452. |
| [17] |
GAO Y, ZHU Y, LI T, et al. Unraveling the high-activity origin of single-atom iron catalysts for organic pollutant oxidation via peroxymonosulfate activation[J]. Environmental Science & Technology, 2021, 55(12): 8318-8328. |
| [18] |
REN W, NIE G, ZHOU P, et al. The intrinsic nature of persulfate activation and N-doping in carbocatalysis[J]. Environmental Science & Technology, 2020, 54(10): 6438-6447. |
| [19] |
NOONAN O, ZHANG H, SONG H, et al. In situ Stöber templating: Facile synthesis of hollow mesoporous carbon spheres from silica-polymer composites for ultra-high level in-cavity adsorption[J]. Journal of Materials Chemistry A, 2016, 4(23): 9063-9071. DOI:10.1039/C6TA02265K |
| [20] |
CAI A, HE H, ZHANG Q, et al. Synergistic effect of N-doped sp2 carbon and porous structure in graphene gels toward selective oxidation of C-H bond[J]. ACS Applied Materials & Interfaces, 2021, 13(11): 13087-13096. |
| [21] |
ZHANG H, NOONAN O, HUANG X, et al. Surfactant-free assembly of mesoporous carbon hollow spheres with large tunable pore sizes[J]. ACS Nano, 2016, 10(4): 4579-4586. DOI:10.1021/acsnano.6b00723 |
| [22] |
CHEN Y, LI Z, ZHU Y, et al. Atomic Fe dispersed on N-doped carbon hollow nanospheres for high-efficiency electrocatalytic oxygen reduction[J]. Advanced Materials, 2019. DOI:10.1002/adma.201806312 |
| [23] |
CHEN J, LI H, FAN C, et al. Dual single-atomic Ni-N4 and Fe-N4 sites constructing Janus hollow graphene for selective oxygen electrocatalysis[J]. Advanced Materials, 2020. DOI:10.1002/adma.202003134 |
| [24] |
QIN L, DING R, WANG H, et al. Facile synthesis of porous nitrogen-doped holey graphene as an efficient metal-free catalyst for the oxygen reduction reaction[J]. Nano Research, 2017, 10(1): 305-319. |
| [25] |
ZHAO T, KUMAR A, XIONG X, et al. Assisting atomic dispersion of Fe in N-doped carbon by aerosil for high-efficiency oxygen reduction[J]. ACS Applied Materials & Interfaces, 2020, 12(23): 25832-25842. |
| [26] |
DUAN X, SU C, ZHOU L, et al. Surface controlled generation of reactive radicals from persulfate by carbocatalysis on nanodiamonds[J]. Applied Catalysis B: Environmental, 2016, 194: 7-15. |
| [27] |
DU N, LIU Y, LI Q, et al. Peroxydisulfate activation by atomically-dispersed Fe-Nx on N-doped carbon: Mechanism of singlet oxygen evolution for nonradical degradation of aqueous contaminants[J]. Chemical Engineering Journal, 2021. DOI:10.1016/j.cej.2020.127545 |
| [28] |
LIU Y, MIAO W, FANG X, et al. MOF-derived metal-free N-doped porous carbon mediated peroxydisulfate activation via radical and non-radical pathways: Role of graphitic N and CO[J]. Chemical Engineering Journal, 2020. DOI:10.1016/j.cej.2019.122584 |
| [29] |
WANG J, DUAN X, GAO J, et al. Roles of structure defect, oxygen groups and heteroatom doping on carbon in nonradical oxidation of water contaminants[J]. Water Research, 2020. DOI:10.1016/j.watres.2020.116244 |
| [30] |
WANG H, GUO W, LIU B, et al. Edge-nitrogenated biochar for efficient peroxydisulfate activation: An electron transfer mechanism[J]. Water Research, 2019, 160: 405-414. |
| [31] |
ZHANG W, LI Y, FAN X, et al. Synergy of nitrogen doping and structural defects on hierarchically porous carbons toward catalytic oxidation via a non-radical pathway[J]. Carbon, 2019, 155: 268-278. |
| [32] |
WANG L, LAN X, PENG W, et al. Uncertainty and misinterpretation over identification, quantification and transformation of reactive species generated in catalytic oxidation processes: A review[J]. Journal of Hazardous Materials, 2021. DOI:10.1016/j.jhazmat.2020.124436 |
| [33] |
LI H, SHAN C, PAN B. Fe(Ⅲ)-doped g-C3N4 mediated peroxymonosulfate activation for selective degradation of phenolic compounds via high-valent iron-oxo species[J]. Environmental Science & Technology, 2018, 52(4): 2197-2205. |
| [34] |
PAN J, GAO B, DUAN P, et al. Improving peroxymonosulfate activation by copper ion-saturated adsorbent-based single atom catalysts for the degradation of organic contaminants: Electron-transfer mechanism and the key role of Cu single atoms[J]. Journal of Materials Chemistry A, 2021, 9(19): 11604-11613. |
| [35] |
LONG Y, DAI J, ZHAO S, et al. Atomically dispersed cobalt sites on graphene as efficient periodate activators for selective organic pollutant degradation[J]. Environmental Science & Technology, 2021, 55(8): 5357-5370. |
| [36] |
PENG L, DUAN X, SHANG Y, et al. Engineered carbon supported single iron atom sites and iron clusters from Fe-rich Enteromorpha for Fenton-like reactions via nonradical pathways[J]. Applied Catalysis B: Environmental, 2021. DOI:10.1016/j.apcatb.2021.119963 |
| [37] |
QI Y, LI J, ZHANG Y, et al. Novel lignin-based single atom catalysts as peroxymonosulfate activator for pollutants degradation: Role of single cobalt and electron transfer pathway[J]. Applied Catalysis B: Environmental, 2021. DOI:10.1016/j.apcatb.2021.119910 |
| [38] |
CHU C, YANG J, ZHOU X, et al. Cobalt single atoms on tetrapyridomacrocyclic support for efficient peroxymonosulfate activation[J]. Environmental Science & Technology, 2021, 55(2): 1242-1250. |
| [39] |
LI Y, YANG T, QIU S, et al. Uniform N-coordinated single-atomic iron sites dispersed in porous carbon framework to activate PMS for efficient BPA degradation via high-valent iron-oxo species[J]. Chemical Engineering Journal, 2020. DOI:10.1016/j.cej.2020.124382 |
 2022, Vol. 39
2022, Vol. 39





