近年来,微流控装置的开发及其在微化工技术、生物技术、微机电系统和微分析系统等方面的应用取得了重大进展[1-2]。微通道是微化工设备中微反应器的重要组成部分,其特征尺度在十到几百微米级别[3]。在微观尺度下,由于通道对流体流动限制作用较强、通道壁面与流体接触面积很大等因素的影响,微通道内流体的流动过程及物质传递和反应速度都与常规通道内有所不同,已有基于宏观尺度的相关理论难以适用。微流控技术具有热质传递效率高、可控性好及操作便利等特点[4-9],是实现高效、低能耗、环境友好的新型化工过程的有效途径。
微通道内的多相流是微化工技术的主要研究方向之一,其中,液液两相流在许多重要的化工过程中都有广泛应用,例如乳化、结晶、萃取等[10-12]。液滴的生成[11, 13-16]、破裂[17-26]、聚并[12, 27-31]、流动[32-35]等调控过程是液液两相流研究中的主要内容。为了实现微流控技术在生物[36],医学[37]和化工[38]领域的应用,精确的液滴调控具有重要意义。作为液滴流动行为的一个重要分支[39],聚并能够引入样品试剂,加速液滴内流体混合[40]或促成化学反应[41-42]。此外,它还可应用于纳米粒子合成、凝胶粒子制备等研究中[43-44]。因此对微通道内液液两相流中液滴的聚并进行研究具有重要意义。本论文针对液滴的聚并方式、聚并动力学、聚并过程的流场演化等内容的研究现状进行了系统的综述。
1 聚并方式基于微液滴的生化反应,例如:微米和纳米粒子的合成,需要2个不同的液滴融合在一起以获得良好的混合效果。因此,可控的液滴聚并成为液滴多步反应中的重要微流控技术[45-47]。液滴聚并是指2个或多个液滴接触并融合的过程,需要克服液滴的表面张力并且会使液滴界面不稳定[48]。目前,液滴聚并主要分为主动聚并和被动聚并[49]。
1.1 主动聚并主动聚并是指利用电场[50]、磁场[51]、温度场[52]、表面声波[53]或激光聚焦[54]等方法引起液滴界面破裂,从而发生聚并。主动聚并比较复杂,例如:利用电场诱发聚并时需要制造电极并精确控制电信号。此外,电极也可能会造成溶液的污染,导致生物分子的相容性受影响[48]。但主动聚并可以加速液滴间表面张力的不稳定性,具有较高的效率[55],因此受到了广泛关注。
电聚并是主动聚并中最常用的方法[56],其原理是通过电感应使液滴具有相反的电荷,从而导致液滴聚并。电场作用的条件非常广泛,可在1 V至几千伏的电压范围和DC至几千赫兹的频率范围内有效控制聚并。此外,当使用电聚并法时,电极可以嵌入微通道中或距离通道几毫米远,且电场方向可以平行于或垂直于液滴表面[48]。
Priest等[57]利用电场破坏了界面上的一系列毛细管波稳定性,从而导致液桥形成并聚并。然而,由于电场和流体界面之间的相互作用很强,因此2者之间相互作用的模型非常复杂。他们认为,在存在液滴的情况下,场线会因液滴的存在而发生偏移,并且可以集中到将其分隔的小薄片中,在局部产生强大的电场强度,且电场在表面活性剂分子的重新分布过程中起主要作用,进一步增加了问题的复杂性。
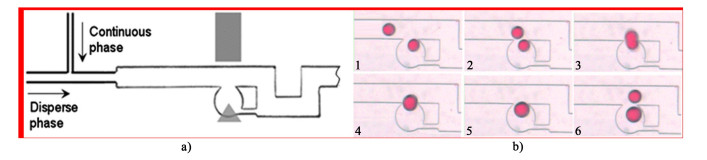
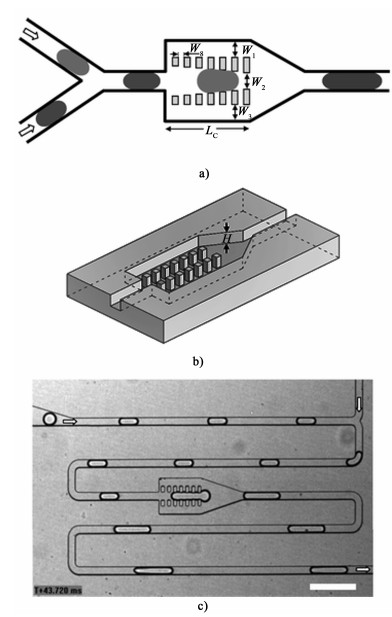
Wang等[58]通过施加电场实现液滴对的聚并来捕获液滴。微芯片的结构如图 1所示。研究发现,液滴沿主通道流动,并且在没有电场的情况下不会进入槽中。但施加电场后液滴进入微槽并被捕获,从而发生聚并。如果去除电场,液滴将再次沿着主通道移动。
Hao等[59]设计了1个局部嵌入电场,以更好地控制微通道中的液滴聚并。根据电润湿和流体动力学控制的原理,可以分别更改液滴的大小和生成频率。观察发现,聚并效率可达98%。在该系统中,使用了1个交叉场来促进液滴的聚并。当关闭电场时,表面活性剂较稳定,尽管液滴彼此挤压,但聚并不会发生。当打开电开关时,由于表面不稳定而发生了聚并。
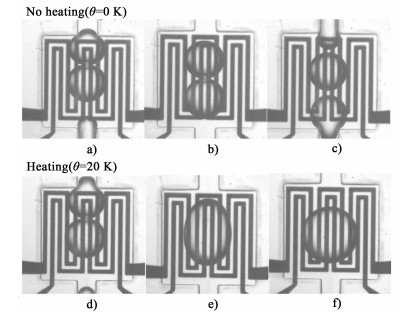
Zagnoni等[50]提出了一种利用电场促进油相中水滴聚并的系统。该系统不需要精确调整电极位置,也不需要液滴与液滴或液滴与电场同步。液滴可以高达50次·s-1的频率相互聚并。其聚并机理以液滴界面处的黏性力、电场力和界面张力之间的均衡为基础,并受通道内液滴流动行为的影响。实验表明,在不同频率、液滴的施加电势和液滴尺寸下,会发生多种类型的液滴聚并,并解释了导致不同聚并结果的聚并机理和总体趋势。实验观察到的聚并流型如图 2所示。
除了通过施加电场来诱发主动聚并外,其他主动聚并方法包括磁场、温度场、表面声波和激光聚焦等。Ray等[51]研究了磁场对非磁性载液中磁流体液滴尺寸控制的影响。磁场导致磁液滴融合,并且利用重新泵送机制研究了产生较大液滴的过程。实验观察到流率比、载体介质黏度和磁场强度对磁流体液滴影响显著。通过调节磁场强度,可以使液滴尺寸增至其初始尺寸的3倍。
Luong等[52]研究了带有微型加热器的腔室内2液滴的热聚并现象,利用集成的电阻传感器来测量加热温度。他们通过改变流速对聚并过程展开了研究,结果表明,液滴流速随着温度升高而减慢,当温度高于临界加热温度时,液滴会与后方液滴接触并发生聚并,如图 3所示。
Sesen等[53]设计了1种新型集成叉指式换能器的微流控芯片来调控液滴聚并。该方法利用表面声波感应的声辐射力使液滴从通道进入小膨胀室,然后使其滞留在膨胀室内直到后续液滴到达。因此对液滴初始间距没有要求。当聚并后的液滴体积达到临界值时,连续相施加的推动力将克服声波辐射力,从而导致聚并后的液滴流出膨胀室。
Baroud等[54]研究了激光聚焦引起的液滴聚并过程。证明了聚焦激光器的局部加热对液滴界面施加的热毛细管力可以阻止微通道内液滴向下游流动,且该方法具有一般性而无需任何特殊加工或移动部件。实验表明,在液滴界面进行局部的激光聚焦会加速液膜之间的表面活性剂分子排出,从而有利于聚并的发生,如图 4所示。
1.2 被动聚并由于主动聚并可能会造成溶液的污染,而被动聚并对溶液几乎不会造成污染,因此对液滴聚并的研究较多采用被动聚并方法。被动聚并方法包括改变通道结构和改变通道壁面润湿性,常用的通道结构有扩张通道结构和分岔口结构。
Fidalgo等[60]提出了利用表面改性来诱导2个或多个液滴聚并。他们通过将亲水性聚丙烯酸(PAA)通过UV光聚合作用刻到含二苯甲酮的聚二甲基硅氧烷(PDMS)平面上,使壁面局部改性。该方法不需要源元件,也不需要液滴的精确同步,并且与标准设备制造技术可兼容。结果表明,该方法允许2个以上液滴一步聚并,并有可能1次合成任何数量的液滴。
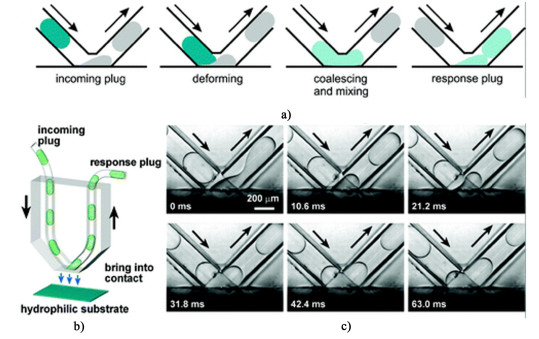
Liu等[61]使用1种新型V型通道研究了液滴的聚并过程。他们发现,在该结构下,聚并由毛细管数控制。在较高的毛细管数下,聚并所需时间更多,且液滴流经拐弯处变形更严重。高于临界毛细管数时,聚并无法发生。聚并过程示意图如图 5所示。
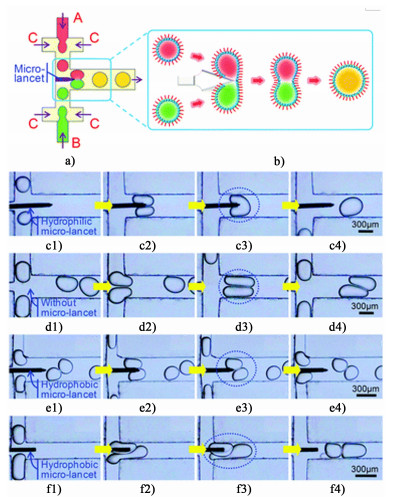
Deng等[62]设计了1种类似于手术的方法可在微通道中实现表面活性剂稳定的液滴聚并。当成对的液滴同时以适当的表面润湿性流过微型针时,其表面会被微型针刮擦,导致表面活性剂局部散开,并通过划开液滴表面促使聚并发生,如图 6所示。该过程可以被认为是显微外科手术,其中使用显微手术刀在液滴表面上绘制裂纹以促进其融合。图 6a)为微通道中微型针的示意图,图 6b)为微型针诱导表面活性剂稳定的乳化液滴聚并的示意图,图 6c)~图 6f)为微型针表面润湿性对液滴聚并的影响。该方法具有高度可控的灵活性和稳定性,并且可以控制不同数量和复杂结构的液滴聚并。
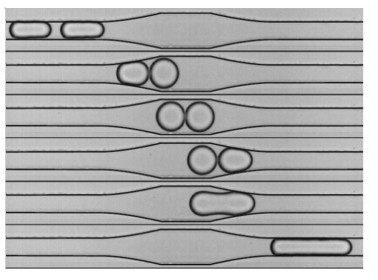
Tan等[63]通过调节通道内2液滴距离实现聚并。研究了液滴在通道内的流动时间(tr)和液膜排出时间(tdr)的关系对聚并的影响,结果表明,当tr/tdr=1.25时会发生液滴两两聚并,随着tr/tdr的增大,液滴聚并数目增多。实验观察到最多6个液滴的聚并。Tan等[64]还设计了3种不同的扩张通道结构:锥形扩张结构、矩形扩张结构和十字整流结构。结果表明,在锥形扩张结构中,由于通道宽度急剧增大,液滴速度迅速减小,造成多个聚并发生,且液滴聚并数目不可控;在矩形扩张结构中,液滴聚并受矩形长度、宽度及两相流率的影响;而十字整流结构通过调整支路通道的流量调整液滴间距,从而缩短液膜排出时间促使液滴聚并。
Bremond等[27]在扩张结构微通道内研究了液滴聚并的过程,如图 7所示。他们发现,当2液滴发生前后接触时,聚并发生在碰撞后的分离阶段而非碰撞阶段。分离导致在接触区域形成2个相对的凸起,从而在聚并过程中加强了界面的连接。他们还发现,通过强制分离2液滴可以使最初被表面活性剂稳定的液滴对趋向不稳定。
Niu等[65]设计了1种在微通道内设置微型柱的结构来诱导液滴聚并,如图 8所示。实验表明,微型柱可以调节液滴之间的距离,液滴进入腔室后速度下降甚至停止,等待后续液滴到达并发生相互接触,当上游连续相压力大于界面张力时,聚并发生。
Wang等[66]在T型微通道内对气泡的聚并过程展开了研究。发现了气泡碰撞后的3种结果:绝对聚并、可能聚并和不聚并。考察了液体黏度和两相表观流速对聚并的影响。结果表明,密闭空间内气泡的聚并过程快于自由空间的聚并过程,液体黏度增加不利于聚并,在可能聚并的流型中,两相表观流速的增大使聚并效率下降。
Ma等[28]通过引入第3相实现液滴在T型口处的聚并,观察到3种聚并类型:尾部聚并、滑移聚并和生成新液滴的不稳定聚并。结果表明,当分散相流率不变时,最终液滴尺寸随连续相毛细管数增加而减小,随第3相毛细管数增加而增加。
Guo等[67]研究了微通道内带有漏斗型扩张室的T型口处液滴的聚并行为。观察到3种聚并类型:不聚并、两两聚并和多个聚并。在两两聚并过程中观察到了3种聚并子类型:滑移聚并、碰撞聚并和挤压聚并。他们还考察了在两两聚并类型下漏斗型扩张室中液滴聚并率的影响因素,结果表明,在连续相流率恒定时,聚并率随分散相流率的增加先减小后增大。在分散相流率恒定时,聚并率随连续相流率的增加先增大后减小。当连续相流率较小时,聚并率随扩张室尺寸的增加而增加,而当连续相流率较大时,聚并率呈相反趋势。在各操作条件下的扩张室的最适宜长宽比均为k=1。
Yi等[68]在带有对称腔室的十字聚焦微通道内研究了液滴的聚并过程。观察到4种流型:长液滴、多个聚并、两两聚并和不聚并。研究了液滴变形度和旋转角度的演变过程,并以此来分析液滴的聚并机理。由于存在停滞时间,在此结构下允许非同步聚并的发生。
2 聚并动力学液膜排干理论常被用于分析液滴的聚并机理,该理论认为液滴聚并包括4个基本过程:1)液滴捕获或定位;2)2个液滴彼此靠近并发生碰撞和变形;3)液滴之间的连续相液膜排出;4)液滴界面破裂并融合[69]。2液滴接触后,可能会附着在一起,具有相互压缩、相对滑动或旋转的趋势,因此聚并不一定会发生。相互接触后2个液滴之间的连续相液膜开始被排出,而多余毛细力有助于液膜的排出[70]。排出速率由许多因素决定,例如碰撞速度和液膜黏度,即毛细管数Ca。已有部分研究针对液膜排出时间和毛细管数展开。
2.1 液膜排出时间Stone等[71]认为若2液滴接触时间足够长,则液滴间液膜会逐渐变薄。当液膜厚度低于临界值时,范德华力等分子间作用力影响明显,促使液膜破裂导致聚并发生。
Klaseboer等[72]对在1种流体中以恒定速度靠近的2个可变形球形液滴之间的液膜排出过程进行了实验和建模。建立了基于润滑理论的数值模型,并得出液膜排出时间tdrain为:
| $ {t_{{\rm{drain}}}} = 40R\sqrt {\frac{{{\mu _{\rm{c}}}}}{{\sigma V}}} $ | (1) |
式(1)中:R为液滴半径,μc为连续相黏度,σ为界面张力,V为表观流速。
Liao等[73]综述了流体粒子聚并的机理和模型,并将机理归纳为5类:湍流波动、黏性剪切力、湍流涡流捕获、浮力和尾流相互作用。他们还提出了针对不同变形度粒子的液膜排出时间关系式,其中,可变形粒子的液膜排出时间遵循如式(2)关系:
| $ {t_{{\rm{drain}}}} \propto \frac{{{\mu _{\rm{d}}}{d^{\frac{3}{2}}}}}{{{\sigma ^{\frac{3}{2}}}}} $ | (2) |
式(2)中: μd为分散相黏度,d为液滴直径,σ为界面张力。
Yeo等[74]研究了表面活性剂含量对液膜排出时间的影响。采用了润滑理论来描述液滴的流动,结果表明,表面活性剂的存在会阻碍液膜排出,膜破裂时间被延长甚至不可发生。他们研究了多种参数对液膜排出动力学的影响,得到了如式(3)关系:
| $ {T_{{\rm{dr}}}} \propto \left( {\frac{{{\mu _{\rm{c}}}}}{\sigma }} \right){\left( {\frac{{{\mu _{\rm{c}}}}}{{{\mu _{\rm{d}}}}}} \right)^\alpha } $ | (3) |
式(3)中: μc为连续相黏度,μd为分散相黏度,σ为界面张力,α<0。
Liu等[75]利用高速显微镜研究了Y型通道交叉角角度对液滴聚并的影响。结果表明,液膜排出时间随两相总流率增加而减小,随通道交叉角角度的增加而减小。由于交叉角角度的增加,使液滴瞬时碰撞速度增大,从而缩短了液膜排出时间。Liu等[39]还对通道相交室形状对液膜排出时间的影响展开了研究。为了实现液滴正面碰撞,设计了3种相交室形状:半圆形、三角形和弧形。实验发现,相交室的存在会延长聚并时间,这是由于液滴进入相交室内的速度大大降低,且半圆形相交室所需聚并时间最长,三角形和弧形相交室所需聚并时间非常接近。
Yi等[68]在带有对称腔室的十字聚焦微通道内研究发现,液膜排出时间与流体表观流速、液滴尺寸和两相黏度比有关。实验发现,当流速增大时,连续相的惯性作用增强,从而液滴间的挤压作用加强,加速了液膜排出过程。他们将液滴开始接触至聚并发生所经过的时间定义为液膜排出时间,并将液膜排出时间通过惯性毛细时间无量纲化,拟合无量纲液膜排出时间t*和无量纲连续相流速u*,得到如式(4)关系式:
| $ {t^*} = 14.02{u^*}^{ - 0.7416} $ | (4) |
临界毛细管数(Cac)是确定是否发生聚并的关键参数[71]。Stone等[71]认为聚并发生在2液滴低速碰撞时(Cac≈10-2),当Ca<Cac时,聚并可以发生,当Ca>Cac,2液滴容易发生相对滑动而不易聚并。
Hu等[76]研究了共聚物对聚二甲基硅氧烷中聚丁二烯液滴聚并的影响。共聚物减小了界面张力,促进了液滴破裂,但不利于聚并发生,且对聚并的影响远大于破裂。实验发现,当添加共聚物使界面张力仅降低3%时,临界毛细管数会下降6倍。当不添加共聚物时,临界毛细管数与液滴半径的关系为:
| $ C{a_{\rm{c}}} \propto {a^{ - 0.82 \pm 0.03}} $ | (5) |
与黏度比的关系为:
| $ C{a_{\rm{c}}} \propto {\lambda ^{ - 0.41 \pm 0.06}} $ | (6) |
Christopher等[12]在常规T型微通道内对液滴聚并展开了研究。实验发现,在低碰撞速度下容易发生聚并,较小的液滴在相互接触过程中会发生相对滑动而无法聚并,液滴较大且流速较快时可能会被夹断。考察了黏度对聚并的影响发现,当液滴黏度较小时,液滴在碰撞过程中会发生快速变形,形成较大的接触区域,加速了液膜排出,有利于聚并发生。当μd/μc<2时,临界毛细管数与黏度比的关系为:
| $ C{a_{\rm{c}}} \propto {\frac{{{\mu _{\rm{d}}}}}{{{\mu _{\rm{c}}}}}^{ - 0.49 \pm 0.04}} $ | (7) |
Liu等[75]研究了Y型微通道内交叉角角度对临界毛细管数的影响。结果表明,临界毛细管数随交叉角角度增加而减小,当角度为30°时,临界毛细管数Ca*=0.024 75。临界毛细管数的减小说明聚并容易发生,因此减小通道相交角角度有利于聚并。Liu等[39]还考察了相交室形状(半圆形、三角形和弧形)对临界毛细管数的影响。弧形相交室的临界毛细管数大于半圆形和三角形相交室内的临界毛细管数,表明受限空间有利于液滴聚并。临界毛细管数随黏度比增加而减小,且在不同相交室形状下均遵循如式(8)关系:
| $ C{a_{\rm{c}}} \propto {\lambda ^{ - 0.75}} $ | (8) |
Ma等[77]设计了1种带有对称扩缩口的T型微通道,实验发现,扩缩口的存在会减慢液滴流动速度,从而允许非同步到达T型口的2液滴发生聚并。结果表明,临界毛细管数随分散相黏度增加而降低,因此增加分散相黏度不利于聚并。他们提出Cac与2相黏度比φ的幂律关系为:
| $ C{a_{\rm{c}}} = 0.004{\varphi ^{ - 0.518}} $ | (9) |
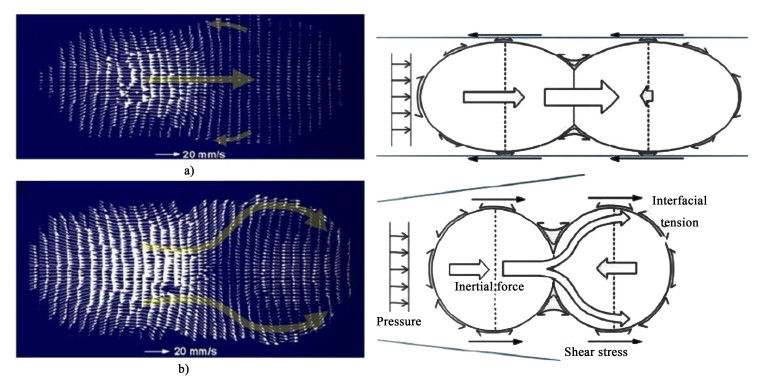
利用流体力学实验方法和微粒子图像测速技术(μ-PIV)研究聚并的流场特征以深入揭示聚并机理已成为重要的研究内容。Jin等[78]研究了直通道和扩张通道中液滴的聚并过程。研究表明,聚并过程包括接触、液膜排出、界面融合、渗漏或包裹等步骤,主要取决于通道的结构和多种力的作用。在直通道中,后方液滴渗入前1个液滴并瞬间溶和,如图 9a)所示。然而,当后方液滴渗入前液滴时,扩张通道中会形成强烈的涡流[图 9b)]。
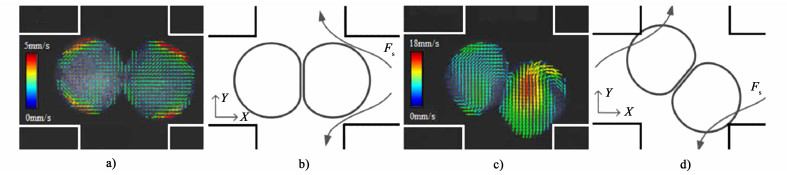
Wang等[79]研究了液滴在十字聚焦通道内不同状态下的内部速度矢量场和黏性力。如图 10a)和图 10b)所示,在接触区域的边缘处的速度矢量沿垂直方向,剪切作用引起2个液滴之间的相互挤压使液膜排出时间显著减少。与图 10a)相比,图 10c)中的速度矢量场完全不同,剪切力不对称。因此,液滴的运动不利于液膜排出,液滴旋转后不会发生聚并。
Liu等[75]利用μ-PIV系统研究了Y形微通道内碰撞和分离引起的聚并过程的速度矢量场。他们发现,液滴内部漩涡的产生是由液滴前部接触区域的相对剪切运动引起的,最小速度出现在液滴与通道壁面之间的接触区域。由于聚并过程中后液滴施加给前液滴的挤压作用,前液滴接触部分的速度显著增加。在分离诱导的聚并中,2个液滴发生相对移动,由于液滴的表面凸起而发生快速聚并,且凸起附近的速度明显提高。
4 结论本文综述了液滴的聚并方式、聚并动力学及流场特征。详细介绍了液滴聚并的主动方法和被动方法的研究进展。此外,还阐述了聚并过程中的液膜排出时间和临界毛细管数等动力学参数及流场的研究。尽管液滴聚并已取得了相当的进展,但仍然有许多科学和工程问题需要深入研究。未来应致力于开展液滴聚并的机理、探索实现高效聚并的方式及拓宽微流控技术中液滴聚并的应用等的研究。
| [1] |
Fu T, Ma Y, Funfschilling D, et al. Bubble formation and breakup mechanism in a microfluidic flow-focusing device[J]. Chemical Engineering Science, 2009, 64(10): 2392-2400. DOI:10.1016/j.ces.2009.02.022 |
| [2] |
Santos J, Trujillo-Cayado L A, Calero N, et al. Development of eco-friendly emulsions produced by microfluidization technique[J]. Journal of Industrial and Engineering Chemistry, 2016, 36: 90-95. DOI:10.1016/j.jiec.2016.01.024 |
| [3] |
Whitesides G M. The origins and the future of microfluidics[J]. Nature, 2006, 442(7101): 368-373. DOI:10.1038/nature05058 |
| [4] |
Song H, Chen D, Ismagilov R F. Reactions in droplets in microfluidic channels[J]. Angewandte Chemie (International Ed in English), 2006, 45(44): 7336-7356. DOI:10.1002/anie.200601554 |
| [5] |
陈光文, 袁权. 微化工技术[J]. 化工学报, 2003, 54(4): 427-439. Chen Guangwen, Yuan Quan. Micro-chemical technology[J]. Journal of Chemical Industry and Engineering (China), 2003, 54(4): 427-439. DOI:10.3321/j.issn:0438-1157.2003.04.004 (in Chinese) |
| [6] |
Xu J, Ahn B, Lee H, et al. Droplet-based microfluidic device for multiple-droplet clustering[J]. Lab on a Chip, 2012, 12(4): 725-730. DOI:10.1039/C2LC20883K |
| [7] |
Fu T, Ma Y. Bubble formation and breakup dynamics in microfluidic devices: A review[J]. Chemical Engineering Science, 2015, 135: 343-372. DOI:10.1016/j.ces.2015.02.016 |
| [8] |
Zhu P, Wang L. Passive and active droplet generation with microfluidics: A review[J]. Lab on a Chip, 2016, 17(1): 34-75. |
| [9] |
Becht S, Franke R, Geißelmann A, et al. Micro process technology as a means of process intensification[J]. Chemical Engineering & Technology, 2007, 30(3): 295-299. |
| [10] |
Hessel V, Löwe H, Schönfeld F. Micromixers-a review on passive and active mixing principles[J]. Chemical Engineering Science, 2005, 60(8/9): 2479-2501. |
| [11] |
Utada A S, Lorenceau E, Link D R, et al. Monodisperse double emulsions generated from a microcapillary device[J]. Science, 2005, 308(5721): 537-541. DOI:10.1126/science.1109164 |
| [12] |
Christopher G F, Bergstein J, End N B, et al. Coalescence and splitting of confined droplets at microfluidic junctions[J]. Lab on a Chip, 2009, 9(8): 1102-1109. DOI:10.1039/b813062k |
| [13] |
Du W, Fu T, Zhu C, et al. Breakup dynamics for high-viscosity droplet formation in a flow-focusing device: Symmetrical and asymmetrical ruptures[J]. AIChE Journal, 2016, 62(1): 325-337. DOI:10.1002/aic.15043 |
| [14] |
Du W, Fu T, Zhang Q, et al. Breakup dynamics for droplet formation in a flow-focusing device: Rupture position of viscoelastic thread from matrix[J]. Chemical Engineering Science, 2016, 153: 255-269. DOI:10.1016/j.ces.2016.07.038 |
| [15] |
van Loo S, Stoukatch S, Kraft M, et al. Droplet formation by squeezing in a microfluidic cross-junction[J]. Microfluidics and Nanofluidics, 2016, 20(10): 1-12. |
| [16] |
Christopher G F, Noharuddin N N, Taylor J A, et al. Experimental observations of the squeezing-to-dripping transition in T-shaped microfluidic junctions[J]. Physical Review E, Statistical, Nonlinear, and Soft Matter Physics, 2008. DOI:10.1103/PhysRevE.78.036317 |
| [17] |
Link D R, Anna S L, Weitz D A, et al. Geometrically mediated breakup of drops in microfluidic devices[J]. Physical Review Letters, 2004. DOI:10.1103/PhysRevLett.92.054503 |
| [18] |
Leshansky A M, Pismen L M. Breakup of drops in a microfluidic T junction[J]. Physics of Fluids, 2009. DOI:10.1063/1.3078515 |
| [19] |
Yamada M, Doi S, Maenaka H, et al. Hydrodynamic control of droplet division in bifurcating microchannel and its application to particle synthesis[J]. Journal of Colloid and Interface Science, 2008, 321(2): 401-407. DOI:10.1016/j.jcis.2008.01.036 |
| [20] |
Hoang D A, Portela L M, Kleijn C R, et al. Dynamics of droplet breakup in a T-junction[J]. Journal of Fluid Mechanics, 2013. DOI:10.1017/jfm.2013.18 |
| [21] |
Chen B, Li G, Wang W, et al. 3D numerical simulation of droplet passive breakup in a micro-channel T-junction using the Volume-Of-Fluid method[J]. Applied Thermal Engineering, 2015, 88: 94-101. DOI:10.1016/j.applthermaleng.2014.11.084 |
| [22] |
Ma R, Fu T, Zhang Q, et al. Breakup dynamics of ferrofluid droplet in a microfluidic T-junction[J]. Journal of Industrial and Engineering Chemistry, 2017, 54: 408-420. DOI:10.1016/j.jiec.2017.06.021 |
| [23] |
Ménétrier-Deremble L, Tabeling P. Droplet breakup in microfluidic junctions of arbitrary angles[J]. Physical Review E, 2006. DOI:10.1103/PhysRevE.74.035303 |
| [24] |
Bedram A, Moosavi A. Droplet breakup in an asymmetric microfluidic T junction[J]. The European Physical Journal E, 2011. DOI:10.1140/epje/i2011-11078-7 |
| [25] |
Ma P, Fu T, Zhu C, et al. Asymmetrical breakup and size distribution of droplets in a branching microfluidic T-junction[J]. Korean Journal of Chemical Engineering, 2019, 36(1): 21-29. DOI:10.1007/s11814-018-0165-y |
| [26] |
Agnihotri S N, Raveshi M R, Bhardwaj R, et al. Droplet breakup at the entrance to a bypass channel in a microfluidic system[J]. Physical Review Applied, 2019. DOI:10.1103/PhysRevApplied.11.034020 |
| [27] |
Bremond N, Thiam A R, Bibette J. Decompressing emulsion droplets favors coalescence[J]. Physical Review Letters, 2008. DOI:10.1103/PhysRevLett.100.024501 |
| [28] |
Ma R, Zhang Q, Fu T, et al. Manipulation of microdroplets at a T-junction: Coalescence and scaling law[J]. Journal of Industrial and Engineering Chemistry, 2018, 65: 272-279. DOI:10.1016/j.jiec.2018.04.038 |
| [29] |
Mazutis L, Griffiths A D. Selective droplet coalescence using microfluidic systems[J]. Lab on a Chip, 2012, 12(10): 1800-1806. DOI:10.1039/c2lc40121e |
| [30] |
Wang K, Lu Y, Yang L, et al. Microdroplet coalescences at microchannel junctions with different collision angles[J]. AIChE Journal, 2013, 59(2): 643-649. DOI:10.1002/aic.13825 |
| [31] |
Zhou Q, Sun Y, Yi S, et al. Investigation of droplet coalescence in nanoparticle suspensions by a microfluidic collision experiment[J]. Soft Matter, 2016, 12(6): 1674-1682. DOI:10.1039/C5SM02924D |
| [32] |
Kinoshita H, Kaneda S, Fujii T, et al. Three-dimensional measurement and visualization of internal flow of a moving droplet using confocal micro-PIV[J]. Lab on a Chip, 2007, 7(3): 338-346. DOI:10.1039/B617391H |
| [33] |
Amini H, Lee W, Di Carlo D. Inertial microfluidic physics[J]. Lab on a Chip, 2014, 14(15): 2739-2761. DOI:10.1039/c4lc00128a |
| [34] |
Sarrazin F, Loubière K, Prat L, et al. Experimental and numerical study of droplets hydrodynamics in microchannels[J]. AIChE Journal, 2006, 52(12): 4061-4070. DOI:10.1002/aic.11033 |
| [35] |
Chen X, Xue C, Zhang L, et al. Inertial migration of deformable droplets in a microchannel[J]. Physics of Fluids, 2014. DOI:10.1063/1.4901884 |
| [36] |
Grünberger A, Wiechert W, Kohlheyer D. Single-cell microfluidics: Opportunity for bioprocess development[J]. Current Opinion in Biotechnology, 2014, 29: 15-23. DOI:10.1016/j.copbio.2014.02.008 |
| [37] |
Liu D, Zhang H, Fontana F, et al. Microfluidic-assisted fabrication of carriers for controlled drug delivery[J]. Lab on a Chip, 2017, 17(11): 1856-1883. DOI:10.1039/C7LC00242D |
| [38] |
Yap S K, Wong W K, Ng N X Y, et al. Three-phase microfluidic reactor networks-Design, modeling and application to scaled-out nanoparticle-catalyzed hydrogenations with online catalyst recovery and recycle[J]. Chemical Engineering Science, 2017, 169: 117-127. DOI:10.1016/j.ces.2016.12.005 |
| [39] |
Liu Z, Wang X, Cao R, et al. Droplet coalescence at microchannel intersection Chambers with different shapes[J]. Soft Matter, 2016, 12(26): 5797-5807. DOI:10.1039/C6SM01158F |
| [40] |
Jin B, Kim Y W, Lee Y, et al. Droplet merging in a straight microchannel using droplet size or viscosity difference[J]. Journal of Micromechanics and Microengineering, 2010. DOI:10.1088/0960-1317/20/3/035003 |
| [41] |
Hung L H, Choi K M, Tseng W Y, et al. Alternating droplet generation and controlled dynamic droplet fusion in microfluidic device for CdS nanoparticle synthesis[J]. Lab on a Chip, 2006, 6(2): 174-178. DOI:10.1039/b513908b |
| [42] |
Frenz L, El Harrak A, Pauly M, et al. Droplet-based microreactors for the synthesis of magnetic iron oxide nanoparticles[J]. Angewandte Chemie International Edition, 2008, 47(36): 6817-6820. DOI:10.1002/anie.200801360 |
| [43] |
Shintaku H, Kuwabara T, Kawano S, et al. Micro cell encapsulation and its hydrogel-beads production using microfluidic device[J]. Microsystem Technologies, 2007, 13(8/9/10): 951-958. |
| [44] |
Seo Y S, Yoon K, Rafailovich M. Highly ordered monolayer formation of silica beads assisted by ultra-sound and microscopic barrier at air/water interface[J]. Journal of Industrial and Engineering Chemistry, 2010, 16(6): 879-883. DOI:10.1016/j.jiec.2010.09.009 |
| [45] |
肖志良, 张博. 基于液滴技术的微流控芯片实验室及其应用[J]. 色谱, 2011, 29(10): 949-956. Xiao Zhiliang, Zhang Bo. Droplet microfluidics: technologies and applications[J]. Chinese Journal of Chromatography, 2011, 29(10): 949-956. (in Chinese) |
| [46] |
邓楠楠, 汪伟, 巨晓洁, 等. 微流控技术操控微尺度液滴及其聚并的研究进展[J]. 中国科学: 化学, 2015, 45(1): 7-15. Deng Nannan, Wang Wei, Ju Xiaojie, et al. Recent advances in microfluidic manipulation and coalescence of microscale droplets[J]. Scientia Sinica Chimica, 2015, 45(1): 7-15. (in Chinese) |
| [47] |
张凯, 胡坪, 梁琼麟, 等. 微流控芯片中微液滴的操控及其应用[J]. 分析化学, 2008, 36(4): 556-562. Zhang Kai, Hu Ping, Liang Qionglin, et al. Control and application of microdroplet in microfluidic chip[J]. Chinese Journal of Analytical Chemistry, 2008, 36(4): 556-562. DOI:10.3321/j.issn:0253-3820.2008.04.029 (in Chinese) |
| [48] |
Shen F, Li Y, Liu Z, et al. Advances in micro-droplets coalescence using microfluidics[J]. Chinese Journal of Analytical Chemistry, 2015, 43(12): 1942-1954. DOI:10.1016/S1872-2040(15)60886-6 |
| [49] |
Baroud C N, Gallaire F, Dangla R. Dynamics of microfluidic droplets[J]. Lab on a Chip, 2010, 10(16): 2032-2045. DOI:10.1039/c001191f |
| [50] |
Zagnoni M, Cooper J M. On-chip electrocoalescence of microdroplets as a function of voltage, frequency and droplet size[J]. Lab on a Chip, 2009, 9(18): 2652-2658. DOI:10.1039/b906298j |
| [51] |
Ray A, Varma V B, Jayaneel P J, et al. On demand manipulation of ferrofluid droplets by magnetic fields[J]. Sensors and Actuators B: Chemical, 2017, 242: 760-768. DOI:10.1016/j.snb.2016.11.115 |
| [52] |
Luong T D, Nguyen N T, Sposito A. Thermocoalescence of microdroplets in a microfluidic chamber[J]. Applied Physics Letters, 2012. DOI:10.1063/1.4730606 |
| [53] |
Sesen M, Alan T, Neild A. Microfluidic on-demand droplet merging using surface acoustic waves[J]. Lab on a Chip, 2014, 14(17): 3325-3333. DOI:10.1039/C4LC00456F |
| [54] |
Baroud C N, de Saint Vincent M R, Delville J P. An optical toolbox for total control of droplet microfluidics[J]. Lab on a Chip, 2007, 7(8): 1029-1033. DOI:10.1039/b702472j |
| [55] |
Grüttner C, Müller K, Teller J, et al. Synthesis and antibody conjugation of magnetic nanoparticles with improved specific power absorption rates for alternating magnetic field cancer therapy[J]. Journal of Magnetism and Magnetic Materials, 2007, 311(1): 181-186. DOI:10.1016/j.jmmm.2006.10.1151 |
| [56] |
Sarrazin F, Prat L, Di Miceli N, et al. Mixing characterization inside microdroplets engineered on a microcoalescer[J]. Chemical Engineering Science, 2007, 62(4): 1042-1048. DOI:10.1016/j.ces.2006.10.013 |
| [57] |
Priest C, Herminghaus S, Seemann R. Controlled electrocoalescence in microfluidics: Targeting a single lamella[J]. Applied Physics Letters, 2006. DOI:10.1063/1.2357039 |
| [58] |
Wang W, Yang C, Li C. On-demand microfluidic droplet trapping and fusion for on-chip static droplet assays[J]. Lab on a Chip, 2009, 9(11): 1504-1506. DOI:10.1039/b903468d |
| [59] |
Gu H, Duits M H, Mugele F. Droplets formation and merging in two-phase flow microfluidics[J]. Int J Mol Sci, 2011, 12(4): 2572-2597. DOI:10.3390/ijms12042572 |
| [60] |
Fidalgo L M, Abell C, Huck W T. Surface-induced droplet fusion in microfluidic devices[J]. Lab on a Chip, 2007, 7(8): 984-986. DOI:10.1039/b708091c |
| [61] |
Liu Y, Ismagilov R F. Dynamics of coalescence of plugs with a hydrophilic wetting layer induced by flow in a microfluidic chemistrode[J]. Langmuir, 2009, 25(5): 2854-2859. DOI:10.1021/la803518b |
| [62] |
Deng N, Sun S, Wang W, et al. A novel surgery-like strategy for droplet coalescence in microchannels[J]. Lab on a Chip, 2013, 13(18): 3653-3657. DOI:10.1039/c3lc50533b |
| [63] |
Tan Y, Ho Y L, Lee A P. Droplet coalescence by geometrically mediated flow in microfluidic channels[J]. Microfluidics and Nanofluidics, 2007, 3(4): 495-499. DOI:10.1007/s10404-006-0136-1 |
| [64] |
Tan Y, Fisher J S, Lee A I, et al. Design of microfluidic channel geometries for the control of droplet volume, chemical concentration, and sorting[J]. Lab on a Chip, 2004, 4(4): 292-298. DOI:10.1039/b403280m |
| [65] |
Niu X, Gulati S, Edel J B, et al. Pillar-induced droplet merging in microfluidic circuits[J]. Lab on a Chip, 2008, 8(11): 1837-1841. DOI:10.1039/b813325e |
| [66] |
Yang L, Wang K, Tan J, et al. Experimental study of microbubble coalescence in a T-junction microfluidic device[J]. Microfluidics and Nanofluidics, 2012, 12(5): 715-722. DOI:10.1007/s10404-011-0912-4 |
| [67] |
Guo W, Zhu C, Fu T, et al. Controllable droplet coalescence in the T-junction microchannel with a funnel-typed expansion chamber[J]. Industrial & Engineering Chemistry Research, 2020, 59(22): 10298-10307. |
| [68] |
Yi H, Zhu C, Fu T, et al. Efficient coalescence of microdroplet in the cross-focused microchannel with symmetrical chamber[J]. Journal of the Taiwan Institute of Chemical Engineers, 2020, 112: 52-59. DOI:10.1016/j.jtice.2020.07.010 |
| [69] |
Gunes D Z, Clain X, Breton O, et al. Avalanches of coalescence events and local extensional flows-Stabilisation or destabilisation due to surfactant[J]. Journal of Colloid and Interface Science, 2010, 343(1): 79-86. DOI:10.1016/j.jcis.2009.11.035 |
| [70] |
Chesters A K. The modelling of coalescence processes in fluid-liquid dispersions: A review of current understanding[J]. Chemical Engineering Research & Design, 1991, 69(4): 259-270. |
| [71] |
Stone H A, Stroock A D, Ajdari A. Engineering flows in small devices[J]. Annual Review of Fluid Mechanics, 2004, 36(1): 381-411. DOI:10.1146/annurev.fluid.36.050802.122124 |
| [72] |
Klaseboer E, Chevaillier J P, Gourdon C, et al. Film drainage between colliding drops at constant approach velocity: Experiments and modeling[J]. Journal of Colloid and Interface Science, 2000, 229(1): 274-285. DOI:10.1006/jcis.2000.6987 |
| [73] |
Liao Y, Lucas D. A literature review on mechanisms and models for the coalescence process of fluid particles[J]. Chemical Engineering Science, 2010, 65(10): 2851-2864. DOI:10.1016/j.ces.2010.02.020 |
| [74] |
Yeo L Y, Matar O K, Perez de Ortiz E S, et al. Film drainage between two surfactant-coated drops colliding at constant approach velocity[J]. Journal of Colloid and Interface Science, 2003, 257(1): 93-107. DOI:10.1016/S0021-9797(02)00033-4 |
| [75] |
Liu Z, Cao R, Pang Y, et al. The influence of channel intersection angle on droplets coalescence process[J]. Experiments in Fluids, 2015, 56(2): 1-4. |
| [76] |
Hu Y, Pine D J, Leal L G. Drop deformation, breakup, and coalescence with compatibilizer[J]. Physics of Fluids, 2000, 12(3): 484-489. DOI:10.1063/1.870254 |
| [77] |
Ma P, Liang D, Zhu C, et al. An effective method to facile coalescence of microdroplet in the symmetrical T-junction with expanded convergence[J]. Chemical Engineering Science, 2020. DOI:10.1016/j.ces.2019.115389 |
| [78] |
Jin B, Yoo J Y. Visualization of droplet merging in microchannels using micro-PIV[J]. Experiments in Fluids, 2012, 52(1): 235-245. DOI:10.1007/s00348-011-1221-0 |
| [79] |
Wang K, Lu Y, Tostado C P, et al. Coalescences of microdroplets at a cross-shaped microchannel junction without strictly synchronism control[J]. Chemical Engineering Journal, 2013, 227: 90-96. DOI:10.1016/j.cej.2012.09.060 |
 2021, Vol. 38
2021, Vol. 38