2. 南开大学化学系, 天津 300071
2. School of Chemistry, Nankai University, Tianjin 300071, China
随着高品质原油储量的日益减少,有效开采和利用占世界原油储量约70%的重油显得愈发重要[1-4]。然而,由于重油具有黏度高、密度大、流动性差和含有杂原子较多等缺点,不能对其直接进行改质升级[5-7]。近来,超临界水改质升级技术因其无需催化剂、生焦少以及经济环保等优势引起越来越广泛的关注[8-11]。Sato等[12]的研究表明沥青质可以在超临界水(SCW)中发生分解,并且其转化率随温度和水密度增加而增加。他们[13]也表明随着极性有机氢化分子的加入,该转化率将得到进一步的提高。Motimoto等[7]进行了油砂沥青在超临界水中改质的研究,得到大量轻质产品和少量焦炭。他们认为这一良好的改质结果是由于超临界水的高分散效应促进了重组分的分子内脱氢并抑制了复合反应的发生。此外,Cheng等[14]进行了减压渣油在超临界水中的热转化研究,得到了和Motimoto等[7]相似的结论。
研究表明,超临界水可以有效地脱除重油中的S、N、Ni和V等杂原子[15-16]。本课题组先前的研究[17-18]给出了异丙基苯硫醚在超临界水中脱硫以及异喹啉在超临界水中脱氮的详细机理。异丙基苯硫醚在超临界水中的脱硫包含4个步骤,超临界水分子主要作为反应物和氢转移催化剂参与反应。异喹啉是1种含氮杂环化合物,可以通过3条路径同时进行开环和脱氮过程,超临界水短链水分子簇可以催化每一步反应从而降低反应能垒。本研究主要关注非杂环含氮化合物苄胺在超临界水中脱氮的详细机理。
Houser等[19]的研究表明,在673 K、26.68 MPa条件下,苄胺在超临界水中反应1 h,转化率近乎为100%。实验产物主要是苯、甲苯以及极少量的联苯。此外,随着温度、压力和反应时间增加,苯甲醇、苯甲醛和亚苄基苄胺(BBA)逐渐消失,这表明它们是中间产物。Taso等[20]进行了BBA在超临界水中的反应,结果发现,约95%的BBA都转化成了苯和甲苯;虽然反应初始时,也有苯甲醇和苯甲醛的生成,但随着时间增长,2者均消失。
虽然前人的研究表明苄胺在超临界水中是不稳定的,但是这些研究并未涉及详细的反应机理。前人的研究结果显示,自由基机理和协同反应机理可能是苄胺-超临界水反应遵循的机理。深入考察超临界水反应系统中的详细脱氮机理,对于更加有效地改质重油具有重要意义。本研究提出了苄胺-SCW反应的可能路径,给出了每条路径中每步基元反应的详细化学反应方程式,并在密度泛函理论的基础上通过量子化学计算和反应能垒比较,确定了最优反应路径;此外,也探究了超临界水分子的催化作用。
1 实验和理论方法 1.1 试剂和设备正十四烷,质量分数为98%;苄胺,质量分数为99%;氮气,体积分数为99.999%;蒸馏水。
在高温高压管式反应器中进行苄胺在超临界水中脱氮的反应,实验设备如图 1所示。反应管的材质是哈氏合金,内径为12.5 mm,恒温反应区(3)长度为228 mm。反应管两端装有内衬管(1)以消除冷体积,反应区中央放有1条自制的金属转子(2)以使反应物充分混合。使用电炉(8)并通过调控控制面板(9)进行程序升温保证实验进行。出于安全考虑,在封头内添加防爆片(7)。由电机、链条、齿轮和齿轮支架组成的转动装置(10),可以匀速转动反应管使其受热均匀并使其中的反应物充分混合。取样口(5)用于实验前的高纯氮吹扫以及试验后的样品采集。将热电偶导线(12)以及热电偶(4)深入反应管中央测量反应管内温度,管内温度通过热电偶传到控制面板上。压力表(6)用于监测反应管内的实时压力。

|
| 1-内衬管; 2-转子; 3-恒温反应区; 4-热电偶; 5-取样口; 6-压力表; 7-防爆片; 8-电炉; 9-控制面板; 10-转动装置; 11-反应器框架; 12-热电偶导线 图 1 实验装置图 Fig.1 Reacting device diagram |
| |
使用一次性注射器分别将10 mL反应物[正十四烷中5.0%(质量分数,下同)的苄胺]和10 mL蒸馏水注入管式反应器。将反应管两端应包裹上保温带并置于电炉恒温区,设置热电偶和控制面板进行程序升温。将温度达到673 K的时间作为反应开始时间,在氮气氛围下反应。反应器转速为30 r·min-1,通过压力表读取水和裂化产物汽化所产生的系统压力(约23~26 MPa)。
油相产物用7890A安捷伦气相色谱-质谱仪和HP-5MS柱(30 m×250 μm×0.25 μm)进行分析。将0.2 μL样品注入温度为300 ℃的注射器入口。氦气作载气。色谱柱用于分离,升温程序为:40 ℃,保持1 min;5 ℃·min-1加热至300 ℃;20 ℃·min-1加热至400 ℃,保持5 min。
1.3 计算方法使用M06和M06-2X函数进行苄胺脱氮反应计算[21]。通过Berny/QST2/QST3方法寻找各反应的过渡态,并在M06/6-311G(d, p)计算水平上对所有反应物、产物以及过渡态(Transition state, TS)进行结构优化。对所有优化后的几何结构使用校正因子0.982[22]进行频率分析,以验证所有优化后的几何结构频率均为正,而过渡态有且只有1个虚频。在相同计算水平下进行内禀反应坐标计算以验证所寻过渡态的正确性。对于单点能(SP)的计算则使用更高精度的M06-2X/6-311+G(d, p)。采用自洽反应场(极性连续模型)方法修正因溶剂效应对几何结构和能量带来的影响[23-24]。所有计算均使用Gaussian09软件包[25]在密度泛函理论的基础上完成。基组重叠误差比反应能垒小若干个数量级,因此计算时忽略不计。
考虑到673 K下的校正焓H0→673 K,将673 K下的相对焓定义为反应能垒(ΔH673 K),通过公式(2)和(3)进行计算。
| $ H_{673 \mathrm{~K}}=\mathrm{SP}+0.982 \mathrm{ZPE}+H_{0 \rightarrow 673 \mathrm{~K}} $ | (1) |
| $ \Delta H_{673 \mathrm{~K}}=H_{\mathrm{TS}}-H_{\mathrm{R}} $ | (2) |
| $ \Delta H_{673 \mathrm{~K}}=H_{\mathrm{TS}}-H_{\mathrm{RC}} $ | (3) |
公式(1)中:SP、ZPE和H0→673 K分别代表物质的单点能、零点校正能和0~673 K的校正焓。公式(2)和公式(3)中:HTS、HR和HRC分别代表过渡态、反应物和反应络合物在673 K的焓值。
2 结果与讨论 2.1 油相产物分析表 1列出了苄胺(5.0%)在超临界水中反应1 h的油相产物分布数据。表 2显示了不同反应时间、温度和压力下的苄胺-SCW产物分布。
| 产物 | 收率/% | 产物 | 收率/% |
| 正戊烯 | 0.067 5 | 正癸烯 | 0.255 2 |
| 戊烷 | 0.076 0 | 癸烷 | 0.242 5 |
| 正己烯 | 0.115 7 | 苄胺 | 0.651 8 |
| 己烷 | 0.098 4 | 正十一烯 | 0.288 7 |
| 苯 | 0.262 4 | 十一烷 | 0.304 9 |
| 正庚烯 | 0.133 6 | 正十二烯 | 0.334 0 |
| 庚烷 | 0.139 2 | 十二烷 | 0.278 8 |
| 甲苯 | 1.919 6 | 十三烷 | 1.081 8 |
| 正辛烯 | 0.171 7 | 正十四烷 | 88.036 3 |
| 辛烷 | 0.159 5 | 十五烷 | 0.825 4 |
| 正壬烯 | 0.208 8 | BBA | 3.226 9 |
| 壬烷 | 0.199 1 | ||
| a实验温度为673 K,压力为23~26 MPa,反应时间为1 h。 | |||
| 产物 | 收率/% | ||||
| 1 h | 3 h | 1 h | 6 h | 12 h | |
| 673 K | 673 K | 723 K | 723 K | 723 K | |
| 26.7 MPa | 26.7 MPa | 35.8 MPa | 35.8 MPa | 35.8 MPa | |
| 氨气 | 66.00 | 101.00 | 109.00 | 74.00 | 87.00 |
| 甲苯 | 48.00 | 49.00 | 49.00 | 48.00 | 47.00 |
| 苯 | 11.00 | 22.00 | 17.00 | 32.00 | 28.00 |
| 苯甲醛 | 13.55 | 4.70 | 8.50 | 0.30 | 0 |
| 苯甲腈 | 0.10 | 0 | 0.20 | 0 | 1.0 |
| 苯甲醇 | 2.00 | 1.40 | 1.80 | 0 | 0 |
| 联苯 | 1.00 | 2.80 | 2.60 | 5.10 | 5.50 |
| BBA | 9.50 | 3.50 | 5.40 | 0 | 0 |
| 其它 | 0.60 | 0.80 | 0.80 | 1.00 | 1.40 |
从表 2可以看出,苄胺-SCW反应的最终产物主要有苯、甲苯和少量的联苯,中间产物则存在苯甲醛、苯甲醇和BBA。图 2a)是反应1 h时正十四烷在超临界水中分解的产物分布图,主要是相同碳数的C5-C15的直链烃,包括大量的烷烃和少量的烯烃。结合图 2和表 1可以看出,苄胺在超临界水中分解的主要产物是苯、甲苯和BBA。这一实验结果与Houser[19]和Taso[20]等的实验结果类似。结合本实验结果与前人[19-20]的实验结果,可以得出,苄胺在超临界水中分解的主要产物是苯和甲苯,而中间产物是苯甲醇、苯甲醛以及BBA。

|
| 图 2 的油相产物GC-MS图:a)反应物为正十四烷;b)反应物为正十四烷和苄胺 Fig.2 GC-MS chromatogram of oil phase products: a) n-tetradecane as a reactant; b) n-tetradecane and benzylamine as reactants |
| |
苄胺分子的原子标号如图 3所示,以下讨论均基于此编号。由于超临界水分子的电解性能极弱,因此它遵循的是自由基反应机理而非离子反应机理[26]。根据实验产物分布,可以推断出,苄胺-SCW反应的第1种可能路径是在1N-2C位发生自由基反应,生成苄基和氨基;然后,氨基夺得苄胺中的H·生成NH3,实现脱氮过程。Taso等[20]的研究表明,可能在1N-2C位发生脱氢反应,并在SCW分子的催化下形成亚胺;然后,亚胺进一步反应生成醛和氨,从而实现脱氮。此外,苄胺分子也可能与醛反应生成BBA。根据以上表述,苄胺-SCW脱氮反应可能包含自由基反应、脱氢反应和醛基反应3种反应系列。这3种反应系列可能存在6种可能的反应路径,如图 4所示。以下讨论均基于这些反应路径展开。

|
| 图 3 苯胺分子的原子标号 Fig.3 Atom labels in benzylamine structure |
| |

|
| 图 4 苄胺在超临界水中脱氮的可能路径 Fig.4 The potential reaction paths of denitrogenation for benzalymine in supercritical water |
| |
通过比较图 4中6条不同反应路径的能垒,找出苄胺-SCW脱氮的最可能路径。
2.3.1 自由基反应系列的能垒对比反应(1)、(3-1)和(3-2)分别是路径1、路径2和路径3中苄胺分子自由基反应系列的第1步反应,其反应方程式和能垒如图 5所示。由于SCW的催化作用是基于短链水分子簇的氢转移效应[27-28],所以它对于这些自由基反应不具有催化作用。反应(1)、(3-1)和(3-2)的能垒分别为315.2、423.4和336.9 kJ·mol-1。反应(3-1)的能垒太高,不可能发生,表明1N—H断键不可能发生,亦即路径2不可能发生。反应(3-2)和反应(1)的能垒之差仅为21.7 kJ·mol-1,2者皆有可能发生,这意味着2C—H断键及1N—2C断键可以同时发生,且1N—2C断键更为容易;路径1和3都有可能发生,且路径1是最佳自由基反应路径。

|
| 图 5 自由基反应系列的反应方程式和能垒 Fig.5 Reaction equations and energy barriers for free radical reaction sequence |
| |
路径1中的反应2是氨基夺氢反应,其反应方程式和能垒如图 6所示。反应(2-3)的能垒最低,可以看做是最主要的反应,氨基将从苄胺分子的2C位夺氢生成NH3和2C位苄胺自由基,从而完成脱氮过程。然后,2C位苄胺自由基参与到路径3的反应中。
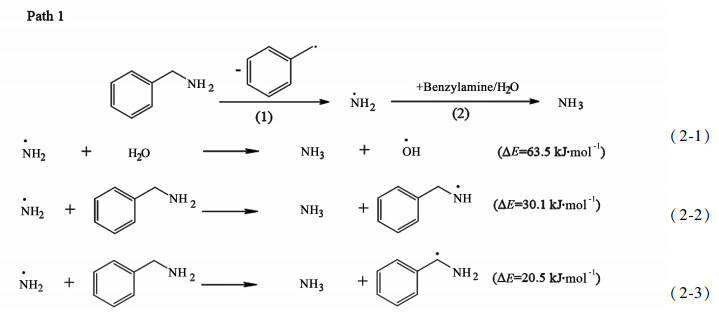
|
| 图 6 氨基夺氢反应的反应方程式和能垒 Fig.6 Reaction equations and energy barriers for amido grabbing hydrogen reaction |
| |
2C位苄胺自由基反应存在2种可能,其反应方程式和能垒如图 7所示。反应(4-2)是2C位苄胺自由基的脱氢链终止反应,反应(5)是2C位到1N位的自由基转化反应,2者的能垒之差仅为3.3 kJ·mol-1,表明2个反应可以同时发生。然而,通过过渡态搜索,未能找到反应(4-1)的过渡态,这意味着该反应不能发生,1N位苄胺自由基不能及时消耗。此外,对于反应(5),反应物的能量(0 kJ·mol-1)低于产物能量(83.2 kJ·mol-1),表示2C位苄胺自由基比1N位苄胺自由基更稳定,2C位自由基会部分转变为1N位自由基,另一部分会发生再脱氢反应生成亚胺结构;而1N位自由基会有更大比例转变回2C自由基,未转变的部分只能发生链终止反应而无法脱氮,故不做讨论。综上所述,2C位苄胺自由基反应中反应(4-2)是主要反应,而反应(5)发生的可能性较小。
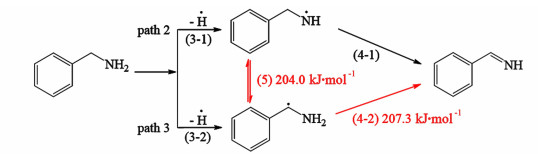
|
| 图 7 2C位苄胺自由基反应的反应方程式和能垒(红色) Fig.7 Reaction equations and energy barriers (red) for 2C position benzylamine free radical reaction |
| |
根据以上对自由基引发反应3条可能路径的讨论可以看出,路径1最可能发生,通过该路径可以实现脱氮过程。
2.3.4 脱氢反应系列的能垒对比脱氢反应系列的反应方程式和能垒如图 8所示。从图 8中可以看出,无论是否存在SCW的催化,反应(9)的能垒均比反应(6)的能垒低125 kJ·mol-1以上,这表明反应(9)是主要的脱氢反应,亦表明路径5是主要脱氢反应路径。该伯胺脱氢机理由本研究首次提出,并通过量子化学计算进行了验证。
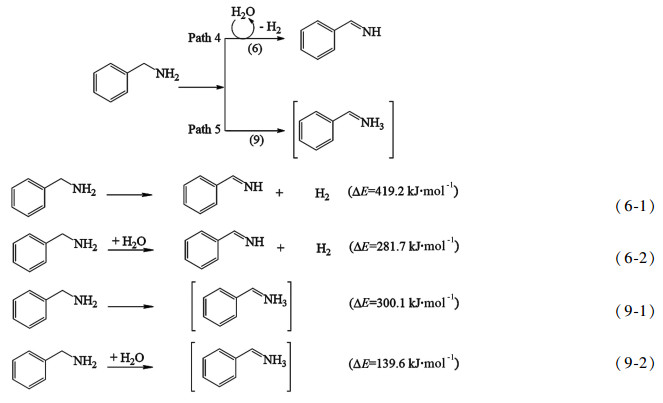
|
| 图 8 脱氢反应系列的反应方程式和能垒 Fig.8 Reaction equations and energy barriers for dehydrogenation reaction sequence |
| |
如上所述,路径5是主要的脱氢反应路径。路径5中的所有反应及各反应的能垒如图 9所示。由图 9b)可以看出,反应(7)、(8)和(10)的能垒分别为190.6、140.0和159.7 kJ·mol-1。反应(7)和(8)的低能垒表明亚胺在SCW中具有较强的反应活性,因此,路径5的后续反应可以迅速发生,生成氨和苯甲醛。
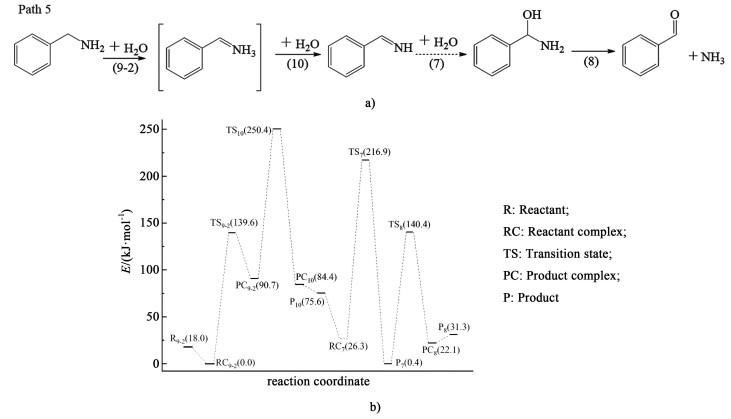
|
| 图 9 a) 路径5;b)路径5中各反应的能垒图 Fig.9 a) Path 5; b) energy barriers profile for Path 5 |
| |
醛基反应系列仅包含路径6,图 10显示了路径6中的所有反应及各反应的能垒图。路径5的反应产物苯甲醛可以作为路径6的反应物,与苄胺分子继续反应。

|
| 图 10 a) 路径6;b)路径6中各反应的能垒图 Fig.10 a) Path 6; b) energy barriers profile for Path 6 |
| |
从图 10a)可以看出,反应(12)和反应(13)的发生具有竞争性。即使不经水的催化,反应(11)的能垒也较低,为109.1 kJ·mol-1,表明该反应易发生。反应(12)相比反应(13)有近62.7 kJ·mol-1的能垒优势,表明反应(12)更易发生,P11发生脱水反应生成大量BBA;但是,反应(12)中产物BBA能量高于反应物能量,这又意味着BBA比反应物更活跃,因此,反应将逆向发生并产生P11,随着时间推移,反应(11)将达到反应平衡。根据能垒数据,反应(11)的平衡倾向于生成P11,反应性较弱的反应(13)会随着P11的大量生成而发生,而反应(13)的平衡倾向于生成P13,其可被后续的低能垒反应快速消耗,通过此路径P11被转化为稳定的最终产物。综上所述,反应(12)是路径6初始的主要反应;但是,经过较长的反应时间后,BBA会迅速与SCW反应生成大量P11;反应(13)将参与到分解过程中;反应(13)的产物P13是不稳定的亚胺羟基结构,易通过低能垒反应(14)(128.7 kJ·mol-1)转变为稳定的酰胺。反应(15)和(16)是酰胺降解生成羧酸和氨的过程,其能垒分别为174.3和122.1 kJ·mol-1。可以看出,反应(14)~(16)即使没有SCW的催化,其能垒也不高,这也是P13可以快速反应完成脱氮过程的原因。
2.3.7 3种不同反应系列的能垒比较在生成亚胺之前,自由基反应系列和脱氢反应系列中的反应是不同的。根据以上对各反应路径的能垒分析,自由基反应系列形成亚胺的最佳反应路径为:(1)→(2-3)→(4-2);脱氢反应系列形成亚胺的最佳反应路径为:(9-2)→(10)。2条路径的限速步骤分别是反应(1)和反应(9-2),因此,通过比较这2个限速步骤,便可得出哪一类反应更易发生。生成苯甲醛后的反应如路径6所示,反应(11)是路径6得以发生的重要前提,通过比较反应(11)和先前限速步骤的能垒,即可获悉路径6是否容易发生。如图 11所示,尽管反应(9-1)(300.1 kJ·mol-1)的能垒与反应(1)(315.2 kJ·mol-1)的能垒近似,但1个水分子催化的反应(9-2)(139.6 kJ·mol-1)的能垒远低于反应(1),这表明脱氢反应比自由基引发反应更容易发生,亦表明苄胺-SCW脱氮反应符合协同反应机理,而不是自由基反应机理。此外,即使没有水的催化,反应(11)的能垒也仅为109.1 kJ·mol-1,因此醛基反应亦会优先发生,然而,路径6发生的先决条件是路径5的发生。所以,苄胺-SCW脱氮反应的最佳路径是路径5和路径6。

|
| 图 11 3个反应系列中初步反应的能垒 Fig.11 Energy barriers for initial reactions in three reaction sequence |
| |
经过量子化学计算,确定了路径5和路径6是最佳反应路径。苄胺-SCW脱氮反应的主要产物是甲苯、氨和少量苯,而中间产物是苯甲醇、苯甲醛和BBA。路径5和路径6的产物为甲苯和氨,与实验结果一致。苯甲酸作为路径6的另外一种产物,可进一步降解并生成甲苯、苯或其他产物,因为它与苄胺脱氮关系不大,所以没有继续讨论。苯甲醛是实验的中间产物,其可以由路径5的两步脱氢反应生成,并通过路径6进一步发生反应。由于反应(13)的能垒(261.2 kJ·mol-1)较高,故反应(12)容易发生并生成中间产物BBA。因此,即使反应时间较短,也能检测到苯甲醛和BBA的存在。随着时间的推移,反应(12)朝反方向发生反应,导致P11的大量积累;当P11充分积累时,反应(13)开始发生;由于反应(14)~(16)的低能垒和中间产物苯甲醛和BBA的消耗,反应迅速发生,实现了苄胺分子的脱氮过程。通过以上量子化学计算与实验结果的比较,可以证明量子化学计算的有效性。
2.5 超临界水分子的催化作用由于苄胺-SCW反应体系中的脱氢反应路径涉及到许多氢转移反应,所以研究水分子在苄胺-SCW反应体系中的催化机理是非常重要的。将脱氢反应路径中的限速步骤反应(9)作为水分子催化反应的1个例子。
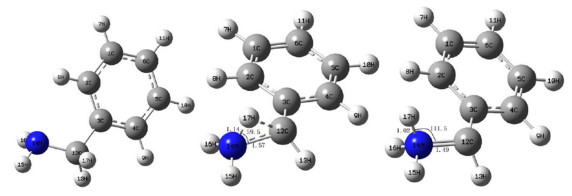
2.5.1 反应(9)的过渡态结构反应(9-1)中的反应物、过渡态(TS1)和产物Ph—CH=NH3经结构优化后的几何结构如图 12所示。在TS1中,2C位的氢原子攻击1N原子,形成1个三元环过渡态。新的N—H键和与N原子相连的2个旧的H原子之间的二面角(156.8°)与反应(9)产物平衡结构中的二面角(112.9°)相差很大。因此,在没有水分子催化的情况下发生反应,H原子需要在1N位重新定向,这是反应(9-1)能垒较高的原因。
|
| 图 12 反应(9-1)中反应物、过渡态和产物的几何结构 Fig.12 Geometries of reactant, transition state (TS1) and product in reaction (9-1) |
| |
反应(9-2)中的反应物、过渡态(TS2)和产物经结构优化后的几何结构如图 13所示。与TS1相比,TS2有1分子水作为催化剂。水分子与苄胺的1N-2C位形成五元环过渡态。在这种结构中,新的N—H键和与N原子相连的2个旧的H原子之间的二面角(122.6°)更接近于产物平衡结构中的二面角(112.9°)。结果表明,由于空间位阻较小,五元环过渡态比三元环过渡态更稳定。由图 9可知,反应(9-2)的能垒(139.6 kJ·mol-1)比反应(9-1)的能垒(300.1 kJ·mol-1)降低了160.5 kJ·mol-1,降幅高达53.5%,SCW分子起到显著的催化作用。

|
| 图 13 反应(9-2)中反应物、过渡态和产物的几何结构 Fig.13 Geometries of reactant, transition state (TS2) and product in reaction (9-2) |
| |
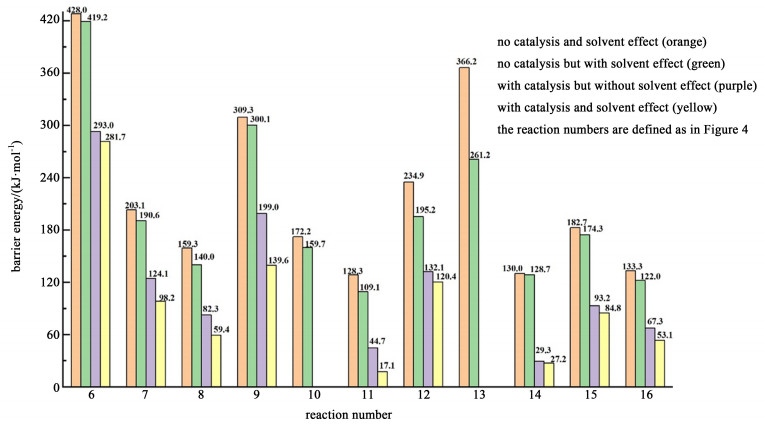
由于自由基反应不发生氢转移,所以其不能被水分子催化。超临界水的溶剂效应以及催化作用(以1分子水的催化为例)对反应(6)~(16)的能垒影响结果对比如图 14所示。经计算,没有搜索到反应(10)和(13)被1分子水催化时的过渡态,可能是因为相邻原子之间的H原子转移很难被水催化。从图 14中可以看出,无论是否有水的催化作用,反应(6)~(16)的能垒受超临界水的溶剂效应的影响,均有一定程度的降低。其中,降低效果最为明显的是反应(13),即使在无水催化的情况下,其能垒也由366.2 kJ·mol-1降低到261.2 kJ·mol-1。与溶剂效应相比,催化作用也可以降低反应能垒,且无论是否考虑溶剂效应,其降低能垒的效果都更为显著。其中,在1分子水的催化下,其他9个反应的能垒均大幅降低,特别是2个限速步骤:反应(9),Δ=160.5 kJ·mol-1;反应(11),Δ=92.0 kJ·mol-1。(Δ:无水催化和1分子催化时的能垒之差)。而反应(13)的后续拉动步骤反应(14)的势垒更是下降到极低的27.2 kJ·mol-1,这也再次证明了苄胺-SCW脱氮反应符合协同反应机理,而不是自由基反应机理。水分子的催化作用加速了反应(12)和(14)的发生,使反应(13)的平衡向产物方向移动。
|
| 图 14 反应能垒对比 Fig.14 Comparison of reaction energy barriers |
| |
苄胺在超临界水中的脱氮反应遵循协同反应机理而非自由基反应机理,最佳反应路径是路径5和路径6。路径5中:1) H原子将从2C位转移到1N位,形成不稳定的5价N作为中间产物;2) 2个与5价N相连的H原子脱离束缚,生成H2和亚胺;3) 亚胺与水分子加成生成中间产物Ph-C(OH)(NH2);4) Ph-C(OH)(NH2) 分解为苯甲醛和氨。路径6中,苯甲醛和苄胺分子反应生成中间产物BBA;中间产物BBA进一步反应实现脱氮过程。
苄胺脱氮过程中,超临界水分子主要作为反应物和氢转移催化剂参与反应。在1个分子水的催化下,限速步骤反应(9)的能垒由300.1 kJ·mol-1降低至139.6 kJ·mol-1,降幅为53.5%;醛基反应路径中的重要步骤反应(11)的能垒由109.1 kJ·mol-1降至17.1 kJ·mol-1,降幅高达84.3%;同样地,其它反应的能垒也大幅降低。此外,超临界水的溶剂效应也在一定程度上降低了反应能垒,在无水催化的情况下反应(13)的能垒由366.2 kJ·mol-1降低到261.2 kJ·mol-1,降幅为28.6%。
| [1] |
Upreti S R, Lohi A, Kapadia R A, et al. Vapor extraction of heavy oil and bitumen: A review[J]. Energy & Fuels, 2007, 21(3): 1562-1574. |
| [2] |
Bridjanian H, Samimi A K. Bottom of the barrel, an important challenge of the petroleum refining industry[J]. Petroleum and Coal, 2011, 53(1): 13-21. |
| [3] |
Kiasari H H, Nokandeh N R, Khishvand M, et al. A review of SAGD-ISSLW[J]. Petroleum Science and Technology, 2014, 32(6): 753-760. DOI:10.1080/10916466.2011.590830 |
| [4] |
Wang Z, Deng S, Gu Q, et al. Supcritical water extraction of Huadian oil shale under isothermal condition and pyrolysate analysis[J]. Energy & Fuels, 2014, 28(4): 2305-2313. |
| [5] |
Santos R G, Loh W, Bannwart A C, et al. An overview of heavy oil properties and its recovery and transportation methods[J]. Brazilian Journal of Chemical Engineering, 2014, 31(3): 571-590. DOI:10.1590/0104-6632.20140313s00001853 |
| [6] |
Shah A, Fishwick R, Wood J, et al. A review of novel techniques for heavy oil and bitumen extraction and upgrading[J]. Energy & Environmental Science, 2010. DOI:10.1039/b918960b |
| [7] |
Morimoto M, Sugimoto Y, Saotome Y, et al. Effect of supercritical water on upgrading reaction of oil sand bitumen[J]. The Journal of Supercritical Fluids, 2010, 55(1): 223-231. DOI:10.1016/j.supflu.2010.08.002 |
| [8] |
Watanabe M, Kato S N, Ishizeki S, et al. Heavy oil upgrading in the presence of high density water: Basic study[J]. The Journal of Supercritical Fluids, 2010, 53(1/2/3): 48-52. |
| [9] |
Amani M J, Gray M R, Shaw J M. Phase behavior of Athabasca bitumen+water mixtures at high temperature and pressure[J]. The Journal of Supercritical Fluids, 2013, 77: 142-152. DOI:10.1016/j.supflu.2013.03.007 |
| [10] |
Kozhevnikov I V, Nuzhdin A L, Martyanov O N. Transformation of petroleum asphaltenes in supercritical water[J]. The Journal of Supercritical Fluids, 2010, 55(1): 217-222. DOI:10.1016/j.supflu.2010.08.009 |
| [11] |
Canıaz R O, Erkey C. Process intensification for heavy oil upgrading using supercritical water[J]. Chemical Engineering Research and Design, 2014, 92(10): 1845-1863. DOI:10.1016/j.cherd.2014.06.007 |
| [12] |
Sato T, Adschiri T, Arai K, et al. Upgrading of asphalt with and without partial oxidation in supercritical water[J]. Fuel, 2003, 82(10): 1231-1239. DOI:10.1016/S0016-2361(03)00019-X |
| [13] |
Sato T, Mori S, Watanabe M, et al. Upgrading of bitumen with formic acid in supercritical water[J]. The Journal of Supercritical Fluids, 2010, 55(1): 232-240. DOI:10.1016/j.supflu.2010.07.010 |
| [14] |
Cheng Z, Ding Y, Zhao L, et al. Effects of supercritical water in vacuum residue upgrading[J]. Energy & Fuels, 2009, 23(6): 3178-3183. |
| [15] |
Li N, Yan B, Xiao X. A review of laboratory-scale research on upgrading heavy oil in supercritical water[J]. Energies, 2015, 8(8): 8962-8989. DOI:10.3390/en8088962 |
| [16] |
Kozhevnikov I V, Nuzhdin A L, Martyanov O N. Transformation of petroleum asphaltenes in supercritical water[J]. The Journal of Supercritical Fluids, 2010, 55(1): 217-222. DOI:10.1016/j.supflu.2010.08.009 |
| [17] |
Wang J, He F, Li Y, et al. New insights into isopropylthiobenzene decomposition in supercritical water[J]. RSC Advances, 2016, 6(96): 93260-93266. DOI:10.1039/C6RA20955F |
| [18] |
He F, Wang J, Li Y, et al. Quantum chemistry calculations on the mechanism of isoquinoline ring-opening and denitrogenation in supercritical water[J]. Industrial & Engineering Chemistry Research, 2017, 56(7): 1782-1790. |
| [19] |
Houser T, Tsao C, Dyla J, et al. The reactivity of tetrahydroquinoline, benzylamine and bibenzyl with supercritical water[J]. Fuel, 1989, 68(3): 323-327. DOI:10.1016/0016-2361(89)90096-3 |
| [20] |
Tsao C, Zhou Y, Liu X, et al. Reactions of supercritical water with benzaldehyde, benzylidenebenzylamine, benzyl alcohol, and benzoic acid[J]. The Journal of Supercritical Fluids, 1992, 5(2): 107-113. DOI:10.1016/0896-8446(92)90027-H |
| [21] |
Zheng J, Zhao Y, Truhlar D G. The DBH24/08 database and its use to assess electronic structure model chemistries for chemical reaction barrier heights[J]. Journal of Chemical Theory and Computation, 2009, 5(4): 808-821. DOI:10.1021/ct800568m |
| [22] |
Alecu I M, Zheng J, Zhao Y, et al. Computational thermochemistry: Scale factor databases and scale factors for vibrational frequencies obtained from electronic model chemistries[J]. Journal of Chemical Theory and Computation, 2010, 6(9): 2872-2887. DOI:10.1021/ct100326h |
| [23] |
Wong M, Wiberg K B, Frisch M. Hartree-Fock second derivatives and electric field properties in a solvent reaction field: Theory and application[J]. The Journal of Chemical Physics, 1991, 95(12): 8991-8998. DOI:10.1063/1.461230 |
| [24] |
Wong M, Frisch M J, Wiberg K B. Solvent effects. 1. The mediation of electrostatic effects by solvents[J]. Journal of the American Chemical Society, 1991, 113(13): 4776-4782. DOI:10.1021/ja00013a010 |
| [25] |
Frisch M J, Trucks G W, Schlegel H B, et al. Gaussian 09 revision A. 1.[M]. Wallingford CT: Gaussian Inc, 2009.
|
| [26] |
Hoffmann M M, Conradi M S. Are there hydrogen bonds in supercritical water?[J]. Journal of the American Chemical Society, 1997, 119(16): 3811-3817. DOI:10.1021/ja964331g |
| [27] |
Kalinichev A G, Churakov S V. Size and topology of molecular clusters in supercritical water: A molecular dynamics simulation[J]. Chemical Physics Letters, 1999, 302(5/6): 411-417. |
| [28] |
Kalinichev A G, Churakov S V. Thermodynamics and structure of molecular clusters in supercritical water[J]. Fluid Phase Equilibria, 2001, 183/184: 271-278. DOI:10.1016/S0378-3812(01)00438-1 |
 2021, Vol. 38
2021, Vol. 38





