以油滴作为分散相,水相作为连续相的水包油(O/W)乳液被广泛用于食品、药品、化妆品、个人护理和其他一些领域[1]。乳液是一种热力学不稳定的胶体体系,容易产生乳析、絮凝、聚结和奥斯特瓦尔德熟化等不稳定现象[2-4]。合成乳化剂常被用于稳定食品工业中的乳液,但是它们可能对人类有毒并对环境产生污染[5]。因此,近年来学者开始更加关注天然生物聚合物的开发。
既包含亲水基团又包含亲脂基团的表面活性蛋白,可以被用作乳化剂并形成稳定的油水界面来防止液滴在乳液中聚集[5]。明胶(gelatin, GE)是由动物皮肤、肌腱、骨中的胶原水解得到的天然蛋白质大分子。明胶在其等电位点(IEP)以下具有正表面电荷,在IEP之上具有负表面电荷。构成蛋白质的氨基酸约有20种,而明胶就含有其中的18种,并且其中7种是人体所必需的,因此营养价值非常高。明胶具有成膜的潜力,它可以形成一种外部屏障,限制光、热和氧的影响来保护食品。明胶具有与表面活性剂相似的性质,但是当明胶被用作单一乳化剂时,乳液倾向于形成大的液滴,并且稳定性很差[6],限制了其在食品加工中的应用。因此,在蛋白质乳液中常加入一些多糖,利用多糖的空间位阻与黏度提高乳液的稳定性[7]。并且由于蛋白质与带电荷多糖的潜在相互作用,可能会产生新的两亲性的复合结构,这些复合物能够代替合成的低摩尔质量的乳化剂[8]。
在蛋白质乳液中通常加入的多糖有阿拉伯胶、黄原胶和壳聚糖等[9-11]。Anari等报道了较低pH=3.6的条件促进了明胶与阿拉伯胶之间的静电吸引作用,在乳液表面产生了更厚的界面层,由于空间斥力的作用所形成的乳液液滴更小、更稳定[9]。Roy等探究了pH=5.5条件下的明胶乳液,壳聚糖的加入改善了乳液的乳析稳定性,乳滴界面层的复合凝聚物保证了乳液的长期稳定性[11]。海藻酸钠(sodium alginate, AL)存在于褐藻的细胞壁中,是由1, 4-连接的α-L-古洛糖醛酸和β-D-甘露糖醛酸的交替结构组成。海藻酸钠是带负电荷的线性聚电解质。当pH值低于pKa(pH=3.38~3.65)值时,羧基的解离受到抑制[12]。海藻酸钠具有许多理想的特性,如胶凝和增稠特性、生物降解性、廉价易得等,这使得海藻酸钠具有广泛的应用价值。AL还与降低血清胆固醇、甘油三酸酯和血糖有关,因此可以预防高血压、糖尿病和肥胖症等疾病。研究发现,AL具有高电荷性的线性结构,在液滴周围形成具高电荷的界面膜,进而通过静电斥力降低乳状液液滴的聚集[13]。利用明胶-海藻酸钠相互作用制备的复合生物膜或凝胶微球在食品包装、生物医药等领域有着广泛的应用[14-15]。Natthiya等探究了由于明胶和海藻酸钠分子之间的静电吸引,特别是在酸性条件下,通过添加海藻酸钠可以明显改善明胶基食品泡沫的稳定性能[16]。然而,关于明胶和海藻酸钠之间的协同作用对乳液体系稳定性影响的报道却十分有限,2者的相互作用对乳液稳定性提高的机制尚不清楚。因此本文拟以明胶与海藻酸钠组合制备乳液,探究2者的协同作用对乳液稳定性的影响。
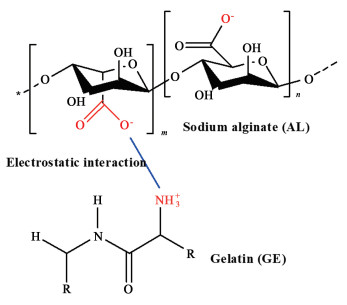
在本研究中,通过Zeta电位法和紫外光谱法研究了明胶与海藻酸钠在25 ℃水溶液中的静电相互作用(图 1)。在此基础上研究了GE与AL浓度比例和溶液的pH值对乳液稳定性的影响。通过稳定性分析仪LUMiFuge116分析了乳液的乳析稳定性和乳析速率。此外,该研究还考察了工艺参数和环境温度对于GE-AL稳定乳液的影响。从微观角度探讨了明胶与海藻酸钠的复合凝聚现象及它们的协同作用对乳液稳定性的影响。该研究对GE-Al的应用和乳液的设计具有一定的指导意义。
|
| 图 1 GE-AL静电相互作用结构原理示意图 Fig.1 The schematic mechanism of GE-AL electrostatic interaction structure |
| |
B型明胶(GE)(凝胶强度为Bloom120,食品级,99%)来源于牛皮购于河南豫中生物科技有限公司。食品级海藻酸钠(AL)(质量分数为99%),购于山东亚亨生物技术有限公司。用于抑制细菌生长的苯甲酸钠(质量分数为99.5%)购于上海迈瑞尔化学技术有限公司。氢氧化钠(NaOH)(AR,质量分数为96%)购于上海阿拉丁。盐酸购于连云港市宏兴化工有限公司。大豆油购于京东超市。
Zeta电位分析仪(Zeta sizer nano ZS90),英国马尔文仪器有限公司;Lambda750 s紫外分光光度计,美国PerkinElmer有限公司; 激光粒度分析仪(Master sizer3000),英国马尔文仪器有限公司;颗粒成像分析仪(Morphonlogi G3),英国马尔文仪器有限公司;LUMiFuge116稳定性分析仪(L.U.M.GmbH,德国)。
1.2 储备液及乳液的制备将明胶和海藻酸钠加入25 ℃的蒸馏水(含0.1%苯甲酸钠)中溶胀1 h,然后升温至40 ℃搅拌溶解过夜。为了测定ζ电位,将储备溶液总浓度在给定的pH值(3.5~7.0)的范围内稀释至0.05%。不同质量浓度比例的GE与AL(R=1∶0, 8∶1, 4∶1, 2∶1, 1∶1, 0∶1)溶液总浓度CT设为0.05%(W/V)。
将大豆油添加到提前制备好的明胶-海藻酸钠的复合水溶液中,使得最终溶液中大豆油含量为5%,明胶和海藻酸钠的总浓度CT为2%(R=1∶0,4∶1,2∶1,1∶1,1∶2),接着使用均质器(型号T10,IKA,德国)在21 200 r/min下乳化10 min。然后为了最大程度地降低稀释效果使用一系列浓度的氢氧化钠和盐酸溶液(10.0,5.0,2.0,1.0,0.5 mol/L)将乳液缓慢调节到不同的pH值(4.5~7.0)。之后,将乳液在室温下放置24 h,然后进行下一次分析。
1.3 Zeta电位的测量ζ电势反映了胶体分散颗粒表面的电势[17]。使用Zetasizer nano ZS90测定溶液的电势值,测定温度25 ℃,平衡时间1 min,每个样品重复测量3次。
1.4 明胶-海藻酸钠复合溶液浊度分析使用紫外分光光度计在600 nm下测定复合溶液的浊度。将样品放置在光程为1 cm的样品池中在25 ℃下测量GE-AL复合溶液的浊度,每个样品平行测定3次,取平均值。浊度(T)定义为:
| $ T = - {\rm{ln}}(I/{I_0}) $ | (1) |
式(1)中:I为透射光强度,I0为入射光强度。
1.5 乳液粒径分析通过激光粒度分析仪测定乳液中液滴的粒度大小分布。乳液样品用水稀释500倍以避免光散射效应,并在室温下以2 000 r/min的搅拌速度进行分析。将水的折射率设定为1.33,将分散相的折射率设定为1.45,将分散相的吸光值设定为0.001。使用体积平均粒径D43来表示平均液滴大小。每个样品重复测定3次,取平均值。
1.6 乳液的微观结构分析通过颗粒成像分析仪,观察乳液的微观结构。将样品滴在载玻片上,然后慢慢盖上盖玻片防止气泡的产生,稳定1 min后在室温下放大50或20倍观察液滴的分布状态。
1.7 乳液乳析稳定分析利用LUMiFuge116稳定性分析仪测量乳液的乳析稳定性。LUMifuge116模拟了重力作用下乳液的乳析、沉降和相分离等过程[18]。如图 2所示它通过6~2 300 g的离心力提高了乳液两相分离速度从而减少了测试时间,并通过测量发射光的透射率来分析样品的粒子分布和稳定性[19]。它不仅可以检测透光率随时间的变化,还可以检测整个样品瓶透过率的变化,并通过计算机对得到的图谱进行积分计算,显示为积分透光率。积分透光率反映了乳液的乳析稳定性,透光率越高,稳定性越差。此外还可以计算透光率曲线的位置随时间的变化率,该变化率可以反映乳液由于不稳定而生成乳析层的乳析速率。透光率曲线随着时间的推移由红色变为绿色。将样品装入2 cm3的试管中,并在30 ℃和2 500 r/min离心转速下测量30 min。
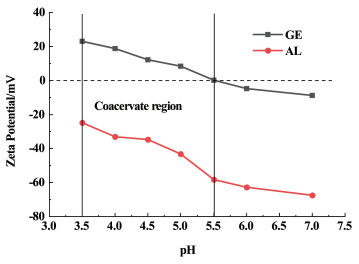
2 结果和讨论 2.1 明胶和海藻酸钠溶液的Zeta电位分析和复合溶液的浊度分析对明胶和海藻酸钠的ζ电势分析可以便于理解pH值对GE和AL之间静电相互作用的影响。从图 3中可以看出,在pH值在3.5~7.0范围内,明胶的ζ电位从23.07 mV降低到-8.69 mV。明胶分子中既含氨基又含羧基,它们的相互作用程度受溶液中pH值的影响。随着pH值的升高,氨基被中和转化为(—NH2),而羧基变为带负电荷的(—COO-),因此溶液中正电荷密度降低。
|
| 图 3 明胶和海藻酸钠溶液(0.05%)在不同pH值下的电势值 Fig.3 Zeta(ζ) potential of pure aqueous (0.05%) gelatin and sodium alginate in different pH |
| |
从图 3中可以看出明胶溶液由正电荷转变为负电荷的等电位点是pH=5.5[20]。随着pH值由3.5升高到7.0,由于海藻酸钠分子链上甘露糖醛酸和古洛糖醛酸的去质子化效应(其pKa值分别为3.38和3.65),其Zeta电位从-27.20 mV下降到-68.50 mV,这与Klassen等[21]所报道的数据是一致的。图 3还显示了蛋白质IPE(pH=5.5)以下的复合物凝聚区,在该区域带相反电荷的大分子之间产生静电相互作用形成复合凝聚物。
浊度变化可以用作反映2种带相反电荷的生物聚合物由于静电吸引产生复合凝聚强弱的指标[22]。根据GE和AL的电荷特征,本实验分析了pH值和GE与AL浓度比R(1∶0~0∶1)对复合凝聚物形成的影响。
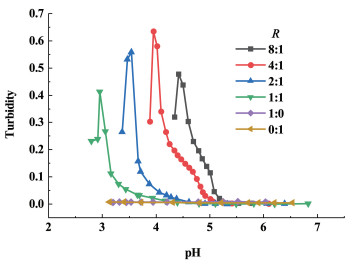
如图 4所示,对于纯0.05%(W/V)的明胶和海藻酸钠纯溶液在考察的pH值范围内并没有出现体系浊度明显的变化。由此在考察的pH值范围内,体系内浊度的增大或减少全部是由2种生物大分子的电荷特性所引起的静电相互作用产生的。在酸滴定过程中,pH值低于5.1时,在每个浓度比例下(R=8∶1~1∶1),体系都会出现浑浊。这表明,在pH值低于5.5(IPE)的范围内,带正电的GE分子和带负电的AL分子形成了不溶性的复合物。随着pH值的进一步降低,浊度显著增加,并最终达到1个峰值,此处的pH值被称为pHopt,表明在该比例下2种大分子的静电相互作用变得最大。当pH值低于pHopt时,浊度开始降低,表明形成的复合凝聚物开始分解,因为海藻酸钠分子链上的羧基的质子化阻碍了与明胶之间的静电相互作用。在浓度比R为4∶1和pH=3.9时,浊度取得最大值,这表明AL分子被GE分子吸附饱和,复合凝聚物的量达到最大值。此外,从图 4中还可以看出,随着浓度比R从1∶1增加到8∶1,浊度曲线移向更高的pH值。造成这种现象的原因可能是: 在R值较高时,每个AL分子都可以吸附更多的GE分子,因此,在高的pH值下带较少正电荷的GE分子足以满足形成复合物的需要。一些学者还发现添加多糖可以改变蛋白质的二级结构。本工作中,在相同pH值的条件下,随着AL浓度升高浊度值降低,这可能是高浓度的海藻酸钠(R=1∶1)抑制了明胶三螺旋结构的形成,然后三螺旋结构的减少影响了GE-AL之间的相互作用[23]。该结果与明胶浓度对明胶-壳聚糖复合系体系的影响相似[11]。
|
| 图 4 不同浓度比例R的浊度曲线(CT=0.05%)随pH值的变化 Fig.4 Turbidity curves for different R (CT=0.05%) as a function of pH |
| |
乳液液滴的粒度分布对于乳液的稳定性特别重要,一般来说,液滴越小,乳液系统越稳定[24]。许多研究报道了乳液制备过程中工艺参数对于乳液粒径的影响,例如均质器的搅拌速度和均质时间[25-26]。在这一部分, 在均质速度16 800、19 000和21 200 r/min和均质时间3~10 min的条件下制备了微米级均匀乳液(R=1∶1)。图 5a)显示出了液滴的显微观察,而图 5b)显示出了搅拌速度和时间与乳液的液滴直径之间的关系。

|
| 图 5 a) 乳液在不同的搅拌速度和搅拌时间3~10 min内的显微结构图、b)乳液在不同的搅拌速度和搅拌时间3~ 10 min内的粒径大小D43显示值为平均值(n=3) Fig.5 a) Micrographs of emulsion droplets at different stirring speed for 3~10 min, b) the particle size distribution D43 of emulsion droplets at different stirring speed after 3~10 min. Average values are shown(n=3) |
| |
可以看出,随着均质化速度和剪切时间的增加,液滴的体积直径逐渐减小,并且液滴的形态变得更加均匀。因此,均质器的速度和剪切时间是形成稳定乳液的重要参数[27]。当均质器转速为19 000 r/min时,乳液分散相对均匀。继续增大均质转速至21 200 r/min,乳液液滴大小更为均匀。但是如果转速过高,反而不利于对体系的稳定。转速过大会导致液滴表面积过大,表面能过高,导致分散均匀的乳液小液滴又重新聚集,不利于乳液的稳定。因此为了系统地研究其他因素(pH值、浓度比和温度)对乳液稳定性的影响,在以下实验中,均质器速度设置为21 200 r/min,剪切时间设置为10 min。
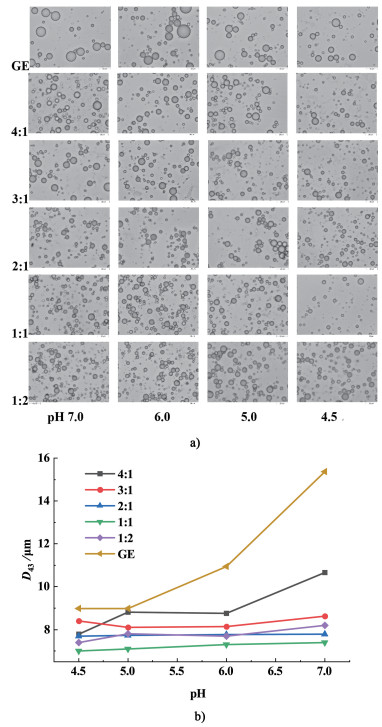
2.3 质量浓度比例R和pH值对乳液稳定性的影响这项工作的目的是研究在不同pH值和不同浓度比例R下明胶和海藻酸钠的协同作用对乳液液滴粒径大小、分散性和乳液稳定性的影响。通过激光粒度分析仪和颗粒成像仪分别测量了在pH值在4.5~7.0范围内和GE与AL质量浓度比R(4∶1~1∶2)以及纯2%GE条件下制备的乳液的平均粒径和液滴的形态。结果见图 6。
|
| 图 6 a) 乳液在不同浓度比例R和不同pH值下的显微结构图(50×);b)乳液在不同浓度比例R和不同pH值下的粒径大小D43显示值为平均值(n=3) Fig.6 a) Micrographs of emulsion droplets at different ratio of R in different pH; b) particle size distribution D43 of emulsion droplets with different R in different pH. Average values are shown(n=3) |
| |
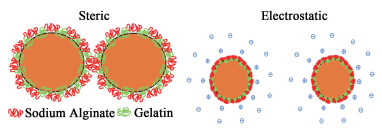
从图 6b)可以看出,在高pH值6.0和7.0的条件下利用纯GE所制备的乳液粒径要明显高于GE-AL,并且随着pH值的升高乳液粒径逐渐增大,乳化效果减弱,这可能是乳滴液滴之间静电排斥力减弱所造成的,Niu等在卵白蛋白-阿拉伯胶体系中同样发现了类似的现象[28]。此外图 6b)中所有浓度比例R(4∶1~1∶2)下乳液液滴粒径随pH值的降低呈下降的趋势,这与图 6a)的微观观察结果是一致的。这得益于随着pH值的降低明胶与海藻酸钠的静电相互作用得到了增强,因此形成了更有益于乳液稳定的界面结构。并且在4∶1到1∶1的浓度比例范围内,随着海藻酸钠比例的增大,乳液粒径逐渐变小,液滴分布更为均匀,这表明更高浓度的海藻酸钠促进了乳液的稳定。当R为1∶1时,与其他浓度比例相比乳液具有更小的液滴粒经,这表明2种生物聚合物在该比例下产生了较好的有利于乳液稳定的协同作用。图 7展示了明胶与海藻酸钠在油水界面存在的相互作用。明胶和海藻酸钠在乳液表面形成稳定的界面层,在液滴之间产生强的静电排斥和空间排斥作用以避免液滴的聚集。在pH=4.5和R为1∶1的比例下,得到的乳液液滴粒径最小为7.0 μm,并且液滴微观形态非常均匀。
|
| 图 7 通过空间和/或静电相互作用实现GE-AL乳液稳定的机理 Fig.7 Mechanisms for GE-AL emulsion stabilization through steric and/or electrostatic interactions |
| |
当R为1∶2时,乳液液滴的平均粒径大于R为1∶1比例下的粒径,造成这一现象的原因可能是明胶量的减少不足以为海藻酸钠提供有效的界面结合点,因此限制了海藻酸钠对乳液稳定性的提高;此外连续相中大量未吸附的海藻酸钠产生的耗尽絮凝是一个重要原因[29]。因此,当GE与AL的浓度比例R超过1∶1时,明胶和海藻酸钠的协同作用降低。
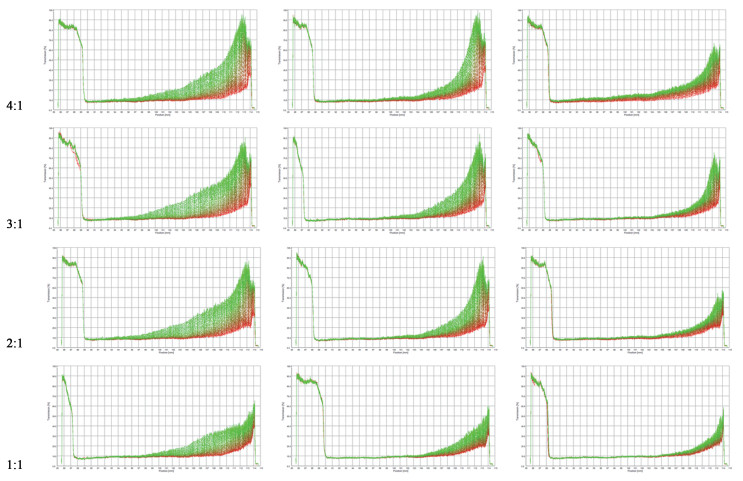
2.4 乳液的乳析稳定性乳液产品在长期放置过程中会出现乳析分层现象。在该工作中,利用LUMiFuge116稳定性分析仪来测量分析了乳液的乳析稳定性。图 8描述了不同GE与AL浓度比例(R=4∶1~1∶1)和不同pH值(4.5~7.0)条件下,乳液在3 000 r/min的转速下离心30 min后的透光率曲线,并且曲线随着时间的推移,由红色变为绿色。容器的整体透光率以及pH=4.5的乳液透光率曲线位置随时间变化的斜率值均已通过电脑统计计算并表示在表 1中。乳液由于离心力的作用变得不稳定而发生乳析,因此透光率曲线位置随时间变化的斜率值反映了乳液生成乳析层的乳析速率。
|
| 图 8 在3 000 r/min的转速下不同R和pH值下的透光率曲线 Fig.8 Transmission profiles at 3 000 r/min with different R and pH values |
| |
| R | integral transmission/% | slope/(μm·s-1) | ||
| pH=7.0 | pH=5.0 | pH=4.5 | pH=4.5 | |
| 4∶1 | 27.82 | 21.25 | 19.43 | -5.612 |
| 3∶1 | 27.55 | 20.05 | 15.01 | -3.312 |
| 2∶1 | 26.87 | 19.33 | 14.97 | -1.744 |
| 1∶1 | 19.58 | 17.61 | 12.23 | -1.433 |
从表 1中可以看出,在所有比例下,pH值为4.5时,积分透光率要比其他pH值条件下的值低,意味着酸性条件更有利于乳液的稳定。而产生这种稳定的原因是在酸性条件更有利于明胶和海藻酸钠形成更厚更致密的乳液界面层,来防止液滴在离心过程中破裂。如前面章节所述,随着pH值降低,由于明胶与海藻酸钠之间更强的静电相互作用可以产生更多更致密的复合凝聚物,因而在油滴表面形成了更厚更紧密的界面层[30]。随着明胶海藻酸钠比例的降低(4∶1至1∶1)积分透光率逐渐降低。这表明乳液变得越来越更稳定,这种趋势与粒度分析的结果是一致的。此外,乳液生成乳析层的乳析速率由R为4∶1比例下的5.621 μm/s降低到R为1∶1比例时的1.433 μm/s。一方面是由于2种生物聚合物更好的协同作用使得乳液液滴产生更强的空间或静电斥力,另一方面也是由于体系中海藻酸钠含量的升高导致体系黏度比较大。依据斯托克斯定律,液滴的沉降速率与体系的黏度成反比,因此导致乳液析出速率的降低。这更加证明了2种聚合物分子在1∶1的比例下有着非常好的稳定乳液的协同作用。当pH值为4.5浓度比例为1∶1时,积分透光率为最低值12.23%,这意味着该乳液的乳析稳定性比在其他条件下更好。
2.5 温度对乳液稳定性的影响在商业应用中,乳液在生产、加工及储藏过程中的热稳定性是非常重要的。Ding等制备了明胶稳定的乳液,并探究了温度对该乳液体系稳定性的影响,结果发现当储藏温度为37~60 ℃时,乳液发生严重分层,乳滴破裂无法再被分散,因此限制了乳液的应用[31]。在该工作中将制备好的乳液(R=1∶1)在25~80 ℃条件下加热约30 min,并通过粒度分布和微观结构观察来研究乳液的热稳定性,结果见图 9。
|
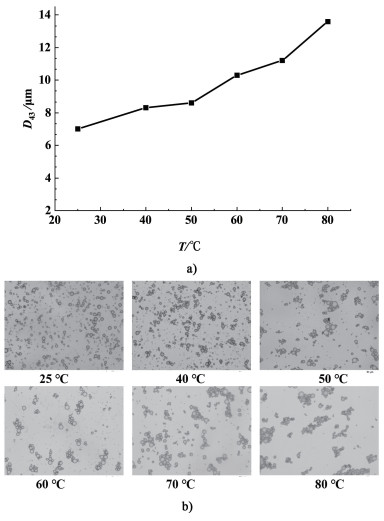
| 图 9 a) 乳液(R=1∶1)在不同温度25~80 ℃的粒径大小D43; b)乳液在不同温度下的显微结构图(20×) 显示值为平均值(n=3) Fig.9 (a) D43 of emulsions (R=1∶1) at different temperature of 25~80 ℃; b) Micrographs of emulsion droplets (R=1∶1) at temperature of 25~80 ℃ |
| |
从图 9a)可以看出,乳液在25 ℃和50 ℃之间的粒径D43有一个从7.0 μm到8.6 μm的小幅增加趋势,这一结果可能是由于多糖吸附在蛋白质包裹的油滴的表面,增加了界面层的厚度和电荷的堆积,从而增加了油滴之间的位阻和静电排斥力。然而,在较高的温度50~80 ℃之间的粒径D43从8.6 μm显著增加到13.6 μm,从图 9b)的微观结构分析中也可以观察到严重的液滴聚集现象。产生这一现象的原因可能是在高温下蛋白质变性因而暴露出更多的反应基团(非极性键等),从而增强了蛋白质稳定的乳液液滴之间的吸引力相互作用[32]。这些结果表明乳液在50 ℃以下具有更好的稳定性。
3 结论研究了GE-AL由于静电相互作用而形成的复合凝聚物以及它们的协同作用对水包油乳液稳定性的影响。随着GE和AL的质量浓度比R从1∶1增加到8∶1, 复合凝聚物的浊度曲线移向更高的pH值。pH低值于5.1时,在所有的浓度比例下GE-AL的静电相互作用都随着pH值的降低而加强。同时我们系统地研究了不同因素(pH值、浓度比R和温度)对乳液稳定性的影响。结果表明,在所有浓度比例下乳液液滴的粒径随着pH值从7.0降至4.5呈下降趋势。在pH值为4.5和1∶1的比例下,GE-AL具有更好的协同作用,乳液粒径较小为7.0 μm,液滴形态均匀,乳析稳定性好(积分透光率12.23%),乳析速率最低为1.433 μm/s。此外,与较高温度相比,乳液在50 ℃以下发生较少的聚集。该研究为利用明胶和海藻酸钠的协同作用提高乳液的稳定性的应用提供了有价值的信息。
| [1] |
Walstra P. Food emulsions: Principles, practice, and techniques[J]. Trends in Food Science & Technology, 1999. DOI:10.1016/S0924-2244(99)00042-4 |
| [2] |
Dickinson E. An introduction to food colloids[M]. England Oxford: Oxford Science Publishers, 1992.
|
| [3] |
Hiemenz P C, Rajagopalan R. Principles of colloid and surface chemistry[M]. Third edition. New York: Marcel Dekker, 1997.
|
| [4] |
Israelachvili J. Intermolecular and surface forces[M]. Third Edition. London, UK: Academic Press, 2011.
|
| [5] |
Dapueto N, Troncoso E, Mella C, et al. The effect of denaturation degree of protein on the microstructure, rheology and physical stability of oil-in-water (O/W) emulsions stabilized by whey protein isolate[J]. Journal of Food Engineering, 2019, 263: 253-261. DOI:10.1016/j.jfoodeng.2019.07.005 |
| [6] |
Surh J, Decker E A, McClements D J. Properties and stability of oil-in-water emulsions stabilized by fish gelatin[J]. Food Hydrocolloids, 2006, 20(5): 596-606. DOI:10.1016/j.foodhyd.2005.06.002 |
| [7] |
Dickinson E. Interfacial structure and stability of food emulsions as affected by protein-polysaccharide interactions[J]. Soft Matter, 2008, 4(5): 932-942. DOI:10.1039/b718319d |
| [8] |
Albano K M, Cavallieri  L F, Nicoletti V R. Electrostatic interaction between proteins and polysaccharides: Physicochemical aspects and applications in emulsion stabilization[J]. Food Reviews International, 2019, 35(1): 54-89. DOI:10.1080/87559129.2018.1467442 |
| [9] |
Anvari M, Joyner (Melito) H S. Effect of fish gelatin-gum Arabic interactions on structural and functional properties of concentrated emulsions[J]. Food Research International, 2017, 102: 1-7. DOI:10.1016/j.foodres.2017.09.085 |
| [10] |
Xu X, Luo L, Liu C, et al. Utilization of anionic polysaccharides to improve the stability of rice glutelin emulsions: Impact of polysaccharide type, pH, salt, and temperature[J]. Food Hydrocolloids, 2017, 64: 112-122. DOI:10.1016/j.foodhyd.2016.11.005 |
| [11] |
Roy J C, Salaün F, Giraud S, et al. Surface behavior and bulk properties of aqueous chitosan and type-B gelatin solutions for effective emulsion formulation[J]. Carbohydrate Polymers, 2017, 173: 202-214. DOI:10.1016/j.carbpol.2017.06.001 |
| [12] |
Simsek-Ege F A, Bond G M, Stringer J. Polyelectrolyte complex formation between alginate and chitosan as a function of pH[J]. Journal of Applied Polymer Science, 2003, 88(2): 346-351. DOI:10.1002/app.11989 |
| [13] |
Fioramonti S A, Arzeni C, Pilosof A M R, et al. Influence of freezing temperature and maltodextrin concentration on stability of linseed oil-in-water multilayer emulsions[J]. Journal of Food Engineering, 2015, 156: 31-38. DOI:10.1016/j.jfoodeng.2015.01.013 |
| [14] |
Amini H, Hashemzadeh S, Heidarzadeh M, et al. Cytoprotective and cytofunctional effect of polyanionic polysaccharide alginate and gelatin microspheres on rat cardiac cells[J]. International Journal of Biological Macromolecules, 2020, 161: 969-976. DOI:10.1016/j.ijbiomac.2020.06.018 |
| [15] |
董宇豪, 陈浩, 吴志宇, 等. 海藻酸钠-鱼明胶复合可食膜的制备及特性研究[J]. 中国食品学报, 2020, 1: 134-140. Dong Yuhao, Chen Hao, Wu Zhiyu, et al. Preparation and characterization of sodium alginate-fish gelatin composite edible film[J]. Journal of Chinese Institute of Food Science and Technology, 2020, 1: 134-140. (in Chinese) |
| [16] |
Phawaphuthanon N, Yu D, Ngamnikom P, et al. Effect of fish gelatine-sodium alginate interactions on foam formation and stability[J]. Food Hydrocolloids, 2019, 88: 119-126. DOI:10.1016/j.foodhyd.2018.09.041 |
| [17] |
Girard M, Turgeon S L, Gauthier S F. Interbiopolymer complexing between β-lactoglobulin and low- and high-methylated pectin measured by potentiometric titration and ultrafiltration[J]. Food Hydrocolloids, 2002, 16(6): 585-591. DOI:10.1016/S0268-005X(02)00020-6 |
| [18] |
Klein M, Aserin A, Svitov I, et al. Enhanced stabilization of cloudy emulsions with gum Arabic and whey protein isolate[J]. Colloids and Surfaces B: Biointerfaces, 2010, 77(1): 75-81. DOI:10.1016/j.colsurfb.2010.01.008 |
| [19] |
Han N S, Woi P M, Basri M, et al. Characterization of structural stability of palm oil esters-based nanocosmeceuticals loaded with tocotrienol[J]. Journal of Nanobiotechnology, 2013. DOI:10.1186/1477-3155-11-27 |
| [20] |
Gonçalves N D, Grosso C R F, Rabelo R S, et al. Comparison of microparticles produced with combinations of gelatin, chitosan and gum Arabic[J]. Carbohydrate Polymers, 2018, 196: 427-432. DOI:10.1016/j.carbpol.2018.05.027 |
| [21] |
Klassen D R, Elmer C M, Nickerson M T. Associative phase separation involving canola protein isolate with both sulphated and carboxylated polysaccharides[J]. Food Chemistry, 2011, 126(3): 1094-1101. DOI:10.1016/j.foodchem.2010.11.138 |
| [22] |
Zhao Y, Khalid N, Shu G, et al. Complex coacervates from gelatin and octenyl succinic anhydride modified kudzu starch: Insights of formulation and characterization[J]. Food Hydrocolloids, 2019, 86: 70-77. DOI:10.1016/j.foodhyd.2018.01.040 |
| [23] |
Sow L C, Toh N Z Y, Wong C W, et al. Combination of sodium alginate with tilapia fish gelatin for improved texture properties and nanostructure modification[J]. Food Hydrocolloids, 2019, 94: 459-467. DOI:10.1016/j.foodhyd.2019.03.041 |
| [24] |
Lam S, Velikov K P, Velev O D. Pickering stabilization of foams and emulsions with particles of biological origin[J]. Current Opinion in Colloid & Interface Science, 2014, 19(5): 490-500. |
| [25] |
Fioramonti S A, Martinez M J, Pilosof A M R, et al. Multilayer emulsions as a strategy for linseed oil microencapsulation: Effect of pH and alginate concentration[J]. Food Hydrocolloids, 2015, 43: 8-17. DOI:10.1016/j.foodhyd.2014.04.026 |
| [26] |
Lamprecht A, Schäfer U F, Lehr C M. Influences of process parameters on preparation of microparticle used as a carrier system for O-3 unsaturated fatty acid ethyl esters used in supplementary nutrition[J]. Journal of Microencapsulation, 2001, 18(3): 347-357. DOI:10.1080/02652040010000433 |
| [27] |
Butstraen C, Salaün F. Preparation of microcapsules by complex coacervation of gum Arabic and chitosan[J]. Carbohydrate Polymers, 2014, 99: 608-616. DOI:10.1016/j.carbpol.2013.09.006 |
| [28] |
McClements D J. Theoretical analysis of factors affecting the formation and stability of multilayered colloidal dispersions[J]. Langmuir, 2005, 21(21): 9777-9785. DOI:10.1021/la0512603 |
| [29] |
Niu F, Zhou J, Niu D, et al. Synergistic effects of ovalbumin/gum Arabic complexes on the stability of emulsions exposed to environmental stress[J]. Food Hydrocolloids, 2015, 47: 14-20. DOI:10.1016/j.foodhyd.2015.01.002 |
| [30] |
Razzak M A, Kim M, Chung D. Elucidation of aqueous interactions between fish gelatin and sodium alginate[J]. Carbohydrate Polymers, 2016, 148: 181-188. DOI:10.1016/j.carbpol.2016.04.035 |
| [31] |
Ding M, Zhang T, Zhang H, et al. Gelatin-stabilized traditional emulsions: Emulsion forms, droplets, and storage stability[J]. Food Science and Human Wellness, 2020. DOI:10.1016/j.fshw.2020.04.007 |
| [32] |
Gu Y S, Decker E A, McClements D J. Influence of pH and ι-carrageenan concentration on physicochemical properties and stability of β-lactoglobulin-stabilized oil-in-water emulsions[J]. Journal of Agricultural and Food Chemistry, 2004, 52(11): 3626-3632. DOI:10.1021/jf0352834 |
 2021, Vol. 38
2021, Vol. 38






