2. 洛阳师范学院化学化工学院, 河南 洛阳 471934
2. School of Chemistry and Chemical Engineering, Luoyang Normal University, Henan Luoyang 471934, China
乙醇被广泛用作汽油添加剂、消毒剂、基本化工原料等;然而,我国的乙醇主要依靠粮食发酵制得,存在产量小、周期长、提纯成本高等问题[1]。我国煤炭资源丰富,由煤炭经合成气制乙醇备受关注,且由合成气经酯制乙醇已经示范运行。然而,该技术路线需分4步实现:以工业级一氧化碳和氢气混合形成的合成气为原料合成甲醇;甲醇脱水制备二甲醚;二甲醚与一氧化碳和氢气的羰化反应制取醋酸甲酯;醋酸甲酯纯化后进行加氢,产物纯化后得到乙醇;该过程存在成本高、工艺繁琐、产率较低等问题。近年来,由合成气直接制乙醇逐渐引起研究者的关注,然而该过程的工业化过程仍然是一个挑战[2]。鉴于金属铜和钴之间的协同催化作用,Cu-Co基催化剂被认为是合成乙醇最具前景的催化剂之一[3]。经过数十年的研究,研究者们普遍认为Cu-Co基催化剂催化合成乙醇的原理为:活性组分Co上发生CO的解离吸附和H2的吸附而生成烷基链,是烃类形成的活性位;活性组分Cu上发生CO的非解离吸附,是醇类形成的活性位;最终,Co活性位上的烷基链与Cu活性位上非解离吸附的CO偶联而生成乙醇等醇类[4]。可见,Cu-Co的协同作用是核心,于是制备紧密接触的Cu-Co纳米双金属是此类催化剂的关键。
钙钛矿型复合氧化物(PTO)可以使铜钴离子均匀分散于钙钛矿结构的晶格中,如形成La0.95Ce0.05Co0.7Cu0.3O3;还原后铜和钴也将均匀分散(均匀混合),易产生相互作用或者形成铜钴合金,有利于Cu-Co协同催化作用的发挥[5]。但钙钛矿复合氧化物的比表面积低,还原过程中,金属铜和金属钴易发生团聚而生成铜纳米颗粒和钴纳米颗粒。大比表面积的ZrO2作为载体,为钙钛矿型氧化物在其表面负载提供了有利条件。我们前期以LaCo0.7Cu0.3O3/ZrO2为催化剂前驱体,制备了ZrO2担载的Cu-Co双金属催化剂,其乙醇选择性大约为50%左右,催化剂还存在着烧结和积碳等问题。
由于CeO2和Co之间的相互作用能够提高Co的分散度,从而促进催化剂表面CO的解离吸附和H2的吸附[6];同时CeO2本身存在简单的氧化还原循环。因此,铈不仅能降低活性金属纳米粒子的烧结程度,而且能借助氧空位消除反应积碳[7-8]。我们之前的工作中[9-11],制备了一系列La1-xCexCo0.7 Cu0.3O3/ZrO2(x=0,0.05,0.15)复合氧化物,还原后得到了一系列Cu-Co双金属催化剂;利用固定床反应器研究了La/Ce比对该催化剂催化性能的影响;结果表明,La0.95Ce0.05Co0.7Cu0.3O3具有最佳的低碳醇合成性能。
本研究进一步采用柠檬酸络合辅助的等体积浸渍法制备了钙钛矿型复合氧化物x% La0.95Ce0.05 Co0.7Cu0.3O3担载于ZrO2表面的催化剂前驱体,还原过程中,Cu和Co间的相互作用有利于形成铜钴合金,助剂镧、铈氧化物的协同作用能够进一步提高催化剂的抗积碳、抗烧结能力,从而优化催化剂性能。本研究主要考察钙钛矿复合氧化物的负载量以及反应温度、空速和压力等对CO转化率及乙醇选择性的影响。所制备的催化剂与之前的催化剂相比,CO转化率提高了5%,乙醇选择性大约为60%左右。
1 实验部分 1.1 催化剂前驱体的制备采用表面活性剂辅助的软模板法制备氧化锆载体。具体步骤如下:在搅拌的条件下,将氨水和一定浓度的硝酸锆同时滴入PEG4000(聚乙二醇)的乙醇溶液中,保持pH值为10(±0.5)。滴加完毕后,在室温下搅拌2 h。向上述溶液中加入一定量无水乙醇,70 ℃搅拌3 h后,老化24 h,得到白色沉淀。沉淀物经过抽滤、洗涤和冷冻干燥后,于600 ℃焙烧3 h,得到ZrO2载体。
采用柠檬酸络合辅助的等体积浸渍法制备x%La0.95Ce0.05Co0.7Cu0.3O3/ZrO2(x=20、30和40)催化剂前驱体。首先配制n(硝酸镧):n(硝酸铈):n(硝酸钴):n(硝酸铜):n(柠檬酸):n(乙二醇)=0.95:0.05:0.70:0.30:2.40:0.40的混合溶液,然后将上述溶液等体积浸渍到一定量的ZrO2载体上。所得样品静置24 h后,放置于恒温干燥箱中80 ℃干燥6 h,随后升温至120 ℃干燥12 h;最终样品在350 ℃和650 ℃下分别煅烧2 h和5 h,得到x%La0.95Ce0.05Co0.7Cu0.3O3/ZrO2。
1.2 催化剂的性能测试在连续进料的固定床反应器上测试催化剂的催化性能,利用气相色谱进行产物分析。测试步骤如下:称取500 mg颗粒大小为40~60目的催化剂前驱体,将其装入反应器中;然后以20 mL·min-1的流速向反应器中通入H2,使催化剂前驱体在600 ℃下原位还原3 h;待反应器冷却至室温后,向反应器中通入合成气,并将反应压力调至4 MPa;合成气组成为V(H2):V(CO):V(N2)=8:4:1,空速为3 000~6 000 mL·(g·h)-1,反应温度为270~300 ℃。
1.3 催化剂的表征样品的N2物理吸附-脱附测试是在Quantachrome Quadra Sorb SI型孔径分布测试仪上进行的,测试温度为-196 ℃。测试前,样品在300 ℃下真空脱气4 h以除去样品表面吸附的杂质。
XRD测试在Bruker D8-Focus型Cu靶X射线衍射仪上进行。Cu_Kα(λ=0.15406 nm)射线作为辐射源,管电压40 kV,管电流为200 mA,扫描速度为5(°)·min-1,扫描范围为20°~80°。
程序升温还原(TPR)测试是在天津大学北洋化工实验设备公司研制的吸附-脱附-还原-反应多功能实验装置上进行的。步骤如下:称取50 mg样品置于石英管中,通入体积比为5%的H2/Ar混合气吹扫,流量设定为30 mL·min-1。从室温以10 ℃·min-1的升温速率升至900 ℃,通过TCD检测器来检测氢的变化。
场发射透射电子显微镜(TEM)在型号为JEOL JEM-2100F的电子显微镜上获得。测试样品经过研磨、超声后分散于乙醇中,并将得到的悬浊液置于铜网上,待样品干燥之后进行测试。线扫描(EDS)也在JEOL JEM-2100F电子显微镜上进行。
2 结果与讨论 2.1 催化剂的XRD表征图 1a)为催化剂前驱体及其还原后的XRD图。与ZrO2的XRD图相比,La0.95Ce0.05Co0.7Cu0.3O3/ZrO2在2θ=23.2°、32.9°、47.3°和58.6°出现了新的衍射峰;新的衍射峰与La0.95Ce0.05Co0.7Cu0.3O3的衍射峰相近,说明La0.95Ce0.05Co0.7Cu0.3O3/ZrO2中形成了良好的钙钛矿结构。还原后钙钛矿的衍射峰消失,说明钙钛矿结构被破坏[12]。同时,煅烧后的前驱体和还原后的催化剂与ZrO2的衍射峰相比,前驱体和催化剂中ZrO2的衍射峰几乎相同,说明在煅烧和还原过程中ZrO2一直处于稳定状态。
图 1b)为30% La0.95Ce0.05Co0.7Cu0.3O3/ZrO2和30% LaCo0.7Cu0.3O3/ZrO2在32°~34°范围内的XRD图。与LaCo0.7Cu0.3O3/ZrO2中钙钛矿的主衍射峰相比,La0.95Ce0.05Co0.7Cu0.3O3/ZrO2中钙钛矿的主衍射峰向高角度偏移;这是由于Ce4+的离子半径(0.092 nm)比La3+的离子半径(0.106 nm)小,Ce4+部分取代La3+之后,减小了LaCo0.7Cu0.3O3的晶面间距,使得2θ角向高角度偏移[12-13];反之,衍射峰的偏移也证明了Ce4+进入到LaCo0.7Cu0.3O3钙钛矿的晶格,即形成了La0.95Ce0.05Co0.7Cu0.3O3物相。
30% La0.95Ce0.05Co0.7Cu0.3O3/ZrO2前驱体在600 ℃还原后,得到催化剂。图 1c)显示了该催化剂在40°~45°范围内的XRD图。在Cu[111](43.3°)与Co[111](44.2°)之间,可以观测到Cu-Co合金的衍射峰,而且未检测到铜单质或钴单质的衍射峰。说明La0.95Ce0.05Co0.7Cu0.3O3/ZrO2催化剂前驱体经还原后,Cu-Co双金属以Cu-Co合金的形式存在,且高度分散在载体表面[5]。
2.2 催化剂的BET表征图 2是ZrO2和x% La0.95Ce0.05Co0.7Cu0.3O3/ZrO2催化剂前驱体的N2物理吸附-脱附等温线与BJH孔径分布曲线。

|
| 图 2 a) N2吸附-脱附等温线与b)BJH孔径分布曲线 Fig.2 a)N2 absorption-desorption isotherms and b)BJH pore size distribution |
| |
由图 2可知,所有样品的吸附-脱附等温线为Ⅳ型吸附-脱附等温线,且伴随有H3型滞后环[14]。这说明样品中存在一定量的介孔,这与BJH孔径分布曲线表征结果一致。由图 2a)可知,x% La0.95Ce0.05 Co0.7Cu0.3O3/ZrO2前驱体的滞后环位于0.7~1.0处,表明该催化剂的孔径分布相对较窄[15]。由图 2b)可知,ZrO2载体、x%La0.95Ce0.05Co0.7Cu0.3O3/ZrO2催化剂前驱体均为介孔结构,且孔尺寸集中分布区间为5~30 nm。
从表 1中可以看出,未负载的ZrO2的比表面积是79 m2·g-1;随着La0.95Ce0.05Co0.7Cu0.3O3负载量的增加,前驱体的比表面积和孔体积逐渐减小;这是由于La0.95Ce0.05Co0.7Cu0.3O3对ZrO2堆积孔的堵塞,导致比表面积和孔体积减小。比表面积和孔径逐渐减小,也说明La0.95Ce0.05Co0.7Cu0.3O3负载到了ZrO2载体上。
| Sample | SBET/(m2·g-1) | Pore size/nm | VBJH/(cm3·g-1) |
| ZrO2 | 79.0 | 16.2 | 0.32 |
| x=20 | 67.9 | 10.9 | 0.19 |
| x=30 | 60.2 | 11.2 | 0.17 |
| x=40 | 54.5 | 11.5 | 0.16 |
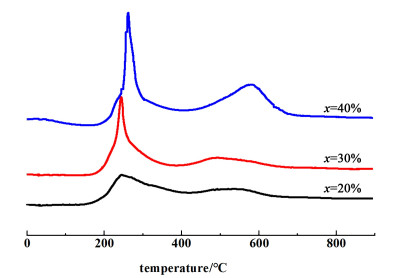
图 3为x%La0.95Ce0.05Co0.7Cu0.3O3/ZrO2催化剂前驱体的程序升温还原曲线。
|
| 图 3 x%La0.95Ce0.05Co0.7Cu0.3O3/ZrO2的TPR图 Fig.3 TPR profiles of x% La0.95Ce0.05Co0.7Cu0.3O3/ZrO2 |
| |
从图 3中可以看出,不同负载量的催化剂均出现2个还原峰。300 ℃左右的低温还原峰对应Cu2+→Cu0和部分Co3+→Co2+的还原,550 ℃左右的还原峰对应Co2+→Co0和部分Co3+→Co2+的还原[16-17]。40%La0.95Ce0.05Co0.7Cu0.3O3/ZrO2前驱体的2个还原峰较x=20%和30%的催化剂前驱体整体向高温方向偏移,这主要是由于随着负载量的升高,钙钛矿颗粒烧结长大[18];而归属于Co的还原峰向高温方向移动且还原峰面积的比例增大,说明在40%样品中,低温还原的Cu纳米粒子对钴离子的促进作用较小,也就是说该样品中Cu和Co之间的协同作用较弱[2]。30%的样品Co的高温还原峰温度最低且还原峰面积较小,说明在该样品中,Cu对Co的催化还原作用最显著,也就是说该样品中Cu-Co之间的协同作用最强。
2.4 催化剂的TEM表征图 4a)为30%La0.95Ce0.05Cu0.7Co0.3O3/ZrO2催化剂前驱体经H2还原之后的TEM图。图 4b)为30%La0.95Ce0.05Cu0.7Co0.3O3/ZrO2催化剂前驱体经还原-反应后的TEM图。

|
| 图 4 a) 30% La0.95Ce0.05Co0.7Cu0.3O3/ZrO2催化剂前驱体经H2还原之后和b)反应之后的TEM图 Fig.4 a) TEM images of 30% La0.95Ce0.05Co0.7Cu0.3O3/ZrO2 catalyst precursor after H2 reduction and b)reaction |
| |
Cu[111]和Co[111]晶面间距分别为0.208和0.205 nm,样品中存在晶面间距为0.207 nm的晶格条纹,归属于Cu-Co合金的[111]晶面[12];0.178 nm的晶格间距是属于Cu-Co合金的[200]晶面;围绕在Cu-Co合金周围的,0.283 nm的晶格间距是属于La2O3的[400]晶面;此外,0.262 nm的晶格间距是属于Zr-Ce-O固溶体的[002]晶面,表明Ce4+离子进入了ZrO2晶格;其余的晶格间距属于ZrO2晶面。说明30%La0.95Ce0.05Cu0.7Co0.3O3/ZrO2催化剂前驱体经还原后形成了La-Ce-O掺杂的ZrO2担载的Cu-Co合金催化剂,与XRD的结果一致。
从图 4b)中仍然能看到0.207 nm的晶格间距,归属于Cu-Co的合金[111]晶面;0.286 nm的晶格间距是属于La2O2CO3的[101]晶面,La2O2CO3是由La2O3和CO2反应形成的,La2O2CO3可以进一步与积碳反应生成La2O3和CO2,La2O2CO3的生成和消耗可以达到消除积碳的目的;0.217 nm的晶格间距是属于Co2C的[020]晶面,Co2C能够吸附CO,使CO与CHx结合从而形成含氧前驱体。此外,0.188 nm的晶格间距是属于Zr-Ce-O固溶体的[220]晶面;其余的晶格间距是属于ZrO2的晶面。这说明反应后催化剂的活性组分仍然为Cu-Co合金,催化剂载体在整个过程中也是稳定存在的。稳定的催化剂结构有利于催化剂稳定性和活性的发挥。
从图 5a)可以看出,还原后的LaCo0.7Cu0.3O3/ZrO2催化剂中,元素Cu和Co的变化趋势是同步的,各个粒子团簇间存在明显的间隔,说明其还原之后形成了Cu-Co合金;反应后粒子团簇间的间距消失[见图 5b)],Cu-Co合金纳米粒子、镧的氧化物粒子团簇出现了明显的聚集,说明30% LaCo0.7Cu0.3O3/ZrO2反应后出现了严重的烧结。而图 5c)显示30%La0.95Ce0.05Co0.7Cu0.3O3/ZrO2在反应后,粒子团簇仍然存在一定的间距,Cu、Co具有相同的变化趋势;说明在反应过程中,还原后形成的Cu-Co合金和镧、铈的氧化物粒子团簇能够保持稳定状态;这说明催化剂中Ce的添加,可以明显改善催化剂的抗烧结性能。

|
| 图 5 a) 30%LaCo0.7Cu0.3O3/ZrO2还原后、b)反应后的EDS线扫图;c)30%La0.95Ce0.05Co0.7Cu0.3O3/ZrO2反应后的EDS线扫描图 Fig.5 EDS line scanning profiles of a) 30%LaCo0.7Cu0.3O3/ZrO2 after reduction and b) after reaction; c)30%La0.95Ce0.05Co0.7Cu0.3O3/ZrO2 after reaction |
| |
由图 6a)可以看出,随着催化剂中La0.95Ce0.05 Co0.7Cu0.3O3负载量的增加,催化剂的活性呈现逐渐增加的趋势;这主要是因为La0.95Ce0.05Co0.7Cu0.3O3负载量较高时,催化剂中的活性组分较多,为合成气吸附提供更多的活性位点。图 6c)~图 6d)为不同负载量催化剂的烃类选择性和醇类选择性,当负载量由20%增加到30%时,烃类的选择性降低,醇类的选择性升高。当负载量由30%进一步提高到40%时,烃类的选择性升高,导致总醇的选择性降低[图 6d)]。综合CO转化率和醇选择性可知,当负载量为30%时,Cu-Co之间的协同作用最显著,催化剂具有较好的催化性能。结合TPR的结果可知,在30% La0.95Ce0.05Co0.7 Cu0.3O3/ZrO2催化剂前驱体中,Cu和Co之间的协同作用最强,因而其醇类选择性最高;同时该催化剂良好的抗积碳和抗烧结性能,也是该催化剂催化性能最优的原因之一。

|
| 图 6 固定床中不同负载量下La0.95Ce0.05Co0.7Cu0.3O3/ZrO2催化CO加氢的性能 Fig.6 Catalytic performance of CO hydrogenation over La0.95Ce0.05Co0.7Cu0.3O3/ZrO2 with different loading amounts in fixed-bed reactor |
| |
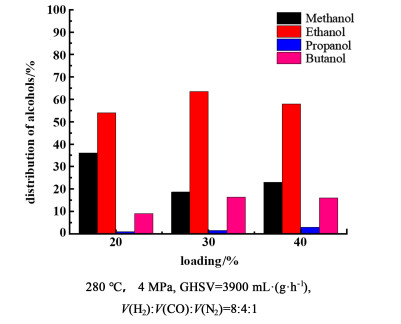
图 7为不同负载量下反应温度为280 ℃时醇的分布数据。
|
| 图 7 固定床中,不同负载量下,La0.95Ce0.05Co0.7Cu0.3O3/ ZrO2催化CO加氢的醇分布 Fig.7 The distribution of alcohols in catalyzing CO hydrogenation over La0.95Ce0.05Co0.7Cu0.3O3/ZrO2 with different loading amounts in fixed-bed reactor |
| |
从图 7中可以看出,30% La0.95Ce0.05Co0.7Cu0.3O3/ZrO2催化剂表现出了较好的低碳醇选择性,这主要是因为催化剂被还原后形成了Cu-Co合金并在ZrO2表面高度分散;同时,在该催化剂中铜和钴之间的协同作用最强[19]。
2.6 空速对催化剂催化性能的影响图 8a)可以看出在T=280 ℃,空速为4 000 mL·(g·h)-1时,催化剂具有较好的催化性能。随着空速的不断增加,CO的转化率持续下降,主要的原因在于空速增加后,CO与H2在催化剂表面的停留时间减少,导致CO的转化率降低[2]。图 8b)为不同空速条件下的醇分布。随着空速的增加,合成气与催化剂活性位点的接触时间变短,链增长作用受到抑制[20],总醇的选择性逐渐降低。综合图 8a)和图 8b)可知,当空速为4 000 mL·(g·h)-1时,催化剂具有较好的催化性能。综上所述,当T=280 ℃,压力为4 MPa,GHSV=4000 mL·(g·h)-1,V(H2):V(CO):V(N2)=8:4:1时,催化剂的催化性能较优,CO转化率为8%,收率为60%。

|
| 图 8 固定床中不同空速条件下La0.95Ce0.05Co0.7Cu0.3O3/ ZrO2催化CO加氢的性能 Fig.8 Catalytic performance of CO hydrogenation over La0.95Ce0.05Co0.7Cu0.3O3/ZrO2 at different GHSV in fixed-bed reactor |
| |
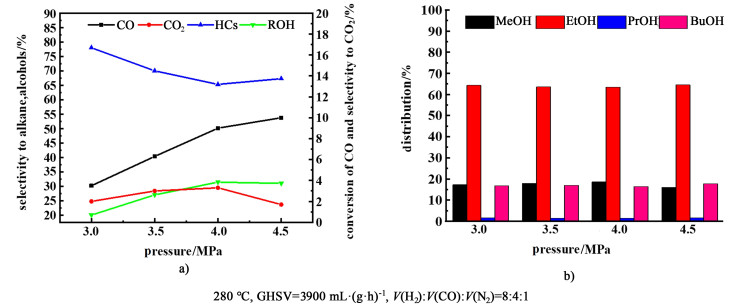
图 9a)可以看出在T=280 ℃,空速为3 900 mL·(g·h)-1时,随着压力的增加,CO的转化率逐渐升高,主要的原因在于合成气直接制乙醇是体积减小的反应,当压力增加后,有利于正反应的进行,导致CO的转化率升高。当反应压力达到4.5 MPa时,催化性能的提升不是很明显,这可能与压力对反应物吸附和生成物脱附的复杂影响有关[21]。图 9b)为不同压力下的醇分布。随着压力的增加,醇分布没有发生明显的变化。综合图 9a)和图 9b)可知,当压力为4 MPa时,催化剂具有较好的性能,CO转化率为9%,收率为63.5%。
|
| 图 9 固定床中不同压力条件下La0.95Ce0.05Co0.7Cu0.3O3/ZrO2催化CO加氢的性能 Fig.9 Catalytic performance of CO hydrogenation over La0.95Ce0.05Co0.7Cu0.3O3/ZrO2 at different pressure in fixed-bed reactor |
| |
采用柠檬酸络合辅助的等体积浸渍法制备了具有La0.95Ce0.05Co0.7Cu0.3O3/ZrO2钙钛矿结构的催化剂前驱体,经还原后形成了La-Ce-O掺杂的ZrO2担载的Cu-Co双金属催化剂。La0.95Ce0.05Co0.7 Cu0.3O3使Cu和Co成比例的均匀分散在大分子中,还原后活性组分Cu-Co均匀分散在大比表面积ZrO2的表面,且具备抗积碳、抗烧结性能。综合考虑CO转化率及低碳醇选择性,催化剂在固定床中,温度为280 ℃,压力为4 MPa,空速为3 900 mL·(g·h)-1,V(H2):V(CO):V(N2)=8:4:1时,展现了最优的催化性能,CO转化率为9%,总醇的选择性为29.7%,总醇中乙醇的选择性为63.5%。
| [1] |
Pan X, Fan Z, Chen W, et al. Enhanced ethanol production inside carbon-nanotube reactors containing catalytic particles[J]. Nature Materials, 2007, 6(7): 507-511. DOI:10.1038/nmat1916 |
| [2] |
Fang Y, Liu Y, Zhang L. LaFeO3- supported nano Co-Cu catalysts for higher alcohol synthesis from syngas[J]. Applied Catalysis A:General, 2011, 397(1/2): 183-191. |
| [3] |
Wang P, Bai Y, Xiao H, et al. Effect of the dimensions of carbon nanotube channels on copper-cobalt-cerium catalysts for higher alcohols synthesis[J]. Catalysis Communications, 2016, 75: 92-97. DOI:10.1016/j.catcom.2015.12.012 |
| [4] |
Xiao K, Bao Z, Qi X, et al. Advances in bifunctional catalysis for higher alcohol synthesis from syngas[J]. Chinese Journal of Catalysis, 2013, 34(1): 116-129. DOI:10.1016/S1872-2067(11)60496-8 |
| [5] |
Liu G, Niu T, Cao A, et al. The deactivation of Cu-Co alloy nanoparticles supported on ZrO2 for higher alcohols synthesis from syngas[J]. Fuel, 2016, 176: 1-10. DOI:10.1016/j.fuel.2016.02.057 |
| [6] |
He L, Teng B, Zhang Y, et al. Development of composited rare-earth promoted cobalt-based Fischer-Tropsch synthesis catalysts with high activity and selectivity[J]. Applied Catalysis A:General, 2015, 505: 276-283. DOI:10.1016/j.apcata.2015.07.041 |
| [7] |
Nematollahi B, Rezaei M, Lay E N. Synthesis of nanocrystalline CeO2 with high surface area by the Taguchi method and its application in methanation[J]. Chemical Engineering & Technology, 2015, 38(2): 265-273. |
| [8] |
Cwele T, Mahadevaiah N, Singh S, et al. Effect of Cu additives on the performance of a cobalt substituted ceria (Ce0.90Co0.10O2-δ) catalyst in total and preferential CO oxidation[J]. Applied Catalysis B:Environmental, 2016, 182: 1-14. DOI:10.1016/j.apcatb.2015.08.043 |
| [9] |
Liu G, Geng Y, Pan D, et al. Bi-metal Cu-Co from LaCo1-xCuxO3 perovskite supported on zirconia for the synthesis of higher alcohols[J]. Fuel Processing Technology, 2014, 128: 289-296. DOI:10.1016/j.fuproc.2014.07.010 |
| [10] |
Tien-Thao N, Zahedi-Niaki M H, Alamdari H, et al. Co-Cu metal alloy from LaCo1-xCuxO3 Perovskites as catalysts for higher alcohol synthesis from syngas[J]. International Journal of Chemical Reactor Engineering, 2007, 5(1): 1-12. |
| [11] |
Tien-Thao N, Alamdari H, Zahedi-Niaki M H, et al. LaCo1-xCuxO3-δ perovskite catalysts for higher alcohol synthesis[J]. Applied Catalysis A:General, 2006, 311: 204-212. DOI:10.1016/j.apcata.2006.06.029 |
| [12] |
Liu G, Pan D, Niu T, et al. Nanoparticles of Cu-Co alloy supported on high surface area LaFeO3-Preparation and catalytic performance for higher alcohol synthesis from syngas[J]. RSC Advances, 2015, 5(4): 31637-31647. |
| [13] |
Kirchnerova J, Alifanti M, Delmon B. Evidence of phase cooperation in the LaCoO3-CeO2-Co3O4 catalytic system in relation to activity in methane combustion[J]. Applied Catalysis A:General, 2002, 231(1/2): 65-80. |
| [14] |
Yang E, Kim N Y, Noh Y S, et al. Steam CO2 reforming of methane over La1-xCexNiO3 perovskite catalysts[J]. International Journal of Hydrogen Energy, 2015, 40(35): 11831-11839. DOI:10.1016/j.ijhydene.2015.06.021 |
| [15] |
Leofanti G, Padovan M, Tozzola G, et al. Surface area and pore texture of catalysts[J]. Catalysis Today, 1998, 41(1/2/3): 207-219. |
| [16] |
Jiao Y, Zhang J, Du Y, et al. Steam reforming of hydrocarbon fuels over M (Fe, Co, Ni, Cu, Zn)-Ce bimetal catalysts supported on Al2O3[J]. International Journal of Hydrogen Energy, 2016, 41(24): 10473-10482. DOI:10.1016/j.ijhydene.2015.09.151 |
| [17] |
Toniolo F S, Magalhães R N S H, Perez C A C, et al. Structural investigation of LaCoO3 and LaCoCuO3 perovskite-type oxides and the effect of Cu on coke deposition in the partial oxidation of methane[J]. Applied Catalysis B:Environmental, 2012, 117/118: 156-166. DOI:10.1016/j.apcatb.2012.01.009 |
| [18] |
Lisi L, Bagnasco G, Ciambelli P, et al. Perovskite-Type oxides:II. Redox properties of LaMn1-xCuxO3 and LaCo1-xCuxO3 and methane catalytic combustion[J]. Journal of Solid State Chemistry, 1999, 146(1): 176-183. DOI:10.1006/jssc.1999.8327 |
| [19] |
Koranne M M, Goodwin J G, Marcelin G. Characterization of silica- and alumina-supported vanadia catalysts using temperature programmed reduction[J]. Journal of Catalysis, 1994, 148(1): 369-377. |
| [20] |
Song Z, Shi X, Ning H, et al. Loading clusters composed of nanoparticles on ZrO2 support via a perovskite-type oxide of La0.95 Ce0.05 Co0.7 Cu0.3 O3 for ethanol synthesis from syngas and its structure variation with reaction time[J]. Applied Surface Science, 2017, 405: 1-12. DOI:10.1016/j.apsusc.2017.02.003 |
| [21] |
Guo S, Li S, Zhong H, et al. Mixed oxides confined and tailored cobalt nanocatalyst for direct ethanol synthesis from syngas:A catalyst designing by using perovskite-type oxide as the precursor[J]. Industrial & Engineering Chemistry Research, 2018, 57(6): 2404-2415. |
 2020, Vol. 37
2020, Vol. 37






