2. 沈阳化工大学化学工程学院, 沈阳 110142
2. Shenyang University of Chemical Technology, Shenyang 110142, China
随着全球工业化及经济的快速发展,人们对能源的需求量越来越大,能源短缺和环境污染已经成为当今科技发展亟待解决的2个问题[1]。而当今世界上主要的传统能源是化石燃料,化石燃料是不可再生、濒临枯竭且燃烧放出大量温室气体的能源,因此全球科学家开始重点关注清洁、高效、无污染的新能源的开发[2-3]。
在新能源的开发中,氢能以相对廉价、运输方便、燃烧后无污染且放热量高等优点一直备受研究者的关注。燃料电池是用氢的最好方式,因此开发低能耗、高效的制氢方法已成为国内外众多科学家重点研究的问题[4-5]。
近年来,研究制氢的方法很多,如煤制氢、石油制氢、天然气制氢、水制氢和生物质制氢等。虽然在生物质能利用方面取得了较好的成果,但在生物柴油的生产过程中,当制备10 t生物柴油时,便有1 t丙三醇副产物,这些副产物给生物柴油生产企业增加了额外的负担, 如何将这些副产物转化为可利用的能源已引起了学者的关注和重视。国外Kiriakos等[6]研究了以Al2O3为载体,Ni、Co和Cu为活性组分的催化剂用于丙三醇水蒸气重整制氢的效果。Iriondo等[7]研究了Ce、Mg、Zr和La等助剂对Ni系催化剂活性的影响。郭瓦力等[8]研究了用于丙三醇水蒸气重整制氢的Pt、Co、Cu和Ni金属催化剂及其制氢过程。本研究以郭瓦力的研究为基础,通过添加金属氧化物来提高Pt系催化剂的抗积碳性、稳定性,进一步优化Pt系催化剂对丙三醇水蒸气重整制氢的工艺的影响。
丙三醇水重整制氢工艺与其他制氢工艺相比有以下优点:产氢量高,反应条件温和,所需能耗低,但丙三醇水重整制氢工艺是一个较为复杂的反应过程,反应中会有大量副产物的产生。因此,如何提高丙三醇水重整制氢过程中氢产率的含量成为本工艺解决的关键问题。目前,丙三醇水重整制氢工艺中多采用单组分金属催化剂,催化活性较好,但随着反应时间的延长,催化剂活性、稳定性下降,积碳严重[9-10]。
本研究以研究丙三醇水重整制氢工艺为基础,重点研究制氢工艺中的催化剂:以Al2O3为载体,采用浸渍法制备了Cu、Co、Ni和Pt为活性组分的催化剂,比较各活性成分的效果。并用金属氧化物对已经制备的Pt/Al2O催化剂进行改性,在管式反应器中对催化剂的活性、稳定性及抗积碳性进行评价,旨在进一步完善丙三醇水重整制氢技术,为丙三醇水重整制氢工艺的发展提供参考和借鉴。
1 实验部分 1.1 实验原料及仪器主要原料:丙三醇:分析纯AR,上海国药集团化学试剂有限公司;蒸馏水;氮气:99.99%,沈阳洪升气体厂;硝酸钴、硝酸铜、硝酸镍、硝酸铂、硝酸铈、硝酸锆和硝酸锂:分析纯AR,上海国药集团化学试剂有限公司。
主要仪器设备:制氢装置(自行开发),平流泵(LB-05C)、管式反应器(Φ17 mm×2.5 mm)、质量流量计(D08-1D/ZM)、温控仪(SR53)、湿式流量计(LML-1);气相色谱仪(SP-2100,Agilent 6890N)等。
1.2 催化剂的制备N/Al2O3 (N-代表活性组分)催化剂的制备是以Al2O3为载体,等体积浸渍法为手段。具体制备过程以Pt/Al2O3催化剂为例:在600 ℃下将Al2O3焙烧6 h制得γ-Al2O3,将一定质量γ-Al2O3浸渍在硝酸铂溶液中,浸渍12 h后,将载体放入鼓风干燥箱进行干燥,干燥后再在马弗炉中700 ℃焙烧7 h,得到Pt/Al2O3催化剂前驱体[11-12]。对所制备的催化剂前驱体用氢氮混合气进行原位还原。
掺杂氧化物催化剂的制备:以Pt-CeO2/Al2O3为例,具体制备过程如下:以Al2O3为载体,等体积分步浸渍法为手段。在600 ℃将Al2O3焙烧6 h制得γ-Al2O3,将一定质量γ-Al2O3浸渍在硝酸铈溶液中,浸渍12 h后,再浸渍到硝酸铂溶液中,浸渍12 h后,将载体放入鼓风干燥箱进行干燥,干燥后再在马弗炉中700 ℃焙烧7 h,得到Pt-CeO2/Al2O3催化剂前驱体。对所制备的催化剂前驱体用氢氮混合气进行原位还原。
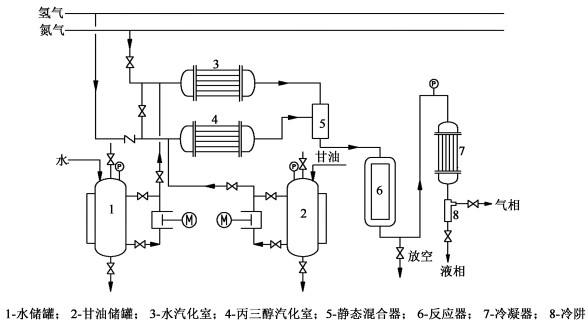
1.3 催化剂性能测试如图 1所示,将一定量的丙三醇(2)和水(1)分别由平流泵计量并输送到丙三醇汽化室(4)和水汽化室(3),在静态混合器(5)中对汽化后的丙三醇和水进行混合,混合后在管式反应器(6)中完成重整制氢反应。后续产物通过冷凝器(7)和冷阱(8)完成气液分离,并利用气相色谱仪对成分进行在线分析。
|
| 图 1 丙三醇水蒸气重整制氢工艺流程 Fig.1 Flow chart of water reforming of glycerol to hydrogen |
| |
气体组成采用SP-2100气相色谱双阀双柱检测,冷凝液组成分析采用Agilent 6890N气相色谱检测,基本测试条件如表 1所示。
| 分析内容 | 固定相 | 检测方式 |
| 气体组成 | GDX-502 | TCD |
| 气体组成 | 5A分子筛 | TCD |
| 冷凝液组成 | SE-54 | FID |
1) n(水)/n(醇):反应器进口处水蒸气物质的量与丙三醇物质的量之比。
2) 丙三醇液空速:单位时间内通过单位体积催化剂的丙三醇体积。
3) 氢产率:丙三醇产生氢气的产量[n(丙三醇)/n(氢气)]。
1.6 催化剂的表征H2-TPR表征,通过Micromeritics公司的AutoChen∏-2920型程序升温氮气还原器于120 ℃下用流速40 mL/min氮气吹扫30 min,然后切换成V(H2)/V(N2)为0.1,流速40 mL/min,降温至100 ℃,平稳基线30 min后以10 ℃/min升温至900 ℃然后降温。
BET表征:在SSA-4300型全自动物理化学吸附仪进行催化剂比表面、孔径、孔容的测定,在300 ℃对催化剂样品进行真空脱气处理4 h,以去除样品已吸附的气体。分析采用N2为吸附质,He为载气,在液氮温度(-196 ℃)下吸附。
催化剂积碳分析:DSC-T300型号索尼数码相机,根据对催化剂反应前后的积碳情况进行分析。
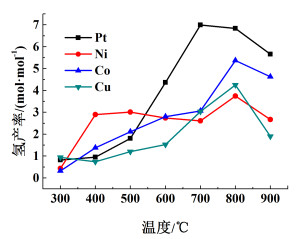
2 实验结果与讨论 2.1 活性组分的确定以N(Pt、Co、Cu和Ni)为活性组分,Al2O3为载体,采用等体积分步浸渍法制备催化剂,在丙三醇流量为0.02 mL/min,水流量为0.08 mL/min,n(水)/n(醇)为16,丙三醇液空速为0.12 h-1,反应温度300~900 ℃条件下,考察不同活性组分对丙三醇水蒸气重整制氢性能的影响,结果见图 2。
|
| 图 2 N/γ-Al2O3催化剂氢产率随温度变化关系图 Fig.2 Relationship between temperature and hydrogen yield of N/γ-Al2O3 catalyst |
| |
由图 2可知:在中温段(500~700 ℃)和高温段(700~900 ℃),氢产率的大小顺序为Pt/Al2O3>Co/ Al2O3>Ni/Al2O3>Cu/Al2O3,当反应温度不高时(300~ 500 ℃),氢产率的大小顺序为Ni/Al2O3>Co/Al2O3>Pt/Al2O3>Cu/Al2O3。因此,对于丙三醇水蒸气重整制氢工艺来说活性组分为Pt(Pt/Al2O3)催化剂更合适。
基于以上,后续的实验以探讨对(Pt/Al2O3)催化剂进行掺杂改性的效果为主。
2.2 金属氧化物掺杂改性的研究在丙三醇流量0.02 mL/min,水流量0.08 mL/min,n(水)/n(醇)为16,丙三醇液空速0.12 h-1,反应温度300~900 ℃条件下,考察CeO2、Li2O和ZrO2助剂掺杂Pt/Al2O3(Pt担载量为0.9%)催化剂对丙三醇水重整制氢性能的影响。本研究通过等体积分步浸渍法制备掺杂改性的Pt系催化剂,并利用BET检测催化剂的比表面积、平均孔半径的大小,利用数码相机观察催化剂的积碳情况。
2.2.1 助剂CeO2担载量的考察不同担载量的Pt-CeO2/Al2O3催化剂对氢产率随温度的影响见图 3。

|
| 图 3 不同担载量的Pt-CeO2/Al2O3催化剂氢产率温度关系曲线图 Fig.3 Relationship between temperature and hydrogen yield of different loading for Pt-CeO2/Al2O3 catalyst |
| |
由图 3可知:当助剂CeO2的担载量为最适宜的3%时,对制氢影响较为显著,在800 ℃时达到最佳催化效果,最大氢产率为3.29。
2.2.2 助剂Li2O担载量的考察不同担载量的Pt-Li2O/Al2O3催化剂对氢产率随温度的影响见图 4。

|
| 图 4 不同担载量的Pt-Li2O/Al2O3催化剂氢产率温度关系曲线图 Fig.4 Relationship between temperature and hydrogen yield of different loading for Pt-Li2O/Al2O3 catalyst |
| |
由图 4可知:助剂Li2O的最适宜担载量为5%,在800 ℃时,5%Li2O/Al2O3催化剂达到最佳催化效果,最大氢产率为4.35。
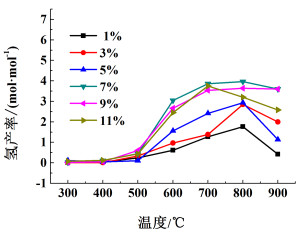
2.2.3 助剂ZrO2担载量的考察不同担载量的Pt-ZrO2/Al2O3催化剂对氢产率随温度的影响见图 5。
|
| 图 5 不同担载量的Pt-ZrO2/Al2O3催化剂氢产率温度关系曲线图 Fig.5 Relationship between temperature and hydrogen yield of different loading for Pt-ZrO2/Al2O3 catalyst |
| |
由图 5可知:助剂ZrO2的最适宜担载量为7%,7%ZrO2/Al2O3在800 ℃时达到最佳催化效果,最大氢产率为3.96。
2.2.4 不同助剂对Pt/Al2O3催化剂的影响分别采用担载量为3%CeO2,担载量为5%Li2O,担载量为7%ZrO2对Pt/Al2O3(Pt担载量为0.9%)催化剂进行改性,并在丙三醇流量0.02 mL/min,水流量0.08 mL/min,n(水)/n(醇)为16,丙三醇液空速0.12 h-1条件下测试对丙三醇水蒸气重整制氢性能的影响,实验结果如图 6所示。

|
| 图 6 Pt系列催化剂氢产率温度曲线图 Fig.6 Relationship between temperature and hydrogen yield of different Pt catalyst |
| |
由图 6可知:助剂Li2O改性的Pt/Al2O3催化剂对丙三醇水重整制氢具有良好的催化活性。丙三醇水重整制氢属于吸热反应,高温有利于反应的进行,但温度过高,易使催化剂积碳,降低催化活性。
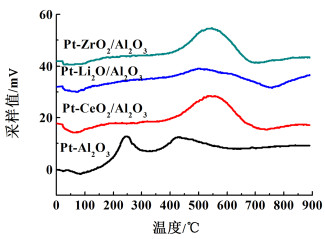
2.3 催化剂的表征为了进一步比较催化剂的催化性能,对Pt/Al2O3、Pt-CeO2/Al2O3(CeO2担载量为3%)、Pt-Li2O /Al2O3(Li2O担载量为5%)和Pt-ZrO2/Al2O3(ZrO2担载量为7%)催化剂进行表征。结果分别列于图 7和表 2。
|
| 图 7 Pt系催化剂TPR谱图 Fig.7 TPR spectrum of Pt catalyst with different auxiliary |
| |
| 物质 | BET比表面积/ (m2·g-1) |
BJH平均孔半径/nm | 总孔容积/ (mL3·g-1) |
| Pt/Al2O3 | 136.037 | 4.77 | 0.368 340 |
| Pt-Li2O/Al2O3 | 135.312 | 6.73 | 0.404 576 |
| Pt-ZrO2/Al2O3 | 127.061 | 4.63 | 0.433 549 |
| Pt-CeO2/Al2O3 | 133.184 | 5.78 | 0.488 908 |
由图 7可知:1) Pt/Al2O3催化剂有2个还原峰,其中峰顶1温度为245 ℃,峰顶2温度为424 ℃;Pt-CeO2/Al2O3改性催化剂的峰顶温度为538 ℃;Pt-Li2O/Al2O3改性催化剂的峰顶温度为501 ℃;Pt-ZrO2/Al2O3改性催化剂的峰顶温度为546 ℃。
2) 改性后催化剂与Pt/Al2O3催化剂相比,还原峰全部向右移动,说明了加入的助剂与原有物相发生反应,因此改变了还原温度。
2.3.2 BET表征由表 2可知:加入助剂会改变Pt/Al2O3催化剂的比表面积、平均孔半径、总孔容积,但助剂Li2O对Pt/Al2O3催化剂的平均孔半径影响最显著,说明比表面积及平均孔半径越大,催化剂的催化效果越优。
2.3.3 铂系列催化剂表面积碳分析各催化剂使用前后的对比图片见图 8~图 11,并列于表 3。

|
| 图 8 Pt/Al2O3催化剂使用前后对比 Fig.8 Comparison of unused and used Pt/Al2O3 catalyst |
| |

|
| 图 9 Pt-ZrO2/Al2O3催化剂使用前后对比 Fig.9 Comparison of unused and used Pt-ZrO2/Al2O3 catalyst |
| |

|
| 图 10 Pt-Li2O/Al2O3催化剂使用前后对比 Fig.10 Comparison of unused and used Pt-Li2O/Al2O3 catalyst |
| |

|
| 图 11 Pt-CeO2/Al2O3催化剂使用前后对比 Fig.11 Comparison of unused and used Pt-CeO2/Al2O3 catalyst |
| |
| 催化剂 | 使用前颜色 | 使用后颜色 | 积碳程度 |
| Pt/Al2O3 | 淡灰色 | 灰黑色 | 少量积碳 |
| Pt-ZrO2/Al2O3 | 淡灰色 | 黑色 | 大量积碳 |
| Pt-Li2O/Al2O3 | 灰白色 | 灰色 | 几乎无积碳 |
| Pt-CeO2/Al2O3 | 黄色 | 深灰色 | 较少量积碳 |
由图 8~图 11可知:助剂的添加改进了Pt系催化剂的抗积碳性,抗积碳性能优劣的顺序为:Pt-Li2O/Al2O3>Pt-CeO2/Al2O3>Pt/Al2O3>Pt-ZrO2/Al2O3。
3 结论1) 设计的催化剂体系适用于丙三醇水蒸气重整制氢反应。
2) 助剂的添加会改变Pt系催化剂的孔径、孔容、比表面积,进而改变催化剂的催化性能,助剂Li2O可增大Pt系催化剂的平均孔半径。
3) 通过比较不同催化剂使用前后的照片可知,Pt-Li2O/Al2O3催化剂抗积碳性能较优。
| [1] |
Charisiou N D, Papageridis K N, Siakavelas G, et al. Glycerol steam reforming for hydrogen production over nickel supported on alumina, zirconia and silica catalysts[J]. Topics in Catalysis, 2017, 60(15/16): 1226-1250. |
| [2] |
Demsash H D, Kondamudi K V K, Upadhyayula S, et al. Ruthenium doped nickel-alumina-ceria catalyst in glycerol steam reforming[J]. Fuel Processing Technology, 2018, 169: 150-156. DOI:10.1016/j.fuproc.2017.09.017 |
| [3] |
Bueno A V, Moura de Oliveira M L. Glycerol steam reforming in a bench scale continuous flow heat recovery reactor[J]. International Journal of Hydrogen Energy, 2013, 38(32): 13991-14001. DOI:10.1016/j.ijhydene.2013.08.082 |
| [4] |
Pompeo F, Santori G F, Nichio N N. Hydrogen production by glycerol steam reforming with Pt/SiO2 and Ni/SiO2 catalysts[J]. Catalysis Today, 2011, 172(1): 183-188. |
| [5] |
Markočič E, Kramberger B, van Bennekom J G, et al. Glycerol reforming in supercritical water:A short review[J]. Renewable and Sustainable Energy Reviews, 2013, 23: 40-48. DOI:10.1016/j.rser.2013.02.046 |
| [6] |
Papageridis K N, Siakavelas G, Charisiou N D, et al. Comparative study of Ni, Co, Cu supported on γ-alumina catalysts for hydrogen production via the glycerol steam reforming reaction[J]. Fuel Processing Technology, 2016, 152: 156-175. DOI:10.1016/j.fuproc.2016.06.024 |
| [7] |
Iriondo A, Barrio V L, Cambra J F, et al. Hydrogen production from glycerol over nickel catalysts supported on Al2O3 modified by Mg, Zr, ce or la[J]. Topics in Catalysis, 2008, 49(1/2): 46-58. |
| [8] |
李磊, 郭瓦力, 李俊磊, 等. 丙三醇水蒸气重整制氢M/Al2O3催化剂[J]. 化工进展, 2013, 32(1): 122-128. Li Lei, Guo Wali, Li Junlei, et al. M/Al2O3 catalysts for hydrogen production via the steam reforming of glycerin[J]. Chemical Industry and Engineering Progress, 2013, 32(1): 122-128. (in Chinese) |
| [9] |
Bossola F, Pereira-Hernández X I, Evangelisti C, et al. Investigation of the promoting effect of Mn on a Pt/C catalyst for the steam and aqueous phase reforming of glycerol[J]. Journal of Catalysis, 2017, 349: 75-83. DOI:10.1016/j.jcat.2017.03.002 |
| [10] |
Cheng C, Foo S Y, Adesina A A. Steam reforming of glycerol over Ni/Al2O3 catalyst[J]. Catalysis Today, 2011, 178(1): 25-33. |
| [11] |
田旭, 郭瓦力, 冯健, 等. NiLaLiPt/γ-Al2O3催化剂煤油水重整制氢的反应行为[J]. 天然气化工:C1化学与化工, 2011, 36(5): 45-48. Tian Xu, Guo Wali, Feng Jian, et al. Reaction behavior of NiLaLiPt/γ-Al2O3 catalyst for water reforming of kerosene to hydrogen[J]. Natural Gas Chemical Industry, 2011, 36(5): 45-48. (in Chinese) |
| [12] |
于涛, 郭瓦力, 王建武, 等. 柴油自热重整制氢工艺过程研究[J]. 天然气化工:C1化学与化工, 2010, 35(1): 46-49, 78. Yu Tao, Guo Wali, Wang Jianwu, et al. Study on process of autothermal reforming of diesel to hydrogen[J]. Natural Gas Chemical Industry, 2010, 35(1): 46-49, 78. (in Chinese) |
 2019, Vol. 36
2019, Vol. 36





