离子液体(ionic liquids, IL)是由体积较大的有机阳离子和无机/有机阴离子构成的离子型化合物。如果阳离子或者阴离子含有磁性中心,即具有单电子有机自由基结构或者金属离子配合物结构,能够被磁化并对外界磁场产生一定的响应[1-2],则称为磁性离子液体(magnetic ionic liquid, MIL)。其具有一般离子液体的液程宽、蒸汽压低、溶解能力良好等特性。由于具有不挥发等特性,许多离子液体可以作为绿色溶剂[3-6]。因离子液体对极性物质有较好的溶解能力,已在分离过程中用作气体吸收剂和液体萃取剂[7-9],在化学反应中用作反应介质或催化剂[10-13],在电化学中用作电解质[14]。
由于离子液体参与构建微乳液在萃取分离等领域具有显著的应用价值,近年来由离子液体参与构筑的微乳液体系研究得较多。黄艳杰等[15]基于胆碱骨架的功能化磁性离子液体体系的相平衡性质,并以这些离子液体为非极性溶剂,以水为极性溶剂,研究了烷基链长度和温度对相平衡性质的影响。Gao等[16]研究发现1-丁基-3-甲基咪唑四氟硼酸盐作为水相、环己烷作为油相微乳液的性质。Kuchlyan等[17]研究了双三氟甲磺酰亚胺基离子液体构建的微乳液性质。本课题组[18]研究CTAB和TritionX-100复配表面活性剂在氯仿作为溶剂时,增强溶离子液体bmimBF4(IL)所形成非水微乳液的电导性质。有些离子液体具有和表面活性剂类似的疏水链,因此在胶团和微乳液体系与表面活性剂相互作用方面应该具有一定的效果,但这方面文献中鲜有研究。这一研究能够拓宽离子液体的应用范围,而且具有一定的应用前景。
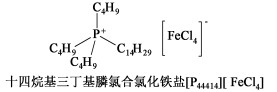
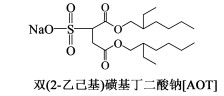
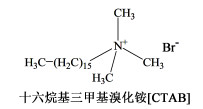
1 实验部分 1.1 仪器和试剂试剂:四丁基膦氯合氯化铁盐[P4444]FeCl4[默尼化工科技(上海)有限公司];十四烷基三丁基膦氯合氯化铁盐[P44414]FeCl4[默尼化工科技(上海)有限公司];十六烷基三甲基溴化铵(CTAB)C19H42NBr(AR,天津市华东试剂厂);双(2-乙己基)磺基丁二酸钠(AOT)C20H37NaO7S(AR,上海阿拉丁生化科技股份有限公司;环己烷C6H12(AR,天津市风船化学试剂科技有限公司)。
 |
(1) |
 |
(2) |
 |
(3) |
 |
(4) |
仪器:电导率仪(DDSJ-308A,上海仪电科学仪器股份有限公司)。
1.2 实验过程 1.2.1 离子液体水溶液中性质测定配制一定浓度的离子液体水溶液,按照测定条件加入到CTAB溶液中,用电导率仪测定电导率和溶液浓度的关系,Origin作图分析。
1.2.2 离子液体非水溶液中性质测定AOT/环己烷/水形成可以形成W/O型的微乳液,将2种磁性离子液体分别配制成浓度为1.0和5.0 mmol/L的水溶液,代替微乳液中的水相,在AOT/环己烷体系中滴加入离子液体水溶液,边滴加边测定电导率,Origin作图分析。
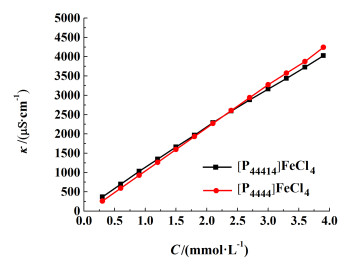
2 结果与讨论 2.1 离子液体在水溶液中与CTAB相互作用 2.1.1 离子液体在水溶液中的电导率不同链长的2种磁性离子液体:四丁基膦氯合氯化铁盐[P4444]FeCl4和十四烷基三丁基膦氯合氯化铁盐[P44414][FeCl4]在水中的电导率随浓度的变化关系见图 1。可见随着浓度的增大,2者的电导率均增大,[P4444]FeCl4变化幅度较大。对于[P44414]FeCl4离子液体,虽然具有14个碳的长链,但是在水溶液中其电导率随浓度的变化没有出现明显的转折点,说明该离子液体在所测定的浓度范围内并没有出现胶团,可能是因为离子液体的带电离子比较多,在水溶液中离子间的排斥作用较强,不具备形成胶团的条件。
|
| 图 1 电导率随[P4444]FeCl4/[P44414]FeCl4浓度的变化 Fig.1 Changes of conductivity with different [P4444]FeCl4/[P44414]FeCl4 concentrations |
| |
图 2中b和c曲线为CTAB与离子液体混合溶液中,保持离子液体的浓度为1.0 mmol/L,电导率随CTAB的浓度的变化关系。曲线a为不加入离子液体,其电导率随CTAB的浓度变化关系。可以看出,CTAB在溶液中形成胶团,并且其临界胶团浓度为1.0 mmol/L。但是加入固定浓度的离子液体后,除了其电导率增大以外,并没有影响其CMC值。这说明在CTAB和离子液体组成的混合溶液中,离子液体并没有与CTAB形成的胶团发生相互作用,而是单纯地提高了溶液的电导率。

|
| 图 2 [P4444]FeCl4/[P44414] FeCl4浓度为1.0 mmol/L与CTAB混合,电导率随CTAB浓度的变化 Fig.2 Changes of conductivity when 1.0 mmol/L [P4444] FeCl4/[P44414]FeCl4 mixed with different CTAB concentrations |
| |
CTAB为具有亲水亲油基团的季铵盐,离子液体为季膦盐,N和P在中心被甲基和长碳链包裹着,头基均带有正电荷,在水溶液中发生相互排斥作用,CTAB形成了胶团,离子液体则游离在水中,不与CTAB发生相互作用,所以离子液体的加入只造成了电导率的升高。
图 3为离子液体与CTAB等物质的量混合时,电导率随离子液体的浓度变化关系。可见随着离子液体的浓度增大,电导率呈现直线上升的趋势,与图 1变化类似,体系中虽然加入了CTAB,但是由于离子液体的电导率太大,不影响其电导率的值,虽然CTAB能够形成胶团,但是由于其电导率的值太小,对离子液体的电导率值并不产生影响。

|
| 图 3 [P4444] FeCl4/[P44414] FeCl4与CTAB等摩尔混合混合,电导率随CTAB的浓度变化 Fig.3 Changes of conductivity in different concentrations CTAB mixed with [P4444]FeCl4/[P44414] FeCl4 equimolarly |
| |
由图 1~图 3可见,在2种不同疏水链长的磁性离子液体和表面活性剂CTAB的混合溶液中,2者之间并不发生相互作用,对CTAB形成的胶团不产生影响。
2.2 离子液体在环己烷中与AOT的相互作用 2.2.1 AOT/环己烷/[P4444] FeCl4体系的电导AOT是在非水溶液中形成反相微乳液表面活性剂的典型代表,以环己烷作为非极性溶剂,在微乳液中的水核中加入水及浓度分别为1.0和5.0 mmol/L离子液体。对微乳液体系进行电导率的测定,比较AOT/环己烷/水体系和AOT/环己烷/磁性离子液溶液体系中电导率的变化情况及趋势。
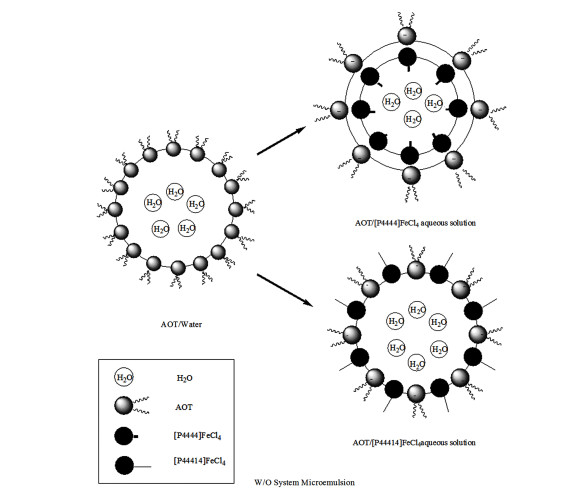
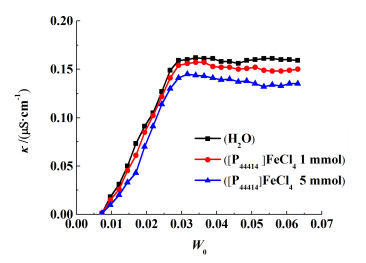
图 4中AOT/环己烷/水和AOT/环己烷/[P4444]FeCl4体系中,电导率随增溶水量的变化趋势为先突然增大,达到最大增溶水量,电导率趋于稳定不变。这种变化的原因是当开始时少量的水加入到环己烷中后,表面活性剂AOT的亲水基团包裹W/O型反相微乳液,亲水基朝向水相,疏水基朝向油相,加水量较少时,由于AOT中没有导电介质,所以开始的电导率接近0,当水分增加到一定值时,AOT在水核中可以发生电离,所以电导率增大。继续增加水量,而且被包裹的水核逐渐增大,直到最后被撑破,开始向双连续相转变,此时电导率将不再增大。
|
| 图 4 AOT/环己烷/水体系和AOT/环己烷/[P4444]FeCl4的导电率-W0的关系图 Fig.4 Conductivity-W0 relationship of AOT/cyclohexane/water system and AOT/cyclohexane/[P4444]FeCl4 system |
| |
图 4为AOT/环己烷/[P4444]FeCl4体系和AOT/环己烷/水体系电导率对比图,最大加溶液量W0为0.065,继续加离子液体的水溶液,体系浑浊,无法形成O/W微乳液。浓度为5.0 mmol/L的磁性离子液体比1.0 mmol/mL的电导率小,这一现象极为反常,原因可能是阴离子表面活性剂AOT电离,形成扩散双电层,加入离子液体超强电解质,压缩AOT双电层,使静电排斥力降低,促进微乳液液滴聚集和絮凝。可见磁性离子液体[P4444]FeCl4的存在对微乳液油-水混合膜的稳定是不利的。对于离子液体[P4444]FeCl4,围绕着P+周围的碳氢链比较短,不能与AOT的疏水链发生相互作用插入油水界面,离子强度又大,对AOT头基的压缩双电层作用强,使水核变小。带正电荷的季膦盐与带负电荷的AOT之间发生静电吸引作用,在很小的水核空间内其分子运动的自由度受到限制,所以造成了电导率降低。加入离子液体的浓度越大,压缩双电荷作用和静电吸引作用越强,水核被压缩得越小,被AOT吸引的正离子越多,造成电导率降低。
2.2.2 AOT/环己烷/[P44414] FeCl4体系的电导图 5是AOT/环己烷/[P44414]FeCl4体系的增水量和电导率的关系图。从图 5中发现[P44414]FeCl4体系的电导率比水体系的大,而且他们的最大增溶水量差别很小。对于[P44414]FeCl4体系,与[P4444]FeCl4相比有1个很长的长碳链,具有表面活性剂的结构。对于磁性离子液体[P44414] FeCl4最多增溶水量为0.3,而[P4444]FeCl4体系中最大增溶水量为0.065,2者相差了近5倍。

|
| 图 5 AOT/环己烷/水体系和AOT/环己烷/[P44414]FeCl4的导电率-W0的关系图 Fig.5 Conductivity-W0 relationship of AOT/cyclohexane/water system and AOT/cyclohexane/[P44414]FeCl4 system |
| |
Akatsuka等[19]研究表明表面活性剂的聚合作用主要由疏水基团之间的平衡作用和头基之间的静电作用决定。[P44414] FeCl4的亲水基团季膦盐带正电荷,与带负电荷的AOT之间发生静电吸引作用,而离子液体14个链长的疏水基团也可以插入微乳液的油水界面,形成混合界面。根据链长相容效应[20],[P44414] FeCl4与AOT疏水链长度不同,两者之间会发生排斥作用。两者头基发生吸引作用,面积变小,疏水碳链发生排斥作用,体积变大,此种结构更加有利于形成反相微乳液,可能的机理如图 6所示。因此AOT/环己烷/[P44414]FeCl4体系较为稳定,也能增溶更多的离子液体水溶液,离子液体在较大的水核环境中可以充分解离,因此5.0 mmol/L比1.0 mmol/L电导率大。
磁性离子液体具有一般离子液体的特性,将[P4444]FeCl4和[P44414] FeCl4离子液体在水溶液中与CTAB和在非水溶液中与AOT的相互作用进行比较,发现由于在水溶液中离子液体的电导率比较大,将电导率较小的CTAB的作用屏蔽,因此不与CTAB发生作用。在非极性溶剂环己烷中,碳链较长的[P44414] FeCl4则与AOT在反胶团的油水界面发生作用,表现出与[P4444]FeCl4相反的性质。
然而在离子液体水溶液作为水核的AOT和环己烷形成的微乳液中,对于[P4444]FeCl4水溶液作为水核体系,随着离子液体浓度的增加电导率减小,而对于[P44414]FeCl4体系,则随着离子液体浓度增加电导率增大。因为[P4444]FeCl4以压缩双电层作用为主,形成的水核较小,不利于离子液体导电。而[P44414]FeCl4则插入AOT形成的油水界面,有利于微乳液的形成。
| [1] |
Li L, Huang Y, Yan G P, et al. Poly(3, 4-ethylenedioxythiophene) nanospheres synthesized in magnetic ionic liquid[J]. Materials Letters, 2009, 63(1): 8-10. |
| [2] |
Okuno M, Hamaguchi H O, Hayashi S. Magnetic manipulation of materials in a magnetic ionic liquid[J]. Applied Physics Letters, 2006, 89(13): 1590. DOI:10.1063/1.2353808 |
| [3] |
Welton T. Room-Temperature ionic liquids. Solvents for synthesis and catalysis[J]. Chemical Reviews, 1999, 99(8): 2071-2084. DOI:10.1021/cr980032t |
| [4] |
Earle M J, Seddon K R. Ionic liquids. Green solvents for the future[J]. Pure and Applied Chemistry, 2000, 72(7): 1391-1398. DOI:10.1351/pac200072071391 |
| [5] |
Anderson J L, Ding J, Welton T, et al. Characterizing ionic liquids on the basis of multiple solvation interactions[J]. Journal of the American Chemical Society, 2002, 124(47): 14247-14254. DOI:10.1021/ja028156h |
| [6] |
Kosmulski M, Gustafsson J, Rosenholm J B. Thermal stability of low temperature ionic liquids revisited[J]. Thermochimica Acta, 2004, 412(1/2): 47-53. |
| [7] |
张香平, 白银鸽, 闫瑞一, 等. 离子液体萃取分离有机物研究进展[J]. 化工进展, 2016, 35(6): 1587-1605. Zhang Xiangping, Bai Yinge, Yan Ruiyi, et al. Progress in ionic liquids for extraction of organic compounds[J]. Chemical Industry and Engineering Progress, 2016, 35(6): 1587-1605. (in Chinese) |
| [8] |
Anderson J L, Armstrong D W. Immobilized ionic liquids as high-selectivity/high-temperature/high-stability gas chromatography stationary phases[J]. Analytical Chemistry, 2005, 77(19): 6453-6462. DOI:10.1021/ac051006f |
| [9] |
邵江娟, 吴昊, 赵雅秋, 等. 离子液体萃取技术及其在中药领域中的应用[J]. 中草药, 2013, 44(24): 3561-3565. Shao Jiangjuan, Wu Hao, Zhao Yaqiu, et al. Ionic liquid extraction technology and its application in field of Chinese materia medica[J]. Chinese Traditional and Herbal Drugs, 2013, 44(24): 3561-3565. (in Chinese) |
| [10] |
Roger S. Catalytic reactions in ionic liquids[J]. Chemical Communications, 2001, 36(23): 2399-2407. |
| [11] |
Wilkes J. Properties of ionic liquid solvents for catalysis[J]. Journal of Molecular Catalysis A:Chemical, 2004, 214(1): 11-17. DOI:10.1016/j.molcata.2003.11.029 |
| [12] |
Harada M, Kimura Y, Saijo K, et al. Photochemical synthesis of silver particles in Tween20/water/ionic liquid microemulsions[J]. Journal of Colloid and Interface Science, 2009, 339(2): 373-381. DOI:10.1016/j.jcis.2009.08.003 |
| [13] |
Olivier-Bourbigou H, Magna L, Morvan D. Ionic liquids and catalysis:Recent progress from knowledge to applications[J]. Applied Catalysis A:General, 2010, 373(1/2): 1-56. |
| [14] |
Hapiot P, Lagrost C. Electrochemical reactivity in room-temperature ionic liquids[J]. Chemical Reviews, 2008, 108(7): 2238-2264. DOI:10.1021/cr0680686 |
| [15] |
黄艳杰, 宋欣欣, 裴渊超, 等. 磁性离子液体微乳液的相平衡性质[J]. 河南师范大学学报:自然科学版, 2013, 41(6): 180-180. Huang Yanjie, Song Xinxin, Pei Yuanchao, et al. Phase equilibrium properties of functionalized ionic liquid microemulsions[J]. J Henan Normal Univ:Nat Sci Ed, 2013, 41(6): 180-180. (in Chinese) |
| [16] |
Gao Y, Li N, Hilfert L, et al. Temperature-Induced microstructural changes in ionic liquid-based microemulsions[J]. Langmuir, 2009, 25(3): 1360-1365. DOI:10.1021/la803452m |
| [17] |
Kuchlyan J, Kundu N, Sarkar N. Ionic liquids in microemulsions:Formulation and characterization[J]. Current Opinion in Colloid & Interface Science, 2016, 25: 27-38. |
| [18] |
刘金彦, 韦力瑗, 廖永娟, 等. 含离子液体的复配表面活性剂微乳液的电导性质[J]. 高校化学工程学报, 2012, 26(3): 436-441. Liu Jinyan, Wei Liyuan, Liao Yongjuan, et al. Conductivity properties of mixed surfactants microemulsions with ionic liquids[J]. Journal of Chemical Engineering of Chinese Universities, 2012, 26(3): 436-441. DOI:10.3969/j.issn.1003-9015.2012.03.012 (in Chinese) |
| [19] |
Akatsuka H, Yamamoto M, Ohara Y, et al. Effect of polyols on the shear-induced structure and rheological properties of behenyl trimethyl ammonium chloride/1-octadecanol/water ternary systems[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2008, 326(3): 169-174. |
| [20] |
Shiao S, Chhabra V, Patist A, et al. Chain length compatibility effects in mixed surfactant systems for technological applications[J]. Advances in Colloid and Interface Science, 1998, 74(1/2/3): 1-29. |
| [21] |
Kundu K, Bardhan S, Saha S K, et al. Water solubilization, conductivity and structural characteristics of single and mixed surfactant water-in-oil microemulsions in absence and presence of ionic liquids[J]. Fluid Phase Equilibria, 2014, 361: 237-249. DOI:10.1016/j.fluid.2013.10.046 |
 2019, Vol. 36
2019, Vol. 36