2. 天津大学化工学院绿色合成与转化教育部重点实验室, 天津 300072
2. Key Laboratory for Green Chemical Technology of Ministry of Education, School of Chemical Engineering and Technology, Tianjin University, Tianjin 300072, China
煤油蒸汽重整在制氢和高超声速飞行领域均有广阔的应用前景[1]。催化剂的积炭和烧结失活是当前该过程所存在的主要问题[2]。高稳定性的催化剂是实现煤油高效、可控重整过程的关键。Bengaard等[3]提出的反应机理认为:碳氢燃料分子被吸附在催化剂表面的双位点上,随后金属Ni选择性攻击吸附的碳氢燃料的终端α-碳并切断该C—C键;水优先吸附在催化剂的载体上并解离成含氧中间体形成可以移动的氧组分,这些可移动的氧组分可以和切断的α-碳中间体反应,故反应优先发生在金属与载体相互作用的界面处。为了尽可能提高燃料重整的效率及氢气产物的选择性,我们设计的具有高活性及稳定性的催化剂应该完美结合结构特性(分散度、金属颗粒的尺寸、比表面积、载体性质)和切断的α-碳中间体与来自解离水的氧组分有效结合及有效地平衡积碳的形成与积炭的氧化。
双金属的协同效应是提升催化剂活性及稳定性的有效方法。Koike等[4]研究了Ni-Fe/Al2O3催化剂用于甲苯水蒸气重整。通过调变Fe的含量制备Ni-Fe合金催化剂,发现金属Fe基本上聚集在Ni的表面形成合金,相比较于单金属Ni/Al2O3催化剂,Fe的引入可以提高催化转化甲苯的活性及抗积炭性能。Li等[5]研究了Mg-Al水滑石负载Ni-Cu制备合金催化剂,当n(Ni)/n(Cu)为4时所制备的催化剂的金属颗粒最小,表现出最好的催化活性及抗积炭性能。
除了添加过渡金属外,用贵金属改性制备双金属催化剂也能较好地提升催化剂的活性及稳定性。Wang等[6]制备了一系列双金属催化剂,发现Re加入到Ni/Al2O3催化剂,能较大程度上提高催化甲苯水蒸气重整的活性、稳定性及耐硫中毒能力。此外,通过W和Ce双助剂改性Ni/Al2O3催化剂,发现当W和Ce同时加入到催化剂上时催化剂具有最好稳定性及耐硫中毒能力。Zheng等[7]研究了几种喷气式JP燃料的预重整,发现Ni和Rh负载在活性氧化铝上表现出较好的低温预重整活性。Guggillia等[8]用溶胶凝胶制备Ru和氧化铈改性的Ni-Al2O3催化剂用于正十二烷水蒸气重整。发现Ru和氧化铈有助于活性组分的还原,且氧化铈的碱性有助于催化剂抗积炭性能的提升。此外,载体也是影响催化剂活性的重要因素。用有序介孔SBA-15封装活性组分是一个很好的抑制活性组分烧结团聚的方法。Tao等[9]用SBA-15为载体负载Ni-CeO2用于甲苯水蒸气重整,在较大的原料处理量下仍展现出较高的甲苯转化率。
本研究采用乙二醇辅助浸渍法将活性组分负载于SBA-15上,利用SBA-15大的比表面积和有序的介孔孔道均匀分散活性组分Ni。重点研究了Pt和CeO2作为助催化剂对正十二烷水蒸气重整的活性及稳定性的影响。
1 实验部分 1.1 材料正十二烷,分析纯,天津科密欧化学试剂公司;乙二醇,分析纯,天津光复精细化工研究院;六水合硝酸铈,分析纯,天津光复精细化工研究院;氯铂酸,分析纯,天津光复精细化工研究院;SBA-15,化学纯,南京先锋纳米科技;氢气,高纯,六方气体公司;氮气,高纯,六方气体公司;氦气,高纯,六方气体公司;氩气,高纯,六方气体公司。
1.2 催化剂制备用乙二醇法共浸渍Ni在SBA-15载体上,金属组分负载量(质量分数,下同)为6%。SBA-15载体购买自南京先丰纳米科技有限公司,使用之前先在干燥箱中120 ℃干燥6 h。一定量的六水合硝酸镍溶解于15 mL乙二醇中,加入1 g先前干燥好的SBA-15,搅拌12 h,然后转移至真空干燥箱(DZF-6020,天津星科仪器仪表贸易公司)150 ℃干燥24 h。得到的粉末样品在550 ℃空气氛中焙烧4 h。制备CeO2或者Pt改性的Ni负载于SBA-15方法与前面类似,CeO2与Pt的负载量分别为6%和1%,制备得到的样品记为6Ni/SBA-15、6Ni-1Pt/SBA-15、6Ni-6CeO2/SBA-15和6Ni-1Pt-6CeO2/SBA-15。
1.3 催化剂表征制备好的催化剂在表征之前需用氢气还原,将粉末样品装载在干锅中置于管式气氛炉通入氮气吹扫里面的空气,设置还原程序,然后通入氢气气氛,其流速控制为50 mL/min,温度控制在600 ℃,还原处理好的样品用样品袋密封。
通过日本理学公司Rigaku D8-Focus型X射线衍射仪测试催化剂的物相。广角X射线衍射测试条件为:Cu靶,Kα射线,管电压40 kV,管电流200 mA,采样步宽0.02°,扫描速度为8(°)/min,扫描范围10°~80°。
使用扫描电子显微镜SEM(Nanosem 430)观测催化剂的相关形貌及反应后催化剂表面积炭形貌。采集催化剂的粒径形貌和尺寸,自带的EDX能谱分析仪可分析样品的元素组成及元素分布(面扫描和线扫描)。放大倍数:20~800 000倍;二次电子分辨率:1.4 nm(1 kV,减速模式)。
采用荷兰FEI公司的Tecnai G2 F20透射电子显微镜(TEM)对催化剂的形貌及内部孔道结构进行观测。最大放大倍数:105万倍;点分辨率:0.24 nm;加速电压:200 kV;极限分辨率:0.14 nm;最小束斑尺寸:0.2 nm;最大倾角:±40°;X射线能谱仪能量分辨率:130 eV。
H2-TPR是在AMI-300化学吸附仪上测试。称量一定质量的粉末样品在Ar气氛下(30 mL/min)400 ℃预处理1 h。冷却至100 ℃后通入10% (体积分数)的H2-Ar混合气体(30 mL/min),以10 ℃/min升至800 ℃。
采用仪器型号为NETZSCH TG 209F3标准谱仪进行热重分析。测试环境:空气氛围,氮气流率50 mL/min,空气流率30 mL/min。测试过程中,称取约10 mg样品于陶瓷坩埚中,以10 ℃/min的速率升温至100 ℃,保持30 min,再以该升温速率升温至800 ℃,得到样品的失量曲线。对得到的失量数据微分,即可得到失重微分DTG曲线。
催化剂比表面积以及孔结构等物理性质是采用Micromeritics TriStar 3000型物理吸附仪在-196 ℃温度下进行N2的吸附脱附测试来测定的。首先样品需经过脱气预处理,在惰性气体(一般为Ar气)吹扫的情况下,温度为300 ℃预处理3 h。得到的数据采用Brunauer-Emmett-Teller (BET)方法计算样品的比表面积,并对N2脱附等温线采用Barren-Joyner-Halenda(BJH)方法评估催化剂的孔分布以及孔容等性质。
1.4 正十二烷水蒸气重整实验正十二烷水蒸气重整在管式固定床反应器中进行。反应前将目数为20~40的催化剂在600 ℃氢气下还原1 h,然后切换成氮气将体系温度稳定至反应温度。用高压计量泵输入计算量的水,在300 ℃气化,保持进料15 min,然后通入液体正十二烷,经300 ℃气化与水蒸气混合通入催化剂床层。反应后产物经过冷凝、干燥,用三通道气相色谱(Micro GC 490,安捷伦公司)在线分析气相产物中各组分的含量。色谱检测器为TCD检测器,色谱柱有3个,分别为活性氧化铝柱(10 m×8 μm)用于检测C3及以上烃类分子,PPU柱(10 m×30 μm)用于检测CO2、乙烷和乙烯,5A MS柱(10 m×12 μm)用于检测H2、N2、CH4和CO。第1和第2通道以He为载气,第3通道以Ar为载气。3根色谱柱的柱温分别为100、100和170 ℃。
根据气相产物分析结果计算正十二烷的转化率[式(1)];根据气相产物分析结果计算气相产物产率及组成[式(2)和式(3)]。
| $ X_{12}=\frac{F_{\mathrm{C}_{1}}^{\mathrm{out}}+2 F_{\mathrm{C}_{2}}^{\mathrm{out}}+3 F_{\mathrm{C}_{3}}^{\mathrm{out}}}{12 F_{\mathrm{C}_{12}}^{\mathrm{in}}} \times 100 \% $ | (1) |
气体产率(μmol/min):
| $ {R\left( {{H_2}} \right) = \frac{{{A_{{{\rm{H}}_2}}}{f_{{{\rm{H}}_2}}}}}{{{A_{{{\rm{N}}_2}}}{f_{{{\rm{N}}_2}}}}} \times R\left( {{{\rm{N}}_2}} \right)} $ | (2) |
| $ {\varphi \left( {{{\rm{H}}_2}} \right) = \frac{{V\left( {{{\rm{H}}_2}} \right)}}{{V\left( {{{\rm{H}}_2}} \right) + V({\rm{CO}}) + V\left( {{\rm{C}}{{\rm{O}}_2}} \right) + V\left( {{\rm{C}}{{\rm{H}}_4}} \right)}} \times 100{\rm{\% }}} $ | (3) |
式(1)中,X12为正十二烷的转化率,%;FC12in为进入反应器的碳总数,mol/min;FC1out为离开反应器的气体产物中C1产物总数(CO+CO2+CH4),mol/min。式(2)中,R(N2)=60 mL/min;R(H2)为氢气的流速(产率);AH2为氢气的峰面积;AN2为氮气的峰面积;fH2为氢气的相对校正因子;fN2为氮气的相对校正因子。式(3)中,φ(H2)为干气中(扣除氮气)氢气的体积分数,%;V(H2)为产物中氢气的体积。
2 实验结果和讨论 2.1 催化剂表征 2.1.1 催化剂孔分布催化剂的氮气吸附脱附等温线及孔径分布曲线如图 1a)和图 1b)所示。从图 1a)可知,制备催化剂的载体以有序介孔氧化硅为材料,因此,催化剂样品都展现出Ⅳ型等吸脱附等温线和H1型滞后环,且孔径分布分成集中(6.0 nm)。

|
| 图 1 a) 氮气吸附脱附等温线,b)孔径分布 Fig.1 a) N2 adsorption-desorption isotherms and b) pore size distribution of the catalysts |
| |
如表 1所示,相比较于纯的SBA-15,负载活性组分及助催化剂后催化剂的比表面积及孔体积均下降,这是因为负载沉积在SBA-15的孔道,堵塞部分氧化硅的介孔。但是,催化剂仍然保持较大的比表面积和较为均匀的孔道,这有利于活性组分的分散及反应物扩散接近活性组分,高活性提供了良好的基础[1]。
| Supports and catalysts | BET surface area/(m2·g-1) | Pore volume/(cm3·g-1)a | Pore size/nmb | Particle size/nmc |
| SBA-15 | 689 | 1.01 | 6.78 | |
| 6Ni/SBA-15 | 384 | 0.76 | 6.43 | 10.1/13.7 |
| 6Ni-1Pt/SBA-15 | 388 | 0.76 | 5.29 | 7.8/9.6 |
| 6Ni-6CeO2/SBA-15 | 375 | 0.70 | 5.74 | 7.2/8.8 |
| 6Ni-1Pt-6CeO2/SBA-15 | 390 | 0.73 | 6.44 | 6.1/7.2 |
| a Total pore volumes were obtained at p/p0=0.99.b BJH adsorption average pore diameter from the adsorption branches of the N2 isotherms.c Determined from TEM images, before reaction/after reaction. | ||||
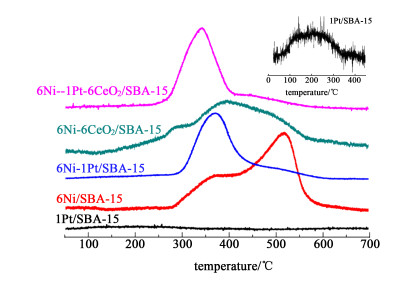
催化剂的H2-TPR数据如图 2所示,1Pt/SBA-15催化剂的还原峰主要集中在100~300 ℃之间(图 2内插图),这是PtO2的还原,其还原温度较低。单纯的6Ni/SBA-15有主要的还原峰在520 ℃,这个还原峰归属于硅酸镍[1],这种组分较难被还原,在该温度旁边360 ℃还原温度对应的还原峰归属于NiO分散在SBA-15孔道内的组分,该组分是催化剂活性体现的主要组成部分。
|
| 图 2 催化剂的程序升温还原 Fig.2 TPR profiles of the as-prepared catalysts |
| |
从图 2可知,当在NiO中加入助催化剂铂后,发现NiO组分变得更容易被还原,主要的还原峰对应的还原温度在360 ℃,这与之前报道的贵金属改性Ni的结果是相符的[10]。氧化铈改性6Ni-1Pt/SBA-15后,发现主要还原峰对应的还原温度降低至400 ℃。当氧化铈和铂同时作为助催化剂时,NiO的还原峰降低至340 ℃。这说明助催化剂的引入能增强与Ni的相互作用,尤其是氧化铈和铂同时作为助催化剂时,这种相互作用会更加明显。这种相互作用有利于提高Ni的分散及抑制Ni被烧结[11]。
2.1.3 催化剂TEM分析催化剂的TEM分析结果如图 3所示,6Ni/SBA-15催化剂的金属颗粒较大,且分散得不均匀,平均粒径在10.1 nm。加入氧化铈作为助催化剂后,6Ni-6CeO2/SBA-15催化剂中能较为明显地观察到Ni的颗粒变小,平均粒径降低至7.2 nm,分散度有所提高。与此类似,加入Pt作为助催化剂,Ni的分散也有所提升,但是也能观察到较大颗粒的金属团聚,很可能是Pt颗粒。当氧化铈与铂同时作为助催化剂时,能进一步减小金属颗粒尺寸(6.1 nm),增加了Ni的分散。如图 3e)和图 3f)所示,金属高度分散在SBA-15上,这说明氧化铈与铂同时作为助催化剂能非常好的提升Ni的分散。

|
| 图 3 新鲜催化剂的透射电镜图 Fig.3 TEM images of the fresh catalysts |
| |
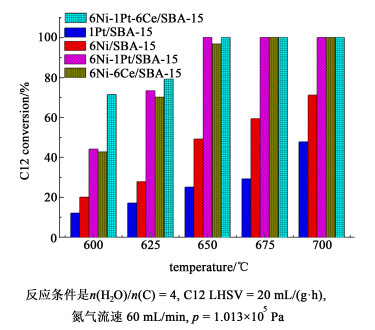
所制备的催化剂催化正十二烷水蒸气重整反应中转化率随温度变化关系如图 4所示。
|
| 图 4 正十二烷转化率随反应温度变化 Fig.4 Effects of reaction temperature for n-dodecane conversion over various catalysts |
| |
根据图 4可知,随着温度的升高正十二烷的转化率逐渐提高,与这个反应的强吸热性质一致。但是不同催化剂转化率提高程度不同,单金属的6Ni/SBA-15和1Pt/SBA-15展现出较低的活性,而当形成双金属的6Ni-1Pt/SBA-15时催化剂活性有所提升。在600 ℃处,1Pt/SBA-15和6Ni/SBA-15正十二烷转化率分别为12.1%和20.1%,而6Ni-1Pt/SBA-15与6Ni-6CeO2/SBA-15正十二烷转化率分别达到了44.1%和42.7%。这说明氧化铈和Pt分别作为助催化剂时均能有效提升催化剂的活性,这可能是Ni和Pt形成合金,通过合金的协同效应,或者是氧化铈与Ni相互作用提升Ni的分散度,从而提升催化剂催化转化正十二烷的能力。当氧化铈和铂共同改性时,催化剂的活性进一步提升,在600 ℃时,正十二烷的转化率达到71.4%,这可能是氧化铈与铂作为助催化剂与Ni产生非常强的相互作用,较好的提高Ni的分散,从而较大程度上增强其活性。
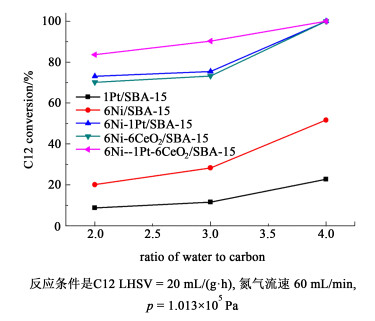
2.2.2 水碳比的影响不同催化剂性能在相同的条件下随水碳比(物质的量之比)变化如图 5所示,随水碳比的提高,正十二烷的转化率提升,主要是因为水是反应物。在相同的水碳比下(如水碳比为2时)各个催化剂催化正十二烷水蒸气重整的活性是不一样的,由高到低的顺序是:6Ni-1Pt-6CeO2/SBA-15>6Ni-6CeO2/SBA-15>6Ni-1Pt/SBA-15>6Ni/SBA-15>1Pt/SBA-15。这一规律与前面转化率随温度变化规律是一致的。
|
| 图 5 正十二烷转化率随水碳比变化 Fig.5 Effects of ratio of water to carbo for n-dodecane conversion over various catalysts |
| |
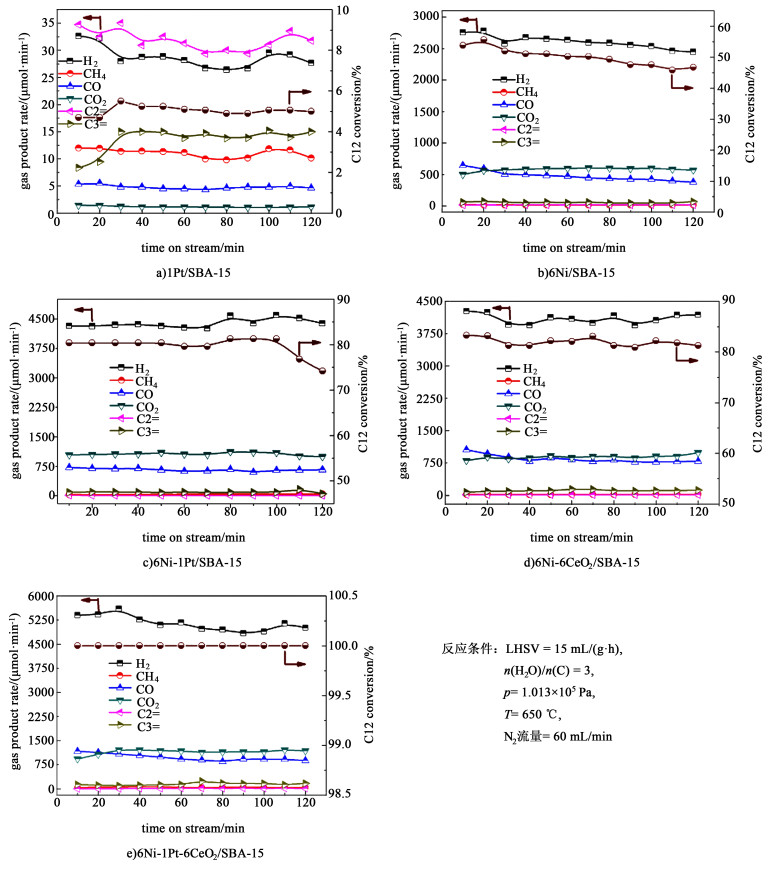
正十二烷转化率随时间变化关系的稳定性实验结果如图 6所示。1Pt/SBA-15催化剂催化正十二烷水蒸气重整的活性极低,正十二烷转化率基本上小于6%,气相产物组成较为复杂,主要是乙烯和丙烯及少量的CO和CO2。说明这个反应主要是热裂解,没有发生水蒸气重整反应。6Ni/SBA-15催化剂活性也不高,转正十二烷化率不到50%,气相产物主要以H2、CO和CO2为主,氢气产率只有2 500 μmol/min,说明这个催化剂主要催化了水蒸气重整反应。当Pt加入到Ni后即6Ni-1Pt/SBA-15催化剂催化活性提高较多,转化率达到80%,产氢速率增加到4 300 μmol/min。这一结果说明Pt是一个较好的助催化剂,Ni-Pt相互作用能增强催化剂的活性,但是该催化剂失活较快,在120 min时催化剂的转化率降低至74.2%。当氧化铈作为助剂时,6Ni-6CeO2/SBA-15时催化剂的活性进一步提升,转化率达到82%,产氢速率增加至4 100 μmol/min,且稳定性较好。当氧化铈和铂同时作为助催化剂时,形成6Ni-1Pt-6CeO2/SBA-15,催化剂的活性及稳定性是最优的。在相同的反应条件下,正十二烷的转化率达到100%,产氢速率提升至5 000 μmol/min,且全程保持100%的转化。这说明氧化铈和铂同时作为助催化剂时能较大程度上提高催化剂的活性及稳定性,这归因于Ni-Pt-CeO2的紧密的相互作用。反应结果数据与前面的H2-TPR和TEM分析结果是一致的。
|
| 图 6 正十二烷转化率及气相产物组成随时间变化 Fig.6 Conversion of n-dodecane versus time on stream over various catalysts |
| |
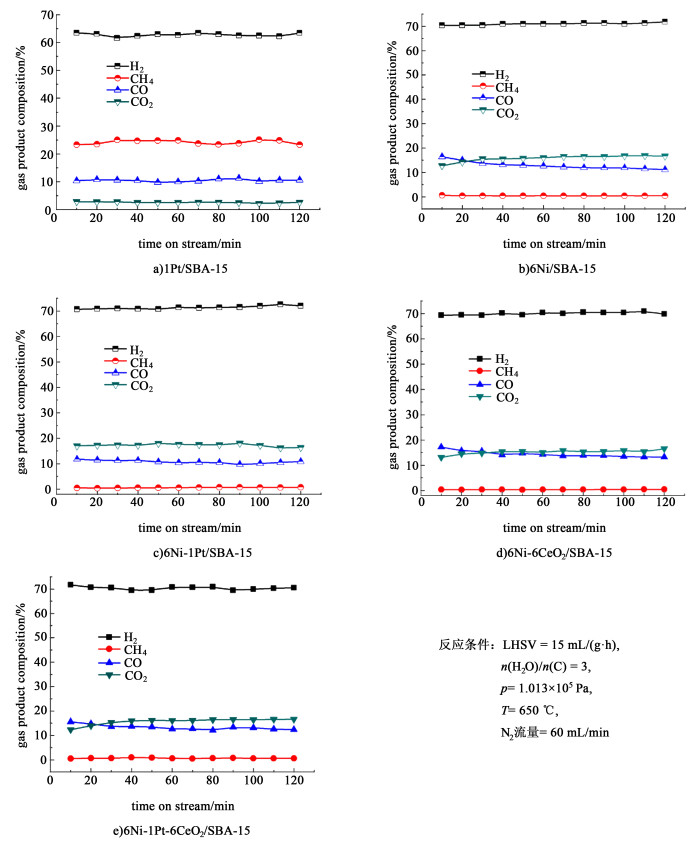
从图 7中可以知道气相产物组成大体只有4种成分:H2、CO、CO2和少量甲烷,这与文献[12]报道的结果是相似的。对于1Pt/SBA-15催化剂,其主要发生的裂解反应而不是重整反应,气相产物组成较为复杂,主要产物是乙烯和丙烯。因此,4种成分H2、CO和CO2差异较大,H2比例均较其它4种催化剂低。而6Ni/SBA-15、6Ni-1Pt/SBA-15、6Ni-6CeO2/SBA-15和6Ni-1Pt-6CeO2/SBA-15这4种催化剂主要发生的重整反应,主要的气相产物是H2、CO、CO2和少量甲烷,且4种组分的摩尔分数接近平衡组成。
|
| 图 7 气相产物百分含量随时间变化 Fig.7 Composition of gas products versus time on stream over various catalysts |
| |
反应后催化剂的XRD分析如图 8所示,6Ni/SBA-15催化剂反应后存在Ni被氧化的现象,因此出现了NiO的峰。由于Ni被氧化了,其催化性能降低,反应活性相对较低,积炭相对较少。反应后的6Ni-1Pt/SBA-15催化剂,Ni特征峰强度相对较大,半峰宽变窄。这说明Ni存在烧结现象。相比较于6Ni/SBA-15催化剂,Pt改性后积炭峰增强,可能是因为其活性相对较高,积炭量也相应增大。这说明Pt的引入可以提高催化剂的活性,但是Pt不能有效地减少积炭,可能原因是大部分Pt金属颗粒在SBA-15表面,这部分Pt对Ni的修饰作用不明显,因此催化剂抗积炭能力并未得到提升。氧化铈改性Ni-Pt催化剂活性提高较多,但是同样积炭也较多。从图 8所示,氧化铈改性Ni-Pt催化剂烧结并不严重,因为Ni和Pt的特征峰并未出现。这说明氧化铈加入可以较好地抑制金属的烧结。

|
| 图 8 稳定性测试后的XRD Fig.8 The XRD patterns of three representative spent catalysts |
| |
用SEM手段分析了反应后催化剂表面的积炭情况,结果如图 9所示,所有催化剂中均可以看见纤维碳。加入Pt助催化剂后,催化剂表面积炭反而增多,这与文献报道的可能不符。但是,结果显示,加入Pt助催化剂后,催化剂的活性及稳定性均有一定的提升,且仍能保持一段时间,这说明Pt的容炭能力较强,这与文献报道的结果是一致的[10]。

|
| 图 9 稳定性测试后SEM分析 Fig.9 SEM images of the spent catalysts |
| |
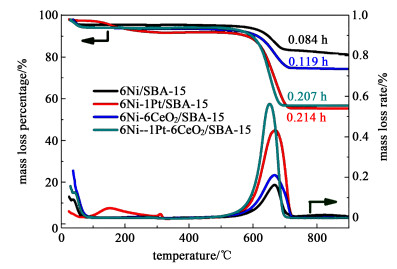
反应后催化剂的积炭量如图 10所示,6Ni/SBA-15的积炭量是最低的,这可能是因为其催化转化正十二烷的能力较弱,反应程度较低,因此积炭较少。加入Pt或者是CeO2后催化剂的积炭反而增加了,这可能是因为反应活性增强,积炭也增加,但是其活性和稳定性均保持得较好,这说明Pt和CeO2的加入使催化剂的容炭能力增强[10, 13]。
|
| 图 10 稳定性测试后催化剂TG-DTG分析 Fig.10 TG and DTG profiles of the spent catalysts |
| |
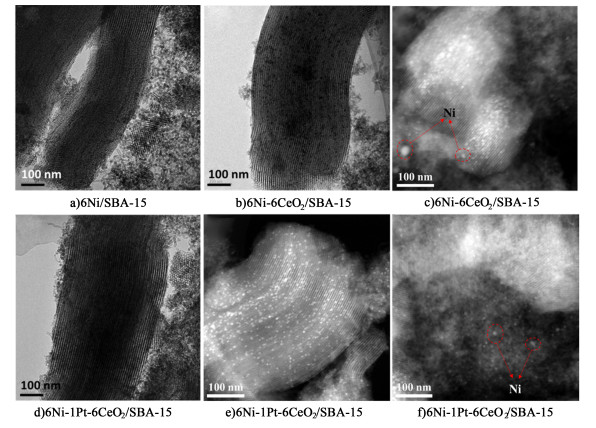
催化剂在反应评价后透射电镜如图 11所示,反应后金属颗粒变大了,即金属颗粒在较高的温度下发生了烧结。尤其是6Ni/SBA-15,反应后其金属粒径较大,达到13.7 nm。反应后催化剂载体SBA-15长程有序结构保持得较好,但是催化剂表面生成了大量的积炭。虽然CeO2改性后,Ni颗粒在反应后仍然变大,且这些较大的颗粒已经脱离了载体。Pt和CeO2协同改性后,反应后金属颗粒尺寸保持的较小(7.2 nm),这为其高活性和稳定性提供了基础。
|
| 图 11 稳定性测试后TEM分析 Fig.11 TEM images of the spent catalysts |
| |
1) CeO2和Pt作为助催化剂可以提高Ni的分散度,降低Ni的还原温度,减小Ni颗粒尺寸。
2) CeO2和Pt作为助催化剂,均能提高催化剂催化正十二烷水蒸气重整的活性及稳定性。
3) CeO2和Pt同时作为助催化剂时,催化剂显示出最高的活性及稳定性。
| [1] |
Xiao Z, Wu C, Li L, et al. Pursuing complete and stable steam reforming of n-dodecane over nickel catalysts at low temperature and high LHSV[J]. International Journal of Hydrogen Energy, 2017, 42(8): 5606-5618. DOI:10.1016/j.ijhydene.2017.01.034 |
| [2] |
Sehested J. Four challenges for nickel steam-reforming catalysts[J]. Catalysis Today, 2006, 111(1/2): 103-110. |
| [3] |
Bengaard H S, Nørskov J K, Sehested J, et al. Steam reforming and graphite formation on Ni catalysts[J]. Journal of Catalysis, 2002, 209(2): 365-384. |
| [4] |
Koike M, Li D, Nakagawa Y, et al. A highly active and coke-resistant steam reforming catalyst comprising uniform nickel-iron alloy nanoparticles[J]. ChemSusChem, 2012, 5(12): 2312-2314. DOI:10.1002/cssc.v5.12 |
| [5] |
Li D, Koike M, Chen J, et al. Preparation of Ni-Cu/Mg/Al catalysts from hydrotalcite-like compounds for hydrogen production by steam reforming of biomass tar[J]. International Journal of Hydrogen Energy, 2014, 39(21): 10959-10970. DOI:10.1016/j.ijhydene.2014.05.062 |
| [6] |
Wang L. Development of novel highly active and sulphur-tolerant catalysts for steam reforming of liquid hydrocarbons to produce hydrogen[J]. Applied Catalysis A:General, 2004, 257(1): 43-47. DOI:10.1016/S0926-860X(03)00590-8 |
| [7] |
Zheng J, Strohm J J, Song C. Steam reforming of liquid hydrocarbon fuels for micro-fuel cells. Pre-reforming of model jet fuels over supported metal catalysts[J]. Fuel Processing Technology, 2008, 89(4): 440-448. DOI:10.1016/j.fuproc.2007.11.024 |
| [8] |
Guggilla V S, Akyurtlu J, Akyurtlu A, et al. Steam reforming ofn-dodecane over Ru-Ni-based catalysts[J]. Industrial & Engineering Chemistry Research, 2010, 49(17): 8164-8173. |
| [9] |
Tao J, Zhao L, Dong C, et al. Catalytic steam reforming of toluene as a model compound of biomass gasification tar using Ni-CeO2/SBA-15 catalysts[J]. Energies, 2013, 6(7): 3284-3296. DOI:10.3390/en6073284 |
| [10] |
Moraes T S, Neto R C R, Ribeiro M C, et al. The study of the performance of PtNi/CeO2-nanocube catalysts for low temperature steam reforming of ethanol[J]. Catalysis Today, 2015, 242: 35-49. DOI:10.1016/j.cattod.2014.05.045 |
| [11] |
Li D, Zeng L, Li X, et al. Ceria-Promoted Ni/SBA-15 catalysts for ethanol steam reforming with enhanced activity and resistance to deactivation[J]. Applied Catalysis B:Environmental, 2015, 176/177: 532-541. DOI:10.1016/j.apcatb.2015.04.020 |
| [12] |
Ming Q. Steam reforming of hydrocarbon fuels[J]. Catalysis Today, 2002, 77(1/2): 51-64. |
| [13] |
Moraes T S, Neto R C R, Ribeiro M C, et al. The study of the performance of PtNi/CeO2-nanocube catalysts for low temperature steam reforming of ethanol[J]. Catalysis Today, 2015, 242: 35-49. DOI:10.1016/j.cattod.2014.05.045 |
 2019, Vol. 36
2019, Vol. 36





