气体分子是自然界中普遍存在的物质,在气-液两相界面中,气相与液相的相互交换过程也一直存在,气体溶解是一种重要的行为。我们理解,气体溶解(简称溶气)是指将气相与液相完全混合,主体是液相,使气相组分均匀分布在液相中的过程。早在19世纪初,亨利就发现了气体在液相中的吸收量与压力呈正比例的关系,由此引发了道尔顿将分压定律推广到气体混合物中的想法,并指出气体混合物中单个组分的溶解度取决于各自的分压,而与混合气体中的其他气体无关。在20世纪初,吉布斯应用了热力学原理来解决相平衡上的化学问题,提出了化学势的概念,建立了关于物相变化的相律。正是因为亨利定律描述了化合物在气液两相的分配规律,成为溶气过程原理的探究以及在化工生产等领域中应用推广的契机。人们越来越意识到,溶气过程参与了整个生态系统的生产和生活活动,涉及自然过程、生物过程、能源过程、环境工程及化工生产等多个领域。作为案例,比如:自然过程中的湖泊、深海及地表水中的水气界面的温室气体(CH4、N2O和CO2)交换通量的研究[1-3],地下水中的各种溶解性气体对于成矿过程的影响和古气候的温度形成的影响[4-5];生物过程中的生物发酵如多种微生物在厌氧条件下将有机质(生活垃圾、畜禽粪便和作物秸秆等)代谢分解为CH4、CO2和H2S等的过程[6-7];环境工程领域中的水处理工艺微生物的好氧/厌氧反应以及脱氮过程中将硝酸根或亚硝酸根转化为氮气的反应[8-10],还有将O2或O3作为反应物参与的催化氧化水中难降解有机污染物的过程[11-12]。由此可以看出,溶气过程贯穿于人类的各类生产实践活动中,但迄今非常缺乏溶气过程原理的归纳与方法技术的应用分析。本研究在回顾溶气过程原理基础上,讨论溶气气浮、好氧生物处理与O3深度处理的技术特征,分析它们的水处理工程应用。
1 溶气原理 1.1 亨利定律众所周知,气体在水中的溶解普遍遵从亨利定律,根据测量技术与量纲的需要,亨利定律表现出多种表达形式。亨利常数通常通过理论估算和模型计算来确定[13-16],主要包括相率平衡法、溶解度-气压法、分子动力法和蒙特卡洛法,温度和压力等各种物理化学条件都会影响不同气体的亨利定律常数[17]。亨利定律的热力学过程更为复杂,除了受温度、压力等物理因素的影响外,溶液的性质如气液平衡化学势、电导率等也会产生影响[18]。常用的亨利定律表达形式归纳如表 1所示。
假设气体分子的Van der Waals体积为bm(m3/mol),根据Van der Waals处理实际气体的思想,修正后的气体状态方程为[20]:
| $ P({V_{\rm{j}}}-{n_{\rm{j}}}{b_{\rm{m}}}) = {n_{\rm{j}}}RT $ | (1) |
式(1)中,nj为存留于水中的间隙空间中气体的量,mol;Vj为水的有效间隙体积。若Vw为水分子的体积,由于
| $ {V_{\rm{j}}} = {\phi _{\rm{j}}}{V_{\rm{w}}} $ | (2) |
合并(1)和(2)式,得到:
| $ {n_{\rm{j}}} = \frac{{p{V_{\rm{j}}}}}{{RT + {b_{\rm{m}}}p}} = \frac{{p{\phi _{\rm{j}}}{V_{\rm{w}}}}}{{RT + {b_{\rm{m}}}p}} $ | (3) |
式(3)即为气体j的间隙填充溶解度方程[20]。
一般来说,非极性分子比极性分子的溶解度小,是因为极性分子与水分子之间主要通过氢键连接,而非极性分子的溶解主要依靠分子之间的色散力发挥作用。要克服水分子间的作用力,形成非极性分子和水分子间的色散力是比较困难的。如果不同气体分子的极性相近时,分子体积大的气体溶解度小。据此推理,在一定环境条件下水相中气体溶解度的大小受溶质分子极性和分子体积大小的影响。
1.2.2 气体水合作用溶解机理根据温度较低时气体的溶解度随温度升高而降低的现象,可以推断,气体分子与水分子之间存在着相互作用,这种作用的强度和方式因气体分子性质而有所不同,把这些作用都统称为水合作用。在一定温度和压力下,气体与水形成水合分子,在水中存在如下平衡[20]:
| $ {\rm{G}}\left( {\rm{g}} \right) + n{{\rm{H}}_2}{\rm{O}}\left( {\rm{l}} \right) \leftrightarrow {\rm{G}}\;\cdot\;n{{\rm{H}}_{\rm{2}}}{\rm{O}}\left( {\rm{l}} \right) + 热量 $ | (4) |
尽管某些气体在室温下其水合作用程度很低,但一定存在。根据化学平衡原理,温度越低,压力越高,生成的水合分子越多,所表现出的溶解气体的溶解量越大。
气体在一定温度、压力条件下达到溶解平衡时的气体水合溶解度方程可表示为[20]:
| $ {K_{\rm{p}}} = \frac{{[{\rm{G}}][{{\rm{H}}_{\rm{2}}}{\rm{O}}]}}{p} = \frac{{{N_{\rm{h}}}}}{{{N_{\rm{m}}}{V_{\rm{w}}}p}} $ | (5) |
式(5)中,Nm为Avogaderlo常数,Nh为水合分子数,故:
| $ {N_{\rm{h}}} = {N_{\rm{m}}}{V_{\rm{w}}}p{K_{\rm{p}}} $ | (6) |
因此,在一定质量水溶液中以水合方式溶解的气体量为:
| $ {n_{\rm{h}}} = \frac{{{N_{\rm{h}}}}}{N} = {V_{\rm{w}}}p{K_{\rm{p}}} $ | (7) |
结合1.2.1的描述可知,水中存在间隙溶解和水合作用2种溶解机理,在实际的溶解过程中,2种机理是同时存在的,因此,气体总的溶解度方程为两者的加和,可表达为:
| $ n = {V_{\rm{w}}}\left( {p{K_{\rm{p}}} + \frac{{p{\phi _{\rm{i}}}}}{{RT + {b_{\rm{m}}}p}}-\frac{{{b_{\rm{m}}}{p^2}{K_{\rm{p}}}}}{{RT + {b_{\rm{m}}}p}}} \right) $ | (8) |
我们从(8)式中可以把气体在水中的溶解度看成是由3项常数加和构成,即:
| $ {k_2} = \frac{{{\phi _i}}}{{RT + {b_{\rm{m}}}p}};{k_3} = \frac{{{b_{\rm{m}}}p{K_{\rm{P}}}}}{{RT + {b_{\rm{m}}}p}} $ | (9) |
| $ c = ({K_{\rm{p}}} + {k_2}-{k_3})p = kp $ | (10) |
所以,总溶解度方程也是变形的亨利方程[20]。
以上研究表明,不同的气体(如He、H2、O2、N2和CO2等)的溶气原理具有差异性,需要有针对性地去讨论它们的技术特征。
2 技术特征 2.1 溶气气浮技术 2.1.1 气泡特征气泡大小是溶气气浮技术的重要因素,对碰撞行为、颗粒附着和上升速度均构成影响。图 1总结了4种气泡类别、气泡尺寸与气泡特性的相对关系。气浮净水工艺中,气泡尺寸过大会使气泡与胶体颗粒结合不稳定,杂质分离率降低,并且会出现撞碎絮粒的现象,从而影响气浮净水效果。经研究分析可知,当水中的悬浮物性质稳定时,气泡尺寸越小,与水中颗粒物黏附时需要的气泡数量越多,增加了气泡与絮体黏结的难度,从而明显地影响胶体颗粒的获气量和上浮速度。普遍认为[21-23],中等尺寸和大气泡直径(300~1 500 μm)对于矿物(细粒和粗颗粒)的浮选是最适宜的。微气泡(< 100 μm)适用于气浮过程固/液或液/液的分离。当浮选分离极小颗粒(甚至胶体)时,需要使用微气泡。一般来说,气泡的产生主要分为2个步骤[24],初始步骤是在小尺寸(< 1 mm)下成核,然后通过聚结迅速形成气泡。实际上气泡的形成是喷嘴或喷射装置中压降产生的气穴现象[25]。然而控制气泡大小的主要影响因素是释放系统的压力降。有研究表明,当压力升高至0.35 MPa时可以产生微气泡。Edzwald等[22]的研究结果显示,系统压力在0.44 MPa时所产生的气泡尺寸已经满足气浮技术的需求。除此之外,其他操作条件也能控制气泡的大小,比如声波功率、喷射管的长度、直径、类型和起泡剂等,例如声波功率从50 W提高至100 W,气泡大小将会有所增大(750~935 nm),当功率大于100 W后,气泡尺寸变化不大[26];喷射管直径越大释放出来的气泡大小也会越大[27]等。
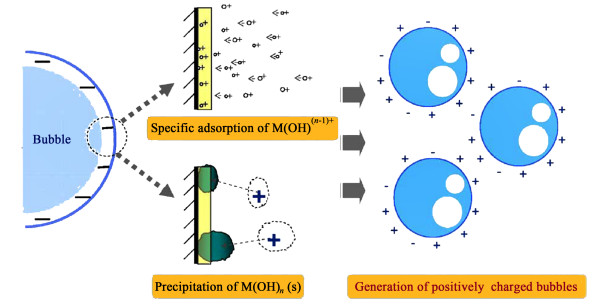
气泡产生之后,需要考虑气泡-气泡以及气泡-颗粒物之间的相互作用。目前,人们普遍认为存在4种作用力[29],包括范德华引力、静电引力、疏水相互作用和流体动力排斥力。然而,目前还只是停留在对作用力的定性描述上,量化表达仍然存在困难。其中,气泡表面带有电荷是产生相互作用力的原因之一。有研究表明,在中性条件的纯水中,气泡表面将带负电荷,表面电位为-30~-50 mV,主要是由于气泡界面吸附了OH-,诱导OH-选择性吸附的机理是水分子对H+(-1 127 kJ/mol)和OH-(-489 kJ/mol)的亲和力不同以及气泡界面处的水分子的偶极取向不同。也正是由于水偶极子取向的不同使氢离子偶极倾向于水相,氧原子指向气相形成了气泡界面的双电层现象。除此之外,有研究也报道了在没有添加化学絮凝剂的水溶液中气泡带负电荷[30],其原因是带负电荷的表面活性剂以及水生腐殖质在气泡表面的积累。气泡的Zeta电位是关于电解质性质,溶液的化学表面活性剂和pH值的函数,通过改变这些因素可以调节Zeta电位大小。在纯水中,气泡表面带负电荷程度主要由pH值影响[31],添加表面活性剂会改变阴离子吸附或阳离子解吸,从而引起气液界面静电动力学性质的改变,影响气泡的Zeta电位;Han等[32]探讨了不同价态絮凝剂加入后气泡Zeta电位的变化,发现随着Mg2+和Ca2+等的添加,气泡Zeta电位从-45 mV变到-20 mV,但加入了Al3+时,Zeta电位由负变为正,加入5 mg/L,电位从-27 mV升到20 mV,证明3价离子可以迅速吸附至气泡上,高价离子具有比低价离子更强的吸附能力,产生更多形成正电荷气泡的趋势。因此,气泡表面的电荷不仅可以改变Zeta电位大小,也可以改变颗粒的荷电性,如图 2所示。总体来说,Zeta电位可作为判断絮凝效果的指标参数。Zeta电位较高的体系,质点间排斥力较大,处于相对稳定状态,不易发生絮凝;而Zeta电位较低的体系,质点间排斥力较小,处于不稳定状态,易发生絮凝;在等电点处质点间排斥力最小,胶体稳定性最低,最易发生絮凝。
除此之外,气泡种类也会影响气浮分离效果。基于亨利定律,溶解的气体不同将会影响浮选的效果[33-34]。如CO2在增强颗粒气泡捕获方面表现出特殊作用[35-36],其它气体如He、Ar、H2、N2和O2的溶解降低了溶液CO2的浓度,并抑制了颗粒/气泡的捕获。
2.1.2 絮体特征通过添加絮凝剂可实现胶体的脱稳和絮团颗粒的形成而有助于气浮过程。根据气浮絮体模型可知[37-38],絮团是由单个胶体颗粒结合而成,其中胶体颗粒的个数会影响絮体的分形维数。胶体颗粒个数大,分形维数也越大,絮体不规则程度提高,使絮团产生更多的空隙和粗糙表面积,有利于黏附和架桥网捕作用,使气浮效果更好。因此,可以通过合理控制絮凝剂的种类、投加量、配比、投加点等操作条件来提高胶体颗粒的团聚与凝结[39-41]。除此之外,气泡和絮团之间能否有效地黏附在一起还取决于废水的溶液性质。例如,废水中同时存在亲水(活性染料、蛋白质、碳水化合物)和憎水(黏土、矿粉和硅酸盐等)2类悬浮胶体颗粒,就能构成稳定的悬浮溶液。加入铁盐或铝盐,在水溶液中产生具有吸附和架桥双重作用的铁铝氢氧化物,形成初级的絮体,当固体颗粒较小时需要加入高分子絮凝剂来促进絮团的生长。所以,普遍的气浮技术都需要借助药剂的投加来提高效果。
2.1.3 流体特征气浮过程其实也是气液固三相共存合作的关系,流体的性质不同也将影响气浮的效果。流体的物性参数包括密度、黏性、压缩性、膨胀性以及表面张力。目前,还很缺乏流体物性与气浮效果的相关性讨论。层流和紊流影响气浮的过程,影响气泡的上浮速率,层流和紊流时的流速由公式(11)和(12)分别描述[42]:
| $ {U_{\rm{F}}} = \frac{g}{{18\mu }}({\rho _{\rm{L}}}-{\rho _{{\rm{S, G}}}}){d^2} $ | (11) |
| $ {\rm{ }}{U_{\rm{F}}} = 1.83{[({\rho _{\rm{L}}}-{\rho _{{\rm{S, G}}}})gd/{\rho _{\rm{L}}}]^{1/2}} $ | (12) |
式(11)和(12)中,ρS, G为挟气胶体颗粒的表观密度,kg/m3;μ为水的动力黏滞系数,Pa·s;d为挟气胶体颗粒直径,m。当流型以层流形式水平流动时,流速较小,容易形成较薄的微气泡絮凝层;当流型为层流流动时,沿着气浮池水平方向,微气泡絮团厚度呈线性下降,在进水口可以形成30~50 cm厚的微气泡絮凝层,在末尾处则只有10~20 cm的微气泡絮凝层;当流体为紊流时,产生较大的流速,容易形成更厚的微气泡絮凝层[43]。然而,过快的紊流流速也会引起气泡在上升过程出现破碎和聚并的现象。
2.2 好氧生物处理技术 2.2.1 传质过程20世纪初,关于气液传质的模型和理论被盛行研究。1923年,由惠特曼提出的双膜理论成为气液传质的基础,接着出现了溶质渗透理论、表面更新理论等的改进。其中,双膜理论一直占据着主导地位。双膜理论主要是提出了气体的溶解由气膜或液膜控制的原则。根据双膜理论公式,认为可以通过改善氧传质系数KLa与总溶解度Cs实现氧扩散能力的提高。其中,水温、压力可以改善O2的溶解度,基于亨利定律,降低温度和提高气体分压可以增大O2的溶解度;同时,加强液相主体紊流程度、降低液膜厚度、加速气液界面的交换过程及增大气液接触面积等方法可以提高KLa值[44];更重要的是,基于间隙填充原理,通过改变废水水质极性以及气泡性质可以提高溶解度。总体来说,气体的传质过程与溶解过程是紧密联系的,归纳起来,影响氧传质的因素主要有温度、压力、废水特征、气泡性质和流体行为等。
2.2.2 反应过程气液传质过程影响O2的相转移效率,而针对废水的好氧生物降解过程,液固传质过程即微生物反应过程也会影响氧的总利用率。理论上,我们可以根据COD、氮化合物的好氧反应、内源呼吸作用等计算出反应过程所消耗的O2量[45],但是,实际过程曝气所提供的O2要远远高于计算量。其中微生物参与的好氧反应一般可以包括有机物的氧化、氨化、亚硝化、硝化、细胞合成代谢以及还原性物质的氧化等,由反应方程式(13)~(19)给予表达(以焦化废水为例)。因此,为了能够在节能下维持水处理的降解效果,应该根据废水量、污染物组成以及参与好氧的反应过程进行理论计算,得出好氧生物处理过程的最低需O2量,然后再合理地进行供氧分配。例如:
有机物氧化(酸化):
| $ \begin{array}{l} {{\rm{C}}_6}{{\rm{H}}_6}{\rm{O}} + 7{{\rm{O}}_2} \to 3{{\rm{H}}_2}{\rm{O}} + 6{\rm{C}}{{\rm{O}}_2}\\ \Delta {G^{⦵}} =-3025.816\;{\rm{kJ/mol}} \end{array} $ | (13) |
氨化:
| $ \begin{array}{l} {\rm{SC}}{{\rm{N}}^-} + 2{{\rm{O}}_2} + 2{{\rm{H}}_2}{\rm{O}} \to {\rm{S}}{{\rm{O}}_4}^{2-} + {\rm{N}}{{\rm{H}}_4}^ + + {\rm{C}}{{\rm{O}}_2}\\ \;\;\;\;\;\;\;\;\Delta {G^{⦵}} =-729.406\;{\rm{kJ/mol}} \end{array} $ | (14) |
| $ \begin{array}{l} {\rm{C}}{{\rm{N}}^-} + + 2{{\rm{H}}_2}{\rm{O}} \to 2{\rm{HC}}{{\rm{O}}_3}^-+ {\rm{N}}{{\rm{H}}_3}\\ \;\;\;\;\;\;\;\;\Delta {G^{⦵}} =-76.105\;{\rm{kJ/mol}} \end{array} $ | (15) |
亚硝化:
| $ \begin{array}{l} {\rm{N}}{{\rm{H}}_4}^ + + 1.5{{\rm{O}}_2} \to {\rm{N}}{{\rm{O}}_2}^-+ 2{{\rm{H}}^ + } + 2{{\rm{H}}_2}{\rm{O}}\\ \;\;\;\;\;\Delta {G^{⦵}} =-189.808\;{\rm{kJ/mol}} \end{array} $ | (16) |
硝化:
| $ \begin{array}{l} {\rm{N}}{{\rm{O}}_2}^-+ 0.5{{\rm{O}}_2} \to {\rm{N}}{{\rm{O}}_3}^-\\ \Delta {G^{⦵}} =-167.528\;{\rm{ kJ/mol}} \end{array} $ | (17) |
还原性物质的氧化:
| $ \begin{array}{l} {{\rm{H}}_2}{\rm{S}} + {\rm{H}}{{\rm{S}}^-} + 4{{\rm{O}}_2} \to 2{\rm{S}}{{\rm{O}}_4}^{2-} + 3{{\rm{H}}^ + }\\ \Delta {G^{⦵}} =-1473.518\;{\rm{ kJ/mol}} \end{array} $ | (18) |
微生物合成反应通式:
| $ {\rm{C}}{{\rm{H}}_m}{{\rm{O}}_n} + a{{\rm{O}}_2} + b{\rm{N}}{{\rm{H}}_3} \to c{\rm{C}}{{\rm{H}}_x}{{\rm{O}}_y}{{\rm{N}}_z} + e{{\rm{H}}_2}{\rm{O}} + f{\rm{C}}{{\rm{O}}_2} $ | (19) |
基于好氧生物处理过程的氧传质与反应过程的气液固三相关系,需要建立明确的氧利用效率及能耗评价指标。针对不同的应用需求,能耗评价参数可以概括为氧的动力效率、转移效率、负荷效率和污泥效率[46]。其中,氧的转移效率[通过鼓风机输送至废水中的溶解氧的含量,以每1 h溶解O2的质量(kg)表示,即O2溶解的过程]和氧的动力效率[每消耗1 kWh电能溶解氧扩散到混合液的量,以kg/(kWh)计]是指曝气装置将O2由空气输送至液相中所必须的能量消耗,主要受鼓风机效率以及曝气方式/效果的影响;氧的负荷效率和氧的污泥效率主要是针对污染物和悬浮固体浓度来定义其效率,以去除1 kg的BOD/COD所需要的O2质量在氧转移和氧动力效率上的表达,是单位污泥量在单位时间内将污染物转化为CO2的需氧量。
2.3 O3催化氧化技术 2.3.1 O3的发生与性质O3分子(氧化还原电位E⦵=2.07 V)由于其共振结构,使两端氧原子电子云密度分布不均匀,从而赋予其强亲电性和亲核性,由此决定了O3具有活泼的化学反应活性以及广泛的应用前景[47]。从1906年第1座以O3氧化作为饮用水处理工艺的水厂在法国Nice投入运行以来,O3氧化技术应用于水处理已有超过100年历史。虽然O3氧化技术具有高效、不产生二次污染等优势,但也存在以下3方面的缺点。1) O3的性质极不稳定,通过高压电离(或电解、化学、光化学反应)方法技术获得的O3,其生产过程是将空气中的部分O2分解为氧原子,氧原子再和氧分子聚合成O3分子,但是,O3分子生成之后会快速分解,降低了过程的有效性。2) O3对有机物的矿化率不高。O3虽然表现出较强的氧化性,但却具有极高的选择性,使得O3在水处理过程中对难降解物质的去除率低,很难彻底去除水中的TOC和COD成分,使反应停留在小分子有机物的水平上,需要进一步的生物降解实现矿化。3) O3利用率低。受限于气液传质,在O3氧化水中有机物时,如果反应器的设计不合理,大部分O3直接以气体的形式从水相中逸散至气相中[48]。一般来说,O3在催化剂表面的吸附形态可分为3种[49-52]:通过固体表面剩余力场作用,O3分子物理吸附于催化剂表面;通过与—OH2+之间氢键以及静电引力实现物理吸附;与强Lewis酸位点结合生成原子氧(E0=2.42 V)实现化学吸附。需要通过加强催化剂表面的吸附行为研究来克服O3氧化技术存在的缺点。
2.3.2 传质与催化反应由于O3催化氧化技术效率涉及气、液、固非均相/多相原理,其中传质、催化反应都是重要的影响因素。传统的O3水处理技术普遍采用的O3反应器模式是产生O3-输送至O3-反应器底部曝气-液相反应的过程,此种模式将带来大量的O3浪费。因此,为了更大程度地提高O3的传质利用效率,提出了多种关于O3气体的原位利用、均匀分布和微孔曝气的反应器。O3制备耦合有机物降解的一体化装置[53-54]利用介质阻挡放电原理产生O3,同时将待处理废水均匀分布于放电室空间内,将产生的O3气体原位利用,这种运行模式不仅避免了O3气体在输送过程的自耗行为,而且节省了反应器的运行空间;由于在放电室空间内均匀分布废水,等离子体与废水作用同时产生其他强氧化性物种如·OH、H2O2和·O等[55-56],也能够更高比例地被污染物所直接吸收利用。利用多孔板负载硅砂填装层对气-液流速的均衡性和流化床内循环对气-液的有效调控,实现O3气体的均匀分布,被证明也是效率提高的一种手段。还有研究发现,改进传统O3反应器,并安装微孔曝气装置可以有效地提高O3的传质与反应效率[57-58]。
除此之外,O3催化剂的研制及界面的调控过程也可以实现反应效率的提高。目前研究报道的非均相催化剂大致归纳为:金属氧化物、金属氧化物表面上的金属负载、矿物质、碳基质材料、黏土和蜂窝陶瓷等[59]。O3催化氧化过程通过3步骤来完成:O3吸附于催化剂表面并分解为高活性自由基、自由基氧化降解吸附于催化剂表面的有机物或扩散至溶液体相中与有机物反应、降解产物从催化剂表面脱附。大量研究表明,O3催化剂表面的活性位点分为Lewis酸位点(化学吸附O3,或催化分解O3)和表面含氧官能团,如表面—OH(催化分解O3)。因此,可控性调节这2种催化位点被认为是O3催化剂研究的前沿方向之一。例如通过Ti掺杂可提高γ-Al2O3催化剂表面Lewis酸位点强度[60],究其原因主要是Al—O—Ti键的生成,其中电子云密度偏向Al(Al的电负性大于Ti)导致Ti展现出缺电子特性(Ti的价态由掺杂前3+升为掺杂后的4+),从而使催化剂表面的Lewis酸强度提高。在电子转移过程中如何有效地将小分子有机酸矿化是O3催化氧化技术面临的挑战。
3 水处理工程应用 3.1 溶气气浮分离技术 3.1.1 给水处理应用溶气气浮工艺在给水处理方面,主要应用于低温低浊,高藻,高色度,含天然有机物、消毒副产物、消毒副产物前驱物和致病微生物等水体的处理。例如,Phoochinda等[61]曾经研究了通气速率、藻类悬浮液pH值和3种表面活性剂(CTAB,SDS和非离子Triton X-100),用于考察浮选栅藻(Scenedesmus quadricauda)的有效性。结果表明,CTAB和SDS提高了通气率,减小了气泡的大小,藻类去除率分别为90%和16%。降低藻类悬浮液的pH值,在SDS添加溶液中去除效率提高到80%,但对于CTAB,没有看到去除效率的改善。同样,Kurniawati等[62]也观察到,当单独使用皂苷时,对于藻类的浮选分离不太有效,但使用5 mg/L的壳聚糖进行预絮凝,使用20 mg/L的皂苷时,能够获得大于93%的微藻细胞分离效率。
尽管气浮浮选技术通常用于去除藻类颗粒,但由于化学絮凝所需的复杂且昂贵的设施和设备,藻类捕获技术的实用性受到限制。近年来,研究人员发现了一种廉价简单而快速的自絮凝现象[63],该现象利用自然重力沉降来实现藻类的絮凝,在较高的pH值条件下实现诱导并且保证此过程对细胞的破坏性较小。Wu等[64]指出,通过将pH值提高到10.6,淡水和海洋微藻的生物量回收率大于90%。同样,Vandamme等[65]使用NaOH、KOH和Ca(OH)2将pH值增加至10.8,实现98%的生物质回收率。由于水净化特殊功能的发现,溶气气浮技术的饮用水深度净化已经走向了应用市场。最近,有研究者[66]开发了一种应急处理富营养化爆发污染的溶气气浮一体化设备,此设备可以在5 min内完成快速凝固作用,并且在PAC用量为220 mg/L,溶解空气在水中的回流比为23.81%,气液分离泵压力为0.38 MPa时,浊度、总磷和叶绿素A的去除率分别达到80%、72%和71%,COD的去除率高达61%。表明流体特征、药剂的协同作用促进了气浮效果的提高。
3.1.2 工业废水处理应用在工业废水处理方面,气浮技术己经广泛应用于冶金、采矿、纺织、造纸和印染等领域,显示出越来越成熟与实用的特征。针对气浮除油过程,絮凝剂的种类具有重要影响。王振波等[67]探讨了溶气压力、表面活性剂及絮凝剂等影响因素对溶气气浮法处理乳化油废水的有效性,结果表明,除油效率与溶气压力呈现一定的正相关关系,究其原因是压力增大有利于产生更多的气泡数量;发现了相比于有机絮凝剂聚丙烯酰胺,无机絮凝剂聚合氯化铝具有较好的絮凝效果,可以提高气泡与油滴碰撞附着的概率;加入活性剂十二烷基硫酸钠可以降低溶液表面张力,降低气泡聚并机率,有效地改善了除油效果。Painmanakul等[68]通过投加明矾强化混凝气浮预处理含油废水,在pH值为9~10条件下,明矾投加量为800~1 400 mg/L时,含油量去除率高达99%。此外,为了能克服气浮仅仅是物理化学过程作用的缺陷,人们将气浮原理与生物处理或者化学氧化融合起来。Zhang等[69]研究了加压曝气与溶气气浮结合的生物反应器中空气压力、溶解氧对污染物去除效率的影响,当压力在0.10~0.50 MPa范围内逐渐增加时,固体悬浮物去除率也逐渐增加,COD的去除在0.40 MPa时达到最大值的86%;DO浓度在0.5~5.5 mg/L范围内增加时,氨氮的去除率也逐渐增加至99%。以上证明了气浮技术对工业废水的处理具有普遍性效果。此外,结合O3/H2O2的气浮技术也逐渐得到研究和重视。
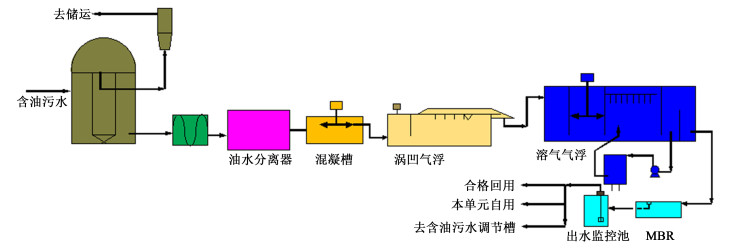
3.1.3 生活污水处理应用城市污水在除油方面也已经有很多气浮技术应用的案例。如图 3所示,简单介绍了含油污水处理的工艺流程,其中主要的过程包括了油水分离器将表层浮油分离,然后加入混凝剂使剩余分散及乳化油形成絮体,通过气浮装置,使絮状物与气泡结合浮水水面,达到分离的目的。Zheng等[70]研究了新型微气泡气浮技术对餐饮废水中油分的分离,结果表明,当操作条件控制聚合氯化铝PAC剂量为20 mg/L,反应时间为15 min,操作压力为0.35 MPa,回流比为25%时,油分、CODcr和浊度的去除效率分别比传统溶气气浮技术高10.3%,22.6%和15.0%,油分和浊度的最大去除效率分别为98.0%和97.5%。主要原因是新型微气泡气浮在操作压力为0.90 MPa时可以连续稳定产生和油滴尺寸相近的气泡尺寸,直径大小为20 μm。说明气浮技术对于乳化油的分离非常有效。
|
| 图 3 含油污水处理工艺流程图 Fig.3 The flow diagram of oily sewage treatment |
| |
生物好氧活性污泥法是废水好氧生物处理技术的原理基础,是在通入O2或空气的条件下,使微生物利用氧分子及有机污染物而产生的一系列生物化学反应的过程。传统的活性污泥生物脱氮工艺如图 4所示,是一个3段式活性污泥过程,主要是遵循硝化反硝化脱氮的模式。其中第1阶段进行好氧除碳单元,第2阶段进行好氧硝化过程,然后进入反硝化反应器实现脱氮。随着技术的发展以及节能的要求,衍生了很多工艺,包括A2/O、A/O和倒置A2/O等。除此之外,我们也需要关注气液固三相之间的传质与反应关系。众所周知,O2与水分子极性不同,在水中的溶解度较低,主要是依靠间隙填充原理来实现溶解。同时,O2的溶解过程受传质限制。目前的实际废水处理工程中,普遍存在充氧效率低和运行费用高的问题,氧转移的动力效率仅为4%~10%;普遍来说,供氧能耗占废水处理总能耗的60%~70%。因此,受供氧过程的限制,废水好氧生物处理技术一般只适用于中、低浓度有机废水的处理,且曝气能耗较高。同时,好氧生物法难以处理含有难降解高分子有机物的废水,主要是因为其相对分子质量大无法进入细胞膜内部而被微生物所利用。

|
| 图 4 传统活性污泥脱氮工艺流程图 Fig.4 The diagram of traditional activated sludge denitrification process |
| |
为了能合理地利用O2,降低能耗,处理过程需要平衡进水容积负荷与耗氧量之间的关系。对此,根据技术控制的需要,多种自动在线控制溶解氧的模式如基于P-FUZZY-PI、自适应专家系统的PID控制模式[71],针对进水有机负荷的不同而自动控制溶解氧的量,实现污染物的有效去除下的最低氧量的利用。除此之外,控制溶解氧的量还可以限制氮的转化过程,实现氨化、亚硝化、硝化在各个阶段的稳定运行。早年就有研究,在25 ℃条件下,AOB和NOB的O2饱和常数[72]分别为0.3和1.1 mg/L,AOB菌对溶解氧的亲和力强于NOB菌,在低于NOB菌O2饱和常数的溶解氧条件下,AOB菌将优先利用水中的溶解氧,而NOB菌因为无法获得满足生长需求的O2而被逐渐淘汰[73]。目前,还有研究表明[74-75],当保证pH值、温度等其它条件适宜的情况下,DO维持0.5~1.0 mg/L时就能够实现亚硝氮的积累,高于2 mg/L时能实现硝化过程,当DO小于0.5 mg/L时反硝化能顺利进行。微生物对有机物的降解过程实质上就是对氧的利用过程。在好氧生物处理废水的工艺中,DO浓度对有机物降解速率影响很大。高春娣等[76]应用交替缺氧好氧SBR工艺处理城市污水,当DO浓度高于2.0 mg/L时,污染物很快能降解完成,继续提高DO不再影响污染物降解速率;当DO浓度低于0.8 mg/L时,污染物的降解速率下降。因此,认为当DO过高时,DO不再是影响微生物代谢有机物的限制性因素。Wang等[77]利用好氧颗粒污泥研究硝化反硝化中发现,当DO值为2 mg/L左右时比较合理,总氮的去除率为61.68%,DO为4 mg/L时,总氮的去除率反而降低为35.22%,此时,当DO维持在2 mg/L时实现同步硝化反硝化除氮,总氮去除效果最佳。另外,运行方式的不同也将造成DO的分布和利用的显著差异[78]。研究表明[46],传统的氧化沟、生物转盘存在停留时间长、处理负荷低以及充氧效果差的缺点,但是新一代好氧生物流化床可以实现高浓度且均匀分布的DO来源,并且可以实现8~12 g/L的污泥浓度流态化运动,达到98%以上的体积利用率,成为非常高效的废水处理好氧生物技术。
3.3 生物尾水的O3催化氧化O3氧化技术应用于有毒/难生物降解废水的生物处理尾水的深度处理领域,究其原因是复杂工业废水经优化的生物处理后,出水中普遍存在低浓度的残余有机污染物,表现为分子的电价饱和以及疏水性能的存在,往往需要通过化学法深度处理,才能保证后续膜法的正常运行。以焦化废水为例,我们发现,焦化废水COD 30~80 mg/L的达标尾水中含有难以生物降解的含氮杂环化合物(0.80~129.70 μg/L)、苯衍生物、烷烃和多环芳烃(PAHs,0.05~3.36 μg/L)等[79],环境风险很高,影响后续的盐分离效果与水回用的风险。考虑到O3催化氧化法兼顾对有机物的选择性氧化、广谱消毒作用,不引入盐分及低二次污染[80]等特征,将其作为膜法脱盐的预处理技术,随着O3生产原理(O3发生器)技术的进步,应用前景越来越广阔。图 5是将O3与脱盐结合的处理工艺流程,先通过O3催化技术将前端出水进行深度处理,降低后续盐分离负荷,然后进入电渗析工艺实现盐分离与回用。由此可见,生物尾水的O3催化氧化技术的研究与发展是十分有必要的。

|
| 图 5 O3催化氧化处理工艺流程图 Fig.5 The flow diagram of ozone catalytic oxidation process |
| |
通过案例研究发现[81],O3氧化过程中有机物的种类发生了改变,主要的含氮有机物包括含氮杂环、腈类等快速被O3氧化,胺类物质出现先增多后减少的过程,随着反应时间的延长也能够被彻底氧化;烯烃、酚类等含不饱和官能团的有机物也能被选择性氧化。O3氧化过程中会形成有机酸类、烷烃类等中间产物,该类物质具有较低的HANs和THMs生成潜能,O3氧化过程可有效减少外排水的环境风险。然而,单独的O3氧化技术也存在其局限性,例如,O3在降解高浓度有机污染物时,存在矿化不彻底以及会产生中间副产物等缺点。一般来说,O3氧化技术适合于去除废水的色度、除臭等,但是对于生物尾水的深度处理,其降解过程缓慢,将带来极大的能耗问题。这主要是由O3在液相中溶解度低及半衰期小的性质所决定的[82]。因此,为了能提高O3氧化的能效,O3催化氧化技术逐渐成为研究热点。例如,Lin等[83]发现紫外光耦合O3催化过程可以增强PAHs的降解效率,约为45.4%,COD残余40 mg/L左右,并且利用O3/H2O2技术对焦化污泥中PAHs的降解效果和影响因素进行分析,结果发现,O3/H2O2技术可以在O3浓度为500 mg/g MLSS下实现PAHs超过95%的去除,且提高H2O2和pH值可以有效的提高PAHs的降解。除此之外,Zhang等[84]研究了各种O3催化剂对尾水的降解过程,与非催化O3氧化相比较,ZnFO-H催化O3降解焦化废水尾水的TOC效率提高了53%。同样地,Ma等[85]将负载了Fe3O4纳米颗粒的生物炭,用于催化O3降解生物处理出水。研究发现,在纳米Fe3O4@CDA用量0.8 g/L,投入O3 3.0 g/L,反应时间120 min时使BOD5/COD从0.05增加到0.32。负载金属氧化物的生物炭具有优异的稳定性和催化活性,原因是基于电子顺磁共振理论可以加速产生·OH。除了通过研制O3催化氧化剂以及协同光催化降解等手段之外,O3反应器的合理选择也可以提高O3的传质与利用,降低能耗。例如,Yang等[86]提出了一种新型的O3接触反应器,采用平行布置多孔管实现气体和水流的有序流动,达到气液均匀分布的效果,相比于传统的O3接触反应器,可以在少添加33%~50%的催化剂条件下实现更高的有机污染物降解率(提高了49%~130%)。另外,Zheng等[87]将微气泡O3发生装置与紫外光催化耦合,发现微气泡-O3化/UV过程中的羟基自由基产生约为比单独的微气泡-O3化和单独的紫外线照射的总产量高1.8倍。该过程中O3分解率约为其它2种的4.1倍,使废水的可生物降解性由0.18提高到0.47,其主要原因是产生的微气泡(平均粒径小于40 μm)相比于大气泡能够更好地提高气液接触时间、提高污染物附着的表面积以及提高O3的传质效率。因此,可以通过改变反应器的内部结构、高径比、曝气孔径等方式来提高O3的传质与反应效率。传质过程强化、反应动力学控制以及基于污染物的催化剂的有效性,它们的结合是O3催化氧化技术未来发展的方向。
4 讨论通过不同的相界面的作用力来实现废水中荷电离子/分子/胶体颗粒的分离成为气浮技术的原理基础。迄今,气浮技术已经发展成为很成熟的技术,其关键特征是通过溶气气泡、流体特性、混合特性与废水中的悬浮物/胶体/油分加以共同作用,再通过水处理药剂以及pH值的控制,有效地实现了介电物质的脱稳,作为预处理手段,达到从废水当中去除绝大部分悬浮物、胶体成分、重金属离子、油分以及部分有机污染物的目的;废水生物好氧处理技术通过曝气手段实现供氧与提供动力的结合,前者主要受溶气气泡尺寸、流体混合、污泥浓度以及废水性质的影响,后者提供大型反应器/工程装置内流体混合均匀的搅拌作用,两者的匹配非常重要,活性污泥利用溶解性的氧分子同化代谢有机污染物,根据供氧量的严格控制,可以实现氨化、厌氧氨氧化、亚硝化、硝化的不同阶段,通过强化的供氧模式,还可以实现高负荷的好氧运行,由此提出,气液传质、液固传质的匹配通过反应器的性能加以实现成为技术的关键;O3的催化氧化过程当中涉及到由气相的O3分子溶解到液相中的传质过程,要求O3分子完全被利用,与此同时,通过控制O3气泡颗粒的大小实现流体的混合,追求污染物对O3需求反应动力学与过程混合动力学之间的协调,克服保持一定的O3平衡浓度下的气泡升流作用所带来的吹脱现象的发生,除此之外,更为重要的是,催化剂界面上的传质-反应-分离过程如何与气液传质过程的吻合成为关键。
综合以上讨论,认为气液混合及其介入的反应与分离过程原理与技术应用已经渗透到化工、能源和环保等领域,今后应该更多关注原理-技术-应用之间在传质尺度、反应器尺度与介质对象应用尺度等不同维度中的规律传递,从特性发现、共性开发与系统集成方面等多功能上必须追求同步的发展。
| [1] |
Pighini S, Ventura M, Miglietta F, et al. Dissolved greenhouse gas concentrations in 40 lakes in the Alpine area[J]. Aquatic Sciences, 2018, 80(3): 32. DOI:10.1007/s00027-018-0583-2 |
| [2] |
Yan X, Xu X, Ji M, et al. Cyanobacteria blooms:A neglected facilitator of CH4 production in eutrophic lakes[J]. Science of the Total Environment, 2018, 651: 466-474. |
| [3] |
Li S, Bush R T, Santos I R, et al. Large greenhouse gases emissions from China's lakes and reservoirs[J]. Water Research, 147: 13-24. DOI:10.1016/j.watres.2018.09.053 |
| [4] |
Mader M, Roberts A M, Porst D, et al. River re charge versus O2 supply from the unsaturated zone in shallow riparian groundwater:A case study from the Selke River (Germany)[J]. Science of the Total Environment, 2018, 634: 374-381. DOI:10.1016/j.scitotenv.2018.03.230 |
| [5] |
Lipczynska-Kochany E. Effect of climate change on humic substances and associated impacts on the quality of surface water and groundwater:A review[J]. Science of the Total Environment, 2018, 640-641: 1548-1565. DOI:10.1016/j.scitotenv.2018.05.376 |
| [6] |
Maragkaki A E, Fountoulakis M, Gypakis A, et al. Pilot-scale anaerobic co-digestion of sewage sludge with agro-industrial by-products for increased biogas production of existing digesters at wastewater treatment plants[J]. Waste Management, 2017, 59: 362-370. DOI:10.1016/j.wasman.2016.10.043 |
| [7] |
Zhai Y, Pérez-Díaz I M, Diaz J T. Viability of commercial cucumber fermentation without nitrogen or air purging[J]. Trends in Food Science & Technology, 2018, 81: 185-192. |
| [8] |
Mcaleer E B, Coxon C E, Richards K G, et al. Groundwater nitrate reduction versus dissolved gas production:A tale of two catchments[J]. Science of the Total Environment, 2017, 586: 372-389. DOI:10.1016/j.scitotenv.2016.11.083 |
| [9] |
Pan J, Ma J, Wu H, et al. Simultaneous removal of thiocyanate and nitrogen from wastewater by autotrophic denitritation process[J]. Bioresource Technology, 2018, 267: 30-37. DOI:10.1016/j.biortech.2018.07.014 |
| [10] |
Pan J, Wei C, Fu B, et al. Simultaneous nitrite and ammonium production in an autotrophic partial denitrification and ammonification of wastewaters containing thiocyanate[J]. Bioresource Technology, 2018, 252: 20-27. DOI:10.1016/j.biortech.2017.12.059 |
| [11] |
Mansouri L, Tizaoui C, Geissen S, et al. A comparative study on ozone, hydrogen peroxide and UV based advanced oxidation processes for efficient removal of diethyl phthalate in water[J]. Journal of Hazardous Materials, 2019, 363: 401-411. DOI:10.1016/j.jhazmat.2018.10.003 |
| [12] |
Wang Q, Zhang Y, Wang H, et al. A pathway of free radical generation via copper corrosion and its application to oxygen and ozone activation for the oxidative destruction of organic pollutants[J]. Research on Chemical Intermediates, 2018, 44(12): 7391-7410. DOI:10.1007/s11164-018-3562-2 |
| [13] |
Compernolle S, Müller J F. Henry's law constants of diacids and hydroxypolyacids:Recommended values[J]. Atmospheric Chemistry and Physics Discussions, 2013, 13: 25125-25156. DOI:10.5194/acpd-13-25125-2013 |
| [14] |
Razdan N K, Koshy D M, Prausnitz J M. Henry's constants of persistent organic pollutants by a group-contribution method based on scaled-particle theory[J]. Environmental Science & Technology, 2017, 51(21): 12466-12472. |
| [15] |
Sousa J M, Ferreira A L, Fagg D P, et al. Temperature dependence of the Henry's law constant for hydrogen storage in NaA zeolites:a Monte Carlo simulation study[J]. Journal of Nanoscience & Nanotechnology, 2012, 12(8): 6785-6791. |
| [16] |
Schnabel T, Vrabec J, Hasse H. Henry's law constants of methane, nitrogen, oxygen and carbon dioxide in ethanol from 273 to 498 K:Prediction from molecular simulation[J]. Fluid Phase Equilibria, 2005, 233(2): 134-143. DOI:10.1016/j.fluid.2005.04.016 |
| [17] |
Fenclová D, Blahut A, Vrbka P, et al. Temperature dependence of limiting activity coefficients, Henry's law constants, and related infinite dilution properties of C4-C6 isomeric n-alkyl ethanoates/ethyl n-alkanoates in water. Measurement, critical compilation, correlation, and recommended data[J]. Fluid Phase Equilibria, 2014, 375: 347-359. DOI:10.1016/j.fluid.2014.05.023 |
| [18] |
Zhang Y, Yu P, Luo Y. Absorption of CO2 by amino acid-functionalized and traditional dicationic ionic liquids:Properties, Henry's law constants and mechanisms[J]. Chemical Engineering Journal, 2013, 214: 355-363. DOI:10.1016/j.cej.2012.10.080 |
| [19] |
王凯雄, 姚铭. 亨利定律及其在环境科学与工程中的应用[J]. 浙江树人大学学报:人文社会科学版, 2004, 4(6): 85-89. Wang Kaixiong, Yao Ming. A critical review of Henry's law and its application in environmental science and engineering[J]. Journal of Zhejiang Shuren University:Social Science Edition, 2004, 4(6): 85-89. (in Chinese) |
| [20] |
付晓泰, 王振平, 卢双舫. 气体在水中的溶解机理及溶解度方程[J]. 中国科学:B辑, 1996(2): 124-130. Fu Xiaotai, Wang Zhenping, Lu Shuangfan. Dissolution mechanism and solubility equation of gas in water[J]. Science in China:Series B, 1996(2): 124-130. (in Chinese) |
| [21] |
Tao D. Role of bubble size in flotation of coarse and fine particles-A review[J]. Separation Science & Technology, 2005, 39(4): 741-760. |
| [22] |
Edzwald J K. Dissolved air flotation and me[J]. Water Research, 2010, 44(7): 2077-2106. DOI:10.1016/j.watres.2009.12.040 |
| [23] |
Prakash R, Majumder S K, Singh A. Flotation technique:Its mechanisms and design parameters[J]. Chemical Engineering and Processing-Process Intensification, 2018, 127: 249-270. DOI:10.1016/j.cep.2018.03.029 |
| [24] |
Kim T, Park H, Han M. Design parameter estimations for adjustable bubble size in bubble generating system[J]. Water Science and Technology, 2017, 77(1): 1-6. |
| [25] |
王晨, 王振波, 李娅萱, 等. 溶气释放头对气浮气泡生成的影响[J]. 过滤与分离, 2016, 26(4): 9-14. Wang Chen, Wang Zhenbo, Li Yaxuan, et al. Effect of dissolved air release head on the generation of flotation bubbles[J]. Journal of Filtration & Separation, 2016, 26(4): 9-14. DOI:10.3969/j.issn.1005-8265.2016.04.003 (in Chinese) |
| [26] |
Cho S, Kim J, Chun J, et al. Ultrasonic formation of nanobubbles and their zeta-potentials in aqueous electrolyte and surfactant solutions[J]. Colloids and Surfaces A:Physicochemical and Engineering Aspects, 2005, 269(1): 28-34. |
| [27] |
Kim H, Choi T. On Bayesian estimation of regression models subject to uncertainty about functional constraints[J]. Journal of the Korean Statistical Society, 2014, 43(1): 133-147. DOI:10.1016/j.jkss.2013.03.005 |
| [28] |
Temesgen T, Bui T T, Han M, et al. Micro and nanobubble technologies as a new horizon for water-treatment techniques:A review[J]. Advances in Colloid and Interface Science, 2017, 246: 40-51. DOI:10.1016/j.cis.2017.06.011 |
| [29] |
Xing Y, Gui X, Cao Y. The hydrophobic force for bubble-particle attachment in flotation-A brief review[J]. Physical Chemistry Chemical Physics, 2017, 19(36): 24421-24435. DOI:10.1039/C7CP03856A |
| [30] |
Okada K, Akagi Y, Kogure M, et al. Effect on sur face charges of bubbles and fine particles on air flotation process[J]. Canadian Journal of Chemical Engineering, 2010, 68(3): 393-399. |
| [31] |
Okada K, Akagi Y, Kogure M, et al. Effect on sur face charges of bubbles and fine particles on air flotation process[J]. Canadian Journal of Chemical Engineering, 2010, 68(3): 393-399. |
| [32] |
Han M, Kim M K, Shin M S. Generation of a positively charged bubble and its possible mechanism of formation[J]. Journal of Water Supply:Research and Technology-Aqua, 55(7/8): 471-478. |
| [33] |
岳鹏.压力溶气法溶气罐内压及释放器倾角对气泡影响的研究[D].西安: 西安石油大学, 2017 Yue Peng. The study on the influence of the dissolved air pressure and release angle on bubbles with the method of dissolved air flotation[D]. Xi'an: Xi'an Shiyou University, 2017(in Chinese) http://cdmd.cnki.com.cn/Article/CDMD-10705-1017177455.htm |
| [34] |
Li C, Zhen K, Hao Y, et al. Effect of dissolved gases in natural water on the flotation behavior of coal[J]. Fuel, 2018, 233: 604-609. DOI:10.1016/j.fuel.2018.06.104 |
| [35] |
Okada K, Akagi Y, Kogure M, et al. Effect on surface charges of bubbles and fine particles on air flotation process[J]. Canadian Journal of Chemical Engineering, 2010, 68(3): 393-399. |
| [36] |
Kim M S, Kwak D H. Effect of zeta potential on collision-attachment coefficient and removal efficiency for dissolved carbon dioxide flotation[J]. Environmental Engineering Science, 2016, 34(4): 272-280. |
| [37] |
桑义敏, 陈家庆, 韩严和, 等. 气浮工艺中气泡-颗粒碰撞效率和理论计算模型研究[J]. 工业水处理, 2014, 34(2): 5-10. Sang Yimin, Chen Jiaqing, Han Yanhe, et al. Bubble-Particle collision efficiency in flotation and its theoretical model[J]. Industrial Water Treatment, 2014, 34(2): 5-10. DOI:10.3969/j.issn.1005-829X.2014.02.002 (in Chinese) |
| [38] |
Wang G, Ge L, Mitra S, et al. A review of CFD modelling studies on the flotation process[J]. Minerals Engineering, 2018, 127: 153-177. DOI:10.1016/j.mineng.2018.08.019 |
| [39] |
Brabcová Z, Karapantsios T, Kostoglou M, et al. Bubble-particle collision interaction in flotation systems[C]//Colloids and Surfaces A: Physicochemical and Engineering Aspects A Collection of Papers Presented at the 10th Eufoam Conference, Greece: Thessaloniki, 2014
|
| [40] |
王静超, 马军, 刘芳. 气浮接触区气泡-颗粒碰撞效率影响因素分析[J]. 工业水处理, 2008(9): 66-69. Wang Jingchao, Ma Jun, Liu Fang. Influential factor analysis of the bubble-particle collision efficiency in the contact zone of dissolved air flotation[J]. Industrial Water Treatment, 2008(9): 66-69. DOI:10.3969/j.issn.1005-829X.2008.09.020 (in Chinese) |
| [41] |
刘颖, 金鑫, 金鹏康, 等. 溶气气浮的微气泡影响因素及其与絮体的结合特性[J]. 中国给水排水, 2018, 34(5): 1-5. Liu Ying, Jin Xin, Jin Pengkang, et al. Characteristics of microbubbles and microbubble-flocs in dissolved ozone flotation process[J]. China Water & Wastewater, 2018, 34(5): 1-5. (in Chinese) |
| [42] |
陈翼孙, 胡斌. 气浮净水技术的研究与应用[M]. 上海: 上海科学技术出版社, 1983.
|
| [43] |
王培艳.平流型加压溶气气浮水处理的研究[D].郑州: 郑州大学, 2013 Wang Peiyan. Research on advection-type pressurized dissolved air flotation water treatment[D]. Zhengzhou: Zhengzhou University, 2013(in Chinese) http://cdmd.cnki.com.cn/Article/CDMD-10459-1013257415.htm |
| [44] |
吴海珍, 韦聪, 于哲, 等. 废水好氧生物处理工艺中氧的传质与强化的理论与实践[J]. 化工进展, 2018, 37(10): 4033-4043. Wu Haizhen, Wei Cong, Yu Zhe, et al. Oxygen dissolution and gas liquid mass transfer in aerobic biological wastewater treatment:Theory and practice[J]. Chemical Industry and Engineering Progress, 2018, 37(10): 4033-4043. (in Chinese) |
| [45] |
杨频, 高飞. 生物无机化学原理[M]. 北京: 科学出版社, 2002.
|
| [46] |
韦朝海, 汝旋, 杨兴舟, 等. 污水生物处理基于氧调控的节能策略[J]. 化工进展, 2018, 37(11): 4121-4134. Wei Chaohai, Ru Xuan, Yang Xingzhou, et al. Energy saving strategy based on oxygen control in wastewater bio-treatment[J]. Chemical Industry and Engineering Progress, 2018, 37(11): 4121-4134. (in Chinese) |
| [47] |
Kasprzyk-Hordern B, Ziolek M, Nawrocki J. Catalytic ozonation and methods of enhancing molecular ozone reactions in water treatment[J]. Applied Catalysis B Environmental, 2003, 46: 639-669. DOI:10.1016/S0926-3373(03)00326-6 |
| [48] |
Kwong C W, Chao C, Hui K, et al. Catalytic ozonation of toluene using zeolite and MCM-41 materials[J]. Environmental Science & Technology, 2008, 42(22): 8504-8509. |
| [49] |
Zhao L, Ma W, Ma J, et al. Characteristic mechanism of ceramic honeycomb catalytic ozonation enhanced by ultrasound with triple frequencies for the degradation of nitrobenzene in aqueous solution[J]. Ultrasonics Sonochemistry, 2014, 21(1): 104-112. DOI:10.1016/j.ultsonch.2013.06.005 |
| [50] |
Nawrocki J. Catalytic ozonation in water:Controversies and questions. Discussion paper[J]. Applied Catalysis B:Environmental, 2013, 142/143: 465-471. DOI:10.1016/j.apcatb.2013.05.061 |
| [51] |
Nawrocki J, Kasprzyk-Hordern B. The efficiency and mechanisms of catalytic ozonation[J]. Applied Catalysis B:Environmental, 2010, 99(1): 27-42. |
| [52] |
Zhang T, Croué J. Catalytic ozonation not relying on hydroxyl radical oxidation:A selective and competitive reaction process related to metal carboxylate complexes[J]. Applied Catalysis B:Environmental, 2014, 144: 831-839. DOI:10.1016/j.apcatb.2013.08.023 |
| [53] |
Hama-Aziz K H, Miessner H, Mueller S, et al. Comparative study on 2, 4-dichlorophenoxyacetic acid and 2, 4-dichlorophenol removal from aqueous solutions via ozonation, photocatalysis and non-thermal plasma using a planar falling film reactor[J]. Journal of Hazardous Materials, 2018, 343: 107-115. DOI:10.1016/j.jhazmat.2017.09.025 |
| [54] |
Bradu C, Magureanu M, Parvulescu V I. Degradation of the chlorophenoxyacetic herbicide 2, 4-D by plasma-ozonation system[J]. Journal of Hazardous Materials, 2017, 336: 52-56. DOI:10.1016/j.jhazmat.2017.04.050 |
| [55] |
Liu M, Preis S, Kornev I, et al. Pulsed corona discharge for improving treatability of coking wastewater[J]. Journal of Environmental Sciences, 2018, 64: 306-316. DOI:10.1016/j.jes.2017.07.003 |
| [56] |
Kovačević V V, Dojčinović B P, Jović M S, et al. Measurement of reactive species generated by dielectric barrier discharge in direct contact with water in different atmospheres[J]. Journal of Physics D Applied Physics, 2017, 50(155205): 19. DOI:10.1088/1361-6463/aa5fde |
| [57] |
Yao K, Chi Y, Wang F, et al. The effect of microbubbles on gas-liquid mass transfer coefficient and degradation rate of COD in wastewater treatment[J]. Water Science & Technology, 2016, 73(8): 1969-1977. |
| [58] |
Zheng T, Wang Q, Zhang T, et al. Microbubble enhanced ozonation process for advanced treatment of wastewater produced in acrylic fiber manufacturing industry[J]. Journal of Hazardous Materials, 2015, 287: 412-420. DOI:10.1016/j.jhazmat.2015.01.069 |
| [59] |
Zhao L, Ma J, Sun Z, et al. Mechanism of heterogeneous catalytic ozonation of nitrobenzene in aqueous solution with modified ceramic honeycomb[J]. Applied Catalysis B Environmental, 2009, 89(3): 326-334. |
| [60] |
Bing J, Hu C, Zhang L. Enhanced mineralization of pharmaceuticals by surface oxidation over mesoporous γ-Ti-Al2O3 suspension with ozone[J]. Applied Catalysis B Environmental, 2017, 202: 118-126. DOI:10.1016/j.apcatb.2016.09.019 |
| [61] |
Phoochinda W, White D A. Removal of algae using froth flotation[J]. Environmental Technology, 2003, 24(1): 87-96. DOI:10.1080/09593330309385539 |
| [62] |
Kurniawati H A, Ismadji S, Liu J C. Microalgae harvesting by flotation using natural saponin and chitosan[J]. Bioresource Technology, 2014, 166: 429-434. DOI:10.1016/j.biortech.2014.05.079 |
| [63] |
Singh G, Patidar S K. Microalgae harvesting techniques:A review[J]. Journal of Environmental Management, 2018, 217: 499-508. |
| [64] |
Wu Z, Zhu Y, Huang W, et al. Evaluation of flocculation induced by pH increase for harvesting microalgae and reuse of flocculated medium[J]. Bioresource Technology, 2012, 110: 496-502. DOI:10.1016/j.biortech.2012.01.101 |
| [65] |
Vandamme D, Foubert I, Fraeye I, et al. Flocculation of Chlorella vulgaris induced by high pH:Role of magnesium and calcium and practical implications[J]. Bioresource Technology, 2012, 105: 114-119. DOI:10.1016/j.biortech.2011.11.105 |
| [66] |
Tian Z, Wang C, Ji M. Full-Scale dissolved air flotation (DAF) equipment for emergency treatment of eutrophic water[J]. Water Science & Technology, 2018, 77(7): 1802-1809. |
| [67] |
王振波, 陈阿强, 杨文三, 等. 溶气气浮分离乳化油的影响因素及其作用机制[J]. 水处理技术, 2017, 43(4): 27-30. Wang Zhenbo, Chen Aqiang, Yang Wensan, et al. The influence factors and mechanisms of emulsified oil separation by dissolved air flotation[J]. Technology of Water Treatment, 2017, 43(4): 27-30. (in Chinese) |
| [68] |
Chawaloesphonsiya N, Guiraud P, Painmanakul P. Analysis of cutting-oil emulsion destabilization by aluminum sulfate[J]. Environmental Technology, 2017, 39(11): 1450-1460. |
| [69] |
Zhang Q, Liu S, Yang C, et al. Bioreactor consisting of pressurized aeration and dissolved air flotation for domestic wastewater treatment[J]. Separation and Purification Technology, 2014, 138: 186-190. DOI:10.1016/j.seppur.2014.10.024 |
| [70] |
Zheng T, Wang Q, Shi Z, et al. Separation of pollutants from oil-containing restaurant wastewater by novel microbubble air flotation and traditional dissolved air flotation[J]. Separation Science & Technology, 2015, 50(16): 2568-2577. |
| [71] |
Khan O, Madhuranthakam C M R, Douglas P, et al. Optimized PID controller for an industrial biological fermentation process[J]. Journal of Process Control, 2018, 71: 75-89. DOI:10.1016/j.jprocont.2018.09.007 |
| [72] |
Manser R, Gujer W, Siegrist H. Consequences of mass transfer effects on the kinetics of nitrifiers[J]. Water Research, 2005, 39(19): 4633-4642. DOI:10.1016/j.watres.2005.09.020 |
| [73] |
Laanbroek H J, Gerards S. Competition for limiting amounts of oxygen between Nitrosomonas europaea and Nitrobacter winogradskyi grown in mixed continuous cultures[J]. Archives of Microbiology, 1993, 159(5): 453-459. DOI:10.1007/BF00288593 |
| [74] |
Jiang H, Liu G, Ma Y, et al. A pilot-scale study on start-up and stable operation of mainstream partial nitrification-anammox biofilter process based on online pH-DO linkage control[J]. Chemical Engineering Journal, 2018, 350: 1035-1042. DOI:10.1016/j.cej.2018.06.007 |
| [75] |
Zou Y, Xu X, Wang X, et al. Achieving efficient nitrogen removal and nutrient recovery from wastewater in a combining simultaneous partial nitrification, anammox and denitrification (SNAD) process with a photobioreactor (PBR) for biomass production and generated dissolved oxygen (DO) recycling[J]. Bioresource Technology, 2018, 268: 539-548. DOI:10.1016/j.biortech.2018.08.015 |
| [76] |
高春娣, 李浩, 焦二龙, 等. 交替好氧缺氧短程硝化及其特性[J]. 北京工业大学学报, 2015, 41(1): 116-122. Gao Chundi, Li Hao, Jiao Erlong, et al. Alternate oxic-anoxic mode realizing nitrification and its characterization[J]. Journal of Beijing University of Technology, 2015, 41(1): 116-122. (in Chinese) |
| [77] |
Wang H, Song Q, Wang J, et al. Simultaneous nitrification, denitrification and phosphorus removal in an aerobic granular sludge sequencing batch reactor with high dissolved oxygen:Effects of carbon to nitrogen ratios[J]. Science of the Total Environment, 2018, 642: 1145-1152. DOI:10.1016/j.scitotenv.2018.06.081 |
| [78] |
赵群英, 田敏, 李侃. DO浓度及其空间分布对Orbal氧化沟去除污染物效果[J]. 净水技术, 2018, 37(8): 87-89. Zhao Qunying, Tian Min, Li Kan. Effect of DO concentration and the spatial distribution on pollutants removal by orbal oxidation ditch[J]. Water Purification Technology, 2018, 37(8): 87-89. (in Chinese) |
| [79] |
Zhang F, Wei C, Hu Y, et al. Zinc ferrite catalysts for ozonation of aqueous organic contaminants:Phenol and bio-treated coking wastewater[J]. Separation and Purification Technology, 2015, 156: 625-635. DOI:10.1016/j.seppur.2015.10.058 |
| [80] |
Wei C, Zhang F, Hu Y, et al. Ozonation in water treatment:The generation, basic properties of ozone and its practical application[J]. Reviews in Chemical Engineering, 2016, 33(1): 49-89. |
| [81] |
韩涛.焦化废水尾水的臭氧深度处理及残余臭氧的利用[D].广州: 华南理工大学, 2015 Han Tao. Advance treatment of coking wastewater effluent with ozone and the utilization of residual ozone[D]. Guangzhou: South China University of Technology, 2015(in Chinese) http://cdmd.cnki.com.cn/Article/CDMD-10561-1016705956.htm |
| [82] |
Bollmann A F, Seitz W, Prasse C, et al. Occurrence and fate of amisulpride, sulpiride, and lamotrigine in municipal wastewater treatment plants with biological treatment and ozonation[J]. Journal of Hazardous Materials, 2016, 320: 204-215. DOI:10.1016/j.jhazmat.2016.08.022 |
| [83] |
Lin C, Liao J, Wu H, et al. Mechanism of ozone oxidation of polycyclic aromatic hydrocarbons during the reduction of coking wastewater sludge[J]. CLEAN-Soil, Air, Water, 2016, 44(11): 1499-1507. DOI:10.1002/clen.v44.11 |
| [84] |
Zhang F, Wei C, Wu K, et al. Mechanistic evaluation of ferrite AFe2O4 (A=Co, Ni, Cu, and Zn) catalytic performance in oxalic acid ozonation[J]. Applied Catalysis A:General, 2017, 547: 60-68. DOI:10.1016/j.apcata.2017.08.025 |
| [85] |
Ma C, Yuan P, Jia S, et al. Catalytic micro-ozonation by Fe3O4 nanoparticles@cow-dung ash for advanced treatment of biologically pre-treated leachate[J]. Waste Management, 2019, 83: 23-32. DOI:10.1016/j.wasman.2018.10.045 |
| [86] |
Yang J, Li J, Zhu J, et al. A novel design for an ozone contact reactor and its performance on hydrodynamics, disinfection, bromate formation and oxidation[J]. Chemical Engineering Journal, 2017, 328: 207-214. DOI:10.1016/j.cej.2017.06.165 |
| [87] |
Zheng T, Zhang T, Wang Q, et al. Advanced treatment of acrylic fiber manufacturing wastewater with a combined microbubble-ozonation/ultraviolet irradiation process[J]. RSC Advances, 5(95): 77601-77609. DOI:10.1039/C5RA14575A |
 2019, Vol. 36
2019, Vol. 36