面对能源紧缺、环境污染等重大问题, 迫切需要开发新型绿色能源。铝-空气电池具有安全、廉价、环保的特点, 是近年新型绿色能源的发展方向之一[1]。铝合金作为铝-空气电池的负极, 也是铝-空气电池研究的重点。但是铝合金作为阳极材料用于化学电源存在2个问题[2], 一是合金表面会形成氧化膜进而造成电极电位下降, 二是在碱性电解液中合金表面会发生析氢腐蚀造成利用率的下降。西南铝厂所加工的Al-Ga-Bi-Pb合金平均电位为-1.44 V[3]。稀土由于其具有特殊的电子层结构[4], 因此在铝合金的合金化中能够发挥一些特殊的作用。Wang等[5]使用硝酸铈作为缓蚀剂得到了较好的缓蚀效果, 齐公台等[6]探讨了稀土对于Al-5Zn-0.015In-1Mg-0.1Sn合金中偏析相的组成的影响, 并且其电化学活性良好, 阳极利用率达到98.24%, 唐有根等[7]通过向Al-5Zn-0.05In-0.1Sn铝合金基体中添加不同量的稀土元素Ce, 发现稀土具有良好的细化晶粒效果, 能够有效地改善铝合金阳极的耐腐蚀性能。从合金化的角度, 我们认为要开发高性能的铝合金负极材料, 首先需明了单一元素对金属铝电化学活性以及自腐蚀性能的影响规律, 在此基础上再进一步深入探讨铝基合金中不同元素间的交互作用对金属铝电化学活性以及自腐蚀性能的影响规律, 已有的研究表明, 稀土元素对金属材料的性能有着独特的影响。我们采用基于量子化学原理的Material Studio软件, 针对不同种类的稀土-铝合金体系进行了详细的体系能量计算, 同时也计算了目前文献报道的用于铝合金负极材料合金化的相关合金元素与铝形成合金体系的能量, 发现稀土元素铈与铝形成的合金体系的能量均较目前文献报道的合金元素各自与铝形成合金体系的能量低。上述理论计算结果表明, 稀土元素铈适合用于对金属铝的合金化。
本研究通过添加不同含量的稀土Ce元素, 并测试其在3 mol/L KOH、3%NaCl溶液中的电化学性能, 来研究稀土对于铝-空气电池负极的影响。
1 试验部分 1.1 铝合金的熔炼与电极制备在井式炉内使用石英坩埚, 分别熔炼1、2、3、4、5和6号6种合金, 相应的Ce的质量分数为0.2%、0.5%、0.8%、1.0%、1.2%和1.5%, 具体成分列于表 1。
| 试样 | 1号 | 2号 | 3号 | 4号 | 5号 | 6号 |
| w(Al)/% | 99.8 | 99.5 | 99.2 | 99.0 | 98.8 | 98.5 |
| w(Ce)/% | 0.2 | 0.5 | 0.8 | 1.0 | 1.2 | 1.5 |
将铝锭在辊压机上进行塑性变形, 形变量为90%。将上述合金制备成厚1 mm, 工作区域为1×1 cm2的铝片, 用AB胶将非工作区域封装。工作区使用400、600、1 000和2 000号砂纸逐级打磨, 无水乙醇去油, 蒸馏水洗涤后备用。
1.2 极化曲线和交流阻抗的测定电化学测试在上海辰华电化学工作站CHI660B上进行。采用三电极两回路体系, 以钌钛网为辅助电极, 参比电极为氧化汞电极。测试溶液为3 mol/L的KOH、质量分数为3%的NaCl。
极化曲线测试时的电位扫描速率为0.5 mV/s, 起扫电位为开路电位, 终止电位为-0.8 V, 测试温度为25 ℃, 测试过程使用磁力转子搅拌器搅拌溶液。交流阻抗测试电位在开路电位正60 mV处, 测试频率范围为0.01 Hz~100 MHz。
1.3 利用率的测定预先称量铝合金电极的质量, 然后在30 mA/cm2下恒电流放电60 min, 取出电极, 使用蒸馏水冲洗, 超声, 吹干, 称重。放电时的温度为25 ℃。计算公式见式(1)和(2):
| $ H = \frac{{{M_2}}}{{{M_0}-{M_1}}} \times 100\% $ | (1) |
| $ {M_2} = \frac{{QM}}{{ZF}} $ | (2) |
式(1)和(2)中, H为利用率; M2为纯用于放电反应消耗铝合金的质量, g; M0为放电前铝合金的质量, g; M1为放电后铝合金的质量, g; Q为放电过程中流过电池的电荷, C; M为摩尔质量, g/mol; Z为铝经过电化学反应生成铝离子所失去的电子数; F为法拉第常数, 数值为96 485 C/mol。
1.4 成分及结构表征使用美国FEI公司Nanosem 430热场发射扫描电子显微镜对按1.3方法测试后的铝合金表面在加速电位为15 kV的条件下进行测试, 放大倍率为800倍。并使用其自带的EDX设备对合金表面做面扫描分析。
1.5 放电性能的测定使用CT2001A型LAND电池测试系统测试阳极合金的放电性能, 以30 mA恒电流进行放电测试, 记录放电电压随时间的变化。其中空气电极由催化层(MnO2为催化剂)、防水层(乙炔黑+PTFE)、集流体(40目Ni网)压制而成。
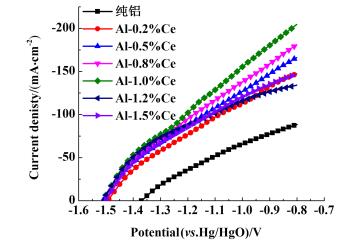
2 结果与讨论 2.1 极化曲线分析图 1为按表 1所炼制Al-Ce合金以及纯铝按1.2中的测试方法测得的极化曲线。
|
| 图 1 不同Ce元素含量的Al-Ce合金的阳极极化曲线 Figure 1 Anodic polarization curves of Al-Ce alloys with different contents of Ce |
| |
由图 1可知, 在所研究的元素Ce含量范围内, 随着电极电位的正移, Al-Ce合金的电流密度不断增大。使用图 1各样品的开路电位与对应的稀土Ce的含量作图, 结果如图 2所示。
|
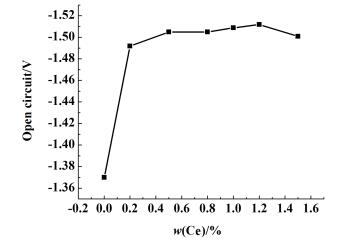
| 图 2 不同Ce含量Al-Ce合金的开路电位 Figure 2 Open circuit of Al-Ce alloys on different Ce concentrations |
| |
从图 2中可以看出, 与纯铝相比Al-Ce合金的开路电位明显负移, 纯铝的开路电位为-1.37 V, 而Al-Ce合金的开路电位在-1.5 V左右。稀土Ce的加入使开路电位负移。使用图 1中各样品-1.2 V电流密度与对应稀土Ce的浓度作图, 结果如图 3所示。

|
| 图 3 不同Ce含量Al-Ce合金的-1.2 V处电流密度 Figure 3 Current density at -1.2 V of Al-Ce alloys on different Ce concentrations |
| |
由图 3可以看出, 纯铝的电流密度为-35 mA·cm-2, 稀土Ce的添加能够明显提高铝阳极的电流密度。电流密度随着Ce含量的增加而增大, 电流密度最大时, Ce的含量为1%, 为-103.90 mA·cm-2。继续添加稀土Ce会导致电流密度的降低。电流密度越大, 说明电极的电化学活性越好[8], 因此以上结果说明稀土元素Ce能有效的改善纯铝的电化学性能。
2.2 利用率分析按1.3中的方法测试了Al-Ce合金利用率, 结果列于表 2。
| 试样 | w(Ce)/% | 利用率/ % | 自腐蚀速率/ (mg·min-1·cm-2) |
| 1 | 0.2 | 65.2 | 0.2343 |
| 2 | 0.5 | 67.5 | 0.2188 |
| 3 | 0.8 | 70.2 | 0.2007 |
| 4 | 1.0 | 72.3 | 0.1865 |
| 5 | 1.2 | 68.4 | 0.2129 |
| 6 | 1.5 | 63.4 | 0.2464 |
| 纯铝 | 0 | 49.5 | 0.3400 |
由表 2可以看出, 纯铝的自腐蚀速率为0.3400 mg·min-1·cm-2, 而添加少量的稀土w(Ce)为0.2%, 即可使铝合金的自腐蚀速率下降到0.2343 mg·min-1·cm-2。继续增加合金中Ce的含量, 合金的自腐蚀速率进一步下降。当w(Ce)为1%时, 合金的自腐蚀速率最低为0.1865 mg·min-1·cm-2。但是, 过量的Ce反而会引起合金自腐蚀速率的下降。
2.3 交流阻抗分析对Al-1.0%Ce合金与Al-1.5%Ce合金按1.2中的方法进行了交流阻抗测试, 测试结果如图 4与图 5所示。
|
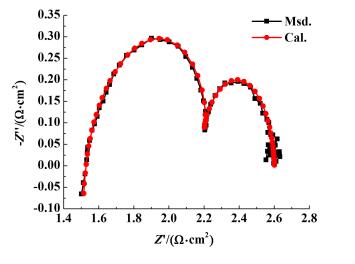
| 图 4 纯Al的交流阻抗谱图 Figure 4 EIS patterns of pure Al |
| |

|
| 图 5 Al-1.0%Ce合金的交流阻抗谱图 Figure 5 EIS patterns of alloy Al-1.0%Ce |
| |
图 4与图 5均由高频区的感抗弧以及中低频区的2个容抗弧组成。高频区的感抗弧是合金在电解液中析氢腐蚀引起的, 而容抗弧则是有界面双电层电容与电化学反应电阻的弛豫过程引起的[9]。2个容抗弧说明发生在Al-Ce表面的电化学反应分两步进行, 反应方程式如下:
| $ {\rm{Al}}-x{{\rm{e}}^-} \to {\rm{A}}{{\rm{l}}^{x + }} $ | (3) |
| $ {\rm{A}}{{\rm{l}}^{x + }}-(3-x){{\rm{e}}^-} \to {\rm{A}}{{\rm{l}}^{3 + }} $ | (4) |
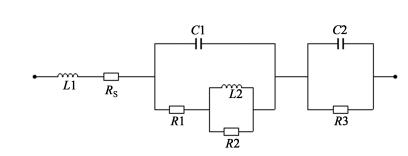
为了更好地分析图 4、图 5和图 6, 使用图 7所示的电路图对交流阻抗谱进行了模拟。图 7中电感L1可能是与析氢反应相关, RS代表溶液电阻; R1和C1分别表示反应(3)中电荷转移阻抗以及双电层电容; L2和R2表示氧化层的相关参数[10]。C2和R3表示反应(4)的相关参数。
|
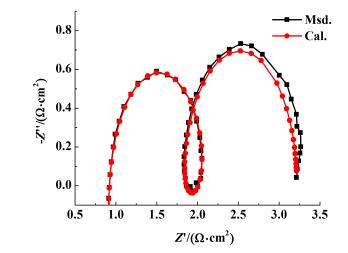
| 图 6 Al-1.5%Ce合金的交流阻抗谱图 Figure 6 EIS patterns of alloy Al-1.5%Ce |
| |
使用软件ZSimDemo以及图 7所示电路图对交流阻抗谱图进行拟合, 拟合结果与交流阻抗谱图列于图 4、图 5和图 6, 由图 4、图 5和图 6可以看出拟合良好, 这说明图 7中所示电路图的合理性。图 7中各电子原件拟合结果列于表 3。
| 项目 | 纯铝 | 4号 | 6号 |
| L1/(×10-7H·cm2) | 9.9840 | 10.6000 | 13.3300 |
| RS/(Ω·cm2) | 1.4880 | 1.1880 | 0.8928 |
| C1/(×10-3F·cm-2) | 0.0370 | 0.0319 | 0.0464 |
| n1 (0 < n < 1) | 0.7095 | 1.0000 | 0.9932 |
| R1/(Ω·cm2) | 0.9224 | 0.8413 | 0.9222 |
| L2/(×10-4H·cm2) | 2.6160 | 1.3290 | 1.4560 |
| R2 (Ω·cm2) | 0.4649 | 0.2074 | 0.3064 |
| C2/(×10-3F·cm-2) | 57.9900 | 29.2900 | 16.8700 |
| n2 (0 < n < 1) | 0.9672 | 1.0000 | 1.0000 |
| R3/(Ω·cm2) | 0.3911 | 0.6419 | 1.4010 |
纯铝的氧化层相关参数L2与R2均大于Al-1.0%Ce和Al-1.5%Ce合金, 这说明稀土Ce的加入能够阻止放电过程中金属铝的钝化。Al-1.5%Ce合金的R1与R3均大于Al-1.0%Ce合金, 这说明Al-1.0%Ce合金的电化学反应进行得更容易, 这也验证了Al-1.0%Ce合金具有更好的电化学活性这一实验现象。另外, 对于Al-1.0%Ce合金R3小于R1, 这说明第1步反应是总反应的速度控制步骤。而Al-1.5%Ce合金的R3大于R1, 这说明第2步反应为速度控制步骤。由此可见, 过量的稀土Ce的加入使得整个反应体系的速度控制步骤发生了改变, 这可能是Al-1.5%Ce电化学活性大幅下降的主要原因。
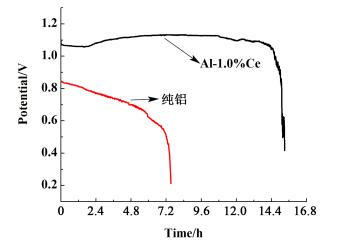
2.4 放电性能图 8为纯铝以及Al-1.0%Ce合金按照1.5中方法测得的放电性能图。
|
| 图 8 纯铝与Al-1.0%Ce合金放电曲线 Figure 8 Discharge behavior of pure Al and Al-1.0%Ce alloy |
| |
由图 8可知, 纯铝恒电流放电时, 性能较差, 电压不稳, 并且放电时间较短, 仅为7 h。添加稀土Ce之后, 放电效果提升较大, 放电时间延长至14 h, 并且电压较稳, 放电电压为1.1 V左右, 最大电压为1.13 V, 稳定时间为10 h。这表明Ce的添加阻止了铝合金的钝化, 带来了长时间的连续放电。
2.5 SEM分析对按1.3的方法进行测试后的Al-Ce合金进行了SEM测试以及EDX面扫描测试, 结果见图 9。从图 9中可以看出, Al-1.0%Ce合金表面平整, 而Al-1.5%Ce合金表面出现了“小坑”, 因此变得粗糙。Al-1.5%Ce合金在进行放电的过程中, 在合金表面出现了点腐蚀, 因此在SEM图中出现了“小坑”。点腐蚀是Al-1.5%Ce合金利用率下降的主要原因。

|
| 图 9 Al-Ce合金SEM图像:a)Al-1.0%Ce, b) Al-1.5%Ce及面扫描图像:c) Al-1.0%Ce, d) Al-1.5%Ce Figure 9 SEM images of Al-Ce alloys:a) Al-1.0%Ce, b) Al-1.5%Ce and EDX surface scanning:c) Al-1.0%Ce, d) Al-1.5%Ce |
| |
从面扫描图像中可以看出稀土Ce主要分布在晶界处, 因此, Al-1.5%Ce合金中Ce在晶界处分布更密集, 这造成了严重的点腐蚀, 由图 1a)、图 1b)、图 1c)和图 1d)中可以看出, 在图 1b)中腐蚀较严重的地方Ce的分布也更密集, 图 1a)中也有类似的情况, 但是不明显。这说明过量的稀土Ce引起了Al-Ce表面的点腐蚀, 从而导致利用率下降。
3 结论1) 向Al中加入稀土Ce能够改变Al的电化学活性, 电流密度随着稀土Ce的加入而增大, 在稀土Ce质量分数为1%时, 电化学活性最好。继续加入Ce会导致电化学活性降低。
2) 过量的Ce会使电化学反应的阻力增大, 并改变反应的速度控制步骤, 这会导致电化学活性降低。
3) 过量的Ce会导致放电过程在电极表面出现点腐蚀, 使得Al-Ce合金的利用率下降。
| [1] |
Wang H, Leung D Y C, Leung M K H. Energy analysis of hydrogen and electricity production from aluminum-based processes[J]. Applied Energy, 2012, 90(1): 100-105. DOI:10.1016/j.apenergy.2011.02.018 |
| [2] |
Egan D R, León C P D, Wood R J K, et al. Developments in electrode materials and electrolytes for aluminium-air batteries[J]. Journal of Power Sources, 2013, 236(25): 293-310. |
| [3] |
王剑. 电池用铝合金阳极材料的开发[J]. 铝加工, 1998, 21(2): 56-59. Wang Jian. Development of aluminum alloy anode material for battery[J]. Aluminium Fabrication, 1998, 21(2): 56-59. (in Chinese) |
| [4] |
康福伟, 王丽萍, 张显有, 等. 微量稀土元素对工业纯铝电阻率的影响[J]. 哈尔滨理工大学学报, 2003, 8(6): 112-114. Kang Fuwei, Wang Liping, Zhang Xianyou, et al. Effects of microscale rare earth elements on electrical resistiviy of industral pure aluminium[J]. Journal of Harbin University of Science and Technology, 2003, 8(6): 112-114. DOI:10.3969/j.issn.1007-2683.2003.06.035 (in Chinese) |
| [5] |
Wang D, Li H, Liu J, et al. Evaluation of AA5052 alloy anode in alkaline electrolyte with organic rare-earth complex additives for aluminium-air batteries[J]. Journal of Power Sources, 2015, 293: 484-491. DOI:10.1016/j.jpowsour.2015.05.104 |
| [6] |
齐公台, 张盈盈. 电池用含稀土铝合金阳极性能的研究[J]. 稀有金属, 2004, 28(6): 1010-1014. Qi Gongtai, Zhang Yingying. RE-Bearing aluminum alloys anode for alkaline battery[J]. Chinese Journal of Rare Metals, 2004, 28(6): 1010-1014. DOI:10.3969/j.issn.0258-7076.2004.06.012 (in Chinese) |
| [7] |
唐有根, 韩红涛, 谢正和, 等. 稀土Ce掺杂铝合金阳极的结构和电化学性能[J]. 中南大学学报:自然科学版, 2006, 37(4): 737-741. Tang Yougen, Han Hongtao, Xie Zhenghe, et al. Structure and electrochemical performance of Al alloy anode doped with rare earth Ce[J]. Journal of Central South University:Science and Technology, 2006, 37(4): 737-741. (in Chinese) |
| [8] |
霍佳磊, 王为. 葡萄糖对铝合金电极电化学活性及自腐蚀的影响[J]. 中国表面工程, 2016, 29(2): 37-42. Huo Jialei, Wang Wei. Effects of glucose on electrochemical activity and self-corrosion of aluminum alloy anode[J]. China Surface Engineering, 2016, 29(2): 37-42. (in Chinese) |
| [9] |
Ma J, Wen J, Gao J, et al. Performance of Al-1Mg-1Zn-0.1Ga-0.1Sn as anode for Al-air battery[J]. Electrochimica Acta, 2014, 129: 69-75. DOI:10.1016/j.electacta.2014.02.080 |
| [10] |
Cho Y J, Park I J, Lee H J, et al. Aluminum anode for aluminum-air battery-Part I:Influence of aluminum purity[J]. Journal of Power Sources, 2015, 277: 370-378. DOI:10.1016/j.jpowsour.2014.12.026 |
 2018, Vol. 35
2018, Vol. 35