微胶囊是指由天然或人工合成的高分子材料制成的具有聚合物囊壁的微型容器或包装物[1-2], 其直径通常在1~1 000 μm范围内[3]。对物质进行微胶囊化, 可以改善和提高物质的外观及其性质, 提高物质的使用效率, 因此微胶囊技术被广泛应用于医药、农业、化工、化妆品和其他日用品的生产中[4]。
制备微胶囊的方法主要有化学法、物理法、物理化学法3大类[5-6]。在每大类方法中依据不同的操作工艺又可以进一步分成若干种制备方法。其中以凝聚法、界面聚合法和原位聚合法应用最广。
随着微胶囊技术的发展与广泛应用, 对微胶囊的大小、单分散性、球形度及膜特性等要求不断提高。传统微胶囊制备技术通常需要高温条件、需要使用破坏性溶剂或反应剧烈, 且制备的微胶囊粒径较大、分布较宽[7], 已不能满足高标准、高效率的应用要求。
近几十年来, 一种制备微胶囊的新方法—微流体技术出现在采矿、动力、环境、医药、化工、石油、核能和冶金等领域, 成为研究的热点。这种新型制备微胶囊的方法与传统方法相比, 具有粒径形态可控、单分散性好、绿色环保低耗等优势, 可以说是针对传统制备方法的弱势而出现的[8]。
一般微流控技术所用的微通道芯片是一体的, 不可拆卸, 制备工艺要求严格, 价格昂贵。鉴于微通道尺寸在10~300 μm间, 即使通过微通道的流体经过严格的过滤, 在操作过程中也易发生堵塞, 特别当用到强挥发性有机溶剂时, 更易因溶质析出而发生堵塞, 给使用带来不便。本研究研制1个可拆卸的T型微通道装置, 只在T型管口处通道的尺寸较小, 而且由2个可拆卸的管路连接而成, 克服了传统微通道芯片中易堵塞, 不能使用挥发性有机溶剂的缺点, 拓宽了该技术的适用范围。此外, 实验中使用的可视化数码摄像系统也方便了过程观察和记录, 加强了实验的可控性。
本研究利用简易的微通道, 结合界面聚合法制备单分散性好、大小可控的聚酰胺微胶囊。在此基础上综合以往研究对影响微胶囊粒径大小及分布的主要因素进行了较系统的研究。
1 实验部分 1.1 试剂与仪器环己烷(分析纯); 三氯甲烷(分析纯); 1, 6-己二胺(分析纯); 二乙烯三胺(分析纯); 对苯二甲酰氯(分析纯); 失水山梨醇单油酸酯(Tween80, 分析纯); 聚乙烯醇(分析纯), 均为天津市元立化工有限公司。实验装置和简易微通道(图 1); 注射泵, W0109-1B, 保定兰格恒流泵有限公司; 高速摄像机, I-SPEEDTR, 英国奥林巴斯公司; 倒置金属显微镜, DMILM, 日本Leica公司; 扫描电镜, Phenom Pure, 荷兰Phenom-World公司; 马尔文粒度分析仪, Mastersize3000, 英国Malvern Instruments公司。

|
| 图 1 实验装置和T型微通道 Figure 1 Experiment equipment and T microchannel |
| |
实验装置如图 1所示。
其中的微通道由不锈钢管(内径Di=0.33 mm)和透明的聚氯乙烯(内径Di=1.4 mm)黏合而成, 在制作的过程中要尽量确保不锈钢管与聚氯乙烯管的水平轴线垂直。
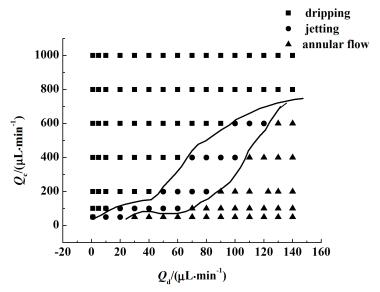
1.2.2 微通道内流体行为的研究实验中, 通过调节连续相和分散相的流量来研究微通道内流体的行为, 并确定形成液滴的适宜流量。其中连续相为含聚乙烯醇1%(质量体积比)的水溶液, 分散相吐温80的含量为0.5%(体积比), 环己烷、三氯甲烷的体积比为3:2。根据实验结果做出不同流量对应的流型图, 结果如图 2所示。
|
| 图 2 有机相与水相形成的流型图 Figure 2 The flow map of oil phase and water phase |
| |
从图 2中可以看出, 在实验选取的流量范围内, 主要观察到了液滴流(dripping)、射流(jetting)和环状流(annular flowing), 其中的环状流可以细分为毛细管流(treading)和管状流(tubing)。在图 2的左上方是液滴流区, 中间部分是射流区, 右下方是环流区, 与标准的微通道的流型分布研究结果基本一致[9]。
1.2.3 微胶囊的制备水相的配制:按需在蒸馏水中加入一定量的聚乙烯醇、己二胺和二乙烯三胺, 搅拌溶解。有机相的配制:按需将一定量的对苯二甲酰氯和吐温80溶于一定体积比的环己烷和三氯甲烷有机溶剂中并混合均匀。
通过设定好流量的恒流泵将水相和有机相分别作为连续相和分散相注入微通道内, 在交叉口处形成液滴的同时反应生成聚酰胺膜, 形成聚酰胺微胶囊。
1.3 分析方法形貌测试:将制备好的微胶囊乳液滴于载玻片上, 盖上盖玻片, 用倒置金属显微镜(DMILM, 日本Leica公司)观察其外观形态; 在SEM(Phenom Pure, 荷兰Phenom-World)样品台上贴上双面胶, 将少许微胶囊产品的粉末撒于双面胶上, 吹去多余的粉末, 然后喷金, 用SEM观察微胶囊的形貌。
粒径测试:对制备的微胶囊乳液取样, 用马尔文粒度分析仪(Mastersize3000, 英国Malvern Instruments公司)测定微胶囊的粒径大小及其分布。
1.4 聚酰胺微胶囊平均粒径和分散系数的计算聚酰胺微胶囊平均粒径和分散系数的计算公式分别为:
| $ \bar d = \sum {f_i}{d_i}/100 $ | (1) |
| $ \varepsilon = \sqrt {\sum {{({d_i}-\bar d)}^2}/100} /\bar d $ | (2) |
式(1)和(2)中, d为微胶囊的平均直径, di为单个微胶囊的直径, fi为直径为di的微胶囊所占总数的百分数, ε为分散系数。
2 结果与讨论 2.1 微胶囊的形貌图 3的微胶囊是在聚乙烯醇的含量为1%(质量体积比), 环己烷和三氯甲烷的体积比为3:2, 吐温80的含量为0.5%(体积比), 单体配比(酰氯:胺)为1:2, 分散相和连续相的流量分别为20和1 000 μL·min-1条件下制备的。

|
| 图 3 聚酰胺微胶囊的形貌图 Figure 3 The morphology of polyamide microcapsules |
| |
图 3a)的光学显微镜照片放大倍数是50倍, 从图 3a)中可以看出, 所制得的聚酰胺微胶囊具有良好的球形度, 且分布均匀。为了进一步确定聚酰胺微胶囊的形态和表观形貌, 在扫描电镜下进行观察, 结果如图 3b)所示, 其放大倍数是260倍。从图 3b)中可以看出, 聚酰胺微胶囊基本为球形, 而且表面较光滑, 但出现了褶皱和塌陷的现象。
2.2 有机相配比对微胶囊粒径的影响界面聚合法制备聚酰胺微胶囊中, 胺在有机相的分配系数对聚合度有很大的影响, 从而能够影响微胶囊的生成。由于胺的分配系数随着有机相的改变而改变, 因此, 改变有机相的组成即环己烷和三氯甲的体积配比能够影响微胶囊的粒径大小和分布。结果如表 1所示。
| V(环己烷)/ V(三氯甲烷) | 平均粒径/μm | 实验结果 |
| 4/1 | 667 | 颗粒较小, 大小不均匀, 放置后有破裂 |
| 3/2 | 859 | 颗粒较大, 壁厚且光滑 |
| 1/4 | 未形成微胶囊 |
由表 1可知, 减少环己烷的量, 微胶囊的尺寸变大, 但三氯甲烷的量太多, 会影响微胶囊的形成甚至导致不能形成微胶囊。可能是胺相对较易溶于三氯甲烷, 随着三氯甲烷用量的增加, 胺的扩散速率快, 反应速率太快导致的。
2.3 表面活性剂用量对微胶囊粒径的影响在微胶囊的制备过程中, 表面活性剂被高度浓缩在分散相形成的液滴表面, 且聚合反应就发生在靠近有机相的一侧, 这要求表面活性剂能把有机相中的单体分散到液滴的表面。2种单体在界面上进行缩聚反应, 生成微胶囊的膜, 包裹芯材形成微胶囊[10]。
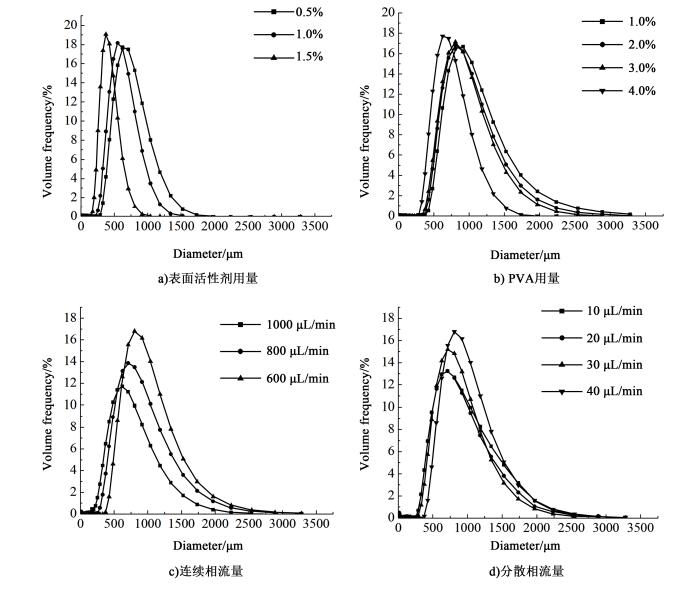
据有关文献知, 非离子表面活性剂和阴离子表面活性剂较适合界面聚合法制备微胶囊[11]。适合于O/W型乳液的表面活性剂的HLB值在8~18之间, 吐温80的HLB值为15, 满足这一条件。吐温80用量对微胶囊粒径的影响如图 4a)所示。
|
| 图 4 影响微胶囊尺寸的主要因素 Figure 4 The influence of main factors on microcapsules size |
| |
从图 4a)中可以看出, 随着表面活性剂用量的增多, 微胶囊的平均粒径减小, 粒径分布变窄。这是由于吐温80的用量越大, 乳化得越充分, 形成的乳液越稳定、液滴越小, 使得以液滴为模板形成的微胶囊的粒径越小, 分布越均匀。
2.4 保护胶体用量对微胶囊粒径的影响在两相分散体系中, 液滴间的吸引力与2种液体的界面张力有直接的关系, 这取决于温度和表面活性剂的浓度。高浓度的表面活性剂能够显著降低表面张力, 产生小的液滴。同样, 如果不在水相介质中加入水溶性保护胶体, 则形成的微胶囊的产率会急剧下降, 当加入保护胶体的量较少时, 形成的乳状液体系会不稳定[12]。本研究中, 高分子保护胶体聚乙烯醇用来抑制分散液滴的聚集。聚乙烯醇对微胶囊粒径的影响如图 4b)所示。
从图 4b)中可以看出, 随着保护胶体用量从1%增加至4%, 微胶囊的平均粒径减小且尺寸分布变窄。可能是由于随着保护胶体用量的增加, 连续相的黏度也增大, 一方面使乳化液更加稳定, 减少其聚集的机会, 另一方面减小了体系的交换, 降低了反应速率, 使形成的微胶囊的粒径变小, 粒径分布均匀。
2.5 连续相流量对微胶囊粒径的影响固定分散相的流量为20 μL·min-1, 在滴状流的流速范围内调节连续相的流量为1 000、800和600 μL·min-1, 考察连续相流量对微胶囊粒径的影响, 结果如图 4c)所示。
从图 4c)中可以看出随着连续相流量的增大, 微胶囊的粒径减小、分布变窄, 各流量下的平均粒径分别为572、734和859 μm。分散系数分别为0.39%、0.47%和0.57%。
2.6 分散相流量对微胶囊粒径的影响固定连续相的流量为1 000 μL·min-1, 在滴状流的流量范围内调节分散相的流量为10、20、30和40 μL·min-1, 考察分散相流量对微胶囊粒径的影响, 结果如图 4 d)所示。
从图 4d)中可以看出随着分散相流量的减小, 微胶囊的粒径减小、分布变窄, 各流量下的平均粒径分别为605、655、735和830 μm。分散系数分别为0.39%、0.42%、0.46%和0.48%。
3 结论利用T型通道微流控技术进行乳化, 能够精确操控微尺度流体并高效均一地进行分散, 从而制备了单分散性好, 大小可控, 粒径在微米范围内, 呈较规则球形的聚酰胺微胶囊。利用此技术制备的微胶囊分散系数ε在0.2%~0.5%范围内(分散系数<5%), 远优于传统制备方法。通过实验分析, 可以得出制备过程各因素对微胶囊的粒径有一定的影响但影响程度各不相同。乳化剂吐温80的用量、保护胶体的用量和两相流量对微胶囊粒径大小及其分布影响较大。其影响规律为:随着吐温80和聚乙烯醇用量的增加, 连续相流量增大和分散相流量的减小, 微胶囊粒径减小、分布变窄。
| [1] |
张杏梅, 韩小龙. 界面聚合法制备聚酰胺微胶囊的缓释性能研究[J]. 化学工业与工程技术, 2008, 29(6): 1-4. Zhang Xingmei, Han Xiaolong. Study on release property of polyamide microcapsules by interfacial polymerization[J]. Journal of Chemical Industry & Engineering, 2008, 29(6): 1-4. DOI:10.3969/j.issn.1006-7906.2008.06.001 (in Chinese) |
| [2] |
Simon B. Microencapsulation:Methods and industrial application[M]. Washington: ACS Book & Journals Division, 1996.
|
| [3] |
Wang W, Zhang M, Chu L. Functional polymeric microparticles engineered from controllable microfluidic emulsions[J]. Accounts of Chemical Research, 2014, 47(2): 373-384. DOI:10.1021/ar4001263 |
| [4] |
徐冬梅, 张可达, 王平, 等. 微胶囊的功能及应用[J]. 精细石油化工, 2003(6): 55-59. Xu Dongmei, Zhang Keda, Wang Ping, et al. Functions and applications of microcapsules[J]. Specialty Petrochemicals, 2003(6): 55-59. (in Chinese) |
| [5] |
许燕霞, 赵亮, 刘媛, 等. 微胶囊的制备技术[J]. 上海化工, 2005, 30(3): 21-24. Xu Yanxia, Zhao Liang, Liu Yuan, et al. The preparation of microcapsule[J]. Shanghai Chemical Industry, 2005, 30(3): 21-24. DOI:10.3969/j.issn.1004-017X.2005.03.008 (in Chinese) |
| [6] |
郝红, 梁正国. 微胶囊技术及其应用[J]. 上海化工, 2002, 22(3): 60-63. Hao Hong, Liang Zhengguo. Microcapsulation technology and its application[J]. Modern Chemical Industry, 2002, 22(3): 60-63. (in Chinese) |
| [7] |
刘袖洞, 何洋, 刘群, 等. 微胶囊及其在生物医学领域的应用[J]. 科学通报, 2000, 45(23): 2476-2485. Liu Xiudong, He Yang, Liu Qun, et al. Microcapsules and its application in biomedical field[J]. Chinese Science Bulletin, 2000, 45(23): 2476-2485. DOI:10.3321/j.issn:0023-074X.2000.23.003 (in Chinese) |
| [8] |
高存梅, 范勇恒, 罗炫, 等. 微流体技术制备功能性微型颗粒的研究进展[J]. 材料导报A:综述篇, 2012, 26(3): 124-128. Gao Cunmei, Fan Yongheng, Luo Xuan, et al. Research progress on preparation of functional microparticles by microfluidic technology[J]. Materials Review A:Review, 2012, 26(3): 124-128. (in Chinese) |
| [9] |
Nisisako T, Torii T, Higuchi T. Novel microreactors for functional polymer beads[J]. Chemical Engineering Journal, 2004, 101: 23-29. DOI:10.1016/j.cej.2003.11.019 |
| [10] |
Morgan P W. Condensation polymers by Interfacial and solution methods[M]. New York: Interscience, 1965.
|
| [11] |
Walter H H. Process for the preparation of microcapsules: US, 5837290[P]. 1988-11-17
|
| [12] |
Alexandridous S, Kiparissides C. Production of oil-containing polyterephthalamide microcapsules by interfacial polymerization. An experimental investigation of the effect of process variables on the microcapsule size distribution[J]. Microencapsulation, 1994, 11(6): 603-614
|
 2018, Vol. 35
2018, Vol. 35





