2. 天津大学化工学院, 天津 300072
2. School of Chemical Engineering and Technology Tianjin University, Tianjin 300072, China
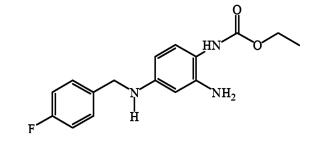
癫痫是一种普遍的严重性神经病学障碍疾病, 以脑神经元异常放电引起反复痫性发作为特征, 全世界已经有5亿确诊的病例[1]。瑞替加滨(Retigabine, Ⅰ), 是一种新型的抗癫痫药物[2], 用于成人难治性癫痫部分性发作的辅助治疗[3], 并于2011年分别在欧盟及美国获准上市销售。瑞替加滨与现有的抗癫痫药物相比具有独特的药理作用, 通过打开特定的神经电压门控钾离子通道, 导致钾离子电流的超极化转变并降低神经元细胞的兴奋性[4]。除了在KCNQ通道上的主要活动, 瑞替加滨还对神经元细胞的兴奋性具有稳定作用[5]。瑞替加滨的化学结构式见图 1。
|
| 图 1 瑞替加滨的化学结构式 Figure 1 The chemical structural formula of Retigabine |
| |
文献报道的瑞替加滨(或其二盐酸盐)合成方法主要有4种:1)以2-硝基-1, 4-苯二胺为原料, 以酸离子交换树脂为催化剂, 与对氟苯甲醛缩合得到亚胺, 再经2次还原后, 与氯甲酸乙酯反应制得瑞替加滨[6-7]。2)以N-(4-氨基苯基)氨基甲酸乙酯为起始原料, 经氨基保护、硝化、脱保护, 得到N-(4-氨基-2-硝基苯基)氨基甲酸乙酯, 再与对氟苯甲醛缩合得到亚胺, 然后再经亚胺还原、硝基还原得到瑞替加滨[8-12]。3)以4-氟-1, 2-二硝基苯为原料, 在非质子溶剂中, 碱性条件下与对氟苄胺发生缩合反应, 生成4-(4-氟苄基胺基)-1, 2-二硝基苯, 经还原、酰化后制得瑞替加滨[13-14]。4)以5-氟-2-硝基苯胺为原料, 与对氟苄胺反应后, 再经雷尼镍(Raney Ni)催化氢化还原硝基后, 与氯甲酸乙酯反应后再与6 mol/L乙醇盐酸溶液反应制得瑞替加滨二盐酸盐[15]。第一种方法缺点在于使用醛, 容易引入杂质。第二种方法缺点在于氨基保护及脱保护过程繁琐, 整体反应步骤较长, 经济性较差, 不利于工业化生产。第三种方法缺点在于起始原料4-氟-1, 2-二硝基苯难以获得。第四种方法的缺点在于邻苯二胺中间体在空气中不稳定, 容易被氧化, 需要在惰性气体保护下制备中间体, 操作复杂而且操作弹性小, 同时所制备的最终产物为瑞替加滨二盐酸盐而非目标产物瑞替加滨。
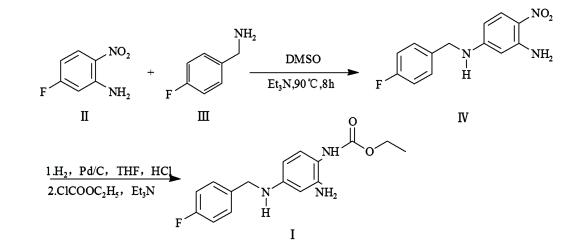
基于对以上合成方法的分析, 我们认为方法四如果解决了中间体不稳定的问题及后处理成盐问题, 将是比较好的工业化路线。本研究在方法四的基础上进行工艺改进。以5-氟-2-硝基苯胺为起始原料, 与4-氟苄胺经亲核取代反应制得2-氨基-4-(4-氟苄胺基)硝基苯, 然后将还原反应与酰化反应合并在同一个反应器中进行, 不经分离直接制备高质量的最终产物瑞替加滨, 合成路线见图 2。该合成工艺方法操作简单, 原料易得, 产品纯度高, 有利于工业化生产。
|
| 图 2 瑞替加滨合成工艺路线 Figure 2 Synthesis route of Retigabine |
| |
YRT-3熔点仪(天津大学精密仪器厂); VARIAN INOVA 500 MHz型核磁共振仪(美国瓦里安公司); micrOTOF-Q Ⅱ质谱(德国Bruker Daltonics公司); Vario Micro cube元素分析仪(德国Elementar公司); Agilent 1260液相色谱系统; 4-氟苄胺(工业品, 金坛市华阳科技有限公司); 5-氟-2-硝基苯胺(工业品, 常州市晔泰精细化工研究所); 三乙胺, 乙醇, N, N-二甲基甲酰胺, 四氢呋喃, 石油醚, 乙酸乙酯, 浓盐酸(AR, 天津市江天化工技术有限公司); 二甲基亚砜, 正己烷(AR, 天津光复精细化工研究所); 氯甲酸乙酯(北京偶合科技有限公司); Pd/C(质量分数为5%, 西安凯立化工有限公司); 高纯氢; 高纯氮(天津市河西区六方高科技气体供应站); 其他试剂均为分析纯; 实验用水为去离子水。
1.2 合成方法 1.2.1 2-氨基-4-(4-氟苄胺基)硝基苯(Ⅳ)的合成将5-氟-2-硝基苯胺(49.93 g, 0.320 mol), 4-氟苄胺(48.03 g, 0.384 mol), 三乙胺(Et3N, 42.1 g, 0.416 mol), 依次加入至反应瓶中, 搅拌下加入二甲基亚砜(DMSO, 84 mL), 升温至轻微回流, 温度89.8 ℃, 并在此温度下反应8 h, TLC跟踪监测。反应结束后, 体系自然降温至室温, 将反应液转移至烧杯中, 机械搅拌下缓慢加入去离子水500 mL, 剧烈搅拌后, 进行抽滤, 得黄色固体, 滤饼用去离子水100 mL洗涤, 抽滤。将固体收集到反应瓶中, 加入80 mL乙醇, 机械搅拌, 并升温至回流, 保温搅拌0.5 h后, 降至室温, 抽滤, 得黄色固体, 滤饼再用100 mL乙醇进行洗涤, 抽滤, 真空干燥, 得黄色固体(Ⅳ)77.65 g, 收率92.94%(以5-氟-2-硝基苯胺计)。1H NMR (500 MHz, DMSO-d6), δ:7.72(d, 1H, Ar-H10, J=9.5 Hz), 7.46(t, 1H, NH, J=5.5 Hz), 7.31~7.36(t、s, 4H, Ar-H3、NH2, J=7.5 Hz, J=6.0 Hz), 7.16(t, 2H, Ar-H2, J=9.0 Hz, J=8.0 Hz), 6.07(d, 1H, Ar-H11, J=8.0 Hz), 5.83(s, 1H, Ar-H7), 4.27(d, 2H, Ar-H5, J=5.0 Hz); 13C NMR (125 MHz, DMSO-d6), δ:162.0(d, J=241 Hz), 154.7, 149.8, 135.5, 129.8(d, J=8 Hz), 127.9, 122.9, 115.8(d, J=33 Hz), 107.1, 94.2, 45.7;ESI-MS m/z: 262.4[M+H]+。
1.2.2 N-[2-氨基-4-(4-氟苄胺基)苯基]氨基甲酸乙酯(瑞替加滨, Ⅰ)的合成将2-氨基-4-(4-氟苄胺基)硝基苯(Ⅳ)(65.28 g, 0.25 mol), 四氢呋喃(THF, 326.5 mL)分别加入到反应瓶中, 机械搅拌, 升温至60 ℃, 使溶解。然后降温至40 ℃, 加入钯碳催化剂[质量分数为5%的Pd/C, 15.73 g(湿质量)]。氮气、氢气各置换3次, 然后通入氢气开始氢化(氢压约101.325 kPa), 反应过程中内温保持在35 ℃, 保温氢化约3 h(直至氢气压力不再变化), 冰浴降温至15 ℃, 开始滴加盐酸水溶液(浓盐酸39.17 g用水稀释至96 mL), 滴加过程中控制温度小于20 ℃。滴加完成后, 继续保温(15~20 ℃)氢化, 使用TLC监控氢化反应终点, 展开剂为V(石油醚):V(乙酸乙酯)=2:1。
氢化反应完成后, 氮气置换氢气3次, 氮气保护降温至15 ℃, 常压下开始滴加三乙胺(Et3N, 70.54 g), 滴加完毕后, 温度降至2 ℃, 开始滴加氯甲酸乙酯四氢呋喃溶液(氯甲酸乙酯27.13 g用四氢呋喃稀释到265 mL), 温度控制在5 ℃以下, 滴加完成后, 保温搅拌15 min。升温至25 ℃, 保温搅拌0.5 h。过滤, 滤液减压蒸馏, 蒸除四氢呋喃。得到青黑色小颗粒固体和水的混合物。混合物加入350 mL去离子水, 搅拌15 min。过滤, 滤饼用150 mL去离子水洗涤2次, 得青黑色固体。加入乙醇150 mL, 减压蒸馏除水, 重复2次, 得黑色固体粉末(Ⅰ, 瑞替加滨粗品)72.94 g。
1.2.3 后处理过程取上述瑞替加滨粗品, 加入反应瓶中, 加入混合溶剂[V(乙醇):V(正己烷)=1:1, 185 mL], 加热至回流, 保温15 min, 降温至10 ℃, 保温搅拌3 h, 抽滤, 滤饼用混合溶剂[V(乙醇):V(正己烷)=1:2, 75 mL]打浆洗涤3次, 抽滤, 滤饼经真空干燥得灰白色固体45.48 g。该固体经混合溶剂(乙醇/正己烷)精制, 得最终产物(Ⅰ, 瑞替加滨)35.16 g, 全部合成工艺总收率43.09%(以5-氟-2-硝基苯胺计), 熔点141.2~142.0 ℃; 质量分数99.9%。元素分析, C16H18FN3O2实测值(计算值, %):w(C)=63.45, 63.24(63.35), w(H)=6.26, 6.23(5.98), w(N)=13.83, 13.79(13.85), w(F)=6.31, 6.29(6.27)。1H NMR (500 MHz, DMSO-d6), δ:8.16(s, 1H, NHCO), 7.35(dd, 2H, Ar-H3, J=6.0 Hz, J=7.5 Hz), 7.11(t, 2H, Ar-H2, J=9.0 Hz, J=8.5 Hz), 6.72(s, 1H, Ar-H10), 5.95(s, 1H, Ar-H10), 5.83~5.89 (d, t, 2H, NH, Ar-H11, J=8.5 Hz), 4.54(s, 2H, NH2), 4.17(dd, 4H, CH2, J=6.0 Hz, J=7.5 Hz), 4.01~4.05(dd, 2H, H13, J=6.5 Hz, J=13 Hz)1.19(s, 3H, CH3); 13C NMR(125 MHz, DMSO-d6), δ:161.7(d, J=240 Hz), 155.8, 147.7, 144.1, 137.5(d, J=2.9 Hz), 129.5(d, J=8.1 Hz), 127.7, 115.6(d, J=21 Hz), 113.7, 102.3, 99.7, 60.4, 46.5, 15.3;ESI-MS m/z: 304.1455[M+H]+。
2 结果与讨论 2.1 2-氨基-4-(4-氟苄胺基)硝基苯(Ⅳ)合成反应条件的确定文献[15]所述的工艺在惰性气体环境下进行, 反应温度为60~70 ℃, 反应时间为30 h。后处理为真空蒸馏DMSO溶剂后, 加入盐酸溶液溶解残渣, 再以甲苯萃取结晶, 最终2-氨基-4-(4-氟苄胺基)硝基苯(Ⅳ)的收率为85%。本研究针对该反应进行了惰性气体影响、反应溶剂、反应温度、反应时间及物料物质的量之比的研究, 发现惰性气体对反应没有明显影响, 同时确定了最适宜反应条件, 改进了后处理方法, 简化了操作步骤, 将反应时间缩短到7.5 h, 反应收率提高到了约93%。
2.1.1 反应溶剂的确定2-氨基-4-(4-氟苄胺基)硝基苯(Ⅳ)的合成反应为典型的亲核取代反应, 一般采用极性非质子性溶剂, 文献[15]中所采用的溶剂为DMSO, 为了寻求更好的反应溶剂, 本研究选择了几种常见的溶剂, 进行了对比试验, 实验结果见表 1。
| 溶剂 | 反应温度/℃ | 反应时间/h | 收率/% (HPLC) | 杂质个数 |
| DMF | 90 | 8.5 | 48.27 | 较多 |
| 丙酮 | 回流 | 8.0 | 0.72 | |
| 乙腈 | 回流 | 8.5 | 29.67 | 较多 |
| 甲醇 | 回流 | 9.5 | 19.00 | 较多 |
| DMSO | 90 | 7.5 | 94.27 | 较少 |
| 注:物料比n(5-氟-2-硝基苯胺):n(4-氟苄胺):n(三乙胺)=1.0:1.8:2.2。 | ||||
由表 1可以看出, 以二甲基甲酰胺(DMF)为溶剂, 在90 ℃反应, 反应速度虽然比较快, 但是杂质较多, 中间体收率较低; 以乙腈、甲醇为溶剂, 在回流温度下反应, 反应8.5~9.5 h后, 原料仍有剩余, 而且杂质也较多, 生成的中间体收率较低。而以丙酮为溶剂, 反应几乎没有进行, 可能是由于沸点低导致反应难以发生。而以DMSO作为反应溶剂, 反应7.5 h后的试验结果最好, 反应完全, 杂质少, 生成的中间体收率较高。
2.1.2 反应物料比的确定本研究对物料比对反应的影响进行了研究, 试验结果见表 2。
| n1:n2:n3 | 反应完全与否(TLC监测) |
| 1.0:1.0:2.2 | 否 |
| 1.0:1.2:2.2 | 能 |
| 1.0:1.1:2.2 | 能 |
| 1.0:1.2:1.2 | 否 |
| 1.0:1.2:1.4 | 能 |
| 1.0:1.2:1.3 | 能 |
| 注:1.n1:n2:n3=n(5-氟-2-硝基苯胺):n(4-氟苄胺):n(三乙胺); 2.溶剂:DMSO; 反应温度:90 ℃; 反应时间:7.5 h。 | |
文献[15]所述工艺物料比为n(5-氟-2-硝基苯胺):n(4-氟苄胺):n(三乙胺)=1:1.8:2.2, 4-氟苄胺和三乙胺用量都较大, 有必要进行物料比的研究, 寻找合适条件以减少原料4-氟苄胺和缚酸剂三乙胺的使用量。试验过程中发现, 先保持n1:n3=1.0:2.2, 当物料比n1:n2=1.0:1.0时, 反应缓慢; 当物料比n1:n2=1.0:1.1或1.2时, 可以反应完全, 为了增加反应的稳定性, 先确定n1与n2的物料比为1.0:1.2。当物料比n1:n2:n3=1.0:1.2:1.2时, 反应速度相对缓慢, 物料有剩余, 为加快反应速度, 提高三乙胺的用量; 当物料比n1:n2:n3=1.0:1.2:1.3或1.4时, 反应结果相当, 且反应起始原料5-氟-2-硝基苯胺可以反应完全, 因此确定最适宜物料比为5-氟-2-硝基苯胺:4-氟苄胺:三乙胺=1.0:1.2:1.3, 此时反应收率为92.94%。
2.1.3 反应温度的确定本研究考察了反应温度对取代反应的影响。试验结果见表 3。
| 反应温度/℃ | 收率/% (HPLC) | 5-氟-2-硝基苯胺转化率/% | 杂质个数 |
| 50 | 57.10 | 57.53 | 2 |
| 70 | 83.11 | 85.75 | 2 |
| 90 | 94.27 | 96.66 | 3 |
| 注:1.溶剂:DMSO; 反应时间:7.5 h; 2.物料比n(5-氟-2-硝基苯胺):n(4-氟苄胺):n(三乙胺)=1.0:1.8:2.2。 | |||
反应过程中发现, 在50 ℃下, 反应比较容易进行, 未见有较大杂质出现, 但反应时间较长, 物料反应不完全。随着温度的升高, 在70 ℃下, 反应速度加快, 同时没有新的杂质出现, 但反应7.5 h后, 5-氟-2-硝基苯胺仍有剩余。反应温度到达90 ℃时, 反应快速进行, 新增杂质较少, 物料在7.5 h后反应完全。由于此温度下已经有新杂质产生, 反应温度和反应转化率符合要求, 而再升高温度会使杂质增加。因此, 综合考虑, 确定反应温度为90 ℃。
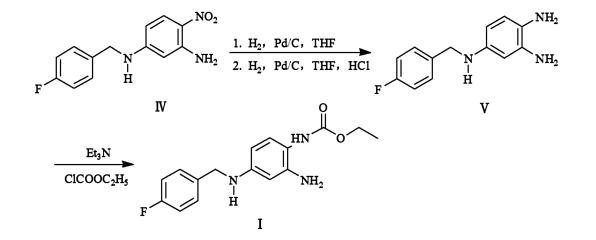
2.2 一锅法合成N-[2-氨基-4-(4-氟苄胺基)苯基]氨基甲酸乙酯(瑞替加滨, Ⅰ)反应条件的确定文献[15]所述瑞替加滨二盐酸盐的合成工艺以Raney Ni为催化剂, 常压下进行氢化反应, 反应完成后, 在惰性气体保护下过滤。然后先后滴加氯甲酸乙酯二氧六环溶液及6 mol/L乙醇盐酸溶液。析出固体, 过滤, 重结晶, 得到瑞替加滨二盐酸盐。由于加氢还原后中间体V为1个苯三胺类结构, 在空气中不稳定, 容易被氧化, 因此在过滤过程中容易产生氧化杂质而使最终产品难以达到质量要求。本研究将加氢反应和酰化反应在同1个反应器中进行, 两步不经分离直接合成最终产物瑞替加滨, 简化了工艺, 减少了杂质的生成。工艺如图 3所示。
|
| 图 3 还原反应与酰化反应 Figure 3 The reduction reaction and acylation |
| |
还原反应为硝基化合物还原加氢成氨基化合物, 通常还原方法有铁粉还原、氯化亚锡还原、催化氢化等, 基于环保的考虑, 目前工业上多采用催化氢化还原的方式。常用的加氢还原催化剂有Raney Ni和Pd/C 2种, 文献[15]由于是分步法, 要获得二胺中间体后再进行下一步反应, 以Raney Ni为催化剂, 但Raney Ni不适合作为一锅法的催化剂, 一方面Raney Ni会同反应过程中产生的盐酸反应而失活, 另一方面催化剂和盐酸的反应产物会在产品中引入重金属杂质。因此本研究选择Pd/C作为还原催化剂, 由于Pd/C催化剂在本反应中可以回收再用, 有效降低了生产成本。
本反应采用了分步氢化的方法, 进行分步氢化的原因在于还原后产物为二胺, 由于二胺类的化合物和Pd/C催化剂吸附力强, 不容易从催化剂表面解吸, 导致反应速度减慢, 阻碍还原反应的进一步进行, 从而使原料不能完全反应, 而较长的反应速度也会使副产物产生的风险提高。因此采用分段氢化还原, 在氢化还原进行一段时间后, 加入盐酸中和二胺, 使产物从催化剂表面解吸下来, 促使反应完全。另外, 由于盐酸的加入活化了Pd/C催化剂, 如果仍然维持原有温度, 会因为反应过于剧烈而导致杂质生成, 因此需要在较低温度下进行。
2.2.1 第一步氢化温度对还原反应的影响氢化温度对产品质量影响较大, 温度高反应快, 但容易产生杂质; 温度低反应时间延长, 但产品质量相对较好。为了探索得到最适宜的氢化温度, 本研究进行了不同氢化温度的对比研究, 结果见表 4。
| 反应温度/℃ | 反应时间/h | 加氢产物TLC图谱 | w[瑞替加滨(Ⅰ)粗品]/%(HPLC) | |
| 原料 | 杂质个数 | |||
| 55 | 5 | 有 | 较多 | 79.79 |
| 45 | 7 | 有 | 较少 | 81.26 |
| 45 | 10 | 有 | 较多 | 84.36 |
| 35 | 16 | 有 | 较少 | 75.18 |
试验结果发现, 在氢化温度为55 ℃时, 杂质较多, 而且原料很难反应完全; 45 ℃反应时, 杂质有所减少; 35 ℃反应时, 反应时间延长之后, 反应不完全, 粗品纯度低。在随后的酰化反应中, 所得到的最终产物瑞替加滨(Ⅰ)的质量也是不同的。
2.2.2 第二步氢化过程, 温度、盐酸的加入量对反应的影响上述对氢化温度的考察结果可以看出, 55 ℃产物杂质多, 收率低, 45和35 ℃反应速度慢, 时间延长会导致杂质增加, 因此较高的反应温度或较长的反应时间都会提高杂质增加的风险。一般而言, 质子酸可以促使Pd/C加氢[16]。同时, 酸的加入还可以使带胺基的产物成盐而使稳定性增强。因此, 本研究在氢化反应进行到一定程度后, 对向反应体系中加入盐酸的可行性进行了研究, 试验结果见表 5。
| 滴加盐酸后的氢化温度/℃ | 反应时间/h | 加氢产物TLC图谱 | w[瑞替加滨(Ⅰ)粗品]/% (HPLC) | |
| 原料 | 杂质个数 | |||
| 10~15 | 4.5 | 无 | 较少 | 81.7 |
| 20 | 1.0 | 无 | 较少 | 76.3 |
| 30 | 1.0 | 无 | 较多 | 72.8 |
| 注:1.m[2-氨基-4-(4-氟苄胺基)硝基苯]:V(四氢呋喃)=1:5;2.THF为溶剂, 反应温度为35 ℃, 保温氢化约2.5 h后开始滴加盐酸。 | ||||
上述试验结果表明, 滴加盐酸后的最适宜氢化温度为10~15 ℃, 加氢产物中杂质较少且原料能够反应完全, 其相对应的最终产物瑞替加滨(Ⅰ)的粗品质量分数也较高。
在上述实验基础上, 本研究继续对盐酸的加入量对反应的影响进行了考察, 试验结果见表 6。
| 浓盐酸加入量/g | 氢化反应总时间/h | w[瑞替加滨(Ⅰ)粗品]/% (HPLC) |
| 0.4 w | 7.0 | 77.5 |
| 0.5 w | 5.0 | 78.7 |
| 0.6 w | 2.5 | 79.2 |
| 0.8 w | 2.5 | 79.8 |
| 注:1.以2-氨基-4-(4-氟苄胺基)硝基苯(Ⅳ)的投料量w(g)为基准; 2.盐酸滴加过程中, 控制温度小于20 ℃; 3.滴加完成后, 继续保温氢化(15~20 ℃)。 | ||
试验过程发现, 盐酸的加入量大对反应速度影响不大, 而加入量过少, 会增加反应时间。试验结果表明, 0.6w的盐酸量能较明显地提高氢化反应速度, 当达到0.8w时氢化反应速度增加不明显。另外, 滴加盐酸时应控制局部温度, 盐酸浓度不宜过大, 应将浓盐酸稀释后再滴加, 稀释程度与滴加速度有关, 温度控制在15~20 ℃, 温度过高会导致杂质增多, 而温度过低不利于氢化反应的进行。
3 结论以5-氟-2-硝基苯胺为起始原料, 与4-氟苄胺经亲核取代反应制得2-氨基-4-(4-氟苄胺基)硝基苯(Ⅳ), 再通过还原反应、酰化反应制得最终产物N-[2-氨基-4-(4-氟苄胺基)苯基]氨基甲酸乙酯(瑞替加滨, Ⅰ)。整个反应过程中, 原料易得, 反应条件温和可控, 操作简单, 合成工艺稳定可靠, 同时收率较高, 并且可以得到质量稳定、质量分数较高的化合物。最终产物的化学结构通过核磁共振、质谱等手段得以确证。
| [1] |
DeBoer H M, Mula M, Sander J W. The global burden and stigma of epilepsy[J/OL]. Epilepsy Behavior, 2008, 12(4): 540-546
|
| [2] |
Czuczwar P, Wojtak A, Cioczek-Czuczwar A, et al. Retigabine:The newer potential antiepileptic drug[J]. Pharmacological Reports, 2010, 62(2): 211-219. DOI:10.1016/S1734-1140(10)70260-7 |
| [3] |
US FDA. FDA approves Potiga to treat seizures in adults[EB/OL].http:\\www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm258834.htm
|
| [4] |
Rundfeldt C. The new anticonvulsant retigabine (D-23129) acts as an opener of K+channels in neuronal cells[J]. European Journal of Pharmacology, 1997, 336(2/3): 243-249. |
| [5] |
Sills G J, Rundfeldt C, Butler E, et al. A neurochemical study of the novel antiepileptic drug retigabine in mouse brain[J]. Pharmacological Research the Official Journal of the Italian Pharmacological Society, 2000, 42(6): 553-557. DOI:10.1006/phrs.2000.0738 |
| [6] |
牛丽萍, 宗利, 武杰, 等.一种合成瑞替加滨的方法: CN, 103570587[P]. 2014-02-12
|
| [7] |
孟月垒, 张宪美, 谈敦潮, 等.瑞替加滨中间体的制备方法和瑞替加滨的制备方法: CN, 103342648A[P]. 2013-10-09
|
| [8] |
朱磊, 王佳乐, 王浦海. 瑞替加滨的合成工艺改进[J]. 中国药物化学杂志, 2014, 24(1): 31-33. Zhu Lei, Wang Jiale, Wang Puhai. Improved synthesis of retigabine[J]. Chinese Journal of Medicinal Chemistry, 2014, 24(1): 31-33. (in Chinese) |
| [9] |
王浦海, 王佳乐, 朱磊, 等.一种瑞替加滨的合成方法: CN, 103724231A[P]. 2014-04-16
|
| [10] |
祁金龙, 张超, 吴茵, 等. 瑞替加滨的合成[J]. 中国医药工业杂志, 2013, 44(3): 223-225. Qi Jinlong, Zhang Chao, Wu Yin, et al. Synthesis of retigabine[J]. Chinese Journal of Pharmaceuticals, 2013, 44(3): 223-225. (in Chinese) |
| [11] |
郑建兵, 王向军, 李贵杰, 等.瑞替加滨及其中间体的制备方法: CN, 103373941A[P]. 2013-10-30
|
| [12] |
容志欢.瑞替加滨及其相关物质的合成方法研究[D].石家庄: 河北医科大学, 2015 Rong Zhihuan. Study on the synthesis of retigabine and its related impurities[D]. Shijiazhuang: Hebei Medical University, 2015(in Chinese) |
| [13] |
谌伦华, 蔡祖安, 张志强, 等.一种瑞替加滨中间体的简单合成方法: CN, 101921195A[P]. 2010-12-22
|
| [14] |
曹云峰, 王辉, 王俊臣. 瑞替加滨的合成工艺改进[J]. 广州化工, 2015, 43(6): 95-97. Cao Yunfeng, Wang Hui, Wang Junchen. Improvement for synthesis of retigabine[J]. Guangzhou Chemical Industry, 2015, 43(6): 95-97. DOI:10.3969/j.issn.1001-9677.2015.06.034 (in Chinese) |
| [15] |
Hans-Reinhold Dieter. Phamaceutically active 1, 2, 4-triamino-benzene derivatives, process for their preparation and pharmaceutical compositions containing them: US, 5384330[P]. 1995-01-24
|
| [16] |
张明森, 黄凤兴, 梁泽生, 等. 精细有机化工中间体全书[M]. 北京: 化学工业出版社, 2007.
|
 2018, Vol. 35
2018, Vol. 35





