Cu2O是一种禁带宽度为2.0 eV的p型半导体[1], 其原料丰富, 制备成本低, 无毒, 在太阳光照射下可产生光生空穴和光生电子, 太阳光理论利用率可达20%[2]。目前, 制备的Cu2O半导体材料形貌主要有量子点、颗粒、薄膜和纳米线等[3-6], 尤其是纳米Cu2O比表面积大, 表面活性较高, 因而在太阳能电池[7-9]、光催化降解[10]和光致变色[11]等领域应用十分广泛。但是Cu2O光生电子和空穴易发生复合, 使其光催化性能降低。CdS作为一种可被可见光激发的n型半导体材料, 禁带宽度为2.4 eV, 在光催化剂[12-14]、太阳能电池[15]以及压电纳米发电机[16]领域有着广泛的应用。利用Cu2O的能带位置和良好的空穴导通性质, 可以将其作为一种敏化剂与n型的CdS半导体进行耦合, 二者复合后在其复合的界面上形成pn型异质结, 该结构可以有效地降低光生载流子的复合几率, 进而提高其在可见光下的催化效果, 在光催化降解方面表现出良好的应用前景[17]。目前, 对Cu2O/CdS复合物的研究主要集中在复合膜和复合球上, 对Cu2O/CdS纳米线鲜有研究, 而在多种复合形式的pn型复合半导体光催化剂中, 只有在组分都暴露出来, 并且彼此没完全裹覆时才能发挥其复合的效能[18], 本研究制备的Cu2O/CdS纳米线是在轴向形成的pn结, 可以使CdS和Cu2O 2种材料都暴露出来, 同时纳米材料由于其尺寸小、比表面积大, 表面活性较高, 具有较高的光催化活性。
本研究以多孔阳极氧化铝(AAO)为模板, 采用控电位法制备了pn型Cu2O/CdS纳米线阵列, 并对样品的表面形貌、结构、半导体类型、光电转化性能、光响应性能和光催化性能进行了表征和测试。
1 实验 1.1 试剂与仪器主要试剂(AR级):CuSO4·5H2O、乳酸、氢氧化钠、氯化镉、硫代硫酸钠、氨水、氯化铵、EDTA-2Na和二次蒸馏水。
仪器:CHI660B型电化学工作站; 氙灯(500 W); S-4800型电子扫描显微镜; JEM-2100F型场发射透射电子显微镜; D8-Focus型X射线衍射仪; TU-1901双光束紫外-可见分光光度计。
1.2 实验方法利用两步阳极氧化法制备AAO模板[19], AAO模板的孔径约为100 nm。在贯通的AAO膜一面溅射1层Au膜作为导电层, 固定在Cu片上, 制成AAO模板电极。利用电化学工作站, 以AAO模板为工作电极, 钌钛网为辅助电极, 饱和甘汞电极为参比电极, 利用控电位法制备Cu2O、CdS纳米线及Cu2O/CdS纳米线。Cu2O纳米线沉积液组成为0.4 mol/L CuSO4+3.0 mol/L乳酸, pH值为10, 沉积液温度为55 ℃, 沉积电位为-0.28 V。CdS纳米线沉积液组成为0.02 mol/L CdCl2+0.075 mol/L Na2S2O3+0.02 mol/L EDTA-2Na, pH值为9.5, 沉积液温度为50 ℃, 沉积电位为-1.0 V。pn型Cu2O/CdS纳米线的制备顺序为:先将AAO模板电极置于Cu2O纳米线沉积液中, 控电位沉积Cu2O纳米线后, 将电极取出用蒸馏水清洗干净, 然后置于CdS纳米线沉积液中, 继续控电位沉积CdS纳米线。沉积结束后, 用二次蒸馏水冲洗工作电极, 60 ℃烘箱干燥后得到Cu2O、CdS纳米线及Cu2O/CdS纳米线。
1.3 Cu2O/CdS纳米线的表征及性能测试利用SEM、TEM和XRD对所制备的纳米线进行形貌和结构表征。采用三电极体系, 利用电化学工作站测试样品的光照开路电位曲线, Cu2O/CdS纳米线阵列(1×2 cm2)为工作电极, 钌钛网为辅助电极, 饱和甘汞电极为参比电极, 电解液为0.5 mol/L Na2SO4溶液, 500 W的氙灯, 室温。测试了4个周期, 每个周期暗态时间和光照时间分别为100 s。光照开路电位差值(Voc)定义为光照下开路电位(Vlight)和黑暗条件下开路电位(Vdark)差值的绝对值, 即Voc=︱Vlight-Vdark︱。Motto-Schokkty测试装置同光照开路电位测试, 不需要光源照射, 电解液为0.2 mol/L K2SO4溶液, 测试频率为100 Hz, 电位间隔为10 mV, 扰动正弦波幅值为5 mV。利用TU-1901双光束紫外-可见分光光度计测试样品的紫外-可见吸收光谱。光催化降解实验是在100 mL、5 mg/L罗丹明B中测试, 催化剂用量为36.4 mg, 光源为500 W氙灯, 室温, 实验从打开光源开始计时, 利用紫外分光光度计每隔1 h测量1次溶液的吸光度值, 光催化降解效率(D)定义为D=(C0-C)/C0×100%, 其中:C0表示罗丹明B溶液的初始浓度, C表示反应过程中某一时间的浓度。
2 结果与讨论 2.1 Cu2O/CdS纳米线的形貌表征图 1a)是AAO模板的SEM图, 图 1a)中AAO模板的孔洞排列整齐, 孔径均匀, 约为100 nm。图 1b)和图 1c)分别为除去AAO模板后的Cu2O纳米线和Cu2O/CdS纳米线的SEM图, 由图 1b)和图 1c)可知, Cu2O纳米线和Cu2O/CdS纳米线表面光滑, 分布均匀, 直径均一, 约为100 nm, 与AAO模板孔径大小一致, Cu2O纳米线的长度约为1 μm, Cu2O/CdS纳米线的长度约为2 μm。图 1d)是除去AAO模板后Cu2O/CdS纳米线的TEM图, 图 1d)中部分Cu2O/CdS纳米线倾斜成簇, 这是因为除去AAO模板后, 纳米线失去支撑而倾斜, 模板除去后, 纳米线更多暴露在外面, 表面积很大, 表面自由能增大, 因趋于稳定而聚集成簇。由图 1d)可知, 纳米线的直径均一, 约100 nm, 这与SEM图中的结果一致。

|
| 图 1 AAO模板a), Cu2O纳米线b), Cu2O/CdS纳米线c)的SEM图及Cu2O/CdS纳米线d)的TEM图 Figure 1 SEM images of AAO a), Cu2O nanowires b), Cu2O/CdS nanowires c) and TEM image of Cu2O/CdS nanowire d) |
| |
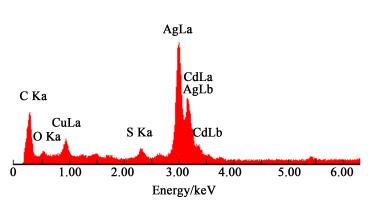
图 2是Cu2O/CdS纳米线的能谱图。
|
| 图 2 Cu2O/CdS纳米线的能谱图 Figure 2 EDS spectra of Cu2O/CdS nanowire |
| |
由图 2可知, 样品由C、O、Cu、S、Cd和Ag元素组成, C峰来源于碳膜, 而Ag峰来源于制备AAO电极的导电银胶。
2.2 Cu2O/CdS纳米线的结构表征图 3是Cu2O/CdS纳米线的XRD谱图。

|
| 图 3 Cu2O/CdS纳米线的XRD谱图 Figure 3 XRD pattern of Cu2O/CdS nanowires |
| |
由图 3可知, 在2θ为30.11°、36.65°、42.98°、61.67°和74.65°处均出现了Cu2O的特征峰, 分别对应立方晶系Cu2O的(110)、(111)、(200)、(220)和(311)晶面; 在2θ为26.65°和52.44°处出现了CdS的特征峰, 对应立方晶系CdS的(111)和(311)晶面, 在2θ为24.93°、26.65°和28.02°处出现了CdS的特征峰, 对应六方晶系CdS的(100)、(002)和(101)晶面。表明纳米线由立方晶系Cu2O、立方晶系与六方晶系混合晶系的CdS组成。
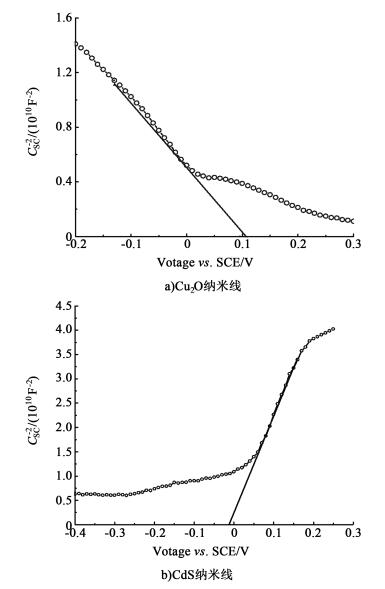
2.3 Motto-Schokkty测试图 4为Cu2O纳米线和CdS纳米线的Mott-Schottky曲线。
|
| 图 4 Cu2O纳米线a)和CdS纳米线b)的Mott-Schottky曲线 Figure 4 Mott-Schottky curves of Cu2O nanowires a) and CdS nanowires b) |
| |
半导体空间电荷电容CSC与电位满足Mott-Schottky关系:
对于n型半导体,
| $ {C_{{\rm{SC}}}}^{-2} = \frac{2}{{{\varepsilon _0}{\varepsilon _{{\rm{SC}}}}e{N_{\rm{D}}}}}(E-{E_{{\rm{fb}}}}-kT/e) $ | (1) |
对于p型半导体,
| $ {C_{{\rm{SC}}}}^{-2} =- \frac{{2}}{{{\varepsilon _0}{\varepsilon _{{\rm{SC}}}}e{N_{\rm{D}}}}}(E-{E_{{\rm{fb}}}} - kT/e) $ | (2) |
式(1)和式(2)中; CSC为空间电荷电容; εSC为半导体相对介电常数; ε0为真空介电常数, 8.85×10-14 F·cm-1; e为1个电子的电荷量; ND为载流子浓度; E为外加电位; Efb为平带电位; k是玻耳兹曼常数, 1.38×10-23 J/K; T表示温度。室温下, kT/e值很小, 约为25 mV, 一般可以忽略不计。在Mott-Schottky曲线中, 根据曲线中线性部分斜率的正负判断半导体类型, 对于n型半导体, 斜率为正, 而对于p型半导体, 斜率为负[20]。由图 4可知, Cu2O纳米线和CdS纳米线的Mott-Schottky曲线中直线段的斜率分别为负值和正值, 说明实验中制备的Cu2O和CdS分别为p型和n型半导体。
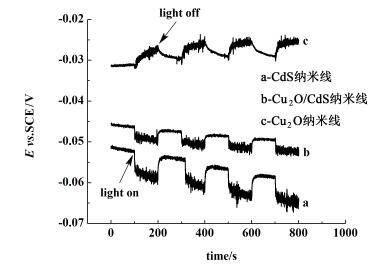
2.4 Cu2O/CdS纳米线的光照开路电位图 5是CdS纳米线、Cu2O/CdS纳米线和Cu2O纳米线的开路电位-时间曲线。
|
| 图 5 CdS纳米线、Cu2O/CdS纳米线和Cu2O纳米线的开路电位-时间曲线 Figure 5 Open-Circuit potential curves of CdS nanowires, Cu2O/CdS nanowires and Cu2O nanowires |
| |
由图 5可知, 样品在受到光源照射和光源撤去瞬间, 开路电位均有1个小的突变, 出现光电响应现象。CdS纳米线的光照开路电位差值约7 mV, Cu2O纳米线约3.9 mV, 而Cu2O/CdS纳米线约3.4 mV。单一CdS纳米线和单一Cu2O纳米线的光照开路电位差值都比较小, 是因为单一CdS纳米线和单一Cu2O纳米线在光照时产生的光生载流子容易在材料内部发生复合。与单一纳米线相比, Cu2O/CdS纳米线的光照开路电位差值有所减小, 这是因为CdS是n型半导体材料, 电子作为多数载流子参与导电, 当光源照射时, CdS提供大量的电子, 使光照开路电位值出现负向偏移, 如图 5中曲线a所示; 而Cu2O是p型半导体材料, 空穴作为多数载流子参与导电, 当受到光源照射时, Cu2O提供大量的空穴, 使光照开路电位值出现正向偏移, 如图 5中曲线c所示。由于这2种偏移趋势相反, 所以Cu2O/CdS纳米线的光生电位在二者叠加后减小, 此外, 受到光源激发时, 光生载流子在CdS和Cu2O之间转移, 导致其开路电位差值变化不明显。
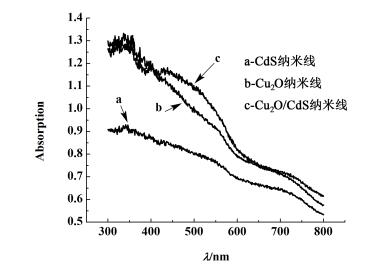
2.5 紫外可见吸收光谱图 6为CdS纳米线、Cu2O纳米线和Cu2O/CdS纳米线的紫外-可见吸收光谱图。
|
| 图 6 CdS纳米线、Cu2O纳米线和Cu2O/CdS纳米线紫外-可见吸收光谱图 Figure 6 UV-Vis absorption spectrums of CdS nanowires, Cu2O nanowires and Cu2O/CdS nanowires |
| |
由图 6可知, CdS纳米线的吸收边在585 nm附近, Cu2O纳米线的吸收边在625 nm附近, Cu2O/CdS纳米线的吸收边在630 nm附近, 根据公式Eg=1240/λ[21], λ为吸收带边波长, CdS纳米线的禁带宽度约为2.12 eV, Cu2O纳米线的禁带宽度约为1.98 eV。与CdS、Cu2O纳米线相比, Cu2O/CdS纳米线的光响应范围略有拓宽, 吸收边发生红移, 吸光度增大, 光响应增强。这是因为Cu2O与CdS形成复合材料后, 在光源照射下, 光生空穴和光生电子分别在不同的半导体上积累, 电子和空穴能有效地分离, 这也有利于提高Cu2O/CdS纳米线的光催化性能。
2.6 Cu2O/CdS纳米线的光催化性能图 7为Cu2O纳米线和Cu2O/CdS纳米线的光催化降解罗丹明B的性能测试曲线。图 7中曲线a是空白对照实验, 指在相同条件下, 只有光源而没有催化剂的情况下罗丹明B的降解效率曲线, 由曲线a可知, 在光照7 h后, 罗丹明B的降解效率约为9.82%, 溶液比较稳定。由曲线b和c可知, 光照7 h后, Cu2O纳米线和Cu2O/CdS纳米线的光催化降解效率分别是48.20%和66.02%。

|
| 图 7 无催化剂、Cu2O纳米线和Cu2O/CdS纳米线的光催化降解性能曲线 Figure 7 Photocatalytic performance of blank, Cu2O nanowires and Cu2O/CdS nanowires |
| |
光催化反应中, 半导体材料吸收光能产生光生电子和光生空穴, 电子具有还原性, 可以将半导体表面的溶解氧还原成超氧负离子(·O2-), ·O2-可以将有机物彻底降解为H2O和CO2; 空穴具有氧化性, 可以将半导体表面的氢氧根离子(OH-)或者水(H2O)氧化成羟基自由基(·OH), ·OH可以氧化溶液中的污染物, 所以光催化降解效率的高低与光生载流子的多少有关。Cu2O/CdS纳米线的降解性能高于Cu2O纳米线, 是因为在光源照射下, 单一Cu2O纳米线产生的光生电子和空穴容易发生复合, 使到达材料表面参与催化降解罗丹明B的光生载流子减少, 从而使其催化降解效率降低, 而Cu2O/CdS半导体材料由于pn结的形成, CdS的导带位置比Cu2O要低, 电子主要在CdS上积累, Cu2O的价带位置比CdS要高, 空穴主要在Cu2O上积累[22], 光生电子和空穴分离, 减少了电子与空穴的复合几率, 使到达材料表面参与催化降解罗丹明B的光生载流子比单一Cu2O纳米线多, 因此Cu2O/CdS纳米线具有较好的光催化降解性能。
3 结论在AAO模板中利用控电位法成功制备了Cu2O/CdS纳米线。SEM和TEM结果显示, Cu2O/CdS纳米线的表面光滑、直径均一, 约100 nm。XRD测试表明, Cu2O/CdS纳米线由立方晶系的Cu2O和立方晶系与六方晶系混合晶系的CdS组成。Mott-Schottky测试表明, Cu2O/CdS纳米线由p型Cu2O和n型CdS组成, 为pn型异质结。与单一CdS、Cu2O纳米线相比, Cu2O/CdS纳米线的吸收边发生红移, 光响应性能增强。光催化性能测试表明Cu2O/CdS纳米线的光催化降解性能优于单一Cu2O纳米线, 这是由于Cu2O与CdS形成复合材料后, 在光源照射下, 光生空穴和光生电子分别迁移到不同的半导体材料上, 使光生电子和空穴分离, 减少了电子与空穴的复合几率, 从而提高了材料的光催化效率。
| [1] |
Yu Y, Du F, Jimmy C Y, et al. One-Dimensional shape-controlled preparation of porous Cu2O nano-whiskers by using CTAB as a template[J]. Journal of Solid State Chemistry, 2004, 177(12): 4640-4647. DOI:10.1016/j.jssc.2004.10.025 |
| [2] |
Olsen L C, Bohara R C, Urie M W. Explanation for low-efficiency Cu2O Schottky-barrier solar cells[J]. Applied Physics Letters, 1979, 34(1): 47-49. DOI:10.1063/1.90593 |
| [3] |
Borgohain K, Murase N, Mahamuni S. Synthesis and properties of Cu2O quantum particles[J]. Journal of Applied Physics, 2002, 92(3): 1292-1297. DOI:10.1063/1.1491020 |
| [4] |
Gou L, Murphy C J. Solution-Phase synthesis of Cu2O nanocubes[J]. Nano Letters, 2003, 3(2): 231-234. DOI:10.1021/nl0258776 |
| [5] |
Baek S K, Lee K R, Cho H K. Oxide pn heterojunction of Cu2O/ZnO nanowires and their photovoltaic performance[J]. Journal of Nanomaterials, 2013, 2013(4): 213-219. |
| [6] |
Wang W, Wang G, Wang X, et al. Synthesis and characterization of Cu2O nanowires by a novel reduction route[J]. Advanced Materials, 2002, 14(1): 67-69. DOI:10.1002/(ISSN)1521-4095 |
| [7] |
Rai B P. Cu2O solar cells:A review[J]. Solar Cells, 1988, 25(3): 265-272. DOI:10.1016/0379-6787(88)90065-8 |
| [8] |
Olsen L C, Addis F W, Miller W. Experimental and theoretical studies of Cu2O solar cells[J]. Solar Cells, 1982, 7(3): 247-279. DOI:10.1016/0379-6787(82)90050-3 |
| [9] |
Musselman K P, Marin A, Schmidt-Mende L, et al. Incompatible length scales in nanostructured Cu2O solar cells[J]. Advanced Functional Materials, 2012, 22(10): 2202-2208. DOI:10.1002/adfm.201102263 |
| [10] |
Kondo J N. Cu2O as a photocatalyst for overall water splitting under visible light irradiation[J]. Chemical Communications, 1998(3): 357-358. DOI:10.1039/a707440i |
| [11] |
Akhavan O, Tohidi H, Moshfegh A Z. Synthesis and electrochromic study of sol-gel cuprous oxide nanoparticles accumulated on silica thin film[J]. Thin Solid Films, 2009, 517(24): 6700-6706. DOI:10.1016/j.tsf.2009.05.016 |
| [12] |
Park H, Choi W, Hoffmann M R. Effects of the preparation method of the ternary CdS/TiO2/Pt hybrid photocatalysts on visible light-induced hydrogen production[J]. Journal of Materials Chemistry, 2008, 18(20): 2379-2385. DOI:10.1039/b718759a |
| [13] |
Li Y, Du J, Peng S, et al. Enhancement of photocatalytic activity of cadmium sulfide for hydrogen evolution by photoetching[J]. International Journal of Hydrogen Energy, 2008, 33(8): 2007-2013. DOI:10.1016/j.ijhydene.2008.02.023 |
| [14] |
Li Y, Tang L, Peng S, et al. Phosphate-Assisted hydrothermal synthesis of hexagonal CdS for efficient photocatalytic hydrogen evolution[J]. Cryst Eng Comm, 2012, 14(20): 6974-6982. DOI:10.1039/c2ce25838b |
| [15] |
Cheng W, Lin Y, Lu S. Nanowires improved charge separation and light utilization in metal-oxide solar cells[J]. Applied Physics Letters, 2011, 99(6): 38-40. |
| [16] |
Lin Y, Song J, Ding Y, et al. Alternating the output of a CdS nanowire nanogenerator by a white-light-stimulated optoelectronic effect[J]. Advanced Materials, 2008, 20(16): 3127-3130. DOI:10.1002/adma.v20:16 |
| [17] |
韩世同, 习海玲, 史瑞雪, 等. 半导体光催化研究进展与展望[J]. 化学物理学报, 2003, 16(5): 339-349. Han Shitong, Xi Hailing, Shi Ruixue, et al. Prospect and progress in the semiconductor photocatalysis[J]. Chinese Journal of Chemical Physics, 2003, 16(5): 339-349. DOI:10.3969/j.issn.1674-0068.2003.05.002 (in Chinese) |
| [18] |
吴欢文, 张宁, 钟金莲, 等. pn复合半导体光催化剂研究进展[J]. 化工进展, 2007, 26(12): 1669-1674. Wu Huanwen, Zhang Ning, Zhong Jinlian, et al. Progress in research of p-n type semiconductor composite photocatalysts[J]. Chemical Industry and Engineering Progress, 2007, 26(12): 1669-1674. DOI:10.3321/j.issn:1000-6613.2007.12.001 (in Chinese) |
| [19] |
Song Z, Xie Y, Yao S, et al. Field emission properties of electrodeposited cobalt nanowire arrays grown in anodic aluminum oxide[J]. Materials Letters, 2011, 65(1): 44-45. DOI:10.1016/j.matlet.2010.09.024 |
| [20] |
庄朋强, 肖占文, 朱向东, 等. 钽阳极氧化膜的半导体性研究[J]. 电子元件与材料, 2011, 30(8): 35-39. Zhuang Pengqiang, Xiao Zhanwen, Zhu Xiangdong, et al. Study on semiconductor properties of anodic oxide films on tantalum[J]. Electronic Components and Materials, 2011, 30(8): 35-39. DOI:10.3969/j.issn.1001-2028.2011.08.010 (in Chinese) |
| [21] |
王维波, 林瑞峰, 林原, 等. 电化学沉积CdSe纳晶薄膜的性能及沉积机理[J]. 感光科学与光化学, 1998, 16(2): 177-181. Wang Weibo, Lin Ruifeng, Lin Yuan, et al. The properties of the electrochemical deposited CdSe nanocrystalline thin films and the mechanism of deposition[J]. Photographic Science and Photochemistry, 1998, 16(2): 177-181. (in Chinese) |
| [22] |
Cheng W, Yu T, Chao K, et al. Cu2O-Decorated CdS nanostructures for high efficiency visible light driven hydrogen production[J]. International Journal of Hydrogen Energy, 2013, 38(23): 9665-9672. DOI:10.1016/j.ijhydene.2013.05.131 |
 2018, Vol. 35
2018, Vol. 35





