2. 天津大学环境科学与工程学院, 天津 300072;
3. 精馏技术国家工程研究中心, 天津 300072
2. School of Environmental Science and Engineering, Tianjin University, Tianjin 300072, China;
3. National Engineering Research Center of Distillation Technology, Tianjin 300072, China
丙酸乙酯是一种用途广泛的有机合成原料和溶剂,用于医药、抗真菌药物、农药、增塑剂、橡胶助剂、染料等领域,也可作为高级日用化妆品香料和有机合成中间体[1]。在传统生产工艺中,丙酸乙酯主要是通过丙酸和乙醇在常压下发生酯化反应进行生产[2],并且通过收集96~100 ℃的馏分来获得较纯的产物。然而,丙酸乙酯和乙醇在常压下会形成共沸体系[3],这样就会降低丙酸乙酯的产率和纯度。对于分离乙醇-丙酸乙酯共沸物系的研究还没有报道,因此,有必要对乙醇-丙酸乙酯共沸体系进行分离工作。
对于共沸体系,不能采用普通精馏分离,需要采用特殊精馏进行分离。要使丙酸乙酯的质量分数达到99%以上,选取萃取精馏法分离乙醇和丙酸乙酯混合物更为合适。萃取精馏是一种分离近沸点或共沸物系的常用方法[4],其中萃取剂的选择尤为重要。本研究通过COSMO-SAC模型筛选和汽液平衡实验验证,确定了对二甲苯适合作为分离乙醇-丙酸乙酯二元共沸物系的萃取剂,并使用Aspen Plus模拟软件对连续萃取精馏分离乙醇-丙酸乙酯共沸物系的过程进行了灵敏度分析,确定了较适宜的工艺参数,为工业生产的设计和操作提供了参考依据。
1 萃取剂的选择 1.1 萃取剂的初步筛选针对乙醇-丙酸乙酯二元物系,按照相似相溶的原理,从常见的有机溶剂中初步筛选了苯胺、乙二醇、对二甲苯、乙腈、二甲基亚砜(DMSO)、二甲基甲酰胺(DMF)作为萃取剂。由于乙二醇的化学性质不稳定,易代谢生成有毒的草酸,苯胺漏置于空气中极易被氧化,由无色液体变质为黄色至红棕色,因此,根据萃取剂的稳定性原则,乙二醇和苯胺不宜作为本体系的萃取剂。最终选择了对二甲苯、乙腈、DMSO和DMF作为预选萃取剂。
1.2 COSMO-SAC模型筛选萃取剂萃取剂选择性是衡量溶剂效果的重要指标[5-6]。萃取剂的选择性可由无限稀释活度系数来表示,即:
| $ S_{{\rm{A, B}}}^\infty = \frac{{\gamma _{{\rm{A, S}}}^\infty }}{{\gamma _{{\rm{B, S}}}^\infty }} $ | (1) |
式(1)中,γA, S∞与γB, S∞分别表示溶质A与B在溶剂S中的无限稀释活度系数,SA, B∞值越大,表明萃取剂S在溶质A和B中的选择性越好。
COSMO-SAC(COSMO segment activity coefficient)模型[7],即COSMO片段活度系数模型,是一种基于量子化学和统计力学理论,从微观的物质结构即可预测物质宏观热力学性质的模型。COSMO-SAC模型通过分别计算出溶质在溶剂中的无限稀释活度系数[8-9],再由式(1)求出各个溶剂对于乙醇-丙酸乙酯二元物系的选择性SA, B∞。为了保证萃取剂筛选过程中外界条件的一致性,本研究均是在293.15 K及101.3 kPa的条件下对萃取剂进行筛选,计算的结果列于表 1中。
| 组分 | 对二甲苯 | 乙腈 | DMSO | DMF |
| 选择性 | 811.9872 | 0.2358 | 246.6139 | 0.1023 |
由表 1可以看出,对二甲苯和DMSO是较好的候选萃取剂。考虑到DMSO的沸点(189.0 ℃,101.3 kPa下)较对二甲苯的沸点(138.5 ℃,101.3 kPa下)更高,这会导致若DMSO作为萃取剂,所需的能耗也会增加不少负担。且对二甲苯的选择性比DMSO更大,因此,最终选择了对二甲苯作为分离乙醇-丙酸乙酯二元共沸物系的萃取剂。
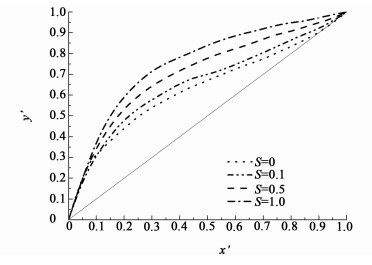
1.3 Aspen Plus模拟确定溶剂比利用Aspen Plus软件中的Wilson模型模拟不同溶剂比(萃取剂与原料的物质的量之比)对二甲苯对乙醇-丙酸乙酯二元汽液平衡的影响,如图 1所示,其中,x′和y′分别表示乙醇汽液相中无溶剂基(扣除对二甲苯)摩尔分数。
|
| 图 1 不同溶剂比下的汽液平衡图 Figure 1 VLE diagram under different solvent ratio |
| |
由图 1的汽液平衡相图可知,随着对二甲苯含量的增多,乙醇对丙酸乙酯的相对挥发度也提高。虽然溶剂比为0.1时能消除共沸现象,但是在乙醇高浓度区,乙醇对丙酸乙酯的相对挥发度仍较小,分离效果不显著;采用溶剂比为0.5时,可以明显提高待分离组分间的相对挥发度;溶剂比为1.0时,虽然也能提高乙醇对丙酸乙酯的相对挥发度,但溶剂比为0.5时已经可以实现有效分离,考虑到溶剂量的增多会增加塔釜的热负荷,故综合考虑分离效果和经济性,溶剂比为0.5时更为合适。
2 实验部分 2.1 实验试剂、装置及步骤所用试剂:丙酸乙酯、乙醇和对二甲苯,均为分析纯。
实验装置:实验中汽液平衡数据的测定采用改进的Othmer汽液平衡釜,详见文献[10-11]。实验装置图如图 2所示。

|
| 图 2 改进的Othmer汽液平衡釜 Figure 2 The modified Othmer vapor-liquid equilibrium still |
| |
实验步骤:在101.3 kPa下,将不同摩尔分数的乙醇-丙酸乙酯与对二甲苯混合,配置成溶剂与原料的物质的量之比为0.5的混合溶液加入平衡釜中,加热至沸腾,平衡温度保持45~60 min后,取汽液样品分析。
2.2 分析方法所有样品采用气相色谱仪(山东鲁南GC2060型)进行定量分析,选用SE-54非极性毛细管色谱柱(30 m×0.32 mm×0.5 μm)。色谱条件:检测器采用氢火焰检测器(FID)。以高纯氮气作为载气,汽化室和检测器温度均为200 ℃,柱温为120 ℃,柱前压为0.1 MPa。每次进样量为0.4 μL,采用面积归一化法定量。每组实验进行3次平行实验。
3 实验结果与讨论在101.3 kPa下,将溶剂比为0.5时的实验汽液平衡数据与采用Aspen Plus软件Wilson模型计算得到的模拟数据作对比,如图 3所示。

|
| 图 3 对二甲苯作用下乙醇-丙酸乙酯汽液平衡图 Figure 3 VLE of ethanol-ethyl propionate with para-xylene |
| |
由图 3可以看出,对二甲苯的加入能够显著提高乙醇-丙酸乙酯的相对挥发度,并且可以打破二元共沸物的共沸组成。Wilson模型的计算值能够与实验值较好地吻合,因此,可以用Wilson模型进行乙醇-丙酸乙酯-对二甲苯萃取精馏模拟。
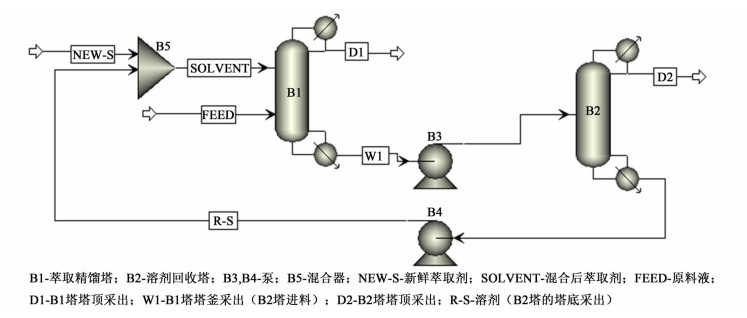
4 萃取精馏模拟及优化 4.1 连续萃取精馏流程连续萃取精馏流程图如图 4所示。
|
| 图 4 连续萃取精馏流程图 Figure 4 Flowchart of continuous extractive distillation |
| |
轻组分乙醇能够从混合物中分离出来,重组分丙酸乙酯同萃取剂对二甲苯一起沿着B1塔向下流入塔底。从B1塔塔釜采出的重组分丙酸乙酯和萃取剂对二甲苯混合液,经泵的作用,作为溶剂回收塔的进料液流入B2塔中。二者存在一定的沸点差,且无共沸现象产生,因此二者较易分离。重组分丙酸乙酯沸点比萃取剂对二甲苯低,作为塔顶产品采出,而萃取剂则由塔釜采出,经过循环回收与新鲜的萃取剂混合后继续使用。
4.2 模拟条件与结果由于乙醇-丙酸乙酯二元物系在共沸点处的液相摩尔组成为(87.5,12.5),因此,萃取精馏模拟过程中原料的进料组成可采用接近共沸点处的组成,本研究设定的原料进料组成的初值为86.5:13.5(物质的量之比)。利用DSTWU模块,对溶剂回收塔的最小理论塔板数进行了计算,结果为30块理论塔板,其余各参数设定初值见表 2。
| 工艺参数 | 萃取精馏塔 | 溶剂回收塔 |
| 理论塔板数N | 30 | |
| 原料进料位置NF | 20 | |
| 萃取剂进料位置NS | 5 | |
| 原料进料量/(kmol·h-1) | 100 | |
| 萃取剂进料量/(kmol·h-1) | 50 | |
| 进料温度/℃ | 25 | |
| 回流比R | 5 | 4 |
| 进料压力/kPa | 120 | 120 |
| 塔顶压力/kPa | 101 | 101 |
| 压降/kPa | 0 | 0 |
| 塔顶采出量/(kmol·h-1) | 86.50 | 13.45 |
固定以上参数,分别考察几组萃取精馏塔的理论塔板数N1和原料进料位置NF1对塔顶产品D1的浓度影响:N1=30,NF1=20时,w(D1)=0.9487;N1=50,NF1=40时,w(D1)=0.9759;N1=60,NF=50时,w(D1)=0.9913。因此,选择萃取精馏塔塔板数为60块,原料进料位置为第50块塔板进行模拟,模拟结果如表 3所示。
| D1 | W1 | D2 | R-S | |
| 温度/℃ | 78.3 | 121.0 | 94.3 | 137.1 |
| n(乙醇)/% | 99.13 | 1.19 | 5.61 | 0 |
| n(丙酸乙酯)/% | 0.01 | 21.24 | 94.39 | 1.59 |
| n(对二甲苯)/% | 0.86 | 77.57 | 0.00 | 98.41 |
由表 3模拟结果可以得出,B1塔塔顶采出的产品中,轻组分乙醇摩尔分数为99.13%,但在塔釜的流股中仍含有1.19%的乙醇,这些乙醇会流入B2塔内,影响到B2塔塔中塔顶产品重组分丙酸乙酯的纯度以及塔釜采出液中萃取剂的纯度。在实际的生产工艺中,我们希望能够在B2塔塔顶得到至少99%纯度的丙酸乙酯产品,塔釜内也含有尽量少的丙酸乙酯组分,降低丙酸乙酯产品损失的同时,达到提高萃取剂利用率的目的。因此,为了进一步提高塔顶产品的纯度,有必要根据初值设定的工艺参数,对其进行工艺参数优化。
4.3 萃取精馏塔的模拟优化采用Aspen Plus模拟软件中的Radfrac模块对萃取精馏塔的工艺参数进行灵敏度分析,选用Wilson活度系数方程分别对原料进料位置、萃取剂进料位置、溶剂比和回流比优化处理。
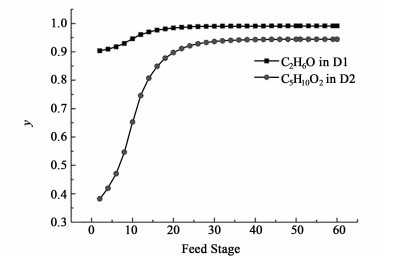
4.3.1 原料进料位置的分析在4.2设定的工艺参数初值的前提下,以原料液的进料位置为自变量,B1塔塔顶D1乙醇的摩尔分数以及B2塔塔顶D2丙酸乙酯的摩尔分数为因变量,进行灵敏度分析,结果如图 5所示。
|
| 图 5 原料进料位置对塔顶产品纯度的影响 Figure 5 Effect of feed stage on product content in the distillate |
| |
由图 5可看出,从第20块塔板之后,B1塔塔顶采出液中乙醇的浓度和B2塔塔顶馏分中丙酸乙酯的浓度均处于缓慢增大的趋势,且在第45至54块塔板进料时,两塔的塔顶产品浓度趋于稳定。因此,当B1塔的理论塔板数为60块时,原料由第50块塔板进料是合适的。
4.3.2 萃取剂进料位置的分析在设定的参数初值不变的情况下,分析萃取剂的进料位置对B1塔塔顶D1乙醇的物质的量浓度以及B2塔塔顶D2丙酸乙酯的物质的量浓度的影响。结果如图 6所示。

|
| 图 6 萃取剂进料位置对塔顶产品纯度的影响 Figure 6 Effect of solvent feed stage on product content in the distillate |
| |
由图 6可以得出,当B1塔的理论塔板数为60块,萃取剂从第10至40块塔板之间进料时,B1塔塔顶乙醇浓度基本保持不变,且均能保持在99%以上。当第25块塔板进料时,B1塔塔顶的乙醇浓度达到最高值,即99.8%。随着萃取剂进料位置的下移,萃取剂与原料液进料位置也越来越近,使得萃取剂与原料液不能完成充分的接触,达不到较好地分离目的,因此,在原料液进料的第50块板附近,B1塔塔顶的产品内乙醇的浓度开始下降。同时,未充分分离的乙醇也会混入B1塔塔釜液中,影响到B2塔塔顶产品中重组分丙酸乙酯的含量。对于B2塔塔顶丙酸乙酯的含量,从第20至30块塔板进料时,其值达到最大,且均保持在98%以上。为了同时保证B1塔和B2塔塔顶主要产品的浓度,本研究选择第25块塔板作为萃取剂进料位置。
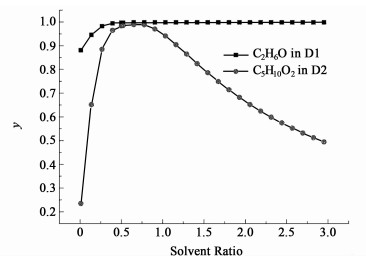
4.3.3 溶剂比的影响在萃取剂进料位置为第25块塔板及其余工艺参数不变的情况下,对溶剂比进行灵敏度分析,探究了溶剂比变化对各塔塔顶主要产品浓度的影响,其结果如下图 7所示。
|
| 图 7 溶剂比对塔顶产品纯度的影响 Figure 7 Effect of solvent ratio on product content in the distillate |
| |
由图 7可以得出,随着溶剂比的增加,B1塔塔顶的乙醇含量也会增大,这是因为加入萃取剂的量越大,萃取剂对二元共沸物的作用力也越大,提高了乙醇对丙酸乙酯的相对挥发度。而当萃取剂含量增加到一定量时,更多的萃取剂会流入到B2塔内,这就使得B2塔内丙酸乙酯的相对含量有所下降,因此当溶剂比大于0.8时,B2塔塔顶产品中丙酸乙酯含量会出现下降的现象,故这里取溶剂比为0.8时进料。
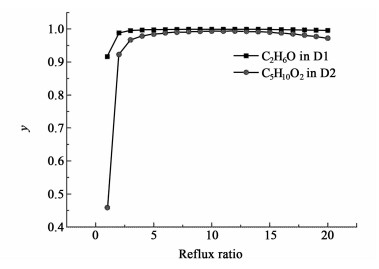
4.3.4 回流比的影响在萃取剂进料位置为第25块塔板、溶剂比为0.8且其余参数不变的条件下,对B1塔的回流比进行灵敏度分析,讨论了回流比变化对各塔塔顶主要产品浓度的影响,其结果如下图 8所示。
|
| 图 8 回流比对塔顶产品纯度的影响 Figure 8 Effect of reflux ratio on product content in the distillate |
| |
由图 8可以得出,回流比从1增大到7时,两塔塔顶主要成分的含量均处于上升的趋势,但当回流比大于12时,2塔塔顶主要成分的含量呈现缓慢下降的趋势,这是因为回流比过大时,各层塔板上萃取剂的含量也会相对降低,从而降低了萃取剂对共沸组分的作用[12],因此,塔顶产品含量会出现下降的现象。故这里选择回流比为7。
4.4 溶剂回收塔的模拟优化在萃取精馏塔B1各个工艺参数优化后的条件下(即萃取剂的进料位置为第25块塔板,原料进料位置为第50块塔板,回流比为7,溶剂比为0.8),对溶剂回收塔B2的进料位置和回流比2个工艺参数进行灵敏度分析,分别考察它们对塔顶产品以及塔釜萃取剂浓度的影响,得到最适宜工艺参数为:进料位置为第11块塔板,回流比为6。
4.5 工艺参数优化结果将对萃取精馏塔和溶剂回收塔优化后的工艺参数列入表 4中。
| 工艺参数 | 萃取精馏塔 | 萃取剂回收塔 |
| 理论塔板数 | 60 | 30 |
| 原料进料位置 | 50 | 11 |
| 萃取剂进料位置 | 25 | |
| 原料进料量/(kmol·h-1) | 100 | |
| 萃取剂进料量/(kmol·h-1) | 82 | |
| 进料温度/℃ | 25 | |
| 回流比 | 7 | 6 |
| 进料压力/kPa | 120 | 120 |
| 塔顶压力/kPa | 101 | 101 |
| 压降/kPa | 0 | 0 |
| 塔顶采出量/(kmol·h-1) | 86.50 | 13.45 |
工艺参数优化后的模拟结果如表 5所示。
| D1 | W1 | D2 | R-S | |
| 温度/℃ | 78.2 | 128.8 | 98.3 | 138.1 |
| n(乙醇)/% | 99.85 | 0.14 | 0.98 | 0 |
| n(丙酸乙酯)/% | 0 | 14.07 | 99.02 | 0.22 |
| n(对二甲苯)/% | 0.15 | 85.79 | 0 | 99.78 |
对比表 2至表 5发现,在设定的工艺参数中,溶剂比、回流比及萃取剂进料位置对塔顶主要产品的浓度影响较大,经优化后,B1塔塔顶乙醇的浓度达到了99.85%,B2塔塔顶采出中丙酸乙酯的含量增至99.02%,满足了分离的要求。
5 结论1) 按照溶剂相似相溶的原理及萃取剂筛选的评定原则,初步筛选了适合分离乙醇-丙酸乙酯二元共沸物系的萃取剂,并利用COSMO-SAC模型计算了待分离组分在萃取剂中的无限稀释活度系数,进而确定了对二甲苯适合作为最优的萃取剂。
2) 在101.3 kPa下,通过将汽液平衡实验数据与Wilson模型计算出来的汽液平衡数据作比对,实验值能与模拟值较好地吻合,表明Wilson模型可用来进行乙醇-丙酸乙酯-对二甲苯三元物系的萃取精馏模拟。
3) 运用Aspen Plus软件对乙醇-丙酸乙酯二元共沸物系进行连续萃取精馏模拟,并获得了优化后的工艺参数:萃取精馏塔中,原料进料位置为第50块塔板,萃取剂进料位置为第25块塔板,回流比为7,溶剂比为0.8,塔顶乙醇的含量可达到99.85%;溶剂回收塔中,进料塔板的位置为第11块塔板,回流比为6,塔顶得到丙酸乙酯含量为99.02%,塔釜回收液中萃取剂含量可达到99.78%以上。
| [1] | Kanwar S, Verma H, Kaushal R, et al. Effect of solvents and kinetic parameters on synthesis of ethyl propionate catalysed by poly(AAc-co-HPMA-cl-MBAm)-matrix-immobilized lipase of pseudomonas aeruginosa BTS-2[J]. World Journal of Microbiology and Biotechnology, 2005, 21(6/7): 1037–1044. |
| [2] |
林世静, 孙阳昭. 对甲苯磺酸催化合成丙酸乙酯[J].
北京石油化工学院学报, 2005, 13(1): 49–52.
Lin Shijing, Sun Yangzhao. Catalytic synthesis of ethyl propionate with p-toluene sulfonic acid[J]. Journal of Beijing Institufe of Petrochemical Technology, 2005, 13(1): 49–52. DOI: 10.3969/j.issn.1008-2565.2005.01.011 |
| [3] | Ortega J, Ocon J, Pena J, et al. Vapor-Liquid equilibrium of the binary mixtures CnH2n+1(OH)(n=2, 3, 4)+propyl ethanoate and+ethyl propanoate[J]. Canadian Journal of Chemical Engineering, 1987, 65(6): 982–990. DOI: 10.1002/cjce.v65:6 |
| [4] |
刘建新, 肖翔. 萃取精馏技术与工业应用进展[J].
现代化工, 2004, 24(6): 14–17.
Liu Jianxin, Xiao Xiang. Extractive distillation technology and its commercial application development[J]. Modern Chemical Industry, 2004, 24(6): 14–17. DOI: 10.3321/j.issn:0253-4320.2004.06.004 |
| [5] | Kyle G, Leng E. Solvent selection for extractive distillation[J]. IEEE Computational Intelligence Magazine, 1965, 57(2): 92–107. |
| [6] | Lek-Utaiwan P, Suphanit B, Douglas L, et al. Design of extractive distillation for the separation of close-boiling mixtures:Solvent selection and column optimization[J]. Computers & Chemical Engineering, 2011, 35(6): 1088–1100. |
| [7] | Lin T, Sandler I. A priori phase equilibrium prediction from a segment contribution solvation model[J]. Industrial & Engineering Chemistry Research, 2002, 41(5): 899–913. |
| [8] |
李瑞, 崔现宝, 吴添, 等. 基于COSMO-SAC模型的离子液体萃取剂的选择[J].
化工学报, 2013, 64(2): 452–469.
Li Rui, Cui Xianbao, Wu Tian, et al. Selection of ionic liquid solvent for liquid-liquid extraction based on COSMO-SAC model[J]. CIESC Journal, 2013, 64(2): 452–469. DOI: 10.3969/j.issn.0438-1157.2013.02.008 |
| [9] | 杨犁.基于COSMO-SAC模型和分子模拟预测复杂系统热力学性质[D].上海: 华东理工大学, 2012 Yang Li. Prediction of thermodynamic properties of complex systems based on COSMO-SAC model and molecular simulation[D]. Shanghai: East China University of Science and Technology, 2012(in Chinese) http://cdmd.cnki.com.cn/Article/CDMD-10251-1012338126.htm |
| [10] | Hou J, Xu S, Ding H, et al. Isobaric vapor-liquid equilibrium of the mixture of methyl palmitate and methyl stearate at 0.1 kPa, 1 kPa, 5 kPa, and 10 kPa[J]. Journal of Chemical & Engineering Data, 2012, 57(10): 2632–2639. |
| [11] | Tang G, Ding H, Hou J, et al. Isobaric vapor-liquid equilibrium for binary system of ethyl myristate+ethyl palmitate at 0.5, 1.0 and 1.5 kPa[J]. Fluid Phase Equilibria, 2013, 347: 8–14. DOI: 10.1016/j.fluid.2013.03.008 |
| [12] | Gil D, Botia C, Ortiz P, et al. Extractive distillation of acetone/methanol mixture using water as entrainer[J]. Industrial & Engineering Chemistry Research, 2009, 48(10): 4858–4865. |
 2018, Vol. 35
2018, Vol. 35





