随着先进便携式电子设备的广泛应用以及环境的压力, 人们对安全价廉、能量密度高且具有持久循环性能的可充电能源存储系统的需求越来越大,锂硫电池是其中最有应用前景的能源存储系统之一[1-3]。锂硫电池一般采用添加导电物质的单质硫作为正极,金属锂作为负极[4]。如果单质硫能够完全放电形成Li2S, 则锂硫电池的理论比容量可达1 675 Ah·kg-1,理论比能量可达2 600 Wh·kg-1,均比普通的锂离子电池高很多[5-6]。尽管锂硫电池具有上述优点,但在商业化过程中仍然存在着很多障碍。首先,在锂硫电池充放电过程中形成的长链多硫化物(Li2Sn, n=4~8)易溶解在电解液中,并能穿过隔膜在正负极之间迁移,造成所谓的穿梭效应,导致电池容量的衰减和库伦效率的降低,这也是制约锂硫电池进一步发展的主要阻碍[7]。其次,在锂硫电池充放电过程中,产物不断地在可溶物与不溶物之间转换,由单质硫(d=2.03 g·cm-3)到Li2S(d=1.66 g·cm-3)的体积变化带来的巨大机械应力容易使极片断裂,进而加速电池容量的衰减[8]。
为了解决多硫化物溶解等问题,国内外的研究工作者进行了大量的研究,Choi等[9-11]通过在硫电极中掺杂Al2O3、V2O5和TiO2等多孔材料来吸附易溶于电解液的多硫化物,进而起到抑制多硫化物穿梭效应的作用。由于分子筛SBA-15具有比表面积大、结构稳定、价格低廉等优点[12],本实验采用南京吉仓纳米科技有限公司生产的高纯介孔分子筛SBA-15,其主要成分为SiO2,将其均匀地添加在硫电极中并测试其电化学性能,通过与未掺杂分子筛SBA-15的电极进行对比,明确分子筛SBA-15的添加对锂硫电池电化学性能的影响。
1 实验方法 1.1 硫碳复合材料的制备以升华硫和介/微孔碳材料BP2000作为反应原料,加入适量的乙醇和球磨珠后以300 r/min的转速湿磨10 h,材料烘干后以同样的转速再干磨2 h。为弥补后面实验中硫的损失,确保有足够的硫可以进入碳孔中,根据经验在球磨时硫与BP2000按照7:2的质量比加入。将球磨后的材料放入石英舟中,在管式炉中加热。首先加热到155 ℃并恒温6 h,然后继续加热到280 ℃并恒温3 h,最后自然冷却,期间一直保持氮气保护。待冷却后将材料研磨后备用。
1.2 结构和形貌的表征采用日本Hitachi公司的S-4800场发射扫描电子显微镜(SEM), 荷兰FEI公司的Tecnai G2 F20型场发透射电子显微镜(TEM)对分子筛SBA-15的形貌及结构进行表征。采用EDAX公司的OXFORD-ISIS300能谱仪(EDS)对吸附过多硫化物的SBA-15进行表面元素含量分析。采用天津市兰力科公司的LK3200型电化学工作站、德国的Zahner IM6e电化学工作站对电池进行循环伏安(CV)、交流阻抗(EIS)等电化学性能测试。
1.3 电化学性能测试将硫碳热复合材料、乙炔黑和聚偏二氟乙烯(PVDF)按质量比7:2:1加入到研钵中, 加入适量N-甲基吡咯烷酮(AR, Aladdin, China)充分研磨混合后用刮刀将浆料均匀涂覆在涂碳铝箔上,在60 ℃的真空烘箱中干燥8 h,制作出普通的锂硫电池正极极片,记为SC。制作含有分子筛SBA-15的正极极片时,按照以上质量比加入上述原料,再分别加入一定量SBA-15使其分别占正极材料总质量的1.0%和1.5%,之后按上述步骤分别制作出含有1.0% SBA-15和1.5% SBA-15的极片,分别记为SCS-1.0和SCS-1.5。将烘干后的3种极片分别冲成直径为14 mm的小圆片作为电池的正极,在高纯氩气氛围的手套箱中,锂片作为电池的负极,多微孔的聚丙烯薄膜celgard 2000作为隔膜,含有1.0 mol/L双三氟甲烷磺酰亚胺锂(LiTFSI)和0.1 mol/L LiNO3的乙二醇二甲醚和1, 3-环氧五环的混合溶液(AR, Guotai-Huarong New Materials, China)作为电解液,最后组装成CR2032扣式电池。
2 结果与讨论 2.1 SBA-15的结构与形貌图 1a)和图 1b)分别为分子筛SBA-15的SEM图和TEM图。

|
| 图 1 SBA-15的a)SEM和b)TEM图,c)SBA-15在氮气下的吸脱附等温曲线及d)其孔径分布图 Figure 1 a) SEM and b) TEM images of SBA-15, c) Nitrogen sorption isotherms and d) pore size distribution of SBA-15 |
| |
由图 1a)可以看出,SBA-15是由粗细均匀的长细棒状的硅基材料堆积而成,SBA-15表面由于材料堆积而形成很多堆积孔,整体呈长条纤维状。由图 1b)的TEM图可看出,SBA-15具有二维六方孔道结构,孔道规整且分布有序。如图 1c)所示,SBA-15在氮气下的吸脱附等温线呈典型的Ⅳ型线,在P/P0=0.6~0.8时,吸附支和脱附支曲线呈陡峭的升降,且具有较大的滞后环出现,说明该样品为典型的介孔材料。由图 1d)的孔径分布曲线可以看出,SBA-15具有较窄的孔径分布,结合图 1b)表明SBA-15具有非常均匀的孔道,其平均孔径约为6.64 nm,由BJH方法测得的其总孔容为0.9182 cm3·g-1。SBA-15较大的孔道和孔容有利于多硫化物及电解液的运输及存储,有利于将多硫化物及电解液有效的吸附在硫电极内部,减少充放电过程中多硫化物的穿梭效应[13],同时SBA-15多孔的特性也可大大缓解电池充放电过程中单质硫和多硫化物之间不断转换而引起的极片的体积变化。
为了验证SBA-15对多硫化物的吸附作用,首先在氩气氛围的手套箱中,将S和Li2S按照物质的量之比3:1加入到乙二醇二甲醚(DME)和1, 3-环氧五环(DOX)的混合溶液(体积比为1:1)中,加热并搅拌8 h,得到Li2S4溶液,然后将干燥后的SBA-15浸泡在Li2S4溶液中1 h,之后用乙二醇二甲醚(DME)和1, 3-环氧五环(DOX)的混合溶液冲洗3次,干燥后使用扫描电子显微镜进行观察并分析其元素组成。图 2a)为经过上述操作后的SBA-15的SEM图,图 2b)~图 2d)为其局部元素的分布情况。由于采用的SBA-15分子筛主要由SiO2组成,所以图 2b)和图 2c)的硅元素和氧元素来自于SBA-15本身,而SBA-15本身不含硫,所以图 2d)中的硫元素应该来自于SBA-15吸附的多硫化物中的硫,证明SBA-15对多硫化物具有吸附作用。

|
| 图 2 a) SBA-15在Li2S4溶液中浸泡并清洗后的SEM图及其b)硅、c)氧、d)硫元素的分布情况 Figure 2 a) SEM images of SBA-15 after soaking in Li2S4 solution and washing, and the distribution of b) silicon, c) oxygen and d) sulfur elements |
| |
图 3为SCS-1.0极片的SEM图及表面元素的分布情况,其中碳和硫元素来源于硫碳复合材料,氧元素来源于SBA-15和黏结剂,其分布不能直观反映SBA-15的分布情况,而硅元素只来源于SBA-15,所以硅的分布情况可以直观反映SBA-15在极片中的分布情况,由于SBA-15的含量较少,所以代表硅元素的点相对较少。由图 3中可以看出极片表面颗粒均匀分布,各元素分布均匀,表明SBA-15与硫碳复合材料在极片中分散均匀。

|
| 图 3 SCS-1.0极片的SEM图及元素分布情况 Figure 3 SEM image of SCS-1.0 electrode and the distribution of elements |
| |
图 4为SC、SCS-1.0和SCS-1.5电池在0.1~2.0 C的倍率性能曲线,3个电池正极的含硫量分别为37.9%、38.1%和38.2%。通过观察发现,初始放电倍率为0.1 C时,初始放电产物和活性物质的不可逆流失,使得3种电池的放电比容量减少的速度均比较快,后续的放电容量逐渐稳定下来。0.2 C倍率下,SCS-1.0和SCS-1.5电池的放电比容量分别稳定在940和840 mAh·g-1左右,比SC电池的放电容量分别高110 mAh·g-1和40 mAh·g-1左右。随着放电倍率的增加,3种电池的放电比容量均呈现下降的趋势,当放电倍率增加到2.0 C时,SCS-1.0电池的放电比容量衰减到670 mAh·g-1左右,但仍然比SC电池的放电比容量高120 mAh·g-1左右,而SCS-1.5电池的放电比容量仅比SC电池的放电比容量高10 mAh·g-1左右。当放电倍率再次降低到0.1 C后,SCS-1.0电池的放电比容量快速恢复到907.1 mAh·g-1。3种电池的倍率性能曲线表明,SCS-1.0电池的倍率性能得到明显的提高,而SCS-1.5电池的倍率性能提高得不明显。这可能是由于SBA-15密集且均匀的孔道可为电解液以及多硫化物在充放电过程中的快速移动提供便利的通道,使极片与电解液的接触更充分,再加上SCS-1.0电池中SBA-15的添加量比较少且分散均匀,所以SCS-1.0电池的倍率性能得到明显提高。而SCS-1.5电池中添加SBA-15的量相对多一点,且SBA-15的导电性差,所以SCS-1.5电池的内阻也会相对增大,进而使得SCS-1.5电池的倍率性能提高的不明显。

|
| 图 4 SC、SCS-1.0和SCS-1.5电池的倍率性能曲线 Figure 4 The rate capabilities of SC, SCS-1.0 and SCS-1.5 cells |
| |
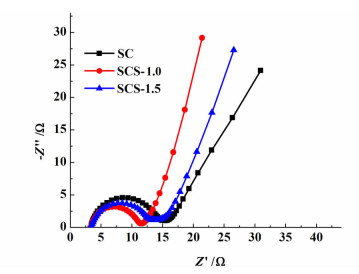
为了进一步研究SBA-15对锂硫电池电化学性能的影响,对3种电池的阻抗进行测试。图 5为SC、SCS-1.0和SCS-1.5 3种电池循环测试前的交流阻抗谱图。从图 5中可以看出,3种电池的交流阻抗图谱均由高频区的近似半圆和低频区的一条倾斜直线组成,近似半圆的半径代表的是电荷转移阻抗(Rct),斜线对应的是锂离子扩散进入材料内部的Warburg阻抗。对比发现,SCS-1.0和SCS-1.5电池的Rct均比SC电池的Rct小且SCS-1.0电池的Rct是3种电池中最小的。这可能是由于多孔的SBA-15对多硫化物起吸附作用,可减少多硫化物溶解到电解液中的量,降低了电解液的黏度,从而减少了充放电过程中电荷转移的阻力,但由于SBA-15导电性差,加入过量反而会增加电池电阻,所以加入适量的SBA-15对电化学反应促进作用最明显。这也进一步解释了SCS-1.0和SCS-1.5电池倍率性能提高的现象。综合3种电池的倍率性能和阻抗分析可知,加入1% SBA-15对电池性能的促进作用最明显,因此下面主要对SC和SCS-1.0电池的性能进行研究。
|
| 图 5 SC、SCS-1.0和SCS-1.5三种电池循环测试前的交流阻抗谱图 Figure 5 EIS curves of SC, SCS-1.0 and SCS-1.5 cells before the cycle test |
| |
图 6为SC和SCS-1.0电池的首次循环伏安曲线图,测试的电压范围为1.5~3.0 V,扫速为0.2 mV·s-1。如图 6所示,2种电池的循环伏安曲线均有2个阴极峰和1个阳极峰。在2.3 V左右峰面积较小的阴极峰对应高价态的长链多硫化物Li2Sn(4 < n < 8)还原成低价态的多硫化物的过程;在2.0 V左右峰面积较大的阴极峰对应低价态的多硫化物还原成Li2S2或Li2S的过程。在2.4 V左右的阳极峰对应的是Li2S2或Li2S转换成单质硫的过程。观察氧化还原峰的位置可以发现,添加1% SBA-15的SCS-1.0电池的2个还原峰的位置均向高电位方向有所偏移,氧化峰的位置则向低电位发生偏移,表明SCS-1.0电池具有更好的可逆性。此外,SCS-1.0电池的氧化还原峰的峰面积与SC电池的氧化还原峰的峰面积相比,均有不同程度的提高,表明添加1% SBA-15后,电池的容量也有所提高。

|
| 图 6 SC和SCS-1.0两种电池的循环伏安曲线图 Figure 6 Cyclic voltammograms of SC and SCS-1.0 cells |
| |
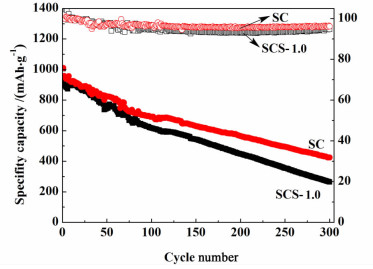
图 7为SC和SCS-1.0 2种电池在1 C倍率下充放电时的循环性能曲线。如图 7所示,随着循环次数的增加,SCS-1.0电池的循环性能比SC电池有明显的提高。含硫量为38.1%的SCS-1.0电池首次放电比容量可达1 010.9 mAh·g-1,含硫量为37.9%的SC电池的首次放电容量为1 000.8 mAh·g-1。随着循环次数的增加,SCS-1.0电池在放电容量上的优势越来越明显,可能是由于随着循环次数的增加,SC电池中越来越多的多硫化物溶解到电解液中,一方面使得硫电极的活性物质不断减少,另一方面使得电解液的黏度增大,进而使得电池电阻不断增大,而SBA-15的加入在一定程度上抑制了上述问题的发生。循环80圈后,SCS-1.0电池在容量上的优势越来越明显,循环300圈后,SCS-1.0电池的放电比容量比SC电池的放电比容量高160 mAh·g-1左右。SCS-1.0电池良好的循环性能得益于SBA-15较大的有序孔道可以吸附电解液和充放电过程中产生的溶于电解液的多硫化物,并为多硫化物溶液的传输提供通道,这样既可以减少多硫化物的流失,又可以从一定程度上解决由于多硫化物溶解而造成的电解液黏度升高的问题,使电解液与电极间的接触更加充分,接触的界面更加稳定。1% SBA-15的加入也使电池的库伦效率有所提高,SCS-1.0电池300圈循环的平均库伦效率比SC电池的平均库伦效率提高8%左右。
|
| 图 7 SC和SCS-1.0两种电池在1 C充放电时的循环性能曲线 Figure 7 Cycling performance of SC and SCS-1.0 cells at 1 C |
| |
将具有较大孔径的介孔分子筛SBA-15添加在锂硫电池的硫电极中,通过物理测试表明SBA-15对多硫化物具有吸附作用; 通过对添加和未添加SBA-15的电池进行一系列电化学测试表明:SCS-1.0电池表现出良好的循环性能和倍率性能,SCS-1.0电池第300循环的放电比容量比SC电池的放电比容量提高200 mAh·g-1左右,平均库伦效率比SC电池平均库伦效率提高8%左右。因此,在硫电极中添加1% SBA-15有利于减少多硫化物的穿梭,有利于锂硫电池电化学性能的提高。
| [1] | Bruce P G. Energy storage beyond the horizon:Rechargeable lithium batteries[J]. Solid State Ionics, 2008, 179(21): 752–760. |
| [2] | Zhang B, Kang F, Tarascon J M, et al. Recent advances in electrospun carbon nanofibers and their application in electrochemical energy storage[J]. Progress in Materials Science, 2016, 76: 319–380. DOI: 10.1016/j.pmatsci.2015.08.002 |
| [3] |
余聪聪, 张晶, 黄成德. 锂硫电池模拟与仿真[J].
化学工业与工程, 2017, 34(5): 89–95.
Yu Congcong, Zhang Jing, Huang Chengde. A mathematical model for a lithium-sulfur cell[J]. Chemcial Industry and Engineering, 2017, 34(5): 89–95. DOI: 10.3969/j.issn.1006-7906.2017.05.020 |
| [4] | Guo J, Yang Z, Yu Y, et al. Lithium-Sulfur battery cathode enabled by lithium-nitrile interaction[J]. Journal of the American Chemical Society, 2012, 135(2): 763–767. |
| [5] |
崔晓兰, 单忠强, 田建华. 聚乙烯吡咯烷酮包覆硫/碳复合材料的制备及其电化学性能[J].
化学工业与工程, 2014, 31(5): 20–24.
Cui Xiaolan, Dan Zhongqiang, Tian Jianhua. Polyvinylpyrrolidone coated sulfur/carbon composite cathode for high-rate lithium-sulfur batteries[J]. Chemcial Industry and Engineering, 2014, 31(5): 20–24. DOI: 10.3969/j.issn.1006-7906.2014.05.005 |
| [6] | Ma G, Wen Z, Jin J, et al. Hollow polyaniline sphere@sulfur composites for prolonged cycling stability of lithium-sulfur batteries[J]. Journal of Materials Chemistry A, 2014, 2(27): 10350–10354. DOI: 10.1039/C4TA00483C |
| [7] | Song M S, Han S C, Kim H S, et al. Effects of nanosized adsorbing material on electrochemical properties of sulfur cathodes for Li/S secondary batteries[J]. Journal of the Electrochemical Society, 2004, 151(6): A791–A795. DOI: 10.1149/1.1710895 |
| [8] | Ye J, He F, Nie J, et al. Sulfur/Carbon nanocomposite-filled polyacrylonitrile nanofibers as a long life and high capacity cathode for lithium-sulfur batteries[J]. Journal of Materials Chemistry A, 2015, 3(14): 7406–7412. DOI: 10.1039/C4TA06976E |
| [9] | Choi Y J, Jung B S, Lee D J, et al. Electrochemical properties of sulfur electrode containing nano Al2O3 for lithium/sulfur cell[J]. Physica Scripta, 2007, 129: 62–65. |
| [10] | Zhang Y, Wang L, Zhang A, et al. Novel V2O5/S composite cathode material for the advanced secondary lithium batteries[J]. Solid State Ionics, 2010, 181(17): 835–838. |
| [11] | Seh Z W, Li W, Cha J J, et al. Sulphur-TiO2 yolk-shell nanoarchitecture with internal void space for long-cycle lithium-sulphur batteries[J]. Nature Communications, 2013, 494: 1331. |
| [12] |
刘慧青, 吴春华, 陈保森, 等. SBA-15负载金属锡催化α-蒎烯环氧化反应[J].
化学工业与工程, 2016, 33(1): 29–34.
Liu Huiqing, Wu Chunhua, Chen Baosen, et al. Epoxidation of α-pinene on tin-modified mesoporous molecular sieve SBA-15[J]. Chemcial Industry and Engineering, 2016, 33(1): 29–34. |
| [13] | Ji X, Evers S, Black R, et al. Stabilizing lithium-sulphur cathodes using polysulphide reservoirs[J]. Nature Communications, 2011, 2: 101–104. |
 2018, Vol. 35
2018, Vol. 35





