2. 天津化学化工协同创新中心, 天津 300072;
3. 天津市功能精细化学品技术工程中心, 天津 300072
2. Collaborative Innovation Center of Chemical Science and Engineering, Tianjin 300072, China;
3. Tianjin Engineering Research Center of Functional Fine Chemicals, Tianjin 300072, China
非小细胞肺癌(ALK)是肺癌中最常见的组织学类型[1],其患者数量百分比高达85%。间变性淋巴瘤激酶(ALK)基因重排是NSCLC中重要的肿瘤驱动基因[2-3],针对ALK融合基因的小分子抑制剂TAE684、色瑞替尼(ceritinib)、克唑替尼(crizotinib)等可以有效抑制肿瘤细胞增殖、诱导肿瘤细胞凋亡,已经被广泛应用于临床治疗[4-9]。利用了分子靶向治疗特异性高,副反应少的优势[10-11]。
作为新药设计中的优势结构——嘧啶类化合物2, 5-二氯-N-[2-(异丙基磺酰基)苯]-4-胺具有抗肿瘤活性好、毒副作用小等优点,且受到药物化学工作者的高度重视,广泛应用于靶向ALK小分子抑制剂TAE684[12]、色瑞替尼(ceritinib)等药物分子的合成上,这使得2, 5-二氯-N-[2-(异丙基磺酰基)苯]-4-胺的合成工艺研究具备重要的应用价值和广阔的市场前景。
目前2, 5-二氯-N-[2-(异丙基磺酰基)苯]-4-胺的合成路线主要如下所示:
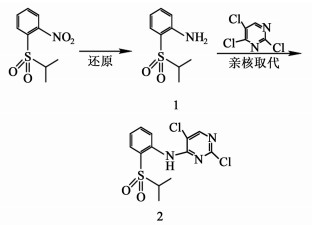 |
以l-(异丙基磺酰基)-2-硝基苯为起始原料,经过还原、亲核取代反应生成目标产物2, 5-二氯-N-[2-(异丙基磺酰基)苯]-4-胺(化合物2)。其中通过还原反应得到的产物2-(异丙基磺酰基)苯胺(化合物1),文献中主要用到的条件有:1)以钯为催化剂, 甲醇为溶剂,标准大气压的氢气还原反应6 h,产物的收率为88%[13]。2)以钯为催化剂,甲醇和四氢呋喃为溶剂,室温下还原反应4 h,产物的收率为91%[14]。文献中化合物2的合成主要是以N, N-二甲基甲酰胺(DMF)为溶剂,氢化钠为缚酸剂,经亲核取代反应制得,并没有对反应条件进行优化,产物的最高收率只有60%[15-17]。因此,目前公开报道的工艺总收率偏低。
本工作展开对化合物2的两步合成工艺研究,优化了第1步还原过程,反应收率达到94.9%;并对关键第2步亲核取代反应进行了反应条件的探究和优化,如溶剂的选择与配比、反应物的配比、缚酸剂的选择与配比、投料方式、后处理重结晶溶剂的选择,使得反应收率相对文献有所提高,达到72.2%,最终产物总收率提高至68.5%。反应后处理简单且产品纯度高,适合工业化生产。
1 实验部分 1.1 试剂与仪器氯化铵、锌粉、N, N-二甲基甲酰胺(DMF)、二甲基亚砜(DMSO),均为AR,天津市光复精细化工研究所;1-异丙基磺酰基-2-硝基苯、2, 4, 5-三氯嘧啶,北京百灵威科技有限公司;无水乙醇、石油醚、乙酸乙酯、二氯甲烷、无水硫酸钠、氢化钠,均为AR,天津科威化工有限公司;溶剂经过干燥及重蒸后使用;柱层析用硅胶(200~300目),烟台新诺化工有限公司。
20 L旋转蒸发仪(巩义市予华仪器有限责任公司);INOVA-500 MHz型核磁共振波谱仪(美国Varian公司);LCQ advantage MAX型液相色谱-ESI质谱联用仪(美国Temrmo fisher公司);LCQ advantage MAX型液相色谱-ESI质谱联用仪(美国Temrmo fisher公司)。
1.2 合成方法 1.2.1 化合物1的合成在250 mL三口瓶中依次加入l-(异丙基磺酰基)-2-硝基苯(5.00 g,22 mmol),氯化铵(4.80 g,90 mmol),无水乙醇和水的混合溶液[80 mL,m(无水乙醇)/m(水)=4],锌粉(10.00 g,153 mmol),机械搅拌下,缓慢升温至90 ℃,回流反应2 h,反应完毕后,冷却至室温,过滤,乙酸乙酯萃取、分液,用水多次洗涤有机相,干燥有机相并浓缩,以V(石油醚):V(二氯甲烷)=10:1对浓缩液进行重结晶,分离提纯得棕黄色固体4.16 g,收率为94.9%。1H-NMR(500 MHz, CDC13),δ:7.66~7.62(m,1H),7.40~7.30(m,1H),6.85~6.78(t,J=10.0 Hz,15.0 Hz,1H),6.73~6.70(d,J=10.0 Hz,1H),5.08(s,2H),3.40~3.30(m,1H),1.30~1.31 (d,J=5.0 Hz,6H);ESI-MS:m/Z=222.0[(M+Na)+](caled for C9H13NO2SNa+: m/Z=222.1)。
1.2.2 化合物2的合成在100 mL三口瓶中依次加入化合物1(1.20 g,6 mmol),DMF和DMSO的混合溶液[11 mL,V(DMF):V(DMSO)=10:1],磁力搅拌至完全溶解,溶液为浅棕色。在冰水浴条件下磁力搅拌,同时将氢化钠(0.10 g,4 mmol)缓慢加入DMF和DMSO混合溶液[3.7 mL,V(DMF):V(DMSO)=10:1]中制备成悬浊液,缓慢滴加至反应器中,搅拌15 min后,缓慢滴加溶解在DMF和DMSO[7.3 mL,V(DMF):V(DMSO)=10:1]中的2, 4, 5-三氯嘧啶(7.30 g,4 mmol)溶液,混合溶液搅拌15 min,然后将滴加氢化钠悬浊液与2, 4, 5-三氯嘧啶溶液的操作重复2次。室温搅拌2 h。反应完毕后,过滤,乙酸乙酯萃取、分液,用水多次洗涤有机相,无水硫酸钠干燥有机相并浓缩。以V(石油醚):V(二氯甲烷)=5:1对浓缩液进行重结晶,分离提纯得白色固体1.50 g,收率为72.2%。1H-NMR(500 MHz,CDCl3),δ:10.06(s, 1H),8.62~8.64(d,J=10.0 Hz,1H),8.30(s,1H),7.91~7.93(m,1H),7.70~7.75(m,1H),7.30~7.34(m,1H),3.18~3.24(m,1H),1.30~1.31(d,J=5.0 Hz,6H);ESI-MS:m/Z=346.1 [(M+H)+](caled for C9H14NO2S+:m/Z=346.0)。
2 结果与讨论由l-(异丙基磺酰基)-2-硝基苯得到化合物1,是典型的还原反应。锌粉还原法相对于氢气还原法等的优势在于锌粉与氯化铵来源广、价格低,且反应条件温和。在反应过程中,还原剂与溶剂的选择等对反应的影响很大,本研究通过优化反应条件,以锌粉为还原剂,弱酸性的氯化铵活化锌粉,乙醇和水为溶剂,加热回流反应2 h的反应条件,最后产物的收率提高至94.9%。
化合物1与2, 4, 5-三氯嘧啶的反应是典型的亲核取代反应,在反应过程中,反应溶剂及缚酸剂的选择十分关键,且反应物料的的配比及投料方式等对产物的收率也有很大影响。通过对比相关文献[15-17],我们发现此步反应具有很大的提升空间,因此考察了反应溶剂的选择及其配比、缚酸剂的选择及其用量、反应物的配比及投料方式、重结晶溶剂的选择对反应过程及产物收率的影响。
2.1 溶剂对产物的影响溶剂能使反应物有效扩散,增大反应物的接触,促进反应的进行,提高产率。本研究在其它条件不变的情况下,考察了不同的溶剂对产物的影响,并且文中用到的溶剂均除水,结果见表 1。
| 序号 | 溶剂 | 产物 |
| 1 | 二氯苯 | 无 |
| 2 | 喹啉 | 无 |
| 3 | 苯甲醚 | 无 |
| 4 | 1, 4-二氧六环 | 无 |
| 5 | 四氢呋喃 | 无 |
| 6 | N, N-二甲基甲酰胺 | 有 |
| 7 | 二甲基亚砜 | 无 |
结果表明,只有在溶剂DMF中才有产物生成,其它溶剂中均没有产物生成。DMF作为极性溶剂能使离去基团—Cl溶剂化,有利于—Cl的离去,从而促进反应的进行;DMF作为非质子性溶剂,其分子中的偶极正端由于位于内部而受到屏蔽,偶极负端暴露于分子外部,容易和其它分子的正端形成偶极-偶极端, 这样在亲核试剂的负端周围很少有溶剂分子,其本身为裸露状态,活性较大,使反应容易进行[18]。
同时,不同的溶剂配比对产物收率也是有影响的,因此,我们在其它条件相同的情况下,考察了不同的溶剂配比对反应的影响,结果见表 2。
| 序号 |
V(N, N-二甲基甲酰胺): V(二甲基亚砜) |
产物收率/ % |
| 1 | 0:1 | 0 |
| 2 | 5:1 | 43.4 |
| 3 | 10:1 | 62.2 |
| 4 | 15:1 | 54.2 |
| 5 | 1:0 | 41.9 |
结果表明,当V(DMF):V(DMSO)为10:1时,产物的收率最高,且明显高于单独使用溶剂DMF,这是因为DMSO的极性比DMF大,极性溶剂能使离去基团溶剂化,更有利于离去基团的离去,从而促进反应的进行。纯DMSO作为反应溶剂无法得到产物是2, 4, 5-三氯嘧啶溶解性很差造成的。因此,本实验选用溶剂的配比为V(DMF):V(DMSO)=10:1。
2.2 反应物配比对产物收率的影响我们发现,反应的过程中,当反应物配比不同时,产物的收率也不同,因此,本论文在其它条件相同的情况下,考察了不同的反应物配比对产物收率的影响,结果如表 3。
| 序号 |
n(2, 4, 5-三氯嘧啶)/ n[2-(异丙基磺酰基)苯胺] |
产物收率/ % |
| 1 | 1.6 | 55.4 |
| 2 | 1.8 | 62.3 |
| 3 | 2.0 | 65.8 |
| 4 | 2.2 | 66.0 |
| 5 | 2.4 | 66.1 |
结果表明,当n(2, 4, 5-三氯嘧啶)/n[2-(异丙基磺酰基)苯胺]=2.0时,产物收率提高的比较明显,而当其配比再增大时,产物收率变化并不大,并且由于2, 4, 5-三氯嘧啶的过量使得后处理及产物分离难度增加。因此,反应物的配比选择n(2, 4, 5-三氯嘧啶)/n[2-(异丙基磺酰基)苯胺]=2.0。
2.3 缚酸剂对产物的影响反应中会释放出HCl,为使反应平衡向生成物方向进行,需加入一定量的缚酸剂,以除去反应生成的HCl。不同的缚酸剂对反应的影响也比较显著, 通过实验,我们发现碳酸钾、碳酸铯为缚酸剂时没有产物生成,只有用氢化钠时才有产物生成, 因此本反应使用了缚酸剂氢化钠,并考察了缚酸剂用量对产物收率的影响,结果见表 4。
| 序号 |
n(氢化钠)/ n[2-(异丙基磺酰基)苯胺] |
产物收率/ % |
| 1 | 1.6 | 55.4 |
| 2 | 1.8 | 60.1 |
| 3 | 2.0 | 63.5 |
| 4 | 2.2 | 64.2 |
| 5 | 2.4 | 64.3 |
从表 4中可以看出,当n(氢化钠)/n[2-(异丙基磺酰基)苯胺]小于2.0时,产物收率较低,随着缚酸剂用量的增加,产物收率增大,当其物质的量之比为2:1时,收率最大,继续增加氢化钠的用量,反应收率并没有明显提高,因此我们选择n(氢化钠)/n[2-(异丙基磺酰基)苯胺]=2.0为缚酸剂较适宜的用量。
2.4 投料方式对产物收率的影响实验过程中,我们发现投料方式不同对产物的收率影响也比较大,因此我们在其他条件相同,保持投入的氢化钠与2, 4, 5-三氯嘧啶的总量一定的情况下, 考察了投料方式对产物收率的影响, 结果见表 5。
| 序号 | 氢化钠与2, 4, 5-三氯嘧啶分批次加入次数 | 产物收率/ % |
| 1 | 1 | 55.3 |
| 2 | 2 | 62.4 |
| 3 | 3 | 72.2 |
| 4 | 4 | 72.3 |
结果表明,随氢化钠与2, 4, 5-三氯嘧啶分批次加入的次数增加时,产物收率逐渐升高。当分3次加入时,产物的收率比较高,为72.2%,当分批次加入的次数再次提高时,对产物收率的影响不明显,因此,我们分3次加入氢化钠与2, 4, 5-三氯嘧啶。
2.5 后处理对产物收率的影响实验中,我们采取了3种混合溶剂进行重结晶操作,分别为V(石油醚):V(二氯甲烷)=5:1,V(环己烷):V(二氯甲烷)=5:1,V(正己烷):V(二氯甲烷)=5:1,在其它条件相同的情况下,考察了它们对产物收率的影响,结果见表 6。结果表明,当用V(石油醚):V(二氯甲烷)为5:1重结晶时,产物的收率最高。
| 序号 | 重结晶溶剂 | 产物收率/% |
| 1 | V(石油醚):V(二氯甲烷)=5:1 | 65.7 |
| 2 | V(环己烷):V(二氯甲烷)=5:1 | 62.1 |
| 3 | V(正己烷):V(二氯甲烷)=5:1 | 61.4 |
通过实验研究,本实验最后确定的条件如下:溶剂V(DMF)/V(DMSO)=10:1;反应物n(2, 4, 5-三氯嘧啶):n[2-(异丙基磺酰基)苯胺]=2:1;缚酸剂n(氢化钠):n[2-(异丙基磺酰基)苯胺]=2:1;并且,反应过程中分3次加入原料2, 4, 5-三氯嘧啶和缚酸剂氢化钠,重结晶溶剂选用V(石油醚):V(二氯甲烷)=5:1。
3 结论对重要的药物中间体2, 5-二氯-N-[2-(异丙基磺酰基)苯]嘧啶-4-胺的两步合成工艺进行了优化改进,通过确定第1步还原过程的条件:缚酸剂为氯化铵,还原剂为锌粉,溶剂为乙醇和水,使得反应收率达到94.9%;第2步亲核取代过程的条件:溶剂配比V(DMF):V(DMSO)=10:1,反应物配比n(2, 4, 5-三氯嘧啶):n[2-(异丙基磺酰基)苯胺]=2:1,缚酸剂用量n(氢化钠):n[2-(异丙基磺酰基)苯胺]=2:1,以及反应过程分3次加入原料2, 4, 5-三氯嘧啶和缚酸剂氢化钠的条件,使得反应收率提高到72.2%。最终产物总收率提高至68.5%。通过优化反应条件,使得药物中间体2, 5-二氯-N-[2-(异丙基磺酰基)苯]嘧啶-4-胺的合成适合工业化生产,从而用于靶向ALK小分子抑制剂TAE684、色瑞替尼等的合成研究,具有广阔的市场前景。
| [1] | Shaw A T, Solomon B. Targeting anaplastic lymphoma kinase in lung cancer[J]. Clinical Cancer Research, 2011, 17(8): 2081–2086. DOI: 10.1158/1078-0432.CCR-10-1591 |
| [2] | Ou S, Bartlett C, Mino-Kenudson M, et al. Crizotinib for the treatment of ALK-rearranged non-small cell lung cancer:A success story to usher in the second decade of molecular targeted therapy in oncology[J]. Oncologist, 2012, 17(11): 1351–1375. DOI: 10.1634/theoncologist.2012-0311 |
| [3] | Choi Y, Takeuchi K, Soda M, et al. Identification of novel isoforms of the EML4-ALK transforming gene in non-small cell lung cancer[J]. Cancer Res, 2008, 68(13): 4971–4976. DOI: 10.1158/0008-5472.CAN-07-6158 |
| [4] | Li Y, Ye X, Liu J, et al. Evaluation of EML4-ALK fusion proteins in non-small cell lung cancer using small molecule inhibitors[J]. Neoplasia, 2011, 13(1): 1–11. DOI: 10.1593/neo.101120 |
| [5] |
葛丹丹, 宫平. 色瑞替尼(ceritinib)[J].
中国药物化学杂志, 2014(5): 420–420.
Ge Dandan, Gong Ping. Ceritinib[J]. China Magazine Pharmaceutical Chemistry, 2014(5): 420–420. |
| [6] | Shaw A T, Kim D W, Nakagawa K, et al. Crizotinib versus chemotherapy in advanced ALK-positive lung cancer[J]. New England Journal of Medicine, 2013, 368(25): 2385–2394. DOI: 10.1056/NEJMoa1214886 |
| [7] | Ettinger D, Akerley W, Borghaei H, et al. Non-Small cell lung cancer, version 2. 2013[J]. J Natl Compr Canc Netw, 2013, 11(6): 645–653. DOI: 10.6004/jnccn.2013.0084 |
| [8] | Stockwell S. FDA approval for zykadia for late-stage lung cancer[J]. Oncology Times, 2014, 36: 10. |
| [9] |
陈少波, 张厚德. 克唑替尼抗肿瘤的研究进展[J].
中国现代医生, 2015(14): 156–160.
Chen Shaobo, Zhang Houde. Research progress of anti tumor of Crizotinib[J]. Chinese Modern Doctor, 2015(14): 156–160. |
| [10] | McDermott U, Iafrate A, Gray N, et al. Genomic alterations of anaplastic lymphoma kinase may sensitize tumors to anaplastic lymphoma kinase inhibitors[J]. Cancer Res, 2008, 68(9): 3389–3395. DOI: 10.1158/0008-5472.CAN-07-6186 |
| [11] | Chen J, Jiang C, Wang S. LDK378:A promising anaplastic lymphoma kinase (ALK) inhibitor[J]. J Med Chem, 2013, 56(14): 5673–5674. DOI: 10.1021/jm401005u |
| [12] | Galkin A, Melnick J, Kim S, et al. Identification of NVP-TAE684, a potent, selective, and efficacious inhibitor of NPM-ALK[J]. Proceedings of the National Academy of Sciences, 2007, 104(1): 270–275. DOI: 10.1073/pnas.0609412103 |
| [13] | Garcia-Echeverria C, Kanazawa T, Kawahara E, et al. 2, 4-Di(phenylamino)pyrimidines useful in the treatment of neoplastic diseases, inflammatory and immune system disorders: WO, 2004080980[P]. 2004-09-23 |
| [14] | Kwiatkowski N, Jelluma N, Filippakopoulos P, et al. Small-Molecule kinase inhibitors provide insight into Mps1 cell cycle function[J]. Nature Chemical Biology, 2010, 6(5): 359–368. DOI: 10.1038/nchembio.345 |
| [15] | Gray N, Zhou W. Compounds that modulate egfr activity and methods for treating or preventing conditions therewith: US, 12/976, 980[P]. 2010-12-22 |
| [16] | Marsilje T, Pei W, Chen B, et al. Synthesis, structure-activity relationships, and in vivo efficacy of the novel potent and selective anaplastic lymphoma kinase (ALK) inhibitor 5-chloro-N 2-(2-isopropoxy-5-methyl-4-(piperidin-4-yl) phenyl)-N 4-(2-(isopropylsulfonyl) phenyl) pyrimidine-2, 4-diamine (LDK378) currently in phase 1 and phase 2 clinical trials[J]. Journal of Medicinal Chemistry, 2013, 56(14): 5675–5690. DOI: 10.1021/jm400402q |
| [17] |
王永珍, 赵砚瑾, 胡文祥, 等. 2, 5-二氯-N-[2-(异丙基磺酰基)苯]-4-胺的合成[J].
昆明理工大学学报, 2012, 37: 300–304.
Wang Yongzhen, Zhao Yanjin, Hu Wenxiang, et al. Synthesis of 2, 5-dichloro-N-[2-(isopropylsulfonyl) phenyl]-pyrimidin-4-amine[J]. Journal of Kunming University of Science and Technology, 2012, 37: 300–304. |
| [18] |
邓维, 刘磊, 郭庆祥. 铜催化交叉偶联反应研究的新进展[J].
有机化学, 2004, 24(2): 150–165.
Deng Wei, Liu Lei, Guo Qingxiang. Recent progress in copper-catalyzed cross-coupling reactions[J]. Chinese Journal of Organic Chemistry, 2004, 24(2): 150–165. DOI: 10.3321/j.issn:0253-2786.2004.02.004 |
 2018, Vol. 35
2018, Vol. 35





