近年来,由于环境污染日趋严重,对油品中硫含量的要求也越来越严格。油品在内燃发动机燃烧过程中有98%的硫转化为SO2,其余作为硫酸盐排放,最终成为可吸入颗粒物的一部分[1],我国中北部地区雾霾天气的频繁出现与油品硫含量较高也不无关系,加快清洁油品的开发已是势在必行。吸附脱硫技术因具有操作条件温和、设备投资小、脱硫效果好、烯烃不被饱和、辛烷值损失小[2]等优点目前受到全世界众多研究者的广泛关注。常用的吸附剂有分子筛、活性炭、金属氧化物、金属有机骨架等[3],此外,管状纳米材料的出现为吸附脱硫提供了新的途径,Crespo等[4]研究表明碳纳米管对噻吩有良好的吸附作用。埃洛石纳米管(HNTs)作为一种天然的无机硅酸盐纳米管,相比碳纳米管和其他纳米管材料,天然无毒、储藏丰富、价格低廉并且具有较高的比表面积和吸附容量,被认为是相当有前景的吸附剂[5]。
埃洛石是由高岭石的片层(硅氧四面体层和管内的铝氧八面体层以1:1的比例组合而形成)在天然条件下卷曲而成,一般有20多层,片层中间是结晶水分子,大部分在自然界中以两端开口的管状形态存在[6]。HNTs的化学和热稳定性良好,表面具有的丰富表面羟基为其提供了较大的离子交换容量和较高的吸附能力[7]。目前HNTs经常用于吸附染料及重金属等污染物,例如Kiani等[8]利用HNTs吸附水溶液中的银离子,最大吸附量达到109.79 mg/g。HNTs在吸附噻吩等硫化物方面的报道较少。齐晓晔等[9]研究发现HNTs本身具有一定的吸附脱硫效果,但脱硫能力有限。有机改性是常见的提升材料性能的方法,在诸多材料领域都有应用[10]。HNTs的层间和内管有较大的修饰空间,可以为有机物的改性提供场所。Mahrez等[11]发现二甲基亚砜改性后的HNTs对于结晶紫有良好的吸附性能,吸附量达到93.6 mg/g。本工作利用有机物二甲基亚砜(DMSO)、甲醇(CH3OH)和表面活性剂十六烷基三甲基溴化铵(HDTMA)为原料对HNTs进行改性,研究了不同有机物改性对HNTs的结构以及吸附脱硫性能的影响,并考察了吸附温度、时间、剂油比对吸附剂脱硫性能的影响。
1 实验部分 1.1 原料和试剂埃洛石纳米管(HNTs,产自广西);二甲基亚砜、甲醇、乙醇、十六烷基三甲基溴化铵、氯化钠、噻吩、正辛烷、溴甲酚绿、甲基红、甲基橙(均为分析纯,购于天津光复精细化工研究所)。
1.2 实验步骤和方法 1.2.1 有机物改性HNTs的制备采用插层法制备[12]HNTs-DMSO和HNTs-CH3OH。在使用前用去离子水对HNTs进行多次洗涤、抽滤,80 ℃常压干燥,研磨过100目筛。取10 g HNTs分散于100 mL DMSO和9 mL H2O的混合溶液中,60 ℃下超声4 h,抽滤干燥制得HNTs-DMSO。将HNTs-DMSO加入一定量甲醇,水浴搅拌24 h,离心分离,洗涤抽滤干燥制得HNTs-CH3OH。
采用离子交换法制备[13]HNTs-HDTMA。取HNTs加入到一定量1 mol/L HCl溶液,搅拌2 h,静置24 h,抽滤,用蒸馏水洗至中性,加一定量1 mol/L NaCl溶液,搅拌48 h,洗涤至不含氯离子,用硝酸银溶液检验,105 ℃烘干,记为HNTs-Na。取2 g HNTs-Na加入100 mL HDTMA溶液,60 ℃搅拌12 h,洗涤抽滤,90 ℃烘干3 h,研磨过筛制得HNTs-HDTMA。
1.2.2 吸附脱硫实验将噻吩溶解于正辛烷溶液中,配制成噻吩含量约为3 000 μg·g-1的模拟汽油。分别取10 mL的模拟汽油置于锥形瓶,按照不同的剂油比[吸附剂质量(g)与模拟油体积(mL)之比]加入一定量的吸附剂样品,然后放在恒温磁力搅拌器上不同温度下搅拌4 h,静态吸附反应后离心分离,取2 mL上层清液采用GB-T 380燃灯法[14]对测定硫含量,脱硫率I和容硫量S通过式(1)和式(2)计算:
| $ I = \frac{{{X_0}-{X_1}}}{{{X_0}}} \times 100\% $ | (1) |
| $ S = \frac{{{X_0}-{X_1}}}{{m/M}} $ | (2) |
其中X0是待测油品硫含量,mg/g;X1是经吸附剂吸附脱硫过后油品的硫含量,mg/g;m是吸附剂用量,g;M是待测油品用量,g。
1.2.3 表征采用荷兰Panalytical公司X′Pert Pro型X射线衍射仪测定样品的晶相结构,辐射源为Co_Kα;采用Nexus FT-IR红外光谱仪测定样品的傅里叶变换红外吸收光谱,扫描范围4 000~300 cm-1;采用Tecnai G2 F20型透射电子显微镜观测样品的微观形貌;采用Quantachrome QuadraSorb SI型全自动吸附仪进行N2吸附-脱附测试,样品先在120 ℃真空条件下处理4 h,再在77 K下进行测试,以BET法计算比表面积,BJH法计算孔径分布。
2 结果与讨论 2.1 XRD表征结果图 1是经过有机物改性过后埃洛石纳米管的XRD谱图。

|
| 图 1 HNTs及其有机改性复合物的XRD图 Figure 1 XRD patterns of HNTs and its organic modification products |
| |
从图 1中可以看到经过有机物改性后的样品在2θ为23.35°、28.61°、40.90°及64.30°处仍然具有埃洛石纳米管的特征衍射峰,表明埃洛石纳米管的基本结构并未破坏,HNTs的(001)面衍射峰在2θ=14.167°处,该峰显示了埃洛石纳米管结构单元层间距,对应的d001=0.72 nm[15]。从HNTs-DMSO的XRD谱图中可以看到经过DMSO改性后,2θ=14.167°处的特征峰明显减弱,而在2θ=9.242°处产生了1个新的(001)面衍射峰,对应的层间距d001=1.110 nm,与文献[11]报道一致,说明DMSO成功插入了HNTs层间使其间距变大。CH3OH的插入与DMSO类似,从HNTs-CH3OH的XRD图中看到原(001)面衍射峰明显减弱,新的(001)面衍射峰出现在2θ=9.404°处,对应的层间距d001=1.091 nm。插层反应的程度(φ)可以通过(001)面衍射峰的强度的比值来计算[16]:
| $ \varphi = {I_{\rm{c}}}/({I_{\rm{c}}} + {I_{\rm{k}}}) $ | (3) |
Ic和Ik分别表示插层复合物新产生的d(001)衍射峰和纯埃洛石d(001)衍射峰的相对强度。由公式可以计算出HNTs-DMSO和HNTs-CH3OH复合物的插层率分别为85.5%和80.7%。HNTs-HDTMA是HNTs通过离子交换法和HDTMA合成的,从HNTs-HDTMA谱图可以看到HNTs的(001)面在2θ=9.200°处,d001=1.153 nm,而2θ=14.167°处仍然出现了较强的HNTs原(001)晶面衍射峰,说明只有部分HDTMA进入了HNTs层间,复合物的插层率为43.2%。
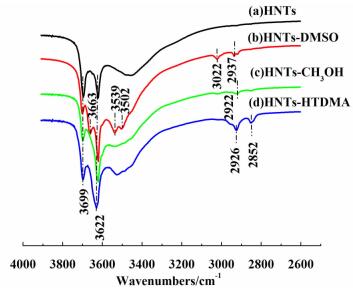
2.2 红外表征结果埃洛石纳米管中有2种羟基基团,波数为3 622 cm-1处的吸收峰是内羟基(硅氧四面体和铝氧八面体构成的层状结构的共享面上)伸缩振动吸收峰,波数为3 699 cm-1处的吸收峰是内表面羟基(非共享面上)的伸缩振动吸收峰[17],图 2为不同有机物改性HNTs的红外光谱图。
|
| 图 2 HNTs及其有机改性复合物的红外谱图 Figure 2 FTIR spectra ofHNTs and its organic modification products |
| |
由图 2可见,经过DMSO插层处理后,HNTs位于3 622 cm-1处的内羟基伸缩振动峰强度未改变,而位于3 699 cm-1处的内表面羟基伸缩振动峰强度减弱,在3 663、3 539和3 502 cm-1处出现了新的吸收峰,这可能是由于原HNTs层间的氢键被破坏,而内表面羟基与DMSO中的S=O基团形成了新的氢键。3 022和2 937 cm-1处出现的吸收峰是DMSO中2个甲基的振动吸收峰。CH3OH的插入同样使得HNTs原层间的氢键破坏,内表面羟基与CH3OH中的羟基形成了新的氢键,所以3 663 cm-1的吸收峰减弱,并且在2 922 cm-1处出现了甲基的振动峰。经过HDTMA改性后,HNTs的红外光谱在2 926和2 852 cm-1处出现2个新的吸收峰,这2个吸收峰分别代表—CH3、—CH2—的变形振动和伸缩振动,表明季铵盐阳离子已接枝在埃洛石纳米管表面。
2.3 电镜和BET表征结果HNTs和HNTs-HDTMA的透射电镜图如图 3所示。

|
| 图 3 HNTs及HNTS-HDTMA的投射电镜图 Figure 3 TEM images of HNTs and HNTS-HDTMA |
| |
埃洛石纳米管具有中空管状结构,两端开口,管道通畅,尺寸分布均匀,长度约0.5~1.0 μm,管内径约20~30 nm,外径约50~70 nm,经过HDTMA修饰后,管壁明显变厚,管径变小,说明季铵盐阳离子进入了HNTs管内。另外BET测试结果发现有机物改性后HNTs的比表面积变化不大,DMSO和CH3OH改性后比表面积由51.24 m2/g增加到55.29和53.02 m2/g,而HDTMA改性后比表面积减小到了48.85 m2/g,可能是由于HDTMA覆盖了埃洛石内表面以及堵塞了部分微孔所致。
HNTs和HNTs-HDTMA的氮气吸附脱附曲线和如图 4所示。

|
| 图 4 HNTs及HNTs-HDTMA的N2吸附脱附曲线 Figure 4 N2 adsorption/desorption isotherms of HNTs and HNTs-HDTMA |
| |
由图 4可知HNTs及HNTs-HDTMA的吸附等温线线均符合第Ⅳ类等温线模型(依据IUPAC分类)[18],HNTs表面同时存在微孔和介孔,随着压力的升高产生H3型的滞后回线是因为在介孔中发生了毛细管凝聚现象。
HNTs和经HDTMA改性过后HNTs的孔径分布如图 5所示。

|
| 图 5 HNTs及HNTs-HDTMA的孔径分布图 Figure 5 The pore diameter distribution of HNTs and HNTs-HDTMA |
| |
由图 5可知经HDTMA改性后HNTs在3~6 nm的微孔和12~20 nm之间的介孔都有所减少,可能是HDTMA在HNTs管内接枝以及插入HNTs层间导致。
2.4 脱硫性能分析 2.4.1 不同有机物改性的HNTs脱硫性能表 1列出了不同有机物改性后的吸附脱硫性能。
| 吸附剂样品 | 脱硫率/% | 容硫量/(mg·g-1) | 容噻吩量/(mg·g-1) |
| HNTs | 29.62 | 4.74 | 12.45 |
| HNTs-DMSO | 46.33 | 7.41 | 19.46 |
| HNTs-CH3OH | 44.57 | 7.13 | 18.72 |
| HNTs-HDTMA | 58.85 | 9.42 | 24.72 |
由表 1可以看出有机物改性后埃洛石纳米管的吸附脱硫性能有不同程度地提高。经过DMSO和CH3OH改性后,脱硫率相比于未改性的29.62%,分别提高到46.33%和44.57%,而HDTMA改性后脱硫率提升最明显,脱硫率达到了58.85%。噻吩分子大小约0.53 nm,而埃洛片层间距大概0.72 nm,从XRD谱图对比可以看出经过二甲基亚砜和甲醇改性后层间距提高到1.1 nm左右,这可能使得噻吩能更容易的进入埃洛石纳米管层间从而提高了其吸附能力。与HNTs-DMSO和HNTs-CH3OH相比,HNTs-HDTMA的脱硫率较高,可能由于管径变化而引起的,埃洛石内径大约10~30 nm,相对于分子尺寸较小的噻吩来说,埃洛石较大的管径可能不利于其吸附,经过季铵盐阳离子表面活性剂HDTMA修饰后,从电镜图中看到其管径明显变小,可能更利于噻吩的吸附。
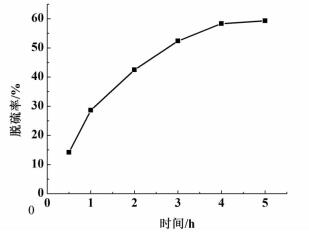
2.4.2 吸附条件对吸附剂脱硫性能的影响在温度为30 ℃,剂油比为1:20的条件下,测定了不同时间下HNTs-HDTMA吸附脱硫效果,结果如图 6所示。
|
| 图 6 吸附时间对HNTs-HDTMA脱硫性能的影响 Figure 6 Effect of adsorption time on desulfurization of the HNTs-HDTMA |
| |
由图 6可知随着时间的增加,吸附剂的脱硫率逐渐增大,在4 h后吸附量基本达到饱和,不再随时间变化,此时吸附剂的活性位基本被占据完全,因此最适宜吸附时间确定为4 h。
在时间为4 h,剂油比为1:20的条件下,测定了不同温度下HNTs-HDTMA吸附脱硫能力。结果见图 7。

|
| 图 7 吸附温度对HNTs-HDTMA脱硫性能的影响 Figure 7 Effect of adsorption temperature on desulfurization of HNTs-HDTMA |
| |
由图 7可知,随着温度的升高,吸附剂的脱硫率先增大后减小,在30 ℃脱硫率最大,温度过高时,可能由于噻吩分子的热运动速度加快使得脱附速率大于吸附速率,发生脱附现象,导致吸附性能下降。因此确定30 ℃为适宜的吸附脱硫温度。
在吸附温度为30 ℃,吸附时间为4 h的条件下考察了剂油比对吸附剂脱硫性能的影响,结果如图 8所示。

|
| 图 8 剂油比对HNTs-HDTMA脱硫性能的影响 Figure 8 Effect of ratio of adsorbent to oil on desulfurization of HNTS-HDTMA |
| |
由图 8可知,随着剂油比的升高,脱硫率和吸附剂的硫容量呈现相反的变化趋势。这是应为在相同处理量下情况下,剂油比升高会使吸附剂提供的吸附位点增多从而导致脱硫率升高,但是吸附剂的利用率会降低,单位质量吸附剂的硫容量会减小。综合考虑选择适宜的剂油比为1:20。
3 结论经过甲醇和二甲基亚砜插层改性后,埃洛石纳米管的管状基本结构没有发生改变,但是层间距发生了一定的改变,插层使得埃洛石的层间距变大,并且吸附脱硫性能增强。经过十六烷基三甲基溴化铵改性后,埃洛石的内径变小,吸附脱硫性能增强,在温度为30 ℃、时间为4 h、剂油比为1:20的条件下容硫量达到9.42 mg/g,脱硫率由未改性HNTs的29.62%提高到58.85%。
| [1] |
石亚华.
石油加工过程中的脱硫[M]. 北京: 中国石化出版社, 2009 Shi Yahua. The desulfurization of petroleum processing[M]. Beijing: China Petrochemical Press, 2009. |
| [2] | Zhang Q, Shi L, Meng X. Deep adsorption desulfurization of liquid petroleum gas by copper-modified bentonite[J]. RSC Advances, 2016, 6: 9589–9597. DOI: 10.1039/C5RA21729F |
| [3] | Ahmed I, Jhung S H. Adsorptive desulfurization and denitrogenation using metal-organic frameworks[J]. Journal of Hazardous Materials, 2016, 301: 259–276. DOI: 10.1016/j.jhazmat.2015.08.045 |
| [4] | Crespo D, Yang R. Adsorption of organic vapors on single-walled carbon nanotubes[J]. Industrial and Engineering Chemistry Research, 2006, 45: 5524–5530. DOI: 10.1021/ie051106b |
| [5] | Rawtani D, Agrawal Y K. Multifarious applications of halloysite nanotubes:Review[J]. Reviews on Advanced Materials Science, 2012, 30(3): 282–295. |
| [6] | Zhou C, Keeling J. Fundamental and applied research on clay minerals:From climate and environment to nanotechnology[J]. Applied Clay Science, 2013, 74(1): 3–9. |
| [7] | Kamble R, Ghag M, Gaikawad S, et al. Halloysite nanotubes and applications:A Review[J]. Journal of Advanced Scientific Research, 2012, 3(2): 25–29. |
| [8] | Kiani G. High removal capacity of silver ions from aqueous solution onto halloysite nanotubes[J]. Applied Clay Science, 2014, 90(12): 159–164. |
| [9] |
祁晓烨, 马智, 张园园, 等. 埃洛石纳米管表面结构对其吸附脱硫性能的影响[J].
化学工业与工程, 2016, 33(5): 21–25.
Qi Xiaoye, Ma Zhi, Zhang Yuanyuan, et al. Effects of surface structure on the desulfurization properties of halloysite nanotubes[J]. Chemical Industry and Engineering, 2016, 33(5): 21–25. |
| [10] |
马智, 朱伟佳, 刘焕焕, 等. 硅铝酸盐纳米管的有机改性研究现状[J].
硅酸盐通报, 2015, 34(5): 1282–1289.
Ma Zhi, Zhu Weijia, Liu Huanhuan, et al. Research progress on organic modificatian for aluminumsilicate nanotube[J]. Bulletin of the Chinese Ceramic Society, 2015, 34(5): 1282–1289. |
| [11] | Mahrez N, Bendenia S, Marouf-Khelifa K, et al. Improving of the adsorption capacity of halloysite nanotubes intercalated with dimethyl sulfoxide[J]. Composite Interfaces, 2015, 22(6): 403–417. DOI: 10.1080/09276440.2015.1036581 |
| [12] | Tan D, Yuan P, Annabi-Bergaya F, et al. A comparative study of tubular halloysite and platy kaolinite as carriers for the loading and release of the herbicide amitrole[J]. Applied Clay Science, 2015, 114: 190–196. DOI: 10.1016/j.clay.2015.05.024 |
| [13] | Liu R, Fu K, Zhang B, et al. Removal of methyl orange by modified halloysite nanotubes[J]. Journal of Dispersion Science & Technology, 2012, 33(5): 711–718. |
| [14] | 抚顺石油工厂. GB/T 380-1977石油产品硫含量测定法(燃灯法)[S]. 北京: 中国标准出版社, 1988 Fushun oil factory. GB/T 380-1977 Determination of sulfur content in petroleum products(lamp method)[S]. Beijing: Standards Press of China, 1988(in Chinese) |
| [15] | Joussein E, Petit S, Churchman J, et al. Halloysite clay minerals-A review[J]. Clay Miner, 2005(40): 383–426. |
| [16] | Sugahara Y, Satokawa S, Kuroda K, et al. Evidence for the formation of interlayer polyacrylonitrile in kaolinite[J]. Clays and Clay Minerals, 1988, 36(4): 343–348. DOI: 10.1346/CCMN |
| [17] | Yuan P, Tan D, Annabi-Bergaya F, et al. Changes in structure, morphology, porosity, and surfaces activity of mesoporous halloysite nanotubes under heating[J]. Clays and Clay Minerals, 2012, 60(6): 561–573. DOI: 10.1346/CCMN.2012.0600602 |
| [18] | Sing K S W. Reporting physisorption data for gas/solid systems with special reference to the determination of surface area and porosity (Recommendations 1984)[J]. Pure and Applied Chemistry, 1985, 57(4): 603–619. DOI: 10.1351/pac198557040603 |
 2018, Vol. 35
2018, Vol. 35





