2. 晋城市阿邦迪能源有限公司, 山西 晋城 048000
2. Jincheng Abound Energy Ltd., Shanxi Jincheng 048000, China
锂离子电池由于具有高能量密度和长寿命而广泛地应用于各种便携式电子产品、电动/混合动力汽车等领域[1]。目前商业化的负极碳材料的理论比容量仅为372 mAh·g-1,不能够满足更高能量密度电池对负极材料的需求。SnO2理论比容量为790 mAh·g-1,充放电平台低(0.6 V vs. Li/Li+),作为可期待的新型锂离子电池负极材料近年来引起了人们的广泛关注[2]。但是SnO2导电性差,而且在充放电过程中与锂合金化形成LixSn(0 < x < 4.4)的合金,体积变化高达300%,引起脱嵌锂过程中发生巨大的体积膨胀,进而造成与集流体脱离、粉化,循环性能随之衰减,这在一定程度上限制了SnO2作为锂离子电池负极材料的应用。
目前,有效解决上述问题的方法之一是优化SnO2结构并将其与碳材料进行复合[3-6]。采用碳材料可以提高电极整体的导电性,同时可以抑制SnO2电极在多次充放电循环过程的结构破损,进而提高SEI膜的稳定性。另一方面,多级结构SnO2不仅具有相对大的比表面积,而且其规整有序的结构相对缩短了锂离子传输路径,有利于减少充放电过程的粒子团聚。Lee等通过柯肯达尔效应制备的中空二氧化锡与石墨的复合物(复合物中SnO2质量分数为60%),利用石墨作为抑制充放电过程材料的体积膨胀,同时二氧化锡可以抑制石墨层与层之间的堆叠。该复合物在0.1 C倍率放电下循环50次容量保持在300 mAh·g-1,相对未复合石墨的SnO2电极容量保持率更高[7]。Gurunathan等通过溶胶法,制备出SnO2多孔微球与碳的复合物(其中SnO2质量分数为50%)。当材料在1.0 C倍率充放电时,首次放电容量为800 mAh·g-1,循环50次后容量仍可达725 mAh·g-1,容量保持率达92%[8]。Lian等制备出的多孔SnO2@C/石墨烯复合物(SnO2质量分数为40%),结构上由石墨烯片层组成三维网状导电网络结合多孔SnO2@C纳米球有效的抑制了SnO2体积膨胀导致容量衰减的问题,电极在100 mA·g-1电流密度下,循环50次容量保持在1 000 mAh·g-1,几乎无衰减[9]。Chen等制备的介孔核壳结构SnO2@C电极(SnO2质量分数为78%),0.3 C恒倍率充放电40次,容量保持在680 mAh·g-1,同时体现了较好的倍率性能[10]。综上可知,将其它结构的SnO2与碳复合可以显著提高材料的电化学性能,因此将多级结构SnO2与碳进行复合可作为改善SnO2电化学性能的一种有效途径。
采用适宜的材料复合方法和合理的组成可以有效地改善SnO2电极充放电循环性能。因而本研究采用水热法制备了多级结构花状SnO2/C复合物,探究了该种多级结构SnO2的制备工艺以及其作为锂离子电池负极材料应用的可能性,制备过程设备简易、易于控制。由于葡萄糖聚合物碳化后的无定形碳在电导和抑制电极形变的良好辅助作用,SnO2/C复合物相对SnO2在循环寿命、倍率性能方面有了显著提高,有效缓解了SnO2充放电过程中容量的衰减。
1 实验 1.1 材料制备采用水热法,称量5.529 g分析纯(质量分数大于99%)SnCl4·5H2O为锡源,4.5 g葡萄糖(碳源)溶于25 mL蒸馏水中。将上述体系磁力搅拌20 min以确保葡萄糖全部溶解。待葡萄糖全部溶解形成均一相的透明溶液时,将上述体系转移至50 mL反应釜内衬中,密封后在马弗炉中加热至180 ℃后,在180 ℃下恒温保持24 h,然后取出反应釜置于空气中冷却至室温。将棕色反应产物用乙醇和蒸馏水反复洗涤3次后,置于鼓风干燥烘箱中60 ℃烘干,待干燥后取相同质量的2份样品分别置于空气氛围和氩气氛围中于600 ℃下煅烧4 h,自然冷却后,即得到多级结构SnO2和SnO2/C复合物。
1.2 电池的组装与制备按8:1:1的质量比分别称取一定量活性物质、导电剂(Super P瑞士Timical公司)、黏结剂(聚偏氟乙烯),加入适量的N-甲基吡咯烷酮作为分散剂,研磨0.5 h混合均匀后,用涂片器将研磨好的浆料均匀地涂布在铜箔上,60 ℃下烘1 h后,放入真空烘箱中,120 ℃烘8 h。用冲片机冲成小圆片,制得工作电极,以金属锂(99.9%,天津中能锂业)为负极,以多孔聚丙烯膜(Celgard 2000)为隔膜,以1 mol/L的LiPF6/EC-DEC(体积比为1:1)作为电解液(天津金牛电源材料有限公司),组装成CR2032型电池。静置12 h后,在充放电测试仪(CT2 001 A,Land)进行电化学性能测试。电池在电压范围为5 mV~2 V(vs. Li/Li+)之间以200 mA·g-1的电流密度下进行恒电流密度充放电循环。在电压范围为5 mV~2 V(vs. Li/Li+),以0.2 mV·s-1进行循环伏安测试(CHI660 A,上海辰华有限公司)。在频率范围为100 kHz~10 mHz,扰动振幅为±5 mV进行交流阻抗测试(Ivium,荷兰Ivium Technologies BV公司)。
1.3 材料的物理性能表征采用X射线衍射仪(XRD,D/max 2500,RigaK)对材料进行晶体结构分析。使用场致发射扫描电子显微镜(SEM,S-4800,Hitachi)观察样品的形貌、颗粒大小。使用透射电子显微镜(TEM,JEM-2100F, 日本电子)来观察材料的超微结构和晶体的晶格结构。
2 结果与讨论 2.1 多级结构SnO2制备工艺的研究调控SnO2结构的关键参数是水热过程中SnCl4的浓度。本研究分别采用0.05、0.10、0.30、0.50、0.70和1.00 mol/L的SnCl4水溶液制备出SnO2,图 1是样品的SEM图。

|
| 图 1 不同浓度的SnCl4溶液制备的SnO2材料SEM图 Figure 1 SEM images of SnO2 prepared by different concentration of SnCl4 solution |
| |
从图 1可以看出,低浓度(0.05 mol/L和0.10 mol/L)下制备的SnO2为纳米颗粒,且0.05 mol/L制备出的SnO2颗粒团聚程度较大;浓度达到0.30 mol/L时,样品呈现花状趋势,但由于SnO2的含量过少,导致形成的花状结构存在未完全负载在模板上,SnO2层不均匀。当浓度提高为0.50 mol/L时,SnO2呈现尺寸在2.5 μm左右的花状微球。仔细观察可以发现,花状微球是由尺寸在150 nm左右、表面为纳米颗粒的中空小球组装而成,SnO2呈现为多级结构;而继续提高浓度(0.70和1.00 mol/L),SnO2微球直径增大至2 μm左右,且浓度越大团聚现象越严重,花状结构消失。故适宜的合成多级结构SnO2的SnCl4溶液浓度为0.5 mol//L。SnO2/C复合物的制备的工艺条件的选择也以合成多级结构SnO2的反应参数为依据。
2.2 多级结构SnO2及其与碳复合物的物化性能图 2为所制备的SnO2/C复合物与SnO2的XRD图谱。
|
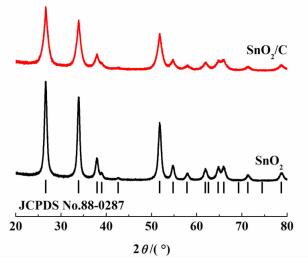
| 图 2 SnO2/C复合物与SnO2 XRD图谱 Figure 2 RD patterns of SnO2/C composite and SnO2 |
| |
从图 2中可以看出,2个样品的特征峰位置一致,均与四方晶系SnO2标准谱图(JCPDS No.88-0287)吻合。XRD图谱上的2θ在26.6°、33.9°和51.8°处的衍射峰分别对应SnO2的(110)、(101)和(211)晶面,没有明显的杂峰,说明反应后葡萄糖炭化为无定形碳,对SnO2的晶型没有影响。
图 3为在多级结构SnO2的基础上制备的SnO2/C复合物的SEM图片。

|
| 图 3 SnO2/C复合物的SEM图片 Figure 3 SEM images of SnO2/C composite |
| |
图 3中可以观察到SnO2/C复合物花状微球平均直径约为2 μm,且表面颗粒堆积更致密规整,其结构可以进一步通过TEM图表征。SnO2/C复合物中的碳含量采用模拟热重法,测得SnO2/C复合物中碳含量为28.39%。
图 4a)和图 4b)分别为SnO2/C复合物的低倍和高倍TEM图谱。

|
| 图 4 SnO2/C复合物的TEM图谱和HRTEM图谱 Figure 4 TEM images of and HRTEM images of SnO2/C composite |
| |
从图 4a)中可以看出,SnO2/C复合物的的形貌与SEM观察的结果一致,内部无定形碳与外部SnO2分层清晰。图 4b)是图 4a)中所示方框的局部放大图,图中标示的晶面间距0.356和0.188 nm分别对应SnO2的(211)晶面和(110)晶面,TEM测试结果与XRD测试结果相对应,进一步证实了所制备的SnO2/C复合物的结晶性良好。
2.3 SnO2及其与碳复合物的电化学性能SnO2/C复合物电极和SnO2电极在200 mA·g-1恒电流密度下循环50次的循环性能曲线如图 5a)所示。图 5b)所示为SnO2/C复合物电极和SnO2电极在不同电流密度下的倍率循环曲线。
|
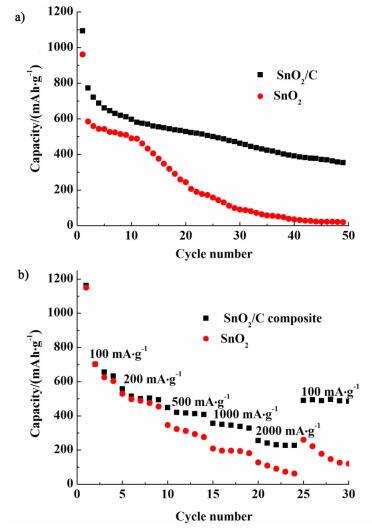
| 图 5 SnO2/C复合物电极和SnO2电极在200 mA·g-1恒电流密度下循环50次的循环性能曲线a)及SnO2/C复合物电极和SnO2电极在不同电流密度下的倍率循环曲线b) Figure 5 Cycling performance of SnO2/C composite electrode and SnO2 electrode at current density of 200 mA·g-1 over 50 cycles a) and rate capacity of SnO2/C composite electrode and SnO2 electrode b) |
| |
从图 5a)可以看出SnO2电极循环12次后,容量仍可保持在460 mAh·g-1,呈现出较好的循环性能,但循环50次后比容量仅保持在20.6 mAh·g-1,出现明显的容量衰减。而SnO2/C复合物电极在循环50次后仍可保持在346.1 mAh·g-1,容量保持较好。如此明显的容量提高可能有以下原因:1)是中空花状SnO2电极可以在一定程度上缓解充放电过程的体积膨胀,但随着循环次数增多,中空结构破坏[11];2)是引入碳源,提高了材料的导电性。无定形碳作为SnO2材料充放电循环过程中的缓冲基底,有效的缓解了SnO2材料充放电过程中体积膨胀的问题[12]。
从图 5b)中可以看出,SnO2/C复合物电极呈现出较好的倍率循环曲线。在低电流密度100 mA·g-1下充放电循环5圈后,SnO2/C复合物电极容量保持在632.4 mAh·g-1;当充放电电流密度增加到1 000 mA·g-1,SnO2/C复合物电极循环5圈后容量保持在328.5 mAh·g-1;电极在2 000 mA·g-1下循环5圈后容量保持在227.8 mAh·g-1,当充放电电流密度回到100 mA·g-1时,SnO2/C复合物电极容量仍可以达到490.2 mAh·g-1,容量保持率为初始放电比容量的77.51%。这说明SnO2/C复合物中无定形碳的支撑可以有效的缓解SnO2充放电过程中的膨胀效应,提高了SnO2电极的倍率性能。然而,SnO2电极随在前10次循环中容量与SnO2/C复合物电极容量相当,但随着充放电电流密度的增加容量而逐渐降低,当充放电电流密度为2 000 mA·g-1时,电极循环5圈后仅为62.9 mAh·g-1。这说明在大电流下循环充放电时,SnO2的体积膨胀效应会更加剧烈,加速材料结构的破坏,从而导致在大电流密度下循环性能差[13]。
图 6a)为SnO2/C复合物电极在室温下的循环伏安曲线,测试范围为:5 mV~2 V(vs. Li/Li+),扫速为0.2 mV·s-1。图 6b)为SnO2电极在相同条件下的循环伏安曲线。
|
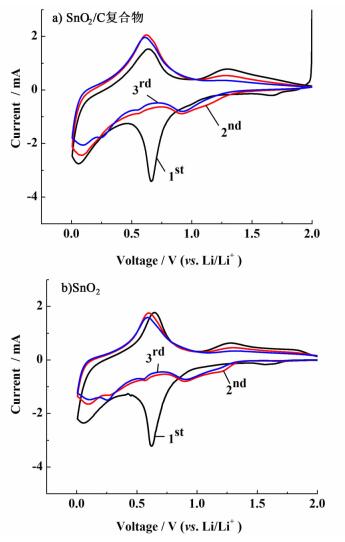
| 图 6 电极循环伏安曲线 Figure 6 Cyclic voltammograms |
| |
从图 6中可以看出,首圈在0.66 V左右有1个强的还原峰,在之后的循环过程中,该峰消失,此峰对应着的是SEI膜的形成;在0.61和1.30 V的氧化峰分别对应着LixSn的去合金化生成金属锡的过程。0.09和0.66 V处的还原峰分别对应金属Sn与Li合金化形成LixSn的过程[14]。第2次和第3次循环,上述氧化峰与还原峰的位置没有明显变化,这意味着首圈后,锂离子的嵌入和脱出的可逆程度较好[15]。从图 6b)中可以看出,其氧化还原峰的峰值电流低于复合物电极,且位于0.62 V的峰值电流随着循环次数继续降低,峰值电位逐渐负移,氧化峰与还原峰的峰值电位差值变大,说明极化程度加大,电化学反应的可逆程度降低[16]。
图 7所示为SnO2/C复合物电极和SnO2电极在200 mA·g-1恒电流密度下充放电50次后的交流阻抗图及等效电路图。
|
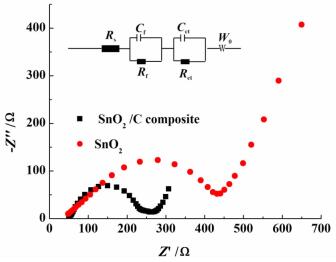
| 图 7 SnO2/C复合物电极和SnO2电极充放电50次后的交流阻抗图及等效电路图 Figure 7 The Nyquist plot of SnO2/C electrode and SnO2 electrode after 50 cycles |
| |
交流阻抗图由高频、中频的半圆和低频的斜线组成。高频区的半圆对应着由SEI膜引起的接触阻抗,中频区为电荷转移阻抗,低频区的斜线对应着锂离子扩散进入电极材料晶格中引起的Warburg阻抗。从图 7中可以看出,SnO2/C复合物电极在循环50次后的电荷转移阻抗远远小于SnO2电极,模拟得到的SnO2/C复合物电极的电荷转移阻抗为85.59 Ω,SnO2电极的为164.38 Ω。这是由于经与碳复合后,材料的导电性更好,提高了电荷转移速率,从而提高电极的容量保持率[17]。
3 结论通过水热法制备出了结晶度良好的多级结构SnO2/C复合物。结果表明复合物中碳的支撑可以有效缓解SnO2电极在充放电过程中的体积膨胀问题,SnO2/C复合物电极的循环性能和倍率性能均有所提高。200 mA·g-1恒电流密度充放电循环50次后仍可保持在346.1 mAh·g-1,容量保持较好。倍率性能测试中SnO2/C复合物电极经过高电流密度(1 000和2 000 mA·g-1)的充放电循环后电流密度再回到100 mA·g-1时,容量保持率为初始充放电比容量的77.51%。因此,这也进一步证实了,具有良好结构和电化学性能的SnO2/C复合物作为锂离子电池负极材料的可行性。
| [1] | Tang Y, Zhang Y, Li W, et al. Rational material design for ultrafast rechargeable lithium battery[J]. Chem Soc Rev, 2015, 44: 5926–5940. DOI: 10.1039/C4CS00442F |
| [2] | Wang Z, Zhou L, Lou X. Metal oxide hollow nanostructures for lithium-ion batteries[J]. Advanced Materials, 2012, 24(14): 1903–1911. DOI: 10.1002/adma.v24.14 |
| [3] | Tian G, Huang K, Qi X, et al. Free-Standing SnO2 nanoparticles@graphene hybrid paper for advanced lithium-ion batteries[J]. Ceramics International, 2014, 40(5): 6891–6897. DOI: 10.1016/j.ceramint.2013.12.009 |
| [4] | Liu H. SnO2 sheet/graphite composite as anode material with improved electrochemical performance for lithium-ion batteries[J]. Journal of Sol-Gel Science and Technology, 2014, 72(3): 644–647. DOI: 10.1007/s10971-014-3536-9 |
| [5] | Ding L, He S, Miao S, et al. Ultrasmall SnO2 nanocrystals:Hot-Bubbling synthesis, encapsulation in carbon layers and applications in high capacity Li-ion storage[J]. Scientific Reports, 2014, 4: 4647. |
| [6] | Liu S, Zhu K, Tian J, et al. Submicron-Sized mesoporous anatase TiO2 beads with trapped SnO2 for long-term, high-rate lithium storage[J]. Journal of Alloys and Compounds, 2015, 639: 60–67. DOI: 10.1016/j.jallcom.2015.03.116 |
| [7] | Lee Y, Jo M R, Song K, et al. Hollow Sn-SnO2 nanocrystal/graphite composites and their lithium storage properties[J]. ACS Applied Materials & Interfaces, 2012, 4(7): 3459–3464. |
| [8] | Gurunathan P, Ette P M, Ramesha K. Synthesis of hierarchically porous SnO2 microspheres and performance evaluation as Li-ion battery anode by using different binders[J]. ACS Applied Materials & Interfaces, 2014, 6: 16556–16564. |
| [9] | Lian Pe, Wang J, Cai D, et al. Porous SnO2@C/graphene nanocomposite with 3D carbon conductive network as a superior anode material for lithium-ion batteries[J]. Electrochimica Acta, 2014, 116: 103–110. DOI: 10.1016/j.electacta.2013.11.007 |
| [10] | Chen L, Yin X, Mei L, et al. Mesoporous SnO2@carbon core-shell nanostructures with superior electrochemical performance for lithium ion batteries[J]. Nanotechnology, 2012, 23(3): 035402. DOI: 10.1088/0957-4484/23/3/035402 |
| [11] | Yin X, Chen L, Li C, et al. Synthesis of mesoporous SnO2 spheres via self-assembly and superior lithium storage properties[J]. Electrochimica Acta, 2011, 56(5): 2358–2363. DOI: 10.1016/j.electacta.2010.11.072 |
| [12] | Liang J, Yu X, Zhou H, et al. Bowl-Like SnO2@carbon hollow particles as an advanced anode material for lithium-ion batteries[J]. Angewandte Chemie, 2014, 53(47): 12803–12807. DOI: 10.1002/anie.201407917 |
| [13] | Zhang L, Zhang G, Wu H, et al. Hierarchical tubular structures constructed by carbon-coated SnO2 nanoplates for highly reversible lithium storage[J]. Advanced Materials, 2013, 25(18): 2589–2593. DOI: 10.1002/adma.201300105 |
| [14] | Wu H, Chen J, Lou X, et al. Synthesis of SnO2 hierarchical structures assembled from nanosheets and their lithium storage properties[J]. The Journal of Physical Chemistry C, 2011, 115(50): 24605–24610. DOI: 10.1021/jp208158m |
| [15] | Liu L, An M, Yang P, et al. Superior cycle performance and high reversible capacity of SnO2/graphene composite as an anode material for lithium-ion batteries[J]. Scientific Reports, 2015, 5: 9055. DOI: 10.1038/srep09055 |
| [16] |
陈然, 虞桢君, 詹亮, 等. 黏结剂对SnO2/石墨烯负极材料电化学行为的影响[J].
化学工业与工程, 2014, 31(3): 44–49.
Chen Ran, Yu Zhenjun, Zhan liang, et al. Effects of binders on the electrochemical performance of SnO2/graphene anode material[J]. Chemical Industry and Engineering, 2014, 31(3): 44–49. |
| [17] | Tan C, Cao J, Abdul M K, et al. High-Performance tin oxide-nitrogen doped graphene aerogel hybrids as anode materials for lithium-ion batteries[J]. Journal of Power Sources, 2014, 270: 28–33. DOI: 10.1016/j.jpowsour.2014.07.059 |
 2018, Vol. 35
2018, Vol. 35





