超级电容器(supercapacitor)是一种介于传统电容器和电池之间的新型储能元件,具有功率密度高、充电时间短、使用寿命长、温度特性好、节约能源和绿色环保等特点,被广泛应用于移动通讯、信息技术、消费电子、电动汽车、航空航天和国防科技等领域,成为研究的重点[1-2]。
金属氧化物作为超级电容器的电极材料利用其自身的氧化还原反应产生赝电容,其比电容值高于基于多孔碳材料的双电层的比电容值。在过去的研究中,过渡金属氧化物因为其高理论比容量受到广大研究者的重视,其中RuO2的电容值可以达到720 F/g,但因为其价格高昂并且对于环境有污染不能被广泛应用[3]。相比较而言,锰系材料因其简单易得和环境友好性在电化学领域受到欢迎,例如Mn(OH)2[4]和MnMoO4[5]。其中以MnO2为应用最广的材料,因为其理论比容量高达1 370 F/g[6]。最近,Devaraj等[7]发现MnCO3也具有储能的特性,在0.1 mol/L的Mg(ClO4)2电解液中比容量达到了216 F/g。但是因为其导电性较差、充放电可逆性能比较差,制约了其应用前景。
为了解决这个问题,很多科学家尝试采用形成复合物的方法解决这个问题[8],他们使用比表面积较大的导电材料为基底,将活性物质负载在上面,构成三维结构。导电材料作为内部传输通道起到了传递电子的作用,极大程度的提高了活性物质的利用率,成为解决此类问题的主要方法。作为基底的导电材料一般选用石墨烯和碳纳米管[9-10],但是C6大规模堆叠使得原始的碳结构没有缺陷,从而影响了反应的活性,而且,这2种材料往往制备方法复杂,不能大规模的生产。而对于本研究选用的炭黑(CB),其外表面有细微的石墨烯层,使得炭质材料的缺陷能够分布在整个表层,大大提高了反应活性。而且炭黑材料的高比表面积、堆积所造成的三维孔道结构和简单易得等优点也成为本研究选择的原因。
本研究首次以粒径40 nm左右的炭黑颗粒作为载体将碳酸锰颗粒包裹,使粒径700 nm左右的碳酸锰颗粒之间通过颗粒尺寸小并且导电性好的炭黑颗粒连接,外部的炭黑颗粒之间形成含有空隙的立体结构。电化学性能方面,复合材料的质量比容比单纯的碳酸锰材料相比翻了1倍,在5 mV/s的扫速下达到了218 F/g,在1 100次循环后的容量保持率达到了92%,较好地克服了金属氧化物活性物质溶解的缺点。合成复合材料为碳酸锰材料的应用提供了新的思考方向,拓宽了碳酸盐类材料的应用领域。
1 实验部分 1.1 主要试剂和仪器设备实验中用到的主要试剂有碳酸氢铵NH4HCO3(AR),硫酸锰MnSO4(AR),硝酸HNO3(AR)。
实验中用到的主要仪器有Philip XL30型场发射扫描电子显微镜(FESEM),加速电压设置为20 kV;日本理学D/max X射线衍射仪(XRD),λ=0.15406 nm;日本岛津TA-50热重分析仪(TGA),氮气气氛下升温速率10 ℃/min。
1.2 MnCO3/CB复合材料的制备商用CB(Vxc-72,256 m2/g,Carbot)用稀硝酸和稀硫酸在80 ℃下水热处理3 h,后用蒸馏水洗至中性。取净化后的CB 0.15 g加入一定量的蒸馏水超声处理30 min,使其均匀分散,称取2 mmol的硫酸锰加入上述混合液中,并持续搅拌3 h。随后将3 mmol的碳酸氢铵缓慢的滴加进上述的混合液中,持续搅拌3 h至反应结束。将沉淀离心用蒸馏水洗涤数次至中性,真空干燥后得到复合物。
1.3 电极的制作将MnCO3/CB复合物和聚四氟乙烯(PTFE)按质量分数95:5称取后分散于无水乙醇中,经超声震荡分散均匀后,真空烘箱中干燥12 h,使用压片机将电极浆料压在500目的不锈钢网上,后与集流体泡沫镍相连接制得电极片。在电化学测试中,采用三电极的测试手段,所用的电解液均为1 mol/L Na2SO4溶液,饱和Hg/Hg2SO4电极作为参比电极,Pt电极作为对电极。
2 结果与讨论 2.1 稀酸纯化对炭黑表面官能团的影响本实验中使用商用CB,加入稀硫酸和稀硝酸后在80 ℃条件下水热3 h,目的是除去CB表面的金属和其他杂质,同时我们发现经过稀酸处理的CB表面的负电基团数量增多,结果如图 1所示,炭黑颗粒表面增加的负电基团(羧基和醌基)使得粒子在水溶液中均匀分散,并且有利于合成均匀的复合物。本研究中采用红外光谱来考察CB表面官能团变化。由图 1可知,位于3 000~3 400 cm-1的强吸收峰是炭黑表面的羟基的伸缩振动峰和KBr吸水所造成的吸收峰;1 047 cm-1处的弱吸收峰表明炭黑表面存在的C—O单键;1 600~1 700 cm-1范围内的强吸收峰属于类醌结构中的C=O双键和—COOH结构中的C=O双键的伸缩振动峰。从红外光谱分析中,我们确定了经过稀酸处理的CB表面的羰基、羧基和醌基等基团的数量增加,表面的电负性增强,有利于在溶液中分散均匀并合成复合物。

|
| 图 1 稀酸纯化后的炭黑颗粒的红外光谱图 Figure 1 FT-IR spectrum of purified CB |
| |
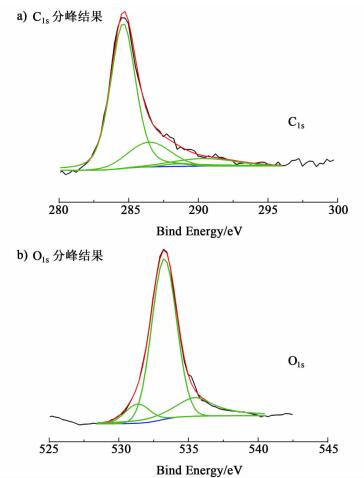
图 1中的红外光谱分析属于定性分析CB表面的官能团,了解了其表面的官能团情况,之后采用XPS光电子能谱分析来定量的分析经过稀酸纯化后CB表面负电基团的情况。C1s和O1s的XPS分峰的曲线在图 2的a)和b)展示,其中黑色为原始测试曲线,蓝色为背景基线,绿色为分峰曲线,红色为拟合曲线,具体的相对峰面积在表 1中展示。
|
| 图 2 经稀酸纯化后炭黑表面XPS谱图 Figure 2 Deconvolutional peak spectrums of purified CB |
| |
| 光电子 | 峰位置/eV | 峰面积比/% |
| C1 s | 290.3 | 9.6 |
| 288.4 | 2.4 | |
| 286.4 | 29.7 | |
| 284.6 | 58.3 | |
| O1 s | 535.4 | 16.9 |
| 533.2 | 71.9 | |
| 531.3 | 11.2 |
对于C1s,有4种不同的结合能的碳原子,结合能为290.3 eV的碳原子属于相邻基团为醌基的较强吸电子基团—COOH上的碳原子,占了所有碳原子中的9.6%;结合能为288.4 eV的碳原子属于内酯类或者弱酸—COOH中的碳原子,只有2.4%;结合能为286.4 eV的碳原子属于醌基中的碳原子占了总碳原子的29.7%,表明在炭黑的颗粒表面和层间的结构中有大量醌基基团和少量的羧基基团;结合能为284.6 eV的碳原子是炭黑本身稠环结构上的碳原子,占了最大的58.3%。对于O1s,有3种不同的结合能的氧原子,结合能为535.4 eV的氧原子是属于炭黑的表面吸附的O2和H2O的结果,占了总氧原子的16.9%;结合能为533.2和531.3 eV的氧原子分别是炭黑表面的C=O键和C—O键中的氧原子,其中C=O双键中的氧原子占了总原子数的71.9%[8]。通过XPS和FT-IR 2种表征手段,我们断定,经过稀硝酸和稀硫酸纯化后的炭黑表面含有大量带有负电的基团(羧基、醌基等),使得在水体系中可以分散均匀,有利于合成均匀的复合物。
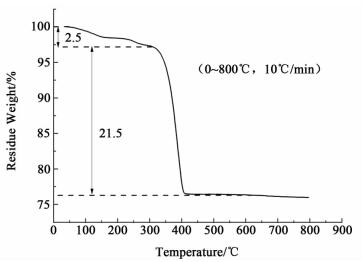
2.2 复合物结构与形貌表征为了确定MnCO3在CB中的负载量,对复合物进行了热失量分析。图 3是复合物在氮气气氛下,温度范围是0~800 ℃,升温速率是10 ℃/min的热失量曲线。
|
| 图 3 MnCO3/CB在氮气气氛下的热失量曲线 Figure 3 TGA curve of MnCO3/CB composite under N2 |
| |
从曲线分析可知,在350 ℃时,失量率达到2.5%,对应着样品中物理吸附水和层间水的质量损失。另一处失量主要集中在400 ℃左右,这一阶段主要是MnCO3受热分解,反应方程式为:
| $ {\rm{MnC}}{{\rm{O}}_{\rm{3}}} \to {\rm{MnO + C}}{{\rm{O}}_{\rm{2}}} \uparrow $ | (1) |
在350~800 ℃之间的失量率达到了21.5%,因为除了结合水失量,仅有此处失量,所以结合文献认定为失去的质量为二氧化碳逸出量,根据反应方程式质量守恒可知MnCO3在混合物中的负载率约为60%[10]。
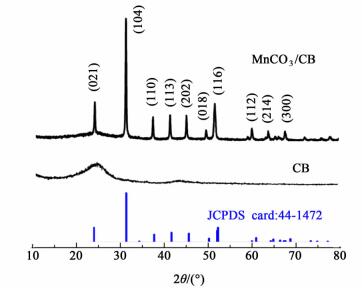
图 4所示是MnCO3/CB复合物和CB的XRD衍射图谱,根据衍射峰对应角度索引可知,MnCO3/CB复合物中的MnCO3晶型为Hexagon型(JCPDS no.44-1472)。复合物峰强度大且形状很尖锐,证明合成的MnCO3结晶性很好。从CB图谱的衍射峰上,根据其2θ的值和半峰宽的距离可以计算出CB的晶格参数La为4.07 nm,这一晶格参数表示了CB的微晶尺寸;根据复合物的XRD峰计算可知复合物中MnCO3颗粒的晶格参数为a=b=0.4790,c=0.17694 nm,该尺寸对于标准的Hexagon型MnCO3(晶胞参数为a=b=0.4810 nm,c=0.1575 nm)来说,在z轴的方向上有所伸长,原因是合成复合物过程中CB表面的缺陷活性位导致层状结构的取向性发生变化,使得晶体粒子的尺寸发生了变化[12-13]。这2个衍射峰图谱对比可以看出CB的衍射峰在复合物的图谱中表现得很不明显,这是因为CB在25°处的衍射峰与MnCO3的(021)峰重合,发生了择优诱导效应,主要表现为MnCO3的强度大而且峰形尖锐的(021)峰。
|
| 图 4 复合物和炭黑的XRD图 Figure 4 XRD results of MnCO3/CB composite and CB |
| |
图 5a)和图 5b)为复合物的扫描电镜图,为了确定颗粒表面的组成,对SEM中的对应位置进行EDS测试,结果列在表 2中。由结果可知,大颗粒组成为MnCO3,因其表面有少量炭黑颗粒的存在,C元素的含量较高,而少量的S元素的含量也是因为炭黑颗粒的存在导致的。由于EDS所测得只是选定的局部表面的元素含量,并不代表整个复合物中的物质的负载量,只做定性研究用。通过复合物的扫描电镜图 5a)可以看出,合成的MnCO3晶体为圆球形莲花状,直径为700~800 nm, 被包裹在絮状的导电炭黑颗粒中,分散均匀。该种莲花状的MnCO3晶体相比于表面光滑的球形,有效的增大了与电解液的接触面积,增加了可以发生赝电容反应的活性位点,有利于提高材料的比电容。图 5b)显示碳酸锰外层导电炭黑颗粒堆积,颗粒直径大约40 nm,而且制成的复合材料并不仅仅是单纯的包裹,还存在没有紧密包裹在碳酸锰外部的炭黑颗粒,连接起来形成了立体的含有空隙的空间结构,这种结构不仅可以有利于电子的传输和导通,也使得电解液中的离子可以通过形成的孔隙结构更好的与材料的内部相接触,进而提高材料的比容量[14]。

|
| 图 5 MnCO3/CB复合物的a), b)FESEM和对应部位的EDS图 Figure 5 a), b)FESEM result of MnCO3/CB composite and EDS result of corresponding part |
| |
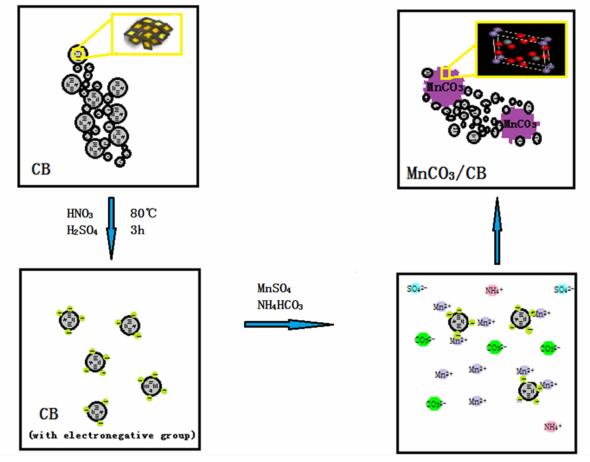
图 6所示是MnCO3/CB复合物合成过程的机理示意图。
|
| 图 6 MnCO3/CB复合物合成机理示意图 Figure 6 The schematic illustration of preparation of MnCO3/CB composite |
| |
一开始炭黑为近球形的无规则多面体结构,粒子间有强烈的凝聚趋势,容易形成“葡萄串状”的结合体,粒径为20~50 nm,其表面为层状的类石墨烯片层。加入稀硫酸和稀硝酸后在80 ℃条件下水热3 h,目的是除去CB表面的金属和其他杂质,并且炭黑颗粒表面增加的负电基团(醌基和羧基基团)使得颗粒在水溶液中均匀分散有利于复合物的制备。在加入了MnSO4和NH4HCO3溶液后,首先炭黑表面的负电基团固定溶液中的正电离子Mn2+,随着时间的进行,溶液中的CO32-与Mn2+形成沉淀,并通过炭黑表面裸露的炭原子将其固定在晶体表面。晶体生长一段时间之后,炭黑表面的炭原子虽然参与了复合,其缺陷位上的其他炭原子仍可以继续固定离子,使得晶体进一步长大,这也是复合物中的碳酸锰晶体粒子的大小比单纯溶液沉淀所得的碳酸锰晶体粒子要大得多的原因[15]。
2.4 电化学性能表征为了进一步确定MnCO3/CB材料的电容特性,将纯碳酸锰和复合物的EIS情况进行对比,结果在图 7a)中展示。EIS主要是从电极动力学的方面来考察材料的性能的,其中高频区半圆弧左端点对应的数值表示整个体系的接触电阻,半圆弧的半径表示了电极充放电电荷的转移电阻(Rct);中频区的直线为Warburg阻抗区,表示电解质离子在电极空隙结构中的扩散电阻[16],如图 7b)中的等效电路图所示。

|
| 图 7 a) 纯MnCO3和MnCO3/CB复合物的阻抗曲线;b)EIS等效电路图 Figure 7 a) Nyquist plots for MnCO3 and composite; b) EIS equivalent circuit diagram |
| |
对比图 7a)中的2条曲线可知,MnCO3材料在与CB复合之后阻抗谱图在高频区的Rct由1.23 Ω减少到0.53 Ω,这是由于加入了CB使得电子转移速度加快,动力学性能得到了显著的改善。中频区的直线也出现了一些不同,与CB进行复合之后,Warburg阻抗区的长度明显地减小,这是由于在复合后,CB的小颗粒堆积在尺寸较大的MnCO3周围,使得电解质离子在活性材料内部扩散阻力变小。通过EIS曲线可知复合材料整体的内阻减小,更有利于获得更好的电化学性能。
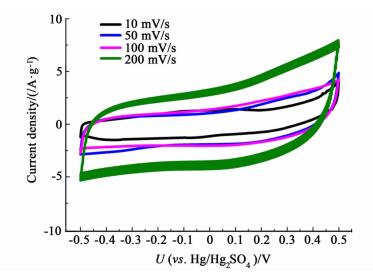
为了进一步研究MnCO3/CB复合材料用作电容器电极时的电化学性能,采用循环伏安表征手段来测试材料在不同的扫描速率下的电容特性,以及采用循环1 100次来测试材料的长时间循环稳定性。图 8所示的是材料在不同扫描速率下的循环伏安图。
|
| 图 8 MnCO3/CB复合物在不同扫描速率下的循环伏安曲线 Figure 8 CV curves of MnCO3/CB composite at different scan rates |
| |
在小扫速下,CV曲线保持矩形的形状,虽然两端出现了部分极化现象,但是整体图形呈现镜面对称,表明了其良好的可逆性。在曲线上并没有出现明显的氧化还原峰,说明在活性物质表面和内部的法拉第反应稳定地进行,当电位发生变化时,响应电流做出反应的速度较快。这是因为,合成的复合物中,CB的良好的导电性和复合物的三维结构有利于电子在体系中的流动,使得反应中所需要的电子能够及时有效地被运输,从而使整个反应能够高效的运行。而且整个材料有发达的空隙结构,使得电解质离子转移的传质阻力较小,也有利于反应的进行。在5 mV/s的扫描速率下, 复合物通过循环伏安曲线积分计算的质量比电容为218 F/g,而在相同扫速下CB的质量电容为57 F/g,证明合成的复合材料不仅有碳质材料的双电层储能特性,也有MnCO3材料的赝电容储能的特性。相对于之前文献中,在1 mol/L的Na2SO4电解液中的纯MnCO3材料的比电容为118 F/g来说[7],比电容提高了接近2倍。为了考察材料的稳定性,我们测试了材料的循环性能。
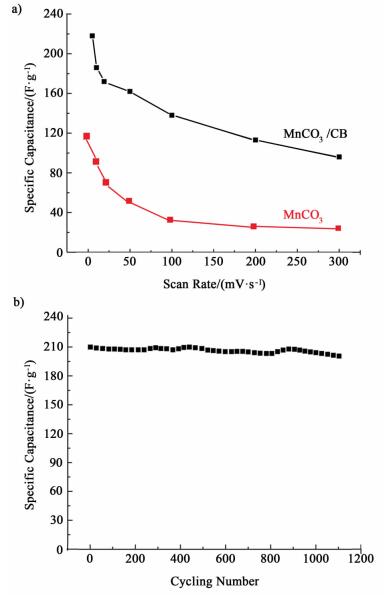
图 9a)中,比容量随着扫描速率的增大逐渐减小,当扫速增大到300 mV/s的时候,比容减小到原来的46%。比电容的衰减主要是因为快速充放电的过程中,电极材料表面积上的活性位点减少导致的,而这与其他的金属氧化物类的电极材料相比,该复合物的衰减较为缓慢,原因是复合材料在循环过程中,MnCO3的溶解受到了抑制,减少了比电容的降低。图 9b)为电极材料的循环曲线,我们希望主要表征电极材料的电化学性能,因而采用了三电极测试体系,由于长时间循环会导致电解液中溶剂的蒸发,导致电解液浓度发生变化进而影响材料电化学特性,因而我们选取了1 100次循环。1 100次循环后电极容量保持率为92%,相比于一般的金属氧化物类材料,克服了循环过程中活性物质溶解的问题,较高的容量保持率也是2种材料复合的结果,CB材料提供了高导电性和带有空隙的三维结构,提高了MnCO3活性位点的利用率和为电子传输提供了传输通道。
|
| 图 9 a) MnCO3/CB复合物和纯MnCO3的在不同扫速下的容量保持率曲线;b)MnCO3/CB复合物在5 mV/s的扫速下循环1 100次的容量保持曲线 Figure 9 a) capacitive retention line of MnCO3/CB and pure MnCO3 at different scan rate; b) capacitive retention line of MnCO3/CB composite at 100 mV/s for 1 100 cycles |
| |
1) 液相沉淀的方法在室温下合成了MnCO3/CB的复合材料,XRD和SEM表征说明MnCO3颗粒均匀复合在炭黑颗粒连接构成的三维结构之中。
2) 通过稀酸纯化的炭黑颗粒不再出现聚集的现象,表面富含了大量的负电基团(醌基和羧基基团),使得炭黑颗粒可以均匀的分散在水溶液中,有利于复合物的合成。
3) 电化学测试表明,MnCO3/CB复合材料电化学性能稳定,相比于纯的MnCO3质量比容量达到了2倍的增长,长时间循环的容量保持率达到了92%。为MnCO3/CB复合材料以后在电化学领域的应用奠定了基础,也为碳酸盐类的超级电容器材料的应用提供了新的思路。
| [1] | Simon P, Gogotsi Y. Materials for electrochemical capacitors[J]. Nature Materials, 2008, 7(11): 845. DOI: 10.1038/nmat2297 |
| [2] |
谢小英, 张辰, 杨全红. 超级电容器电极材料研究进展[J].
化学工业与工程, 2014, 31(1): 63–71.
Xie Xiaoying, Zhang Chen, Yang Quanhong. The development of electrode materials for supercapacitors[J]. Chemcial Industry and Engineering, 2014, 31(1): 63–71. |
| [3] | Liu C, Li F, Cheng M. Advanced materials for energy storage[J]. Adv Mater, 2010, 22(8): E28–E62. DOI: 10.1002/adma.v22:8 |
| [4] | Nayak P K, Devaraj S, Munichandraiah N. An eqcm investigation of electrochemical precipitation of Mn(OH)2 and its capacitance behavior[J]. Electrochemical and Solid-State Letters, 2010, 13(11): F29–F32. DOI: 10.1149/1.3479665 |
| [5] | Mai L, Yang F, Zhao Y, et al. Hierarchical MnMoO4/CoMoO4 heterostructured nanowires with enhanced supercapacitor performance[J]. Nature Communications, 2011, 2(1): 503–507. |
| [6] | Devaraj S, Gabriel G S, Gajjela S R, et al. Mesoporous MnO2 and its capacitive behavior[J]. Electrochemical and Solid-State Letters, 2012, 15(4): A57. DOI: 10.1149/2.016204esl |
| [7] | Devaraj S, Liu H, Balaya P. MnCO3:A novel electrode material for supercapacitors[J]. Journal of Materials Chemistry A, 2014, 2(12): 4276–4281. DOI: 10.1039/c3ta14174h |
| [8] | Bose S, Kuila T, Mishra A K, et al. Carbon-based nanostructured materials and their composites as supercapacitor electrodes[J]. J Mater Chem, 2012, 22(3): 767–784. DOI: 10.1039/C1JM14468E |
| [9] | Frackowiak E, Beguin F. Carbon materials for the electrochemical storage of energy in capacitors[J]. Carbon, 2001, 39(6): 937–950. DOI: 10.1016/S0008-6223(00)00183-4 |
| [10] | Jia F, Chen M, Wang C, et al. Three-Dimensional nano MnO2/CB composite and its application for electrochemical capacitor[J]. Materials Letters, 2012, 78: 127–130. DOI: 10.1016/j.matlet.2012.03.030 |
| [11] |
李莹, 张寿春, 吕春祥. 富氮多孔碳纤维的制备及其在超级电容器中的应用[J].
化学工业与工程, 2014, 31(3): 34–38.
Li Ying, Zhang Shouchun, Lü Chunxiang. Preparation of Nitrogen-Enriched porous carbon fibers as supercapacitor electrode materials[J]. Chemcial Industry and Engineering, 2014, 31(3): 34–38. |
| [12] | Ghosh D, Giri S, Dhibar S, et al. Reduced graphene oxide/manganese carbonate hybrid composite:High performance supercapacitor electrode material[J]. Electrochimica Acta, 2014, 147: 557–564. DOI: 10.1016/j.electacta.2014.09.130 |
| [13] |
张竞赛, 杜萍, 张晶. 石墨烯/聚苯胺/MnO2的制备及其电容性能[J].
化学工业与工程, 2016, 33(2): 58–64.
Zhang Jingsai, Du Ping, Zhang Jing. Preparation and capacitance performance of graphene/PANI/MnO2 composite[J]. Chemcial Industry and Engineering, 2016, 33(2): 58–64. |
| [14] | Wang D, Li F, Liu M, et al. 3D aperiodic hierarchical porous graphitic carbon material for high-rate electrochemical capacitive energy storage[J]. Angewandte Chemie, 2008, 120(2): 379–382. DOI: 10.1002/(ISSN)1521-3757 |
| [15] | Wang J, Chen M, Wang C, et al. Preparation of mesoporous carbons from amphiphilic carbonaceous material for high-performance electric double-layer capacitors[J]. Journal of Power Sources, 2011, 196(1): 550–558. DOI: 10.1016/j.jpowsour.2010.07.030 |
| [16] |
刘嫄嫄, 时志强, 乔志军, 等. 大容量锂离子电容器用锂化硬炭负极[J].
化学工业与工程, 2015, 32(6): 36–40.
Liu Yuanyuan, Shi Zhiqiang, Wang Chengyang, et al. High energy lithium ion capacitor with pre-lithiated hard carbon anode[J]. Chemcial Industry and Engineering, 2015, 32(6): 36–40. |
 2018, Vol. 35
2018, Vol. 35





