近年来,橄榄石结构的LiFePO4一直是锂离子电池领域的研究热点。由于其具有较高的理论容量(170 mAh·g-1)、稳定的充放电电压平台(3.4~3.5 V)、高温下的热稳定性、原材料价格低廉、无毒无污染等优点[1-2],已经被广泛应用于手机、数码相机、笔记本电脑等各类新兴电子产品和便携式电子设备产品中,此外,还被应用于电动汽车、电动工具、混合电动汽车和电动自行车等领域[3-4]。
但是,LiFePO4也存在着明显的缺点,例如:室温下,电子导电率(~10-9 S·cm-1)和锂离子扩散速率(~1.8×10-14 cm2·s-1)较低[5],导致高倍率充放电性能较差和实际比容量较低;较低的振实密度导致其体积比能量较低,这些因素都将限制该材料的实际应用价值[6]。目前,人们已经将注意力集中在改善LiFePO4的电化学性能方面,例如改进合成工艺,合成粒径小且分布均匀、高比表面积的产物;包覆或分散导电性碳、添加导电剂(金属)等[7],增加颗粒间的导电性,降低极化,提高大电流充放电时的可逆容量;体相掺杂金属离子[8],使晶体内部形成缺陷,从根本上改善材料的电导率。
目前,制备LiFePO4的方法很多,主要有溶胶-凝胶法[9]、碳热还原法[10]、溶剂热法[11]、水热法[12]、共沉淀法[13]和微波法[14]等。传统的高温固相法合成周期长,晶型无规则,颗粒粒度较大且不均匀,这些问题都将影响Li+的扩散速率,从而降低电极材料的导电性,降低实际比容量。而本研究采用水热反萃法一步合成前驱体LiFePO4,最后通过高温煅烧得到终产物LiFePO4/C。此法简便快捷、绿色环保、原料无毒无污染,非常适合工业化生产。因此,水热反萃法是一种合成锂离子电池正极材料LiFePO4的优选方法。
1 实验部分 1.1 LiFePO4/C的制备在锥形瓶中按体积比2:1依次加入环烷酸、异辛醇,磁力搅拌下加入适量的1:1氨水进行皂化,然后加入配置好的Fe2+溶液,磁力搅拌30 min,分液洗涤,即可获得载Fe2+有机相。准确称取一定量的LiOH,加水至LiOH完全溶解,在磁力搅拌下加入一定体积3 mol·L-1的H3PO4和少量的抗坏血酸。将水相和有机相按一定比例引入高压反应釜内,密封并开启搅拌,设置反应温度为250 ℃,反应3 h后停止。降温冷却到80 ℃后,保温5 h,离心分离得到灰色产物,用蒸馏水和无水乙醇反复洗涤数次,置于80 ℃的烘箱中干燥得到前躯体LiFePO4,最后混合一定量的葡萄糖在充满氩气的管式炉中煅烧得到终产物LiFePO4/C。
1.2 材料的表征本实验采用日本理学的Rigaku D/max-2500型X射线衍射仪对所制得的样品结构进行分析,Cu_Kα为辐射源,波长0.15406 nm,工作电压:30 kV,工作电流:20 mA,Ni滤波片,扫描速度:2(°)/min,扫描步长:0.02°,采用步进扫描方式,扫描范围:10°~80°。利用日本日立公司S4800型扫描电子显微镜对材料的形貌以及颗粒大小进行观察,加速电压为0.5~30.0 kV,最小步进为0.1 kV。
1.3 电化学性能的测试组装CR2032型扣式电池测试材料的容量。用JJ500型电子分析天平按质量比8:1:1称取活性物质、乙炔黑和PVDF(聚偏氟乙烯),混合均匀,涂膜制备正极片,正极片直径为14 mm,厚度200 μm。在充满氩气的真空手套箱[Lab2000,北京伊特克斯惰性气体系统(北京)有限公司]中组装CR2032型扣式电池,负极为金属锂片,电解液为1 mol·L-1的LiPF6/碳酸乙烯酯(EC)+碳酸二甲酯(DMC)+碳酸甲乙酯(EMC)的混合溶液(体积比为1:1:1),隔膜为Celgard2400聚丙烯多孔膜。采用蓝电测试系统(CT2 001 A,武汉金诺有限公司)在不同倍率下测试电池的充放电性能,充放电电压为2.5~4.2 V。采用美国生产的电化学分析仪(Gamry,PCI4-750)进行了循环伏安的测试(2.5~4.2 V, v=0.1 mV·s-1)。
2 结果与讨论 2.1 结构分析图 1是分别在550、600、650、700、750和800 ℃下煅烧4 h所得产品的XRD衍射图,随着煅烧温度的升高,各晶面衍射峰变得越来越尖锐,说明晶体晶型发育趋于完善;另外,各个衍射峰位置和强度与LiFePO4的XRD标准图谱(JCPDS PD#40-1499)十分吻合,且没有杂质峰出现,形成了纯度较高的LiFePO4相。图 2是在650 ℃下分别煅烧2、4、8和12 h产品的XRD衍射图。所有样品的衍射峰和LiFePO4的XRD标准图谱也十分吻合,当煅烧时间从2 h延长至4 h时,样品的主要衍射峰明显变强,半峰宽变窄,但当煅烧时间长于4 h时,样品的衍射峰强度基本没有变化,表明4 h的样品已经结晶完整。由此说明在同一温度下,较短的煅烧时间范围内延长煅烧时间有利于正交晶系LiFePO4的晶体发育,但煅烧时间太长反而对样品的结晶度影响不大。

|
| 图 1 不同煅烧温度下分别煅烧4 h的样品的XRD图 Figure 1 XRD patterns of samples synthesized for 4 h at different sintering temperatures |
| |

|
| 图 2 在650 ℃下不同煅烧时间的样品的XRD图 Figure 2 XRD patterns of samples synthesized at 650 ℃ for different sintering time |
| |
图 3给出了不同煅烧条件下产物的SEM图。从图 3中可以看出合成的材料为尺寸较小的类棒状结构,颗粒表面均比较光滑,说明在各煅烧条件下得到的产品结晶比较完全。由图 3a)(600 ℃)、图 3b)(650 ℃)和图 3c)(700 ℃)可知,随着温度的升高,样品颗粒出现团聚长大的现象;由图 3b)和3d)可知,650 ℃下煅烧12 h的样品颗粒比4 h的大且有团聚现象,说明煅烧温度的升高和煅烧时间的延长都会促使颗粒粒径变大。而这些现象都不利于改善材料的电化学性能,因为团聚和黏结会使Li+在LiFePO4颗粒内部的扩散阻力增大,不可逆容量增大,颗粒粒径变大也会延长Li+的扩散路径,这些都会导致Li+的脱出和嵌入过程变得困难,从而影响LiFePO4的电化学性能。

|
| 图 3 不同煅烧条件下样品的SEM图 Figure 3 SEM images of samples synthesized at different conditions |
| |
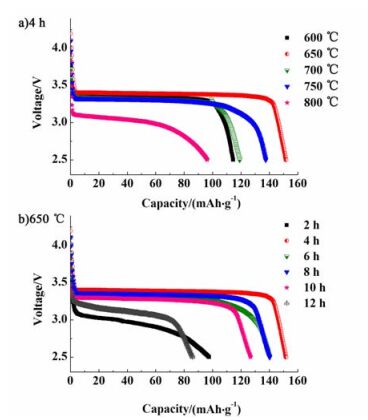
图 4是不同煅烧条件下的LiFePO4/C在0.1C的首次放电曲线。图 4a)是分别在600、650、700、750和800 ℃下煅烧4 h得到的LiFePO4/C的首次放电曲线,由图 4a)知,只有煅烧800 ℃的样品电压平台不够平缓,且电压较低,说明其极化程度较大,而其它样品在3.4 V附近均有较平缓的电压平台。样品的首次放电比容量分别为114.5、151.7、119.1、137.4和96.4 mAh·g-1,说明随着煅烧温度的升高,材料的首次放电比容量呈现先增大后减小的趋势,其中800 ℃样品具有最低的首次放电比容量。原因可能是当温度低于650 ℃时,虽然产物颗粒较小且比较均匀,但是结晶度不完好,所以导致放电容量较低;当温度高于650 ℃时,产物结晶度较好,但是高温易使颗粒聚集长大,Li+的脱嵌距离增加,导致放电容量降低。图 4b)是在650 ℃下分别煅烧2、4、6、8、10和12 h得到的LiFePO4/C的首次放电曲线,由图 4b)知,煅烧时间为4、6、8和10 h时,样品在3.4 V附近有1个平缓的放电平台,放电比容量分别为151.7、140.3、140.1和126.9 mAh·g-1,而煅烧时间为2和12 h时,样品的放电平台极不平缓,并且放电电压低,首次放电比容量也较低,分别为97.6和85.9 mAh·g-1,说明煅烧时间太短或过长都会导致材料的电化学性能较差,可能是由于煅烧时间太短不能使晶体充分发育完善,而时间过长又会导致晶体粒径过大,使Li+脱嵌变得困难。
|
| 图 4 在不同煅烧温度下煅烧4 h a)和650 ℃下煅烧不同时间b)样品的首次放电曲线图 Figure 4 Initial discharge curves of samples synthesized at ifferent sintering temperatures for 4 h a) and at 650 ℃ for different sintering time b) |
| |
图 5是650 ℃下煅烧4 h的LiFePO4/C样品在不同倍率下的循环性能曲线,在0.1、0.2、0.5、和1.0 C的首次放电比容量分别为151.7、154.8、149.8和139.1 mAh·g-1,且在不同倍率下各循环10周期后的容量几乎无衰减。而且循环40周期后,电流密度再次回到0.1 C时,放电比容量可达到161.9 mAh·g-1,为理论比容量(170 mAh·g-1)的95.24%。原因可能是样品循环40周期后已经完全达到活化状态。

|
| 图 5 650 ℃煅烧4 h所得样品的循环性能图 Figure 5 Cycling performance of the sample synthesized at 650 ℃ for 4 h |
| |
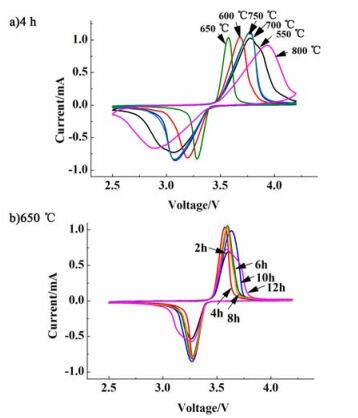
图 6是不同煅烧条件下的LiFePO4/C样品的循环伏安曲线,测试电压范围是2.5~4.2 V,扫描速度是0.1 mV·s-1。
|
| 图 6 不同煅烧温度下煅烧4 h a)和650 ℃下煅烧不同时间b)样品的循环伏安曲线 Figure 6 CV curves of samples obtained under different sintering temperatures for 4 h a) and at 650 ℃ for different sintering time b) |
| |
图 6a)是分别在550、600、650、700 ℃、750和800 ℃下煅烧4 h得到的样品的循环伏安曲线。图 6b)是在650 ℃下分别煅烧2、4、6、8、10和12 h得到的样品的循环伏安曲线。每个循环伏安曲线都有1个氧化峰和还原峰,分别与氧化还原电对Fe2+/Fe3+在充放电过程中的电极反应相对应,即代表锂离子的脱出和嵌入过程。在CV曲线中,充放电电压平台之间的距离越小,氧化还原峰越尖锐,材料的电极反应动力学过程和电化学性能表现得越优越。由2组循环伏安曲线图易知,650 ℃下煅烧4 h的样品不但在3.5 V附近有1对峰型尖锐、对称性较好的氧化还原峰,而且峰电位偏离平衡电位的程度最小,说明其极化程度最小,内部阻抗最小,Li+脱嵌可逆性最强,从而证实其电化学活性最优。而其它样品的CV曲线峰型较宽,充放电电压平台之间的距离较大,说明它们的电化学动力学过程受到阻碍,电极极化现象比较严重,电化学性能较差。
3 结论采用水热反萃法一步合成了前躯体LiFePO4,并在氩气保护下经过高温煅烧得到终产物LiFePO4/C,而煅烧条件的选择对LiFePO4/C产品的物理性能以及电化学性能都具有重要的影响。XRD和SEM测试结果表明,在650 ℃下煅烧4 h的产品具有较好的结晶度和分散性,电化学测试结果表明:此条件下合成的样品具有良好的电化学性能,在0.1 C下首次放电比容量为151.7 mAh·g-1,且在0.1、0.2、0.5和1.0 C下分别循环10周期后的容量几乎无衰减,当电流密度再次回到0.1 C时,放电比容量可达到161.9 mAh·g-1,为理论比容量的95.24%。
| [1] | Tian L, Chen L. Liquid-Phase preparation electrochemical property of LiFePO4/C nanowires[J]. Journal of Central South University of Technology, 2014, 21(2): 477–481. DOI: 10.1007/s11771-014-1963-y |
| [2] | Chen C, Liu G, Wang Y, et al. Preparation and electrochemical properties of LiFePO4/C nanocomposite using FePO4·2H2O nanopaticles by introduction of Fe3(PO4)2·8H2O at low cost[J]. Electrochimica Acta, 2013, 113: 464–469. DOI: 10.1016/j.electacta.2013.09.095 |
| [3] |
田建华, 李向军, 位辰先, 等. LiFePO4/C复合材料的制备和性能[J].
化学工业与工程, 2007, 24(1): 1–4.
Tian Jianhua, Li Xiangjun, Wei Chenxian, et al. Preparation and properties of LiFePO4/C composite material[J]. Chemical Industry and Engineering, 2007, 24(1): 1–4. |
| [4] | Deng S, Wang H, Liu H, et al. Research Progress in improving the rate performance of LiFePO4 cathode materials[J]. Nano-Micro Letters, 2014, 6(3): 209–226. DOI: 10.1007/BF03353785 |
| [5] | Hu Y, Ren J, Wei Q, et al. Synthesis of rod-like LiFePO4/C materials with different aspect ratios by polyol process[J]. Acta Phys-Chim Sin, 2014, 30(1): 75–82. |
| [6] | Miao C, Bai P, Jiang Q, et al. A novel synthesis and characterization of LiFePO4 and LiFePO4/C as a cathode material for lithium-ion battery[J]. Journal of Power Sources, 2014, 246: 232–238. DOI: 10.1016/j.jpowsour.2013.07.077 |
| [7] | Muxina K, Izumi T. Synthesis of carbon-coated LiFePO4 nanoparticles with high rate performance in lithium secondary batteries[J]. Journal of Power Sources, 2010, 195(1): 3661–3667. |
| [8] | Li L, Li X, Wang Z, et al. Stable cycle-life properties of Ti-doped LiFePO4 compounds synthesized by co-precipitation and normal temperature reduction method[J]. Journal of Physics and Chemistry of Solids, 2009, 70(1): 238–242. DOI: 10.1016/j.jpcs.2008.10.012 |
| [9] | Peng W, Jiao L, Gao H, et al. A novel sol-gel method based on FePO4·2H2O to synthesize submicrometer structured LiFePO4/C cathode material[J]. Journal of Power Sources, 2011, 196(5): 2841–2847. DOI: 10.1016/j.jpowsour.2010.10.065 |
| [10] |
徐峙晖, 赖琼玉, 吉晓阳. 用碳热还原法合成LiFePO4及其电化学性能研究[J].
四川大学学报:工程科学版, 2005, 37(4): 77–80.
Xu Zhihui, Lai Qiongyu, Ji Xiaoyang. LiFePO4 synthesized by carbonthermal reduction and the study of electrochemical performance[J]. Journal of Sichuan University:Engineering Science, 2005, 37(4): 77–80. |
| [11] | Vadivel M A, Muraliganth T, Manthiram A. Rapid microwave-solvothermal synthesis of phospho-olivine nanorods and their coating with a mixed conducting polymer for lithium ion batteries[J]. Electrochemistry Communications, 2008, 10: 903–906. DOI: 10.1016/j.elecom.2008.04.004 |
| [12] | Franger S, Lecras F, Bourbon C, et al. LiFePO4 synthesis routes for enhanced electrochemical performance[J]. Electrochemical and Solid State Letter, 2002, 5(10): A231–A233. DOI: 10.1149/1.1506962 |
| [13] | Zhu B, Li X, Wang Z, et al. Novel synthesis of LiFePO4 by aqueous precipitation and carbothermal reduction[J]. Materials Chemistry and Physics, 2006, 98(2): 373–376. |
| [14] | Park K S, Son T J, Chung H T, et al. Synthesis of LiFePO4 by co-precipitation and microwave heating[J]. Electrochemistry Communications, 2003, 5(10): 839–842. DOI: 10.1016/j.elecom.2003.08.005 |
 2017, Vol. 34
2017, Vol. 34





