随着社会经济以及工业、运输业的繁荣发展,由于汽车尾气以及工厂废气等引起的大气污染问题引起了人们越来越多的关注。化石燃料的不完全燃烧产生的CO严重地影响了环境以及人们的健康。研究者们研发了各种催化剂用于CO催化氧化反应,比如过渡金属氧化物催化剂[1-2]、贵金属催化剂[3-4]等。贵金属催化剂由于价格昂贵而且储量有限,应用受到了较大的限制。近年来,金属氧化物催化剂在氧化消除CO方面取得了很大的进展,很多金属氧化物都对CO催化氧化反应表现出了较高的活性,特别是过渡金属氧化物,比如Co3O4、CuO、CeO2等[5]。单一的金属氧化物催化剂比如Co3O4和CuO,虽然活性较高但是容易失活,而CeO2和SiO2,虽然稳定性很好但是活性较差。因此,将两者结合起来,可以通过形成的复合金属氧化物催化剂中2种金属氧化物之间的相互作用取得好的活性、稳定性和抗水性,比如NiO/CeO2[6]、CuO/CeO2[7]、CuO-CeO2/ZrO2[8]等。另外,虽然有些金属氧化物催化活性较低,但是通过掺杂其他的金属氧化物或者改变催化剂的形貌能够达到较好的活性,比如说CeO2[9]和SnO2[10-11]。CeO2是一种重要的稀土材料,由于Ce4+↔Ce3+离子对的转换而具有较高的储氧能力,并广泛应用于环境催化方面。早在19世纪70年代,铈基催化剂就在汽车尾气污染物的控制和消除领域获得了不断的发展。CeO2的储氧能力和稳定性等可以通过掺杂其它金属氧化物得到进一步提高,比如ZrO2[12]、Al2O3[13]和SnO2[14]。SnO2由于含有丰富的表面氧物种也常用做环境催化剂和载体[15]。在我们之前的研究中发现,锡铈复合氧化物催化剂对于甲烷催化燃烧有着较大的促进作用[14],但是其在CO催化氧化领域的研究还没有报道过。
本研究用共沉淀法制备了SnO2-CeO2复合氧化物催化剂,并考察了其结构和氧化还原性能对其催化性能的影响。
1 试验部分 1.1 催化剂的制备通过共沉淀法制备Sn0.3Ce0.7O2和Sn0.7Ce0.3O2催化剂。取一定物质的量之比的SnCl4·5H2O和Ce(NO3)3·6H2O试剂,分别溶于150 mL蒸馏水中搅拌30 min,溶解均匀后混合,然后用氨水缓慢滴入上述混合溶液至溶液pH值为9,将所得沉淀物用蒸馏水反复洗涤除去Cl-1。将洗涤后的沉淀物在110 ℃干燥12 h。在相同的实验条件下,通过沉淀法制备SnO2和CeO2催化剂。
1.2 催化剂的表征通过德国布鲁克AXS有限公司的D8-S4衍射仪分析催化剂的结构,其中操作电压为40 kV,电流为40 mA,射线源为Cu_Kα,采集范围为10°~90°。
H2-TPR测试在天津先权公司的TP-5080全自动化学吸附仪上进行。在石英反应器中放入30 mg催化剂样品,在8% H2/N2混合气中以10 ℃·min-1的升温速率从室温程序升温到900 ℃。
CO-TPR测试在固定床反应器中进行。在石英反应器中放入50 mg催化剂样品,在350 ℃的N2中预处理30 min,然后降至50 ℃,在7% CO/N2混合气中以10 ℃·min-1的升温速率从50 ℃程序升温到900 ℃。
1.3 催化剂的活性评价催化剂的活性测试在固定床反应器中进行,其中石英反应管的内径为4.5 mm,催化剂粒度为60~100目,催化剂用量50 mg,反应气体组成如下:1% CO,20% O2,N2为平衡气体;气体总流速为150 mL·min-1,空速为270 000 h-1。试验前,催化剂在500 ℃下于20% O2/N2下预处理1.0 h。反应温度通过置于催化剂床层中间部位的热电偶测量。在每个反应温度下停留0.5 h,以便得到稳定的CO转化率。采用北分谱齐分析仪器技术有限公司生产的型号为GXH-104C的红外线性气体分析仪检测反应尾气。CO的转化率通过式(1)计算。
| ${X_{{\rm{CO}}}} = {C_{{\rm{C}}{{\rm{O}}_{\rm{2}}}}}/({C_{{\rm{CO}}}} + {C_{{\rm{C}}{{\rm{O}}_{\rm{2}}}}}) \times 100\% $ | (1) |
式(1)中,CCO和CCO2分别为尾气中CO和CO2的物质的量浓度。
2 结果与讨论 2.1 结构性质图 1为催化剂的XRD衍射谱图。其中Sn0.3Ce0.7O2和CeO2催化剂的衍射峰可以归属为立方萤石结构的CeO2相(JCPDS no.43-1002),SnO2催化剂可以归属为金红石结构的SnO2相(JCPDS no.41-1445),而Sn0.7Ce0.3O2同时呈现了SnO2和CeO2物相。Sn0.3Ce0.7O2没有呈现SnO2相的衍射峰,原因可能是SnO2高度分散或者Sn进入了CeO2的晶格中形成了固溶体。Sn0.3Ce0.7O2和Sn0.7Ce0.3O2的衍射峰强度变弱而且明显变宽,说明催化剂的晶体结构对称性降低、晶粒尺寸减小。另外,可以观察到相对于CeO2,Sn0.3Ce0.7O2和Sn0.7Ce0.3O2的衍射峰向高角度偏移。Sn2+和Sn4+的离子直径分别为0.093和0.071 nm[14],Ce3+和Ce4+的离子直径分别为0.110和0.097 nm[15],Sn离子的直径小于Ce离子的直径。因此可以推断半径较小的Sn进入了CeO2的晶格中,从而引起了晶格收缩,形成了固溶体结构。

|
| 图 1 催化剂的XRD谱图 Figure 1 XRD patterns of the catalysts |
| |
图 2为催化剂的TEM图。

|
| 图 2 催化剂的TEM照片 Figure 2 TEM images of the catalysts |
| |
由图 2可知,Sn0.7Ce0.3O2和Sn0.3Ce0.7O2的晶粒尺寸明显小于SnO2和CeO2,该结果与XRD结果一致。并且与SnO2和CeO2相比,Sn0.7Ce0.3O2和Sn0.3Ce0.7O2催化剂晶粒大小、形状更加均一。
从表 1中可知,与SnO2和CeO2相比,锡铈复合氧化物催化剂的比表面积和孔容有了较明显的提高,这可能是因为Sn0.7Ce0.3O2和Sn0.3Ce0.7O2有着较小的晶粒尺寸。其中,SnO2的比表面积最小,而Sn0.7Ce0.3O2具有最大的比表面积。催化剂的比表面积的顺序与CO氧化活性一致,说明较大的比表面积对CO氧化反应有一定促进作用。
| catalyst | SBET/
(m2·g-1) | pore volume/
(cm3·g-1) | pore size/
nm |
| SnO2 | 17.9 | 0.090 | 20.4 |
| Sn0.7Ce0.3O2 | 50.2 | 0.114 | 9.6 |
| Sn0.3Ce0.7O2 | 49 | 0.096 | 7.8 |
| CeO2 | 29.8 | 0.056 | 7.6 |
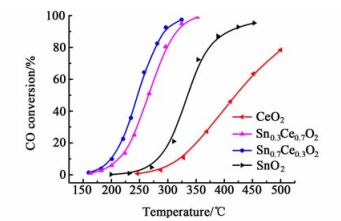
图 3为催化剂的CO催化氧化活性曲线。
|
| 图 3 催化剂的CO催化氧化活性曲线 Figure 3 Conversion curves of the catalysts upon the catalytic CO oxidation |
| |
从图 3中可以看出相对于纯SnO2和CeO2催化剂来说,Sn0.7Ce0.3O2和Sn0.3Ce0.7O2催化剂获得了较高的CO催化氧化活性。其中CO催化氧化活性由高到低依次为Sn0.7Ce0.3O2>Sn0.3Ce0.7O2>SnO2>CeO2。Sn0.7Ce0.3O2在200 ℃时转化率达到了10%,在240 ℃时转化率达到了50%。而SnO2在280 ℃时转化率达到了10%,在330 ℃时转化率达到了50%。Sn0.7Ce0.3O2达到10%转化率的温度比SnO2提高了80 ℃,达到50%转化率的温度比SnO2提高了90 ℃。根据之前研究人员的报道,在CeO2中掺杂Pr以及Cu能够明显的提高催化剂的活性,在SnO2中掺杂Ta后催化剂CO催化氧化活性得到了一定的提高[9, 18]。与本研究掺杂后的催化剂相比,活性的提高基本一致。
2.3 催化剂的氧化还原性能图 4为催化剂的H2-TPR谱图。SnO2催化剂有2个还原峰,200~500 ℃的较弱的低温还原峰为表面Sn4+到Sn2+的还原,500 ℃以上的高温还原峰为体相Sn4+到Sn2+的还原以及表面Sn2+的还原[15-17]。CeO2催化剂的2个较弱的还原峰从低温到高温分别为表面Ce4+和体相Ce4+的还原[19-20]。Sn0.3Ce0.7O2催化剂的低温还原峰为表面Sn4+到Sn2+的还原,高温还原峰为表面Ce4+到Ce3+的还原。Sn0.7Ce0.3O2催化剂的3个还原峰从低温到高温分别为表面Sn4+的还原、表面Ce4+的还原和体相Sn4+的还原。

|
| 图 4 催化剂的H2-TPR谱图 Figure 4 The H2-TPR profiles of the catalysts |
| |
由图 4可以看出,与SnO2和CeO2催化剂相比,锡铈复合氧化物表面Sn4+的还原和表面Ce4+的还原峰位置都向低温偏移,而且表面Ce4+的还原峰面积有了较大的提高。这些结果表明形成锡铈固溶体后,催化剂的表面Sn4+和表面Ce4+的氧化能力有了明显的提高。这可能是因为催化剂中Ce4+/Ce3+和Sn4+/Sn2+离子对的相互作用,形成了Sn4++2Ce3+↔Sn2++2Ce4+氧化还原平衡[8]。从TEM结果来看,形成固溶体后,颗粒粒晶变小,导致表面相位增加,Ce和Sn等容易还原,这也可能是导致还原峰位置向低温偏移且表面Ce4+还原峰面积增加的原因。催化剂表面Sn4+的氧化能力由高到低顺序为Sn0.7Ce0.3O2>Sn0.3Ce0.7O2>SnO2>CeO2,与CO催化氧化活性顺序一致,所以推测催化剂的表面Sn4+为反应的活性物种。其中活性最高的Sn0.7Ce0.3O2催化剂有着最强的表面Sn4+的氧化能力。
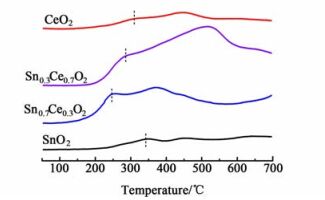
为了研究催化剂在CO气氛下的氧化还原性质,我们测定了催化剂的CO-TPR谱图,如图 5所示。所有的催化剂都有3个主要的还原峰。相对于SnO2和CeO2催化剂,Sn0.7Ce0.3O2和Sn0.3Ce0.7O2催化剂的还原峰面积明显增加,表明SnO2和CeO2之间存在较强的相互作用。另外,SnO2-CeO2复合金属氧化物催化剂低温还原峰的位置也向低温偏移,表明催化剂的氧化能力明显提高,特别是Sn0.7Ce0.3O2。CO-TPR结果与H2-TPR结果一致。
|
| 图 5 催化剂的CO-TPR谱图 Figure 5 The CO-TPR profiles of the catalysts |
| |
研究了SnO2、Sn0.7Ce0.3O2、Sn0.3Ce0.7O2和CeO2催化剂对于CO催化氧化的性能。结果发现Sn0.7Ce0.3O2表现出了最好的催化活性。通过研究催化剂的结构性质,我们发现锡掺杂进CeO2的晶格形成了固溶体结构,而且锡铈复合氧化物的颗粒尺寸较小,比表面积较大。通过研究催化剂的氧化还原性能,发现由于SnO2-CeO2之间存在较强的相互作用,而且不论还原气体是CO还是H2,锡铈复合氧化物的氧化能力都有明显的提高。结果表明,较大的比表面积和较高的表面Sn4+氧化能力能够促进CO氧化能力。
| [1] | Xie X, Li Y, Liu Z, et al. Low-Temperature oxidation of CO catalyzed by Co3O4 nanorods[J]. Nature, 2009, 458(7239): 746–749. DOI: 10.1038/nature07877 |
| [2] | Xu J, Deng Y, Luo Y, et al. Operando Raman spectroscopy and kinetic study of low-temperature CO oxidation on an α-Mn2O3 nanocatalyst[J]. Journal of Catalysis, 2013, 300: 225–234. DOI: 10.1016/j.jcat.2013.01.010 |
| [3] | Chen M, Cai Y, Yan Z, et al. Highly active surfaces for CO oxidation on Rh, Pd, and Pt[J]. Surface Science, 2007, 601(23): 5326–5331. DOI: 10.1016/j.susc.2007.08.019 |
| [4] | Ouyang X, Scott S L. Mechanism for CO oxidation catalyzed by Pd-substituted BaCeO3, and the local structure of the active sites[J]. Journal of Catalysis, 2010, 273(2): 83–91. DOI: 10.1016/j.jcat.2010.04.020 |
| [5] |
陈业娜, 孟明. 焙烧温度对CuO/Co3O4-CeO2催化剂CO优先氧化性能的影响[J].
化学工业与工程, 2015, 32(2): 1–5.
Chen Yena, Meng Ming. Effect of calcination temperature on the catalytic performance of CuO/Co3O4-CeO2 catalyst for preferential CO oxidation[J]. Chemical Industry and Engineering, 2015, 32(2): 1–5. |
| [6] |
孙敬方, 葛成艳, 姚小江, 等. 固相浸渍法制备NiO/CeO2催化剂及其在CO氧化反应中的应用[J].
物理化学学报, 2013, 29(11): 2451–2458.
Sun Jingfang, Ge Chengyan, Yao Xiaojiang, et al. Preparation of NiO/CeO2 catalysts by solid state impregnation and their application in CO oxidation[J]. Acta Phys-Chim Sin, 2013, 29(11): 2451–2458. DOI: 10.3866/PKU.WHXB201309041 |
| [7] |
孙敬方, 张雷, 葛成艳, 等. 固相浸渍法和湿浸渍法制备CuO/CeO2催化剂及其CO氧化性能的对比研究[J].
催化学报, 2014, 35(8): 1347–1358.
Sun Jingfang, Zhang Lei, Ge Chengyan, et al. Comparative study on the catalytic CO oxidation properties of CuO/CeO2 catalysts prepared by solid state and wet impregnation[J]. Chinese Journal of Catalysis, 2014, 35(8): 1347–1358. |
| [8] |
杨志强, 毛东森, 杨超杰, 等. 制备方法对CuO-CeO2/ZrO2催化CO氧化性能的影响[J].
无机化学学报, 2012, 28(7): 1353–1359.
Yang Zhiqiang, Mao Dongsen, Yang Chaojie, et al. Effect of preparation method on catalytic performance of CuO-CeO2/ZrO2 for CO oxidation[J]. Chinese Journal of Inorganic Chemistry, 2012, 28(7): 1353–1359. |
| [9] | Pu Z, Liu X, Jia A, et al. Enhanced activity for CO oxidation over Pr-and Cu-doped CeO2 catalysts:Effect of oxygen vacancies[J]. The Journal of Physical Chemistry C, 2008, 112(38): 15045–15051. DOI: 10.1021/jp805389k |
| [10] | Wang X, Xiao L, Peng H, et al. SnO2 nano-rods with superior CO oxidation performance[J]. Journal of Materials Chemistry A, 2014, 2(16): 5616–5619. DOI: 10.1039/C3TA15109C |
| [11] | Li Y, Peng H, Xu X, et al. Facile preparation of mesoporous Cu-Sn solid solutions as active catalysts for CO oxidation[J]. RSC Advances, 2015, 5(33): 25755–25764. DOI: 10.1039/C5RA00635J |
| [12] | Bozo C, Guilhaume N, Garbowski E, et al. Combustion of methane on CeO2-ZrO2 based catalysts[J]. Catalysis Today, 2000, 59(1): 33–45. |
| [13] | Cargnello M, Jaén J J D, Garrido J C H, et al. Exceptional activity for methane combustion over modular Pd@CeO2 Subunits on Functionalized Al2O3[J]. Science, 2012, 337(6095): 713–717. DOI: 10.1126/science.1222887 |
| [14] | Liu C, Xian H, Jiang Z, et al. Insight into the improvement effect of the Ce doping into the SnO2 catalyst for the catalytic combustion of methane[J]. Applied Catalysis B:Environmental, 2015, 176: 542–552. |
| [15] |
柴澍靖, 李静, 白雪芹, 等. 水热法制备SnO2纳米颗粒的CO氧化性能[J].
化学工业与工程, 2017, 34(5): 19–24.
Chai Shujing, Li Jing, Bai Xueqin, et al. CO oxidation performance over SnO2 nanoparticles prepared with hydrothermal method[J]. Chemical Industry and Engineering, 2017, 34(5): 19–24. |
| [16] | Yao X, Xiong Y, Zou W, et al. Correlation between the physicochemical properties and catalytic performances of CexSn1-xO2 mixed oxides for NO reduction by CO[J]. Applied Catalysis B:Environmental, 2014, 144: 152–165. DOI: 10.1016/j.apcatb.2013.06.020 |
| [17] | Yao X, Yu Q, Ji Z, et al. A comparative study of different doped metal cations on the reduction, adsorption and activity of CuO/Ce0.67M0.33O2 (M=Zr4+, Sn4+, Ti4+) catalysts for NO+CO reaction[J]. Applied Catalysis B:Environmental, 2013, 130: 293–304. |
| [18] | Han X, Xu X, Liu W, et al. CO oxidation on Ta-modified SnO2 solid solution catalysts[J]. Solid State Sciences, 2013, 20: 103–109. DOI: 10.1016/j.solidstatesciences.2013.03.019 |
| [19] | Baidya T, Gupta A, Deshpandey P A, et al. High oxygen storage capacity and high rates of CO oxidation and NO reduction catalytic properties of Ce1-xSnxO2 and Ce0.78Sn0.2Pd0.02O2-delta[J]. The Journal of Physical Chemistry C, 2009, 113(10): 4059–406. DOI: 10.1021/jp8060569 |
| [20] | Sellick D R, Aranda A, García T, et al. Influence of the preparation method on the activity of ceria zirconia mixed oxides for naphthalene total oxidation[J]. Applied Catalysis B:Environmental, 2013, 132: 98–106. |
 2017, Vol. 34
2017, Vol. 34





