在全球石油资源日渐枯竭,环境污染愈演愈烈的大背景下,稀薄燃烧技术应运而生[1]。与传统发动机相比,稀燃发动机可节约15%~20%的燃油,尾气中一氧化碳 (CO) 和碳氢化合物 (CH) 的含量也大大降低[2]。然而,传统三效催化剂在高空燃比下对NOx的消除效率过低[3],难以满足日益严格的尾气排放标准[4]。因此,研究和开发新型高效催化剂,在稀燃条件下消除NOx,已经成为环境催化领域最具紧迫性和挑战性的课题之一。
20世纪90年代早期,日本Toyota公司提出NOx储存还原技术 (NOx Storage and Reduction),来解决稀燃条件下NOx的消除问题[5-6]。其设计的Pt/Ba/Al2O3催化剂也已经成功投放使用无硫或超低硫燃料的日本市场。该技术就是将三效催化剂和NOx吸附组分结合起来,其工作原理为:当发动机在稀燃条件下运行时,Pt将NO氧化为NO2,NO2与邻近的储存组分 (Ba) 发生反应,以硝酸钡或亚硝酸钡形式储存起来;间歇富燃条件时,硝酸盐和亚硝酸盐分解放出NOx,它们在三效催化剂作用下,被还原性气体CO、CH和H2等,还原为环境友好的N2[7]。
近年来,大量的研究表明,铜基催化剂对NOx消除具有良好的活性[8-11],且催化剂成本低,具有替代贵金属催化剂的潜在可能。我们研究发现,CuO/K2CO3/TiO2催化剂对NOx储存还原具有很高的催化活性,尤其是CuO负载量为8%的催化剂,该催化剂对NOx储存量达到1.559 mmol/g,对NOx还原效率达到99%,且在NOx还原过程中无N2O产生。但是铜基催化剂的活性与焙烧温度密切相关,到目前为止,关于焙烧温度对于CuO/K2CO3/TiO2催化剂活性的影响尚没有任何报道。故本研究采用连续浸渍法,制备了不同温度焙烧的CuO/K2CO3/TiO2三元催化剂,考察了它们对NOx的储存还原性能,优化了催化剂的焙烧温度区间,应用BET、XRD、HR-TEM、SEM、H2-TPR和in-situ DRIFTS等技术对催化剂的结构和性能进行详细表征,并探讨了焙烧温度对于催化剂性能的影响。
1 实验部分 1.1 催化剂制备催化剂的制备采用连续浸渍法,具体步骤如下:将载体TiO2(P25, 57 m2/g) 等量浸渍于Cu (NO3)2·3H2O[w(CuO):8%]水溶液中,120 ℃烘干后分别于350、450、550、650和750 ℃下焙烧3 h,得到不同温度焙烧的催化剂前驱体。然后将前驱体等量浸渍于K2CO3溶液中 (K2CO3负载量为20%),相同条件下烘干后,于350 ℃焙烧1 h即得不同温度焙烧的CuO-K2CO3/TiO2催化剂,记为T-CuO-K2CO3/TiO2,T表示不同焙烧温度。
1.2 催化剂表征 1.2.1 比表面测试 (BET)催化剂比表面积测试在77 K于美国Quantachrome公司生产的QuadraSorb SI仪器上进行。实验前,样品先于300 ℃真空条件下处理3 h。样品用量0.3 g左右,采用BET吸附曲线的线性部分 (p/p0为0.089~0.297) 计算催化剂比表面积,孔容由吸附脱附曲线最大吸附量计算。
1.2.2 X射线粉末衍射 (XRD)XRD测试采用日本理学公司生产的Rigaku D/Max-2500型多晶粉末衍射仪,Cu_Kα (λ=0.15418 nm) 作为辐射源,管电流为200 mA,管电压为40 kV,扫描范围2θ为20°~90°,步长为0.02°。
1.2.3 透射、扫描电子显微镜 (HR-TEM和SEM)催化剂的微观结构采用JEM-2100F型透射电子显微镜进行观察,操作电压200 kV。取少量催化剂研磨后,超声分散于乙醇中,再将含有样品的乙醇液体置于铜网支撑的碳膜上进行观察。样品的扫描电镜测试在日立公司S-4800型场发射扫描电子显微镜上进行,操作电压为5.0 kV。
1.2.4 程序升温还原 (H2-TPR)程序升温还原 (H2-TPR) 测试在天津Xianquan公司生产的TP-5079动态吸附仪上进行。以φ(H2)=8%的H2/N2混合气为还原气,样品用量为30 mg,气体流速为30 mL/min,样品温度从室温升到600 ℃,升温速率10 ℃/min。
1.2.5 原位漫反射红外光谱 (In-situ DRIFTS)原位漫反射红外光谱 (In-situ DRIFTS) 在Thermo Nicolet公司生产的Nicolet Nexus光谱仪上进行,配备可以加热到600 ℃的原位反应池,采用液氮冷却的MCT检测器,累计扫描32次,光谱分辨率为4 cm-1。实验气氛为400×10-6 NO+5%O2+N2。每次实验前,15 mg样品在350 ℃下用高纯He处理0.5 h后,采集背景谱图,然后在同样温度下进行吸附实验,并采集样品不同吸附时间的红外谱图。
1.3 催化剂活性评价新鲜催化剂对NOx的储存量测试 (NSC) 是在配有内径为8 mm的石英管的固定床反应器中进行,催化剂用量500 mg (40~60目)。实验温度为350 ℃,实验气氛为400×10-6NO和5% O2的混合气体以400 mL/min的流速通过催化剂,对应的空速为40 000 h-1。反应器出口的NO、NO2和NOx浓度由美国Thermo Scientific公司生产的Model 42i-HL型发光式NO-NO2-NOx监测仪在线检测。
新鲜催化剂对NOx的还原性能测试是在配有内径为8 mm的石英管的固定床反应器中进行。实验温度为350 ℃,稀燃状态持续3 min,富燃状态持续1 min,测试15个循环,催化剂对NOx的还原效率基于最后2个循环的数据测得。在稀燃状态下,400×10-6 NO+5% O2和N2混合气体以150 mL/min的流速通过催化剂;在富燃状态下,实验气氛变为1 000×10-6 C3H6和N2混合气。同时,N2O的浓度通过SICK MAIHAK公司生产的S710型模块化气体分析仪在线监测。
2 实验结果与讨论 2.1 催化剂的储存和还原性能对经过不同温度焙烧的催化剂进行NOx的储存测试,活性曲线如图 1所示。

|
| 图 1 T-CuO-K2CO3/TiO2催化剂在350 ℃的NOx储存曲线 Figure 1 NOx storage curves for the samples T-CuO-K2CO3/TiO2 at 350 ℃ |
| |
由图 1可以看出储存刚开始阶段,NOx浓度迅速下降,350、450和550 ℃焙烧的催化剂2 min之内就可以到达底部;在底部停留一段时间后,由于储存位逐渐达到饱和,NOx浓度开始缓慢上升,最后达到稳定状态;当焙烧温度为650和750 ℃时,催化剂对NOx的储存性能显著下降,NOx浓度不能到达底部,大量NOx溢出。不同温度焙烧的载体负载的催化剂的NOx储存量列于表 1中,不难发现,焙烧温度为350和450 ℃的催化剂储存活性最佳,均达到1.7 mmol/g以上。
| Catalysts | NSC/ (mmol·g-1) |
NRP/ % |
SBET/ (m2·g-1) |
PV/ (cm3·g-1) |
| 350-CuO-K2CO3/TiO2 | 1.746 | 99.6 | 26.4 | 0.13 |
| 450-CuO-K2CO3/TiO2 | 1.809 | 99.8 | 28.8 | 0.14 |
| 550-CuO-K2CO3/TiO2 | 1.399 | 98.3 | 15.7 | 0.09 |
| 650-CuO-K2CO3/TiO2 | 1.126 | 88.1 | 7.6 | 0.03 |
| 750-CuO-K2CO3/TiO2 | 0.408 | 52.8 | 2.4 |
不同焙烧温度的催化剂,在稀/富燃测试中NOx随时间的变化曲线如图 2所示。

|
| 图 2 样品T-CuO-K2CO3/TiO2在稀/富燃循环测试中NOx的变化曲线 Figure 2 NOx concentration curves of T-CuO-K2CO3/TiO2 during lean/rich cycles |
| |
从图 2中可以发现,在稀燃状态下,当焙烧温度不同时,不同催化剂的NOx浓度也呈现不同的变化趋势。对于350和450 ℃焙烧的催化剂,NOx浓度很快达到底部,接近0;在22个循环测试中,稀燃阶段NOx出口浓度几乎为0,这进一步说明催化剂具有最佳NOx储存性能;对于750-CuO-K2CO3/TiO2催化剂,随着储存还原的进行,稀燃阶段NOx浓度不断升高,大量NOx溢出,表明该催化剂NOx储存能力较差、稳定性不佳。到达最后1个循环时,在550、650以及750 ℃焙烧的催化剂对应NOx的出口浓度分别为9×10-6、55×10-6和256×10-6。当切换到富燃气氛时,不稳定的硝酸盐和亚硝酸盐迅速分解释放出NOx,NOx浓度瞬间达到最大值,进而迅速被C3H6还原为环境友好的N2。基于最后2个稀/富燃循环测试,计算了催化剂对NOx的平均还原效率列于表 1中。
2.2 催化剂BET结果不同温度焙烧CuO/K2CO3/TiO2催化剂的比表面积和孔径分布数据列于表 1中。
从表 1中可以看出,350~450 ℃焙烧的催化剂比表面积和孔容相近。随着焙烧温度的进一步升高,催化剂的表面积、孔容迅速减小,这是因为催化剂颗粒尺寸快速增加,载体P25中锐钛矿相TiO2逐渐向金红石相TiO2转变,晶粒也逐渐长大[12]造成比表面积减少。750 ℃焙烧的催化剂与450 ℃焙烧的样品相比,比表面积显著降低,这是因为催化剂介孔结构遭到破坏,孔道发生坍塌,催化剂严重烧结。催化剂的比表面积大小顺序与其NOx储存活性基本一致,表明Cu和K物种在催化剂上的分散性对催化活性有直接影响。
2.3 XRD结果图 3为不同温度焙烧的T-CuO-K2CO3/TiO2催化剂的XRD谱图。

|
| 图 3 T-CuO-K2CO3/TiO2催化剂的XRD谱图 Figure 3 XRD patterns of T-CuO-K2CO3/TiO2 samples |
| |
从图 3中可以看出,随着焙烧温度的升高,载体P25的晶体结构发生明显变化。焙烧温度达到550 ℃时,锐钛矿型TiO2衍射峰的强度减弱,金红石型TiO2衍射峰的强度增强;焙烧温度达到750 ℃时,P25载体中锐钛矿型TiO2几乎消失,金红石型TiO2衍射峰的强度最强,峰型也变得很尖锐;随着焙烧温度的升高650和750 ℃焙烧的样品谱图中CuO衍射峰强度增强,峰型变尖锐,说明焙烧温度过高时,高分散状态的CuO物种发生烧结,使CuO颗粒增大,这种大颗粒的CuO相的形成对NO氧化反应不利,因此高温焙烧的样品的催化性能相对较低。另外还可以发现,750-CuO-K2CO3/TiO2催化剂XRD谱图中出现K2CO3衍射峰,表明该催化剂中存在较大颗粒的体相K2CO3,这对NOx的储存显然是不利的。
2.4 HR-TEM和SEM结果应用HR-TEM和SEM对催化剂的表面形貌进行了表征,如图 4所示。
|
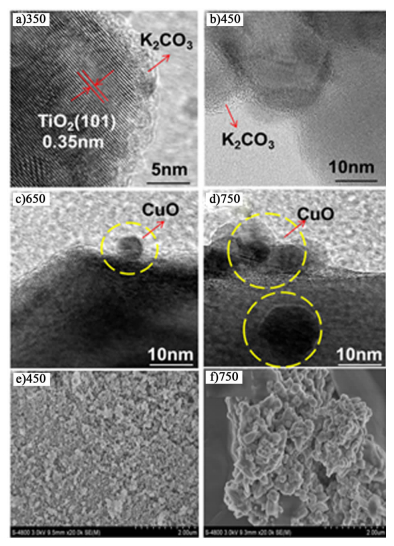
| 图 4 T-CuO-K2CO3/TiO2系列催化剂的HR-TEM和SEM谱图 Figure 4 HR-TEM and SEM images of T-CuO-K2CO3/TiO2 |
| |
350 ℃焙烧的催化剂,表面出现了非常明显的晶格条纹,通过计算晶格间距,该催化剂表面的晶格条纹代表TiO2物种 (101) 晶面,如图 4中标注所示;并没有发现K2CO3和CuO物种相对应的晶格条纹。通过仔细观察不难发现,催化剂表面覆盖了一层以无定形或高分散的状态存在的物质,推测为K2CO3物种;随着焙烧温度增加,高分散的CuO物种发生烧结,颗粒不断长大。这和上述的XRD结果是相一致的。通过SEM扫描电镜分析,得出了催化剂更为直接的微观结构信息。可以看到450 ℃焙烧的样品主要以较小的片状或块状形式存在,催化剂表面孔道多、粗糙度较大,这有利于催化剂对反应物的吸附[13]。750 ℃焙烧的样品,催化剂呈无规则形状,催化剂颗粒尺寸明显长大,由于催化剂孔道的堵塞,导致比表面积、孔容及孔径都降低。
2.5 H2-TPR结果为了研究不同焙烧温度的催化剂的氧化还原性能,我们对催化剂进行了H2-TPR测试,结果如图 5所示。
|
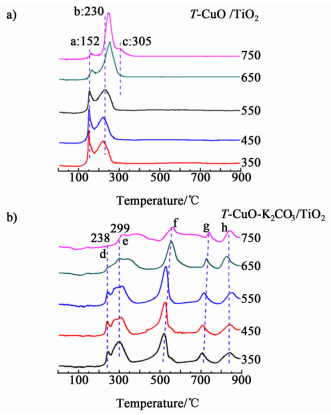
| 图 5 不同样品的H2-TPR谱图 Figure 5 H2-TPR profiles of different samples |
| |
从图 5a) 中可以看出,不同温度焙烧的催化剂的还原峰有所不同,谱图中出现低温a和高温b 2个还原峰。a峰归属为表面高分散的CuO物种的还原,高温还原峰归属为大颗粒CuO物种的还原[14-15]。可以看出,随焙烧温度升高低温还原峰逐渐减小,表明表面高分散的CuO物种,发生烧结颗粒不断长大,当焙烧温度达到750 ℃时,高温峰变大且尖锐,同时向高温方向偏移,低温还原峰几乎消失,此时CuO物种烧结严重,颗粒进一步长大。图 5b) 为T-CuO-K2CO3/TiO2催化剂的TPR谱图,负载K2CO3后催化剂中铜物种的还原峰均向高温方向发生偏移,K2CO3对CuO物种有稳定作用,K-Cu之间存在相互作用,K物种修饰在CuO表面,导致CuO物种难于被还原,这与Guerrero等[16]报道的Na-Cu相互作用相近。高温区还原峰与K2CO3物种的分解有关,其中f区还原峰为表面K2CO3分解,放出CO2稀释了气流中的H2而产生的“假耗氢峰”[17],由于K2CO3负载量一样,750 ℃焙烧的样品f区还原峰最小,表明表面K2CO3物种减少,出现大量体相K2CO3这与前面XRD结果一致。高温区g、h的还原峰与K2CO3与TiO2发生固相反应[18]有关。
2.6 In-Situ DRIFTS结果分析为了研究不同焙烧温度的CuO-K2CO3/TiO2系列对NOx的吸附状态,我们对催化剂进行了NO和O2在催化剂上共同吸收的in-situ DRIFTS表征,结果如图 6所示。

|
| 图 6 NO和O2在T-CuO-K2CO3/TiO2催化剂上吸附随时间变化的in situ DRIFTS谱图 Figure 6 Isothermal time-dependent in-situ DRIFT spectra of NO/O2 adsorption at 350 ℃ over T-CuO-K2CO3/TiO2 |
| |
对于样品350和450 ℃焙烧的催化剂,在1 220~1 210和1 282 cm-1波数处出现红外振动峰,分别对应桥式二齿硝酸盐和单齿硝酸盐[19]。1 480 cm-1波数处出现倒峰,归属为碳酸氢盐v(C—O)[20],表明K2CO3物种参与到了NOx储存反应中反生分解。550和650 ℃样品谱图变化不大,但随焙烧温度升高,相同时间内红外峰的强度变弱,这与催化剂对NOx储存的活性顺序一致。750 ℃焙烧的催化剂样品,只在1 248 cm-1波数处出现双齿亚硝酸盐的红外振动峰[21],表明催化剂对NOx的氧化能力减弱。同时该催化剂红外谱图中由碳酸盐分解产生的倒峰几乎消失,说明参与到NOx储存反应的表面K2CO3物种减少,这与XRD表征中K2CO3物种主要以体相形式存在相一致。
3 结论系统考察了不同温度焙烧的CuO-K2CO3/TiO2催化剂结构和储存还原性能。NOx储存还原测试结果表明:该系列铜基催化剂在350~450 ℃焙烧温度区间内活性最佳,其中450 ℃焙烧的CuO/K2CO3/TiO2催化剂活性最佳,NSC为1.808 mmol/g,经过22个稀富燃循环测试保持稳定,对NOx还原效率达到99.8%,进一步升高焙烧温度催化剂活性逐渐降低。新鲜催化剂的表征结果表明,焙烧温度主要从两个方面影响催化剂的活性:影响铜物种的存在状态,随焙烧温度升高,表面高分散的CuO物种减少,CuO发生烧结颗粒长大体相CuO增多,导致催化剂对NOx氧化性能减弱。另一方面,随着焙烧温度的提高,载体的结构发生变化,催化剂孔道堵塞导致孔容、比表面积显著减小,催化剂上负载的K2CO3不能良好地分散,形成颗粒较大的体相K2CO3物种,不利于NOx储存。
| [1] | 王建昕. 汽车排气污染治理及催化转化器[M]. 北京: 石油工业出版社, 2000 |
| [2] |
郭丽红, 刘咏, 孟明. 稀燃NOx储存-还原催化剂[J].
化学进展, 2009, 21(5) : 965–970.
Guo Lihong, Liu Yong, Meng Ming. NOx storage reduction catalysts used for lean burn NOxremoval[J]. Progress in Chemistry, 2009, 21(5) : 965–970. |
| [3] | Kašpar J, Fornasiero P, Hickey N. Automotive catalytic converters:Current status and some perspectives[J]. Catal Today, 2003, 77 : 419–449. DOI: 10.1016/S0920-5861(02)00384-X |
| [4] | Granger P, Parvulescu V I. Catalytic NOx abatement systems for mobile sources:From three-way to lean burn after-treatment technologies[J]. Chem Rev, 2011, 111 : 3155–3207. DOI: 10.1021/cr100168g |
| [5] | Takahashi N, Shinjoha H, Iijimaa T, et al. The new concept 3-way catalyst for automotive lean-burn engine:NOx storage and reduction catalyst[J]. Catal Today, 1996, 27 : 63–69. DOI: 10.1016/0920-5861(95)00173-5 |
| [6] | Matsumoto S. De-NOx catalyst for automotive lean-burn engine[J]. Catal Today, 1996, 29 : 43–45. DOI: 10.1016/0920-5861(95)00259-6 |
| [7] | Roy S, Baiker A. NOx storage-reduction catalysis:From mechanism and materials properties to storage-reduction performance[J]. Chem Rev, 2009, 109(9) : 4054–4091. DOI: 10.1021/cr800496f |
| [8] | Wang Q, Jong S. NOx storage and reduction over Cu/K2Ti2O5 in a wide temperature range:Activity, characterization, and mechanism[J]. Appl Catal A, 2009, 358 : 59–64. DOI: 10.1016/j.apcata.2009.01.039 |
| [9] | Vijay R, Hendershot R J, Rivera-Jiménez S M, et al. Noble metal free NOx storage catalysts using cobalt discovered via high-throughput experimentation[J]. Catal Commun, 2005, 6 : 167–171. DOI: 10.1016/j.catcom.2004.12.004 |
| [10] | Xu L, McCabe R, Ruona W, et al. Impact of a Cu-zeolite SCR catalyst on the performance of a diesel LNT+SCR system[J]. SAE Tech Pap, 2009 . DOI: 10.4271/2009-01-0285 |
| [11] | Liu J, Li X, Zhao Q, et al. The selective catalytic reduction of NO with propene over Cu-supported Ti-Ce mixed oxide catalysts:Promotional effect of ceria[J]. J Mol Catal A:Chem, 2013, 378 : 115–123. DOI: 10.1016/j.molcata.2013.06.005 |
| [12] | Ohno T, Sarukawa K, Tokieda K, et al. Morphology of a TiO2 photocatalyst (Degussa, P-25) consisting of anatase and rutile crystalline phases[J]. J Catal, 2001, 203 : 82–86. DOI: 10.1006/jcat.2001.3316 |
| [13] | Hamadanian M, Reisi-Vanani A, Majedi A. Synthesis, characterization and effect of calcination temperature on phase transformation and photocatalytic activity of Cu, S-codoped TiO2nanoparticles[J]. Appl Surf Sci, 2010, 256 : 1837–1844. DOI: 10.1016/j.apsusc.2009.10.016 |
| [14] | Yoong L S, Chong F K, Dutta B K. Development of copper-doped TiO2 photocatalyst for hydrogen production under visible light[J]. Energy, 2009, 34 : 1652–1661. DOI: 10.1016/j.energy.2009.07.024 |
| [15] | Zhu H, Dong L, Chen Y. Effect of titania structure on the properties of its supported copper oxide catalysts[J]. J Colloid Interface Sci, 2011, 357 : 497–503. DOI: 10.1016/j.jcis.2011.02.012 |
| [16] | Guerreroa S, Guzmána I, Aguila G, et al. Sodium-Promoted NO adsorption under lean conditions over Cu/TiO2 catalysts[J]. Catal Commun, 2009, 11 : 38–42. DOI: 10.1016/j.catcom.2009.08.006 |
| [17] | Zhang Y, Liu D, Meng M, et al. A highly active and stable non-platinic lean NOx trap Catalyst MnOx-K2CO3/K2Ti8O17 with ultra-low NOx to N2O selectivity[J]. Ind Eng Chem Res, 2014, 53 : 8416–8425. DOI: 10.1021/ie501034u |
| [18] | Liu C, He M, Lu X, et al. Reaction and crystallization mechanism of potassium dititanate fibers synthesized by low-temperature calcination[J]. Cryst Growth Des, 2005, 5 : 1399–1404. DOI: 10.1021/cg049602a |
| [19] | Hadjiivanov K I. Identification of neutral and charged NxOy surface species by IR spectroscopy[J]. Catal Rev Sci Eng, 2000, 42 : 71–144. DOI: 10.1081/CR-100100260 |
| [20] | Morterra C, Magnacca G. A case study:Surface chemistry and surface structure of catalytic aluminas, as studied by vibrational spectroscopy of adsorbed species[J]. Catal Today, 1996, 27 : 497–532. DOI: 10.1016/0920-5861(95)00163-8 |
| [21] | Prinetto F, Manzoli M, Morandi S, et al. Pt-K/Al2O3 NSR catalysts:Characterization of morphological, structural and surface properties[J]. J Phys Chem C, 2009, 114 : 1127–1138. |
 2017, Vol. 34
2017, Vol. 34





