近年来,由于空心纳米微球具有质量轻、密度小、比表面积大等独特性质,越来越多的研究人员对其制备方法以及应用开展了广泛的探索。通过对其进行物理和化学性质的调控与修饰,空心结构的纳米微粒已经被广泛应用于催化[1-2]、药物控释[3]、光电子[4]、能源储存[5]以及环保[6]等诸多领域。二氧化硅材料具有卓越的机械性能,良好的热稳定性,易修饰性,低毒性和优异的生物相容性。纳米空心介孔硅球 (HMS) 则兼具空心微球与介孔微球的优点,中空内腔可以作为储存容器或者微反应器,介孔外壳则允许物质通过孔道进行扩散,在药物负载方面拥有难以比拟的优势,经过修饰后的HMS可拥有刺激响应的特性,实现药物的靶向输送与控制释放,在生物医药领域,尤其是智能型药物控释等方面具有巨大的潜力。
结合HMS与其他材料的特点,实现以HMS为基础的多功能 (如磁性、荧光、光热作用等特性) 材料是其在生物医药应用中的发展趋势[7]。例如Shi等[8]制备出了用多环芳烃/聚苯乙烯磺酸层包覆介孔的IBU-HMS@PEM系统,有望用于癌症药物布洛芬在生物体内的响应控制释放。
相比于聚合物与脂质体的药物载体,用保护刻蚀法[9]制备的HMS工艺相对简单,能够批量生产,并且大大降低了生产成本,满足未来临床以及商业要求。RAFT聚合作为活性可控自由基聚合中适用范围最广的方法之一,操作条件温和,引发条件简单,适应单体范围宽,常被用于表面接技改性,引入具有特定功能、可控相对分子质量的聚合物,对材料进行表面修饰改性,获得需要的特性[10]。
Mei等[11]用硬模板法制备了空心介孔硅球,并在其表面修饰上溴代异丁酰溴,引入含有pH值敏感的缩醛基团的疏水单体和含有聚乙二醇结构的亲水单体,成功用于阿霉素的负载和控制释放。然而,接枝过程中容易覆盖介孔通道,降低了药物的负载与释放效率,而本研究采用先接枝后刻蚀的方式避免了介孔通道被覆盖的问题。
在之前的研究中,我们开发了以PDMAEMA为保护剂对硅球进行刻蚀制备HMS的方法[12],本工作在此基础上,将固载了有机硅RAFT试剂BTPT的硅球进行DMAEMA的RAFT表面接枝聚合反应,将得到的表面修饰聚合物PDMAEMA的纳米硅球 (SiO2@PDMAEMA) 在常温下进行刻蚀,获得了pH值、温度双响应聚合物修饰的纳米空心介孔硅球 (HMS@PDMAEMA),并利用多种表征方法对其结构和形貌进行了表征。
1 实验部分 1.1 实验原料甲基丙烯酸-2-(二甲氨基) 乙酯 (DMAEMA,阿拉丁试剂有限公司),使用前减压蒸馏精制。甲苯用金属钠除水,回流12 h减压蒸馏。RAFT试剂三甲氧基硅基丙基三硫代羰基苄基酯 (BTPT) 参照文献[13]合成。其他试剂均为分析纯,直接使用。
1.2 制备过程 1.2.1 二氧化硅微球的制备采用Stöber法[14]制备单分散的二氧化硅微球,以200 nm硅球的制备为例,具体方法如下:常温下将十六烷基三甲基溴化铵1.46 g溶解于90 mL蒸馏水和100 mL异丙醇的混合溶液中,再加入1.4 mL氨水 (质量分数约为28%),在剧烈搅拌下滴加正硅酸乙酯5.8 mL,滴加完毕后在40 ℃水浴中搅拌24 h。得到硅球的分散体系进行离心,用异丙醇和去离子水洗涤并离心数次,干燥得到白色粉末状的二氧化硅微球。
1.2.2 SiO2@BTPT的制备将0.5 g硅球分散于10 mL甲苯中,搅拌下加入0.3 g BTPT,油浴加热至120 ℃,在氮气环境中回流12 h。冷却到常温后在8 000 r/min的转速下离心10 min,将沉淀物用二氯甲烷洗涤并离心3次,放置在真空干燥箱中常温干燥,最终得到SiO2@BTPT。
1.2.3 SiO2@PDMAEMA的制备取0.2 g的SiO2@BTPT、0.8 g的DMAEMA、0.01 g的AIBN和6 g THF于反应瓶中,磁力搅拌混合均匀,通氮气除氧20 min后密封,置于60 ℃水浴中搅拌下聚合反应24 h,将所得产物用石油醚沉析3次,真空干燥,得SiO2@PDMAEMA。
1.2.4 PDMAEMA的制备称取2.8 g的DMAEMA、0.1 g的BTPT、0.01 g AIBN和6 g THF于反应瓶中,磁力搅拌混合均匀,通氮气除氧20 min后密封,置于60 ℃水浴中搅拌下反应24 h,将所得聚合物PDMAEMA用石油醚沉析3次,真空干燥。
1.2.5 HMS@PDMAEMA的制备将0.02 g的PDMAEMA溶解于10 g蒸馏水中,取0.05 g的SiO2@PDMAEMA分散于溶液中,混合均匀后滴加氨水,使NH3质量分数为0.3%,pH值约为10。在常温常压下搅拌7 d进行刻蚀,将得到的HMS@PDMAEMA分散体在12 000 r/min转速下离心10 min,去除上层溶液,用适量去离子水洗涤并离心3次,真空干燥。
1.3 表征 1.3.1 红外 (IR) 测定采用KBr压片法,使用BIO-RAD FTS3000红外分光光度计,在常温下测定。
1.3.2 热重 (TG) 测定分别取10 mg的SiO2、SiO2@BTPT、SiO2@PDMAEMA样品,在梅特勒差示量热分析仪上 (Mettler Toledo TGA/DSC) 对其进行热重分析,氮气为保护气,从25 ℃升到700 ℃,升温速率为10 ℃/min。
1.3.3 接枝PDMAEMA的相对分子质量测定在聚四氟乙烯反应釜中,将10 mg的HMS@PDMAEMA分散于3 mL THF中,加入0.5 mL的HF水溶液 (40%, 质量分数),密封后在常温下搅拌12 h,用Na2CO3水溶液中和,透析洗涤获得了聚合物,冷冻干燥得到接枝链PDMAEMA (gPDMAEMA),用于GPC测试。所用仪器为Agilent 1100型高效液相色谱,UV检测器,色谱柱为KF-803L,柱温30 ℃,流动相为THF,流速为1 mL/min,进样量为50 μL。
1.3.4 透射电镜 (TEM) 测定微球的外部形貌和内部结构采用JEM-2100F型透射电子显微镜观测。将含有纳米微球的乙醇分散液滴到碳支持膜上,干燥待测。
1.3.5 HMS@PDMAEMA的pH值响应行为用2 mol/L的磷酸盐缓冲液配制pH值分别为4.75、5.96、7.38和9.12的水溶液,将少量HMS@PDMAEMA分散于上述水溶液中,用超声清洗机震荡后用马尔文公司的Nano ZS型纳米粒度及zeta电位仪 (使用633 nm氦-氖激光器) 测定微球的粒径。
2 结果与讨论 2.1 SiO2@PDMAEMA的制备为了确定接枝过程中每个阶段的产物是否成功合成,对于不同修饰阶段的纳米微球做了红外分析和热重分析,并对接枝PDMAEMA做了GPC测定。
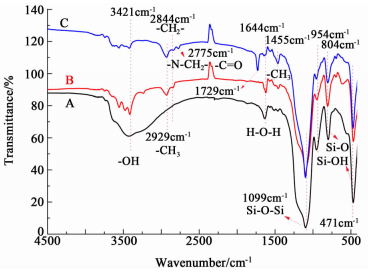
2.1.1 IR结果分析图 1是不同修饰阶段的硅球的红外谱图。
|
| 图 1 不同修饰阶段的硅球的红外谱图 Figure 1 FTIR spectra of the silica microspheres collected at different stages after modifying |
| |
其中图 1A为原始SiO2的红外谱图,在1 099 cm-1的弯曲振动峰属于Si—O—Si,在954和3 300~3 660 cm-1范围的振动峰为Si—OH,在805和471 cm-1的特征峰是由于Si—O的伸缩和弯曲振动,1 644 cm-1是吸附自由水的弯曲振动峰。图 1B中为SiO2@BTPT的红外谱图,除了硅球上的特征峰外,还可以看到图 1中2 929 cm-1的—CH3伸缩振动峰和2 844 cm-1的—CH2—伸缩振动峰。另外,修饰后在3 300~3 660 cm-1属于Si—OH的伸缩震动峰变弱,这是由于硅球表面羟基与BTPT上三甲氧基硅烷发生了反应,证明硅球表面成功地接枝上了BTPT。图 1中C是SiO2@ PDMAEMA的红外谱图,除了上述特征峰外,还有明显的1 729 cm-1酯羰基伸缩振动峰,以及2 775 cm-1处的—N—CH2—反对称伸缩振动峰,表明在硅球表面成功地合成了聚合物PDMAEMA。
2.1.2 TG结果分析为了进一步说明每个阶段的产物成功合成,对于不同的修饰阶段的微球做了热重分析,如图 2所示。

|
| 图 2 不同阶段的热重分析 Figure 2 TG curves for different stages |
| |
将各阶段样品分别从常温加热到700 ℃,测试出SiO2(A)、SiO2@BTPT (B)、SiO2@PDMAEMA (C) 的质量损失分别是13.85%、20.91%和32.13%。其中,SiO2@BTPT与SiO2质量损失相差7.06%,通过计算可知SiO2@BTPT中BTPT在硅球表面的接枝密度为0.12 mmol/g。而SiO2@PDMAEMA与SiO2质量损失相差18.28%,表明将PDMAEMA成功地接枝到了硅球表面。
2.1.3 gPDMAEMA的GPC分析为了测量接枝在硅球表面的PDMAEMA分子量的大小,用HF溶解了HMS@PDMAEMA中的硅球部分,测定了所获聚合物的GPC,结果如图 3所示,数均相对分子质量为9 834,分布系数为1.028。表明采用RAFT表面接枝聚合得到的聚合物相对分子质量可控,且分布窄,为研究聚合物相对分子质量对药物控释的影响奠定了基础。

|
| 图 3 gPDMAEMA的GPC图 Figure 3 GPC trace of the gPDMAEMA |
| |
为考察刻蚀效果,对HMS@PDMAEMA做了透射电镜分析,并对经历刻蚀条件后的PDMAEMA做了红外测定,考察其结构变化。
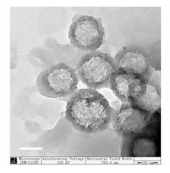
2.2.1 TEM分析自模板法[15]能优先刻蚀掉二氧化硅微球的内部,并且产物尺寸均一性高、形貌可控,已被大量运用于制备中空结构。实验中发现,如果在水中不加入PDMAEMA,将SiO2@PDMAEMA用氨水直接刻蚀,空心效果不佳。在水中加入在质量分数为0.2%的PDMAEMA后,刻蚀效果良好,所图 4所示。
|
| 图 4 HMS@PDMAEMA的透射电镜图 (比例尺为100 nm) Figure 4 TEM image of HMS@PDMAEMA (Scale bar is 100 nm) |
| |
图 4中直观地展现了其空心结构,并且硅球上存在接枝聚合物物收缩于其表面,说明刻蚀后PDMAEMA仍保留在硅球表面。
2.2.2 PDMAEMA在刻蚀前后的IR分析将质量分数为0.5%的PDMAEMA水溶液加氨水调节pH值为9.5,常温下搅拌7 d,真空干燥后测定红外 (图 5B),1 729 cm-1为酯羰基非对称伸缩振动峰,并且有叔胺的特征峰N—CH3(2 820和2 770 cm-1)。与原始PDMAEMA红外谱图 (图 5A) 一致。其中图 5B在3 500 cm-1的振动峰为水的羟基,是干燥不彻底所致。证明经历常温刻蚀过程,PDMAEMA未发生水解反应,结构没发生变化。

|
| 图 5 刻蚀前后的PDMAEMA的红外谱图 Figure 5 FTIR spectra of PDMAEMA before and after etching |
| |
为了检测纳米空心介孔硅球表面PDMAEMA在不同pH值环境中的响应性,采用动态光散射测定了0.1 mg/mL的HMS@PDMAEMA在不同pH值水溶液中的流体力学直径,如图 6所示。

|
| 图 6 PDMAEMA粒径随pH值的变化 Figure 6 pH dependence of hydrodynamic diameter of HMS@PDMAEMA |
| |
随着溶液的pH值从4.75增加到9.12,HMS@PDMAEMA的流体力学直径不断降低。这是因为在酸性环境中,PDMAEMA链段部分或全部质子化,成为带正电的聚电解质,链与链间的静电排斥作用和链与溶剂间的相互作用使得聚合物链伸展,导致流体力学直径较大。在中性或碱性环境中,PDMAEMA聚合物链去质子化,收缩成团,吸附于硅球表面。同时聚合物链与链间的相互吸引作用强于溶剂效应,聚合物链更倾向于收缩聚集,从而导致流体力学直径的缩小。
HMS@PDMAEMA对pH值的响应特性为其作为药物载体提供了可行性,满足控制释放的条件:在酸性条件下,聚合物链伸展,介孔通道呈开放状态,可以进行药物的负载和释放;在弱碱性条件下,聚合物链收缩,覆盖介孔通道,完成对药物的储存,避免药物在人体正常组织中释放。
3 结论使用有机硅RAFT试剂BTPT对二氧化硅微球进行修饰,合成SiO2@BTPT,再利用RAFT表面接枝聚合制备SiO2@PDMAEMA。在常温下,于PDMAEMA水溶液中用氨水对SiO2@PDMAEMA进行刻蚀,得到HMS@PDMAEMA,并利用多种表征手段对其结构和形态进行了表征。借助PDMAEMA的pH值敏感性,可通过控制HMS表面接枝链段在水溶液中的舒展或收缩,进而控制硅球表面介孔通道的开合,可用于药物的控制释放。因此,HMS@PDMAEMA在生物医药等领域具有潜在的应用价值。
| [1] | Huang X, Zhang H, Guo C, et al. Simplifying the creation of hollow metallic nanostructures:One-Pot synthesis of hollow palladium/platinum single-crystalline nanocubes[J]. Angewandte Chemie-International Edition, 2009, 48(26) : 4808–4812. DOI: 10.1002/anie.v48:26 |
| [2] | Kim S W, Kim M, Lee W Y, et al. Fabrication of hollow palladium spheres and their successful application to the recyclable heterogeneous catalyst for Suzuki coupling reactions[J]. Journal of the American Chemical Society, 2002, 124(26) : 7642–7643. DOI: 10.1021/ja026032z |
| [3] | Tang S, Huang X, Chen X, et al. Hollow mesoporous zirconia nanocapsules for drug delivery[J]. Advanced Functional Materials, 2010, 20(15) : 2442–2447. DOI: 10.1002/adfm.v20:15 |
| [4] | Liu J, Qiao S, Chen J, et al. Yolk/Shell nanoparticles:New platforms for nanoreactors, drug delivery and lithium-ion batteries[J]. Chemical Communications, 2011, 47(47) : 12578–12591. DOI: 10.1039/c1cc13658e |
| [5] | Jayaprakash N, Shen J, Moganty S S, et al. Porous hollow carbon@sulfur composites for high-power lithium-sulfur batteries[J]. Angewandte Chemie-International Edition, 2011, 50(26) : 5904–5908. DOI: 10.1002/anie.v50.26 |
| [6] | Liu S, Yu J, Jaroniec M. Tunable photocatalytic selectivity of hollow TiO2 microspheres composed of anatase polyhedra with exposed {001} facets[J]. Journal of the American Chemical Society, 2010, 132(34) : 11914–11916. DOI: 10.1021/ja105283s |
| [7] | Slowing I I, Trewyn B G, Giri S, et al. Mesoporous silica nanoparticles for drug delivery and biosensing applications[J]. Advanced Functional Materials, 2007, 17(8) : 1225–1236. DOI: 10.1002/(ISSN)1616-3028 |
| [8] | Zhu Y, Shi J, Shen W, et al. Stimuli-Responsive controlled drug release from a hollow mesoporous silica sphere/polyelectrolyte multilayer core-shell structure[J]. Angewandte Chemie-International Edition, 2005, 44(32) : 5083–5087. DOI: 10.1002/(ISSN)1521-3773 |
| [9] | Zhang T, Zhang Q, Ge J, et al. A self-templated route to hollow silica microspheres[J]. Journal of Physical Chemistry C, 2009, 113(8) : 3168–3175. DOI: 10.1021/jp810360a |
| [10] | Moad G, Rizzardo E, Thang S H. Living radical polymerization by the RAFT process-A third update[J]. Australian Journal of Chemistry, 2012, 65(8) : 985–1076. DOI: 10.1071/CH12295 |
| [11] | Mei X, Chen D, Li N, et al. Facile preparation of coating fluorescent hollow mesoporous silica nanoparticles with pH-sensitive amphiphilic diblock copolymer for controlled drug release and cell imaging[J]. Soft Matter, 2012, 8(19) : 5309–5316. DOI: 10.1039/c2sm07320j |
| [12] | Guo R, Zhong Q, Dong A, et al. Facile fabrication of silica nanocapsules with well-defined mesoporous shell via a poly (N, N-dimethylaminoethyl methacrylate)-assisted self-template etching process[J]. Journal of Nanoscience & Nanotechnology, 2016, 16(9) : 9708–9715. |
| [13] | Rotzoll R, Nguyen D H, Vana P. Trithiocarbonates containing trimethoxysilyl functionalities as mediating agents in reversible addition-fragmentation chain transfer (RAFT) polymerization of methyl acrylate[J]. Macromolecular Symposia, 2008, 275(1) : 1–12. |
| [14] | Stöber W, Fink A, Bohn E. Controlled growth of monodisperse silica spheres in the micron size range[J]. Journal of colloid and interface science, 1968, 26(1) : 62–69. DOI: 10.1016/0021-9797(68)90272-5 |
| [15] | Fang X, Zhao X, Fang W, et al. Self-Templating synthesis of hollow mesoporous silica and their applications in catalysis and drug delivery[J]. Nanoscale, 2013, 5 : 2205–2218. DOI: 10.1039/c3nr34006f |
 2017, Vol. 34
2017, Vol. 34





