酸性氯化铜蚀刻液是一种主要成分为氯化铜、盐酸的酸性蚀刻液体,其广泛应用于印制电路板行业[1]。随着蚀刻反应的进行,蚀刻液的溶液组成会逐渐发生改变,其中主要的反应方程式为
| $ {\rm{C}}{{\rm{u}}^{2 + }} + {\rm{Cu}} \to 2{\rm{C}}{{\rm{u}}^{2 + }} $ | (1) |
溶液中Cu(Ⅰ)浓度逐渐升高,Cu(Ⅱ)浓度逐渐降低。当蚀刻液中Cu(Ⅰ)浓度超过0.05 mol/L后,蚀刻液将变为蚀刻废液,不能再继续使用[2]。据统计,印制电路板行业每天约产生6 000 t蚀刻废液,其中有大约一半为酸性氯化铜蚀刻废液,这些蚀刻废液的直接排放将造成环境的严重污染和资源的巨大浪费[3]。
酸性氯化铜蚀刻废液的回收方法主要有化学法及电化学法。其中化学法回收氯化铜蚀刻废液存在回收率低、回收成本高、无法原位回收等缺点。而为了克服传统化学法的缺陷,电化学法被引入酸性氯化铜蚀刻液再生回收的研究中[4-5]。在电化学回收酸性氯化铜蚀刻液的反应中,阳极可能发生的电化学反应为:
| $ {\rm{C}}{{\rm{u}}^ + } - {{\rm{e}}^ - } \to {\rm{C}}{{\rm{u}}^{2 + }} $ | (2) |
阴极可能发生的电化学反应为:
| $ {\rm{C}}{{\rm{u}}^{2 + }} + {{\rm{e}}^ - } \to {\rm{C}}{{\rm{u}}^ + } $ | (3) |
| $ {\rm{C}}{{\rm{u}}^ + } + {{\rm{e}}^ - } \to {\rm{Cu}} $ | (4) |
阳极、阴极反应同时进行,从而达到原位回收酸性氯化铜蚀刻液的目的。阳极液由于大量的氯离子存在,可能在高电位下发生析氯反应。
电化学回收酸性氯化铜蚀刻废液可分为常规电解法、隔膜电解法、离子膜电解法。1985年Ott等[6]曾报道过一套常规电解装置,阳极采用平板电极,阴极采用旋转型电极。该方法虽然实现了酸性蚀刻液的原位回收,但槽电压较高、阳极有氯气析出、设备投资较大。1998年Oxley[7]报道了一种隔膜电解装置,蚀刻废液先后经过2个电解槽电解后再生成功。这套装置操作电压较低,无氯气析出,但处理量较小、设备费用大。Hillis[8]曾报道过一套离子膜回收装置,通过阴离子交换膜使阴阳极室分开,阴极液浓度为阳极液浓度1/10。这套装置的操作电压较高(6~10 V)且无法避免氯气的析出。杨征宇等[9]报道过一套离子膜电解回收装置,该装置采用碳毡做阳极,铜板做阴极,用阴离子交换膜将阴阳极室分开,通过控制阳极电位防止氯气析出,达到了电解回收的目的。但由于碳毡电极活性较低,亲水性较差,体系可能造成电解不均匀及局部析气。因此需要开发一种对Cu(Ⅰ)/Cu(Ⅱ)电对具有高电化学活性的电极材料。
电极在电化学回收酸性氯化铜蚀刻液中扮演着重要的角色,它为电极反应提供了反应场所。石墨毡作为一种比表面积大、稳定性强、导电性强且对金属离子电对的电化学反应具有一定催化作用的多孔电极,曾被报道用做酸性氯化铜蚀刻液电化学回收及全钒液流电池的电极材料[10-11]。然而石墨毡材料电化学活性低、亲水性差等缺陷,降低了石墨毡电极对金属离子电对的电化学性能。因此,对石墨毡电极进行一定的修饰,提高其对金属离子电对的电化学活性是十分必要的。研究表明[12-14],在石墨毡表面增加含氧官能团和含氮官能团,可以增强其对V(IV)/V(V)电对的电化学活性。而关于石墨毡电极对Cu(Ⅰ)/Cu(Ⅱ)电对的电化学活性的研究未见报道。
本研究采用将石墨毡、尿素、水一同在管式炉中高温处理的方法,对石墨毡电极进行氮掺杂修饰,得到了对Cu(Ⅰ)/Cu(Ⅱ)电对具有高电化学活性的石墨毡电极,并考察了处理时间、处理温度对氮掺杂效果的影响。对修饰后石墨毡的电化学性能和电解性能进行了测试。
1 实验 1.1 实验试剂及仪器实验所用氯化铜,氯化亚铜,盐酸,尿素等均购于天津市科密欧试剂有限公司;聚丙烯腈基石墨毡(200 mm×200 mm×5 mm)购于北京三业碳素有限公司;阴离子交换膜为美国Membranes International公司生产的AMI-7001型阴离子交换膜。
1.2 电极材料的制备石墨毡电极预处理:将石墨毡用打孔器制成直径d=14 mm、厚h=5 mm的圆形片状电极,用无水乙醇浸泡并超声1 h,以除去石墨毡纤维表面的杂质;取出后的石墨毡用去离子水反复冲洗后,在120 ℃下于真空干燥箱内真空干燥8 h。
石墨毡电极氮掺杂:将预处理好的石墨毡置于磁舟中,同时称取尿素3.0 g、去离子水1.5 g置于另一个磁舟。2个磁舟并排放入管式炉炉管中,随后将炉管抽成真空(真空度:-0.1 MPa)。以10 ℃/min的升温速率将管式炉温度升温至160 ℃,并恒温1 h,使尿素充分分解,管式炉炉管内压力达到常压,此时管式炉炉管中主要存在NH3、水蒸气、CO2。若炉管内压力超过常压,则打开出气阀放空,使炉管内压力维持常压状态。反应方程式为
| $ {\text{CO}}{\left( {{\text{N}}{{\text{H}}_2}} \right)_2}\xrightarrow{{160{\text{℃}}}}{\text{N}}{{\text{H}}_3} + {\text{HCNO}} $ | (5) |
| $ {\text{HCNO}} + {{\text{H}}_2}{\text{O}} \to {\text{N}}{{\text{H}}_3} + {\text{C}}{{\text{O}}_2} $ | (6) |
在160 ℃下恒温1 h后,设定管式炉升温速率为10 ℃/min,将管式炉温度分别升至500、600、700、800 ℃,在每个温度下分别恒温12 h。为考察处理时间对石墨毡氮掺杂效果的影响,在700 ℃下,设定的恒温时间为6、12、24 h。最后设定降温速率为5 ℃/min,待管式炉温度降为室温后将石墨毡电极取出。
1.3 电极材料的表征傅里叶红外光谱(FT-IR):将石墨毡样品与干燥后的溴化钾(质量比1:100)充分研磨压片后进行FT-IR测定。X射线光电子能谱(XPS):将石墨毡充分研磨成粉末状,进行XPS测试。场发射扫描电子显微镜(SEM):将石墨毡纤维固定在导电胶上,进行SEM测试,观察氮掺杂前后石墨毡纤维形貌是否发生变化。
1.4 电化学测试三电极体系测试线性极化曲线(LSV)及循环伏安曲线(CV):配制300 mL电解液(CuCl2 1.00 mol/L,CuCl 0.15 mol/L,HCl 2.00 mol/L);以铂片(3 mm×3 mm)做对电极,Ag/AgCl/3.5 mol/L KCl电极(相对标准氢电极,E=0.205 V)做参比电极;分别使用原始石墨毡及氮掺杂后的石墨毡做工作电极。在25 ℃下,用2273型电化学工作站以20 mV/s的扫描速率测试CV曲线,以0.05 mV/s的扫描速率测试LSV曲线。
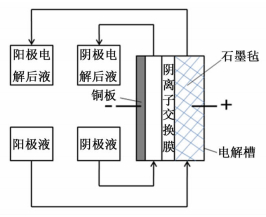
1.5 电解实验电解实验流程如图 1所示。电解槽采用铜板做阴极,石墨毡做阳极;阴极室与阳极室用阴离子交换膜隔开;使用Ag/AgCl 3.5 mol/L KCl电极(相对标准氢电极,E=0.205 V)作参比电极。控制电解实验电流密度为300 A/m2,测试不同流量下阳极对酸性氯化铜蚀刻废液的电解效果,并计算阳极电流效率。阳极电流效率按式(7)计算:
| $ \varepsilon = \frac{{Fv\left( {{C_{{\text{Out,C}}{{\text{u}}^ + }}} - {C_{{\text{In,C}}{{\text{u}}^ + }}}} \right)}}{I} $ | (7) |
|
| 图 1 电解实验过程示意图 Figure 1 Schematic of experimental process of electrochemical regeneration of acidic cupric chloride etchant |
| |
其中,F、ν、COut, Cu+、CIn, Cu+、I分别代表法拉第常数、阳极流量、阳极液入口处Cu(Ⅰ)浓度、阳极液出口处Cu(Ⅰ)浓度、电流强度。
2 结果与讨论 2.1 FT-IR分析图 2为700 ℃进行氮掺杂12 h后的石墨毡及原始石墨毡的FT-IR图。其中原始石墨毡样品出现明显的—NH及—OH伸缩振动峰(3 416)、C—H伸缩振动峰(2 920)、C—N及C=O伸缩振动峰(1 644)、—OH弯曲振动峰(1 384)。氮掺杂后石墨毡样品的FT-IR谱图发生了明显的变化,其中—NH及—OH官能团的伸缩振动特征峰(3 441)明显变宽且强度增加,而—OH官能团的弯曲振动特征峰(1 384)并未发生明显变化,这说明处理后的石墨毡纤维表面负载上了一定量的含氮官能团;C—H官能团特征峰明显变弱(2 920),说明石墨毡表面C—H官能团的比例降低;C—N的特征峰(1 644)强度明显增强,说明有一部分N以掺杂的形式与石墨毡结合。

|
| 图 2 石墨毡的FT-IR谱图 Figure 2 FT-IR spectra of pristine graphic felt |
| |
图 3a)所示为原始石墨毡及700 ℃掺杂12 h石墨毡的XPS谱图,其中原始石墨毡未能检测出氮元素存在,氮含量为0%,而700 ℃掺杂12 h的石墨毡样品检测到含氮量为2.68%,并在结合能400 eV处出现了明显的含氮官能团峰。图 3b)为700 ℃掺杂12 h石墨毡关于氮1 s杂化的XPS拟合图。

|
| 图 3 原始石墨毡与700 ℃掺杂12 h石墨毡XPS谱图a)700 ℃掺杂12 h石墨毡N1s杂化拟合图b) Figure 3 XPS survey spectrum of pristine graphic felt and treated at 700 ℃ for 12 h a) fine-scanned N1s spectrum of graphic felt treated at 700 ℃ for 12 h b) |
| |
由图 3中可以看出存在3种形式的含氮官能团,分别为:吡啶氮,结合能398.5 eV;吡咯氮,结合能400.3 eV;石墨氮,结合能401.3 eV。其中吡啶氮和吡咯氮含量较多,分别为50%及35.5%;石墨氮含量相对较少,为14.5%。
2.3 SEM分析由图 4a)及图 4b)的SEM图可以看出,原始石墨毡纤维表面较光滑,而700 ℃氮掺杂12 h后的石墨毡出现了一定程度的蚀刻,表面变得粗糙,但整体形貌并没有太大改变;由图 4c)及图 4d)可以看出,700 ℃氮掺杂24 h及800 ℃氮掺杂12 h的石墨毡纤维出现了断裂及表面蚀刻等现象,这是由于反应温度的升高及反应时间的延长使石墨毡纤维强度变弱,相比于掺杂温度较低及掺杂时间较短的石墨毡纤维在制样时更易发生断裂。

|
| 图 4 不同掺杂条件下石墨毡SEM图 Figure 4 SEM images |
| |
图 5和图 6分别展示了不同氮掺杂条件下得到的石墨毡电极的CV曲线,其电化学参数分别归纳于表 1和表 2中。

|
| 图 5 25 ℃下不同石墨毡电极(原始石墨毡电极及700 ℃下处理不同时间的石墨毡电极)的CV曲线 Figure 5 CV curves recorded at 25 ℃ using pristine graphic felt and treated at 700 ℃ for different time |
| |

|
| 图 6 25 ℃下不同石墨毡电极(原始石墨毡电极及不同温度处理12 h石墨毡电极)的CV曲线 Figure 6 CV curves recorded at 25 ℃ using pristine graphic felt and treated at different temperature for 12 h |
| |
由图 5和图 6的CV曲线可以看到,电位范围在1.1~1.3 V(相对于标准氢电极)之间的氧化峰表示Cu(Ⅰ)/Cu(Ⅱ)电对的电化学氧化反应;电位范围在0.74~0.8 V之间的还原峰表示Cu(Ⅰ)/Cu(Ⅱ)电对的电化学还原反应;当氧化电位超过1.4 V后,开始有析氧反应的发生;当还原电位达到0.6 V以下时发生析氢反应。从表 1中可以发现,经过氮掺杂后的石墨毡电极的氧化峰电流密度(Ipa)及还原峰电流密度(Ipc)均较原始石墨毡有较大的提高,其中对于酸性蚀刻废液回收有着重要意义的氧化峰电流密度提高较多。700 ℃处理12 h的石墨毡电极氧化峰电流密度达到4.038 A/g,较原始石墨毡电极的峰电流密度提高了36.6%,这表明处理后的石墨毡电极对于溶液中Cu(Ⅰ)氧化为Cu(Ⅱ)的电化学活性有很大的提高。其中700 ℃处理12 h的石墨毡电极具有最高的峰电流密度,说明在这一条件下处理得到的石墨毡电极对于Cu(Ⅰ)/Cu(Ⅱ)电对的氧化反应具有最高的电化学活性。
由XPS结果分析可知,氮掺杂后石墨毡纤维含氮量增加2.68%。因此可判断使氮掺杂后石墨毡电极的电化学活性提高的主要原因是石墨毡表面含氮官能团增加。一方面,含氮官能团的存在增加了石墨毡纤维的亲水性,使溶液中Cu(Ⅰ)更容易吸附在石墨毡电极纤维表面,增强了Cu(Ⅰ)与石墨毡纤维之间的传递。另一方面,Cu(Ⅰ)及Cu(Ⅱ)在酸性蚀刻液中以[CuCl2]-和[CuCl4]2-络合物的形式存在,这些显电负性的络合离子更易与石墨毡表面存在的—NH3+结合,这很大程度上增加了铜离子与石墨毡纤维表面的物质传递。吡啶型和吡咯型的掺杂态氮是强吸电子基团,可以使石墨毡碳纤维表面的电子云发生偏离,形成使铜离子更易结合的空穴,从而使电极的电化学活性增强。
700 ℃掺杂24 h及800 ℃掺杂12 h后的石墨毡电极的电化学性能降低。这是由于掺杂时间的增长及掺杂温度的升高会使石墨毡纤维变脆,从而使纤维在制样及测试过程中更易断裂脱落,导致石墨毡电极质量低于其标称质量,使电极的表观质量比性能下降。
图 7是原始石墨毡电极及700 ℃掺杂12 h石墨毡电极的线性极化曲线(LSV)。

|
| 图 7 25 ℃下不同石墨毡电极(原始石墨毡电极和700 ℃处理12 h石墨毡电极)的稳态极化曲线 Figure 7 LSV curves recorded at 25 ℃ using pristine graphic felt and treated at 700 ℃ for 12 h |
| |
由图 7可以看出,25 ℃下原始石墨毡在电位为0.65 V(相对标准氢电极)时开始Cu(Ⅰ)的氧化;电位在0.68~1.40 V被Cu(Ⅰ)离子扩散控制,反应达到极限电流密度,其极限电流密度值为0.25 A/g;电位超过1.45 V时,体系开始有氧气及氯气析出。而处理后的石墨毡在电位为0.60 V时开始Cu(Ⅰ)的氧化;电位在0.65~1.35 V被Cu(Ⅰ)离子扩散控制,反应达到极限电流密度,其极限电流密度值为0.26 A/g;电位在1.35 V时开始有氧气和氯气的析出。与原始石墨毡相比,处理后石墨毡电极的阳极电位低了约0.50 V,这说明修饰后的石墨毡电极对于Cu(Ⅰ)的电化学氧化活性增强。
2.5 电解实验结果分析在电流密度为300 A/m2下,用两种石墨毡做阳极进行酸性蚀刻液电解再生回收的实验数据如表 3所示。
| 电极 | 阳极流量v/(mL·min-1) | 阳极电位E/V | 槽电压△Ecell/V | 阳极电流效率ε/% | CIn, Cu+/(mol·L-1) | COut, Cu+/(mol·L-1) |
| 原始石墨毡 | 6.0 | 1.23 | 1.61 | 99.1 | 0.10 | 0.0137 |
| 10.0 | 1.03 | 1.60 | 98.7 | 0.10 | 0.0484 | |
| 修饰后石墨毡 | 6.0 | 1.07 | 1.56 | 99.6 | 0.10 | 0.0133 |
| 10.0 | 0.93 | 1.53 | 99.5 | 0.10 | 0.0480 |
从表 3中可以看出,使用氮掺杂的石墨毡电极时阳极电位较使用原始石墨毡时低0.10~0.15 V,槽电压较使用原始石墨毡时低0.05 V左右。而阳极电位和槽电压的降低可避免氯气的析出,同时节约体系能耗。
3 结论1) 通过将石墨毡与尿素一同在管式炉中进行热处理的方法,可以成功对石墨毡进行氮掺杂修饰,掺杂后的石墨毡含氮量增加了2.68%,其中氮元素分别以吡啶氮、吡咯氮、石墨氮的形式存在。
2) 含氮官能团的存在增强了Cu(Ⅰ)与石墨毡纤维表面的传递,进而提高了石墨毡电极对于Cu(Ⅰ)/Cu(Ⅱ)电对的电化学活性。
3) 采用掺杂后的石墨毡做酸性蚀刻液电解回收阳极时可以有更低的阳极电位,更小的槽电压,这对于抑制电解析气及降低反应能耗具有重要意义。
| [1] | Li C P L, Ciccolo P, Yee D K W, et al. Inner-Layer copper reliability of electroless copper processes[J]. Circuit World , 2010, 36(1) : 31–37. DOI: 10.1108/03056121011015077 |
| [2] | Cordani J L, Letize R A. Copper etchant compositions: US, 4784785[P]. 1988-01-01 |
| [3] | 胡耀红, 赵国鹏, 谢素玲, 等. 印刷线路板含铜废蚀刻液的回用处理(一)[J]. 胡耀红, 赵国鹏, 谢素玲, 等. 2009. 印刷线路板含铜废蚀刻液的回用处理(一)[J]. 电镀与涂饰 , 2009 , 28 (10) : 32–35. Hu Yaohong, Zhao Guopeng, Xie Suling, et al. Reuse treatment of spent copper-containing etching solution for printed circuit board-Part I[J]. Electroplating & Finishing , 2009, 28(10) : 32–35. |
| [4] | Cakir O. Copper etching with cupric chloride and regeneration of waste etchant[J]. Journal of Materials Processing Technology , 2006, 175(1/3) : 63–68. |
| [5] | 王红华, 蒋玉思. 酸性氯化铜液蚀刻化学及蚀刻液再生方法评述[J]. 王红华, 蒋玉思. 2008. 酸性氯化铜液蚀刻化学及蚀刻液再生方法评述[J]. 印制电路信息 , 2008 (10) : 57–60. Wang Honghua, Jiang Yusi. The chemistry of acidic cupric chloride etching process and review on regenerating methods for cupric chloride etchant[J]. Printed Circuit Information , 2008(10) : 57–60. |
| [6] | Ott R, Reith H. Method and apparatus for regeneration of a copper-containing etching solution: US, 4508599[P]. 1985-04-02 |
| [7] | Oxeley J E. Electrolytic regeneration of acid cupric chloride etchant: US, 5421966[P]. 1995-06-06 |
| [8] | Hillis M R. Method for the electrolytic regeneration of etchants for metals: US, 4468305[P]. 1984-08-28 |
| [9] | Yang Z, Huang C, Wang Y, et al. A new electrolytic method for on-site regeneration of acidic copper(II) Chloride etchant in printed circuit board production[J]. International Journal of Electrochemical Science , 2013(8) : 6 258–6 268. |
| [10] | Li X, Huang K, Liu S, et al. Characteristics of graphite felt electrode electrochemically oxidized for vanadium redox battery application[J]. Trans Nonferrous Mat Soc Chin , 2007, 17(1) : 195–199. DOI: 10.1016/S1003-6326(07)60071-5 |
| [11] | Zoraida G, Cristina B, Patricia A, et al. Thermally reduced graphite oxide as positive electrode in vanadium redox flow batteries[J]. Carbon , 2012, 50(3) : 828–834. DOI: 10.1016/j.carbon.2011.09.041 |
| [12] | Sun B, Skyllas-Kazacos M. Modification of graphite electrode materials for vanadium redox flow battery application—I. Thermal treatment[J]. Electrochimical Acta , 1992, 37(2) : 1 253–1 260. |
| [13] | Sun B, Skyllas-Kazacos M. Chemical modification of graphite electrode materials for vanadium redox flow battery application—part II. Acid treatment[J]. Electrochimica Acta , 1992, 37(13) : 2 459–2 465. DOI: 10.1016/0013-4686(92)87084-D |
| [14] | He Z, Su A, Gao C, et al. Carbon paper modified by hydrothermal ammoniated treatment for vanadium redox battery[J]. Lonics , 2013, 19(7) : 1 021–1 026. |
 2016, Vol. 33
2016, Vol. 33





