早在20世纪60年代,Indig和Snyder首次提出直接硼氢化钠燃料电池概念[1]。直接硼氢化钠燃料电池(DBFC)是以碱性硼氢化钠为阳极燃料,O2或者酸性H2O2为氧化剂,从而将化学能直接转化为电能。与质子交换膜燃料电池(PEMFC)相比,DBFC克服了燃料的储存与运输问题,也不存在阳极催化剂的CO中毒现象。此外,DBFC还具有理论开路电压高、工作温度低、功率密度较高、NaBH4及其氧化产物NaBO2稳定且无毒、NaBO2可循环利用、环境友好等特点,受到广大科研工作者的关注,特别是在便携式电源方面有巨大的优势[2-4]。
然而,长期以来DBFC的应用一直受到硼氢化钠水解反应的限制。开发设计高选择性和高催化活性的DBFC阳极催化剂,从而提高BH4-阳极动力学速度,抑制BH4-水解析氢,实现8电子反应,是DBFC阳极催化剂研究的重要方向,也是实现DBFC商业化的关键性问题。DBFC阳极催化剂的研究以贵金属为主,主要有Pt、Pd、Au、Ag等以及过渡金属,其中以Pt、Pd、Au和Ni的研究最为广泛[3, 5]。合金催化剂具有较高的稳定性和催化活性,并且可以降低成本,DBFC阳极催化剂的研究主要集中在Pt、Au及Pd的二元合金催化剂[6-8]。
目前有关Pd-Ag/C合金催化剂在硼氢化钠电氧化反应中的电化学行为的研究尚未报道过。本研究以硼氢化钠作为还原剂,柠檬酸钠为保护剂,在室温下制备了不同原子比的Pd-Ag/C催化剂,并研究分析了其对硼氢化钠电化学行为的影响。
1 试验部分 1.1 试剂和仪器硼氢化钠,氢氧化钠,二水合硝酸钯,硝酸银,柠檬酸钠,均为分析纯,购自天津市光复精细化工研究所;导电碳黑(VULCAN XC-72,CABOLT);Nafion膜溶液(DE520,上海河森电气有限公司);乙醇(体积分数为95%),去离子水,购自天津江天化工技术有限公司;α-氧化铝抛光粉(粒径30~50 nm),α-氧化铝抛光粉(粒径0.5~0.7 μm),均购自天津艾达恒晟科技发展有限公司。
循环水真空泵(SHZ-DⅢ型,巩义市英峪高科仪器厂),恒温磁力搅拌器(85-2,巩义市予华有限责任公司),电热真空干燥箱(DZG-403),电化学工作站(PARSTAT-2273,Princeton Applied Research),高功率数控超声波清洗器(KQ-400KDB,昆山市超声仪器有限公司)。
1.2 催化剂的制备分别称取所需质量的二水合硝酸钯、硝酸银和柠檬酸钠,加入到100 mL去离子水中。逐滴加入过量的0.1 mol/L NaBH4,并搅拌2 h,再加入一定质量的导电碳黑,室温下搅拌12 h。然后减压抽滤,并用热的去离子水多次洗涤。最后将所得过滤物,在80 ℃下真空干燥24 h,研磨即得到Pd-Ag/C催化剂。所制备的不同原子比的Pd-Ag/C催化剂分别为Pd/C、Pd80Ag20/C、Pd75Ag25/C、Pd67Ag33/C、Pd50Ag50/C、Ag/C,其金属负载量均为20%。
1.3 催化剂XRD表征催化剂的晶粒大小和晶体结构分析在日本理学D/MAX-2500型X射线衍射仪上进行,衍射源为Cu_Kα靶,λ=0.154 056 nm,管电压为40 kV,电流为200 mA,扫描速度为5(°)/min,扫描角度范围2θ为10°~90°。
1.4 电化学性能测试电化学测试在2273电化学工作站上进行,采用三电极体系,以Pd-Ag/C或Pd/C为工作电极,Ni网(2.0 cm×2.5 cm)为辅助电极,Ag/AgCl(KCl,3.5 mol/L)为参比电极(文中电位值无特别说明均是相对于该电极电位)。电解液分别是3 mol/L NaOH溶液和0.1 mol/L NaBH4+3 mol/L NaOH混合溶液,循环伏安法的电位窗口为-1.0~0.5 V和-1.2~0.6 V;电化学阻抗谱测试频率范围为0.01~10 000 Hz,正弦波幅为5 mV,测试电压为开路电位,所有测试均在室温下进行。
称取10 mg催化剂于5 mL小烧杯中,分别加入0.75 mL乙醇和0.25 mL Nafion膜溶液,超声2 h至分散均匀后,将5 μL分散液滴加到抛光好的玻碳电极(直径为4 mm)上,然后将电极置于真空干燥箱中,60 ℃下干燥30 min,即得到工作电极。玻碳电极在每次使用前应抛光处理,首先依次用α-氧化铝抛光粉(粒径30~50 nm)、α-氧化铝抛光粉(粒径0.5~0.7 μm)在麂皮上抛光,然后分别用乙醇、水超声清洗。
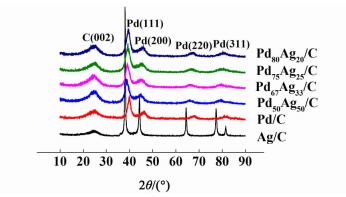
2 结果与讨论 2.1 催化剂的XRD表征图 1为催化剂Pd/C、Ag/C和Pd-Ag/C的XRD衍射图。
|
| 图 1 催化剂Pd/C、Ag/C和Pd-Ag/C的XRD谱图 Figure 1 XRD patterns of Pd/C, Ag/C and Pd-Ag/C catalysts |
| |
如图 1在约25°处都有1个衍射峰,这是碳载体Vulcan XC-72的衍射峰,为具有密排六方结构的石墨(002)晶面衍射峰(参见PDF#75-1621)。Ag/C的XRD图谱在2θ分别为38°、44°、64°、77°、82°处有4个明显的衍射峰,分别对应具有面心立方结构Ag的(111)、(200)、(220)、(311)、(222)晶面(参见PDF# 87-0597)。在Pd/C和Pd-Ag/C的XRD图谱中,40°、46.2°、67.8°、81.4°处的峰分别对应具有面心立方结构Pd的(111)、(200)、(220)、(311)晶面(参见PDF#65-6174)。对比XRD谱图可知Pd-Ag/C催化剂中并没有出现Ag衍射峰,也没有PdO、Ag2O及AgOH的衍射峰,其可能以无定形态存在或者量很少。与Pd/C衍射峰相比,Pd-Ag/C对应的衍射峰所在的2θ角明显负移,并且随着Ag含量的减少负移程度也减弱,表明金属Ag进入到Pd的晶格中,与Pd形成了合金[9]。
表 1为催化剂晶粒尺寸及晶格常数。其中晶粒尺寸的估算采用Sherrer公式
| 催化剂 | Pd(220)衍射峰 角度/(°) |
晶粒尺寸/ nm |
晶格常数/ nm |
| Pd/C | 39.9 | 7.9 | 0.3898 |
| Pd80Ag20/C | 39.5 | 5.7 | 0.3929 |
| Pd75Ag25/C | 39.3 | 2.6 | 0.3966 |
| Pd67Ag33/C | 39.1 | 3.9 | 0.3986 |
| Pd50Ag50/C | 38.8 | 13.2 | 0.4001 |
| Ag/C | 38.1 | 27.5 | 0.4087 |
采用PdO的还原峰对所制备催化剂电化学活性表面积进行表征[8, 11],电化学活性表面积计算公式为:ECSA=Q/(0.424×[Pd]),其中,Q(mC)表示PdO还原的积分电量值,[Pd](mg)表示Pd在工作电极上的负载量,0.424(mC/cm2)表示单层PdO还原所需电荷值。
图 2为Pd/C和Pd-Ag/C催化剂所制电极在3 mol/L NaOH溶液中的循环伏安曲线,扫描速率为50 mV/s。

|
| 图 2 Pd/C和Pd-Ag/C电极在3 mol/L NaOH溶液中的循环伏安曲线,扫描速率:50 mV·s-1 Figure 2 Cyclic voltammograms of Pd/C and Pd-Ag/C in 3 mol/L NaOH at scan rate of 50 mV·s-1 |
| |
计算可得,Pd/C、Pd80Ag20/C、Pd75Ag25/C、Pd67Ag33/C、Pd50Ag50/C电化学活性表面积分别为54.44、187.28、227.28、166.88和145.62 cm2/mg。由图 2可以看出在所制备的催化剂中,Pd75Ag25/C的ECSA最大,且Pd-Ag/C合金催化剂的电化学活性表面积(ECSA)均高于Pd/C催化剂,同时Ag的掺杂使氧化钯的还原峰电位发生正移。通过Ag的掺杂可以大大提高催化剂的电化学活性表面积,这可能是由于催化剂粒径较小,分散均匀引起的。
图 3为Pd/C和Pd-Ag/C催化剂所制电极在0.1 mol/L NaBH4+3 mol/L NaOH溶液中的循环伏安曲线,扫描速率为20 mV·s-1。

|
| 图 3 Pd/C和Pd-Ag/C电极在0.1 mol/L NaBH4+3 mol/L NaOH溶液中的循环伏安曲线,扫描速率为20 mV·s-1 Figure 3 Cyclic voltammograms of Pd/C and Pd-Ag/C in 0.1 mol/L NaBH4+3 mol/L NaOH at scan rate of 20 mV·s-1 |
| |
由图 3可以看出,在正扫和反扫过程中各有1个明显的氧化峰,均为硼氢化钠反应中间产物BH3OH-的电氧化反应。采用正扫过程中氧化峰峰a的电流密度来评价催化剂的催化活性[12]。可知Pd/C、Pd80Ag20/C、Pd75Ag25/C、Pd67Ag33/C、Pd50Ag50/C的峰电流密度分别为0.0567、0.0506、0.0781、0.0760和0.0439 A·cm-2。其中Pd75Ag25/C峰a的电流密度为0.0781 A·cm-2,催化活性最高,是Pd/C电流密度的1.38倍。可见适量Ag的掺杂可以有效降低催化剂的成本,并提高硼氢化钠电氧化反应的催化活性。此外Ag的掺杂对催化剂的峰形有一定影响,可能是反应机理发生改变,且随着Ag掺杂量的减少,其循环伏安曲线越来越接近Pd/C的循环伏安曲线。
计时电流曲线可以有效评估催化剂的催化活性和硼氢化钠电氧化反应的稳定性。图 4a)为Pd/C和Pd-Ag/C电极在0.1 mol/L NaBH4+3 mol/L NaOH溶液中的计时电流曲线,电位阶跃为-1.2~-0.2 V。图 4b)为相应的Cottrell曲线,即it1/2-t关系曲线。图 4c)为前5 s i-t-1/2拟合直线,Pd/C、Pd80Ag20/C、Pd75Ag25/C、Pd67Ag33/C、Pd50Ag50/C拟合直线斜率分别为0.017、0.013、0.024、0.021和0.009。

|
| 图 4 a) Pd/C和Pd-Ag/C电极在0.1 mol/L NaBH4+3 mol/L NaOH溶液中的计时电流曲线,电位阶跃为-1.2~-0.2 V;b)相应的Cottrell曲线;c)前5 s i-t-1/2拟合直线 Figure 4 a) Chronoamperometry curves of Pd/C and Pd-Ag/C electrodes in 0.1 mol/L NaBH4+3 mol/L NaOH, potential step from -1.2~0.2 V; b) Cottrell plot generated from the chronoamperometry data; c)i-t-1/2 fitted lines within 5 s |
| |
从图 4a)中可以看出,当电位阶跃时各电极均存在电流衰减的现象,前10 s电流衰减较快,20 s后达到拟稳态,100 s时所制备的催化剂对硼氢化钠电氧化反应催化活性大小顺序为Pd75Ag25/C>Pd67Ag33/C>Pd/C>Pd80Ag20/C>Pd50Ag50/C,结论与循环伏安曲线一致,进一步说明Ag的掺杂可以提高催化剂的催化活性。从图 4b)可以看出it1/2随着时间的增大而增大,表明BH4-的电氧化反应并不受扩散控制[13]。此外,递增的cottrell曲线说明反应过程中电极表面并没有中毒。同时cottrell曲线进一步证明了在所制备的催化剂中Pd75Ag25/C对硼氢化钠的催化活性最高。在硼氢化钠燃料电池体系中,常采用Cottrell方程估算硼氢化钠电氧化反应过程中的转移电子数[14]。假设不同电极的面积和测试体系的扩散系数相同,则由Cottrell方程
图 5为Pd/C和Pd-Ag/C电极在0.1 mol/L NaBH4+3 mol/L NaOH溶液中的交流阻抗谱。

|
| 图 5 Pd/C和Pd-Ag/C电极在0.1 mol/L NaBH4+3 mol/L NaOH溶液中的交流阻抗谱 Figure 5 Electrochemical impedance spectroscopes of Pd/C and Pd-Ag/C electrodes in 0.1 mol/L NaBH4+3 mol/L NaOH |
| |
从图 5中可以看出不同电极的阻抗谱类似,均为半径不同的不完全半圆弧。半圆弧包括双电层电容过程和电化学氧化反应,而且半圆弧的半径与硼氢化钠电氧化反应的阻力有关,半径越小,电化学反应阻抗越小,硼氢化钠电氧化反应越容易进行,催化剂的活性越高。不同电极硼氢化钠电化学氧化反应阻抗大小顺序为Pd75Ag25/C < Pd67Ag33/C < Pd/C < Pd80Ag20/C < Pd50Ag50/C,催化活性次序与之相反。该测试结果,与循环伏安曲线和计时电流曲线的结论一致。
3 结论采用硼氢化钠还原法制备了一系列的Pd-Ag/C合金催化剂,并研究了其对硼氢化钠电氧化反应的电催化活性。研究结果表明:适量Ag的掺杂不仅可以提高催化剂的催化活性,并且可以提高硼氢化钠电氧化反应过程中的转移电子数,有利于提高燃料利用率。此外合金催化剂单位质量Pd的催化活性均高于Pd/C,故Ag的掺杂可以提高催化剂的催化活性并降低成本。
| [1] | Indig M E, Snyer R N. Sodium borohydride, an interesting anodic fuel[J]. Journal of the Electrochemical Society , 1962, 109(11) : 1104–1106. DOI: 10.1149/1.2425247 |
| [2] | Liu B, Li Z, Suda S. Anodic oxidation of alkali borohydrides catalyzed by nickel[J]. Journal of the Electrochemical Society , 2003, 150(3) : A398–A402. DOI: 10.1149/1.1553785 |
| [3] | Ma J, Choudhury N A, Sahai Y. A Comprehensive review of direct borohydride fuel cells[J]. Renewable and Sustainable Energy Reviews , 2010, 14 : 183–199. DOI: 10.1016/j.rser.2009.08.002 |
| [4] | Finkelstein D A, Letcher C D, Jones D J, et al. Self-Poisoning during BH4- oxidation at Pt and Au, and in situ poison removal procedures for BH4- fuel cells[J]. J Phys Chem C , 2013, 117 : 1571–1581. |
| [5] | Jimenez I M, Leon C P, Shah A A, et al. Developments in direct borohydride fuel cells and remaining challenges[J]. Journal of Power Sources , 2012, 219 : 339–357. DOI: 10.1016/j.jpowsour.2012.06.091 |
| [6] | Concha B M, Chatenet M. Direct oxidation of sodium borohydride on Pt, Ag and alloyed Pt-Ag electrodes in basic media Part Ⅱ. Carbon-Supported nanoparticles[J]. Electrochimica Acta , 2009, 54 : 6130–6139. DOI: 10.1016/j.electacta.2009.04.074 |
| [7] | He P, Wang X, Liu Y, et al. Comparison of electrocatalytic activity of carbon supported Au-M (M=Fe, Co, Ni, Cu and Zn) bimetallic nanoparticles for direct borohydride fuel cells[J]. International Journal of Hydrogen Energy , 2012, 37 : 11984–11993. DOI: 10.1016/j.ijhydene.2012.05.054 |
| [8] | Behmenyar G, Akin A N. Investigation of carbon supported Pd-Cu nanoparticles as anode catalysts for direct borohydride fuel cell[J]. Journal of Power Sources , 2014, 249 : 239–246. DOI: 10.1016/j.jpowsour.2013.10.063 |
| [9] | Nguyen S T, Law H M, Nguyen H T, et al. Enhancement effect of Ag for Pd/C towards the electrooxidation in alkaline media[J]. Applied Catalysis B: Environmental , 2009, 91 : 507–515. DOI: 10.1016/j.apcatb.2009.06.021 |
| [10] | Li H, Sun G, Cao L, et al. Comparison of different promotion effect of PtRu/C and PtSn/C electrocatalysts for ethanol electrooxidation[J]. Electrochimica Acta , 2007, 52(24) : 6130–6139. |
| [11] | Grden M, Lukaszewski M, Jerkiewicz G, et al. Electrochemical behaviour of palladium electrode: Oxidation, electrodissolution and ionic adsorption[J]. Electrochimica Acta , 2008, 53 : 7583–7598. DOI: 10.1016/j.electacta.2008.05.046 |
| [12] | Wang G, Gao Y, Wang Z, et al. Investigation of PtNi/C anode electrocatalysts for direct borohydride fuel cell[J]. Journal of Power Sources , 2010, 249 : 185–189. |
| [13] | Atwan M H, Macdonald C L B, Northwood D O, et al. Colloidial Au and Au alloy catalysts for direct borohydride fuel cells: Electrocatalysis and fuel cell performance[J]. Journal of Power Sources , 2006, 158 : 36–44. DOI: 10.1016/j.jpowsour.2005.09.054 |
| [14] | Wei J, Wang X, Wang Y, et al. Investigation of carbon supported Au hollow nanospheres as electrocatalysts for electrooxidation of sodium borohydride[J]. International Journal of Hydrogen Energy , 2009, 34 : 3360–3366. DOI: 10.1016/j.ijhydene.2009.02.014 |
 2016, Vol. 33
2016, Vol. 33





