2. 天津大学化工学院, 天津 300072
2. School of Chemical Engineering and Technology, Tianjin University, Tianjin 300072, China
多晶型现象是指同一种物质存在2种或2种以上晶体结构,也叫同质异象或者同质多象现象;广义的多晶型包括了假多晶型即溶剂化物,溶剂化即结晶形式中含有已知量或者未知量的溶剂,若其中的溶剂为水,则溶剂化物即为水合物[1]。水分子和药物分子之间相互作用会影响晶体的晶格能,进而影响活性药物分子的溶解度、溶解速度、稳定性以及其生物利用度[2-5]。
据统计,至少有1/3的活性药物组分(API)可以形成水合物[6],根据水分子与药物分子之间的作用力不同,水合物可以分为3种类型:独立位点水合物即结合水合物(isolated site hydrates),通道水合物(channel hydrates)以及离子配位水合物(ion-associated hydrates)[7]。独立位点水合物中,水分子与水分子之间没有作用力,水分子和药物分子通过氢键和范德华力相互作用,脱水温度相对较高,在DSC中有尖的脱水吸热峰,TG中失重较窄,IR图谱中有尖的氢键振动峰[8]。通道型水合物中水分子与其相邻的水分子形成氢键,且沿某一晶轴呈链状分布,此类水合物脱水温度较独立位点水合物低,同时水分子的脱去不改变原来的晶体结构,形成的空隙可以被其他溶剂分子填充,在DSC中的脱水吸热峰和TG中的失量峰较宽,IR图谱中在相对较低的频率下有尖的氢键吸收峰[9]。当药物分子中有金属离子存在时,若与水分子形成离子配位键,即为离子配位水合物,因离子键一般很强,此类水合物脱水温度会很高[10]。
阿托伐他汀钙(atorvastatin calcium),商品名为立普妥(Lipitor),是目前临床最常用的降血脂药,化学名称为7-[2-(4-氟苯基)-3-苯基-4-(苯胺基甲酰基)-5-(2-丙基)吡咯-1-基]-3,5-二羟基庚酸钙;[R,(R*,R*)]-2-(4-氟苯基)-β,α-二羟基-5-(1-甲基乙基)-3-苯基-[(苯胺基)-羟基]-1H-吡咯-1-庚酸钙盐,相对分子质量约为1209.42,CAS号为344423-98-9,结构式如图 1。

|
| 图 1 阿托伐汀钙分子结构式 Figure 1 Chemical structure of atorvastatin hemi calcium |
| |
Ⅰ和Ⅱ晶型是其最重要的2个晶型[11],然而这2种晶型都为阿托伐他汀钙的水合物形式,并且都是三水化合物,是否这些水分子的存在模式和结合方式都一样呢?脱水过程是否完全一样呢?本研究针对这2个问题,对阿托伐他汀钙的水合物的多晶型的存在现象,水溶剂分子的结合方式和脱水过程进行了详细研究。本研究由阿托伐他汀内酯制备了阿托伐他汀钙Ⅰ晶型,通过Ⅰ晶型的悬浮转晶得到了Ⅱ晶型,并对晶型Ⅰ和Ⅱ进行了固相表征,主要研究了Ⅰ和Ⅱ晶型中水分子的结合方式和脱水过程对晶体产品的影响,为结晶工艺和干燥过程以及脱水转晶提供指导。
1 实验部分 1.1 实验药品与试剂阿托伐他汀内酯(质量分数大于99.8%),美国辉瑞制药公司;四甲基叔丁基醚(分析纯),甲醇(分析纯),氢氧化钠(质量分数大于99.5%)和一水乙酸钙(质量分数大于99.5%),天津市江天化工技术有限公司;去离子水,市售。
1.2 Ⅰ和Ⅱ晶型的制备将15.0 g阿托伐他汀内酯在室温下溶解在83 mL四甲基叔丁基醚和38 mL甲醇中,得到的内酯溶液加热到50.5 ℃,配制191 mL含有0.15 mol/L氢氧化钠的水溶液,与内酯溶液混合,维持混合液温度在49~55 ℃之间,反应46 min得到阿托伐他汀开环钠盐;冷却到29 ℃并弃置有机层,添加62 mL四甲基叔丁基醚到剩下的混合物中提取水层并弃置有机层;在得到的溶液中缓慢(超过30 min)加入一水乙酸钙溶液(2.5 g一水乙酸钙和81 mL水),保持反应温度在52.7~53.2 ℃之间,反应17 h,不断搅拌,降至室温,抽滤,在60 ℃和低压(~5 mm in Hg vacuum)下干燥产物,得到阿托伐他汀钙Ⅰ晶型。
将10 g阿托伐他汀钙Ⅰ晶型添加到120 mL甲醇和80 mL水的混合溶剂中,恒温30 ℃,搅拌72 h,抽滤,50 ℃干燥,得到阿托伐他汀钙Ⅱ晶型。
1.3 Ⅰ和Ⅱ晶型的固相表征 1.3.1 扫描电镜分析(SEM)采用日立台式扫描电子显微镜TM3000对产品进行晶体形态表征,将少量样品放在黏着双面胶的金属片上,观察前进行喷金处理。
1.3.2 X射线粉末衍射分析(PXRD)采用日本理学(Rigaku D/max-2500)X射线粉末衍射分析仪,射线源Cu_Kα(0.15405 nm),扫描范围为2°~50°(2θ),步长为0.02°,速率为1.2(°)/min,电源设置为40 kV,100 mA。
1.3.3 卡尔费休水分析(KF)Ⅰ/Ⅱ晶型中水含量的测定在梅特勒卡尔费休水分分析仪(Mettler Toledo V20 Volumetric KF Titrator)上完成,仪器在滴定前和滴定后均用酒石酸钠二水合物标定。每个样品均测试至少3次,当3次测量值相差小于0.2%时,将3次测量值取平均用来表示测量结果。
1.3.4 热分析(DSC)和热重分析(TGA)TGA和DSC 分析采用瑞士Mettler Toledo TGA/DSC 1/500,氮气为保护气,测试温度范围为25~200 ℃,升温速率为5 K/min,样品质量范围为5~10 mg,其中DSC测试时,样品置于扎孔的Al2O3坩埚中。
1.3.5 动态蒸汽吸附分析(DVS)Ⅰ/Ⅱ晶型等温吸附曲线的测定采用美国TA Instruments的DVS VTI-SA。测试前,阿托伐他汀钙Ⅰ、Ⅱ晶型均经过重结晶提纯处理,实验温度恒定为25 ℃,吸附和脱附过程均在湿度10%、20%、30%、40%、50%、60%、70%、80%和90%条件下测量药物的质量变化。
2 结果与讨论 2.1 阿托伐他汀钙Ⅰ/Ⅱ晶型的扫描电镜和粉末衍射图谱阿托伐他汀钙Ⅰ和Ⅱ晶型在晶体形态差异较小,均呈细长棒状(见图 2)。

|
| 图 2 阿托伐他汀钙的扫描电镜照片 Figure 2 SEM photoes of atorvastatin calcium |
| |
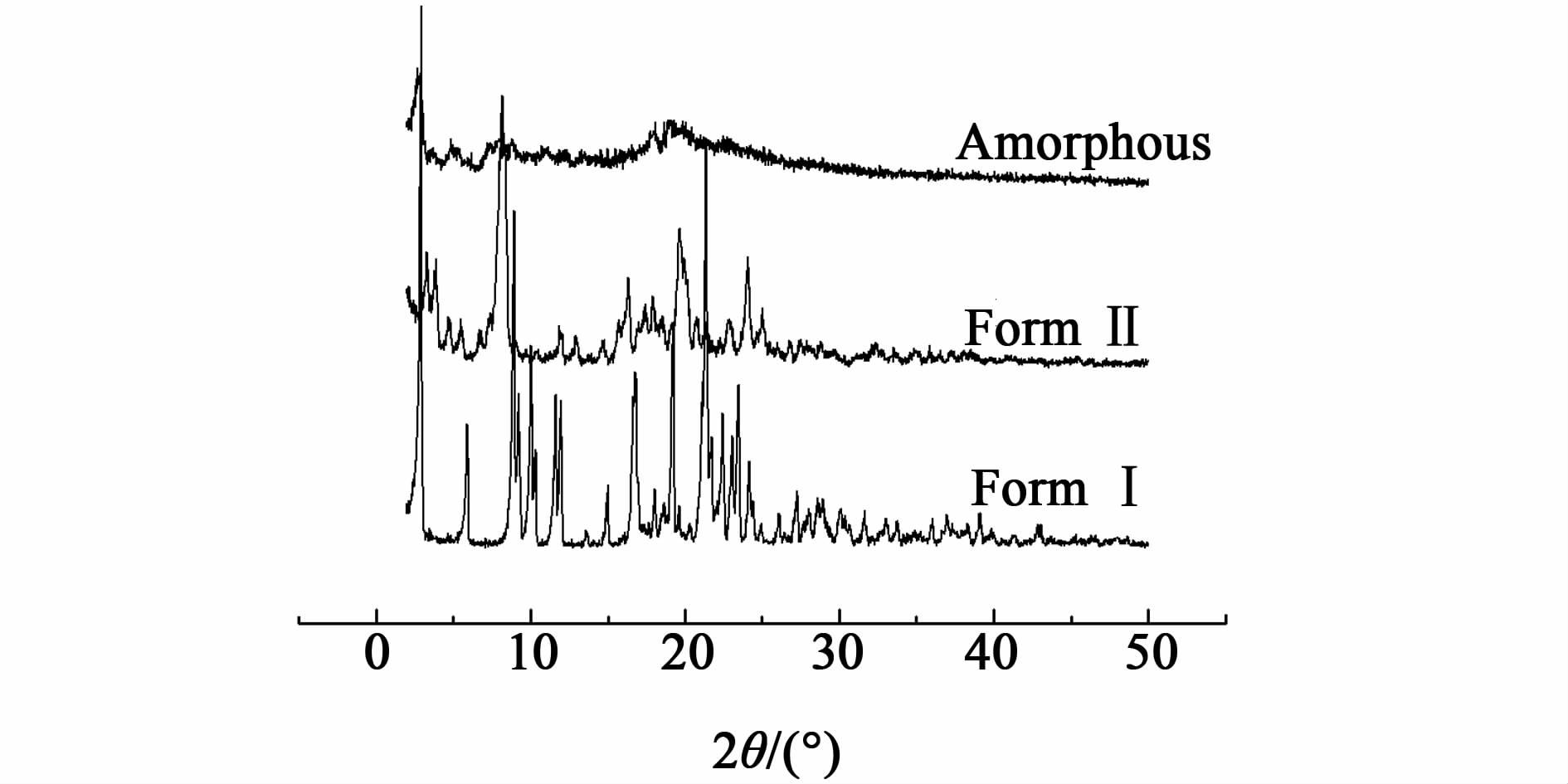
为了验证实验所得的产物是阿托伐他汀钙Ⅰ和Ⅱ晶型,我们对产物进行了X射线粉末衍射分析。如图 3所示,实验制得的Ⅰ和Ⅱ晶型的PXRD特征峰峰有明显的不同,其中,Ⅰ晶型的特征峰出现在2.9±0.2,5.9±0.2,8.9±0.2,9.2±0.2,10.1±0.2,10.3±0.2,11.6±0.2,11.9±0.2,16.8±0.2,19.2±0.2,21.4±0.2,23.5±0.2;Ⅱ晶型的特征峰则在3.3±0.2,3.9±0.2,8.2±0.2,16.3±0.2,19.7±0.2,24.1±0.2,均符合阿托伐他汀钙的晶型专利[11]。不同的粉末衍射特征峰表明这2种晶型的晶体结构之间结构存在差异。
|
| 图 3 阿托伐他汀钙晶型Ⅰ/Ⅱ和无定型的粉末衍射图 Figure 3 Powder X-ray diffraction patterns of atorvastatin calcium form Ⅰ,form Ⅱ and amorphous |
| |
专利报道[11],Ⅰ晶型包含1至8个水分子,一般为三水合物,Ⅱ晶型为水合物,产物水含量分析结果如表 1,通过计算可以得出晶型Ⅰ和Ⅱ均为阿托伐他汀钙的三水合物。
| 项目 | 含水量/%(质量分数) | |
| Ⅰ晶型 | Ⅱ晶型 | |
| 样品1 | 5.10 | 4.62 |
| 样品2 | 4.83 | 4.47 |
| 样品3 | 4.63 | 4.58 |
| 平均值 | 4.85 | 4.56 |
| 理论值 | 4.47 | 4.47 |
| 平均物质的量 | 3.20 | 2.70 |

|
| 图 4 阿托伐他汀钙Ⅰ/Ⅱ晶型热重分析 Figure 4 TGA curves of atorvastatin calcium forms Ⅰ and Ⅱ |
| |
热重分析中Ⅰ和Ⅱ晶型的失水总量符合卡尔费休水含量的测试结果,但在升温过程中Ⅰ和Ⅱ晶型却表现出截然不同的失水特点。晶型Ⅰ有3个明显的失水台阶,从75 ℃到115 ℃失水1.52%,从115 ℃到120 ℃失水1.48%,从120 ℃到150 ℃失水1.58%,总失水量为5.58%。晶型Ⅱ在整个升温过程中只有1个失水台阶,从开始升温到125 ℃总失水量为5.76%;通过计算得到,理论上1 mol水在阿托伐他汀钙三水合物中的质量分数即为1.49%,即,晶型Ⅰ中的3个水分子是随温度的升高逐步脱去的,晶型Ⅱ中的3个水是同时脱去的。
图 5可以让我们更好地理解Ⅰ和Ⅱ晶型的脱水过程,如图 5。晶型Ⅰ在73.49、110.20和130.96 ℃分别有3个吸热峰,对应TGA中3个不同的失水台阶,在154.74 ℃熔化,185 ℃分解;晶型Ⅱ只在 57.53 ℃有1个大的吸热峰,在173.84 ℃熔化,195 ℃分解,由于晶型Ⅱ的熔化温度和降解温度很接近,DSC中熔化峰会影响降解峰出现的位置,从TG图中可以看出2种晶型的分解温度基本上是同步的,在185 ℃附近,说明2种晶型脱水熔化以后完全一样,都是在185 ℃附近开始降解。很明显,晶型Ⅱ符合通道水合物的特点,晶型Ⅰ中则既有通道水又有结合水,结构更为复杂。

|
| 图 5 阿托伐他汀钙Ⅰ/Ⅱ晶型差示扫描量热分析 Figure 5 DSC curves of atorvastatin calcium forms Ⅰ and Ⅱ |
| |
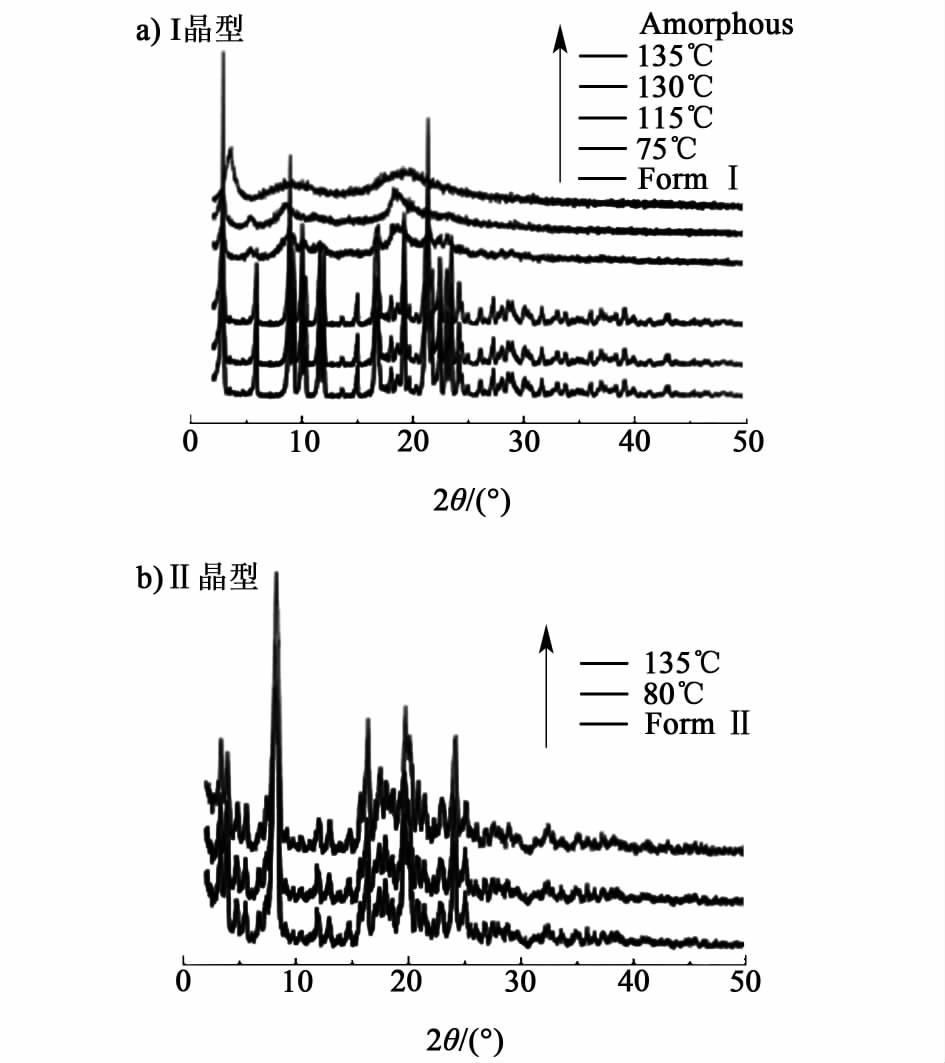
水分子因为其和有机药物分子的结合方式不同而分为通道型水合物和结合型水合物,在一些复杂的晶胞结构中,通道水和结合水会同时存在[12];阿托伐他汀钙Ⅰ晶型即为此类化合物,热重分析表明75和115 ℃,Ⅰ晶型分别脱去1分子水和脱去2分子水,此时将样品从TG分析坩埚中迅速取出,进行PXRD分析,结果见图 6。
|
| 图 6 阿托伐他汀钙PXRD Figure 6 PXRD patterns of atorvastatin calcium |
| |
由图 6可知,其PXRD并没有发生变化,这符合通道水的特点,因其不参与晶胞结构的构建,通道水的脱去并不影响物质的粉末衍射谱图,而在130 ℃附近,因第3分子水的脱除,Ⅰ晶型的PXRD开始发生变化,在135 ℃时,第3分子水已经完全脱除时,其PXRD图谱已经类似于阿托伐他汀钙无定型,这符合结合水的特征,结合水和药物分子间形成氢键,进而参与到晶格的构建,它的脱去会引起晶格的坍塌,缺陷甚至无定型化。Ⅱ晶型的变温PXRD分析表明,Ⅱ晶型的中3个水分子全为通道水。
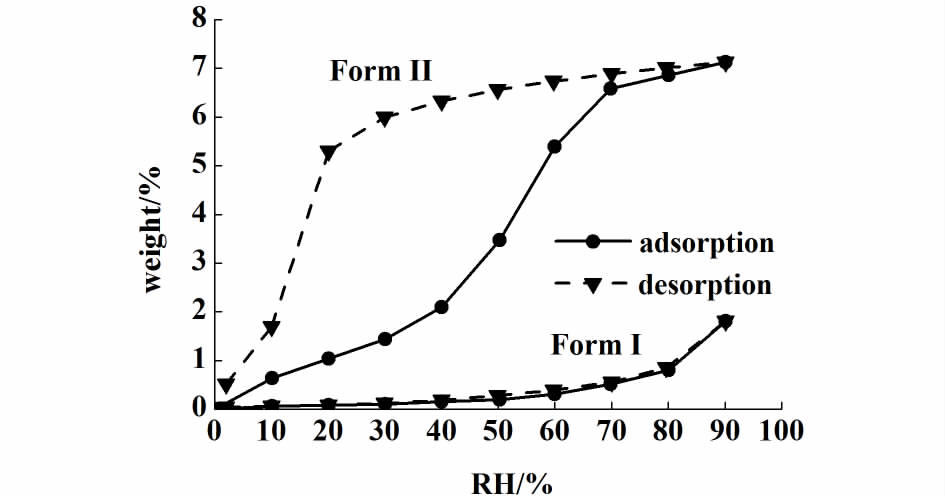
2.5 Ⅰ和Ⅱ晶型的吸湿性分析25 ℃时阿托伐他汀钙Ⅰ晶型和Ⅱ晶型等温吸附曲线如图 7所示。
|
| 图 7 25 ℃时阿托伐他汀钙Ⅰ晶型和Ⅱ晶型等温吸附曲线 Figure 7 DVS isotherm plot for atorvastatin calcium form Ⅰ and form Ⅱ at 25 ℃ |
| |
Ⅰ晶型属于轻度吸湿,在相对湿度小于80%时,Ⅰ晶型的质量分数变化小于1%,属于表面物理吸附过程,说明Ⅰ晶型在日常的湿度条件是稳定存在的。Ⅱ晶型则属于中度吸湿,其等温吸附曲线符合通道水合物的特点,药物质量随着湿度增大产生台阶式的增加,这表明药物晶体表面吸附的平衡水在高湿度条件下进入到晶格内部,形成了固定计量比或者非固定计量比的水合物,并且,Ⅱ晶型在吸湿过程中,当湿度大于40%时,其质量开始大幅度增加,在脱附过程中,当湿度降至20%以下时,药物质量才开始大幅下降,即药物质量呈台阶式增加及降低的临界湿度点并不一致,吸附和脱附过程不可逆,这是很多药物吸湿过程中普遍存在的现象[13]。
3 结论由阿托伐他汀内酯合成得到了阿托伐他汀钙Ⅰ晶型,由Ⅰ晶型制得了Ⅱ晶型;X射线粉末衍射分析证实了这2种不同的晶型;卡尔费休法测得Ⅰ和Ⅱ晶型的水含量分别为4.85%和4.56%,平均摩尔含水量均为3,但TGA和DSC分析中,Ⅰ晶型的3个水分子呈阶梯状失去,Ⅱ晶型则1次性失去3个水分子,利用TG,我们得到了不同温度下已经失去部分水的Ⅰ和Ⅱ晶型样品,再进行粉末衍射分析的结果表明,Ⅰ晶型中3个水分子中包含1个结合水,2个通道水,而Ⅱ晶型中的3个水分子均为通道水。Ⅰ和Ⅱ晶型等温吸附曲线的特点也符合这一判断。
| [1] | Bernstein J. Polymorphism-A perspective[J]. Crystal Growth Des,2011 : 632–650 |
| [2] | Cabri W, Ghetti P, Alpegiani M, et al. Cefdinir: A comparative study of anhydrous vs. monohydrate form: Microstructure and tabletting behavior[J]. Eur J Pharm Biopharm,2006 : 212–221 |
| [3] | Kawashima Y, Niwa T, Takeuchi H, et al. Characterization of polymorphs of tranilast anhydrate and tranilast monohydrate when crystallized by two solvent change spherical crystallization techniques[J]. J Pharm Sci,1991 : 472–478 |
| [4] | Allen P, Rahn P, Sarapu A, et al. Physical characterization of erythromycin: Anhydrate, monohydrate, and dihydrate crystalline solids[J]. J Pharm Sci,1978 : 1087–1093 |
| [5] | Henwood S, Liebenberg W, Tiedt L, et al. Characterization of the solubility and dissolution properties of several new rifampicin polymorphs, solvates, and hydrates[J]. Drug Dev Ind Pharm,2001 : 1017–1030 |
| [6] | Hilfiker R. Polymorphism in the pharmaceutical industry[M]. Weinheim: Hilfiker R, 2006 . |
| [7] | Tian F, Qu H, Zimmermann A, et al. Factors affecting crystallization of hydrates[J]. J Pharm Pharmacol,2010 : 1534–1546 |
| [8] | Zimmermann A, Tian F, Diego H, et al. Structural characterization and dehydration behavior of siramesine hydrochloride[J]. J Pharm Sci,2009 : 3596–3607 |
| [9] | Sun C, Zhou D, Grant D, et al. Theophylline monohydrate[J]. Acta Crystallorg Sect E,2002 : 368–370 |
| [10] | Gossman W, Wilson S, Oldfield E. Three hydrates of the bisphosphonate risedronate, consisting of one molecular and two ionic structures[J]. Acta Crystallogr C,2003 : 33–36 |
| [11] | Briggs C, Harasawa K, Ichikawa S, et al. Crystalline[R-(R*,R*)]-2-(4-dfluorophenyl)-β,α-dihydroxy-5-(1-methylethyl)-3-phenyl-4-[(phenylamino)carbonyl]-lH-pyrrole-1-heptanoic acid hemi calcium salt (Atorvastatin): US, 005969156[P]. 1999-10-19 |
| [12] | Giron D, Goldbronn C, Mutz M, et al. Solid state characterizations of pharmaceutical hydrates[J]. J Therm Anal Calorim,2002 : 453–465 |
| [13] | 王博超. 盐酸多奈哌齐结晶过程研究[D]. 天津: 天津大学, 2008 |
 2016, Vol. 33
2016, Vol. 33





