近几十年来,电化学储能技术的研究和发展一直受到各国能源、交通、电力等部门的重视。在电化学储能技术当中,锂离子电池具有能量密度高、使用寿命长、能量效率高等优点,具有广阔的发展空间[1]。磷酸铁锂电池(LFP)具有成本低、安全性好的优势[2, 3],目前已在国内实现了储能示范应用,而锰酸锂电池(LMO),尤其是以层状富锂锰酸锂材料为正极的锰酸锂电池不仅克服了尖晶石型锰酸锂电池的高温性能差的缺点[4, 5, 6],解决了磷酸铁锂电池能量密度低和倍率性能差的问题,同时具有成本低、对环境友好的优点,已成为目前国内外广泛关注的研究热点。
对于储能电池,因材料体系不同会使电池外特性上有所差别,包括电压特性曲线、能量密度、功率输出/输入能力等,在储能应用中需要在不破坏电池的前提下充分认识不同体系电池外特性的差异及产生原因,循环充放电测试是最直接的一种认识手段,但耗时长、效率低,且不能反映出引起电池差异产生的根本原因。交流阻抗技术(Electrochemical impedance spectroscopy,EIS)是研究电化学界面过程的重要方法,目前已被广泛应用于研究电池内部锂离子嵌入/脱出反应过程[7],通过EIS分析可以辨别电池的内部动力学信息,反映出电池外特性差异的根源。
本论文以储能用LMO电池为研究对象,通过建立等效电路解析反映LMO电池中锂离子嵌入/脱出电化学反应过程、电荷扩散过程的相关参数,研究这些参数随电池荷电状态(state of charge,SOC)变化的规律;并对电池进行高温充放电循环,对高温循环前后的电池EIS谱进行对比分析,研究高温循环对于电池内特性的影响。
1 实验部分研究对象为国内某厂家生产的储能用20 Ah LMO电池产品,正极为层状富锂锰酸锂材料,负极为硬碳材料,电解液为1 mol/L LiPF6/EC-DMC。
在室温下(20±2 ℃),对LMO电池产品进行3次0.5 C倍率的恒流充放电测试,以最后一次放电容量记为该电池的容量。对电池充电到100%SOC,静置3 h后进行EIS测试,然后以0.5 C倍率对电池放电,放电量为电池容量的5%,静置3 h后进行EIS测试,反复进行以上操作,直至电池SOC降为0%。EIS测试采用瑞士万通Auto Lab Pgstat302N电化学工作站,测试频率为10 mHz~10 kHz,振幅10 mV,阻抗谱的拟合分析采用电化学工作站配套软件Nova进行,拟合x2<0.01,常相位角元件(Constant Phase Element,CPE)的n在0.4~0.6之间。
LMO电池在进行EIS测试后,进行1.0 C倍率的45 ℃高温循环充放电,荷电状态为20%~80% SOC,循环充放电700次后,对LMO电池在室温下进行EIS测试。
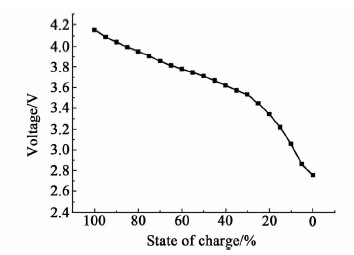
2 结果与讨论 2.1 LMO电池阻抗谱分析锂离子电池的电压是正负极电极电位的差值,因此电池电极材料的电位随着电池荷电状态变化特点决定了电池的电压随SOC变化的情况,图 1是LMO电池开路电压曲线(Open circuit voltage,OCV)。
|
| 图 1 LMO电池的开路电压曲线 Fig. 1 The OCV curve of LMO battery |
| |
从图 1中可知,LMO电池的开路电压随荷电状态呈明显的单调性变化,因为LMO电池中的正极LMO材料在锂离子嵌入/脱嵌过程中没有发生相变,所以没有明显的电压平台。
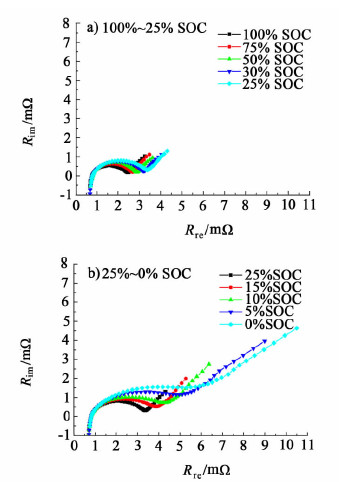
从图 1看出LMO电池的开路电压曲线从100%SOC到30%SOC左右基本保持一个斜率,而从30%SOC左右到0%SOC时电池开路电压曲线的斜率发生了变化。因此,选取100%、75%、50%、30%、25%SOC和25%、15%、10%、5%、0%SOC等2组不同SOC下的EIS谱进行对比,从EIS谱的变化与电池OCV的变化特征进行关联性分析,图 2是这两组不同SOC下的电池EIS谱图。
|
| 图 2 LMO电池的EIS谱 Fig. 2 The EIS plots of LMO battery |
| |
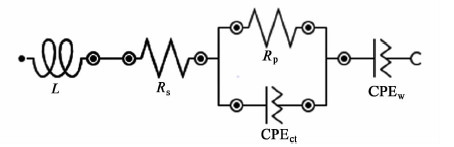
从图 2可知,以25%SOC为转折点,在不同的SOC区域,LMO电池EIS谱呈不同的变化趋势。图 2a)是100~25%SOC的LMO电池EIS谱,随着电池SOC的下降,电池EIS谱的高频半圆圆弧逐渐延长,圆弧高度略有提高,但是低频容抗部分未见明显变化;图 2b)是25%~0%SOC的LMO电池的EIS谱,随着电池的SOC从25%SOC继续下降,不仅电池高频圆弧进一步延长,且圆弧高度和低频容抗部分也明显提高。LMO电池的EIS谱的这些变化,说明随着电池SOC的变化,电池内部的欧姆阻抗、电化学阻抗等均发生了改变,为了定量分析这些变化,以图 3所示等效电路对这些EIS谱进行拟合,通过最小二乘法求解电路元件参数值。
|
| 图 3 LMO电池的等效电路 Fig. 3 The equivalent circuit of LMO battery |
| |
图 3所示等效电路中,L为电感,Rs为电池欧姆电阻,Rp为电池电化学反应电阻,CPEct和CPEw分别代表LMO电池发生电化学反应和电荷扩散阻抗的常相位角元件。通过对LMO电池的EIS谱进行等效电路拟合,得到等效电路中的各电路元件参数值,具体见图 4和图 5所示。
|
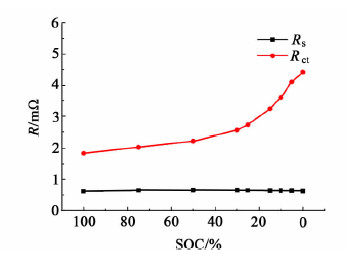
| 图 4 LMO电池的欧姆电阻和电化学电阻vs.SOC Fig. 4 Rs and Rct vs. SOC of LMO battery |
| |
|
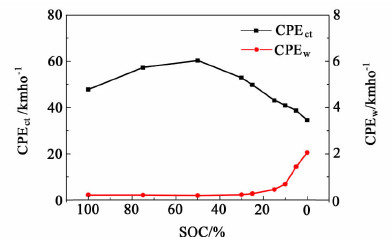
| 图 5 LMO电池的CPE参数值(1/Yo)vs. SOC Fig. 5 CPE parameter value(1/Yo) vs. SOC |
| |
图 4是等效电路中的欧姆电阻、电化学反应电阻。
从图 4中可知,LMO电池的欧姆电阻始终在1 mΩ以内,变化不大;而电化学反应电阻随着电池SOC下降逐渐变大,且在25% SOC左右呈明显上升趋势,这表明随着电池SOC降低,LMO电池内部的锂离子嵌入/脱出反应阻力变大。
图 5是代表电化学反应以及电荷扩散过程的CPE值(1/Yo)。
从图 5可知,LMO电池电化学反应的CPE值明显大于电荷扩散过程的CPE值,说明LMO电池因电化学反应引起的电容效应要弱于电荷扩散产生的电容效应;并且扩散阻抗CPE值在25%SOC以下开始逐渐提高,表明在此荷电状态以下LMO电池中的电荷在电极材料中的扩散逐渐变得困难,同时电荷扩散的电容效应也发生了弱化,因电荷扩散产生的极化现象将越来越明显。
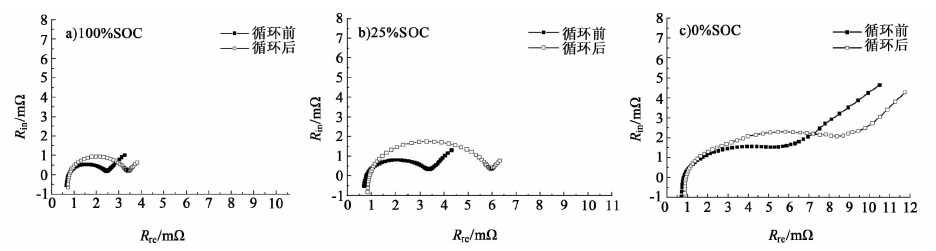
2.2 高温循环前后电池阻抗谱对比分析LMO电池在经历了高温循环测试后其容量发生了衰减,其衰减是由于电池的内特性发生了变化所导致的,即电池内部电化学体系发生了不可逆的变化,为了表征这种变化,对比了循环前后LMO电池在100%SOC、25%SOC和0%SOC等3个荷电状态的EIS谱,如图 6所示。
|
| 图 6 LMO电池循环前后的阻抗谱 Fig. 6 the EIS plots of LMO battery before and after cycle test |
| |
从图 6可知,LMO电池经历了高温循环后,EIS谱发生了显著变化,表现为高频圆弧直径明显变长,且高频圆弧的容抗也比循环前明显提高。高温循环前后LMO电池的EIS谱的变化,通过等效电路拟合求解得到的电路元件参数值可以进行定量的分析,如图 7所示。

|
| 图 7 LMO电池循环前后的电化学电阻和CPE参数值(1/Yo) vs.SOC Fig. 7 Rct and 1/Yo vs. SOC of LMO battery before and after cycle test |
| |
从图 7a)可知高温循环后,LMO电池的电化学反应电阻发生了较大幅度的提高,这说明LMO电池高温循环使得电池电极材料固液相界面的电荷转移过程发生了劣化。另外,从图 7b)可知LMO电池在高温循环后,电池电化学反应的CPE值也明显提高,且电荷扩散过程的CPE值降低。这说明高温循环弱化了因电化学反应产生的电容效应,同时加强了因电荷扩散产生的电容效应。
3 结论以储能用LMO电池为研究对象,通过建立等效电路解析了反映LMO电池中锂离子嵌入/脱出电化学反应过程、电荷扩散过程的相关参数,并对比了高温循环前后LMO电池EIS谱的变化,取得如下结论。
1)LMO电池的开路电压变化呈两个不同的区间,相应的LMO电池的EIS谱在这两个区间也存在不同的变化趋势;
2)LMO电池的电化学反应电阻大于欧姆电阻,且随着电池SOC的降低而逐渐提高,且与开路电压的变化区间相一致;LMO电池电化学反应引起的电容效应弱于电荷扩散产生的电容效应,在20%SOC以下时LMO电池扩散阻抗CPE值逐渐提高。
3)LMO电池经历高温循环测试后,电池的电化学电阻显著提高,同时因电化学反应产生的电容效应发生了弱化。
| [1] | 马华, 从长杰, 王驰伟. 储能用锂离子动力电池研究进展[J]. 化学工业与工程,2014,31 (3) : 26–33 Ma Hua, Cong Changjie, Wang Chiwei. Research progress on lithium-ion batteries for energy storage application[J]. Chemcial Industry and Engineering,2014,31 (3) : 26–33 |
| [2] | Feng X, Fang M, He X, et al. Thermal runaway features of large format prismatic lithium ion battery using extended volume accelerating rate calorimetry[J]. Journal of Power Sources,2014,255 (1) : 294–301 |
| [3] | Zhang C, Liang Y, Yao L, et al. Effect of thermal treatment on the properties of electrospun LiFePO4-carbon nanofiber composite cathode materials for lithium-ion batteries[J]. Journal of Alloys and Compounds,2015,627 (1) : 91–100 |
| [4] | Yamagiwa K, Morita D, Yabuuchi N, et al. Improved high-temperature performance and surface chemistry of graphite/LiMn2O4 Li-ion cells by fluorosilane-based electrolyte[J]. Electrochimica Acta,2015,160 (1) : 347–356 |
| [5] | Wang Y, Chen L, Wang Y, et al. Cycling stability of spinel LiMn2O4 with different particle sizes in aqueous electrolyte[J]. Electrochimica Acta,2015 : 178–183 |
| [6] | 姜倩倩, 马聪, 王兴尧, 等. 锰酸锂合成方法的研究进展[J]. 化学工业与工程,2013,30 (2) : 19–25 Jiang Qianqian, Ma Cong, Wang Xingyao, et al. Progress in synthesis of lithium manganese oxide[J]. Chemcial Industry and Engineering,2013,30 (2) : 19–25 |
| [7] | Feng L, Xu X, Shui M, et al. The potential dependent electrochemical impedance spectroscopy and lithium diffusion kinetics of LiFePO4[J]. Solid State Ionics,2014,265 (1) : 49–54 |
 2016, Vol. 33
2016, Vol. 33





