2. 天津化学化工协同创新中心, 天津 300072
2. Collaborative Innovation Center of Chemical Science and Chemical Engineering(Tianjin), Tianjin 300072, China
L-丙氨酸-L-谷胺酰胺(CAS NO. 39537-23-0)又称作丙谷二肽,是重要的氨基酸类肠外营养剂,其主要功效在于对人体条件性必需的氨基酸——谷氨酰胺的有效补充。它可替代不宜作为药品的谷氨酰胺对人体补充该种氨基酸,促进肌肉蛋白合成,改善危重病人的临床与生化指标;维持肠道功能,保持机体氮平衡;增强免疫能力,对手术病人的中性白细胞功能的正常化,对淋巴细胞、T淋巴细胞、辅助细胞的增加均具有明显促进作用。资料显示,及时补充丙谷二肽,可以显著缩短病人住院治疗和恢复的时间[1]。丙谷二肽既可以单独作为药物使用,也可以同其它氨基酸复配,开发保健品、抗疲劳药物,因此具有医疗和经济的双重意义,市场前景广阔。
|
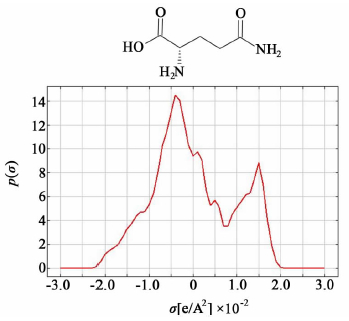
| 图 1 L-丙氨酸-L-谷胺酰胺化学结构及其σ profile图 Fig. 1 Chemical structure and σ profile of N-(2)-L-alanyl-L-glutamine |
| |
工业上的丙谷二肽合成路线比较复杂,通常反应不完全并伴有副反应发生,最后得到的粗品需要经过多次纯化才能满足医药需求[2]。结晶技术以其温和的操作条件,简单的设备,极高的分离效率以及低廉的成本被选作丙谷二肽纯化的主要手段[3, 4]。目前国内普遍采用[5]的水-乙醇溶析结晶工艺存在产品粒度小,长径比大,易聚结等问题,导致过滤及干燥时间长,溶剂残留高,堆密度小,影响其下游应用。为此需要对现有结晶工艺进行改进,选择新的更为合适的溶析剂是一种有效的方法。
化学工业常用的溶剂种类较多,完全通过实验筛选合适的溶剂会耗费大量的人力、物力和时间,使用可靠的理论模型预测混合体系的物理化学性质变得尤为重要。这种理论预测通常可分为两类,一类是对真实体系的实验热力学数据进行拟合,通过内插或外推得到热力学信息,如活度系数模型和平衡态模型[6];另一类则主要依靠化合物结构信息,而与实验数据关系不大,如基团贡献法和本研究采用的真实溶剂似导体屏蔽模型[7, 8](conductor-like screening model for real solvents,COSMO-RS)。COSMO-RS是Klamt等提出的一种有效的预测流体热力学性质的方法。该方法基于量子化学和统计热力学,能够较准确地预测溶解度、相平衡、活度系数等流体热力学性质。在本研究中,利用COSMO-RS模型可以正确地定性描述丙谷二肽在几种溶剂及混合溶剂中的溶解行为,并且发现丙谷二肽在异丙醇-水体系中对溶剂组成和温度变化最为敏感,因此异丙醇被选为溶析-冷却耦合结晶的目标溶析剂。
在实验验证预测结果的过程中,我们发现异丙醇不仅具有如预测一样的较强溶析能力,还能较好地控制产品形貌。由于到目前为止,有关丙谷二肽溶解度数据的文献非常稀少,因此本研究测定了丙谷二肽在水-异丙醇体系中的不同温度(293.15~318.15 K)和不同溶剂质量配比[m(异丙醇)/m(水)为0.5~4.0]条件下的溶解度,并从中推导出相应的溶解热力学性质,并据此开发出合适的溶析冷却耦合结晶工艺,得到高纯度的颗粒状丙谷二肽晶体颗粒,提高其商用价值。
1 实验过程实验原料丙谷二肽购自阿拉丁试剂(中国,上海),质量分数为99.5%。有机溶剂购自江天化学试剂公司(中国,天津),分析纯,使用时未进一步纯化;水为去离子水。
本研究采用重量法测定丙谷二肽在不同溶剂配比和温度下的溶解度,其中混合溶剂的质量配比分别为m(异丙醇):m(水)为0.5、1.0、1.5、2.0、2.5、3.0和4.0,温度范围则为293.15~328.15 K,每5 K 1个温度间隔。取过量的在45 ℃、1 000 Pa(绝对压力)真空干燥条件下干燥48 h的丙谷二肽粉末投入带恒温水浴夹套的100 mL反应釜中,底部配有磁力搅拌,转速300 r/min。按照质量配比精确配制所选用的7组混合溶剂,各取60 mL倒入反应釜中,顶部植入热电偶温度计读取体系温度(精确至±0.1 K),侧口有冷凝管回流,釜内为常压,水浴夹套连接CF41型控温水浴(Julabo,德国,精度±0.1 K)。开启磁力搅拌器,设定水浴温度,平衡24 h后关闭磁力搅拌,恒温静置12 h,使过量的丙谷二肽固体沉淀在反应釜底部。用带0.45 μm孔径滤膜的注射器抽取上清液5 mL转移至干燥48 h并精确测定质量的表面皿中,同一温度条件下每个反应釜连续小心地取样3次,鼓风条件下挥发表面皿中的溶剂,然后置于真空干燥箱中45 ℃减压至1 000 Pa干燥24 h,取出称质量后继续减压干燥4 h,至表面皿质量变化小于0.1%,认为残余固体不含溶剂,干燥过程结束。
实验过程中所有的称量操作使用电子分析天平AB204-S(Mettler Toledo,瑞士),精确度±0.1 mg。
式(1)定义了摩尔溶解度(x1):
| $${x_1} = \frac{{{m_1}/{M_1}}}{{\sum\limits_{i = 1}^n {{m_i}/{M_i}} }}$$ | (1) |
其中n=3,m1和 M1分别代表所取清液中溶质丙谷二肽的质量和摩尔质量,m2和 M2分别代表溶剂异丙醇的质量和摩尔质量;m3和M3则分别代表了溶剂水的质量和摩尔质量。
溶解度测试实验中取样后的固-液混合物利用布氏漏斗减压过滤,滤渣在35 ℃下减压至1 000 Pa干燥8 h后进行XRD分析。
XRD分析采用日本理学Rigaku D/max-2500 X射线衍射仪(Rigaku,日本),射线源为Cu_Kα(0.071073 nm),扫描范围为2°到50°,扫描速率为0.067(°)/s。
DSC分析采用DSC 1/500型差示扫描量热仪(梅特勒-托利多,瑞士)进行,使用压盖标准铝坩埚(顶部扎孔),样品质量3~4 mg,保护气为氮气(流速2.5 mL/s)。测试温度范围298.15~523.15 K,升温速率5 K/min。
2 COSMO-RS模型Klamt提出的COSMO-RS是一个普遍用于预测液体热力学平衡性质的理论[7, 8, 9]。COSMO模型的基础是一个溶质分子的“溶剂可及表面”,分子在有限介电溶剂中的表面电荷分布被近似为在1个导体中的表面电荷分布。COSMO-RS热力学方法以溶质和溶剂分子的表面屏蔽电荷密度为基础计算分子表面片段之间的相互作用,并以此定量它们之间的极性和氢键相互作用能。分子表面屏蔽电荷密度分布,即σ profile,是COSMO模型的重要概念,也是热力学性质计算的基础。通过溶剂和溶质分子的σ profile可以计算分子间相互作用能,再通过统计热力学方法可推导出溶剂和溶质分子各自在溶液中的化学势,由此计算出活度系数,并进一步求出溶解度及过量焓等热力学性质。
应用COSMO-RS方法计算真实混合物溶液行为的总体来说分两部分工作:首先,通过DFT计算,可得到相应的*.cosmo文件;然后通过相关软件产生σ-profile,并将其用于热力学性质的计算。应用COSMO-RS的详细步骤和方程以及所使用参数可参见参考文献[7, 8]。
3 溶解度模型随着广大科研工作者对结晶过程以及溶解度数据的深入研究,很多热力学模型例如ABC模型(modified Apelblat modle),λh模型以及范特霍夫(van’t Hoff)方程被提出并运用于溶解度数据的拟合及预测,极大地扩展了离散溶解度数据的运用和预测未知溶剂中溶解度[6]。其中溶解的热力学性质(吉布斯自由能、溶解焓和熵)可以通过范特霍夫方程计算出来。
本研究中测得的丙谷二肽的溶解度数据使用modified Apelblat 方程,λh 方程,van’t Hoff方程以及(NIBS)/Redlich-Kister model拟合二元混合溶剂体系。
3.1 Van’t Hoff方程考虑到溶剂的影响,van’t Hoff方程描述了真实溶液中摩尔溶解度与温度之间的关系,如式(2)。
| $$\ln {x_1} = - \frac{{\Delta {H_{\rm{d}}}}}{{RT}} + \frac{{\Delta {S_{\rm{d}}}}}{R}$$ | (2) |
其中 x1是溶质的摩尔溶解度,T是溶液的绝对温度; ΔHd和ΔSd分别是溶解焓和熵,R是气体常数。
3.2 Modified Apelblat 方程Modified Apelblat 方程是常用的拟合摩尔溶解度x1与溶液绝对温度T的经验方程:
| $$\ln {x_1} = A + \frac{B}{T} + C\ln T$$ | (3) |
其中A, B, C是实验常数,A和B的值代表溶液活度系数的变化,而C的值则反映了温度对熔化焓的影响。
3.3 λh方程λh方程能够使用2个参数来拟合大多数固液相平衡系统,其表达式如下:
| $$\ln \left( {1 + \lambda \frac{{1 - {x_1}}}{{{x_1}}}} \right) = \lambda h\left( {\frac{1}{T} - \frac{1}{{{T_{\rm{m}}}}}} \right)$$ | (4) |
其中x1是摩尔溶解度,T和Tm分别是实验温度和正常的熔点,λ和h是两个由溶解度数据决定的可调参数。参数λ被当做是反映溶液系统的非理想性的平均联系数,而h代表着溶液的焓,这两个参数可以通过实验数据回归得到。
3.4 (NIBS)/Redlich-Kister 模型近似理想二元溶剂(Nearly Ideal Binary Solvent)(NIBS)/Redlich-Kister 模型表达式为:
| $$\ln {x_1} = {x_{\rm{B}}}\ln {X_{\rm{B}}} + {x_{\rm{C}}}\ln {X_{\rm{C}}} + {x_{\rm{B}}}{x_{\rm{C}}}\sum\limits_{i = 1}^n {{s_i}{{\left( {{x_{\rm{C}}} - {x_{\rm{B}}}} \right)}^i}} $$ | (5) |
其中xB和xC指的是未加溶质时二元混合溶剂的初始摩尔分率。XB和XC分别代表溶质在两种纯溶剂的饱和溶液中的摩尔分率,对于二元溶剂系统,方程可变形为:
| $$\ln {x_1} = {B_0} + {B_1}{x_2} + {B_2}x_2^2 + {B_3}x_2^3 + {B_4}x_2^4$$ | (6) |
其中B0,B1,B2,B3和B4,是由最小二乘法分析实验数据得到模型参数,x1是溶质在混合溶液中的摩尔分率,x2是异丙醇在混合溶液中的摩尔分率。此外B0,B1,B2,B3和B4的值还与温度T存在如式(7)的全局关系,可以依此计算出任意温度和溶剂组成条件下的溶解度。
| $$B = e + fT$$ | (7) |
其中B指的是方程(6)中的B0,B1,B2,B3,B4,而T是绝对温度;e和f都是经验参数。由此得到的全局丙谷二肽在水-异丙醇体系下溶解度表达式如式(8)。
| $$\begin{array}{c} \ln \left( {{x_1}} \right) = {e_0} + {e_1}{x_2} + {e_2}x_2^2 + {e_3}x_2^3 + {e_4}x_2^4 + \\ \left( {{f_0} + {f_1}{x_2} + {f_2}x_2^2 + {f_3}x_2^3 + {f_4}x_2^4} \right)T \end{array}$$ | (8) |
文献中已有许多关于实测的溶液热力学数据和COSMO-RS计算的预测值对比的论文,有些体系的预测结果与实验值吻合较好[10],而对有些体系只是半定量或定性吻合[11]。这是由于在对后一类体系的COSMO-RS计算中,所涉及物质的固-液相转变自由能没有实验数据作为参考值,只能从该物质的*.cosmo文件通过QSPR方法进行估算,导致对该体系的预测结果不够准确。因此,预测时输入溶质的熔点和熔融焓或者给定条件下的溶解度值等实验数据做为固-液相转变自由能的计算依据可以提高精度[12]。通过DSC测试发现丙谷二肽在215.5 ℃分解,在此将分解温度视为熔融温度,并使用ICAS软件[13, 14]估算其熔融焓为38.17 kJ/mol。
出于对药物生产的安全性及与水相溶性的考虑,水、乙醇、正丙醇和异丙醇被当作候选溶剂。丙谷二肽及相应溶剂的cosmo文件利用Materials Studio软件(Accelrys,美国)中的DMOL3模块通过DFT计算产生[15]。对分子结构优化的过程中使用GGA/BPE函数,DNP基组的设置。精度为“fine”,其余使用默认设置。所得cosmo文件输入COSMOthermX (C30_13.01)软件[16]即可进行热力学性质计算。本研究计算了293.15~318.15 K温度范围内丙谷二肽在渐变的水-醇质量比下的溶解度,结果见表 1。
| T/K | xexp | xcal | |||
| Apelblat | λh | van't Hoff | COSMO-RS | ||
| m(propanol-2-ol):m(water)=0.5 | |||||
| 293.15 | 2.86E-02 | 2.83E-02 | 3.09E-02 | 3.09E-02 | 6.94E-02 |
| 298.15 | 3.42E-02 | 3.48E-02 | 3.49E-02 | 3.50E-02 | 7.33E-02 |
| 303.15 | 4.17E-02 | 4.10E-02 | 3.94E-02 | 3.94E-02 | 7.75E-02 |
| 308.15 | 4.60E-02 | 4.63E-02 | 4.42E-02 | 4.42E-02 | 8.21E-02 |
| 313.15 | 5.05E-02 | 5.03E-02 | 4.94E-02 | 4.94E-02 | 8.71E-02 |
| 318.15 | 5.28E-02 | 5.28E-02 | 5.51E-02 | 5.51E-02 | 9.24E-02 |
| m(propanol-2-ol):m(water)=1.0 | |||||
| 293.15 | 5.21E-03 | 5.35E-03 | 5.65E-03 | 5.64E-03 | 2.81E-02 |
| 298.15 | 6.55E-03 | 6.20E-03 | 6.19E-03 | 6.19E-03 | 3.04E-02 |
| 303.15 | 6.76E-03 | 6.98E-03 | 6.77E-03 | 6.78E-03 | 3.28E-02 |
| 308.15 | 7.54E-03 | 7.65E-03 | 7.39E-03 | 7.41E-03 | 3.54E-02 |
| 313.15 | 8.33E-03 | 8.16E-03 | 8.06E-03 | 8.07E-03 | 3.82E-02 |
| 318.15 | 8.45E-03 | 8.50E-03 | 8.78E-03 | 8.76E-03 | 4.13E-02 |
| m(propanol-2-ol):m(water)=1.5 | |||||
| 293.15 | 4.59E-03 | 4.59E-03 | 4.23E-03 | 4.63E-03 | 1.56E-02 |
| 298.15 | 4.72E-03 | 4.72E-03 | 4.46E-03 | 4.72E-03 | 1.71E-02 |
| 303.15 | 4.85E-03 | 4.84E-03 | 4.70E-03 | 4.81E-03 | 1.87E-02 |
| 308.15 | 4.92E-03 | 4.92E-03 | 4.96E-03 | 4.90E-03 | 2.04E-02 |
| 313.15 | 4.98E-03 | 4.99E-03 | 5.23E-03 | 4.99E-03 | 2.23E-02 |
| 318.15 | 5.05E-03 | 5.04E-03 | 5.52E-03 | 5.07E-03 | 2.43E-02 |
| m(propanol-2-ol):m(water)=2.0 | |||||
| 293.15 | 2.23E-03 | 2.32E-03 | 2.00E-03 | 2.40E-03 | 1.01E-02 |
| 298.15 | 2.77E-03 | 2.62E-03 | 2.85E-03 | 2.98E-03 | 1.11E-02 |
| 303.15 | 2.89E-03 | 2.88E-03 | 2.65E-03 | 3.17E-03 | 1.23E-02 |
| 308.15 | 2.99E-03 | 3.07E-03 | 2.96E-03 | 3.27E-03 | 1.35E-02 |
| 313.15 | 3.15E-03 | 3.18E-03 | 3.17E-03 | 3.34E-03 | 1.49E-02 |
| 318.15 | 3.26E-03 | 3.22E-03 | 3.37E-03 | 3.55E-03 | 1.63E-02 |
| m(propanol-2-ol):m(water)=3.0 | |||||
| 293.15 | 1.29E-03 | 1.29E-03 | 2.00E-03 | 1.40E-03 | 6.51E-03 |
| 298.15 | 1.34E-03 | 1.34E-03 | 1.63E-03 | 1.52E-03 | 7.31E-03 |
| 303.15 | 1.41E-03 | 1.41E-03 | 1.75E-03 | 1.60E-03 | 8.18E-03 |
| 308.15 | 1.49E-03 | 1.49E-03 | 1.90E-03 | 1.61E-03 | 9.14E-03 |
| 313.15 | 1.59E-03 | 1.58E-03 | 2.07E-03 | 1.76E-03 | 1.02E-02 |
| 318.15 | 1.68E-03 | 1.68E-03 | 2.27E-03 | 1.86E-03 | 1.13E-02 |
| m(propanol-2-ol):m(water)=4.0 | |||||
| 293.15 | 1.91E-04 | 2.15E-04 | 2.00E-04 | 2.00E-04 | 5.94E-03 |
| 298.15 | 3.01E-04 | 2.67E-04 | 3.58E-04 | 3.33E-04 | 6.64E-03 |
| 303.15 | 3.11E-04 | 3.08E-04 | 3.09E-04 | 3.46E-04 | 7.40E-03 |
| 308.15 | 3.14E-04 | 3.30E-04 | 3.41E-04 | 3.49E-04 | 8.22E-03 |
| 313.15 | 3.20E-04 | 3.30E-04 | 3.44E-04 | 3.58E-04 | 9.13E-03 |
| 318.15 | 3.30E-04 | 3.09E-04 | 3.29E-04 | 3.73E-04 | 1.01E-02 |
计算显示丙谷二肽在考察温度范围内的纯水中易溶,在考察的醇类中难溶。溶解度顺序为水>>乙醇>正丙醇>异丙醇;相对于温度因素,丙谷二肽对溶剂质量比更敏感;在相同的溶剂质量比的条件下,异丙醇与水混合溶剂的溶解度对温度最敏感,因此异丙醇被选为溶析-冷却耦合结晶的候选溶剂。
为了研究温度和溶剂组成对丙谷二肽溶解度的影响,本研究测定了293.15~318.15 K温度范围内混合溶剂质量组成为m(异丙醇)/m(水)=0.5~4.0范围内丙谷二肽在体系内的平均溶解度数据。每个条件下取3次样,得到的结果取平均值为该条件下的溶解度,列于表 1,其中xexp为实验测得的平均溶解度,xcal为热力学模型计算值。
通过XRD检测溶解度测试中固-液平衡后的固相,没有发现丙谷二肽出现多晶型或溶剂化的现象。
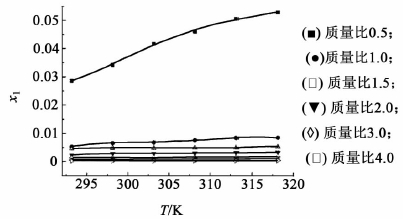
溶解度实验数据列于表 1,以温度为横坐标,摩尔分数溶解度为纵坐标,分别对m(异丙醇)/m(水)为0.5,1.0,1.5,2.0,3.0和4.0等7种不同溶剂组成的溶解度曲线绘图,见图 2。
|
| 图 2 L-丙氨酸-L-谷胺酰胺在不同异丙醇与水质量配比的混合溶剂中的摩尔分率溶解度曲线图 Fig. 2 Solubility data of N-(2)-L-alanyl-L-glutamine in isopropanol-water solvents of different mass fraction |
| |
从图 2中可明显看出来随着混合溶剂中的溶析剂异丙醇的含量增大,丙谷二肽在其中的溶解度降低。以293.15 K条件下为例,溶剂质量配比为0.5:1的溶解度是配比为1:1条件下的5.488倍,是质量配比为4:1条件下的149.686倍。可知对于丙谷二肽水溶液体系来说,异丙醇为可靠高效的溶析剂,其产率可以达到99%以上。随着温度的升高,丙谷二肽在混合溶剂中的溶解度增大。例如配比为0.5条件下,318.15 K条件下丙谷二肽的溶解度是293.15 K条件下的1.845倍,而在质量配比为4.0的溶剂组成下,同样的温度溶解度差异1.728倍。证明冷却结晶也是一种可选的结晶方式,但是在不改变溶剂组成的条件下单独降温,其产率低于50%。
为了扩展溶解度数据的应用范围和定量地描述固液平衡,使用热力学模型对实验溶解度数据进行拟合,包括modified Apelblat方程,λh方程,van’t Hoff方程对实验溶解度数据分别进行拟合,并使用(NIBS)/Redlich-Kister模型针对二元混合溶剂体系进行全局分析。通过拟合溶解度数据使得目标函数f=(xcal-xexp)/xexp最小化得到模型参数模型参数列于表 2,拟合误差REMS列于表 3。
| 模型 | 参数 | m(异丙醇)/m(水) | |||||
| 0.5 | 1.0 | 1.5 | 2.0 | 3.0 | 4.0 | ||
| modified Apelblat | A | 897.00 | 601.00 | 967.00 | 641.00 | -167.70 | 1722.00 |
| B | -42 872.00 | -28 984.00 | -49 330.00 | -30 430.00 | 6 463.90 | -79 719.00 | |
| C | -133.00 | -89.00 | -150.00 | -96.00 | 24.50 | -257.00 | |
| λh | λ | 0.50 | 0.02 | 0.02 | 0.02 | 0.01 | 0.01 |
| h | 4 051.50 | 45 243 | 134 860 | 131 870 | 131 460 | 123 850 | |
| m(异丙醇)/m(水) | modified Apelblat | λh | Van’t Hoff |
| 0.5 | 1.07E-06 | 2.12E-05 | 2.06E-05 |
| 1.0 | 2.31E-07 | 5.29E-07 | 4.96E-07 |
| 1.5 | 5.18E-10 | 5.06E-07 | 4.06E-09 |
| 2.0 | 3.83E-08 | 1.43E-07 | 8.83E-08 |
| 3.0 | 1.31E-10 | 1.39E-07 | 9.85E-10 |
| 4.0 | 2.16E-09 | 3.49E-08 | 5.85E-09 |
使用得到的拟合模型参数即可计算出实验温度范围内任意温度点的溶解度数据,对比实验值和拟合值可知modified Apelblat方程拟合效果较好,λh和van’t Hoff方程的精度也能接受。而在298.15 K条件下的溶解焓,溶解熵及自由能可以由Vant Hoff方程计算得到。由计算结果可知丙谷二肽在水-异丙醇体系的溶解为吸热且非自发过程;在定温条件下随着溶析剂的加入,溶解度下降而自由能增加。
| m(异丙醇)/m(水) | ΔHd/(J·mol-1) | ΔSd/(J·mol-1·K-1) | ΔGd/(J·mol-1) |
| 0.5 | 17 900.0 | 32.0 | 8 519.2 |
| 1.0 | 13 674.0 | 4.0 | 12 501.4 |
| 1.5 | 12 878.8 | -14.9 | 14 653.6 |
| 2.0 | 9 670.0 | -17.0 | 16 243.8 |
| 3.0 | 8 475.3 | -26.5 | 17 246.7 |
| 4.0 | 10 141.0 | -34.0 | 20 108.1 |
为了进一步扩展丙谷二肽在异丙醇和水的二元混合溶剂的溶解度数据,使用(NIBS)/Redlich-Kister 模型拟合,得到模型参数即可计算出实验温度范围内任意温度任意组成下的溶解度数据。
结果如式(9),其中拟合误差R2 =0.9953,拟合精度优于modified Apelblat方程(R2=0.9901),由模型系数可知溶剂组成x2对溶解度x1的影响要远远大于温度T的影响。
| $$\begin{array}{l} \ln \left( {{x_1}} \right) = 2.7 - 227.2{x_2} + 1254.4x_2^2 - 2605.8x_2^3 + \\ 1785.7x_2^4 + \left( {0.6{x_2} - 3.7x_2^2 + 8.43x_2^3 - 6.2x_2^4} \right)T \end{array}$$ | (9) |
通过对丙谷二肽在异丙醇/水混合体系下溶解度数据的研究,我们得知在溶析结晶的初始阶段丙谷二肽在水中的溶解度较大,少量加入溶析剂异丙醇即可显著地降低其溶解度,因此初浓度不能过大,而且溶析剂滴加速率也不能太快,否者容易爆发成核导致晶体颗粒变小,容易发生聚结,产品溶媒残留增加。在这个思路下进行了定温条件下(298.15和318.15 K)的溶析结晶工艺实验。丙谷二肽初始浓度为10%(水质量分数,下同),异丙醇滴加速率为0.5%/min(以结晶器中水的质量为基础,即溶析剂相对于水的质量分数,下同),终点同时停止滴加异丙醇,养晶40 min 后直接过滤,工艺总时间4 h,收率分别为99.42% 和99.01%。得到的产品偏光显微镜照片分别如图 3a)和3b)(200倍,图 3~图 5中右下角标尺长度均为1 mm)。

|
| 图 3 丙谷二肽溶析结晶200倍偏光显微镜照片 Fig. 3 Polarizing microscope photo of N-(2)-L-alanyl-L-glutamine crystallization from isopropanol-water system(scale of 200 times) |
| |

|
| 图 4 298.15 K下丙谷二肽产品显微镜照片 Fig. 4 Polarizing microscope photo of N-(2)-L-alanyl-L-glutamine by fast anti-solvent crystallization from isopropanol-water system at 298.15 K |
| |

|
| 图 5 不同降温速率下丙谷二肽溶析结晶照片 Fig. 5 Polarizing microscope photo of N-(2)-L-alanyl-L-glutamine crystallization at the cooling rate |
| |
由图 3可知相同初始浓度和异丙醇滴加速率下低温条件下溶析结晶得到的产品尺寸更大。因为低温下溶解度小,随着溶析剂的加入,过饱和度变大推动晶体快速生长。
实施了298.15 K条件下2.0%/min滴加溶析剂的实验,终点养晶40 min后直接过滤,工艺时间1.5 h,收率99.38%,产品显微镜照片如图 4a)。
由图 4可知在较快的滴加速率下容易爆发成核导致晶体聚结,不利于单个晶体长大。
基于以上结果设计冷却结晶工艺,即在相同的初始浓度(10%)和溶剂配比(1.0:1.0)下滴加溶析剂异丙醇至饱和后,以不同的冷却速率(1.0 K/min,0.1 K/min)降温得到丙谷二肽晶体,从318.15 K降温至298.15 K,达到降温终点养晶时间40 min,工艺时间分别为1.5和4.5 h,收率分别为42.12%和42.14%,产品的200倍偏光显微镜照片分别如图 5a)和图 5b)。
由图 5可知,慢速降温有利于晶体长大,但是耗费工艺时间较长,对于工业生产是不利的。而且单纯的溶析结晶得到的产品长径比较大,约为12,增大过滤阻力;冷却结晶得到的产品长径比约为8,但是收率较低,仅为42.1%。综合考虑将2种方式结合起来,即在较低的初始浓度下(10%)于高温下(318.15 K)滴加溶析剂异丙醇使溶液接近饱和,然后中速冷却(0.5 K/min)至过饱和自发成核,至298.15 K继续滴加溶析剂增大过饱和度使小晶体长大,得到长径比8.2,产率99.2%并且生产周期3 h经济的最适宜工艺,得到的产品照片如图 5b)。
6 结论利用COSMO-RS模型计算不同温度、不同质量比的水-醇体系中丙谷二肽的溶解度,发现丙谷二肽在水-异丙醇体系中对溶剂组成和结晶温度等参数的敏感性优于工业常用的水-乙醇体系。通过实验验证,发现COSMO-RS预测结果与实验溶解度数据在数值上存在一定的误差;但是异丙醇确实如同预测一样是一种有效的溶剂,并且溶解度随温度及配比的变化趋势的预测也与实验结果一致。这一结果说明COSMO-RS计算是进行结晶体系溶剂筛选的有效辅助工具。
通过实验测定丙谷二肽在水-异丙醇体系中不同温度不同质量比下的溶解度数据,并在此基础上推算出298 K下丙谷二肽在水-异丙醇体系中的溶解焓、熵和自由能数值。分别使用热力学模型modified Apelblat方程,λh方程,van’t Hoff方程以及(NIBS)/Redlich-Kister模型拟合溶解度数据,得到丙谷二肽在该溶剂体系中的模型参数。其中使用NIBS模型可以较为精确地计算出在试验范围内任意温度和组成条件下的溶解度数据,指导工艺生产。计算表达式如式(9)。
通过实验分析溶析温度、降温速率、溶析剂滴加速率以及耦合方式对产品粒度和形貌的影响,开发了产品形态改善,产率较高并且生产周期经济的溶析-冷却耦合结晶工艺。
| [1] | 胡芹, 张川莉, 何茜. 力肤在造血干细胞移植中的应用及护理观察[J]. 职业卫生与病伤,2004,19 (4) : 283–286 Hu Qin, Zhang Chuanli, He Qian, et al. Observation of N(2)-L-alanyl-L-glutamine in hematopoietic stem cell transplantation and nursing[J]. Occupational Health and Damage,2004,19 (4) : 283–286 |
| [2] | 陈再新, 夏正君, 蒋龙. N (2)-L-丙氨酰-L-谷氨酰胺的合成工艺研究[J]. 精细与专用化学品,2010,7 (7) : 33–36 Chen Zaixin, Xia Zhengjun, Jiang Long, et al. Research of synthesis of N(2)-L-alanyl-L-glutamine[J]. Fine and Specialty Chemicals,2010,7 (7) : 33–36 |
| [3] | Mullin J W. Crystallization[M]. US: A Butterworth-Heinemann Title, 2001 . |
| [4] | 鲍颖, 王永莉, 王静康. 溶析结晶研究进展[J]. 化学工业与工程,2004,21 (6) : 438–443 Bao Ying, Wang Yongli, Wang Jingkang. Progress in dilution crystallization[J]. Chemical Industry and Engineering,2004,21 (6) : 438–443 |
| [5] | Wang G, Wang Y, Zhang J, et al. Modeling and simulation of thermodynamic properties of N-(2)-L-alanyl-L-glutamine in different solvents[J]. Ind Eng Chem Res,2014 : 3 385-3 392 |
| [6] | Prausnitz J M, Lichtenthaler R M, de Azevedo E G. Molecular thermodynamics of fluid-phase equilibria[M]. US: Prentice Hall, Upper Saddle River, . |
| [7] | Eckert F, Klamt A. Fast solvent screening via quantum chemistry:COSMO-RS approach[J]. AIChE Journal,2002,48 (2) : 369–385 |
| [8] | Klamt A. COSMO-RS, from quantum chemistry to fluid phase thermodynamics and drug design[M]. Amsterdam: Elsevier B V, 2005 . |
| [9] | Mo T, Gmehling J. Solvent-Like conductor shielded real model(COSMO-RS)[J]. Progress in Chemistry,2008,20 (10) : 1 487-1 494 |
| [10] | Klamt A, Frank E, Diedenhofen M. Prediction or partition coefficients and activity coefficients of two branched compounds using COSMOtherm[J]. Fluid Phase Equilibria,2009 : 15–18 |
| [11] | Zilnik L F, Jazbinsek A, Hvala A, et al. Solubility of sodium diclofenac in different solvents[J]. Fluid Phase Equilibria,2007 : 140–145 |
| [12] | COSMOThermX User Guide:Version C30_1301[M]. Germany:COSMOlogic GmbH & Co. KG, Leverkusen, 2012 |
| [13] |
Gani R.
|
| [14] | Sun Y, Li Z, Xie C, et al. Measurement and correlation of the solid-liquid equilibrium of 6-tert-buty-3-methylphenol and 2-tert-buty-4-methylphenol binary system[J]. Frontiers of Chemical Science and Engineering,2013,7 (1) : 110–115 |
| [15] | Eric M, Richard O, Liu Y, et al. Sigma-Profile database for using COSMO-based thermodynamic methods[J]. Ind Eng Chem Res,2006 : 4 389-4 415 |
| [16] | COSMOthermX Program, Release C3.0, Revision 13.01[M]. COSMOlogic GmbH &Co KG, Leverkusen, Germany, 2013 |
 2016, Vol. 33
2016, Vol. 33





