随着全球人口数量的增长和经济的快速发展,化石能源的消耗量迅速增加,从而造成了严重的环境问题。寻找一种可再生的清洁能源来替代石化能源已经成为了世界各国关注的一大焦点。
生物质是重要的可再生能源,而生物柴油是近期备受关注的一种生物质能。由植物油或动物油等为原料通过酯交换而制成的长链脂肪酸甲酯或乙酯称为第一代生物柴油[1]。与传统的石化能源相比,其硫及芳烃含量低、闪点高、十六烷值高、具有良好的润滑性,可部分添加到石化柴油中。然而,第一代生物柴油具有含氧量高、热稳定性差、pH值高及热值低等缺点。针对第一代生物柴油所存在的问题,人们开发了第二代生物柴油,即由动植物油脂经过脱氧得到的柴油类烃[2]。
动植物油中氧的脱除主要通过加氢脱羰、加氢脱羧和加氢脱氧三种路径[3]。加氢脱氧所采用的催化剂包括贵金属、硫化物、过渡金属磷化物、氮化物及碳化物等[4, 5, 6]。贵金属催化剂是很有效的加氢脱氧催化剂,但因其储量有限、价格昂贵,不适合大规模的工业应用;硫化物催化剂具有良好的加氢脱氧催化性能,但是在使用过程中硫容易流失,且易积碳失活,这些缺点都影响其工业应用。近年来,人们发现Ni2P催化剂在动植物油加氢脱氧反应中表现出了优异的性能[7, 8, 9, 10]。
目前,Ni2P催化剂的制备方法有多种,包括热溶剂法、程序升温还原法和次磷酸盐热分解法等[11]。与用磷酸盐、亚磷酸盐为磷源相比,次磷酸盐在较低温度下会发生热分解释放出磷化氢并与Ni反应生成Ni2P,而较低的还原温度有望实现原位制备催化剂。本研究以次磷酸为磷源制备了Ni2P/SiO2催化剂,以月桂酸甲酯作为模型化合物,研究了还原温度对催化剂结构及其对月桂酸甲酯加氢脱氧反应性能的影响,并与以磷酸盐为磷源制备的Ni2P/SiO2催化剂进行了比较。
1 实验部分 1.1 催化剂的制备 1.1.1 催化剂前驱体的制备将Ni(NO3)2·6H2O分别和NH4H2PO4、H3PO2配制成水溶液,其中磷镍元素物质的量之比为2∶1。将配好的溶液等体积浸渍在SiO2载体上,常温静置晾干后,将NH4H2PO4与Ni(NO3)2的水溶液浸渍的样品在120 ℃干燥12 h,再由10 ℃·min-1升至500 ℃焙烧4 h,得到以NH4H2PO4作为磷源的催化剂前驱体(标记为I)。H3PO2与Ni(NO3)2的水溶液浸渍的样品在40 ℃的空气中干燥4 h后继续升温至70 ℃干燥4 h,得到以H3PO2作为磷源的催化剂前驱体(标记为Ⅱ)。
1.1.2 Ni2P/SiO2催化剂的制备将1 g催化剂前驱体装入石英管反应器,在H2(200 mL·min-1)中进行程序升温还原,由室温以2 ℃·min-1的升温速率升至一定的还原温度(T)后恒温3 h,然后降至室温,用体积分数为0.5%的O2/N2(320 mL·h-1)钝化4 h。由前驱体Ⅰ和Ⅱ制备的催化剂分别标记为Ⅰ-T和Ⅱ-T,其中T表示还原温度(℃)。
1.2 催化剂的表征 1.2.1 H2程序升温还原在自制的装置中进行,在内径4 mm的U型石英管中加入150 mg催化剂前驱体,在体积分数为10%的H2/N2(60 mL·min-1)中由30 ℃升温至850 ℃,升温速率为2 ℃·min-1,气体产物由HIDEN HPR20质谱仪在线检测。
1.2.2 X-射线衍射表征(XRD)催化剂的XRD测试采用D8 Focus 型多晶粉末衍射仪,Cu_Kα(λ=0.15406 nm)作为辐射源,管电压40 kV,管电流40 mA,扫描范围10°~90°,扫描速度8(°)·min-1。
1.2.3 CO化学吸附采用改装102色谱仪进行测试。将100 mg钝化Ni2P/SiO2催化剂样品装入U型石英管反应器中,用H2(流量为60 mL·min-1)在450 ℃下还原1 h,再用He(流量为80 mL·min-1)吹扫1 h,并在He气氛中降至30 ℃恒温。待色谱的基线稳定后,采用CO脉冲进样(50 μL/次)至吸附饱和。CO信号通过热导池检测器检测。
1.2.4 NH3程序升温脱附(NH3-TPD)采用改装102色谱仪进行测试。将60 mg钝化Ni2P/SiO2催化剂样品装入U型石英管反应器中,用H2(流量为60 mL·min-1)在450 ℃下还原1 h,降温至100 ℃后吸附NH3 30 min,再用He(流量为60 mL/min)在100 ℃下吹扫,直至色谱的基线稳定。采用程序升温脱附NH3,升温速率为15 ℃·min-1,反应器尾气经NaOH干燥后进入热导池检测器(TCD)检测。
1.2.5 H2-程序升温脱附(H2-TPD)采用改装102色谱仪进行测试。将100 mg钝化Ni2P/SiO2催化剂样品装入U型石英管反应器中,用H2(流量为60 mL·min-1)在450 ℃下还原1 h,降温至30 ℃后吸附H2 30 min,再用N2(流量为60 mL·min-1)在30 ℃下吹扫,直至色谱基线稳定。采用程序升温脱附H2,升温速率为15 ℃·min-1,反应器尾气经NaOH干燥后进入热导池检测器(TCD)检测。
1.3 催化剂的活性评价采用内径为12 mm的不锈钢管固定床反应器进行反应。将与石英砂均匀混合的钝化Ni2P/SiO2催化剂样品装入反应器,样品上下分别装填2 g和1 g石英砂。在H2(100 mL·min-1)中首先以10 ℃·min-1的升温速率升至450 ℃进行预还原60 min,然后降至300 ℃,H2压力升至3.0 MPa,向反应器中通入月桂酸甲酯(质量空速为14 h-1)进行反应,H2与月桂酸甲酯物质的量之比为25。在300 ℃反应3 h后升温至320和340 ℃,在各温度反应时间均为3 h。液相产物采用装有HP-5毛细管柱(30 m×0.32 mm×0.5 μm)的SP-3420型气相色谱仪进行分析,以四氢萘为内标进行定量。
2 结果及讨论 2.1 H2-TPR结果图 1为两种催化剂前驱体在H2-TPR过程中气相产物的在线质谱图。由H2-TPR过程中所生成的气体组成变化情况可以推测还原反应的历程。随着温度的升高,前驱体I在480 ℃产生PH3,同时也伴随水的生成,此时磷酸根开始还原,生成的PH3与Ni反应生成Ni2P[12][总反应式如式(1)]。前驱体Ⅱ在230 ℃就开始产生PH3,是次磷酸根发生歧化反应生成PH3、P和磷酸根的缘故[13, 14],PH3会与Ni反应生成磷化镍;随着温度升到450 ℃,磷酸根进一步发生还原反应生成PH3,同时有水的生成,生成的PH3继续与Ni反应生成Ni2P[总反应式如式(2)]。很明显,与前驱体Ⅰ相比,前驱体Ⅱ开始生成PH3的温度明显较低,这有利于在较低温度条件下制备Ni2P。

|
| 图 1 前驱体Ⅰ和Ⅱ在H2-TPR过程中气相产物的在线质谱图 Fig. 1 Online mass spectrogram of the gas phase products of precursor Ⅰ and precursor Ⅱ in the process of H2-TPR |
| |
前驱体Ⅰ和前驱体Ⅱ还原反应的反应式为:
| $${\rm{N}}{{\rm{i}}_3}{\left( {{\rm{P}}{{\rm{O}}_4}} \right)_2} + {{\rm{H}}_2} \to {\rm{N}}{{\rm{i}}_{\rm{2}}}{\rm{P + P}}{{\rm{H}}_{\rm{3}}}{\rm{ + P + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}$$ | (1) |
| $${\rm{N}}{{\rm{i}}_{\rm{2}}}{\rm{P + P}}{{\rm{H}}_{\rm{3}}}{\rm{ + P + }}{{\rm{N}}_{\rm{2}}}{\rm{O + NO + }}{{\rm{H}}_{\rm{2}}}{\rm{O}}$$ | (2) |
图 2为两种催化剂前驱体在不同还原温度得到的催化剂的XRD谱图。图 2中14°~32°之间比较宽的衍射峰归属于无定型的SiO2载体。2θ=40.8°、44.6°、47.3°及54.3°处的衍射峰归属于Ni2P物相。较低还原温度制备的Ⅱ-450和Ⅱ-500的XRD谱图中Ni2P 衍射峰较弱;随还原温度提高,Ⅱ-550和Ⅱ-600的XRD谱图中Ni2P衍射峰逐渐明显。表 1给出了由谢乐公式计算的各Ⅱ-T催化剂中Ni2P的晶粒尺寸。由于Ⅱ-450和Ⅱ-500样品的Ni2P衍射峰较弱,无法由谢乐公式计算其中Ni2P晶粒尺寸。在较低还原温度下,前驱体Ⅱ主要是由发生歧化反应,PH3与Ni反应生成Ni2P量比较少,还有歧化得到的磷酸根没有发生还原留在催化剂表面。随着还原温度的升高,磷酸根开始发生还原生成PH3并与Ni反应,Ni2P的生产量增多、晶粒长大且晶型逐渐完整。Ⅰ-600的Ni2P晶粒尺寸小于Ⅱ-600,这是由于对于前驱体Ⅰ而言600 ℃的还原温度较低,磷酸根没有完全被还原,得到的Ni2P量较少。

|
| 图 2 不同催化剂的XRD图 Fig. 2 XRD patterns of different catalysts |
| |
| 催化剂 | Ⅱ-450 | Ⅱ-500 | Ⅱ-550 | Ⅱ-600 | Ⅰ-600 |
| Ni2P晶粒尺寸/nm | 4.3 | 9.4 | 6.4 | ||
| CO吸附量/(μmol·g-1) | 1.1 | 7.8 | 28 | 37 | 23 |
| NH3脱附量/(μmol·g-1) | 85 | 82 | 81 | 36 | 49 |
CO化学吸附量代表催化剂表面镍活性位的密度。CO的吸附量主要由两个因素决定:Ni2P晶粒大小和剩余的磷。Ni2P晶粒越小,CO化学吸附量越大;剩余的磷越多,覆盖表面镍活性位致使CO吸附量越少。残P量与前驱体的还原难易程度有关,前驱体越难还原,所制备得到的催化剂表面残P量越多。由表 1可以看到,随还原温度的提高,由前驱体Ⅱ制备的催化剂的CO吸附量显著增加,这是由于在较低还原温度时催化剂表面有大量的未被还原的磷覆盖了镍活性位。由图 1可知,随着还原温度的升高,表面未被还原的P开始反应生成PH3,表面P的流失使得Ni活性位更多的暴露出来,从而CO吸附量大大的增加。Ⅰ-600催化剂中Ni2P晶粒尺寸小于Ⅱ-600催化剂,从Ni2P晶粒尺寸角度而言Ⅰ-600催化剂应具有较高的CO吸附量越大;实际上,Ⅰ-600催化剂吸附量低于Ⅱ-600催化剂,这可能与前驱体Ⅰ比前驱体Ⅱ难以还原导致表面较多磷物种覆盖Ni位有关。
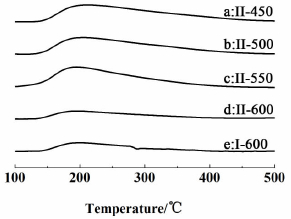
2.4 NH3-TPD结果图 3为不同催化剂的NH3-TPD图,表1给出了各催化剂上NH3脱附量。
|
| 图 3 不同催化剂的NH3-TPD图 Fig. 3 NH3-TPD profiles of different catalysts |
| |
由图 3可以看出,Ⅱ-T系列催化剂均在200 ℃有一个脱附峰,其归因于较弱的酸中心,与P—OH基团上NH3的脱附有关;随着还原温度的提高,NH3脱附峰的面积逐渐减小,说明催化剂表面的弱酸中心有所减少,可能与催化剂表面的P减少有关。Ⅱ-600的酸量明显低于Ⅱ-550,说明催化剂表面过量的P大量地被还原,使催化剂表面的弱酸中心大量减少。Ⅱ-600的NH3脱附量小于Ⅰ-600,也说明前驱体Ⅱ在600 ℃更易于还原且有较多P流失。
2.5 H2-TPD结果图 4为不同的催化剂的H2-TPD图。

|
| 图 4 不同催化剂的的H2-TPD图 Fig. 4 H2-TPD profiles of different catalysts |
| |
通常情况下,400 ℃以下的脱附峰与Ni2P颗粒表面的吸附氢有关,而高于400 ℃的脱附峰与溢流氢有关。图 4中各种催化剂在100 ℃时均开始出现脱附峰,Ⅱ-T随着还原温度的升高,各催化剂的峰面积也逐渐增大,说明H2的脱附量增大,随着还原温度的升高前驱体Ⅱ表面过量的P开始被还原,暴露的Ni位增多,这与CO化学吸附量得到的结果一致。400 ℃以上的脱附峰也随着还原温度升高面积变大,这说明溢流氢的量增大,脱附温度升高,脱附变困难。Ⅱ-600和Ⅰ-600的峰型相似,说明两者表面吸附氢物种环境相近。
2.6 催化剂月桂酸甲酯脱氧性能月桂酸甲酯脱氧有3种途径:加氢脱氧、加氢脱羧和加氢脱羰。在Ni2P/SiO2催化剂上,液相产物主要有正十一烷(n-C11)和正十二烷(n-C12),它们分别是加氢脱羰和加氢脱氧路径的产物。此外,还检测到一些含氧中间体(十二酸、十二醛、十二醇、十二酸十二酯和甲醇)及少量裂化产物(辛烷、庚烷、癸烷和壬烷等)。气相产物主要有CO和CH4。
图 5a)中给出了月桂酸甲酯在不同催化剂上的转化率。随着反应温度由300 ℃上升到340 ℃,各催化剂上月桂酸甲酯的转化率均提高。然而,随着反应温度提高,它们活性升高的程度却不尽相同。总体而言,Ⅱ-600的活性最好。值得说明的是,在300 ℃时Ⅱ-550的活性最好,这与CO化学吸附的结果略有不同。表 1数据表明,Ⅱ-450的CO吸附量很小,但其却表现出了一定的活性。课题组前期研究表明[15],Ni2P/SiO2催化剂活性不仅与暴露在催化剂表面的Ni位有关,还与催化剂表面P—OH基团提供的酸中心有关;并且,金属Ni位和P—OH基团之间还会存在协同作用促进月桂酸甲酯的转化。Ⅱ-450具有一定的活性可能与上述因素有关。随着前驱体Ⅱ还原温度的提高,所制备催化剂表面酸量减少、CO吸附量增加,但300 ℃时Ⅱ-550的活性高于Ⅱ-600,这可能与金属Ni位和P—OH基团的协同作用有关。然而,在320和340 ℃时,Ⅱ-600催化剂活性却高于Ⅱ-550。由于评价反应是连续进行,与300 ℃时Ⅱ-550活性高于Ⅱ-600不同,320和340 ℃时Ⅱ-600活性高于Ⅱ-550可能与其具有较高稳定性有关,其较高的稳定性使随温度提高及反应进行仍能保持较好的活性。此外,Ⅱ-600的活性略高于Ⅰ-600,与其具有较高CO吸附量有关。

|
| 图 5 不同催化剂的月桂酸甲酯脱氧性能 Fig. 5 Hydrodeoxygenation of methal laurate over different catalysts |
| |
图 5b)中给出了月桂酸甲酯在不同催化剂上C11和C12的2种烷烃产物总选择性(即S(C11+C12))。随着反应温度的提高,各催化剂上S(C11+C12)也随着增加,这与月桂酸甲酯的转化率的变化趋势一致,也表明提高反应温度促进了月桂酸甲酯脱氧。
图 5c)给出了不同催化剂上C11和C12的2种脱氧产物的物质的量之比。C11/C12物质的量之比反映了脱羰和加氢脱氧2条脱氧路径的选择性,C11/C12物质的量之比越高说明加氢脱羰的路径越显著。随着反应温度由300 ℃升到340 ℃,各催化剂上C11/C12物质的量之比均提高,说明较高的反应温度有利于加氢脱羰反应路径的进行。在相同反应温度下,随着前驱体Ⅱ还原温度的提高,所制备催化剂上C11/C12物质的量之比逐渐增加,说明较高的还原温度也有利于加氢脱羰反应路径进行。由表征结果可以看到,较高还原温度制备的催化剂表面暴露的金属位较多但酸量较低,这都有利于脱羰反应的进行。总体而言,不同反应温度下Ⅰ-600上C11/C12物质的量之比高于Ⅱ-T样品。如前所言,脱氧反应既可在金属Ni位上进行,也可以发生在P—OH基团所提供的B酸中心上[16, 17, 18]。B酸中心提供的H+进攻羰基上的氧,可以通过β消除整个羧基生成C11产物;但当催化剂表面的B酸中心较强时,其容易解离出加氢能力较强的H+,H+进攻羰基时就可以直接加氢脱氧生成C12产物[17]。结合H2-TPR及NH3-TPD的结果,Ⅱ-T表面过剩的P存在使得Ⅱ-T催化剂表面具有较多的B酸中心。在前驱体Ⅱ的还原过程中,次磷酸发生歧化反应主要生成PH3和HPO2-4,所制备催化剂表面过量的P主要来自于H2PO2-和HPO2-4,而在I催化剂的表面过量的P主要是来自未被还原的PO3-4。在次磷酸根中,P直接与2个H相连,强烈的极化作用使得磷原子的电子云密度降低,增强了磷氧键而削弱了氢氧键,使得其酸性较强。因此,与以磷酸盐作为磷源相比,以次磷酸作为磷源制备的磷化镍催化剂更有利于加氢脱氧路径。
图 5d)给出不同催化剂上含氧中间体化合物(十二醛、十二醇、十二酸和十二酸十二酯)的总选择性(即Soxy)。前期工作表明[9],含氧中间体化合物仍以脱羰及加氢脱氧2个途径脱氧。随着反应温度升高,Soxy都有明显的降低,说明较高的反应温度有利于脱氧反应的进行。相同反应温度下,随着前驱体Ⅱ还原温度提高,所制备催化剂上Soxy明显下降,说明较高的还原温度得到的催化剂有利于脱氧反应的进行。与CO化学吸附结果相关联,脱氧反应主要发生在金属位上。此外,Ⅱ-600在各反应温度下的Soxy均略低于Ⅰ-600,说明Ⅱ-600具有更好的脱氧性能。
3 结论以次磷酸作为磷源制备了Ni2P/SiO2催化剂前驱体,研究了还原温度对催化剂结构和性能影响。在较低温度下得到的催化剂中Ni2P晶型不完整,且催化剂表面有大量未被还原的P存在;随还原温度提高,Ni2P晶型完整并发生烧结,但由于P的流失导致表面Ni位数量增加;在月桂酸甲酯的脱氧反应中,催化剂活性随着还原温度的提高而增大,还原温度为600 ℃时所制备的催化剂活性较佳。此外,与以磷酸盐为磷源制备的催化剂相比,以次磷酸为磷源制备的Ni2P/SiO2催化剂的表面酸性加强,故其更利于催化加氢脱氧反应路径。
| [1] | Ma F, Hanna M A. Biodiesel production:A review[J]. Bioresource Technology,1999 : 1–15 |
| [2] | 王昶, 黄晓明, 贾青竹, 等. 生物柴油开发与应用[J]. 化学工业与工程,2008,25 (6) : 549–553 Wang Chang, Huang Xiaoming, Jia Qingzhu, et al. Development and application of biodiesel oil[J]. Chemical Industry and Engineering,2008,25 (6) : 549–553 |
| [3] | Simacek P, Kubicka D, Sebor G, et al. Hydroprocessed rapeseed oil as a source of hydrocarbon-based biodiesel[J]. Fuel,2009,88 (3) : 456–460 |
| [4] | Ramanathan S, Oyama S T. New catalysts for hydroprocessing:Transition metal carbides and nitrides[J]. Journal of Physical Chemical,1995,99 (44) : 16 365-16 372 |
| [5] | Alexander A M, Hargreaves J S J. Alternative catalytic materials:Carbides, nitrides, phosphides and amorphous boron alloys[J]. Chemical Society Reviews,2010,39 (11) : 4 388-4 401 |
| [6] | Wang W, Yang Y, Bao J, et al. Characterization and catalytic properties of Ni-Mo-B amorphous catalysts for phenol hyydrodeoxygenation[J]. Catalysis Communications,2009 : 100–105 |
| [7] | Phuong B, Juan A C, Oyama S T, et al. Studies of the synthesis of transition metal phosphides and their activity in the hydrodeoxygenation of a biofuel model compound[J]. Journal of Catalysis,2012 : 184–198 |
| [8] | Yang Y, Chen J, Shi H. Deoxygenation of methyl laurate as a model compound to hydrocarbons on Ni2P/SiO2, Ni2P/MCM-41, and Ni2P/SBA-15 catalysts with different dispersions[J]. Energy & Fuels,2013,27 (6) : 3 400-3 409 |
| [9] | Chen J, Shi H, Li L, et al. Deoxygenation of methyl laurate as a model compound to hydrocarbons on transition metalphosphide catalysts[J]. Applied Catalysis B-Environmental,2014 : 870–884 |
| [10] | Shi H, Chen J, Yang Y, et al. Catalytic deoxygenation of methyl laurate as a model compound to hydrocarbons on nickelphosphide catalysts:Remarkable support effect[J]. Fuel Processing Technology,2014 : 161–170 |
| [11] | 刘理华, 李广慈, 刘迪, 等. 过渡金属磷化物的制备和催化性能研究[J]. 化学进展,2010,22 (9) : 1 701-1 708 Liu Lihua, Li Guangci, Liu Di, et al. Preparation and catalytic performance of transition metal phosphides[J]. Process in Chemistry,2010,22 (9) : 1 701-1 708 |
| [12] | Rodriguez J A, Kim J Y, Hanson C J. Physical and chemical properties of MoP, Ni2P, and MoNiP hydrodesulfurization catalysts:Time-Resolved X-ray diffraction, density functional, and hydrodesulfurization activity studies[J]. Journal of Physical Chemical B,2003,107 (26) : 6 276-6 285 |
| [13] | Song L, Zhang S. A versatile route to synthesizing bulk and supported nickel phosphides by thermal treatment of a mechanical mixing of nickel chloride and sodium hypophosphite[J]. Powder Technology,2011 : 713–716 |
| [14] | Shi G, Shen J. New synthesis method for nickel phophide nanoparticles:Solid phase reaction of nickel cations with hypophosphites[J]. Journal of Materials Chemistry,2009 : 2 |
| [15] | Guo T, Chen J, Li K. Promotion effect of steam treatment on activity of Ni2P/SiO2 for hydrodechlorination of chlorobenzene[J]. Chinese Journal of Catalysis,2012,33 (7) : 1 080-1 085 |
| [16] | Senol O I, Ryymin E M, Viljava T R, et al. Effect of hydrogen sulphide on the hydrodeoxygenation of aromatic and aliphatic oxygenates on sulphided catalysts[J]. Journal of Molecular Catalysis A:Chemical,2007,277 (1) : 107–112 |
| [17] | Laurent E, Delmon B. Study of the hydrodeoxygenation of carbonyl, carboxylic and guaiacyl groups over sulfided CoMo/γ-Al2O3 and NiMo/γ-Al2O3 catalysts. I:Catalytic reaction schemes[J]. Applied Catalysis A,1994 : 77–96 |
| [18] | Zuo H, Liu Q, Wang T, et al. Hydrodeoxygenation of methyl palmitate over supported Ni catalysts for diesel-like fuel production[J]. Energy & Fuels,2012 : 3 747-3 755 |
 2016, Vol. 33
2016, Vol. 33





