2. 中国电子科技集团第十八研究所, 天津 300381
2. Tianjin Institute of Power Sources, Tianjin 300381, China
超级电容器也叫做电化学电容器,是一种介于传统电容器和电池之间的新型储能元件[1]。根据储能机理,超级电容器可以分为双电层电容器和赝电容器[2],其中电极材料是决定电容器性能的主要因素之一。
MnO2由于具有储量丰富,环境友好,且理论比电容高等优点成为近年来的研究热点,但MnO2的电子导电性差,表面形态密集等缺点也限制了其实际应用[3, 4, 5]。为了提高MnO2的利用率,一些研究致力于制备不同形貌和结构的MnO2,如MnO2纳米棒[6],纳米球[7],纳米线[8],纳米花[9]等,但这并不能从根本上提高MnO2的利用率。石墨烯自从进入人们的视线就引起广泛关注,完美的石墨烯结构是平面六边形点阵,每个碳原子均为sp2杂化,并贡献剩余1个p轨道上的电子形成大π键,π电子可以自由移动,赋予石墨烯良好的机械稳定性和电子导电性[10, 11]。基于石墨烯的各种优良特性,很大一部分研究集中在制备石墨烯/MnO2复合物[12, 13, 14]。石墨烯/MnO2的复合物中MnO2与石墨烯的协同作用显著提高了电极的电子导电性,但并不能改善MnO2密集的表面形态,且MnO2易在石墨烯上发生团聚。聚苯胺(PANI)是一种高分子导电聚合物,具有导电率高,柔韧性好,且分子上有大量苯环,本身也有电容特性等优点。因此,在石墨烯/MnO2中加入聚苯胺(PANI),制备石墨烯/PANI/MnO2三元复合物成为一个新的研究方向,但关于石墨烯/聚苯胺/MnO2三元复合物制备的文献甚少。仅有的报道文献中多采用的是原位聚合法制备,尚无用π-π共轭吸附法结合液相沉淀法制备石墨烯/PANI/MnO2复合物。本研究通过π-π共轭吸附法及接下来的液相沉淀法制备了石墨烯/聚苯胺/MnO2三元复合物并考察了PANI的含量及PANI复合方式对电极性能的影响。
1 实验部分 1.1 主要试剂天然鳞片石墨,苯胺,过硫酸铵,浓盐酸,高锰酸钾,硫酸锰,无水硫酸钠,氯化钾,琼脂粉,N-甲基吡咯烷酮,去离子水。无特别指出时,所用试剂均为分析纯,天津光复试剂有限公司提供。
1.2 复合材料的制备1)石墨烯的制备:氧化石墨由改进的Hummers法[15]制备,称取氧化石墨20 mg于250 mL烧杯中,加入30 mL去离子水,超声4 h使其充分分散,得到氧化石墨烯水溶液,将其置入50 mL水热反应釜中,180 ℃下反应6 h,过滤、洗涤,得到黑色的固体,即为石墨烯。
2)PANI的制备:采用化学氧化法制备PANI,制备过程简述如下,称取一定量的的苯胺单体,将其溶于1 mol/L HCl水溶液中,再称取对应量的APS[n(苯胺):n(APS)=1:1]溶于1 mol/L HCl溶液中,并将APS溶液逐滴加入到上述苯胺溶液中,冰水浴搅拌6 h,洗涤过滤并放入干燥箱中干燥12 h,研磨后得到聚苯胺。
3)三元复合物的制备:采用两步法制备石墨烯/PANI/MnO2三元复合物。第一步采用π-π共轭吸附法制备石墨烯/PANI复合物。将上述制备的石墨烯分散到50 mL N-甲基吡咯烷酮溶液中,依次称PANI 0,2.5,5,10,15 mg溶于50 mL N-甲基吡咯烷酮中,将上述两种液体混合,于常温下搅拌24 h,过滤,洗涤,依次得到GP0,GP2.5,GP5,GP10和GP15。第二步采用液相沉淀法制备石墨烯/PANI/MnO2三元复合物。将第一步制备的GPx分散到50 mL去离子水中,称取120 mg硫酸锰加到上述分散液中,常温搅拌6 h,再加入3 mL 0.2 mol/L高锰酸钾溶液,常温搅拌12 h,洗涤,过滤,干燥,样品分别记为GPM0,GPM2.5,GPM5,GPM10,GPM15。
改变PANI与石墨烯的复合方式,在第一步中采用原位聚合法将苯胺单体聚合到石墨烯上。具体如下:上述制备的石墨烯分散到50 mL去离子水中,量取苯胺单体50,100 μL溶于10 mL 1 mol/L HCl溶液中并加到石墨烯的分散液中,对应量的APS溶于1 mol/L HCl中,并于冰水浴条件下逐滴加到上述溶液中,并在冰水浴条件下搅拌6 h,过滤,洗涤,干燥,所得样品依次记为GA50,GA100;与MnO2复合的方法同上。所制备的样品记为GAM50,GAM100。
1.3 物相表征样品的物相分析在日本理学Rigaku D/max 2500V/PC型X射线衍射仪上进行,采用Cu_Kα靶,λ=0.154056 nm,管电压为40 kV,电流为200 mA,扫描速度4(°)·min-1,扫描角度范围2θ为5°~65°;样品的形貌和颗粒尺寸采用FEI-Nanosem430场发射扫描电镜(SEM)。
1.4 电极的制备及电化学测试将样品、炭黑和PTFE黏结剂按75:20:5的比例混合,加入适量乙醇,超声分散1 h,得到的悬浮液均匀涂于尺寸为1 cm×1 cm的正方形泡沫镍上,涂膜后放入干燥箱中60 ℃下干燥12 h,干燥后的电极用15 MPa压力压片成型,制得工作电极。电化学测试在Princeton Applied Research PAR2273工作站上进行。采用三电极体系,Pt片为辅助电极,饱和甘汞电极为参比电极,0.5 mol/L Na2SO4溶液做电解液,循环伏安法的电位窗口为-0.1~0.8 V。电化学阻抗谱测试的正弦波幅为±5 mV,频率范围为10 mHz~100 kHz。电化学测试均在35 ℃下进行。
电极的比电容通过循环伏安测试进行计算,计算公式为[16]:
| ${{C}_{m}}=i/\left( mv \right)$ | (1) |
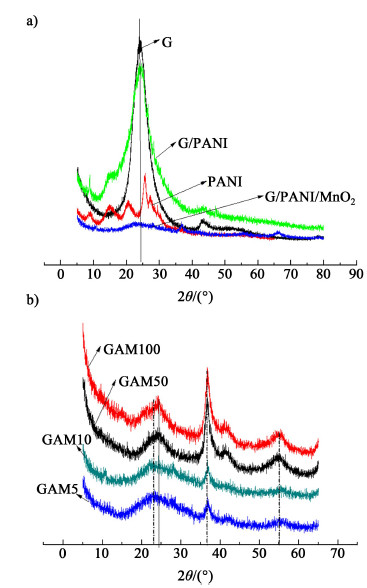
图 1a)是石墨烯、PANI、G/PANI和G/PANI/MnO2的XRD图。图 1b)是GAM50、GAM100、GPM5、GPM10的XRD图。
|
| 图 1 XRD图 Fig.1 XRD patterns |
石墨烯在23.9°处出现了1个较强的衍射峰,在42.8°出现了1个较弱的衍射峰,其分别对应于(002)和(100)面[17]。PANI在15.3°,20.7°,25.2°处均有衍射峰出现,分别对应于emeraldine盐的(001),(020),(200)晶面[18]。位于37.0°和54.9°的峰是MnO2的特征峰。由图 1b)可知,4个三元样品均在37.0°附近出现1个强衍射峰,在54.9°处附近有1弱衍射峰。由图 1还可以看出π-π吸附法制备的三元复合物和原位聚合法制备的三元复合物的石墨烯的峰位置稍有偏移。可能是因为π-π共轭吸附法中PANI中的苯环与石墨烯的六元环形成大π键,使石墨烯的峰位置偏移。这正好解释了PANI不同聚合方式对复合物电容性能的影响。
2.1.2 SEM表征图 2表示的分别是石墨烯[图 2a)和图 2b)],GPM0[图 2c)和图 2d)],GAM50[图 2e)和图 2f)],GPM5[图 2g)和图 2h)],GPM10[图 2i)和图 2j)]不同倍率下的SEM图。

|
| 图 2 样品不同倍率下的SEM图 Fig.2 The SEM imagesat different maginification |
样品GPM0中MnO2明显发生团聚,黏在一起,孔隙率小,这不利于电解液进入电极内部;三元复合物中,由于PANI的加入,有效改善了MnO2的团聚,使其分散性变好,粒径变小,空隙率变大。从图 2d)、图 2f)、图 2h)和图 2j)上还可以看出,PANI的加入还改变了MnO2的表面形态,使其表面变得粗糙,呈现类似蜂窝状的形貌。对比GAM50[图 2e)和图 2f)]和GPM5[图 2g)和图 2h)]可以发现PANI的复合方式对复合物会产生一定的影响。图 2e)和图 2f)中MnO2仍有一定程度的团聚,部分MnO2成块的黏在一起,远不如GPM5[图 2g)和图 2h)]中的分散均匀,这正好与2.2中循环伏安测试结果一致。对比GPM5[图 2g)和图 2h)]和GPM10[图 2i)和图 2j)],可以看出,PANI的量对复合物形貌有影响,这可能是由于PANI的量不同,MnO2形成时的活性位点或晶核数就不同,进而影响MnO2的形貌。这也解释了循环伏安测试中,不同PANI含量的样品的电容性能不同。
2.2 电化学测试 2.2.1 π-π共轭法中PANI的含量对电极电化学性能的影响图 3是样品GPM0,GPM2.5,GPM5,GPM10和GPM15在5 mV下的循环伏安图。

|
| 图 3 各样品在5 mV·s-1下的循环伏安图 Fig.3 Cyclicvoltammograms of samples with scan rate of 5 mV·s-1 |
由图 3可见,各样品的循环伏安曲线呈明显的矩形,且当电压反向时,响应电流几乎瞬间改变,这表明所制备的电极具有较好的电容性能。当PANI的量为5 mg时,响应电流值最大。根据式(1)计算可得GPM0,GPM2.5,GPM5,GPM10,GPM15各样品的比电容值分别为162.3、160.0、240.0、214.0和184 .0 F·g-1。
在循环伏安测试中,可逆反应公式:
| ${{i}_{\text{p}}}=0.4463nFSC_{O}^{0}{{\left( nF/RT \right)}^{\frac{1}{2}}}D_{o}^{\frac{1}{2}}{{v}^{\frac{1}{2}}}$ | (2) |
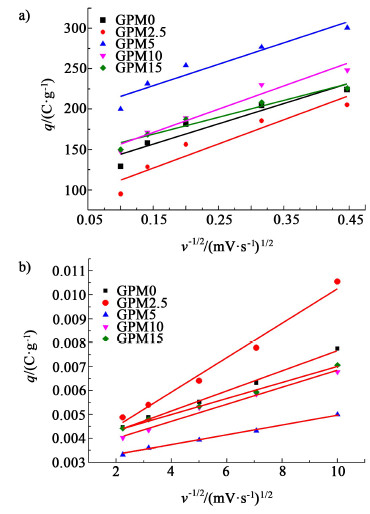
由式(1)和式(2)可知,比电容Cm与v-1/2成正比,因此当扫速较低时,电解液中的H+、Na+有足够的时间进入到电极内部参加电化学反应;当扫速很大时,H、Na+来不及进入电极内部,故电化学反应只能在电极表面进行,电极内部的活性物质不能有效贡献电容。故以q-1对v1/2作图可得1条直线,将直线外推到与纵轴相交,即扫速υ→0时的比电容,此时近似认为活性物质全部参与了电化学反应;同理当以q对ν-1/2作图也可得到1条直线,将其外推与纵轴相交,通过交点即得扫速ν→∞时的比电容,此时近似认为仅有位于电极表层的活性物质参与了电化学反应[19, 20]。见图 4和表 1。
|
| 图 4 π-π共轭法中各样品的外层比容量a)和内层比容量b)与扫速的关系图 Fig.4 The outer a) and inner b) specific capacitance of samples in π-π method with respect to sweep rates |
| 样品 | 内层比容量/(F·g -1) | 外层比容量/(F·g -1) |
| GPM0 | 256.0 | 130 |
| GPM2.5 | 270.3 | 98 |
| GPM5 | 333.3 | 205 |
| GPM10 | 277.8 | 140 |
| GPM15 | 250.0 | 150 |
由表 1可以看出,当PANI的量为5 mg时,该样品的内层比容量和外层比容量明显优于其他样品。适量PANI的加入不但改善了MnO2密集的表面形态,增大活性成分的有效接触面积,且PANI本身导电性很好,进而减小了MnO2之间的接触电阻,改善了电极内部的传质和传荷环境。
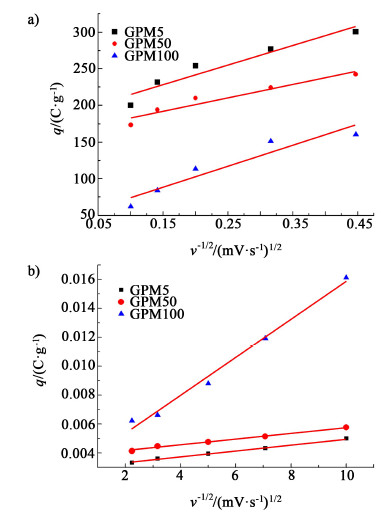
2.2.2 PANI复合方式对电极电化学性能的影响图 5是PANI不同复合方式下样品GPM5,GAM50,GAM100的循环伏安图。图 6描述了与扫速的关系。

|
| 图 5 GPM5,GAM50,GAM100在5 mV·s-1下的循环伏安图 Fig.5 Cyclicvoltammograms of samples GPM5,GAM50, GAM100 at scan rate of 5 mV·s-1 |
|
| 图 6 样品GPM5, GAM50,GAM100的外层比容量a)和内层比容量b)与扫速的关系图 Fig.6 The outer a) and innerb) Specific capacitance of samples GPM5,GAM50,GAM100 with respect to sweep rates |
由图 5可知,样品的循环伏安图都呈现较好的矩形,但电流响应明显不同,GPM5的电流响应值明显高于GAM50的电流响应值。这说明了PANI的复合方式会影响所制备的三元复合物的电容性能。这可能是由于π-π共轭法中,PANI上的苯环和石墨烯的六元环发生共轭作用生成大π键[21],使PANI均匀吸附在了石墨烯上,而原位聚合法中,PANI可能在石墨烯的表面附着不均匀,这对后续MnO2的复合会产生一定的影响。
由表 2可以看出样品GPM5无论是内层比容量还是外层比容量都明显高于样品GAM50。这表明π-π共轭法制备的三元复合物的电容性能更好。这些说明用π-π共轭法将PANI复合到石墨烯上,更有利于提高MnO2的电化学利用率。
| 样品 | 内层比容量/(F·g -1) | 外层比容量/(F·g -1) |
| GPM5 | 333.3 | 205 |
| GAM50 | 256.4 | 175 |
| GAM100 | 250.0 | 60 |
图 7为GPM0,GPM5,GAM50的交流阻抗谱图和交流阻抗谱图的等效电路图。

|
| 图 7 GPM0,GPM5,GAM50的交流阻抗谱图和交流阻抗谱图的等效电路图 Fig.7 Nyquist plots of GPM0,GPM5,GAM50 and equivalent circuit of the experimental impedance spectra |
从图 7中可以看出,各样品的交流阻抗谱图均由高频区的圆弧部分和低频区的直线部分组成。高频区与横轴的交点表示的是所有符合欧姆定律的电阻,包括溶液电阻和集流体电阻;半圆直径代表电荷转移电阻;低频区的直线部分,包括电极的扩散过程和电极电容性能过程;直线的斜率用来表示电极电容性能的优劣,直线越趋于垂直于实轴,则说明电极材料的准电容性能越好[22, 23, 24]。利用ZSimpWin软件对阻抗进行模拟,其拟合值见表 3。
| R L | C DL | R C | Z W | C F | |
| GPM0 | 0.1174 | 0.00007 | 0.07830 | 0.17670 | 0.0603 |
| GPM5 | 0.1917 | 0.01249 | 0.05580 | 0.01615 | 0.1497 |
| GAM50 | 0.1189 | 0.05819 | 0.00189 | 0.03500 | 0.0822 |
由表 3可以看出,3个样品的RL值虽有差异,但相差并不太大。说明导电聚合物PANI的加入使复合物的导电性有所增加,但并不显著。比较CF值,发现GPM5的赝电容值明显高于GPM0和GAM50。这都说明在石墨烯/MnO2中加入PANI可以在一定程度上增大电极的赝电容。
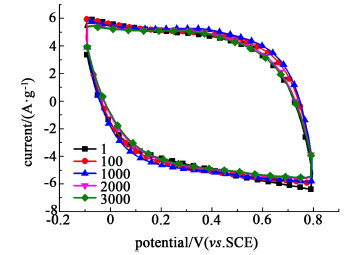
2.2.4 样品GPM5的循环寿命图 8为GPM5的循环寿命曲线。
|
| 图 8 GPM5的循环寿命曲线(扫速50 mV·s-1) Fig.8 The cycle life of GPM5 at scan rate 50 mV·s-1 |
用循环伏安法测试GPM5电极的循环稳定性,在扫速为50 mV·s-1条件下测定3 000个周期。由公式(1)计算得到第1、100、1 000、2 000和3 000次循环后的比电容分别为137、132、135、129和128 F·g-1。可以看出即便3 000次循环后比电容也只减小到原始值的92.7%。这表明由π-π共轭法制得的三元复合物不仅比电容值提高很多,循环稳定性也很强。
3 结论利用石墨烯和PANI的π-π共轭作用将PANI复合到石墨烯表面,继而结合液相沉淀法,制备了石墨烯/PANI/MnO2三元复合物。对复合物进行XRD、SEM物理表征和循环伏安、交流阻抗电化学测试。所得结论如下:1)加入PANI制备的三元复合物的比电容较二元复合物的比电容有较大的提升,GPM5的比电容比GPM0的比电容提高50%。2)PANI的量对复合物的性能有较大影响。当PANI的质量分数为4%时,制备的复合物的比电容值最大。3)PANI的复合方式对复合物的电化学性能也有一定影响。用π-π共轭法制备的三元复合物的性能要优于原位聚合法。4)所制备的样品GPM5的循环稳定性很好,经3 000次循环伏安测试后比电容仍保持为原始值的92.7%。
| [1] | Li Y, Zhao N, Shi C, et al. Improve the supercapacity performance of MnO2-decorated graphene by controlling the oxidization extent of graphene[J].The Journal of Physical Chemistry C,2012,116: 25 226-25 232 |
| [2] | Yang W,Gao Z,Wang J, et al. Synthesis of reduced graphenenanosheet/urchin-like manganese dioxide composite and high performance as supercapacitor electrode[J].ElectrochimicaActa,2012,69: 112-119 |
| [3] | Li Q, Liu J, Zou J, et al. Synthesis and electrochemical performance of multi-walled carbon nanotube/polyaniline/MnO2 ternary coaxial nanostructures for supercapacitors[J].Journal of Power Sources,2011, 196: 565-572 |
| [4] | Zheng Y, Du Q, He M,et al.Synthesis and electrochemical properties of graphite oxide/MnO2/conducting polymer ternary composite for supercapacitor[J].Micro & Nano Letters, 2012, 7(8):778-781 |
| [5] | Chen Y, Zhang Y, Geng D,et al. One-Pot synthesis of MnO2/graphene/carbon nanotube hybrid by chemical method[J].Carbon,2011,49: 4 434-4 442 |
| [6] | Yuan L, Lu X, Xiao X, et al.Flexible solid-state supercapacitors based on carbon nanoparticles/MnO2nanorods hybrid structure[J].ACS Nano, 2012, 6 (1): 656-661 |
| [7] | Liu J, Fan L, Qu X. Low temperature hydrothermal synthesis of nano-sized manganese oxide for supercapacitors[J]. Electrochimica Acta, 2012,66:302-305 |
| [8] | Jiang H,Zhao T, Ma J, et al.Ultrafine manganese dioxide nanowire network for high-performance supercapacitors[J].Chem Commu, 2011, 47: 1 264-1 266 |
| [9] | Chen Y, Hsu Y, Lin Y, et al. Highly flexible supercapacitors with manganese oxide nanosheet/carbon cloth electrode[J]. Electrochimica Acta, 2011, 56: 7 124-7 130 |
| [10] | Zhou Y, Wu M. Single-Parameter quantum charge and spin pumping in armchair graphene nanoribbons[J]. Phys Rev B, 2012, 86:85 406-85 415 |
| [11] | Zhang Y, Sun Q, Xie X. The effect of disorder on the valley-dependent transport in zigzag graphene nanoribbons[J].Journal of Applied Physics, 2011, 109(12):123 718-123 724 |
| [12] | Zhang J, Ren L, Deng L, et al.Graphene-MnO2 nanocomposite for high-performance asymmetrical electrochemical capacitor[J]. Materials Research Bulletin,2014,49:577-583 |
| [13] | Deng S, Sun D, Wu C, et al.Synthesis and electrochemical properties of MnO2nanorods/graphene composites for supercapacitorapplications[J]. Electrochimica Acta, 2013, 111:707-712 |
| [14] | Cheng Q, Tang J, Ma J,et al.Graphene and nanostructured MnO2 composite electrodes for supercapacitors[J].Carbon,2011,49:2 917-2 925 |
| [15] | Hummers W, Offeman R. Preparation of graphitic oxide[J]. J Am Chem Soc, 1958, 80(6):1 339-1 339 |
| [16] | Aleela M R,Ramaprabhu S. Nanocrystalline metal oxides dispersed multiwalled carbon nanotubes as supercapacitor electrodes[J]. J Phys Chem C,2007,111(21): 7 727-7 734 |
| [17] | Yan J, Wei T, Shao B, et al.Preparation of a graphenenanosheet/polyaniline composite with high specific capacitance[J].Carbon, 2010,48:487-493 |
| [18] | Yan J, Wei T, Fan Z, et al. Preparation of graphenenanosheet/carbon nanotube/polyaniline composite aselectrode material for supercapacitors[J].Journal of Power Sources, 2010, 195: 3 041-3 045 |
| [19] | Soudan P, Gaudet J, Guay D, et al. Electrochemical properties of ruthenium-based nanocrystalline materials as electrodes for supercapacitors[J].Chem Mater, 2002,14: 1 210-1 215 |
| [20] | Toupin M, Brousse T, BéLanger D. Influence of microstructure on the charge storage properties of chemically synthesized manganese dioxide[J].Chem Mater,2002,14: 3 946-3 952 |
| [21] | Bai H, Xu Y, Zhao L, et al. Non-Covalent functionalization of graphene sheets by sulfonatedpolyaniline[J].Chem Commun, 2009, 13(13): 1 667-1 669 |
| [22] | Wei W, Cui X, Chen W, et al. Improved electrochemical impedance response induced by morphological and structural evolution in nanocrystalline MnO2electrodes[J]. Electrochimica Acta, 2009,54: 2 271-2 275 |
| [23] | Hsieh Y C, Lee K T, Lin Y P, et al. Investigation on capacity fading of aqueous MnO2·nH2O electrochemical capacitor[J]. Journal of Power Sources, 2008, 177: 660-664 |
| [24] | Devaraj S, Munichandraiah N. Electrochemical supercapacitor studies of nanostructured a-MnO2 synthesized by microemulsion method and the effect of annealing[J]. Journal of The Electrochemical Society,2007,154 (2): A80-A88 |
 2016, Vol. 33
2016, Vol. 33





